Atomphysik II
Werbung

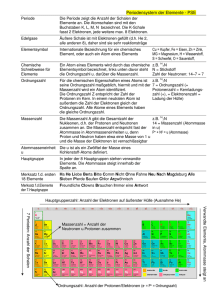
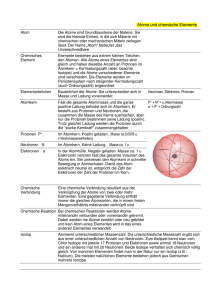
inhalt file:///I|/fernlehre skriptum/Studienbrief2/inhalt.htm Atomphysik II Das Periodensystem - Radioaktivität Bis ins 17. Jhdt. versuchte man in der Alchimie die Materie zu "veredeln". Berühmt wurden die Alchimisten durch ihre Bemühungen Gold zu machen. Obwohl ihnen dies nicht gelang, waren es ihre Experimente und in weiterer Folge die empirische Chemie, die zur Systematisierung der Eigenschaften der Elemente führte. Das Periodensystem hat seinen Ursprung in diesen Untersuchungen. Unter Berücksichtigung des Atommodells ist es eine der Elektronenkonfiguration entsprechende Anordnung der Elemente. In gewisser Weise kam der Traum der Alchimisten durch die Entdeckung der Radioaktivität zu einer späten Erfüllung. Beim radioaktiven Zerfall kommt es nämlich zu einer Umwandlung der Elemente. Den durch Neutronenbeschuß gezielt hervorgerufenen Kernzerfall nennt man Kernspaltung. Zusammen mit der Kernfusion (Kernverschmelzung) stellt sie die prinzipielle Möglichkeit einer uneingeschränkten Umformung der Elemente ineinander dar. Während die kontrollierte Kernspaltung bereits in zahlreichen Atomkraftwerken technisch realisiert ist, ist eine kontrollierte Kernfusion noch nicht gelungen. Die Radioaktivität ist ein Phänomen dem gerade in heutiger Zeit große gesellschaftliche Beachtung zukommt, da sie ein beträchtliches Gefahrenpotential in sich birgt. Für eine Urteilsbildung ist jedoch die Kenntnis der grundlegenden physikalischen Zusammenhänge eine Mindestvoraussetzung. Wir werden also im Folgenden die physikalischen Grundlagen zum Phänomen der Radioaktivität behandeln. Das Periodensystem Radioaktivität: Die Entdeckung des Phänomens Die verschiedenen Arten der Radioaktivität - Zerfallsreihen (Isotope) Kernfusion und Kernspaltung - Das Zerfallsgesetz (Halbwertszeit) 1 von 1 05.02.00 15:11 teil1 file:///I|/fernlehre skriptum/Studienbrief2/teil1.htm Das Periodensystem Wiederholen wir zunächst kurz, was wir in den vorangehenden Kapiteln besprochen haben. Näherungsweise kann ein isoliert gedachtes Atom als Kugel aufgefaßt werden, deren Radius in der Größenordnung von 100 pm liegt. Es besteht aus Atomkern und Atomhülle. Der Durchmesser des Atomkerns ist im Vergleich zum Durchmesser des Atoms sehr klein; sein Radius liegt in der Größenordnung von 0.01 pm. Stellt man sich ein Atom als eine stark vergrößerte Kugel von einem Radius mit 10 m vor, so hätte darin der Atomkern einen Radius von nur 1 mm. In diesem kleinen Atomkern ist praktisch die gesamte Masse des Atoms konzentriert. Bei einem Element mit einer Dichte von 1000 kg/m3 beträgt die Materialdichte im Kern 10^15 kg/m3 oder 1 Mill t/cm^3. Die Atomhülle ist praktisch materiefrei; sie enthält nur elektrisch negativ geladene Teilchen, die Elektronen. Alle Atome sind aus nur wenigen Bausteinsorten aufgebaut, zum groben Verständnis des Atombaues reicht es aus, sich auf Protonen, Neutronen und Elektronen zu beschränken (nur das Elektron ist ein Elementarteilchen). Bisher haben wir mehr oder weniger immer nur die Atomhülle behandelt. Zur vollständigen Beschreibung des Atoms gehört jedoch wesentlich auch der Atomkern. Im Atomkern sind Protonen und Neutronen enthalten. Sie haben etwa die gleiche Masse. Das Proton besitzt außer seiner Masse eine positive Ladung, und zwar die kleinste bekannte Ladung, das elektrische Elementarquantum [e=1,602 10^-19 C (Coulomb)]. Im elektrisch neutralen Atom sind in seiner Hülle ebensoviele negative Ladungen (Elektronen) vorhanden, wie positive Ladungen (Protonen) im Atomkern enthalten sind. Die Ruhmasse eines Protons beträgt 1,672 10^-24 g. 6,02252 10^23 Protonen haben die Masse von 1,0069 g. Man bezeichnet die Masse von 6,02252 10^23 Teilchen als relative Atommasse und die Zahl der in ihr enthaltenen Teilchen als die Avogadrosche Konstante, früher auch Loschmidtsche Zahl genannt. Sie hat die Einheit mol^-1. Neben den Protonen sind in allen Atomkernen (mit Ausnahme des leichten Wasserstoffkernes) Neutronen vorhanden. Sie unterscheiden sich von den Protonen dadurch, daß sie elektrisch neutral sind, also keine Ladung tragen. Die Ruhmasse des Neutrons beträgt 1.674 10^-27 kg und die relative Atommasse 1,0081. Die Masse eines Elektrons ist sehr viel kleiner als diejenige eines Protons oder Neutrons, nämlich 1/1836 der Masse eines Protons. Die Massenzahl A eines Atoms ist die Summe der Zahlen seiner Protonen P und Neutronen N (A=P+N). Protonen und Neutronen werden durch die sehr starken Kernkräfte im Atomkern zusammengehalten. Die Zahl der in einem Atomkern enthaltenen Neutronen ist in der Regel mindestens so groß wie die der Protonen. Mit wachsender Atommasse wird die Zahl der Neutronen größer als die Zahl der Protonen: der Urankern mit der Massenzahl 238 enthält 92 Protonen und 146 Neutronen. Die Zahl der Protonen in einem Kern wird Ordnungszahl, Kernladungszahl oder 1 von 3 05.02.00 15:13 teil1 file:///I|/fernlehre skriptum/Studienbrief2/teil1.htm Atomnummer genannt. In einem neutralen Atom ist sie gleich der Anzahl der Elektronen in der Atomhülle. Unter einem Element wird ein Stoff verstanden, welcher in Atome gleicher Ordnungszahl (und damit gleicher Elektronenanzahl in der Atomhülle) zerlegt werden kann. Durch die Angabe der Ordnungszahl ist ein Element eindeutig charakterisiert; es wäre daher nicht nötig, es zusätzlich durch Name und Symbol zu kennzeichnen. Beispielsweise ist das Element mit der Ordnungszahl 1 Wasserstoff, das Element mit der Ordnungszahl 6 Kohlenstoff und dasjenige mit der Ordnungszahl 92 Uran. Gegenwärtig sind 107 Elemente bekannt, von denen etwa 90 in der Natur vorkommen. Der gedankliche Aufbau der Elektronenhüllen der einzelnen Atome ist in der Weise möglich, daß, beginnend mit dem leichtesten Atom, dem Wasserstoffatom, Elektronen schrittweise (unter gleichzeitiger Zugabe je eines Protons und der erforderlichen Neutronen in den Atomkern) in den energetisch günstigsten Zustand, d.h. jenen minimaler Energie, eingefügt werden. Dabei muß wie schon oben erwähnt das Pauli-Prinzip berücksichtigt werden. Mit Hilfe des Pauli-Prinzips ist es möglich, die Elektronen in einem Atom und ihre Quantenzustände zu charakterisieren. Innerhalb eines Atoms kann es maximal zwei Elektronen mit der Hauptquantenzahl n 1 geben. Bei n = 1 können nämlich - wie wir schon gezeigt haben - sowohl die Nebenquantenzahl l als auch die magnetische Quantenzahl m nur den Wert null haben. Die beiden Elektronen mit der Hauptquantenzahl n = 1 können nur s-Elektronen (l=0) sein (ms = +1/2,-1/2). Mit der Hauptquantenzahl n = 2 sind acht verschiedene Elektronenzustände möglich, da l = 0 oder 1 = 1 sein kann; für l = 0 (s-Elektronen) stehen zwei Elektronenzustände zur Verfügung, nämlich ms = + 1/2 und -1/2 und bei l = 1 gibt es 6 p-Elektronen-Zustände entsprechend der möglichen Werte für m (m=0,+1,-1). Jeder dieser Zustände kann durch zwei Elektronen mit verschiedenen Spinquantenzahlen besetzt werden. Es sind also in einem Atom maximal acht Elektronen mit der Hauptquantenzahl n = 2 möglich: zwei 2s- und sechs 2p-Elektronen. Analog können 18 Elektronen für n = 3 und 32 Elektronen für n = 4 in einem Atom auftreten. Die Anzahl der Elektronen, welche maximal bei gegebener Hauptquantenzahl n möglich ist, ist 2n^2. Im folgenden Periodensystem sind die ersten 36 Elemente dargestellt. Die Zahlen unter den Elementen sind die Massenzahlen. Da die meisten Elemente in der Natur als Isotopengemische (Isotop: Nuklid gleicher Ordnungszahl, aber verschiedener Neutronenzahl) vorkommen, sind die Zahlen nicht ganzzahlig. Durch Klicken auf ein Element wird die Elektronenkonfiguration des betreffenden Elementes angezeigt. Gehen Sie die einzelnen Elemente durch und verfolgen Sie, wie die einzelnen Energieniveaus aufgefüllt werden. 2 von 3 05.02.00 15:13 teil2 file:///I|/fernlehre skriptum/Studienbrief2/teil2.htm Die Entdeckung des Phänomens Ursprünglich untersuchte Röntgen 1895 die Kathoden- (Elektronen-) Strahlen. Um das durch die Kathodenstrahlen hervorgerufene schwache Fluoreszenzlicht sehen zu können, hatte Röntgen das sichtbare Licht seines Kathodenstrahlrohres mit undurchsichtigem schwarzem Papier vollkommen abgeschirmt. Dennoch bemerkte er beim Betrieb des Entladungsrohrs ein kräftiges Leuchten an allen in der Nähe befindlichen fluoreszierenden Salzen, obwohl kein sichtbares Licht und erst recht keine Kathodenstrahlen auf die Salze auftreffen konnten. Zunächst glaubte man die Röntgenstrahlen, durch die die Salze zum Fluoreszieren angeregt wurden, seien selbst die Folge eines Fluoreszenzeffektes wenn die Elektronen auf die Wand der Kathodenstrahlröhre treffen. Wilhelm Conrad Röntgen (1845-1923). Um dieser Vermutung nachzugehen hat Becquerel eine sorgfältig in schwarzes Papier eingehüllte Fotoplatte verwendet, auf der keine Spur einer Belichtung zu bemerken war, wenn sie über mehrere Stunden intensiver Sonnenbestrahlung ausgesetzt wurde. Auf die derartig verpackte Platte hat er einen Uransalzkristall gelegt, mit dem er schon früher bei seinen Fluoreszenzuntersuchungen experimentiert hatte. Platte und Kristall hat er dann der Sonnenstrahlung ausgesetzt, um das Uransalz zum Fluoreszieren zu bringen. Nach dem Entwickeln der Fotoplatte stellte Becquerel auf ihr eine Schwärzung in der Form des Uransalzkristalles fest. Er glaubte damit seine Annahme, daß die Fluoreszenz mit einer Emission von Röntgenstrahlen einhergeht, als bewiesen ansehen zu können. Wie wir wissen, existiert der vermutete Zusammenhang zwischen Fluoreszenz und Röntgenstrahlung nicht. Die Röntgenstrahlen gehen von den Elektronen aus, die beim Auftreffen auf die Glaswandung des Entladungsrohres abgebremst werden, wobei die Fluoreszenz lediglich eine Begleiterscheinung ist. Bei den heute verwendeten Röntgenröhren werden die Elektronen nicht an der Glaswand, sondern gewöhnlich beim Auftreffen auf eine Wolfram-Elektrode abgebremst. Die Emission von Röntgenstrahlen ist hier mit keinerlei Fluoreszenzerscheinungen verbunden. 1 von 3 05.02.00 15:13 teil2 file:///I|/fernlehre skriptum/Studienbrief2/teil2.htm Ein zufälliges Ereignis hat dann die Physiker zu der Erkenntnis geführt, daß die Schwärzung der Fotoplatte eigentlich gar nichts mit der Fluoreszenz des Uransalzes zu tun hat. Becquerel wollte seine Versuche mit der Fotoplatte und dem Uransalzkristall wiederholen. Da die Sonne jedoch nur zeitweise schien, reichte die Lichtmenge nicht aus um das Uransalz zum Fluoreszieren zu bringen. Erlegte also den Plattenbehälter zurück in eine dunkle Schublade, wobei er das Uransalz auf ihm liegen ließ. Da sich das Wetter aber nicht besserte, entwickelte er schließlich die Photoplatten in der Erwartung, sehr schwache Bilder zu bekommen. Tatsächlich erschienen aber die Silhouetten des Uransalzkristalls in sehr großer Intensität. Bei den weiteren Untersuchungen hat Becquerel festgestellt, daß das beobachtete Phänomen tatsächlich mit der Fluoreszenz nichts zu tun hat und ausschließlich auf die Anwesenheit des Urans zurückzuführen ist. Er hat dann bemerkt, daß die Wirkung des Uransalzes nicht von seinem physikalischen oder chemischen Zustand abhängt und daß die Strahlen, die eine Zeit lang als Becquerel-Strahlen bezeichnet wurden, die Luft genauso zu ionisieren vermögen wie die Röntgenstrahlen. 1898 hat Rutherford begonnen, die ionisierende Wirkung der Becquerel-Strahlung zu studieren. Dabei hat er festgestellt, daß die Strahlung nicht homogen ist und eine ionisierende Komponente hat, die bereits von einer dünnen Papierschicht absorbiert wird und deren Reichweite auch in der Luft nur einige Zentimeter beträgt. Die andere Komponente hat ein sehr viel kleineres Ionisationsvermögen, aber eine wesentlich größere Reichweite. Rutherford hat diese Strahlen ohne weitere Begründung nach den ersten Buchstaben des griechischen Alphabets als α- und β -Strahlen bezeichnet. Es soll an dieser Stelle noch bemerkt werden, daß Villard 1900 eine dritte Form der Strahlen, die γ -Strahlen, entdeckt hat, die eine weitaus größere Reichweite (Durchdringungsvermögen) als die β-Strahlen haben. Becquerel konnte schließlich nachweisen, daß die β-Strahlen von korpuskularer Natur sind und eine negative Ladung tragen. Nachdem der Quotient ihrer Ladung zu ihrer Masse bestimmt worden war, konnte man sie mit den Elektronen identifizieren, die vor nicht allzu langer Zeit entdeckt worden waren. Die Identifizierung der α-Strahlen war nicht so einfach. 1902 ahnte Rutherford bereits, daß die α-Strahlen aus zweifach ionisierten Heliumatomen bestehen; den endgültigen Beweis hat er jedoch erst im Jahre 1909 erbracht. 2 von 3 05.02.00 15:13 teil2 file:///I|/fernlehre skriptum/Studienbrief2/teil2.htm Ablenkung radioaktiver Strahlung im Magnetfeld In den ersten Jahren des 20. Jahrhunderts hat sich also ein im großen und ganzen richtiges Bild über die Radioaktivität durchgesetzt. Die Natur der Strahlung war bekannt, und man wußte, daß α-Strahlen aus Ionen mit einer positiven Ladung bestehen, wobei man sogar vermutete, daß diese Ionen Helium-lonen sind. Die β-Strahlen waren als Elektronenstrahlen identifiziert worden, und schließlich hat man geahnt, daß die γ-Strahlen den Röntgenstrahlen verwandt sind. Man hat auch gewußt, daß ein Element in einem bestimmten Akt entweder nur α- oder nur ß-Strahlen emittiert und daß sich die Atome bei der Emission dieser Strahlung chemisch umwandeln. Das Zerfallsgesetz war bereits aufgestellt und der Begriff der Halbwertszeit des Zerfalls eingeführt worden. Man darf aber nicht vergessen, daß diese Beobachtungen noch nicht kernphysikalisch gedeutet worden sind, weil vom Atom noch nicht bekannt war, daß es aus einem zentralen Kern und einer Hülle besteht. Zurück 3 von 3 05.02.00 15:13 teil3 file:///I|/fernlehre skriptum/Studienbrief2/teil3.htm Die verschiedenen Arten der Radioaktivität Instabile Kerne senden bei ihrer Umwandlung charakteristische Strahlen aus. Bei Elementen mit Ordnungszahlen über 83 sind alle Isotope radioaktiv. Der Zeitpunkt der radioaktiven Umwandlung für ein einzelnes Atom ist völlig unbestimmt, für eine große Menge von Atomen gelten jedoch die statistischen Gesetze der Zerfallsgeschwindigkeit (siehe weiter unten). Die Radioaktivität wird charakterisiert durch die Natur der Strahlung, die Strahlungsenergie, die Zerfallsgeschwindigkeit der Kerne und schließlich die Strahlungsaktivität. α-Strahlen sind doppelt positiv geladene Heliumkerne; sie werden mit Geschwindigkeiten bis zu 10% der Lichtgeschwindigkeit aus den radioaktiven Kernen ausgestoßen. Sie üben eine stark ionisierende Wirkung aus. β -Strahlen sind schnell bewegte, freie Elektronen. Sie sind etwa 7300 mal leichter als α-Teilchen und können beinahe Lichtgeschwindigkeit erreichen. β-Strahlen haben meist geringere kinetische Energie sowie ein geringeres Ionisierungsvermögen als α-Strahlen, γ -Strahlen können als Begleiterscheinung beim α- wie auch beim α-Zerfall auftreten. Sie sind hochenergetische elektromagnetische Strahlen. Die drei Arten radioaktiver Strahlung Die Strahlungsenergie wird meist in MeV/Atom angegeben. Ein eV ist jene Energie, die einem Elektron oder Proton beim Durchlaufen der Potentialdifferenz von 1 Volt erteilt wird. 1 eV= 1,6 10^-22 kJ und liegt in der Größenordnung des bei chemischen Reaktionen auftretenden Energieumsatzes. Die kinetischen Energien von α-Teilchen liegen meist zwischen 4 und 11MeV/Atom, sind also 10^6 bis 10^7 mal so groß wie etwa die typischen Energieänderungen bei chemischen Reaktionen. Unter der Strahlungsaktivität wird der Quotient aus der Anzahl der Zerfallsakte 1 von 3 05.02.00 15:14 teil3 file:///I|/fernlehre skriptum/Studienbrief2/teil3.htm und der Zeit verstanden. Die Strahlungsaktivität eines bestimmten radioaktiven Präparates ist seiner Menge proportional. Ein Curie (Ci) entspricht etwa der Aktivität von 4 g Radium bzw. derjenigen Menge eines radioaktiven Stoffes, welche 3.7 1O^10 Zerlallsakte pro Sekunde aufweist. Zerfallsreihen (Isotope) Ein Nuklid ist eine Atomart, die durch ihre Ordnungszahl und ihre Massenzahl definiert ist. Zur Kennzeichnung wird die Massenzahl links oben dem chemischen Symbol vorangestellt. 1H ist das Nuklid des Wasserstoffes mit der Massenzahl 1, 16O das Nuklid des Sauerstoffes, mit der Massenzahl 16. Häufig wird außerdem die Ordnungszahl dem Symbol des Elements, und zwar links unten, vorangestellt, also 11H für das Wasserstoffnuklid mit der Massenzahl 1 und 816O für das Sauerstoffnuklid mit der Massenzahl 16. Isotope sind Nuklide gleicher Ordnungszahl, aber verschiedener Neutronenzahl und demnach verschiedener Massenzahl. Sie sind Nuklide ein und desselben Elements. In der Regel sind sie chemisch gleichartig, unterscheiden sich aber in physikalischen Eigenschaften. Nuklide gleicher Massenzahl, aber verschiedener Ordnungszahl und verschiedener Neutronenzahl sind Angehörige verschiedener Elemente und werden Isobare genannt; sie können daher auf chemischem Weg leicht voneinander getrennt werden. Diejenigen Elemente, welche in der Natur in einer einzigen Nuklidgattung vorkommen, nennt man Reinelemente oder mononuklidische Elemente (z.B. Fluor). Die meisten in der Natur vorkommenden Elemente sind jedoch Isotopengemische, polynuklidische oder Mischelemente. Bei Aussendung von α-Strahlen (He-Kerne) erfolgt eine Verringerung der Massenzahl um vier Einheiten (ein He-Kern enthält 2 Protonen und 2 Neutronen) und eine Verringerung der Ordnungszahl um zwei Einheiten. Beispiel: Aus 88226Ra entsteht durch Emission von α-Strahlen das Edelgas Radon 86222Rn. Die Kernreaktion hat unmittelbar eine Umbildung der Elektronenhülle zur Folge, da das Rn-Atom zwei Elektronen weniger enthält als das Radiumatom. Bei β-Strahlung wird ein Elektron aus dem Kern (nicht ein Elektron aus der Atomhülle) ausgestoßen. Man kann sich vorstellen, daß im Kern die Umwandlung eines Neutrons in ein Proton unter Abgabe eines Elektrons erfolgt: n => p + e. Durch Emission des Elektrons aus dem Atomkern bleibt die Massenzahl des Kerns unverändert, aber die Ordnungszahl wird um eine Einheit erhöht. Beispiel: Aus Protactinium-234 (Ordnungszahl 91) entsteht Uran-234 (Ordnungszahl 92). 2 von 3 05.02.00 15:14 teil3 file:///I|/fernlehre skriptum/Studienbrief2/teil3.htm Ausschnitt aus der Uran-RadiumZerfallsreihe Bei einem radioaktiven Umwandlungsprozeß können Nuklide entstehen, welche wieder radioaktiv sind. Da sich die Massenzahl entweder überhaupt nicht oder nur um vier Einheiten ändern kann, sind vier verschiedene Zerfallsreihen möglich. Davon kommen in der Natur nur drei vor: die Thorium-Reihe, die Uran-Reihe und die Actinium-Reihe. Endprodukt einer Zerfallsreihe ist entweder ein Blei- oder ein Wismut-Isotop. Zurück 3 von 3 05.02.00 15:14 teil4 file:///I|/fernlehre skriptum/Studienbrief2/teil4.htm Kernfusion und Kernspaltung Die Atommasse eines Atoms ist geringer als die Summe der Massen der in ihm enthaltenen Protonen und Neutronen. Die für Helium (2p, 2n) berechnete Atommasse ist 4,0300, der gefundene Wert 4,0026. Die Differenz zwischen berechnetem und gefundenem Wert wird als Massendefekt bezeichnet. Er beträgt demnach für Helium 0.0274 Masseneinheiten. Der Massendefekt ist ein Maß für die gesamte Bindungsenergie der Nukleonen (Protonen und Neutronen) in einem Atomkern. Er ist das Massenäquivalent der bei der Bildung der Kerne abgegebenen Bindungsenergie. Bei der Bildung des Heliums aus Protonen und Neutronen tritt ein Verlust an Masse (Zuwachs an Bindungsenergie) ein, welcher in Energie umgewandelt wird. Zur Einleitung der Kernfusion sind allerdings Temperaturen von vielen Millionen Grad Celsius erforderlich, wie sie beispielsweise in der Sonne vorherrschen oder auch bei der Explosion einer Atombombe erreicht werden. Daher ist es möglich, mit Hilfe einer Atombombe eine Kernverschmelzung auszulösen, gegenwärtig jedoch nur die unkontrollierte Form (Wasserstoffbombe). Kernbindungsenergie pro Nukleon Die Kernbindungsenergie pro Nukleon steigt bei den sehr leichten Atomen mit zunehmender Massenzahl zunächst steil an und erreicht schon beim Sauerstoff einen Wert um 8 MeV pro Nukleon. Die größte Bindungsenergie pro Nukleon wird bei Kernen mit Massenzahlen um etwa 60 gefunden. Sie nimmt sodann mit steigender Ordnungszahl wieder ab. Durch die Spaltung schwerer Atomkerne (Kernspaltung), z.B. von Uran, in zwei Atomkerne mittlerer Massenzahl wird ebenfalls Masse in Energie umgewandelt. 1 von 3 05.02.00 15:14 teil4 file:///I|/fernlehre skriptum/Studienbrief2/teil4.htm Das Zerfallsgesetz (Halbwertszeit) Die Geschwindigkeit des radioaktiven Zerfalles ist von äußeren Bedingungen (Druck, Temperatur) unabhängig und für ein radioaktives Nuklid charakteristisch. Die je Zeiteinheit zerfallende Zahl der Atome eines radioaktiven Stoffes ist in jedem Augenblick zu der Anzahl N(t) der noch nicht zerfallenen Atome proportional: Die Zerfallskonstante λ gibt an, welcher Bruchteil der Masse des radioaktiven Stoffes je Sekunde umgewandelt wird. Sie ändert sich im Laufe der Zeit nicht. Für Radium ist λ = 1,36 10^-11 s (je Sekunde zerfallen von l g Ra 1,36 10^-11 g). Trennen wir in obiger Gleichung die Variablen N und t erhalten wir: Durch unbestimmte Integration erhalten wir: Für die Zahl N(t) der zur Zeit t noch nicht zerfallenen Atome ergibt sich also: (Zerfallsgesetz) Dabei ist N0 die Zahl der Atome zum Zeitpunkt t=0. Als Halbwertszeit wird die Zeit verstanden, innerhalb der sich die Hälfte der ursprünglich vorhandenen Atome umwandelt. Unter Berücksichtigung des Zerfallsgesetzes ist sie durch folgenden Ausdruck gegeben: Im folgenden Programm haben Sie die Möglichkeit den radioaktiven Zerfall dreier Substanzen zu untersuchen. Wählen Sie die Substanzen durch Klicken auf das Feld "Atom" links oben. Zunächst haben Sie 90 aktive Atome dieser Substanz. Geben Sie in der entsprechenden Zeile ein Zeitintervall ein (zwischen 1 und 100, ganzzahlig) und drücken Sie "Enter". Durch Klicken auf das Feld "Nächstes Zeitintervall" können Sie beobachten wieviele der aktiven Atome innerhalb des Zeitintervalls zerfallen. Wiederholtes Klicken auf dieses Feld läßt die Zeit immer um das eingegebene Zeitintervall weiter laufen. In der Grafik rechts wird die Anzahl der noch aktiven Atome angezeigt. Nach 10 Zeitintervallen können Sie durch Klicken auf das Feld "Zurücksetzen" wieder von vorne beginnen und eine andere Atomart wählen. Aufgaben: Versuchen Sie die Halbwertszeit der einzelnen Substanzen zu ermitteln. Bei gegebenem Zeitintervall und gegebener Atomart: Ist die Rate der pro Zeiteinheit zerfallenden Atome im Mittel konstant? Wieso gibt es im Einzelfall Abweichungen? 2 von 3 05.02.00 15:14 teil4 file:///I|/fernlehre skriptum/Studienbrief2/teil4.htm Wenn nur mehr ein Atom aktiv ist: Steigt seine Zerfallswahrscheinlichkeit mit fortschreitender Zeit? Zurück 3 von 3 05.02.00 15:14