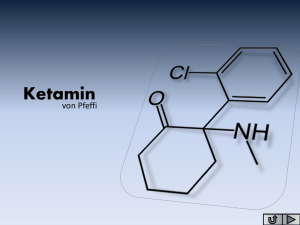
Phytopharmaka zur Behandlung entzündlicher Erkrankungen des
Werbung

PHARMAZEUTISCHE WISSENSCHAFT Phytopharmaka zur Behandlung entzündlicher Erkrankungen des Bewegungsapparates Erkrankungen des rheumatischen Formenkreises spielen aufgrund vielfältiger Ursachen eine zunehmend größere Rolle in den Industrieländern. Neben der konventionellen Therapie mit steroidalen und nichtsteroidalen Antiphlogistika sind Phytopharmaka mindestens als adjuvante Therapeutika von Interesse. Wegen der geringeren Nebenwirkungen sind sie insbesondere zur Behandlung chronischer Erkrankungen geeignet, bei denen eine Einnahme über einen längeren Zeitraum nötig ist. Die wichtigsten innerlich eingesetzten Arzneipflanzen werden hier vorgestellt. Einleitung Entzündungen können in fast allen Geweben des menschlichen Körpers auftreten. Viele dieser entzündlichen Prozesse können als relativ harmlos eingestuft werden und bedürfen keiner intensiven Behandlung. Meist reicht die topische oder perorale Anwendung herkömmlicher, entzündungshemmender Arzneistoffe wie Ibuprofen oder Acetylsalicylsäure aus. Grundsätzlich kann man Entzündungen als Abwehrmechanismen des Körpers ansehen, deren komplexer Verlauf mit der Aktivierung von Monozyten, Granulozyten und Lymphozyten sowie der Freisetzung und Aktivierung humoraler Mediatoren einhergeht [1]. Der inflammatorische Prozess beginnt mit einem Stimulus, der entweder über die Aktivierung der Cyclooxygenase-2 (Cox-2) zur Bildung von Prostaglandinen (PG), insbesondere PGE2, führt oder der über die Aktivierung der induzierbaren Nitroxidsynthase (iNOS) die Bildung von Nitroxid (NO) anregt [2]. Die gebildeten Prostaglandine lösen dann ihrerseits in den Zellen die Bildung weiterer Cytokine aus, die in unterschiedlicher Menge gebildet werden und die Anlockung von Leukozyten in der entzündeten Region fördern. 8 Entzündungen können akut und chronisch verlaufen. Akute Verlaufsformen sind auf Tage bis Wochen beschränkt und führen im Allgemeinen nicht zu dauerhaften Schädigungen des Gewebes. Die Behandlung solcher Erkrankungen ist auch mit Arzneistoffen problemlos möglich, die bei längerer Einnahme häufig zu Nebenwirkungen führen. Anders sieht es bei chronischen Entzündungen aus. Aufgrund der gestiegenen Lebenserwartung in unserer Wohlstandsgesellschaft verzeichnen wir heute einen wesentlich größeren Teil älterer Menschen in der Bevölkerungsstruktur als noch vor hundert Jahren. Dadurch bedingt ist eine deutliche Zunahme von degenerativen bzw. rheumatischen Erkrankungen zu beobachten. Ungefähr drei Viertel der 55 – 60-Jährigen leiden an schmerzhaften Erkrankungen des Bewegungsapparates, wobei eine Unterscheidung zwischen degenerativen und entzündlichen Erkrankungen leicht anhand der Symptomlage getroffen werden kann. Charakteristisch für degenerative Prozesse (Arthrose) ist der Belastungsschmerz, während entzündliche Verlaufsformen an geröteten und geschwollenen Gelenken zu erkennen sind, die ohne einen Zusammenhang mit körperlicher Belastung (vor allem nachts) stark schmerzen [3]. Über die auslösenden Faktoren solcher entzündlich rheumatischer Erkrankungen herrscht immer noch Unklarheit. Neben Infektionen (Streptokokken, Toxoplasmose, Hepatitis B, Röteln) werden vor allem genetische Faktoren und Autoimmunreaktionen als Ursachen für das Auftreten rheumatischer Erkrankungen angesehen. Auf molekularer Ebene sind Cytokine wesentlich an der Entstehung von Rheuma beteiligt. Solche Botenstoffe werden als chemotaktische Reize von Immunzellen freigesetzt, um das Entzündungsgeschehen bei Erkennen pathogener Fremdstoffe anzufachen und so einer erfolgreichen Immunabwehr zu dienen. Bei entzündlich-rheumatischen Erkrankungen ist die Regulation dieser proinflammatorisch wirkenden Stoffe wie z.B. Interleukin-1β (IL-1β) und Tumornekrosefaktor-α (TNF-α) gestört, wodurch es zu einer dauerhaften Erhaltung der Entzündungsprozesse ohne pathogenen Auslösefaktor kommt. Diese Stoffe werden außerdem für die Aktivierung knorpelabbauender Enzyme verantwortlich gemacht, was die zusätzlichen destruktiven Prozesse im Laufe der rheumatischen Erkrankung erklärt [3]. Die gleichzeitig auftretenden Schmerzen werden durch Prostaglandine und Leukotriene ausgelöst, die auf unterschiedlichen Biosynthesewegen mit Hilfe der Cyclooxygenase bzw. Lipoxygenase aus der Arachidonsäure gebildet werden [3]. Aus den genannten Gründen kann eine Therapie auf unterschiedlichen Wegen zu einer Verbesserung der Gelenkfunktion bzw. Reduktion der auftretenden Schmerzen führen. Neben physikalischen und ergotherapeutischen Maßnahmen sind u.a. Analgetika, nichtsteroidale Antiphlogistika (NSAR), Glucocorticoide und Immunsupressiva gebräuchlich, deren Nebenwirkungen aber hinlänglich bekannt sind und häufig zu einem Abbruch der Therapie führen. Auf der Suche nach besser verträglichen, ebenso gut wirksamen Präparaten werden vielfach Phytopharmaka eingesetzt, die heute jedoch die gleichen Anforderungen hinsichtlich Wirksamkeit, Unbedenklichkeit und Qualität erfüllen müssen. Im Folgenden werden die wichtigsten pflanzlichen Arzneimittel zur externen und internen Anwendung vorgestellt. Fotos: Sertürner (3), Botanikfoto Afrikanische Teufelskralle – Harpagophyti radix In Südafrika wurden die Wurzeln von Harpagophytum procumbens traditionell als bitteres Tonikum sowie als Fieber- und Schmerzmittel verwendet. In Europa wird die Droge hauptsächlich zur Behandlung von Erkrankungen des rheumatischen Formenkreises eingesetzt, so finden sich in der aktuellen Online-Version der Roten Liste insgesamt 23 Präparate, die Extrakte aus der afrikanischen Teufelskralle enthalten [4]. Zur Anwendung gelangen Extrakte aus den sekundären Speicherwurzeln, die mindestens 1,1 % Harpagosid (1) enthalten [5]. Dieses Iridoidglykosid wird weder im Magen noch im Darmsaft gespalten und gut resorbiert [6]. Die im Blut messbaren Konzentrationen korrelieren gut mit der Stärke der beobachteten Wirkung [7]. Die dosisabhängige antientzündliche Wirkung konnte sowohl in vitro über die Hemmung der COX-2 und Cytokinfreisetzung [8,9] als auch in verschiedenen Tiermodellen nachgewiesen werden [10,11]. In etwa zehn wenig aussagekräftigen klinischen Studien konnte jeweils nur ein Wirksamkeitstrend bei degenerativen Gelenkerkrankungen und Rückenschmerzen erkannt werden [12], besser sind die in referierten Zeitschriften veröffentlichten Studienergebnisse. Dort konnte mit unterschiedlichen Extrakten mit einer Tagesdosis zwischen 24 und 100 mg Harpagosid in randomisierten Doppelblindstudien eine dosisabhängige, signifikante Wirkung gegenüber Placebo gezeigt werden [13,14]. In einer weiteren Studie fand man abschließend heraus, dass die Behandlungskosten im Vergleich zur konventionellen Therapie deutlich gesenkt werden können, wenn die Harpagophytum-Extrakte allein oder zusammen mit anderen Therapeutika eingesetzt werden [15]. Die besten Harpagophytum-Extrakte (60 mg Tagesdosis) führten sogar im Vergleich mit dem COX-2 Hemmstoff Rofecoxib (12,5 mg Tagesdosis) zu einer vergleichbaren Anzahl schmerzfreier Patienten nach 6 Wochen [8]. Wichtig ist die Konzentration an Harpagosid im jeweiligen Extrakt. So konnte eindeutig gezeigt werden, dass die in der Monographie der „European Scientific Cooperative on Phytotherapy (ESCOP)“ zur Behandlung schmerzhafter Arthrosen empfohlene Tagesdosis von 100 mg (etwa 10 g Wurzel) zu einer signifikant besseren Schmerzreduktion führt als die in der deutschen Monographie empfohlene halbe Dosis [16]. In den in der Roten Liste aufgeführten 28 Präparaten sind ganz unterschiedliche Extrakte enthalten. Zur besseren Transparenz ist bei den nicht zur homöopathischen Therapierichtung gehörenden Präparaten das Droge-Extrakt-Verhältnis (DEV) angegeben. Mit dieser Angabe ist es möglich, die enthaltenen Extraktmengen in Drogenäquivalente umzurechnen. Auf dieser Ebene können die unterschiedlichen Präparate dann in etwa verglichen werden. Für die zur Behandlung rheumatischer Erkrankungen hergestellten Fertigarzneimittel wurden Extraktmengen zwischen 140 und 600 mg eingesetzt. Die jeweiligen DEV lagen zwischen 1,5-2,5:1 (d.h. 1 Teil Extrakt entspricht 1,5-2,5 Teilen Droge) und 5-10:1. Rechnet man mit Hilfe der Einnahmeempfehlung pro Tag die maximale Drogenmenge pro Tag aus, so ergeben sich maximale Höchstmengen zwischen 2,5 und 8,0 g. Alle Präparate liegen damit unter der von der ESCOP geforderten Tagesdosis von 9g Droge [5]. Weidenrinde – Salicis cortex Die Weidenrinde ist eine weithin bekannte Droge, die Salicylderivate vom Typ des Salicins (2) enthält. In der ESCOP Monographie wird für die Weidenrinde eine Tagesdosis für Erwachsene von 240 mg Salicin pro Tag gefordert [16a]. Das Salicin besitzt selbst keine ent- 9 PHARMAZEUTISCHE WISSENSCHAFT zündungshemmende Aktivität, es wird als Salicylalkoholglucosid nach Abspaltung der Glucose zu Salicylsäure oxidiert. Aus 240 mg eingenommenem Salicin entstehen so etwa 90 mg Salicylsäure [17]. Offenbar ist die Salicylsäure nicht allein an der Wirkung der Weidenrinde beteiligt, denn auch die enthaltenen Flavonoide tragen über die Hemmung der Lipoxygenase und durch ihre antioxidativen Eigenschaften wesentlich zur Schmerzlinderung bei [18]. Die ebenfalls beobachtete Hemmung der Cytokinfreisetzung konnte bisher jedoch noch nicht einem Inhaltsstoff zugeordnet werden [19]. Auch zur Wirkung der Weidenrinde wurden mehrere Studien an Weidenrinde – Salicis cortex unterschiedlichen Patientenkollektiven durchgeführt. Zwei Doppelblindstudien zeigten die Wirksamkeit des Extraktes (DEV 814:1, 70 % Ethanol, Salicingehalt > 15 %) gegenüber Placebo bei Patienten mit chronischen Rückenschmerzen bzw. Hüft- und Knieschmerzen [20, 21]. Auch für die Weidenrinde konnte gezeigt werden, dass die in Deutschland vorgeschlagene Dosis von 120 mg Salicin/Tag zu gering gewählt wurde. Mit der von der ESCOP vorgeschlagenen doppelt so hohen Dosierung konnten wesentlich bessere Ergebnisse erzielt werden [20, 21]. Daneben konnte auch gezeigt werden, dass durch die adjuvante Therapie mit Weidenrindenextrakten der Verbrauch an NSAR deutlich gesenkt werden kann, was zu einer wesentlichen Verringerung der Therapiekosten führt. Die Behandlungsdauer ist nicht limitiert, so dass die Weidenrinde auch bei chronischen Krankheitsverläufen eingesetzt werden kann. Mit einer dauerhaften Hemmung der Thrombozytenaggregation muss nicht gerechnet werden [22]. Die Onlineversion der Roten Liste verzeichnet unter dem Wirkstoff Weide insgesamt 9 Präparate, darunter 3 homöopathische bzw. anthroposophische Kombinationen und ein phytotherapeutisches Kombinationspräparat. Legt man die von der ESCOP geforderte Salicintagesdosis von 240 mg zugrunde, so errechnet sich bei einem Salicingehalt von 1 % (Mindestgehalt DAB) eine tägliche Drogenmenge von 24 g/Tag. Von den in der Roten Liste aufgeführten Präparaten erreicht nur ein Präparat diesen Wert näherungsweise. Die übrigen Präparate erfüllen zwar alle die in Deutschland geforderte Norm, liegen aber nur bei der Hälfte der ESCOP Angaben. Brennnesselkraut/-blätter – Urticae herba Auch Extrakte aus den Blättern bzw. dem Kraut von Urtica dioica werden therapeutisch zur Schmerzbehandlung bei Erkrankungen des rheumatischen Formenkreises eingesetzt. In der ESCOP-Monographie wird eine Tagesdosis von bis zu 15 g Droge als Tee verteilt auf drei Gaben empfohlen [23]. Als wirksame Substanzen mit antirheumatischer Wirkung wird neben Flavonoiden und bisher unbekannten Cytokin-freisetzenden Stoffen vor allem die Kaffeoyläpfelsäure (3) angesehen. Diese Verbindung inhibiert genauso wie auch die Extrakte die Cyclooxygenase, die 5-Lipoxygenase wird dagegen von den Extrakten nur gering beeinflusst, während die isolierte Verbindung dosisabhängig die Bildung des Leukotrien B4 hemmt [24]. Innerhalb der Pflanze ist die Kaffeoyläpfelsäure ungleichmäßig verteilt. Die höchsten Konzentrationen wurden je nach Extraktionsbedingungen bisher in den Blättern gefunden [25]. Obwohl die Kaffeoyläpfelsäure als einer der Wirkstoffe der Droge bzw. der daraus hergestellten Extrakte angesehen werden muss, ist die klinische Effizienz der angewandten Präparate nicht an den Gehalt an Kaffeoyläpfelsäure gebunden [26]. Weitere Untersuchungen in vitro deuten darauf hin, dass Brennnesselextrakte durch Hemmung des Transkriptionsfaktors NF-κB zu einer Reduktion von nachfolgend gebildeten Entzündungsmediatoren führen. Gleichzeitig konnte beobachtet werden, dass die Extrakte über die Aktivierung des nukleären Rezeptors PPARγ zu einer Supprimierung proinflammatorischer Gene führen. Als Wirksubstanz konnte 13-Hydroxyoctadecatriensäure (13-HOTE) identifiziert werden. Dieses so genannte Oxylipin interagiert genauso wie die getesteten Extrakte mit beiden oben genannten Zielproteinen [27]. Im Vergleich zur Teufelskralle wurden bisher nur wenige klinische Untersuchungen mit Urtica dioica durchgeführt. In allen bisher durchgeführten Studien konnte jedoch eindeutig gezeigt werden, dass die geprüften Urtica-Extrakte einer Placebo-Medikation deutlich überlegen sind [28]. Von den 37 Präparaten, die die Rote Liste mit dem Wirkstoff Brennnessel verzeichnet, sind nur sechs Präparate als Phytotherapeutika zur Anwendung bei Rheuma zugelassen. Bei den übrigen handelt es sich entweder um Präparate zur Behandlung der benignen Prostatahyperplasie oder um registrierte homöopathische Arzneimittel ohne Indikationsangabe. Berechnet man die täglich zugeführte Drogenmenge mit Hilfe der Dosierungsangaben der enthaltenen Extraktmengen und dem DEV, so erhält man bei Einnahme der jeweils vorgeschlagenen Höchstmengen Drogenäquivalente zwischen 10 und 14 g/Tag. Auch hier liegt die zugefügte Tagesdosis, wenn auch nur geringfügig, unterhalb der von der ESCOP vorgeschlagenen Tagesdosis von 15 g Droge. Brennnesselkraut/-blätter – Urticae herba 10 Neben den oben genannten Drogen werden auch Kombinationspräparate zur Behandlung rheumatischer Erkrankungen eingesetzt. Eines der bekanntesten wird aus frischen Blättern und Rinde der Pappel (Populus tremula), dem Kraut der Goldrute (Solidago virgaurea) und der Rinde der Esche (Fraxinus excelsior) gewonnen. Das Präparat ist auf das Flavonoid Rutin (4), Salicin (2) und Fraxin (5) standardisiert. Die empfohlene Tagesdosierung beträgt dreimal 30-50 Tropfen. Die entzündungshemmende Wirkung dieses Kombinationspräparates wurde sowohl in vitro als auch in vivo nachgewiesen [29]. Die antiphlogistische Wirkung beruht im Wesentlichen auf der Reduktion von Entzündungsmediatoren durch Hemmung der Cyclooxygenase und Lipoxygenase, unterstützt durch ausgeprägte antioxidative Eigenschaften [29]. In randomisierten, placebokontrollierten Doppelblindstudien konnte die Wirksamkeit dieses Extraktes bei geringen bis mäßigen Beschwerden belegt werden. Auch mit diesem Extrakt konnte insbesondere wegen der geringen Nebenwirkungsrate und Toxizität eine Kostenreduktion während der konventionellen Rheumatherapie erzielt werden. Kontraindiziert sind solche Präparate lediglich bei Überempfindlichkeit gegenüber Salicylaten. Fotos: Sertürner (2), Archiv; Abbildungen: Passreiter Kombinationspräparate Zertifizierte Fortbildung Weitere pflanzliche Antirheumatika zur innerlichen Anwendung Neben den hier vorgestellten häufig verwendeten pflanzlichen Antirheumatika gibt es eine ganze Reihe weiterer Arzneipflanzen zur innerlichen Anwendung. Zu ihnen zählen zum Beispiel die Johannisbeerblätter, die von der ESCOP Monographie zur adjuvanten Behandlung rheumatischer Erkrankungen empfohlen werden [30]. Abbildung 1 Goldrute – Solidago virgaurea Johannisbeerblätter enthalten mindestens 1,5 % Flavonoide, berechnet als Rutin. Auch für Johannisbeerblätter konnte in vitro und in vivo gezeigt werden, dass sowohl die Biosynthese der Prostaglandine als auch die der Leukotriene beeinflusst wird [31]. Die Extrakte wirkten bei allen Untersuchungen stärker als die isolierten Einzelstoffe, weshalb entweder synergistische Effekte einzelner Substanzen vorliegen oder das Wirkprinzip noch nicht gefunden wurde. Klinische Untersuchungen mit Johannisbeerblättern wurden bisher noch nicht durchgeführt. Ganz anders beim Indischen Weihrauch, Boswellia serrata. Diese aus der Ayurvedischen Medizin Indiens stammende als „Salai guggal“ bezeichnete Droge wurde pharmakologisch im Tübinger Institut von Prof. Ammon eingehend untersucht [32,33]. Aus dem Harz hergestellte Extrakte führten zu einer deutlichen Abnahme des Leukotrien B4 über eine Hemmung der 5-Lipoxygenase. Als Wirkstoffe in den Extrakten wurden die Boswelliasäuren, z.B. die Acetyl-11-keto-β-Boswelliasäure (6) erkannt, die auch als Reinsubstanzen zu einer signifikanten, dosisabhängigen Abnahme der durch Aktivität der 5-Lipoxygenase hergestellten Produkte führten [33]. Da die Boswelliasäuren im Gegensatz zu vielen anderen Hemmstoffen der 5-Lipogenase den Prostaglandinstoffwechsel nicht hemmen, handelt es sich bei diesen Verbindungen um selektive Hemmstoffe der 5-Lipoxygenase, die demnach gut bei allen Erkrankungen mit erhöhter 5-Lipoxygenaseaktivität einsetzbar sein könnten. In Bezug auf die Behandlung rheumatischer Erkrankungen ist die gleichzeitige Wirkung auf die humane Leukozytenelastase von besonderem Interesse, da dieses Enzym bei Entzündungen in Gelenken wesentlich an der Knorpelauflösung und daraus resultierenden Problemen beteiligt ist. Leider ist es bisher aufgrund fehlender Finanzmittel nicht gelungen, hinreichend aussagekräftige klinische Studien für eine Zulassung der Weihrauch-Extrakte vorzulegen. Die bisher vornehmlich in Indien durchgeführten Untersuchungen belegen jedoch eindrucksvoll die Wirksamkeit der Extrakte bei verschiedenen Krankheitsbildern. Es bleibt zu hoffen, dass in Kürze das Geld für eine breiter angelegte Studie zur Verfügung stehen wird, damit auch der indische Weihrauch als Arzneimittel genutzt werden kann. Abbildung 2 Abbildung 3 Abbildung 4 Abbildung 5 11 PHARMAZEUTISCHE WISSENSCHAFT Abbildung 6 Literatur 1 Shek PN and Shephard RJ Physical exercise as a human model of limited inflammatory response. Can. J. Physiol Pharmcol. 1998; 76: 589-597. 2 Pass HI, Mew D, Pass HA, Temeck BK The macrophage, TNF, and other cytokines. Chest. Surg. Clin. N. Am. 1995; 5: 73-90. 3 Schulz V, Hänsel R Rationale Phytotherapie. 5. Auflage, Springer Verlag, Berlin; 2004. 4 Rote Liste online, www.roteliste.de 5 Harpagophyti radix. ESCOP Monograph 2nd Ed. 2003, Fascicule 2. 6 Chrubasik S, Sporer F, Dillmann-Marschner R, Friedmann, A, Wink, M. Physikalisch Chemische Eigenschaften von Harpagosid und invitro Freisetzung von Harpagosid aus Harpagophytum Tabletten. Phytomedicine 2000; 6: 469-473. 7 Loew D, Moellerfeld J, Schroedter A, Puttkammer S, Kaszkin M. Investigation on the pharmacokinetic properties of Harpagophytum extracts and their effects on eicosanoid biosynthesis in vitro and ex viso. Clin. Pharmacol. Ther. 2001; 69:356-64. 8 Chrubasik S, Fiebich B, Black A, Pollack S Treating low back pain with an extract of Harpagophytum that inhibits cytokine release. Eur. J. Anaesthesiol. 2002; Suppl. 9 Fiebich B, Heinrich M, Hiller K-O, Kammerer N Inhibition of TNF_ in LPS-stimulated primary human monocytes by Harpagophytum extract SteiHap 69. Phytomedicine 2001; 8:28-30. 10 Baghdikian B, Lanhers MC, Fleurentin J, Ollivier E, Maillard C, Balansard G, Mortier F An analytical study, anti-inflammatory and analgesic effects of Harpagophytum procumbens and Harpagophytum zeyheri. Planta med. 1997; 63:171-176. 11 Chrubasik S, Wink M Zur pharmakologischen Wirkung der Teufelskralle (Harpagophytum procumbens). Forschende Komplementärmed. 1995; 2: 323-325. Der Autor Professor Dr. Claus Passreiter Wissenschaftlicher Mitherausgeber des Apotheken-Magazins 12 12 Chrubasik S Effectiveness and safety of Harpagophytum extract. Phytomedicine 2000; Suppl II: 83. 13 Chrubasik S, Zimpfer C, Schütt U, Ziegler R Effectiveness of Harpagophytum procumbens in treatment of acute low back pain. Phytomedicine 1996; 3:1-10. 14 Chrubasik S, Junck H, Breitschwerdt H, Conradt C, Zappe H Effectiveness of Harpagophytum extract WS 1531 in the treatment of exacerbation of low back pain: a randomized placebo-controlled double-blind study. Eur. J. Anaesthesiol. 1999; 16:118-129. 15 Chrubasik S, Schmidt A, Junck H, Pfisterer M Wirksamkeit und Wirtschaftlichkeit von Teufelskrallenextrakt bei Rückenschmerzen: erste Ergebnisse einer Anwendungsbeobachtung. Forsch. Komplementärmed. 1997; 4, 332-336. 16 Harpagophyti Radix, BAnz. 1989, 43. 16a Salicis cortex. ESCOP Monograph 2nd Ed. 2003., Fascicule 4. 17 Schmid B, Kötter, J, Heide L Pharmacokinetics of Salicin after oral administration of a standardized willow bark extract. Eur. J. Clin. Pharmacol. 2001; 57:387-391. 18 Chrubasik S Weidenrindenextrakt. Dtsch. Apoth. Ztg. 2000; 140:83-85. 19 Chrubasik S, Fiebich B, Black A, Pollack S Treating low back pain with Salix extract that inhibits COX-2 release and the release of cytokines. Eur. J. Anaesthesiol. 2002; Suppl. 20 Chrubasik S, Eisenberg E, Balan E, Weinberger T, Luzzatti R, Conradt Ch Treatment of low back exacerbations with willow bark extract: a randomized double-blind study. Am. J. Med. 2000; 109, 914. 21 Schmid B, Lüdtke R, Selbmann HK, Tschirdewahn B., Schaffner W., Heide L Wirksamkeit und Verträglichkeit eines standardisierten Weidenrindeextraktes bei Arthrose Patienten: Randomisierte, placebo-kontrollierte Doppelblindstudie. Z. Rheumatologie 2000; 59:1-7. 22 Krivoy N, Pavlotzky E, Chrubasik S, Eisenberg E, Brooks G Effect of Salicis Cortex extract on human platelet aggregation. Planta med. 2001; 67: 209-213. 23 Urticae folium/herba. ESCOP Monograph 2nd Ed. 2003. Fascicule 4. 24 Obertreis B, Giller K, Teucher T Antiphlogistische Effekte von Extractum Urticae dioicae foliorum im Vergleich zu Kaffeoyläpfelsäure. Drug. Res. 1996; 46:52-56. 25 Bauer R, Holz A, Chrubasik S Kaffeoyläpfelsäure als Leitsubstanz in Zubereitungen aus der Brennnessel (Urtica dioica). In Chrubasik S Loew D (eds) Rheumatherapie mit Phytopharmaka. Stuttgart. Hippokrates-Verlag, 1997, pp 112-120. 26 Chrubasik S, Bauer R, persönliche Mitteilung. 27 Klingelhöfer S. Isolierung und Charakterisierung antiinflammatorischer Oxylipine aus Blattextrakten von Urtica dioica L., Dissertation Universität Kiel, 2001. 28 Randall C, Randall H, Dobbs F, Hutton C, Sanders H.. Randomized controlled trial of nettle sting for treatment of base-of-thumb pain. J R Soc Med. 2000; 93:305. 29 Kruedener S, Schneider W, Elstner E. Effects of extracts from Populus tremula, Solidago virgaurea L. and Fraxinus excelsior L. on various myoperoxidase systems. Arzeimittel Forsch. 1996; 46:809814. 30 Ribis nigri folium. ESCOP Monograph 2nd Ed. 2003, Fascicule 4. 31 Pham HC, Ifansyah N, Chahine R, Mounayar-Chalfoun A, Gleye J, Moulis C Comparative effects on total flavonoids extracted from Ribes nigrum leaves, rutin and isoquercitrin on biosynthesis and release of prostaglandins in the ex-vivo rabbit heart. Prostagl. Leokotr. Med. 1986; 22: 295-300. 32 Wildfeuer A, Neu IS, Safayhi H, Metzger G, Wehrmann M, Vogel U, Ammon HP. Effects of boswellic acids extracted from a herbal medicine on the biosynthesis of leukotrienes and the course of experimental autoimmune encephalomyelitis. Arzneimittelforschung. 1998; 48:668. 33 Ammon HP. Boswellic acids (components of frankincense) as the active principle in treatment of chronic inflammatory diseases. Wien Med Wochenschr. 2002; 152:373. Fortbildungs-Fragebogen 3/2008 Faxnummer: 02 08 / 6 20 57 41 ▼ ▼ Hier finden Sie die Fortbildungsfragen zum Hauptartikel. Bei Beantwortung und Faxantwort erhalten Sie einen Fortbildungspunkt auf dem Postweg. Sie erhalten den Fortbildungspunkt für die Kategorie „Bearbeiten von Lektionen“ (rezertifiziert durch die Bundesapothekerkammer, Veranstaltungs-Nr.: BAK 2006/36). Es ist pro Aufgabe nur eine Antwort richtig. Die Lösungen werden Ihnen zusammen mit dem Fortbildungspunkt mitgeteilt. Bitte tragen Sie unbedingt Ihre Postanschrift und Ihre Telefon-Nummer (für evtl. Rückfragen) in das Faxformblatt ein! 1. Entzündungen sind Abwehrmechanismen des Körpers, die mit der Aktivierung folgender Zellen einhergehen: A) 앮 Granulozyten B) 앮 Erythrozyten C) 앮 Hepatozyten D) 앮 Thrombozyten E) 앮 Parazyten 6. Die Kaffeoyläpfelsäure 1. hemmt die Freisetzung von Leukotrien B4. 2. ist im Kraut von Urtica dioica enthalten. 3. ist in der Pflanze gleichmäßig verteilt. 4. ist für die Wirksamkeit der verschiedenen Brennnessel-Extrakte nicht entscheidend. 5. ist einer der wirksamen Bestandteile der Brennnessel. 2. Charakteristisch für degenerative Prozesse (Arthrose) sind: A) 앮 Schmerzende Gelenke ohne Belastung. B) 앮 Nächtliche Schmerzen. C) 앮 Gerötete Gelenke. D) 앮 Schmerz bei Belastung. E) 앮 Schmerz auch bei Schonhaltung. A) 앮 B) 앮 C) 앮 D) 앮 E) 앮 3. Bei A) 앮 B) 앮 C) 앮 D) 앮 E) 앮 1,2,4 und 5 sind richtig. 1,2 und 3 sind richtig. 1,2,3 und 4 sind richtig. 3,4 und 5 sind richtig. 2,3, und 5 sind richtig. 7. Bei Langzeittherapie mit Weidenrindenextrakten kommt es zu keiner dauerhaften A) 앮 Entzündungshemmung. B) 앮 Verringerung des Verbrauches an NSAR bei Kombinationsbehandlung. C) 앮 Hemmung der Cytokinfreisetzung. D) 앮 Als Roburans. E) 앮 Hemmung der Thrombozytenaggregation. Harpagosid handelt es sich um ein Triterpenglykosid. einen Sesquiterpenlacton. ein Iridoidglykosid. das Monoterpenalkaloid. ein bitter schmeckendes Phenol. 4. Die in der ESCOP Monographie geforderte Salicin-Tagesdosis beträgt für Erwachsene A) 앮 120 mg. B) 앮 240 mg. C) 앮 360 mg. D) 앮 60 mg. E) 앮 180 mg. 8. Bei der Acetyl-11-keto-β-Boswelliasäure handelt es sich um einen selektiven Hemmstoff der A) 앮 Cyclooxygenase. B) 앮 Phospholipase A2. C) 앮 5-Lipoxygenase. D) 앮 Prostaglandinsynthase. E) 앮 Glucuronidase. 5. Beim DEV handelt es sich um A) 앮 den Verein deutscher Entzündungserkrankter. B) 앮 das Verhältnis aus Droge und Extrakt. C) 앮 das Verhältnis aus Drogenextrakt und Einwaage. D) 앮 das Verhältnis aus Droge und Extraktionsmittel. Berufsbezeichnung: 앮 Apotheker/in 앮 PTA BITTE UNBEDINGT IHRE POSTANSCHRIFT HIER EINTRAGEN! Ja, ich möchte das ApothekenMagazin regelmäßig erhalten! Bitte ankreuzen Lösen Sie – exklusiv für Abonnenten – den ABO-Fragebogen in dieser Ausgabe und Sie erhalten einen zusätzlichen Fortbildungspunkt! Ich abonniere das Apotheken-Magazin zum Jahresvorzugspreis von 25,– EUR (10 Ausgaben inkl. MwSt. und Versand, Inland). Das Abonnement gilt für ein Jahr und kann danach jederzeit gekündigt werden. Wichtig: Dieses Angebot gilt nur in der Bundesrepublik Deutschland. Gebr. Storck GmbH & Co. Verlags-oHG · Duisburger Straße 375 (C-Gebäude) 46049 Oberhausen · Telefon 02 08-8 48 02 24 · Fax 02 08-8 48 02 42 Apothekenstempel Faxnummer: 02 08 / 6 20 57 41 13