Skriptum - Universität Wien
Werbung

Biophysik I
Aufbau und Strukturanalyse von Biomolekülen
Dieter Baurecht
Institut für Biophysikalische Chemie, Universität Wien, 2006
(Version 1.3, 18.10.2007)
Dieter Baurecht
Biophysik I
INHALTSVERZEICHNIS
1
WAS IST BIOPHYSIK
1
2
HIERARCHIE BIOLOGISCHER SYSTEME
2
3
GRUNDLAGEN CHEMISCHER BINDUNG
3
3.1
Die Ionenbindung (herteropolare Bindung)
3.1.1
Ionenkristalle
3.1.2
Gitterenergie von Ionenkristallen
3
3
4
3.2
Die kovalente Bindung (Atombindung, homöopolare Bindung)
3.2.1
Valenzbindungstheorie
3.2.2
Die Molekülorbitaltheorie
3.2.3
Hybridisierung
3.2.4
π-Bindung
3.2.5
Polare Atombindung, Dipole
3.2.6
Elektronegativität
6
6
7
8
9
10
11
3.3
Van der Waals-Kräfte
12
3.4
Die Wasserstoffbrückenbindung
13
4
STRUKTUR UND FUNKTION DER PROTEINE
15
4.1
Aminosäuren, die Bausteine der Proteine
4.1.1
Grundstruktur
4.1.2
Die 20 Aminosäuren
4.1.3
pK-Werte von Aminosäuren
15
15
16
19
4.2
20
Die Peptidbindung
4.3
Die dreidimensionale Proteinstruktur
4.3.1
Primärstruktur
4.3.2
Sekundärstruktur
4.3.3
Tertiärstruktur
4.3.4
Quartärstruktur
21
21
21
24
25
4.4
Proteinfunktionen
4.4.1
Enzyme als Biokatalysatoren
4.4.1.1 Die Wirkungsweise von Enzymen
4.4.1.2 Enzymkinetik
27
27
28
29
5
LIPIDE
34
6
SPEKTROSKOPISCHE METHODEN ZUR STRUKTURAUFKLÄRUNG
36
6.1
Eigenschaften elektromagnetischer Strahlung
6.1.1
Spektralbereiche elektromagnetischer Strahlung
36
36
Dieter Baurecht
6.1.2
6.1.3
6.2
Energie der elektromagnetischen Strahlung
Absorption von Licht, Lambert-Beer Gesetz
UV/Vis Spektroskopie
36
37
38
6.3
Optische Rotation und Circulardichroismus
6.3.1
Optische Rotation
6.3.2
Zirkulardichroismus
6.3.3
Molekulare Ursachen
6.3.4
Experimentelle Techniken zur Messung von OR und CD
38
38
41
42
44
6.4
Infrarot Spektroskopie
6.4.1
IR-aktive Schwingungen, Dipolmomentsänderungen
6.4.1.1 Beispiel CO2 Schwingungstypen
6.4.2
Vibrations-Energieniveaus im 2-atomigen Molekül
6.4.2.1 Modell des klassischen harmonischen Oszillators
6.4.2.2 Der quantenmechanische harmonischen Oszillators
6.4.2.3 Der quantenmechanische anharmonische Oszillator
6.4.3
Vibrationsmoden mehratomiger Moleküle
6.4.3.1 Schwingungsfreiheitsgrade, Normalschwingungen
6.4.3.2 Gruppenschwingungen und Gerüstschwingungen
6.4.3.3 Beispiel: Normalschwingungen der Amidbindung
6.4.4
Messprinzip der IR-Spektroskopie
6.4.4.1 Fourier Transform Infrarot (FTIR)-Spektrometer
6.4.4.2 ATR-Spektroskopie
44
44
45
46
46
47
48
49
49
49
51
52
52
53
6.5
Raman-Spektroskopie
6.5.1
Teilchenmodell
6.5.2
Klassische Theorie der Raman Streuung
6.5.3
Raman-aktive Schwingungen
6.5.4
Raman-Spektrometer
55
55
56
56
58
6.6
Kernspinresonanzspektroskopie
6.6.1
Einleitung
6.6.2
Kernspin
6.6.3
Chemische Verschiebung
6.6.4
Spin-Spin Kopplung
6.6.5
Messtechnik
6.6.5.1 Klassische Beschreibung des NMR-Experiments
6.6.5.2 Continuous Wave
6.6.5.3 Puls-Fourier-Transform-Spektroskopie
6.6.6
Biophysikalische Anwendungen der NMR
6.6.6.1 Beobachtung der Helix-Knäuel-Umwandlung an Proteinen
6.6.6.2 NMR an Membranen
6.6.6.3 Ortsaufgelöste NMR-Spektroskopie
59
59
60
61
62
63
63
65
65
66
66
67
68
7
70
ÜBUNGSBEISPIELE
7.1
pH Wert
70
7.2
Isoelektrischer Punkt und Ladungsverteilungen
71
Biophysik I
1 Was ist Biophysik
Wer den Umfang der klassischen Fächer wie Physik, Chemie oder Biologie annähernd erahnen
kann, wird verstehen, dass die Biophysik, die mit all diesen Disziplinen verknüpft ist, nicht gerade
einfach zu definieren ist. Im Prinzip wird der Begriff für alle Versuche biologische Vorgänge auf
physikalisch-chemischen Niveau zu erklären verwendet. Das reicht von Systemen auf molekularer
Ebene (Molekulare Biophysik) bis zu mechanischen Eigenschaften biologische Systeme
(Biomechanik). Einige Teildisziplinen sind (1):
•
•
•
•
•
•
•
Molekulare Biophysik
Neurobiophysik
Photobiophysik
Biomechanik
Kybernetik
Evolution
Strahlenbiophysik
Diese Vorlesung wird sich im wesentlichen dem Bereich Molekulare Biophysik widmen. Dabei
werden der Aufbau, die Strukturanalyse und die Funktion von Biomolekülen und Biomembranen
behandelt. Die grundlegenden biophysikalischen Kenntnisse dieser Systeme spielen in vielen
grundlegenden Fachbereichen (Physik, Chemie, Biologie) aber auch in anwendungsorientierten
Fachbereichen (Medizin, Pharmakologie, Biotechnologie) eine große Rolle.
Was ist Biophysik
1
Dieter Baurecht
2 Hierarchie biologischer Systeme
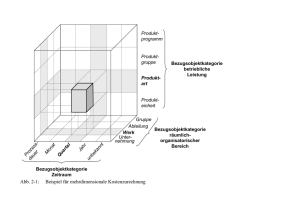
Der Aufbau biologischer Systeme erfolgt in klar abgrenzbaren hierarchischen Systemen (Abb. 1).
Mit jeder neuen Organisationsstufe steigt die Komplexität der ablaufenden Prozesse. Es ist
(momentan?) nicht möglich, die Lebensvorgänge eines Organismus gänzlich mit physikalischen
Beschreibungen auf der Basis atomarer Wechselwirkungen zu verstehen. Daher wird auf allen
Ebenen der Hierarchie mit unterschiedlichen Methoden und Ansätzen geforscht, und es wird
schrittweise vorgegangen. Auf jeder neuen Organisationsstufe kommen neue Phänomene hinzu, die
bei weniger komplexen Systemen nicht auftreten. Die "Sprache" der einzelnen Disziplinen wird
dadurch auch unterschiedlich sein. Für Physiker die im Fach Biophysik tätig sind ist es daher auch
wichtig die Sprache der anderen Disziplinen zu verstehen.
Abb. 1: Hierarchie biologischer Systeme mit typischer Anzahl an Atomen (aus 2)
2
Hierarchie biologischer Systeme
Biophysik I
3 Grundlagen chemischer Bindung
Die Bindungskräfte, die zur Bildung chemischer Verbindungen führen, sind unterschiedlicher
Natur. Es werden daher verschiedene Grenztypen der chemischen Bindung unterschieden:
•
•
•
•
•
die Ionenbindung
die kovalente Bindung
die metallische Bindung
die van der Waals-Bindung
die Wasserstoffbindung
Diese Bindungstypen sind "Idealtypen", es bestehen fließende Übergänge.
3.1 Die Ionenbindung (herteropolare Bindung)
Ionenbindungen entstehen durch Vereinigung von ausgeprägten metallischen Elementen (Alkali-,
Erdalkalielemente) mit ausgeprägt nichtmetallischen Elementen (Halogene, Sauerstoff).
3.1.1 Ionenkristalle
Als typisches Beispiel einer Ionenbindung soll Natriumchlorid NaCl besprochen werden. Bei der
Reaktion von Natrium mit Chlor werden von den Na-Atomen, die die Elektronenkonfiguration
1s22s22p63s1 besitzen, die 3s-Elektronen abgegeben. Dadurch entstehen die einfach positiv
geladenen Ionen Na+. Diese Ionen haben die Elektronenkonfiguration des Edelgases Neon
1s22s22p6. Man sagt, sie haben Neon-konfiguration. Die Cl-Atome nehmen die abgegebenen
Elektronen unter Bildung der einfach negativ geladenen Ionen Cl- auf. Aus einem Cl-Atom mit der
Elektronen-konfiguration 1s22s22p63s23p5 entsteht durch Elektronenaufnahme ein Cl-Ion mit der
Argonkonfiguration 1s22s22p63s23p6. Stellt man die Elektronen der äußersten Schale als Punkte dar
läßt sich dieser Vorgang folgendermaßen formulieren:
Durch Elektronenübergang vom Metallatom zum Nichtmetallatom entstehen aus den neutralen
Atomen elektrisch geladene Teilchen, Ionen. Die positiv geladenen Ionen bezeichnet man als
Kationen, die negativ geladenen als Anionen.
Wegen der veränderten Elektronenkonfiguration zeigen die Ionen gegenüber den neutralen Atomen
völlig veränderte Eigenschaften. Cl- und Na-Atome sind chemisch aggressive Teilchen. Die Ionen
Na+ und Cl- sind harmlose, reaktionsträge Teilchen. Die chemische Reaktionsfähigkeit wird durch
die Elektronenkonfiguration bestimmt. Teilchen mit der abgeschlossenen Elektronenkonfiguration
der Edelgase sind chemisch reaktionsträge. Dies gilt nicht nur für die Edelgasatome selbst, sondern
auch für Ionen mit Edelgaskonfiguration.
Kationen und Anionen ziehen sich aufgrund ihrer entgegengesetzten elektrischen Ladung an. Die
Anziehungskraft wird durch das Coulombsche Gesetz beschrieben. Es lautet für ein Ionenpaar
F=
z K ez A e
4πε 0 r 2
1
(1)
Es bedeuten: zK und zA Ladungszahl des Kations bzw. Anions, e Elementarladung, ε0 elektrische
Feldkonstante, r Abstand der Ionen.
Die Anziehungskraft F ist proportional dem Produkt der Ionenladungen zKe und zAe. Sie ist
umgekehrt proportional dem Quadrat des Abstandes r der Ionen.
Die elektrostatische Anziehungskraft ist ungerichtet, das bedeutet, dass sie in allen Raumrichtungen
wirksam ist. Daher umgeben sich die positiven Na+-Ionen symmetrisch mit möglichst vielen
negativen Cl--Ionen und die negativen Cl--Ionen mit positiven Na+-Ionen. Aus den Elementen
Natrium und Chlor bildet sich daher nicht eine Verbindung, die aus Na+ Cl--Ionenpaaren besteht,
Grundlagen chemischer Bindung
3
Dieter Baurecht
sondern es entsteht ein Ionenkristall, in dem die Ionen eine regelmäßige dreidimensionale
Anordnung, ein Kristallgitter bilden. Abb. 2 zeigt die Anordnung der Na+- und Cl--Ionen im NaClKristall. Jedes Na--Ion ist von 6 Cl--Ionen und jedes Cl--Ion von 6 Na+-Ionen in oktaedrischer
Anordnung umgeben. Charakteristisch für die verschiedenen Kristallgitter-Typen ist die
Koordinationszahl KZ. Sie gibt die Anzahl der nächsten gleich weit entfernten Nachbarn eines
Gitterbausteins an. Im NaCl-Kristall haben beide Ionensorten die Koordinationszahl sechs.
Abb. 2: a) Kristallgitter des NaCl-Ionenkristalls (Natriumchlorid-Typ). In den drei Raumrichtungen
existiert die gleiche periodische Folge von Na+- und Cl--Ionen. Damit die Struktur des Gitters besser
sichtbar wird, sind die Ionen nicht maßstabgetreu, sondern nur als kleine Kugeln dargestellt. b) Im NaClGitter hat jedes Na-Ion 6 Cl-Ionen als Nachbarn, die ein Oktaeder bilden. Jedes Cl-Ion ist von 6 Na-Ionen
in oktaedrischer Anordnung umgeben. Für beide Ionensorten ist also die Koordinationszahl KZ = 6. Jedes
Ion ist daher gleich stark an sechs Nachbarn gebunden (aus 3).
Ionenverbindungen bestehen also nicht aus einzelnen Molekülen, sondern sind aus Ionen
aufgebaute Kristalle, in denen zwischen einem Ion und allen seinen entgegengesetzt geladenen
Nachbarionen starke Bindungskräfte vorhanden sind.
3.1.2 Gitterenergie von Ionenkristallen
Die Gitterenergie von Ionenkristallen ist die Energie, die frei wird, wenn sich Ionen aus unendlicher
Entfernung einander nähern und zu einem Ionenkristall ordnen. Man kann die Gitterenergie von
Ionenkristallen berechnen. Der einfachste Ansatz berücksichtigt nur die Coulombschen
Wechselwirkungskräfte zwischen den Ionen und die Abstoßungskräfte zwischen den
Elektronenhüllen.
Ein Ionenpaar, dessen Ladungen als Punktladungen zKe und zAe im Abstand r betrachtet werden,
hat die elektrostatische potentielle Energie (Coulomb-Energie)
z K z Ae 2
EC =
4πε 0 r
(2)
Da zA negativ ist, ist auch die Coulomb-Energie (bezogen auf unendliche Entfernung der Ionen)
negativ. Befindet sich das Ion der Ladung zKe in einem Kristall, dann kann die Coulomb-Energie
dieses Ions nur durch Berücksichtigung der Wechselwirkung mit allen benachbarten Ionen
berechnet werden. Als Beispiel sei das NaCl-Gitter betrachtet (Abb. 2). Ein Na+-Ion hat in der 1.
Koordinationssphäre im Abstand r 6 Cl--Nachbarn, es folgen 12 Na+ im Abstand r√2, 8 Cl- im
Abstand r√3, 6 Na+ im Abstand r√4, 24 Cl- im Abstand r√5 usw. Die Coulomb-Energie eines Na+Ions im NaCl-Kristall beträgt mit zK=-zA also
EC = −
z K2 e 2
z 2 e2
12
8
6
24
+
−
+
− ... = − K A
(6 −
4πε 0 r
4πε 0 r
2
3
4
5
(3)
Der Klammerausdruck hängt nur von der Gittergeometrie ab, sein Konvergenzwert wird MadelungKonstante A genannt. A hat für das NaCl-Gitter den Wert 1,7476. Beachtet man die
Wechselwirkungen aller Ionen, so erhält man für 1 mol NaCl die Coulomb-Energie
4
Grundlagen chemischer Bindung
Biophysik I
(
)
1
1 z K2 e 2 AN A z K2 e 2 AN A
z K2 e 2 AN A
−
EC = EC , Na + + EC ,Cl − = −
=−
2
2
4πε 0 r
4πε 0 r
4πε 0 r
(4)
NA = 6,022 1023 mol-1 ist die Teilchenanzahl, die ein Mol eines jeden Stoffes enthält (AvogadroKonstante). Der Faktor ½ ist nötig, da man sonst jede Ionen/Ionen Wechselwirkung zweimal zählen
würde.
Die Abstoßungsenergie kann nach Born mit der Beziehung
Er =
(5)
B
rn
beschrieben werden. B und n sind Konstanten, die empirisch bestimmt werden müssen. n hängt
vom Ionentyp ab, läßt sich aus der Kompressibilität von Salzen ableiten und hat meist Werte
zwischen 6 und 10. Ein großer n-Wert bedeutet, dass die Abstoßungskräfte mit wachsendem r sehr
viel schneller abnehmen als die Coulomb-Anziehungskräfte, aber mit abnehmendem r schneller
zunehmen (Abb. 3).
Abb. 3: Energiebeträge bei der Bildung eines Ionenkristalls als Funktion des Ionenabstands. Schon bei
großen Ionenabständen wird Coulomb-Energie frei. Sie wächst bei abnehmendem Abstand mit 1/r. Die
Abstoßungsenergie ist bei größeren Ionenabständen viel kleiner als die Coulomb-Energie, wächst aber
mit abnehmendem Abstand rascher an. Die resultierende Gitterenergie durchläuft daher ein Minimum.
Die Lage des Minimums bestimmt den Gleichgewichtsabstand der Ionen r0 im Gitter. Bei r0 hat die
freiwerdende Gitterenergie den größtmöglichen Wert, der Ionenkristall erreicht einen Zustand tiefster
Energie (aus 3).
Für die Gitterenergie in Abhängigkeit von r erhält man also
z K2 e 2 AN A B
Ug = −
+ n
4πε 0 r
r
Beim Gleichgewichtsabstand muss Ug ein Minimum aufweisen, für das gilt
dU g
z 2 e 2 AN A nB
=0= K
− n+1
4πε 0 r02
r0
dr r =r
0
wodurch bei bekanntem r0, B bestimmt werden kann
B = −
z K2 e 2 AN
n 4 πε 0
A
r0n − 1
und für Ug bei r = r0
Ug = −
z K2 e 2 AN A z K2 e 2 AN A r0n −1
z K2 e 2 AN A 1
+
=
−
1 −
n 4πε 0 r0 n
4πε 0 r0
4πε 0 r0 n
Grundlagen chemischer Bindung
(6)
5
Dieter Baurecht
Im ersten Term ist die Coulomb-Energie, im zweiten Term die Abstoßungsenergie enthalten. Da nWerte von 8 bis 10 häufig sind, ist die Gitterenergie im wesentlichen durch den Beitrag der
Coulomb-Energie bestimmt. Eine Änderung von n hat nur einen geringen Einfluss auf den Wert
von Ug. Die Größe der Gitterenergie ist ein Ausdruck für die Stärke der Bindungen zwischen den
Ionen im Kristall. Daher hängen einige physikalische Eigenschaften der Ionenverbindungen von der
Größe der Gitterenergie ab. Die Berechnung der Gitterenergie kann noch verbessert werden, wenn
außer der Coulomb-Energie und der Abstoßungsenergie weitere Energiebeträge, z.B. die van der
Waals-Energie und die Nullpunktsenergie berücksichtigt werden. Unter der Nullpunktsenergie
versteht man die Schwingungsenergie der Ionen, die der Kristall auch bei 0 K aufweist. Sie
vermindert den Gesamtbetrag der Gitterenergie nur wenig. Die van der Waals-Anziehung ist
zwischen allen Teilchen wirksam. Sie kommt durch Wechselwirkung von Dipolmomenten zustande
(siehe 3.3).
3.2 Die kovalente Bindung (Atombindung, homöopolare Bindung)
Der Zusammenhalt von zwei Atomen erfolgt durch ein gemeinsames Elektronenpaar (oder
mehrere), indem die Elektronenhüllen beide Atombereiche derart durchdringen, dass die
Atomorbitale einander überlappen. Der klassische Valenzstrich ist einem gemeinsamen
Elektronenpaar gleichzusetzen.
Unter Benützung vereinfachter Annahmen dienen zur näherungsweisen Beschreibung der
Atombindung zwei Methoden, die Valenzbindungstheorie (VB-Theorie) und die
Molekülorbitaltheorie (MO-Theorie).
Bei der Valenzbindungstheorie wird von den Atomorbitalen der ungebundenen Atome ausgegangen
und die wesentliche, bei der Molekülbildung eintretende Änderung als Überlappung der
Atomorbitale der benachbarten Atome aufgefasst (Wechselwirkung der Atome bei ihrer
Annäherung).
Bei der Molekülorbitaltheorie werden alle Elektronen eines Moleküls als zu einem einheitlichen
Elektronensystem gehörend angesehen. Nach Konstruktion der Molekülorbitale werden diese in
Reihenfolge zunehmender Energie unter Beachtung des Pauli-Prinzips besetzt.
3.2.1 Valenzbindungstheorie
Die Valenzbindungstheorie geht von einzelnen Atomen aus, berücksichtigt die Wechselwirkung der
Atome bei ihrer Annäherung und erklärt die Bindung durch die Überlappung bestimmter dafür
geeigneter Atomorbitale. Die Bildung des H2-Moleküls läßt sich nach der VB-Theorie wie folgt
beschreiben. Bei der Annäherung zweier Wasserstoffatome kommt es zu einer Überlappung der 1sOrbitale. Überlappung bedeutet, dass ein zu beiden Atomen gehörendes, gemeinsames Orbital
entsteht, das aufgrund des Pauli- Verbots mit nur einem Elektronenpaar besetzbar ist und dessen
beide Elektronen entgegengesetzten Spin haben müssen. Die beiden Elektronen gehören nun nicht
mehr nur zu den Atomen, von denen sie stammen, sondern sie sind ununterscheidbar, können
gegenseitig die Plätze wechseln und sich im gesamten Raum der überlappenden Orbitale aufhalten.
Das Elektronenpaar gehört also beiden Atomen gleichzeitig an. Die Bildung eines gemeinsamen
Elektronenpaares führt zu einer Konzentration der Elektronendichte im Gebiet zwischen den
Kernen, während außerhalb dieses Gebiets die Ladungsdichte im Molekül geringer ist als die
Summe der Ladungsdichten, die von den einzelnen, ungebundenen Atomen herrühren. Die Bindung
kommt durch die Anziehung zwischen den positiv geladenen Kernen und der negativ geladenen
Elektronenwolke zustande. Die Anziehung ist um so größer, je größer die Elektronendichte
zwischen den Kernen ist. Je stärker zwei Atomorbitale überlappen, um so stärker ist die
Elektronenpaarbindung. Atombindungen, die wie bei H2 durch Überlappung von zwei s-Orbitalen
Zustandekommen, nennt man σ-Bindungen.
6
Grundlagen chemischer Bindung
Biophysik I
Abb. 4: σ-Bindungen, die durch Überlappung von s- mit p-Orbitalen gebildet werden können. Bei σBindungen liegen die Orbitale rotationssymmetrisch zur Verbindung der Kerne (aus 3).
3.2.2 Die Molekülorbitaltheorie
Die Molekülorbitaltheorie (Mulliken und Hund 1928) geht von einem einheitlichen
Elektronensystem des Moleküls aus. Die Elektronen halten sich nicht in Atomorbitalen auf, die zu
bestimmten Kernen gehören, sondern in Molekülorbitalen, die sich über das ganze Molekül
erstrecken und die sich im Feld mehrerer Kerne befinden. Hält sich ein Elektron gerade in der Nähe
eines Kernes auf, so wird es von den anderen Kernen wenig beeinflusst werden. Bei
Vernachlässigung dieses Einflusses verhält sich das Elektron so, als ob es sich in einem
Atomorbital des Kerns befände. Das Molekülorbital in der Nähe des Kerns ist näherungsweise
gleich einem Atomorbital. In der Nähe des Kerns A z.B. ähnelt das Molekülorbital dem
Atomorbital ψA. Entsprechend ähnelt das Molekülorbital in der Nähe des Kerns B dem Atomorbital
ψ B.
Abb. 5: Linearkombination von 1s-Atomorbitalen zu Molekülorbitalen. Dargestellt ist sowohl der Verlauf
der Wellenfunktion ψ als auch die räumliche Form der Elektronenwolken der Molekülorbitale. Beide
MOs besitzen σ-Symmetrie, d.h. sie sind rotationssymmetrisch in Bezug auf die x-Achse (aus 3).
Grundlagen chemischer Bindung
7
Dieter Baurecht
Molekülorbitale sind in der einfachsten Näherung Linearkombinationen von Atomorbitalen. Man
nennt diese Methode, Molekülorbitale aufzufinden, abgekürzt LCAO-Näherung (linear combination
of atomic orbitals).
Die Ermittlung der Molekülorbitale für das Wasserstoffmolekül H2 ist anschaulich in Abb. 5
dargestellt. Die 1s-Orbitale der beiden H-Atome kann man auf zwei Arten miteinander
kombinieren. Die erste Linearkombination ist eine Addition führt zu einem Molekülorbital, in dem
die Elektronendichte zwischen den Kernen der Wasserstoffatome konzentriert ist. Dadurch kommt
es zu einer starken Anziehung zwischen den Kernen und den Elektronen. Man nennt dieses
Molekülorbital daher bindendes MO. Elektronen in diesem MO haben eine niedrigere Energie als
in 1s-Atomorbitalen (Abb. 6).
Die Subtraktion der 1 s-Atomorbitale führt zu einem MO mit einer Knotenebene zwischen den
Kernen. Die Elektronen halten sich bevorzugt außerhalb des Überlappungsbereiches auf, das
Energieniveau des Molekülorbitals liegt über denen der 1s-Atomorbitale. Dieses MO nennt man
daher antibindendes MO. Antibindende Molekülorbitale werden mit einem * bezeichnet.
Abb. 6: Energieniveaudiagramm des H2-Moleküls. Durch Linearkombination der 1s-Orbitale der HAtome entstehen ein bindendes und ein antibindendes MO. Im Grundzustand besetzen die beiden
Elektronen des H2-Moleküls das σb-MO. Dies entspricht einer σ-Bindung (aus 3).
3.2.3 Hybridisierung
Zur Erklärung des räumlichen Baus von Molekülen eignet sich das von Pauling entwickelte
Konzept der Hybridisierung.
sp3-Hybridorbitale. Im Methanmolekül, CH4, werden von dem angeregten C-Atom vier σBindungen gebildet. Da zur Bindung ein s-Orbital und drei p-Orbitale zur Verfügung stehen, sollte
man erwarten, dass nicht alle C-H-Bindungen äquivalent sind und dass das Molekül einen
räumlichen Aufbau besitzt, wie ihn Abb. 7a. Die experimentellen Befunde zeigen jedoch, dass CH4
ein völlig symmetrisches tetraedrisches Molekül mit vier äquivalenten C-H-Bindungen ist (Abb. 7b)
Wir müssen daraus schließen, dass das C-Atom im Bindungszustand vier äquivalente Orbitale
besitzt, die auf die vier Ecken eines regulären Tetraeders ausgerichtet sind. Diese vier äquivalenten
Orbitale entstehen durch Kombination aus dem s- und den drei p-Orbitalen. Man nennt diesen
Vorgang Hybridisierung, die dabei entstehenden Orbitale werden Hybridorbitale genannt (Abb. 8).
8
Grundlagen chemischer Bindung
Biophysik I
Abb. 7: a) Geometrische Anordnung, die die Atome im Methanmolekül besitzen müssten, wenn das CAtom die C-H-Bindungen mit den Orbitalen 2s, 2px, 2py, 2pz ausbilden würde. Das an das 2s-Orbital
gebundene H-Atom hat wegen der Abstoßung der Elektronenhüllen zu den anderen H-Atomen die gleiche
Entfernung. b) Experimentell gefundene Anordnung der Atome im CH4-Molekül. Alle C-H-Bindungen
und alle H-C-H-Winkel sind gleich. CH4 ist ein symmetrisches, tetraedrisches Molekül (aus 3).
Abb. 8: Bildung von sp3-Hybridorbitalen. Durch Hybridisierung der s-, px-, py-, und pz-Orbitale entstehen
vier äquivalente sp3-Hybridorbitale, die auf die Ecken eines Tetraeders gerichtet sind. Die sp3Hybridorbitale sind aus zeichnerischen Gründen vereinfacht dargestellt (aus 3).
•
Die Anzahl gebildeter Hybridorbitale ist gleich der Anzahl der Atomorbitale, die an der
Hybridbildung beteiligt sind.
• Es kombinieren nur solche Atomorbitale zu Hybridorbitalen, die ähnliche Energien
haben, z.B.: 2s, 2p; 3s, 3p, 3d; 3d, 4s, 4p.
• Die Hybridisierung führt zu einer völlig neuen räumlichen Orientierung der
Elektronenwolken.
Weitere Beispiele für häufige Hybridisierungen sind in Tab. 1 aufgezählt.
Tab. 1: Häufig auftretende Hybridisierungen
3.2.4 π-Bindung
Im Molekül N2 sind die beiden Stickstoffatome durch eine Dreifachbindung aneinander gebunden.
Dadurch erreichen beide Stickstoffatome ein Elektronenoktett. Die drei Bindungen im N2-Molekül
sind nicht gleichartig. Dies geht aus der Lewis-Formel nicht hervor, wird aber sofort klar, wenn
man die Überlappung der an der Bindung beteiligten Orbitale betrachtet. Jedem N-Atom stehen drei
p-Elektronen für Bindungen zur Verfügung. Durch Überlappung der px-Orbitale, die in Richtung
Grundlagen chemischer Bindung
9
Dieter Baurecht
der Molekülachse liegen, wird eine σ-Bindung gebildet. Wie auch die MO-Theorie zeigt, ist jedoch
anzunehmen, dass die σ-Bindung durch sp-Hybridorbitale gebildet wird, die zu einer stärkeren
Überlappung führen. Bei den senkrecht zur Molekülachse stehenden py- und pz-Orbitalen kommt es
zu einer anderen Art der Überlappung, die als π-Bindung bezeichnet wird. Die Dreifachbindung im
N2-Molekül besteht aus einer σ-Bindung und zwei äquivalenten π-Bindungen. Die beiden πBindungen sind senkrecht zueinander orientiert.
Große Bedeutung haben π-Bindungen bei Kohlenstoffverbindungen. In der Abb. 9 sind die
Bindungsverhältnisse für das Molekül Ethylen (Ethen) H2C=CH2 dargestellt. Für das Auftreten von
π-Bindungen gilt:
Einfachbindungen sind σ-Bindungen. Doppelbindungen bestehen aus einer σ-Bindung und einer πBindung, Dreifachbindungen aus einer σ-Bindung und zwei π-Bindungen. π-Bindungen, die durch
Überlappung von p-Orbitalen gebildet werden, treten bevorzugt zwischen den Atomen C, O und N
auf, also bei Elementen der 2. Periode. (Doppelbindungsregel). Bei Atomen höherer Perioden ist die
Neigung zu (p-p) π-Bindungen geringer.
Abb. 9: Bindungen in Ethen, C2H4. a) Lewisformel. b) Valenzelektronenkonfiguration des angeregten CAtoms. Drei Valenzelektronen bilden sp2-Hvbridorbitale. c) Jedes C-Atom bildet mit seinen drei sp2Hybridorbitalen drei σ-Bindungen. d) Die p-Orbitale, die senkrecht zur Molekülebene stehen, bilden eine
π-Bindung (aus 3).
3.2.5 Polare Atombindung, Dipole
Die Atombindung und die Ionenbindung sind Grenztypen der chemischen Bindung. In den meisten
Verbindungen sind Übergänge zwischen diesen beiden Bindungsarten vorhanden.
Eine unpolare kovalente Bindung tritt in Molekülen mit gleichen Atomen auf, z.B. bei F2 und H2.
Die Elektronenwolke des bindenden Elektronenpaares ist gleichmäßig zwischen den beiden Atomen
verteilt, die Bindungselektronen gehören beiden Atomen zu gleichen Teilen.
Bei Molekülen mit verschiedenen Atomen, z. B. HF, werden die bindenden Elektronen von den
beiden Atomen unterschiedlich stark angezogen. Das F-Atom zieht die Elektronenwolke des
bindenden Elektronenpaares stärker an sich heran als das H-Atom. Die Elektronendichte am FAtom ist daher größer als am H-Atom. Am F-Atom entsteht die negative Partialladung δ-‚ am HAtom die positive Partialladung δ+.
Die Partialladung δ gibt eine tatsächlich auftretende Ladung an. Die Atombindung zwischen H
und F enthält einen ionischen Anteil, sie ist eine polare Atombindung. Moleküle, in denen die
Ladungsschwerpunkte der positiven Ladung und der negativen Ladung nicht zusammenfallen,
stellen einen Dipol dar (Abb. 10).
10
Grundlagen chemischer Bindung
Biophysik I
Abb. 10: Beispiele für Dipole (aus 3).
Beim Grenzfall der Ionenbindung, z.B. bei LiF, wird das Valenzelektron des Li-Atoms vollständig
vom F-Atom an sich gezogen, es hält sich nur noch in einem Orbital des Fluoratoms auf. Dadurch
entstehen die Ionen Li+ und F-.
r
Dipolmoleküle besitzen ein messbares Dipolmoment µ . Haben die positive Ladung +xe und die
r
negative Ladung -xe einen Abstand l (Richtung: von der positiven zur negativen Ladung), so
beträgt das Dipolmoment:
r
r
r
(7)
µ = xe ⋅ l = q ⋅ l
Die SI-Einheit des Dipolmoments ist Cm. Bei Moleküldipolen benutzt man als Einheit meist das
Debye(D): 1 D = 3,336.10-30 Cm. Zwei Elementarladungen im Abstand von 10-10m (1 Å) erzeugen
ein Dipolmoment von 4,80 D. Das Dipolmoment ist ein Vektor, dessen Spitze zum negativen Ende
des Dipols zeigt. Das Dipolmoment eines Moleküls ist die Vektorsumme der Momente der
einzelnen Molekülteile. Für einige Moleküle sind die Dipolmomente in Tab. 2 angegeben.
Tab. 2: Dipolmomente einiger Moleküle in D (aus 3).
Molekül
HF
HCl
HBr
HI
Dipolmoment
1,82
1,08
0,82
0,44
Molekül
H20
H2S
NH3
CO
Dipolmoment
1,85
0,97
1,47
0,11
3.2.6 Elektronegativität
Unter Elektronegativität wird die Tendenz eines Atoms verstanden, innerhalb eines Moleküls
Elektronen an sich zu ziehen. Mulliken fand, dass die Elektronegativität eines Atoms der Differenz
seiner Ionisierungsenergie und Elektronenaffinität proportional ist. Dies bedeutet anschaulich, dass
die Tendenz eines gebundenen Atoms, die Bindungselektronen an sich zu ziehen, um so größer ist,
je größer die Fähigkeit des Atoms ist, sein eigenes Elektron festzuhalten und ein zusätzliches
Elektron aufzunehmen.
Die Elektronegativitäten nach Mulliken beziehen sich aber nicht auf den Grundzustand des Atoms,
sondern auf seinen Valenzzustand (Hybridisierung). Mulliken-Elektronegativitäten sind OrbitalElektronegativitäten. Man muss daher zu ihrer Berechnung die Ionisierungsenergie und
Elektronenaffinität dieser Orbitale kennen. Als Beispiel seien die Elektronegativitäten für die
Orbitale der verschiedenen Valenzzustände des C-Atoms in Tab. 3 angegeben.
Tab. 3: Elektronegativitäten für die Orbitale der verschiedenen Valenzzustände des C-Atoms (aus 3).
Valenzzustand
s1p3
(sp)2π2
Orbital
s
p
sp
π
x
4,84
1,75
3,29
1,69
Valenzzustand
(sp2)3π1
(sp3)4
Orbital
sp2
π
sp3
x
2,75
1,68
2,48
Die Elektronegativität wächst mit zunehmendem s-Charakter der Hybridorbitale. Die
Elektronegativität der σ-Orbitale ist größer als die der π-Orbitale. In einer Mehrfachbindung kann
also die Polarität der σ-Bindung anders als die der π-Bindung sein. Als Folge der unterschiedlichen
Grundlagen chemischer Bindung
11
Dieter Baurecht
Orbital-Elektronegativität ist z. B. im Brommethan CH3Br ein Dipolmoment mit negativem
Ladungsschwerpunkt am Brom vorhanden, während im Bromethin BrC≡CH ein Dipolmoment mit
positivem Ladungsschwerpunkt am Brom auftritt. Brom mit der Elektronegativität 2,7 kann vom
sp3-hybridisierten Kohlenstoff Elektronen an sich ziehen, während der sp-hybridisierte Kohlenstoff
die Bindungselektronen vom Brom an sich zieht. Eine Skala mit absoluten Elektronegativitäten
erhält man aus der Beziehung
x=
I − E ea
2
(8)
wenn man die Ionisierungsenergien und Elektronenaffinitäten des Grundzustands der Atome in eV
einsetzt.
Im PSE (Periodensystem der Elemente) nimmt die Elektronegativität mit wachsender Ordnungszahl
in den Hauptgruppen ab, in den Perioden zu. Die elektronegativsten Elemente sind also die
Nichtmetalle der rechten oberen Ecke des PSE (Abb. 11). Das elektronegativste Element ist Fluor.
Die am wenigsten elektronegativen Elemente sind die Metalle der linken unteren Ecke des PSE.
Aus der Differenz der Elektronegativitäten der Bindungspartner kann man die Polarität einer
Bindung abschätzen. Je größer ∆x ist, um so ionischer ist die Bindung.
Abb. 11: Elektronegativität der Hauptgruppenelemente. Mit steigender Ordnungszahl Z nimmt innerhalb
der Perioden die Elektronegativität zu innerhalb der Gruppen ab. Rechts oben im PSE stehen daher die
Elemente mit ausgeprägtem Nichtmetallcharakter, links unten die typischen Metalle (aus 3).
3.3 Van der Waals-Kräfte
Die van der Waals-Kräfte kommen durch Anziehung zwischen Dipolen zustande, sie sind also
elektrostatischer Natur. Die Reichweite ist sehr gering (sie ist praktisch auf die nächsten Nachbarn
beschränkt), denn da die Wechselwirkungsenergie proportional r6 ist, nimmt sie mit wachsendem
Abstand viel schneller ab als die Ionen-Ionen-Wechselwirkung. Man unterscheidet drei
Komponenten der van der Waals-Kräfte.
Wechselwirkung permanenter Dipol-permanenter Dipol (Richteffekt). Bei der Anziehung von
Dipolen mit einem permanenten Dipolmoment kommt es zu einer Ausrichtung der Dipole, die
dadurch in einen energieärmeren Zustand übergehen. Der Richteffekt ist temperaturabhängig, da die
Wärmebewegung der Ausrichtung der Dipole entgegenwirkt.
Wechselwirkung permanenter Dipol-induzierter Dipol (Induktionseffekt). Ein permanenter
Dipol induziert in einem benachbarten Teilchen ein Dipolmoment, es kommt zu einer Anziehung.
Besitzt das benachbarte Teilchen ein permanentes Dipolmoment, so überlagern sich
Induktionseffekt und Richteffekt. Der Induktionseffekt ist temperaturunabhängig.
Wechselwirkung fluktuierender Dipol-induzierter Dipol (Dispersionseffekt). In allen Atomen
und Molekülen entstehen durch Schwankungen in der Ladungsdichte der Elektronenhülle
12
Grundlagen chemischer Bindung
Biophysik I
fluktuierende Dipole. Im Nachbaratom werden durch diese „momentan“ vorhandenen Dipole
gleichgerichtete Dipole induziert, so dass eine Anziehung entsteht. Da mit zunehmender Größe der
Atome bzw. Moleküle die Elektronen leichter verschiebbar sind, lassen sich leichter Dipole
induzieren, die van der Waals-Anziehung nimmt zu. Für unterschiedliche Partikel beträgt die
Wechselwirkungsenergie (nach London 1930 auch London-Energie genannt)
U=
3 α1α 2 I1 ⋅ I 2
2 r 6 I1 + I 2
(9)
α1 und α2 sind die Polarisierbarkeiten der Teilchen, I1 und I2 die Ionisierungsenergien.
3.4 Die Wasserstoffbrückenbindung
Wasserstoffbrücken sind relativ schwache Wechselwirkungen, spielen aber für biologische
Makromoleküle wie DNA und Proteine eine zentrale Rolle. Außerdem sind sie Ursache vieler
Eigenschaften, durch die das Wasser zu einem ganz besonderen Lösungsmittel wird. In einer
Wasserstoffbrücke teilen sich zwei elektronegative Atome wie Stickstoff oder Sauerstoff ein
Wasserstoffatom (Abb. 12).
Abb. 12: Wasserstoffbrückenbindungen (Wasserstoff-Bindungen) bilden über Wasserstoffatome die
zwischen anderen elektronegativeren Atomen sind. Dabei ist das Wasserstoffatom an ein elektronegatives
Atom kovalent gebunden. Die Bindungen zwischen zwei Aminosäuren stehen in Konkurrenz zu
Bindungen zu Wassermolekülen (aus 5).
Zur Donorgruppe der Wasserstoffbrücke gehören das Wasserstoffatom selbst und das Atom, an das
es enger gebunden ist; an die Akzeptorgruppe dagegen ist das Wasserstoffatom weniger stark
gebunden (Abb. 13). Wasserstoffbrücken sind im Grunde elektrostatische Wechselwirkungen. Das
relativ stark elektronegative Atom, an welches das Wasserstoffatom gebunden ist, zieht
Elektronendichte vom Wasserstoff ab, sodass dieser eine positive Partialladung (δ+) erhält. Deshalb
kann er elektrostatische Wechselwirkungen zu einem Atom mit negativer Partialladung (δ-)
ausbilden.
Wasserstoffbrücken sind viel schwächer als kovalente Bindungen. Ihr Energiegehalt beträgt 4
bis 13 kJ mol-1, im Vergleich zu rund 418 kJ mol-1 einer kovalenten Bindung zwischen Kohlenstoff
und Wasserstoff. Außerdem sind Wasserstoffbrücken etwas länger als kovalente Bindungen: Ihre
Bindungslänge (gemessen vom Wasserstoffatom) liegt zwischen 0,15 und 0,26 nm; die beiden
Atome, die außer dem Wasserstoff an der Bindung beteiligt sind, haben somit einen Abstand von
0,24 bis 0,35 nm. Die stärksten Wasserstoffbrücken haben das Bestreben, eine gestreckte Form
anzunehmen, sodass Donor, Wasserstoffatom und Akzeptor eine Gerade bilden.
Beispiele für Wasserstoffbrückenbindungen sind z.B. die Stabilisierung der Sekundärstruktur der αHelix (Abb. 24) des β-Faltblatts (Abb. 26) und der β-Schleife (Abb. 27).
Grundlagen chemischer Bindung
13
Dieter Baurecht
Abb. 13: Wasserstoffbrücken unter Beteiligung von Stickstoff- und Sauerstoffatomen. Man erkennt die
Lage der Partialladungen (δ+ und δ-, aus 4).
14
Grundlagen chemischer Bindung
Biophysik I
4 Struktur und Funktion der Proteine
Die biophysikalischen Eigenschaften lebender Systeme sind durch die Eigenschaften der beteiligten
Biomoleküle bestimmt. Dabei ist die Anzahl unterschiedlicher Moleküle und deren Spezifität zwar
sehr groß, der grundlegende Aufbau vieler Moleküle aber sehr ähnlich. Zu den wichtigsten
Vertretern auf der hierarchischen Ebene der Biomoleküle für Strukturgebung,
Stoffwechselfunktion, Energiespeicherung und Informationsübertragung gehören die Proteine
(Eiweiße), die Lipide (Fette) und die Sacherosen (Zucker).
4.1 Aminosäuren, die Bausteine der Proteine
Proteine sind lineare Polymerketten, die aus einer Kombination von nur 20 unterschiedlichen
Bausteinen (Aminosäuren) aufgebaut sind (Abb. 14).
Abb. 14: Schematischer Aufbau eines ungefalteten Proteins (aus 5).
4.1.1 Grundstruktur
Die Bausteine (elementare Struktureinheiten) für das Protein sind die Aminosäuren. Alle
proteinbildenden Aminosäuren weisen die gleiche Grundstruktur auf (Ausnahme: Prolin):
Aminogruppe (NH2, NH3+), Carboxylgruppe (COOH, COO-), Wasserstoffatom und ein "Rest" R
(dieser Rest bestimmt die Eigenschaften der Aminosäure und wird auch als Seitenkette bezeichnet),
die alle an ein C-Atom gebunden sind (Abb. 15). Dieses zentrale Atom wird als α−Kohlenstoffatom
bezeichnet, weil es der (sauren) Carboxylgruppe benachbart ist.
Abb. 15: Struktur einer Aminosäure. Nichtionisierte Form und Zwitterion (aus 6).
Aminosäuren in Lösung liegen bei neutralem pH-Wert als dipolare Ionen (Zwitterionen) und nicht
als ungeladene Moleküle vor. Im dipolaren Zustand ist die Aminogruppe protoniert (-NH3+) und die
Carboxylgruppe dissoziiert (-COO-). Der Dissoziationsgrad und damit der Ladungszustand einer
Aminosäure ändert sich mit dem pH-Wert (Abb. 16). In saurer Lösung (z.B. pH 1) liegt die
Carboxylgruppe nichtionisiert (-COOH) und die Aminogruppe ionisiert (-NH3+) vor, in alkalischer
Lösung (z.B. pH 11) ist dagegen die Carboxylgruppe ionisiert (-COO-) und die Aminogruppe
nichtionisiert (-NH2). Für die Stabilität und Funktion von Proteinen sind die Säure- und
Baseneigenschaften der Aminosäuren sehr wichtig.
Abb. 16 Dissoziationsgrad und Ladungszustand einer Aminosäure in Abhängigkeit von dem pH-Wert
(aus 6).
Struktur und Funktion der Proteine
15
Dieter Baurecht
4.1.2 Die 20 Aminosäuren
Abb. 17: Die Strukturen der 20 Aminosäuren bei einem pH von 7. Alle sind in Projektion auf eine Ebene,
die den α-Kohlenstoff enthält, dargestellt. In natura sind die Aminogruppe bzw. der Wasserstoff oberhalb
und die Carboxylgruppe bzw. die Seitenkette unterhalb der Blattebene angeordnet. In Klammern die für
Aminosäuren üblichen 3 Buchstaben Abkürzungen (aus 2).
16
Struktur und Funktion der Proteine
Biophysik I
Es ist nützlich, die 20 natürlichen Aminosäuren (Abb. 17) in Gruppen einzuteilen. Man
unterscheidet Aminosäuren mit aromatischen, unpolaren sowie polaren Seitenketten, wobei letztere
auch Ladung tragen können. Bei pH 7 sind Asp und Glu negativ, Lys und Arg positiv geladen.
Unpolare Seitenketten haben, gemäß dem Prinzip ´Gleiches löst Gleiches´, eine geringe Löslichkeit
in Wasser. Hierzu gehören Ala, Val, Ile, Leu, Phe, Trp und Met. Eine große Löslichkeit haben
neben den bereits erwähnten geladenen Seitenketten auch Asn, Gln, Ser und Thr. Bei den anderen
Aminosäuren ist die Einteilung schwieriger. Es muss auch berücksichtigt werden, dass bei der
Untersuchung von Proteinen die Aminosäuren als Teil eines Polypeptids und nicht als einzelne
Aminosäuren (Zwitterionen) vorliegen. Eine Klassifizierung aufgrund der Polarität zeigt Tab. 4. Die
polaren Eigenschaften spielen bei der Strukturbildung von Proteinen eine große Rolle, da unpolare
Seitenketten energetisch günstiger im inneren der Proteine, polare Seitenketten eher zum
umgebenden Wasser gewand sein werden.
Tab. 4: Klassifizierung der Aminosäuren aufgrund der polaren Eigenschaften der Seitenkette
unpolar
Trp
Ile
Tyr
Phe
Leu
Val
Met
Cys
Ala
Gly
polar
Pro
Ser
Thr
Asn
Gln
geladen (bei pH 7)
Asp (–)
Glu (–)
Lys (+)
Arg (+)
↑ steigende Hydrophobizität
Exkurs: Säure-Base-Theorie
Im folgenden sind die Konzentrationen in den Gleichgewichtskonstanten und daraus abgeleiteten
Formeln häufig als absolute Konzentrationen [C] angegeben. Genaugemommen müssen diese
durch die Standardkonzentrationen [C]*, für die Standardbedingungen, bei denen die
Gleichgewichtskonstante angegeben ist, dividiert werden. Da die Standardkonzentrationen im
0
-System [C]0 meist 1[M] sind werden diese in der Schreibweise häufig einfach weggelassen. Das
Argument der log Funktion muss aber natürlich immer dimensionslos sein. Zur Definition des
Massenwirkungsgesetzes, der Gleichgewichtskonstanten und der Referenzzustände siehe (7).
Konjugiertes Säure-Base-Paar
Eine Säure ist ein Protonendonor, eine Base ein Protonenakzeptor. Wird eine Säue ionisiert entsteht
ihre konjugierte Base. Wird eine Base protoniert entsteht ihr konjugierte Säure. Sie bilden
gemeinsam ein konjugiertes Säure-Base-Paar.
Säure ⇔ H+ + Base
CH3-COOH ⇔ H+ + CH3-COO(Essigsäure)
(Acetat)
+
+
NH4 ⇔ H + NH3
(Ammoniumion)
(Ammoniak)
Die Dissoziation des Wassers
Wasser kann in Hydronium- (H3O+) und Hydroxylionen (OH-) dissoziieren. Vereinfacht wird das
Hydroniumion meist durch ein Wasserstoffion (Proton, H+) ersetzt.
Struktur und Funktion der Proteine
17
Dieter Baurecht
H2O ⇔ H+ + OHDie Gleichgewichtskonstante K0 (siehe 7) im Referenzsystem
Dissoziation lautet:
0
([H+]0=1M; [OH-]0=1M) dieser
( 10 )
[H + ][OH − ]
+
−
[H + ]0 [OH − ]0 [H ][OH ]
=
K0 =
x H 2O
x H 2O
Die in Klammern geschriebenen Größen sind die molaren Konzentrationen der gelösten Stoffe (die
durch die molare Referenz-Konzentration dividiert werden müssen, im 0-System 1 M). Für das
Lösungsmittel wird der Molenbruch xH2O angegeben (xH2O = Wasserteilchen[mol]/Gesamtteilchen
[mol]). Da die Konzentration des Lösungsmittels [H2O] >> [H+], [OH-], ändert sich [H2O] bei der
Dissoziation (Ionisation) des Wassers kaum und kann als konstant [H2O] = 55,5 M angesehen
werden; der Molenbruch wird damit zu xH2O = 1. Damit vereinfacht sich ( 10 ) zum Ionenprodukt
des Wassers Kw:
( 11 )
K w = [H + ][OH − ]
Bei 25°C ist Kw = 1x10-14 (= dimensionslos, da ja die Konzentrationen durch die
Standardkonzentrationen, z.B. 1M, dividiert wurden). Bitte beachten, dass bei steigender
Protonenkonzentration gleichzeitig die Hydoxylionenkonzentration sinken muss und vice versa!
pH und pK Werte
Die tatsächliche Protonenkonzentration einer wässrigen Lösung wird indirekt durch den pH-Wert
angegeben der für verdünnte Lösungen mit guter Näherung (Aktivität = Konzentration) gegeben ist
als:
( 12 )
pH = −log[H + ]
Auch hier ist [H+] dimensionslos also als [H+]/[1M] zu verwenden. Die Protonenkonzentration in
[M] ist somit
[H + ] = 10 − pH
( 13 )
Der Zustand in dem [H+] = [OH-] = 10-7 ([H+] [OH-] = 10-14) ist wird als neutral bezeichnet (pH =
7,0). Steigt die Wasserstoffionenkonzentration wird die Lösung zu einem Protonendonator und
damit zur Säure. Der pH-Wert wird bei steigender Wasserstoffionenkonzentration kleiner.
Das Ionisationsgleichgewicht einer Säure ist analog zum Wasser gegeben durch:
HA
⇔
H+ + A-
Die Gleichgewichtskonstante für diese Ionisation ist die Säuredissoziationskonstante Ks:
KS =
[H + ][A − ]
[HA]
( 14 )
Starke Säuren (z.B. HCl) dissoziieren in wässriger Lösung vollständig in Anionen und Protonen.
Die Konzentration der Wasserstoffionen ist folglich identisch mit der absoluten Säurekonzentration
[HA]. Daher ist der pH der Lösung einer starken Säure einfach –log[HA].
Eine schwache Säure (z.B. Essigsäure) ist eine Säure, die nicht vollständig dissoziiert. Der pH
einer schwachen Säure hängt sowohl von der absoluten Säurekonzentration [HA] als auch von der
Säurekonstanten KS ab.
18
Struktur und Funktion der Proteine
Biophysik I
Durch Umformen und Logarithmieren von ( 14 ) erhält man
1
1
[A − ]
+ log
log + = log
Ks
[HA]
[H ]
[A − ]
− log[H + ] = −logK s + log
[HA]
( 15 )
und mit der Definition des pKS
pK S = −log[K S ]
( 16 )
die Henderson-Haselbalch-Gleichung
pH = pK S + log
[Base]
[Säure]
( 17 )
Dabei ist zu beachten, dass [Base] und [Säure] die Konzentrationen im Gleichgewicht (und nicht
etwa die Anfangskonzentrationen beim Herstellen einer Lösung) sind.
Man kann damit den pH-Wert einer Lösung berechnen, wenn man das molare Verhältnis von
[Base]/[Säure], und den pKS-Wert der Säure kennt, bzw. den pKS-Wert der Säure berechnen, wenn
der pH einer bekannten Lösung gemessen wird (siehe Beispiel 7.1).
Ist eine Säure zur Hälfte dissoziiert ([HA] = [A-]) wird [H+] = KS und damit pKS = -log[H+] = pH.
Das heißt, dass bei einem pH der dem pKS einer Säure entspricht die Hälfte der Moleküle
dissoziiert sind.
4.1.3 pK-Werte von Aminosäuren
Die Aminosäuren besitzen zumindest zwei ionisierbare Gruppen (die Seitenkette oft noch eine
dritte): eine α-Carboxylgruppe und eine protonierte α-Aminogruppe. Abhängig vom pH-Wert der
Lösung liegen diese beiden Gruppen in unterschiedlich ionisierter Form vor (siehe auch Beispiel
7.2). Jede dieser funktionellen Gruppen besitzt einen eigenen pK-Wert. Beim Glycin (siehe 4.1.2)
beträgt z.B. der pK-Wert der α-Carboxylgruppe 2,3, der pK-Wert der α-Aminogruppe 9,6. Die pKWerte dieser Gruppen sind in anderen Aminosäuren ähnlich, können aber in anderen Verbindungen
stark unterschiedlich sein (Beispiel Essigsäure: pK(COOH) = 4,8). Neben den beiden ionisierbaren
α-Gruppen finden sich bei einigen Aminosäuren auch noch ionisierbare Gruppen an der Seitenkette
deren pK-Werte von 3,9 (Asparaginsäure) bis zu 12,5 (Arginin) reichen.
Struktur und Funktion der Proteine
19
Dieter Baurecht
Tab. 5: Die pK-Werte der Aminosäuren (aus 2).
4.2 Die Peptidbindung
In Proteinen ist die α-Carboxylgruppe einer Aminosäure mit der α-Aminogruppe einer zweiten
Aminosäure durch eine Peptidbindung (auch Amidbindung genannt) verknüpft. Die Bildung dieser
Bindung unter Abspaltung eines Wassermoleküls ist für zwei Aminosäuren (Dipeptid) in Abb. 18
dargestellt. Das Gleichgewicht dieser Reaktion liegt auf der Seite der Hydrolyse; daher bedarf die
Biosynthese von Peptidbindungen eines beträchtlichen Energieaufwands, während die Spaltung
thermodynamisch freiwillig abläuft.
Abb. 18: Bildung einer Peptidbindung zwischen zwei Aminosäuren unter der Abspaltung von Wasser
(aus 6).
Viele durch Peptidbindungen verknüpfte Aminosäuren bilden eine unverzweigte Polypeptidkette
(Abb. 19). Eine solche Kette hat eine bestimmte Richtung, da ihre Bausteine zwei unterschiedliche
Enden besitzen, nämlich die α-Amino- und die α-Carboxylgruppen. Vereinbarungsgemäß nimmt
man das Aminoende als Beginn der Polypeptidkette.
20
Struktur und Funktion der Proteine
Biophysik I
Abb. 19: Ein Pentapeptid. Die einzelnen Aminosäurereste sind eingerahmt. Der Kettenanfang ist
definitionsgemäß am Aminoende (N-Terminus, aus 6).
Die Peptideinheit ist starr und planar, wobei der Wasserstoff fast immer gegenständig – in transPosition – zum Sauerstoff liegt (Abb. 20). Die partielle Doppelbindung (Abb. 21) zwischen dem
Kohlenstoff und dem Stickstoff der Peptidbindung verhindert eine Rotation um diese Bindung.
Dieser partielle Doppelbindungscharakter kann aus den in Abb. 20 gezeigten Bindungslängen
r
abgelesen werden. Die Peptidgruppe ist durch ein großes Dipolmoment p ausgezeichnet (3.7 D).
Die Bindungen beiderseits der starren Peptideinheit weisen im Gegensatz zur partiellen
Doppelbindung zwischen dem Kohlenstoff und dem Stickstoff eine große Rotationsfreiheit auf.
Abb. 20: Die Peptidgruppe ist eine starre, planare Einheit. Die Standardbindungslängen sind in nm
angegeben (aus 6).
Abb. 21: Partieller Doppelbindungscharakter der Peptidbindung (aus 6).
4.3 Die dreidimensionale Proteinstruktur
4.3.1 Primärstruktur
Die Reihenfolge der Aminosäuren in einer Polypeptidkette ist die Primärstruktur. Diese gibt noch
keine Information bezüglich der Räumlichen Anordnung der einzelnen Seitenketten.
4.3.2 Sekundärstruktur
Der erste Schritt zur dreidimensionalen Struktur wird an der Ausrichtung der einzelnen Seitenketten
zueinander beschritten, was wiederum durch Struktur der Hauptkette (des Rückgrads) der
Polypeptidkette bestimmt wird. Die Möglichkeiten dafür sind allerdings beschränkt. Die
Amidbindung selbst ist ja planar und weist somit keine Möglichkeit zur Variabilität auf. Auf beiden
Seiten der starren Peptidbindung ist die Kette frei drehbar. Den Rotationswinkel um die Bindung
zwischen dem Stickstoffatom und dem α-Kohlenstoffatom bezeichnet man als phi ϕ, den um die αKohlenstoffatom-Carbonylkohlenstoffatom-Bindung als psi Ψ (Abb. 22). Die Konformation der
Hauptkette ist vollständig festgelegt, wenn ϕ und Ψ für jeden Rest der Kette definiert sind. G.N.
Ramachandran erkannte, dass aus sterischen Gründen ϕ und Ψ nicht beliebige Werte annehmen
Struktur und Funktion der Proteine
21
Dieter Baurecht
können. Die erlaubten Bereiche kann man in Raumkontourdiagrammen, den Ramachandran-Plots
darstellen. Sie unterscheiden sich für unterschiedliche Seitenketten. Abb. 23 zeigt für Poly-LAllalin drei getrennte mögliche Bereiche. In ersten Bereich liegen die Winkelwerte für antiparallele
und parallele β-Faltblattstrukturen, im zweiten Bereich liegt die rechtsgängige α-Helix und im
dritten Bereich die linksgängige α-Helix. Obwohl die linksgängige α-Helix sterisch erlaubt ist,
kommt sie nicht vor, da sie energetisch wesentlich weniger begünstigt ist, als die rechtsgängige.
Abb. 22: Definition von ϕ und Ψ, die die räumliche Anordnung benachbarter Aminosäuren bestimmen
(aus 5).
Abb. 23: Ramachandran-Plot mit erlaubten Werten von ϕ und Ψ für Poly-L-Allalin (grün, dunkel).
Glycin kann noch zusätzliche Konformationen annehmen (gelb, hell), weil es eine sehr kleine Seitenkette
hat (aus 6).
Die Winkel ϕ und Ψ bestimmen die Sekundärstruktur einer Gruppe benachbarter Seitenketten.
Die Sekundärstrukturelemente können sich von wenigen Peptidbindungen (β-Schleife mit 4
Peptidbindungen) bis zu sich periodisch wiederholenden Kombinationen (α-Helix, β-Faltblatt)
bestimmt sein. Häufig in Proteinen vorkommende Sekundärstrukturelemente sind die α-Helix, das
antiparallele β-Faltblatt und die β-Schleife.
22
Struktur und Funktion der Proteine
Biophysik I
Abb. 24A-C: Modell einer rechtsgängigen α-Helix. In A sind nur die α-Kohlenstoffatome auf einem
helikalen Faden dargestellt, in B nur die Stickstoffe (N), die α-Kohlenstoffe (Cα) und die
Carbonylkohlenstoffe (C) des Rückgrads; C zeigt die gesamte Helix. Wasserstoffbrückenbindungen (in C
durch Punkte dargestellt) stabilisieren die Helix (aus 6).
Abb. 25: Querschnitt durch eine α-Helix. Die Seitenketten ragen nach außen. Die van-der-Waals-Radien
der Atome sind in Wirklichkeit größer als hier dargestellt, so dass es im Inneren der α-Helix fast keinen
freien Raum gibt (aus 6).
Struktur und Funktion der Proteine
23
Dieter Baurecht
Abb. 26: Antiparalleles β-Faltblatt. Benachbarte Stränge laufen in entgegengesetzte Richtungen.
Wasserstoffbrücken zwischen NH- und CO-Gruppen von nebeneinanderliegenden Strängen stabilisieren
dabei die Struktur Die Seitenketten befinden sich über und unter der Faltblattebene (aus 6).
Abb. 27: Struktur einer β-Schleife. Die CO- und NH-Gruppen von Rest 1 und 4 bilden eine
Wasserstoffbrücken, wodurch sich eine stark gekrümmte Schleife ergibt (aus 6).
4.3.3 Tertiärstruktur
Domänen mit einer bestimmten Sekundärstruktur bilden die Grundeinheit der Tertiärstruktur. Man
versteht darunter auch die räumliche Beziehung von Aminosäureresten, die innerhalb der linearen
Sequenz weit voneinander entfernt sind.
Die unterschiedliche Verteilung von polaren und unpolaren Resten bestimmt ganz wesentlich den
dreidimensionalen Aufbau von Proteinen. In wässriger Umgebung bestimmt das starke Bestreben
hydrophober Reste, dem Wasser zu "entkommen", die Proteinfaltung. Hydrophobe Gruppen sind
thermodynamisch stabiler, wenn sie im Inneren des Moleküls vereint sind, als wenn sie in die
wässrige Umgebung ragen. Die Polypeptidkette faltet sich also spontan so, dass die hydrophoben
Seitenketten im Inneren versteckt sind und die polaren, geladenen Reste an der Oberfläche liegen
(Abb. 28).
24
Struktur und Funktion der Proteine
Biophysik I
Abb. 28: Graphische Darstellung eines dreidimensionalen Modells des Proteins Cytochrom c.
Aminosäuren mit unpolaren Seitenketten (farbig) befinden sich im Inneren des Moleküls, wo sie
miteinander wechselwirken. Polare, hydrophile Aminosäureketten (grau) sind an der Außenseite des
Moleküls lokalisiert, wo sie mit der polaren wässrigen Lösung wechselwirken (aus 8).
4.3.4 Quartärstruktur
Proteine können auch aus mehr als einer Polypeptidkette bestehen. Diese zeigen dann eine weitere
Organisationsebene (Abb. 29). Jede Polypeptidkette eines solchen Proteins wird als Untereinheit
bezeichnet. Die Quartärstruktur beschreibt die räumliche Anordnung solcher Untereinheiten und die
Art ihrer Kontakte. Die einzelnen Ketten eines Proteins mit mehreren Untereinheiten können
identisch oder verschieden sein.
Die gesamte Hierarchie der verschiedenen Strukturelemente ist in Abb. 30 dargestellt.
Struktur und Funktion der Proteine
25
Dieter Baurecht
Abb. 29: Dreidimensionale Struktur des Hämoglobins als Beispiel für die Quartärstruktur eines Proteins.
Die vier Untereinheiten sind in den verschiedenen Farben dargestellt. Jede besitzt eine sauerstoffbindende
Hämgruppe (rot) (aus 6).
Abb. 30a-f: Hierarchie der Proteinstrukturen (aus 8).
26
Struktur und Funktion der Proteine
Biophysik I
4.4 Proteinfunktionen
4.4.1 Enzyme als Biokatalysatoren
Ein Katalysator ist eine Substanz, die eine chemische Reaktion beschleunigt, ohne irgendwie
verändert daraus hervorzugehen. Die Beschleunigung der Reaktionsgeschwindigkeit kann sehr groß
sein. Beispielsweise beschleunigt die Carboanhydrase die Reaktion CO2 + H2O -> H2CO3 um den
Faktor 107. Die meisten bekannten Biokatalysatoren sind Proteine. Der zeitliche Verlauf einer
katalysierten biochemischen Reaktion wird durch die Enzymkinetik beschrieben. Bevor wir uns mit
der Enzymkinetik befassen können, müssen wir die grundlegenden Eigenschaften der Kinetik
chemischer Reaktionen verstehen.
Exkurs: Kinetik der chemischen Reaktion
Bis jetzt haben wir chemische Reaktionen nur im Gleichgewicht behandelt. Wie schnell sich ein
Gleichgewicht einstellt wurde bis jetzt nicht berücksichtigt. Hier wollen wir nun die Grundlagen
kinetischer Reaktionen behandeln.
Der einfachste Fall einer chemischen Reaktion besteht aus nur zwei Reaktanden, einem Edukt und
einem Produkt. Ist die Umwandlung vom Edukt zum Produkt irreversibel ergibt sich folgende
Reaktionsgleichung (z.B. radioaktiver Zerfall eines Isotops):
k
A
→
B
Die Kinetik einer solchen Reaktion wird bestimmt durch die Konzentration des Edukts und eine für
die Reaktion typische Geschwindigkeitskonstante k. Die Geschwindigkeit der Reaktion kann durch
die zeitliche Abnahme des Edukts oder die zeitliche Zunahme des Produkts beschrieben werden:
v=−
d [ A] d [ B ]
=
dt
dt
( 18 )
Für eine einfache Reaktion dieser Art ist die Geschwindigkeit zu jeder Zeit proportional zur
verbliebenen Konzentration des Edukts:
v = k[ A]
( 19 )
Die Proportionalitätskonstante k ist die Geschwindigkeitskonstante. Die Geschwindigkeitskonstante ist unabhängig von der Konzentration der Reaktanden, wird aber von anderen Parametern
wie Temperatur oder pH abhängen und kann durch einen Katalysator verändert werden (es handelt
sich dann in Wirklichkeit allerdings um eine andere Reaktion). Durch Kombination von ( 18 ) und
( 19 ) erhält man:
d [ A]
= − k[ A]
dt
( 20 )
Eine Reaktion, die Gleichung ( 20 ) erfüllt, folgt einer Kinetik 1. Ordnung. Die Geschwindigkeit
ist proportional der Konzentration einer Spezies „hoch eins“.
Ist die betrachtete Reaktion reversibel (z.B. die Strukturumwandlung eines Moleküls, wobei Edukt
und Produkt unterschiedliche Strukturen des gleichen Moleküls sind) wird die Reaktionsgleichung
zu:
k1
A ←→
B
k−1
Struktur und Funktion der Proteine
27
Dieter Baurecht
In diesem Fall ist k1 die Geschwindigkeitskonstante für die Hinreaktion und k-1 die
Geschwindigkeitskonstante für die Rückreaktion. Gehen wir wieder von einer Kinetik 1. Ordnung
aus ergibt sich als Geschwindigkeitsgleichung:
d [ A]
= −k1[ A] + k −1[ B ]
dt
( 21 )
In diesem Fall entwickeln sich [A] und [B] von Ihren Anfangswerten zu den Gleichgewichtswerten
([A]eq und [B]eq), die im allgemeinen nicht null sind. Im Gleichgewicht geht allerdings d[A]/dt
gegen 0 und wir erhalten den Zusammenhang zwischen der Gleichgewichtskonstanten K und den
Geschwindigkeitskonstanten:
K=
[ B]eq
[ A]eq
=
( 22 )
k1
k −1
Sind auf der Edukt-Seite der Reaktionsgleichung zwei Moleküle vorhanden und der Prozess
irreversibel erhalten wir:
k
A1 + A2 →
B
Die Geschwindigkeit mit der zwei Moleküle miteinander reagieren hängt unter anderem davon ab,
wie oft die Moleküle zusammenstoßen. Die Zusammenstöße finden als Ergebnis zufälliger
Diffusion statt. Die Frequenz der Zusammenstöße ist dem Produkt der beiden Konzentrationen der
Molekülspezies proportional:
( 23 )
d [ B]
= k[ A1 ][ A2 ]
dt
Folgt eine Reaktion der Gleichung ( 23 ) spricht man von einer Kinetik 2. Ordnung, weil die
Geschwindigkeit proportional zum Produkt zweier Konzentrationen ist.
4.4.1.1 Die Wirkungsweise von Enzymen
Die Gleichgewichtskonstante K für eine Reaktion
k1
A ←→
B
k−1
ist strikt abhängig von den thermodynamischen Faktoren der Edukte und Produkte (Lit. 7).
∆G 0
−
[ B] k1
=
= e RT
K0 =
[ A] k −1
( 24 )
Die Zugabe von Enzymen zu einem Prozess kann also das Gleichgewicht nicht verschieben,
sondern nur die Geschwindigkeit der Reaktion wesentlich erhöhen (die Zeit bis das Gleichgewicht
hergestellt ist wesentlich verringern). Der Grund für diese Beschleunigung ist, dass die
Reaktionsgeschwindigkeit nicht von den Energiezuständen der Edukte und Produkte abhängt,
sondern im wesentlichen von der freien Energie des Übergangszustandes, der erreicht werden muss,
damit die Reaktion überhaupt stattfinden kann (Abb. 31). Dieser Zustand liegt energetisch höher als
Anfangs- und Endzustand der Reaktion. Die Menge freier Energie, die benötigt wird, um den
Übergangszustand zu erreichen, wird als Aktivierungsenergie bezeichnet.
28
Struktur und Funktion der Proteine
Biophysik I
∆G
0
Abb. 31: Ein Enzym beschleunigt eine Reaktion durch Absenken von ∆G‡. Das Enzym ändert weder die
freie Energie des Substrats (Edukts) noch die des Produkts und damit auch nicht Änderung der freien
Energie der Reaktion ∆G0, sondern verringert die freie Energie des Übergangszustandes. Die Pfeile
markieren die Aktivierungsenergie (∆G‡) der katalysierten (kurz) und unkatalysierten (lang) Reaktion
(modifiziert aus 8).
4.4.1.2 Enzymkinetik
4.4.1.2.1 Ein Substrat Reaktion
Wir betrachten die enzymatische Reaktion:
k1
→
k
2→
k −1
(k − 2 )
E + S ← ES ← E + P
( 25 )
in der aus Enzym E und Substrat S mit der Geschwindigkeitskonstanten k1 der Enzym-SubstratKomplex ES gebildet wird. ES kann mit der Geschwindigkeitskonstanten k-1 wieder dissoziieren
oder mit der Geschwindigkeitskonstanten k2 zu P werden, wobei dann das Enzym wieder freigesetzt
wird. Die Rückreaktion wollen wir hier vernachlässigen, da wir uns darauf beschränken, die
Anfangsgeschwindigkeit der Reaktion im stationären Zustand zu messen. Am Anfang ist [P] sehr
klein und daher die gesamte Rückreaktion sehr gering. Gesucht ist die
Produktbildungsgeschwindigkeit v (Kinetik 1. Ordnung):
v Anfang =
d[P]
= k 2 [ES] - k - 2 [P][S] = k 2 [ES] , da [P]t ≈0 <<
dt
( 26 )
Um den zeitlichen Verlauf der Konzentration [ES] zu bestimmen wird der Begriff des stationären
Zustandes ("steady state") eingeführt. Nach kurzer Anfangsphase (gewöhnlich weniger als einige
Sekunden) bleibt [ES], bis das Substrat stark abgebaut ist, in etwa konstant (Abb. 32). Unter
Annahme des Reaktionsschemas ( 25 ) und den kinetischen Grundgleichungen 1. und 2. Ordnung
ergibt sich mit dieser Stationaritätshypothese
d[ES]
= k1[E][S] − (k −1 + k 2 )[ES] = 0
dt
Struktur und Funktion der Proteine
( 27 )
29
Dieter Baurecht
Abb. 32: Konzentration von freiem Enzym [E], Substrat [S], Enzym-Substrat-Komplex [ES] und Produkt
[P] im Verlauf der Reaktion. Der gelb unterlegte Bereich der oberen Grafik (Anfang der Reaktion, [P]<<)
ist in vergrößerter Form in der unteren Grafik dargestellt. Nach kurzer Anfangsphase (gewöhnlich
weniger als einige Sekunden) bleibt [ES] in etwa konstant. Die Näherung des stationären Zustandes ist in
dieser zweiten Phase anwendbar (aus 8).
Da die Anfangskonzentration des Enzyms [E]0 zu jeder Zeit die Summe aus gebundenem Enzym
[ES] und freiem Enzym [E] sein muss gilt
[E]0 = [E] + [ES]
( 28 )
Damit wird ( 27 ) zu:
k1 ([E]0 − [ES])[S] = (k −1 + k 2 )[ES]
( 29 )
k1[E]0 [S] − k1[ES][S] = (k −1 + k 2 )[ES]
k1[E]0 [S] = (k −1 + k 2 + k1[S])[ES]
[ES]stat. =
[E]0 [S]
k −1 + k 2
+ [S]
k1
und man erhält mit der definierten Michaelis-Menten-Konstanten
Km =
k −1 + k 2
k1
( 30 )
die Michaelis-Menten Gleichung:
v Anf. =
d[P]
[S]
= k 2 [ES] = k 2 [E]0
dt
K m + [S]
( 31 )
Wenn man die rechte Seite der Gleichung ( 31 ) ansieht, erkennt man dass die maximale
Geschwindigkeit in Abhängigkeit der Substratkonzentration [S] dann auftritt, wenn [S]>>Km ist:
30
Struktur und Funktion der Proteine
Biophysik I
v max = k 2 [E]0
( 32 )
wodurch die Michaelis-Menten Gleichung auch folgendermaßen angegeben wird:
v = v max
[S]
K m + [S]
( 33 )
Um bei einer gegebenen Enzym Substrat Reaktion zu überprüfen, ob sie durch eine einfache
Michaelis-Menten Kinetik beschrieben und somit die Michaelis-Menten-Konstante bestimmt
werden kann, wird die Anfangsgeschwindigkeit (Produktbildungsgeschwindigkeit) v als Funktion
der Substratkonzentration [S] gemessen. Zur einfachern Darstellung wird dazu Gleichung ( 33 )
durch Kehrwertbildung linearisiert (Abb. 33):
K
1
1
1
=
+ m
v v max v max [S]
( 34 )
und graphisch 1/v als Funktion von 1/[S] dargestellt.
Abb. 33 Lineweaver-Burk Plot. Linearisierte Darstellung der Michaelis-Menten Gleichung zur
Bestimmung von vmax und Km (aus 8).
Eine Vorstellung über die Größe und Bedeutung von Km erhält man, wenn man [S] = Km wählt.
Nach Gleichung ( 33 ) wird dann v = vmax/2. Km entspricht also der Substratkonzentration, bei der
die Produktbildungsgeschwindigkeit halbmaximal ist. Ein kleiner Km-Wert bedeutet also, dass
schon bei geringer Substratkonzentration der Umsatz relativ hoch ist. Das Enzym hat somit eine
hohe Affinität zu seinem Substrat.
4.4.1.2.2 Kinetik enzymatischer Reaktionen mit zwei Substraten
In der Realität sind Enzymreaktionen in den seltensten Fällen einfache Enzym-Substrat Reaktionen
( 25 ). Häufig sind anstelle von einem Substrat mehrere Substrate beteiligt und es gibt auch
Hemmungen der Reaktion die wiederum von verschiedensten Parametern abhängen können. Neben
der Bestimmung kinetischer Größen ist es eine wichtige Aufgabe der Enzymkinetik, auch den
Reaktionsmechanismus zu bestimmen. Da unterschiedliche Modelle des Reaktionsmechanismus zu
unterschiedlichen theoretischen Abhängigkeiten der Produktbildungsgeschwindigkeit führen,
können durch experimentelles Ermitteln der Produktbildungsgeschwindigkeit Rückschlüsse auf den
Reaktionsmechanismus gewonnen werden.
Betrachten wir eine Reaktion, bei der zwei Substrate S1 und S2 zu den Produkten P1 und P2
umgewandelt werden. Eine Möglichkeit des Reaktionsablaufes ist, dass S1 zuerst an das Enzym
bindet und den binären Komplex ES1 bildet. Das Binden von S2 kann dann zur Bildung des tertiären
Komplexes ES1S2 führen, der zur Bildung der Produkte führt ( 35 ). Dieser Prozess wird als
geordneter Mechanismus bezeichnet.
Struktur und Funktion der Proteine
31
Dieter Baurecht
( 35 )
Ein weiteres Schema ist, dass die Bildung von S1 an das Enzym direkt zur Bildung von P1 führt,
wodurch das Enzym in einer veränderten Form E' belassen wird. S2 bindet dann an E', wird zu P2
und wandelt dabei das Enzym wieder in seine ursprüngliche Form um ( 36 ). Dieser Prozess wird
als "Pingpong-Mechanismus" bezeichnet, um das Springen des Enzyms zwischen den Zuständen
E und E' zu betonen.
( 36 )
Nach Aufstellen der kinetischen Gleichungen für die unterschiedlichen Reaktionsmechanismen
können durch experimentelles Ermitteln der Produktbildungsgeschwindigkeiten bei variierenden
Substratkonzentrationen Rückschlüsse über das vorliegende Reaktionsschema getroffen werden
(immer nur ausschließende Schlüsse!).
Die Herleitung der kinetischen Gleichungen für den geordneten Mechanismus ergibt ähnlich zu der
oben für ein Substrat gezeigten folgende Beziehung:
K K 1
1
1 K m2
1
1 +
+
K m1 + m 2 d 1
=
v vmax [ S 2 ] vmax
[ S 2 ] [ S1 ]
( 37 )
Wobei Kd1 die Dissoziationskonstante für ES1 (k-1/k1) ist, und Km1,2 die Michaeliskonstanten für S1
und S2 sind.
Anderseits ergibt sich für den "Pingpong-Mechanismus" folgende kinetische Gleichung:
1
1 K m 2 K m1 1
1 +
+
=
v vmax [ S 2 ] vmax [ S1 ]
( 38 )
Misst man nun bei konstanten [S2] und variablen [S1] für verschiedene [S2] die
Anfangsgeschwindigkeiten der Produktbildungsgeschwindigkeit und trägt die Ergebnisse wieder in
linearisierter Darstellung auf erhält man unterschiedliche Kurvenscharen, die sowohl auf den
Reaktionsmechanismus schließen lassen, als auch die kinetischen Konstanten bestimmen .
Abb. 34: Doppelt reziproke Darstellung der Kinetik eines geordneten Mechanismus. Die Messungen, die
bei verschiedenen definierten Werten für [S2] durchgeführt werden, ergeben eine Schar von Geraden, die
sich links von der Ordinate schneiden (aus 8).
32
Struktur und Funktion der Proteine
Biophysik I
Abb. 35: Doppelt reziproke Darstellung der Kinetik des "Pingpong-Mechanismus". Die Messungen, die
bei verschiedenen definierten Werten für [S2] durchgeführt werden, ergeben eine Schar paralleler
Geraden, die sich links von der Ordinate schneiden (aus 8).
Struktur und Funktion der Proteine
33
Dieter Baurecht
5 Lipide
Definitionsgemäß sind Lipide wasserunlösliche Biomoleküle, die in organischen Lösungsmitteln
wie Chloroform sehr gut löslich sind. Lipide haben ein breites Spektrum biologischer Funktionen:
Sie dienen als Brennstoffmoleküle, als hochangereicherte Energiespeicher, als Signalmoleküle und
als Membrankomponenten. Hier wollen wir uns hauptsächlich mit Lipiden in ihrer Funktion als
Membrankomponenten befassen. Zwei Hauptarten von Lipiden finden sich in biologischen
Membranen: Phospholipide und Stereoide. Die in den meisten Membranen vorherrschenden
Phospholipide sind Phosphoglycerine, also Phosphatester des Glycerins. Ein Phosphoglycerine
besteht aus einem Glycinrückgrad, zwei Fettsäureketten und einem phosphorylierten Alkohol
(Abb. 36, Abb. 37)
Abb. 36: Komponenten eines Phosphoglycerids (aus 6).
Abb. 37: Phosphatidylcholin (Lecitin) (aus 8).
Abb. 38: Strukturformel und Kalottenmodelle von A) Palmitat (C16, gesättigt) und B Oleat (C18,
ungesättigt). Die cis-Doppelbindung im Oleat bewirkt einen Knick in der Kohlenwasserstoffkette (aus 6).
34
Lipide
Biophysik I
Die langkettigen Fettsäuren in Phospho- und Glykolipiden enthalten gewöhnlich eine gerade
Anzahl von Kohlenstoffatomen, typischerweise zwischen 14 und 24. Die Fettsären mit 16 und 18
Kohlenstoffatomen kommen dabei am häufigsten vor. Fettsäuren können gesättigt (jedes C-Atom
bindet an 2 H Atome) oder ungesättigt (C=C Doppelbindung meist in cis-Konfiguration in der
Kette) vorliegen. Die Zahl der Doppelbindungen und die Länge der Fettsäuren in den
Membranlipiden haben einen großen Einfluss auf die Membranfluidität. Die Strukturen der
ionisierten Formen (physiologische Bedingungen) zweier sehr häufiger Fettsäuren sind in Abb. 38
dargestellt. Weitere in Membranen häufig vorkommende Fettsäuren sind in Tab. 6
zusammengefasst.
Tab. 6: In Membran-Phospholipiden häufige Fettsäuren (aus 8)
Fügt man zu dem Phosphatidylcholin aus Abb. 37 die beiden Fettsäuren aus Abb. 38 als Reste
hinzu erhält man 1-Palmityl-2-oleyl-phosphatidylcholin, das in den meisten Membranen höherer
Organismen zu finden ist (Abb. 39).
Abb. 39: 1-Palmityl-2-oleyl-phosphatidylcholin
Lipide
35
Dieter Baurecht
6 Spektroskopische Methoden zur Strukturaufklärung
6.1 Eigenschaften elektromagnetischer Strahlung
6.1.1 Spektralbereiche elektromagnetischer Strahlung
Moleküle, Atome, Elementarteilchen, etc. besitzen verschiedene Energieformen: z.B. Rotation,
Schwingungen, Spinn etc.
Die Unterteilung der elektromagnetischen Strahlung in verschiedene spektroskopische Bereiche
beruht im wesentlichen auf der Art der Wechselwirkung der jeweiligen Strahlungsenergie
(Wellenlänge, Frequenz, Wellenzahl) mit möglichen Energieübergängen der unterschiedlicher
Energieformen.
Abb. 40: Spektralbereiche und ihre Wechselwirkung mit Materie (aus 9).
Radiowellenbereich (nmr, esr): Beruht auf Spin-Umkehr von Kernbausteinen (Neutronen,
Protonen) oder Elektronen.
Mikrowellenbereich (Rotations-Spektroskopie): Änderung der Rotationsenergie von Molekülen.
Infrarotbereich (Vibrationsspektroskopie): Änderung der Schwingungsenergie von Molekülen.
Sichtbarer und Ultraviolett (UV) Bereich (UV-Vis Spektroskopie): Übergänge von
Valenzelektronen in Molekülen.
Röntgen-Bereich (X-Ray): Übergänge in den inneren Schalen von Atomen oder Molekülen.
γ-Strahlung: Umordnung von Kernbausteinen.
6.1.2 Energie der elektromagnetischen Strahlung
Max Planck: Die Energie eines Lichtquants hängt nur von der Frequenz ν der elektromagnetischen
Strahlung ab:
E = hν = h
c
λ
= hcν~
( 39 )
mit dem Planck’schen Wirkungsquantum h, der Lichtgeschwindigkeit c und der in der
Infrarotspektroskopie üblichen Wellenzahl ν~ = 1 / λ [cm-1].
36
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
6.1.3 Absorption von Licht, Lambert-Beer Gesetz
Die möglichen Energiezustände eines Systems (z.B. eines Moleküls) sind nicht kontinuierlich
veränderbar sondern nur in diskreten Schritten (quantisiert). Der Übergang zwischen zwei
Energieniveaus E1, E2 kann nur stattfinden, wenn das System Energie mit dem Betrag
∆E = E1 − E2 = hν aufnehmen (absorbieren) oder abgeben (emittieren) kann.
Alle, in Materie vorkommenden Energiezustände können, durch quantenmechanische
Auswahlregeln beschränkt, in andere Energiezustände übergehen. Die, für den Übergang in ein
höheres Energieniveau notwendige Energie kann bei spektroskopischen Untersuchungen von der
einfallenden Strahlung absorbiert (aufgenommen) werden. Dadurch vermindert sich die Intensität
der einfallenden Strahlung im entsprechenden Frequenzbereich (Energiebereich). Die Intensität I
oder Strahlungsflussdichte ist proportional zum Quadrat des elektrischen Feldes der Lichtwelle:
I ∝ E2 .
Bezeichnet man die frequenzabhängige Strahlungsintensität vor der Probe (Referenz, Background)
mit I0(ν) und die frequenzabhängige Strahlungsintensität nach der Probe mit I(ν) so ergibt sich für
die Durchlässigkeit (Transmission) T der Probe folgendes Verhältnis:
T (ν ) =
I (ν )
I 0 (ν )
( 40 )
Die Transmission in Abhängigkeit der Frequenz aufgetragen ergibt das Transmissionsspektrum.
Wenn eine Probe bei einer bestimmten Frequenz ν1 keine Strahlung absorbiert, ist die Intensität
I(ν1) gleich I0(ν1). Die Transmission wird damit T(ν1)=1 (100%). Entsprechend ergibt sich für eine
Frequenz ν2, bei der die gesamte Strahlung absorbiert wird ein I(ν2)=0, und damit eine
Transmission T(ν2)=0.
Bereits 1760 fand Lambert, dass die Abnahme der Strahlungsintensität bei ihrem Weg durch die
Materie proportional zur jeweiligen Intensität erfolgt:
dI ′ = −αI ′dx
( 41 )
Durch Integration erhält man für eine Probe der Dicke d:
I
d
∫
I ′= I 0
dI ′
= − ∫ α dx
I′
0
ln
( 42 )
I
= −α d
I0
Beer erkannte 1852 den Einfluss der Konzentration c auf die Strahlungsschwächung:
ln
( 43 )
I
= −α ′c d
I0
wobei α' den Napier'schen Absorptionskoeffizient (natürlicher log) angibt.
Durch Übergang zum dekadischen Logarithmus bekommt man das Lambert-Beer'sche Gesetz:
T=
I
= e −α ′c d = 10−ε c d
I0
bzw. frequenzabhängig T (ν ) =
I (ν )
= 10−ε (ν )c d
I 0 (ν )
( 44 )
mit ε (ν ) = α ′(ν ) ⋅ log(e ) und dem dekadischen Absorptionskoeffizienten ε (ν ) (Stoffkonstante).
Der Exponent ist die zur Konzentration und Schichtdicke proportionale Absorbanz A(ν )
A(ν ) = ε (ν ) ⋅ c ⋅ d
Spektroskopische Methoden zur Strukturaufklärung
( 45 )
37
Dieter Baurecht
mit dem molarern Extinktionskoeffizient ε(ν) (dekadisch), der Konzentration c in mol/l und
der Schichtdicke d der Probe in cm.
Dieser von Bouguer, Lambert und Beer beschriebene Zusammenhang gilt für verdünnte Lösungen
(bei höheren Konzentrationen kommt es zu Wechselwirkungen zwischen den Molekülen, die eine
Änderung von ε bewirken können). Damit lässt sich das Absorptionsspektrum (A als Funktion
von ν) darstellen.
Die Darstellung in Form der Transmission wird häufig verwendet, um Spektren qualitativ zu
beschreiben (wo treten Absorptionen auf, chemische Analyse). Der Vorteil der Darstellung als
Absorbanz folgt aus dem linearen Zusammenhang zwischen Absorbanz und Probenkonzentration
(Probendicke). Deshalb werden bei quantitativen Fragestellungen im allgemeinen
Absorptionsspektren angegeben.
6.2 UV/Vis Spektroskopie
(folgt)
6.3 Optische Rotation und Circulardichroismus
6.3.1 Optische Rotation
Optische Rotation und Circulardichroismus sind zwei stets miteinander gekoppelte
Erscheinungsformen der optischen Aktivität und resultieren aus der Wechselwirkung eines
Mediums mit linear polarisiertem Licht. Ihr Verständnis wird erleichtert, wenn man linear
polarisiertes Licht nach Fresnel als Überlagerung zweier gleicher Anteile links- und rechts-zirkular
polarisierten Lichtes auffasst (Abb. 41).
38
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
1
t, 0, Cos 2 π t
0
2.5
5
1
0
-1
1
1
0
10-1
7.5
t, Sin 2 π t , 0
0
2.5
5
1
0
-1
-1
1
0
10-1
7.5
t, - Sin 2 π t , 0
0
2.5
5
1
0
-1
11
0
7.5
10-1
2.5
5
1
0
-1
-1
1
0
10-1
7.5
2.5
0
5
2
4
1
0
-1
11
0
7.5
10-1
t, 0, 2 Cos 2 π t
6
8
0
1
0
1
0
1
0
1
0
1
0
-1
1
0
-1
0
-1
1
t, - Sin 2 π t , Cos 2 π t
0
-1
1
1
t, Sin 2 π t , Cos 2 π t
0
0
0
-1
2
1
10
2
1
0
-1
-2
1
-2
0
-1
0
-1
-1
0
1
Abb. 41a-f (von oben nach unten): Linear und zirkular polarisiertes Licht. Die Vektorkomponenten
{t,x,y} geben die Zeit t und die Komponenten des E-Feld in x- und y-Richtung an. a linear polarisiert in
Y-Richtung, b linear polarisiert in x-Richtung mit Phasenverschiebung π/2 gegenüber a. c linear
polarisiert in x-Richtung mit Phasenverschiebung -π/2 gegenüber a. d links-zikular polarisiertes Licht als
Summe aus a und b, e rechts-zirkular polarisiertes Licht als Summe von a und c. f Die Summe aus links(d) und rechts-zirkular (e) polarisiertem Licht ergibt wieder linear polarisiertes Licht.
Optisch aktive Medien besitzen für links- und rechts-zirkular polarisiertes Licht verschiedene
Brechungsindizes nl ≠ nr, und damit auch unterschiedliche Ausbreitungsgeschwindigkeiten vl ≠ vr
(da n=c/v). Der Laufzeitunterschied innerhalb einer Länge d’ für die beiden Wellen wird damit
∆t = t l − t r =
d ′ d ′ n l d ′ n r d ′ ∆n ⋅ d ′
−
=
−
=
vl vr
c
c
c
( 46 )
mit ∆n = nl − nr , und damit der Unterschied in der Phasenlage
∆ϕ = ω ⋅ ∆t = 2πν
∆n ⋅ d ′
∆n ⋅ d ′
= 2π
c
λv
( 47 )
mit der Wellenlänge des Lichts im Vakuum λv .
Spektroskopische Methoden zur Strukturaufklärung
39
Dieter Baurecht
1
t, Sin 6 t , Cos 6 t
0
1
0
0
2.5
5
-1
-1
1
7.5
0
10 -1
-1
-1
0
1
0
1
1
t, - Sin 6.2513 t , Cos 6.2513 t
0
1
0
2.5
0
5
-1
1
7.5
0
10 -1
-1
-1
2
t, Sin 6 t - Sin 6.2513 t , Cos 6 t + Cos 6.2513 t
1
0
2
4
6
8
0
-1
-2
10
2
1
0
-1
-2
2
-2
1
0
-1
-2
-1
0
1
2
α
∆ϕ
ϕl
ϕr
Abb. 42 Optische Rotation. Die rechts zirkular polarisierte Welle ist um ∆ϕ gegenüber der links zirkular
polarisierten Welle verschoben. Der resultierende Phasenwinkel α wird als optische Rotation bezeichnet.
Die optische Rotation α erhöht sich mit der Dicke der Probe und bleibt nach Austritt aus der Probe
konstant. Die optische Rotation wird durch unterschiedliche Winkelgeschwindigkeiten (ω=1, 6/2π)
simuliert.
Die optische Rotation α wird nach Abb. 42 zu
α=
ϕl + ϕr
2
α [rad ] = π
− ϕl =
ϕ l + ϕ l + ∆ϕ
2
− ϕl =
∆n ⋅ d ′
( 48 )
λv
α [ grad ] = α [rad ]
∆ϕ
2
180
π
=
180 ⋅ ∆n ⋅ d ′
λv
Um den Drehwinkel als Stoffkonstante angeben zu können, bezieht man auf eine Schichtdicke d in
Dezimetern und die Konzentration c in [g/cm³] und spezifiziert die Temperatur T und die
Wellenlänge λ
40
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
[α ]λ =
T
( 49 )
α grad ⋅ cm 3
c⋅d
g ⋅ dm
Für Vergleiche ähnlicher Stoffe empfiehlt sich eine molare Basis. Bei Polymeren bezieht man sich
auf die Molmasse der Polymerisationseinheit, so z.B. bei Proteinen auf die mittlere
Aminosäurerestmasse (MRW, mean residue weight)
[m]λ
T
MRW α
=
100 c ⋅ d
( 50 )
grad ⋅ cm 2
dezimol
6.3.2 Zirkulardichroismus
t, 10-t
30
1
Sin 6 t , 10-t 30 Cos 6t
1
0
2.5
0
0
5
-1
11
7.5
0
-1
10
0
1
t, - 10-t 50 Sin 6.2513 t , 10-t 50 Cos 6.2513 t
1
0
2.5
0
5
-1
1
7.5
0
10 -1
t, 10-t 30 Sin 6 t - 10-t 50 Sin 6.2513 t ,
10-t 30 Cos 6 t + 10-t 50 Cos 6.2513 t
2
1
0
2
4
6
8
2
1
0
-1
-2
2
-2
1
0
-1
10-2
0
-1
-2
-1
0
1
2
Abb. 43: Zirkulardichroismus. In einem Medium, das Zirkulardichroismus zeigt, wird links- und rechtszirkular polarisiertes Licht unterschiedlich gedämpft εl ≠ εr und breitet sich unterschiedlich schnell aus
nl ≠ nr. Als Folge ergibt sich elliptisch polarisiertes Licht.
Ein weiterer Aspekt der Wechselwirkung von polarisiertem Licht mit optisch aktiven Medien
besteht darin, dass dieses für die links- und rechts-zirkular polarisierte Komponente einen
unterschiedlichen Extinktionskoeffizient besitzt, εl ≠ εr. Dies hat zur Folge, dass die Amplituden des
in links- und rechts-zirkularlinear polarisiertes Licht zerlegten linear polarisierten Lichtes nach dem
Austritt aus der Probe unterschiedlich sind, was nach dem Zusammensetzten elliptisch polarisiertes
Licht ergibt (Abb. 43).
Die Elliptizität ist definiert als der Arcustangens des Verhältnisses von kleiner zu großer
Hauptachse (Abb. 44).
Spektroskopische Methoden zur Strukturaufklärung
41
Dieter Baurecht
Abb. 44: Zirkulardichroismus. Die E-Feld Vektoren des links- und rechts-zirkular polarisierten Lichtes
weisen nach dem Durchdringen optisch aktiver Materialien unterschiedliche Amplitude und Phase auf.
Dadurch entsteht elliptische Polarisation mit der Elliptizität θ = arctan(b/a) und um den Winkel α
gedrehter Hauptachse (aus 1).
Da die Transmission dem Quadrat des elektrischen Feldvektors proportional ist (T=I/I0=E²/E0²), gilt
( 51 )
El ,r = k Tl ,r
tan θ =
T − Tr
Tl − Tr
b El − Er
=
= l
=
a El + Er
Tl + Tr Tl + 2 TlTr + Tr
( 52 )
und da der Unterschied zwischen Tr und Tl und auch θ sehr klein ist
θ≈
1 ∆T
[rad ]
4 T
( 53 )
Mit dem Lambert-Beerschen Gesetz gilt:
A = − log(T )
A′ = − log(T + ∆T )
Taylor − Re ihe
=
∆T 1
− log(T ) −
T ln 10
⇒
∆T
= ( A − A′) ln 10
T
( 54 )
Damit wird ( 53 ) zu
θ=
( 55 )
ln(10)
∆A[rad ] = 33∆A[ grad ]
4
Die Elliptizität θ ist also dem Circulardichroismus ∆ε proportional (∆A = ∆ε c d).
6.3.3 Molekulare Ursachen
Die Quantentheorie der optischen Aktivität geht bereits auf Rodenfeld (1928) zurück. Nach ihrer
Kernaussage ist die optische Aktivität eines Moleküls daran gebunden, dass ein bestimmter
Elektronenübergang sowohl elektrisch als auch magnetisch erlaubt ist und dass die beiden
Übergangsmomente nicht senkrecht aufeinander stehen.
Die bekannteste Quelle optischer Aktivität ist das asymmetrische Kohlenstoffatom. Durch die
verschiedenen Liganden ist das Elektronensystem um das Kohlenstoffatom asymmetrisch. Man
spricht dabei von einem chiralen Chromophor. Beispiele sind die beiden Enantiomere des Alanins
(Abb. 45).
Bei Biopolymeren gibt es eine zusätzliche optische Aktivität durch die Asymmetrie der
Konformation (z.B. in Proteinen der Sekundärstruktur). Selbst bei vorliegender Symmetrie ist
optische Aktivität keineswegs selten. Der Grund liegt dann in einer asymmetrischen Störung des
Chromophors durch seine molekulare Umgebung.
42
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
Abb. 45: Die Enantiomere des Alanins. Durch die vier verschiedenen Liganden gibt es keine Symmetrie.
Das Molekül ist daher optisch aktiv (aus 1).
Exkurs: Nomenklatur der Enantiomere
Bestehen Moleküle aus gleichen Atomen und gleichen Bindungen, unterscheiden sich aber in ihrer
räumlichen Anordnung wie Bild und Spiegelbild, handelt es sich dabei um Enantiomere (Abb. 45).
Diese haben meist identische Schmelzpunkte, Siedepunkte, Löslichkeiten, Dichten, etc.
unterscheiden sich aber in der Wechselwirkung mit polarisiertem Licht. Um die beiden absoluten
Konfigurationen unterscheiden zu können gibt es unterschiedliche Ansätze. Ursprünglich
kennzeichnete man bei optisch aktiven Substanzen die rechtsdrehende Form mit dem Buchstaben d
(destro = rechts), die linksdrehende mit l (laevo = links) und die Racemform (50%d+50%l
Gemisch) mit dl-, ohne über die räumliche Anordnung der Substituenten am Kohlenstofftetraeder
etwas aussagen zu können. Als Erster hat E. Fischer (1891) am Beispiel der Glucose den Versuch
unternommen, ein System der konfigurativen Beziehungen Enantiomerer zu entwickeln. Im Jahre
1917 postulierte Wohl den Glycerinaldehyd als Bezugssubstanz für die Konfiguration optisch
aktiver Verbindungen und zwar schrieb er dem rechtsdrehenden Glycerinaldehyd willkürlich die dKonfiguration zu (Abb. 46). Die Präfixe d- und 1- gaben nunmehr die jeweilige relative
Konfiguration am asymmetrischen C-Atom im Raum an, während die tatsächlich gemessenen
Drehwerte (+) und (-) hinzugefügt wurden, z.B. d(+)-Glycerinaldehyd und d(-)-Glycerinsäure. Um
Verwechslungen der Angabe von d- und 1- für Drehsinn oder Konfiguration zu vermeiden, wurden
d- und 1- später durch klein gedruckte große Buchstaben D- und L- ersetzt. Sie geben lediglich die
Konfiguration am Chiralitätszentrum an, ohne den jeweiligen Drehungssinn zu berücksichtigen.
Das Bezugssystem bleibt weiterhin der D(+)-Glycerinaldehyd.
D-
L-
Abb. 46: Das Bezugssystem für die D-, L-Nomenklatur ist der Glycerinaldehyd. Ein Tetraeder, an dessen
Spitze die Aldehydgruppe steht und dessen vordere Kante rechts mit OH und links mit H besetzt ist,
definiert die D-Form. Die umgekehrte Anordnung von H und OH führt zum nicht kongruenten,
spiegelbildisomeren Raummodell, dem des L(-)Glycerinaldehyds (aus 10).
Da die D-, L- Nomenklatur eigentlich auf der Struktur von Glycerinaldehyd basiert, wurde später
von Chan, Ingold und Prelog (CIP-System) eine allgemeingültige absolute Konfiguration mittels
des RS-Systems definiert. Danach werden die 4 Liganden am Chiralitätszentrum nach ihrer
Priorität, d.h. nach fallender Atomnummer (Ordnungszahl) der am Chiralitätszentrum direkt
Spektroskopische Methoden zur Strukturaufklärung
43
Dieter Baurecht
gebundenen Atome (Vicinalatome), geordnet. Sind mindestens zwei der Vicinalatome gleich, so
werden die Atomnummern der mit ihnen verbundenen Atome der zweiten Sphäre für die
Zuordnung herangezogen. Notfalls muss man noch die Atome der dritten Sphäre in Betracht ziehen.
Das Tetraedermodell wird dann so angeordnet, dass das Atom mit der niedrigsten Priorität nach
rückwärts gerichtet ist, dann lassen sich die verbleibenden Atome (oder Atomgruppen) auf
zweierlei Weise anordnen. Einmal können sie mit fallender Priorität im Uhrzeigersinn und zum
anderen entgegengesetzt angeordnet sein. Man definiert die Konfiguration mit den Deskriptoren (R)
(rectus = rechts, richtig) und (S) (sinister = links, verkehrt) (Abb. 47).
Abb. 47: Das Tetraedermodell wird so angeordnet, dass das Atom mit der niedrigsten Priorität - in diesem
Fall H - nach rückwärts gerichtet ist, dann lassen sich die verbleibenden Atome (oder Atomgruppen) auf
zweierlei Weise anordnen. Einmal können sie mit fallender Priorität im Uhrzeigersinn und zum anderen
entgegengesetzt angeordnet sein. Man definiert die Konfiguration mit den Deskriptoren (R) (rectus =
rechts, richtig) und (S) (sinister = links, verkehrt); für den ersten Fall als (R)-Form und den zweiten als
(S)-Form (aus 10).
Beim Glycerinaldehyd ist die D- mit der (R)-Form und die L- mit der (S)-Form identisch.
6.3.4 Experimentelle Techniken zur Messung von OR und CD
Bei der Messung der optischen Rotation geht es im wesentlichen um die Bestimmung der Richtung
des linear polarisierten Lichtes. Dies wird durch eine Kreuzstellung von zwei Polarisatoren
(Polarisator und Analysator) bestimmt (minimieren des Ausgangssignals). Zusätzlich wird mit Hilfe
eines Modulators alternierend eine Drehung des Analysators um +1° und -1° erzeugt. In den beiden
Stellungen ergibt sich nur dann ein gleiches Signal, wenn sich der Analysator exakt in der
Kreuzstellung befindet.
CD:
lin. Pol. 45° durch doppelbrechendes Medium -> pp, vp Gangunterschied -> zirkular pol.
Gangunterschied kann durch Pockels Effekt verändert werden -> links- rechts-zirkular.
Messung der unterschiedlichen Intensitäten -> delta E
6.4 Infrarot Spektroskopie
6.4.1 IR-aktive Schwingungen, Dipolmomentsänderungen
Damit eine Molekülschwingung Infrarotlicht absorbieren kann, muss diese ein sich änderndes
Dipolmoment besitzen. Klassisch gesehen muss die Schwingung ein elektromagnetisches Feld
erzeugen, welches mit dem elektromagnetischen Feld der einfallenden Welle in Wechselwirkung
r
treten kann. Das Dipolmoment µ ist definiert als (3.2.5):
r
r
( 56 )
µ = q ⋅l
r
mit der Ladung q und dem Abstand zwischen den Ladungen l . Die Änderung des Dipolmomentes
mit der Zeit ist damit
r
r
( 57 )
dµ
Mi =
dt
44
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
r
Ist für eine bestimmte Schwingung M i = 0 , so kann diese Schwingung keine Infrarotstrahlung
absorbieren.
Dipolmomentsänderungen durch Vibrationen:
Durch die Bewegung der einzelnen Atome
r
kommt es zu Änderungen des Abstandes l zwischen den Atomen. Besitzen die Atome zusätzlich
partielle Ladungen so verursachen diese Bewegungen Änderungen des Dipolmomentes.
6.4.1.1 Beispiel CO2 Schwingungstypen
Symmetrische Streckschwingung (symmetric stretching vibration)
Abb. 48 Symmetrische Streckschwingung von CO2. Dipolmoment des gesamten Moleküls während der
gesamten Bewegung gleich 0 (aus 9).
Asymmetrische Streckschwingung (asymmetric stretching vibration)
Abb. 49 Asymmetrische Streckschwingung von CO2. Durch die asymmetrische Bewegung kommt es zu
einer Änderung des Dipolmomentes (aus 9).
Biegeschwingung (bending vibration)
Abb. 50 Biegeschwingung von CO2. Durch die Änderung der Bindungswinkel kommt es zu einer
Änderung des Dipolmomentes (aus 9).
Spektroskopische Methoden zur Strukturaufklärung
45
Dieter Baurecht
6.4.2 Vibrations-Energieniveaus im 2-atomigen Molekül
Klassisches Modell: Kräftegleichgewicht durch abstoßende Kräfte gleich geladener Teilchen
(Atomkerne, Elektronenwolken) und anziehende Kräfte des Kerns eines Atoms mit der
Elektronenwolke des anderen Atoms. Dadurch bleiben die Atome in einem mittleren Abstand, in
dem die beiden Kräfte ausgeglichen sind. d.h. die Energie des Systems (Moleküls) ist ein
Minimum.
6.4.2.1 Modell des klassischen harmonischen Oszillators
Als einfachstes Modell für ein 2-atomiges Molekül kann die Kraft zwischen den Atomen wie eine
Federkraft mit Hilfe des Hook’sches Gesetz beschrieben werden:
(
)
FFeder = − k r − req = − kψ
( 58 )
req ... Gleichgewichtsabstand (Abb. 51)
(
)
ψ = r − req ... Auslenkung aus der Ruhelage
k ... Kraftkonstante (Federkonstante)
FFeder ... Rückstellkraft der Feder
Negatives Vorzeichen: wird eine Masse in Richtung r bewegt so wirkt die Federkraft in Richtung -r.
Betrachtet man die Energie, die man in das System stecken muss um die Feder auszulenken,
benötigt man eine Kraft, die in Richtung von r wirken muss.
(
)
F = k r − req = k ⋅ ψ
( 59 )
Die dafür benötigte Energie ergibt sich zu:
E = ∫ F (r ′)dr ′ =
2
k
k
r − req ) = ψ 2
(
2
2
( 60 )
Dies ist die Energie die benötigt wird, um den Abstand der Atome von req auf r zu ändern (Abb.
51).
Abb. 51. Parabolischer Verlauf der Energie als Funktion der Änderung des Abstandes zwischen den zwei
Atomen (das erste Atom A befindet sich in dieser Darstellung immer im Punkt r=0, aus 9).
46
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
Wird eine Masse (Atom) dieses Systems ausgelenkt und losgelassen, so wird das System eine
Schwingung um den Gleichgewichtsabstand req durchführen.
In der Mechanik wird gezeigt, dass die Bewegung von zwei Teilchen mit den Massen m1 und m2
und dem Abstand req um einen gemeinsamen Schwerpunkt erfolgt. Die Bewegung der beiden
Teilchen kann auf die Bewegung eines einzelnen fiktiven Teilchens reduziert werden. Die Masse
dieses Teilchens bezeichnet man als reduzierte Masse µ
µ=
m1 ⋅ m2
m1 + m2
( 61 )
Die Bewegungsgleichung dieses Systems erhält man, indem ein Kräftegleichgewicht zwischen der
durch die Feder ausgeübten Kraft und der entgegen wirkenden Trägheitskraft ansetzt.
FFeder = µ ⋅ a
− k ⋅ψ = µ ⋅
( 62 )
d ψ
dt 2
2
und erhält damit folgende Differentialgleichung
( 63 )
d 2ψ
k
⋅ ψ = −ω 2ψ
2 = −
µ
dt
mit der Lösung
ψ = ψ 0 ⋅ sin(ω ⋅ t )
mit
ω=
( 64 )
k
µ
Die
ω
Frequenz
( 64 ) mit der das System schwingt hängt also nur von der reduzierten Masse µ und damit von
beiden Massen m1 , m2 , und von der Kraftkonstanten k ab.
6.4.2.2 Der quantenmechanische harmonischen Oszillators
Beim klassischen harmonischen Oszillator hängt die Energie von der Auslenkung ψ 0 ab und ist
somit kontinuierlich veränderbar. Die Lösung der Schrödingergleichung führt zu den
quantenmechanisch möglichen Zuständen der untersuchten Systeme. Für den harmonischen
Oszillator ergeben sich dabei folgende mögliche Energiezustände
1
E k = k + h ⋅ f osz mit k = 0,1,2...
2
( 65 )
Aus der Wechselwirkung mit dem elektromagnetischen Feld ergeben sich für ein 2-atomiges
Molekül mit einem sich ändernden Dipolmoment nur folgende erlaubte Übergänge (Auswahlregel)
∆k = ±1
( 66 )
Die Energiedifferenz eines Übergangs ist damit beim harmonischen Oszillator für alle Übergänge
gleich (Abb. 52)
1
1
∆E = E i − E i ±1 = k i + h ⋅ f osz − k i ±1 + h ⋅ f osz = ( k i − k i ±1 ) h ⋅ f osz
2
2
∆E = ± h ⋅ f osz
Spektroskopische Methoden zur Strukturaufklärung
( 67 )
47
Dieter Baurecht
Vergleicht
man
die
benötigte
Energiedifferenz
für
( 67 ) mit der Energie einer einfallenden elektromagnetischen Welle ( 39 )
∆E = ± h ⋅ f osz = h ⋅ ν
einen
Übergang
( 68 )
so erkennt man, dass die Schwingungsfrequenz des Moleküls f osz mit der Frequenz der
elektromagnetischen Strahlung ν übereinstimmen muss, damit ein Übergang und damit die
Absorption des Lichtquants möglich wird. Dies ist auch klassisch interpretierter. Das schwingende
Molekül kann Strahlung nur dann absorbieren, wenn es mit einer kohärenten Schwingung (gleiche
Frequenz) in Wechselwirkung tritt.
Abb. 52. Erlaubte Energieniveaus und Übergänge eines zweiatomigen Moleküls unter Annahme einer
einfachen harmonischen Bewegung (aus 9).
Zum Schluss sei noch einmal darauf hingewiesen, dass ein 2-atomiges Molekül nur dann
elektromagnetische Strahlung absorbieren kann, wenn es aus unterschiedlichen Atomen aufgebaut
ist, da sonst kein sich änderndes Dipolmoment vorhanden ist (Die Auswahlregel für dieses System
würde keine Übergänge ermöglichen).
6.4.2.3 Der quantenmechanische anharmonische Oszillator
Der anharmonische Oszillator beschreibt ein realeres Energiepotential das durch die empirisch
ermittelte Morsefunktion ( 69 ) gegeben ist (Abb. 53).
[
E = Deq. 1 − e
48
]
a ( req . − r ) 2
( 69 )
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
Abb. 53 Erlaubte Schwingungsenergiezustände und exemplarische Übergänge eines 2-atomigen Moleküls
unter Annahme des Energiepotentials eines anharmonischen Oszillators (aus 9).
Durch Lösung der Schrödingergleichung ergeben sich folgende Energieniveaus:
2
1
1
Ek = k + h ⋅ f e - k + h ⋅ f e ⋅ x e ± [
2
2
]3...
mit k = 0,1,2...
( 70 )
Im Gegensatz zum harmonischen Oszillator sind aufgrund der Auswahlregeln hier auch Übergänge
zwischen weiter entfernten Energieniveaus möglich (Übergänge höherer Ordnung).
∆k = ±1,2,3,...
( 71 )
6.4.3 Vibrationsmoden mehratomiger Moleküle
6.4.3.1 Schwingungsfreiheitsgrade, Normalschwingungen
Ein Molekül mit N Atomen besitzt 3N Bewegungsfreiheitsgrade. Translationen aller Atome in den
3 Raumrichtungen und Rotationen um die drei Koordinatenachsen ändern jedoch weder die
Abstände der Atome noch die Winkel zwischen den Atomen. Es bleiben also 3N-6
Schwingungsfreiheitsgrade. Bei linearen Molekülen sind nur zwei Rotationsfreiheitsgrade
abzuziehen, da eine Rotation um die Molekülachse die Lage der Atome nicht ändert. Lineare
Moleküle besitzen also 3N-5 Schwingungsfreiheitsgrade. Diese 3N-6 (3N-5) Schwingungen heißen
Normal- oder Grundschwingungen, bei denen sich alle Atome des Moleküls mit gleicher
Frequenz und gleicher Phase bewegen.
6.4.3.2 Gruppenschwingungen und Gerüstschwingungen
Bei großen Molekülen können niemals alle Normalschwingungen zugeordnet werden. Viele
Funktionelle Gruppen besitzen jedoch charakteristische Schwingungen die weitgehend unabhängig
vom Rest des Moleküls sind. Diese Schwingungen werden Gruppenschwingungen (Abb. 54, Abb.
55) genannt.
Spektroskopische Methoden zur Strukturaufklärung
49
Dieter Baurecht
Die Vielzahl der restlichen Normalschwingungen bilden hingegen oft ein charakteristisches Muster
(Fingerprint) für das Molekülgerüst und werden daher Gerüstschwingungen (Abb. 55) genannt.
Abb. 54 Bezeichnungen für verschiedene Arten von Gruppenschwingungen (aus 11).
Abb. 55: Absorptionsbereiche des IR-Spektrums. Gruppenschwingungen und Gerüstschwingung von
Aceton (aus 11).
50
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
6.4.3.3 Beispiel: Normalschwingungen der Amidbindung
Zur theoretischen Berechnung der Normalschwingungen der Amidgruppe wird ein vereinfachtes
Modell der Amidbindung verwendet (12). Dabei werden neben den zentralen Atomen der
Amidbindung O, C, N und H die vorne und hinten angrenzenden Strukturen nur mehr als zwei
einzelne Teilchen betrachtet (Abb. 56).
Abb. 56: Modell der Amidbindung bei der die angrenzenden Strukturen nur mehr als einzelne
Masseteilchen C1 und C4 betrachtet werden (aus 12).
Die Normalkoordinatenanalyse der 6 Teilchen ergibt 3*6-6=12 Normalschwingungen (Abb. 57).
Abb. 57: Normalschwingungen der modellhaften Amidbindung aus Abb. 56. (a) NH strech; (b) amide I;
(c) amide II; (d) amid III; (e) amide IV; (f) amide V; (g) amide VI; (h) :amide VII; (i) 1070; (j) 909; (k)
498; (l) 274 (aus 12).
Spektroskopische Methoden zur Strukturaufklärung
51
Dieter Baurecht
6.4.4 Messprinzip der IR-Spektroskopie
Um ein IR-Spektum zu erhalten, muss man die Intensität der IR-Strahlung in Abhängigkeit von der
Wellenlänge messen können. Seit den achtziger Jahren haben die klassischen IR-Spektrometer (mit
Beugungsgitter oder Prismen als Monochromator) entscheidend zugunsten der leistungsfähigeren
FTIR-Spektrometer (FT = Fourier Transform, 6.4.4.1) an praktischer Bedeutung verloren.
Um Transmissions- und/oder Absorptionsspektren zu ermitteln, muss die Intensitätsverteilung der
IR-Strahlung vor der Probe I0(ν) sowie die Intensität I(ν), der im IR-Strahl vorkommenden
Wellenlängen nach der Probe bekannt sein (6.1.3). Da die Konstruktion von Spektrometern eine
Vielzahl von optischen Elementen erfordert, ist es nicht möglich, die Intensitätsverteilungen der IRStrahlung direkt vor bzw. nach der Probe zu messen. Transmissions- und Absorptionsspektren
können jedoch auch berechnet werden, wenn man die Intensitätsverteilung der IR-Strahlung einmal
ohne Probe (Referenzspektrum = I0(ν)) und einmal mit der Probe im Strahlengang (Einkanalspektrum der Probe = I(ν)) misst. Dazu wird der IR-Strahl in zwei Lichtbündel gleicher Intensität
aufgeteilt, von denen eines die Probe durchläuft. Das zweite Lichtbündel dient als Vergleichsstrahl
(Referenz) und durchläuft, z.B. bei Lösungen, eine Küvette mit dem reinen Lösungsmittel. Als
weitere und bei modernen Fair-Geräten übliche Möglichkeit können Referenz- und
Probenmessungen zeitlich getrennt, im selben Strahlengang durchgeführt werden.
Das Spektrometer enthält eine Strahlungsquelle, die ständig einen für das entsprechende
Spektrometer charakteristischen Frequenzbereichbereich emittiert. Als Strahlungsquelle im IRBereich kommt z.B. eine Wendel aus Siliciumcarbid (Globar) zum Einsatz, die bei einer
Temperatur von 1500 K, IR-Strahlung produziert. Mittels optischer Komponenten (i.a. Spiegel)
wird der IR-Strahl gebündelt und nach dem Durchstrahlen eines Probenraumes über einen
Monochromator, der die Strahlung in seine einzelnen Frequenzbereiche zerlegt, zu einem
Detektor geleitet [in FTIR-Spektrometern durchläuft der Strahl vor der Probe ein Interferometer
(Abb. 58) und keinen Monochromator]. Der Detektor registriert die Intensität der einfallenden
Strahlung, und wandelt diese in elektrische Signale um, die von einem Schreiber als Spektrum
aufgezeichnet werden können. Die Signale können auch von einem Computer, mit zusätzlichen
Elektronik-Komponenten erfasst, und EDV-mäßig weiterverarbeitet werden.
6.4.4.1 Fourier Transform Infrarot (FTIR)-Spektrometer
Bei FTIR-Spektrometern wird am Detektor das sogenannte Interferogramm aufgezeichnet. Dieses
wird erst durch eine nachträgliche Fourier-Transformation in ein konventionelles IR-Spektrum
umgewandelt (Abb. 58).
52
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
Abb. 58. Blockdiagramm eines FTIR Spektrometers. Die Abbildung zeigt auch das Interferogramm einer
monochromatischen Lichtquelle λ (z.B. Laser) und das daraus, durch die Fourier-Transformation
erhaltene Spektrum. δ...optischer Wegunterschied zwischen festen und beweglichen Spiegel (patt
difference, retardation, aus 13).
6.4.4.2 ATR-Spektroskopie
In Abb. 59 wird die konventionelle Transmissions-Technik und die ATR-Technik (Abgeschwächte
Total Reflexion) gegenübergestellt. Bei der ATR-Technik wird die Probe in engen Kontakt mit
dem, im IR-Bereich transparenten ATR-Kristall gebracht. Der Einfallswinkel des IR-Stahls θ muss
größer sein als der kritische Winkel, ab dem im ATR-Kristall Totalreflexion auftritt. Die Strahlung
wird dadurch an der Grenzfläche zwischen Kristall und Probe totalreflektiert. Bedingt durch die
physikalischen Eigenschaften der Totalreflexion (Stetigkeit des elektromagnetischen Feldes) dringt
das elektromagnetische Feld dabei auch in das angrenzende Medium (Probe) ein. Dabei kann von
der Probe Strahlung absorbiert und die Strahlungsintensität abgeschwächt weden.
Spektroskopische Methoden zur Strukturaufklärung
53
Dieter Baurecht
Abb. 59: Vergleich von Transmissions- und ATR-Spektroskopie. n1, n2 Brechungsindizes des ATRKristalls (n1) und der Probe (n2), D Detektor (aus 14).
Die Feldstärke, der in das angrenzende Medium eindringenden Strahlung, nimmt exponentiell mit
der Tiefe ab. Die Eindringtiefe des Strahls dp, gibt die Tiefe an, bei der die Feldstärke nur mehr den
1/e-ten Teil der Feldstärke im Kristall besitzt. Sie wird von mehreren Größen beeinflusst:
dp =
λ1
2 ⋅ π ⋅ (sin2 θ) − n2
21
=
λ Vakuum
2 ⋅ π ⋅ n2 ⋅ (sin2 θ) − n2
1
( 72 )
2
λ1(=λVakuum/n1) gibt die Wellenlänge der Strahlung im Kristall an, θ den Einfallswinkel des IRStrahls im Kristall (Abb. 59) und n21 das Verhältnis der Brechungsindizes im Kristall n1 und in der
Probe n2 (n21=n2/n1).
Da im allgemeinen weder die Wellenlänge λ1 noch der Brechungsindex der Probe n2 frei gewählt
werden kann, ist eine Änderung der Eindringtiefe nur durch den Brechungsindex des Kristalls n1
und den Einfallswinkel θ möglich. Der Einfallswinkel θ wird jedoch auch von der Geometrie der
optischen Elemente vorgegeben (Abb. 60). Soll bei der Untersuchung von dünnen Schichten die
Eindringtiefe gering sein, um den hinter der Schicht liegenden „Background“ aus der Messung
auszuschließen, muss also n1 möglichst groß sein.
Abb. 60: Schematischer Aufbau einer ATR-Optik. Über die Spiegel S wird das IR-Licht auf den ATR
Kristall gelenkt. In diesem kommt es auf der oberen und der unteren Grenzschicht zu mehreren
Totalreflexionen. Auf der Austrittsseite wird das IR-Licht wiederum von Spiegeln in den ursprünglichen
Strahlengang abgelenkt (aus 14).
Der praktische Aufbau einer ATR-Optik ist in Abb. 60 dargestellt. Durch mehrere Totalreflexionen
wird erreicht, dass die zu untersuchende Schicht mehrmals „durchdrungen“ wird (aktive
Totalreflexionen). Damit kann auch bei extrem dünnen Proben (z.B. Monoschichten) eine, für die
54
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
Analyse ausreichende Gesamtabsorption erreicht werden. Zusätzlich kann die Probe auf beiden
Seiten des Kristalls aufgetragen werden, was zu einer Verdoppelung aktiver Totalreflexionen führt.
6.5 Raman-Spektroskopie
Wenn Licht Materie durchdringt kommt es neben den bereits besprochenen Wechselwirkungen
(Absorptionen) auch zu reinen Streueffekten. Wird das Licht vollkommen elastisch gestreut, hat
das gestreute Licht die selbe Energie wie vor der Streuung, allerdings eine andere Richtung
(Rayleigh Streuung). Wird eine Probe mit monochromatischem Licht durchstrahlt misst man in
allen Raumrichtungen das gestreute Licht mit gleicher Wellenlänge. Zusätzlich findet man aber in
der Streustrahlung auch Licht mit diskreten Frequenzen knapp über und knapp unter der Frequenz
des ursprünglichen einfallenden Lichts. Dieser Effekt wird als Raman-Streuung bezeichnet.
6.5.1 Teilchenmodell
Wird Licht als Teilchen (Photon) betrachtet, so ist die Energie eines Photons hν. Die Photonen
können nun Stöße mit den Molekülen eingehen. Ist der Stoß vollkommen elastisch, werden die
Teilchen in Ihrer Energie ungeändert abgelenkt. Kommt es jedoch zu einer inelastischen Kollision
kann Energie zwischen dem Teilchen und dem Photon ausgetauscht werden. Das Molekül kann
dabei Energie in der Höhe ∆E vom Photon aufnehmen oder auch an das Photon abgeben. ∆E muss
dabei wiederum dem Unterschied in den Energieniveaus vibratorischer (oder rotatorischer)
Energiezustände des Moleküls entsprechen. Wenn das Molekül Energie vom Photon aufnimmt so
wird das gestreute Licht nur mehr die Energie hν-∆E, bzw. die Frequenz ν-∆E/h aufweisen.
Umgekehrt wird die Frequenz des gestreuten Photons bei Energieaufnahme um ∆E/h erhöht.
Die gestreute Strahlung mit um ∆E/h niedrigerer Frequenz wird als Stokes Strahlung bezeichnet,
die Strahlung mit höherer Energie als Anti-Stokes Strahlung (Abb. 61). Die Intensität der Stokes
Strahlung ist generell intensiver jedoch noch immer klein gegenüber der Intensität der Raleigh
Streuung.
Abb. 61: Prinzipielle Darstellung eines Raman-Spektrums. Man erkennt, dass die Raman-Linien
unterhalb und oberhalb der Rayleigh-Linie symmetrisch angeordnet sind. Die jeweiligen
Wellenzahlverschiebungen entsprechen den Schwingungsfrequenzen des Moleküls. Die Verschiebung zu
niedrigeren Wellenzahlen (niedrigere Frequenz und niedrigere Energie) nennt man Stokes-Verschiebung
und die dazugehörigen Banden bezeichnet man als Stokes-Linien. Dementsprechend bezeichnet man die
Verschiebung zu höheren Wellenzahlen (höhere Frequenz und höhere Energie) als Anti-StokesVerschiebung und die Banden als Anti-Stokes-Linien. Die Wellenzahl der Rayleigh-Linie entspricht in
Wirklichkeit der Wellenzahl der anregenden Strahlung. Um die Raman-Spektren einfacher mit IRSpektren vergleichen zu können, setzt man den Wert der Rayleigh-Linie auf Null. Der Betrag der RamanVerschiebungen ist aber für alle Anregungswellenlängen gleich. Desweiteren misst man in der RamanSpektroskopie häufig nur die Stokes-Linien, da sie intensiver als die Anti-Stokes-Linien sind. Deshalb
wird das negative Vorzeichen oft weggelassen (von: http://www.chemgapedia.de).
Spektroskopische Methoden zur Strukturaufklärung
55
Dieter Baurecht
6.5.2 Klassische Theorie der Raman Streuung
Die klassische Beschreibung der Raman Streuung beruht auf dem Begriff der Polarisierbarkeit
von Molekülen. Wenn ein Molekül einem elektrischen Feld ausgesetzt wird kommt es zu
Änderungen in der Ladungsverteilung im Molekül und einem damit verbundenem induzierten
Dipolmoment. Die Größe des induzierten Dipols µi hängt von der Größe des äußeren elektrischen
Feldes E und der Fähigkeit des Moleküls den Dipol zu induzieren (Polarisierbarkeit α) ab.
µ i = αE
( 73 )
Wird das Molekül dem Feld einer elektromagnetischen Welle
E = E0 sin (2πνt )
( 74 )
ausgesetzt wird der induzierte Dipol ebenfalls mit dieser Frequenz oszillieren
µ i = αE = αE0 sin (2πνt )
( 75 )
Wird die Polarisierbarkeit α jedoch auch durch Änderungen der Molekülgeometrie, z.B. durch
Vibrationen des Moleküls beeinflusst, so ist α nicht mehr konstant sondern wird durch die
Molekülschwingung moduliert,
α = α 0 + α M sin (2πν M t )
( 76 )
und der induzierte Dipols µi wird zu
µi = α 0 E0 sin (2πνt ) + α M E0 sin (2πν M t )sin (2πνt )
( 77 )
Mit Hilfe der trigonometrischen Relation
sin (α )sin (β ) =
( 78 )
1
[cos(α − β ) − cos(α + β )]
2
wird ( 77 ) zu
1
2
µ i = α 0 E0 sin (2πνt ) + α M E0 [cos(2π (ν − vM )t ) − cos(2π (ν + vM )t )]
( 79 )
Damit hat der oszillierende Dipol Frequenzkomponenten mit ν und ν m vM .
6.5.3 Raman-aktive Schwingungen
Die Frequenzkomponenten mit den Frequenzen der Stokes und Anti-Stokes Linien, ν m vM treten
nach ( 79 ) nur auf, wenn α M ≠ 0 ist. Eine Molekülschwingung ist daher nur dann Raman-aktiv,
wenn die Molekülschwingung die Polarisierbarkeit des Moleküls moduliert.
Wenn ein Molekül eine geringe oder keine Symmetrie aufweist sind im allgemeinen alle
Schwingungsmoden Raman-aktiv. Bei Molekülen mit höherem Symmetriegrad ist es im
allgemeinen nicht ohne nähere Untersuchungen möglich, eine Aussage zu treffen ob einzelne
Schwingungsmoden die Polarisierbarkeit des Moleküls modulieren und damit Raman-aktiv sind.
Eine allgemein gültige Regel (mutual exclusion) ist jedoch, dass bei Molekülen mit
Symmetriezentrum Infrarot-aktive Schwingungen Raman-inaktiv und IR-inaktive Schwingungen
Raman-aktiv sind. Als Beispiel dafür ist in Abb. 62 die Änderung der Polarisierbarkeit α und des
Dipolmoments µ bei der symmetrischen und asymmetrischen Streckschwingung des CO2-Moleküls
gezeigt (siehe auch Abb. 48-Abb. 50).
Im Prinzip liefert die Ramanstreuung dieselbe Information wie die Infrarotabsorption, nämlich die
Frequenzen der Molekülschwingungen. Beide Effekte beruhen jedoch auf ganz unterschiedlichen
physikalischen Prozessen. Infrarotabsorption geschieht dann, wenn die Molekülschwingung eine
Änderung des permanenten Dipolmoments verursacht, während Ramanstreuung auftritt, wenn die
Molekülschwingung die Polarisierbarkeit moduliert. Zusätzlich existieren für Ramanstreuung und
56
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
Infrarotabsorption unterschiedliche Auswahlregeln, die von den Symmetrieeigenschaften des
Moleküls abhängen.
Abb. 62: Änderung der Polarisierbarkeit α und des Dipolmoments µ bei der symmetrischen und
asymmetrischen Streckschwingung des CO2-Moleküls (aus 11).
Die Raman-Spektroskopie eignet sich daher besonders zur Charakterisierung unpolarer oder wenig
polarer Bindungen, wie z. B. C≡C, C=C, N=N, C-C, O-O, S-S sowie von Ringen. Die
Gerüstschwingungen von (C-C)-Bindungen in Ringen sind im Raman-Spektrum meist wesentlich
stärker als im IR-Spektrum. Dadurch lassen sich die Strukturen von Molekülgerüsten zuordnen.
Umgekehrt sind die starken und charakteristischen IR-Banden polarer Gruppen wie C=O und O-H
im Raman-Spektrum nur schwach vertreten. Dies ermöglicht, auch Wasser als Lösungsmittel zu
verwenden. In der IR-Spektroskopie ist Wasser wegen seiner starken Eigenabsorption ein schlecht
geeignetes Lösungsmittel. Dagegen können von wässrigen Lösungen ohne weiteres RamanSpektren aufgenommen werden, da in Glasküvetten gearbeitet wird und Wasser ein linienarmes,
wenig intensives Raman-Spektrum besitzt.
Ein Vergleich zwischen den Banden des Raman- und IR-Spektrums von Dichlorethylen ist in Abb.
63 und in Tab. 7 dargestellt.
Abb. 63: IR-Transmissionsspektrum und Laser-Raman-Spektrum
Bandenzuordnung ist in Tab. 7 angegeben (aus 11).
Spektroskopische Methoden zur Strukturaufklärung
von
Dichlorethylen.
Die
57
Dieter Baurecht
Tab. 7: Zuordnung der IR- und Ramanbanden von Dichlorethylen (Abb. 63, aus 11).
6.5.4 Raman-Spektrometer
Zur Messung des Raman-Spektrums benötigt man monochromatisches Licht aus einer sehr
intensiven Lichtquelle, dessen Wellenlänge zwischen dem UV- und IR-Gebiet liegen muss, da dort
mit wenig Störabsorptionen zu rechnen ist. Allerdings können Fluoreszenz-Strahlungen aus
Verunreinigungen der zu untersuchenden Probe das intensitätsschwache Raman-Streulicht
vollkommen überdecken und die Aufnahme eines Raman-Spektrums unmöglich machen.
Die Einführung des Lasers in den sechziger Jahren hat die benötigten Substanzmengen auf wenige
Milligramm reduziert, die Registrierzeit von Stunden auf Minuten verkürzt und gleichzeitig das
Signal-Rausch-Verhältnis verbessert. Ursache ist die enorme Steigerung der Bestrahlungsdichte (ca.
10 Größenordnungen) gegenüber dem leistungsschwachen Quecksilber-Niederdruck-Brenner.
Abb. 64: Schematischer Aufbau eines klassischen dispersiven Raman-Spektrometers. Das aus der LaserLichtquelle kommende monochromatische Licht tritt durch die Probe und wird vom Spiegel S1
reflektiert, um die Intensität zu verdoppeln. Das Raman-Streulicht wird meist quer zur
Durchstrahlungsrichtung beobachtet und mit einer Linse auf den Eintrittsspalt 1 fokussiert. Der Spiegel
SZ verdoppelt die Intensität des Streulichtes. Am Gitter wird die Streustrahlung spektral zerlegt und nach
Durchgang des Austrittsspaltes 2 auf den photoelektrischen Detektor fokussiert (aus 11).
In Abb. 64 ist der Aufbau eines dispersiven Raman-Spektrometers schematisch angegeben. Ein
großer Vorteil dispersiver Raman-Geräte besteht in der Vielzahl der einsetzbaren Laserquellen
58
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
überwiegend im sichtbaren Spektralbereich. Fluoresziert z.B. eine Substanz, so kann schon der
Wechsel der Erregerlinie zu einem auswertbaren Spektrum führen. Des Weiteren ergeben die
Wellenlängen im sichtbaren Bereich höhere Raman-Intensitäten als die bei den FT-Raman-Geräten
genutzte Anregung mit Wellenlängen im nahen Infrarotbereich.
Aktuelle FT-Raman-Spektrometern benutzten den Neodym-YAG-Laser als Lichtquelle. Er emittiert
bei 1064 nm, einer Energie, die für die Anregung der störenden Fluoreszenz nicht ausreicht. Erkauft
wird dieser Vorteil mit einer erheblich geringeren Intensität des Raman-Streulichts, die den Einsatz
der Fourier-Transform-Technik zur Detektion erfordert. Da deren Vorteile jedoch den
Intensitätsverlust des Neodym-YAG-Lasers überkompensieren, dürften die FT-Geräte auch im
Raman-Bereich die klassischen Spektrometer ablösen. Eine Alternative dazu sind Arraydetektoren,
die im Raman-Spektrum zu detektierenden UV-Vis Bereich wesentlich günstiger sind als im IRBereich. Weitere verwendete Anregungswellenlängen sind 785 nm, 633 und 532 nm.
6.6 Kernspinresonanzspektroskopie
6.6.1 Einleitung
Die Kernspinresonanzspektroskopie (nuclear magnetic resonance, NMR) ist insofern einzigartig, als
sich mit ihr die atomare Struktur von Makromolekülen in Lösung ermitteln lässt, vorausgesetzt
allerdings, dass es gelingt, eine hochkonzentrierte Lösung (>1 mM oder 15 mg ml-1 bei einem
Protein von 15 kd) herzustellen. Diese Methode basiert auf der Tatsache, dass bestimmte
Atomkerne über einen inneren Magnetismus verfügen. Nur bei wenigen Isotopen ist diese
Eigenschaft, der Spin, vorhanden. Die für die Biochemie am wichtigsten Isotope für NMRSpektroskopische Untersuchungen sind in Tab. 8 zusammengefasst. Das einfachste Beispiel liefert
der Kern des Wasserstoffatoms (1H), ein Proton.
Die Drehbewegung, der Spin, eines Protons erzeugt ein magnetisches Moment. Dieses Moment
kann, wenn ein externes magnetisches Feld angelegt wird, eine von zwei möglichen
Orientierungen oder Spinzuständen (α und ß) einnehmen. Die Energiedifferenz zwischen den
beiden Zuständen ist der Stärke des angelegten Feldes proportional. Dabei ist der α-Zustand mit
seiner etwas niedrigeren Energie geringfügig stärker besetzt (bei einem Routineexperiment um
einen Faktor 1,00001), da seine Feldrichtung mit der des äußeren Feldes ungefähr übereinstimmt.
Ein rotierendes Proton im α-Zustand kann in einen erregten ß-Zustand angehoben werden, indem
man einen elektromagnetischen Strahlungsimpuls (einen Hochfrequenz- oder RF-Impuls von radio
frequency) anlegt, welcher die der Energiedifferenz zwischen α- und ß-Zustand entsprechende
Frequenz bereitstellt. Unter diesen Bedingungen ändert sich der Spin von α nach ß.
Das Resonanzspektrum für ein Molekül lässt sich ermitteln, indem man das magnetische Feld bei
konstanter Frequenz der elektromagnetischen Strahlung variiert oder indem man das Feld konstant
hält und die Frequenz der Strahlung ändert. Diese Eigenschaften lassen sich nutzen, um das
chemische Umfeld des Wasserstoffkerns zu untersuchen. Der Elektronenfluss um einen
magnetischen Kern erzeugt ein geringfügiges lokales Magnetfeld, das dem angelegten Feld
entgegenwirkt. Die Stärke dieser Gegenkraft hängt von der umgebenden Elektronendichte ab.
Folglich werden Kerne in unterschiedlicher Umgebung bei geringfügig verschiedenen Feldstärken
oder Strahlungsfrequenzen ihren Zustand ändern, das heißt Resonanz zeigen. Die Kerne der
angeregten Probe emittieren elektromagnetische Strahlung, deren Frequenz sich messen lässt.
Diesen Frequenzunterschied, den man auch als chemische Verschiebung bezeichnet, drückt man in
Bruchteilen δ (ppm, parts per million) aus, bezogen auf eine hinzugefügte Vergleichssubstanz,
beispielsweise ein wasserlösliches Tetramethylsilanderivat. So weist ein Methylproton (-CH3)
typischerweise eine chemische Verschiebung δ von 1 ppm auf, ein aromatisches Proton hingegen
eine chemische Verschiebung von 7 ppm. Die chemischen Verschiebungen für die meisten
Wasserstoffkerne in einem Proteinmolekül liegen im Bereich von 0 bis 9 ppm.
Bei vielen Proteinen ist es möglich, mit dieser Technik der so genannten eindimensionalen NMR
fast alle Protonen darzustellen. Aus diesen Informationen können wir dann auf die Veränderungen
schließen, die eine bestimmte chemische Gruppe unter verschiedenen Bedingungen erfährt - bei
Spektroskopische Methoden zur Strukturaufklärung
59
Dieter Baurecht
einem pH-bedingten Konformationswechsel eines Proteins von einer ungeordneten Struktur zur αHelix beispielsweise.
Noch mehr Informationen erhalten wir, wenn wir untersuchen, wie sich der Spin verschiedener
Protonen auf deren Nachbarn auswirkt. Erzeugt man durch einen Hochfrequenzimpuls eine
vorübergehende Magnetisierung, kann man den Spin eines Kerns verändern und die Auswirkungen
dieser Veränderung auf den Spin der Nachbaratome untersuchen. Besonders informativ ist in
diesem Zusammenhang ein zweidimensionales Spektrum, das sich durch die so genannte NOESY
Spektroskopie (nuclear Overhauser enhancement spectroscopy) ergibt, die eng benachbarte
Protonenpaare graphisch darstellt, auch wenn diese in der Primärstruktur nicht nahe beieinander
liegen. Grundlage dieser Methode ist der Kern-Overhauser-Effekt (nuclear Overhauser effect,
NOE), eine Wechselwirkung zwischen zwei Kernen, die umgekehrt proportional zur sechsten
Potenz des Abstands zwischen beiden ist. Die Magnetisierung wird von einem angeregten auf einen
nicht angeregten Kern übertragen, wenn beide nicht mehr als 0,5 nm voneinander entfernt sind. Mit
anderen Worten, dieser Effekt liefert ein Mittel, innerhalb der dreidimensionalen Struktur eines
Proteins die Lage von Atomen in Relation zueinander nachzuweisen.
6.6.2 Kernspin
Proton und Neutron besitzen einen Spin von ½. Erfahrungsregel zum Gesamtspin von
Atomkernen mit mehreren Protonen und Neutronen:
•
•
•
Kerne mit gerader Anzahl von Protonen und Neutronen haben Spin 0 (4He, 12C, 16O).
Kerne mit ungerader Anzahl von Protonen und Neutronen (ungerader Ladungszahl, aber
gerader Massenzahl) haben ganzzahligen Spin (2H, 14N: Spin=1, 10B: Spin=3).
Kerne mit ungrader Massenzahl haben halbzahligen Spin (1H, 13C, 15N: Spin=½, 17O:
Spin=5/2)
Die Spinquantenzahl des Kerns I kann daher nur ganz- oder halbzahlige Werte annehmen: I = 0,
1/2, 1, 3/2, ...
Der Eigendrehimpuls ergibt sich zu
p = I ( I + 1)
( 80 )
h
2π
und damit das magnetische Moment
µ = γ I ( I + 1)
( 81 )
h
2π
mit dem Magnetogyrischen Verhältnis γ , einer Konstante die für eine Kernart charakteristisch ist
und die unter anderem von Ladung und Masse des Kerns bestimmt wird.
Im homogenen, statischen Magnetfeld B0 nimmt der Drehimpulsvektor P bestimmte ausgewählte
Winkel zum B0-Vektor ein (Richtungsquantelung). Ist das Feld in z-Richtung wird:
pz = m
( 82 )
h
2π
mit der magnetischen oder Orientierungs-Quantenzahl m = +I, I-1, ... -I+1, -I
Für das 1H Atom mit I = ½, ergeben sich damit zwei Zustände m = ± ½.
Diese Eigenzustände sind energetisch in die Kern-Zeeman-Niveaus aufgespalten:
60
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
Em = − µ z B0 = −γp z B0 = −γm
h
B0
2π
⇒ ∆E = γ
h
B0
2π
( 83 )
Eingestrahlte Energiequanten vom Betrag ∆E können eine Spin-Inversion bewirken. Die Frequenz
dieser Strahlung wird als Resonanzfrequenz (Tab. 8) bezeichnet und beträgt:
ν=
B
∆E
=γ 0
h
2π
( 84 )
Der Energieunterschied der aufgespaltenen Niveaus ist bei realen Experimenten sehr gering (z.B.
4x10-26 J bei 1.4 T). Im thermischen Gleichgewicht gehen die Kerne eine Boltzmann-Verteilung ein
und es ergibt sich für das Verhältnis der Besetzungszahlen:
∆E
−
N m = −1 / 2
= e kT
N m = +1 / 2
( 85 )
Für Raumtemperatur und ein 1.4092 T Feld ergibt sich damit z.B.
N m = −1 / 2
4 ⋅ 10−26
) ≈ exp( −1 ⋅ 10− 5 ) ≈ 1 − 1 ⋅ 10− 5
≈ exp( −
− 21
N m = +1 / 2
4.2 ⋅10
( 86 )
also beinahe ein Verhältnis von 1 oder ein nur sehr geringfügig häufiger besetztes niedrigeres
Energieniveau.
Tab. 8: Eigenschaften von für die NMR-Spektroskopie organischer Verbindungen relevanter Kerne (aus 11).
6.6.3 Chemische Verschiebung
Die tatsächliche Resonanzfrequenz einer bestimmten Kernsorte hängt von der Magnetfeldstärke B
ab. Die am Kernort wirkende effektive Magnetfeldstärke unterscheidet sich von B0 um das am Ort
durch den Elektronenspin induzierte Feld σB0 , das immer in entgegengesetzter Richtung wirkt
(Abschirmung):
Beff = B0 − σB0
Spektroskopische Methoden zur Strukturaufklärung
( 87 )
61
Dieter Baurecht
Je stärker ein Kern abgeschirmt ist, je größer ist σ und desto kleiner wird Beff und damit die
Resonanzfrequenz ν ( 84 ).
Da die Lage der Resonanzfrequenz von B0 abhängt, wird ν eines bestimmten Kern X nicht durch
eine absolute Skala, sondern durch die Lage zur einer Referenzverbindung angegeben. Bei der 1H
und 13C-NMR-Spekroskopie hat sich dafür Tetramethylsilan (TMS, Si(CH3)4) eingebürgert.
∆ν = ν ( X ) − ν (TMS ) =
γ
∆B
2π
( 88 )
Zur Bestimmung der Signallage definiert man als chemische Verschiebung δ des Kern X den
Zahlenwert
δ ( X ) = 106
∆ν
ν ref
( 89 )
mit δ ( ref ) = 0
δ ist eine dimensionslose (ppm), von der Messfrequenz bzw. Magnetfeldstärke unabhängige,
für den betrachteten Kern in seiner Umgebung charakteristische Größe.
Abb. 65: NMR Spektren von Essigsäure (CH3COOH) in CDCl3. a 1H-NMR Spektrum. b
Spektrum (aus 11).
13
C-NMR
6.6.4 Spin-Spin Kopplung
Die in der Kenresonanz gemessenen Signale zeigen häufig eine Feinstruktur. Nach der Anzahl der
Teilbanden spricht man von einem Singulett, Dublett, Triplett, Quadruplett usw., allgemein:
Multiplett. Ursache ist die Wechselwirkung mit Nachbarkernen, die ein magnetisches Moment
besitzen. Diese Spin-Spin-Kopplung tritt zwischen Kernen derselben Sorte (homonuklear) und
zwischen Kernen verschiedener Elemente (heteronuklear) auf und bedeutet, dass die Orientierung
des Spins eines Kerns A das lokale Magnetfeld am koppelnden Kern X beeinflusst und umgekehrt.
Für zwei Kerne A und X, die beide den Kernspin 1/2 haben, existieren entsprechend den vier
möglichen Spin-Einstellungen grundsätzlich vier Energieniveaus. Ohne Spin-Spin Wechselwirkung
(J = 0) ergeben sich für A und X jeweils zwei energiegleiche Absorptionen (Abb. 66, Mitte). Durch
die Kopplung J wird diese Entartung aufgehoben. Definitionsgemäß hat J ein positives Vorzeichen,
62
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
wenn bei gleicher Spin-Ausrichtung der beiden Kerne im äußeren Feld B0 die Energie eines
Niveaus durch die Kopplung wächst. Bei entgegengerichteter Spin-Einstellung nimmt die Energie
dann um denselben Betrag ab. Das umgekehrte Verhalten gilt für J< 0. Beide Fälle führen dazu,
dass die beiden Singulettsignale der A- bzw. X-Resonanz jeweils in Dubletts aufspalten (Abb. 66).
Abb. 66: Die vier möglichen Spin-Einstellungen und Energieniveaus eines Zwei-Spin-Systems
(m = ±1/2) und die zugehörigen Kernresonanz-Übergänge (aus 11).
Die Größe der Kopplung wird durch die Kopplungskonstante J beschrieben.
ω A ( X α ) = ω A + J AX , ω X ( Aα ) = ω X + J AX ,
ω A ( X β ) = ω A − J AX , ω X ( Aβ ) = ω X − J AX .
( 90 )
Für Protonen-Protonen-Kopplung liegen die Konstanten etwa zwischen -20 und +20 Hz. Bei
anderen Kernen können sehr viel höhere Werte auftreten. So beträgt im Acetylen die 13C-13CKopplung 171,5 Hz und die (C-H)-Kopplung 250Hz.
Von besonderer Bedeutung ist, dass die Kopplungskonstanten unabhängig vom äußeren Magnetfeld
B0 sind. Zwei in einem Spektrum auftretende Resonanzlinien können die Singulettsignale zweier
nicht koppelnder Kerne mit unterschiedlicher chemischer Verschiebung sein oder ein Dublett, das
auf einen einzigen Kern zurückgeht, der mit einem anderen, koppelnden Kern ein AX-System
bildet. Eine Unterscheidung ist ganz einfach durch die Aufnahme von zwei Spektren mit
unterschiedlicher Messfrequenz möglich. Bleibt der Linienabstand gleich, so handelt es sich um ein
Kopplungsphänomen; wächst der Abstand (in Hz) mit zunehmender Messfrequenz, dann liegen
zwei Singulettabsorptionen vor.
6.6.5 Messtechnik
6.6.5.1 Klassische Beschreibung des NMR-Experiments
Die Ausrichtung der Kernspins im äußeren Magnetfeld führt zu einer makroskopisch messbaren
Magnetisierung M = χ ⋅ H 0 (χ = Suszeptibilität). Die Größe von M erhält man aus der Verteilung
der Spins auf die beiden Zustände α und ß, welche der Boltzmann Statistik genügt:
∆E
nα
= e kT = e
nβ
γh H 0
kT
≈ 1+
γhH 0
( 91 )
kT
(nα, nß = Zahl der Spins im Zustand α bzw. ß, k = Boltzmann-Konstante, T = absolute Temperatur).
Die Rechnung liefert für Protonen bei einer Messfrequenz von 100 MHz
nα 1000016
=
n β 1000000
d.h. die Kernspins sind wegen der im Vergleich zur thermischen Energie geringen Energiedifferenz
auf die beiden Zustände α und ß nahezu gleich verteilt und nur etwa 0,001 % aller Kernspins der
Probe stehen für einen Absorptionsvorgang zur Verfügung.
Spektroskopische Methoden zur Strukturaufklärung
63
Dieter Baurecht
Im klassischen Bild präzedieren die Kernspins mit der Larmorfrequenz ωL um die Achse des
äußeren Magnetfeldes; ihre Komponenten in Richtung des Feldes addieren sich zur
Längsmagnetisierung Mz auf, während sich die Komponenten in der Ebene senkrecht zur Richtung
des Feldes gerade kompensieren (Abb. 67a).
Induziert man nun mit Hilfe eines äußeren hochfrequenten Magnetfeldes H1 =H1cos(ωt), das in xRichtung linear polarisiert sei, Übergänge zwischen den beiden Spinzuständen, so wird durch
Absorption und stimulierte Emission bei genügend hoher Feldstärke H1x eine Gleichverteilung des
Spins auf die Zustände α und ß erreicht; hierdurch wird Mz = 0. Außerdem erzwingt das Hf-Feld
eine in-Phase-Präzession der Kernspins, so dass man eine Quermagnetisierung M⊥ in der Ebene
senkrecht zum Feld H0 beobachtet (Abb. 67b). Diese oszilliert mit der Lamorfrequenz (ωL der
Kernspins und induziert in einer senkrecht zur Senderspule orientierten Empfängerspule eine
messbare Spannung, die zur Registrierung des Resonanzvorganges verwendet werden kann (Prinzip
der Kerninduktion). Nach Abschalten des Hf-Feldes H1 laufen gleichzeitig zwei als Relaxation
bezeichnete Prozesse ab:
1. Es stellt sich allmählich wieder die Gleichgewichtsmagnetisierung M0 in Richtung des Feldes ein,
wobei die angeregten Spins ihre Energie an die Umgebung (kurz als Gitter bezeichnet) abgeben
(Abb. 67c). Die hierfür charakteristische Zeit heißt longitudinale oder Spin-GitterRelaxationszeit T1.
2. Daneben geht auch die Phasenkohärenz der in Phase präzedierenden Spins wieder verloren (Abb.
67d), z.B. durch Spin-Spin-Austausch, wobei die Spins zweier Kerne, von denen einer im unteren
und einer im oberen Niveau ist, gleichzeitig umklappen. Auch Inhomogenitäten des äußeren
Magnetfeldes, die unterschiedliche Larmorfrequenzen der individuellen Kernspins zur Folge haben,
können zum Verlust der Phasenkohärenz führen. Die charakteristische Zeit für diesen Vorgang
heißt transversale oder Spin-Spin-Relaxationszeit T2, die auch sehr anschaulich als
"Phasengedächtniszeit" bezeichnet wird.
Abb. 67: Schematische Darstellung des Kernresonanzexperiments im klassischen Bild. a Im
Gleichgewichtszustand sind die Kernspins auf die beiden Zustände α und ß nach Boltzmann verteilt. b Im
Fall von Resonanz erhält man (bei genügend starkem Hf-Feld) eine Gleichverteilung auf α und ß und eine
in-Phase-Präzession der Kernspins mit der Larmorfrequenz ωL. c Die longitudinale Relaxation stellt die
Gleichgewichtsverteilung der Kernspins wieder her. d Während der transversalen Relaxation geht die
Phasenkohärenz der Kernspins wieder verloren. In der Praxis laufen die beiden Relaxationsprozesse c und
d gleichzeitig ab.
64
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
6.6.5.2 Continuous Wave
Zur Durchführung eines Kernresonanzexperiments benötigt man ein statisches Magnetfeld H0 zur
Ausrichtung der Kernspins, ein hochfrequentes Wechselfeld H1 =H1cos(ωt) zur Anregung von
Absorption und einen Detektor, der den Resonanzvorgang registriert.
In Abb. 68 ist das Blockschaltbild eines einfachen sog. „continuous wave (cw)“-Spektrometers
dargestellt. Der Magnet, zwischen dessen Polschuhen sich die Probe befindet, liefert das statische
Feld H0. An die Homogenität dieses Magnetfeldes werden sehr hohe Anforderungen gestellt, da
sich bereits Abweichungen in der Größenordnung von 10-8, wegen der daraus resultierenden
unterschiedlichen Larmorfrequenz der einzelnen Kernspins, in der Breite und Form der
Resonanzlinie bemerkbar machen.
Die Senderspule überträgt das im Hf-Sender kontinuierlich erzeugte monochromatische
Hochfrequenzfeld H1 auf die Probe, welche im Resonanzfall Energie aus dem Hf-Feld absorbiert.
Vermittels der dadurch auftretenden Quermagnetisierung wird in der senkrecht zur Senderspule
angeordneten Empfängerspule eine Wechselspannung induziert, verstärkt und mittels eines
Oszillographen oder Schreibers aufgezeichnet.
Zum Aufzeichnen eines Spektrums verändert man entweder kontinuierlich das Magnetfeld H0 bei
festgehaltener Frequenz des Feldes H1 (Field Sweep) oder man variiert diese Frequenz bei
konstantem äußeren Feld (Frequency Sweep).
Abb. 68: Prinzipieller Aufbau eines NMR-Spektrometers (aus 11).
6.6.5.3 Puls-Fourier-Transform-Spektroskopie
Eine wesentliche Erweiterung der Möglichkeiten der NMR-Spektroskopie erbrachte die Einführung
der Puls-Fourier-Transform-Spektroskopie sowie der Einsatz von Magneten mit supraleitenden
Spulen und der dadurch möglichen Anwendung stärkerer statischer Magnetfelder. In einem PulsFourier-Transform-Spektrometer (FT-Spektrometer) erfolgt die Anregung der Probe nicht durch
kontinuierliche Einstrahlung eines monochromatischen Hf-Feldes, sondern mittels eines kurzen
Hochfrequenzpulses, der alle Frequenzen aus dem gesamten Bereich der möglichen chemischen
Verschiebung eines Kerns enthält. Hierdurch wird die Magnetisierung Mz der Probe in Richtung des
Feldes H0 vermindert und eine Quermagnetisierung aufgebaut, die Magnetisierung also insgesamt
um einen Winkel gekippt, der von der Energie des Pulses abhängt. Man spricht von einem 90°-Puls,
wenn Mz = 0 und M⊥ maximal werden. In der Praxis läßt sich dieser Winkel durch die Pulsdauer (~
10-5 s) festlegen.
Spektroskopische Methoden zur Strukturaufklärung
65
Dieter Baurecht
In der Empfängerspule wird wie im CW-Experiment durch Auftreten der Quermagnetisierung eine
Spannung induziert, die nach Abschalten des Hf-Senders entsprechend den individuellen
Relaxationszeiten der einzelne Kerne abklingt. Man nennt diesen Prozess den freien
Induktionsabfall, engl. „free induction decay“, FID. Ein FID enthält Informationen über die
Lamorfrequenzen aller durch den Puls angeregten Kerne. Er ist die Fouriertransformierte des
gewöhnlichen Kernresonanzspektrums, das man daher durch eine Fourier-Transformation aus dem
gespeicherten FID gewinnen kann. Die gesamte zur Aufnahme eines NMR-Spektrums notwendige
Zeit beträgt also nur Sekunden, während zum Abtasten des Spektrums mit einem CW-Spektrometer
meist einige Minuten benötigt werden. Die dadurch in kurzer Zeit erzielbare
Empfindlichkeitssteigerung ist einer der entscheidenden Fortschritte der FT-Spektroskopie. Erst
nach Einführung dieser Technik wurde es möglich, an Kernen mit geringer natürlicher Häufigkeit
oder geringer Empfindlichkeit Kernresonanzmessungen durchzuführen.
6.6.6 Biophysikalische Anwendungen der NMR
6.6.6.1 Beobachtung der Helix-Knäuel-Umwandlung an Proteinen
Am Beispiel der Protonenspektren von Proteinen sollen einige Anwendungen der NMRSpektroskopie an Makromolekülen erläutert werden.
Typischerweise trifft man bei solchen Systemen zunächst auf das Problem der Auflösung und
Zuordnung einzelner Linien. Einerseits erhält man wegen der großen Zahl chemisch ähnlicher
Gruppen, aus denen die Makromoleküle aufgebaut sind, NMR-Spektren mit sehr vielen, z. T.
überlagerten Linien. Andererseits sind diese einzelnen Linien aufgrund der relativ langen
Korrelationszeit globulärer Proteine bereits sehr stark verbreitert, so dass sich aus ihrer
Überlagerung häufig nur breite Banden ergeben. Die wesentlichen Bereiche der
Protonenresonanzen von Aminosäuren liegen zwischen 1 und 4,5 ppm für die aliphatischen
Gruppen (aliphatisch = nicht aromatisch) und zwischen 7 und 9 ppm für die aromatischen Reste
(Histidin, Phenylalanin, Tryptophan und Tyrosin).
Bei dem Zusammenschluss von Aminosäuren zu Peptiden und Proteinen unter Ausbildung von
Peptidbindungen werden im NMR-Spektrum Primärstruktureffekte sichtbar, die vorwiegend die
Cα-Protonen betreffen. Man beobachtet hier eine Tieffeldverschiebung um etwa 0,5 ppm, während
die Signale der restlichen Protonen kaum Veränderungen zeigen. Das Spektrum eines Proteins oder
Peptids, das im statistischen Knäuel vorliegt, entspricht daher in erster Näherung der Summe der
konstituierenden Aminosäuren. Im nativen Zustand (gefaltetem Zustand) treten dagegen durch die
Ausbildung der Sekundär- und Tertiärstruktur zusätzliche Linienverschiebungen auf. Sie sind
bedingt durch intramolekulare Wechselwirkungen oder durch magnetische Anisotropien, die z.B.
von dem Ringstromeffekt aromatischer Aminosäuren hervorgerufen werden können. Aus der
Analyse solcher Verschiebungen lassen sich Aussagen zur Konformation von Proteinen in
Lösung gewinnen.
Abb. 69 zeigt den Einfluss der Hitzedenaturierung auf das Spektrum von Lysozym aus Hühnereieiweiß. Im nativen Zustand, in dem das Protein noch bei 56°C vorliegt, findet man Linien zwischen
-0,5 und 0,8 ppm sowie 10-11 ppm, die außerhalb des üblichen Resonanzbereichs von Aminosäuren
liegen. Bei Erhöhung der Temperatur wird das Protein teilweise denaturiert, was sich am
Verschwinden dieser Linien im Protonenspektrum verfolgen lässt. Außerdem beobachtet man unter
Denaturierung das Auftreten schärferer Linien wegen der Zunahme der Beweglichkeit der
Polypeptidkette.
Sofern solche Konformationsänderungen in einzelnen Teilschritten erfolgen, lassen sich diese oft
mit Hilfe der NMR-Spektroskopie beobachten und analysieren. Die Interpretation solcher
Übergänge hinsichtlich einzelner Domänen eines Proteins setzt jedoch voraus, dass zumindest eine
teilweise Zuordnung der Linien des NMR-Spektrums zu individuellen Aminosäuren möglich ist.
66
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
Abb. 69: 1H-NMR-Spektren einer 10%igen Lysozym-Lösung in H2O, pH 3,3 bei zunehmenden
Temperaturen. Bei 56°C liegt das Molekül in der globulären Konformation (Kugelform) vor, bei
Temperaturzunahme beobachtet man Denaturierung (Übergang einer geordneten Sekundärstruktur in eine
zufällige), bis schließlich bei 73°C das Molekül im statistischen Knäuel vorliegt (aus 1).
6.6.6.2 NMR an Membranen
Auch biologische Membranen und Modellmembransysteme lassen sich mittels der
Kernresonanzspektroskopie untersuchen. Neben der 1H-NMR wird hierbei vielfach die 13C-NMR
angewandt, aber auch die 31P-NMR zur Beobachtung der Phospholipide und die 2H-NMR, sofern
man die Membranlipide geeignet deuteriert hat.
Eine wesentliche Bedingung für den Einsatz hochauflösender NMR-Spektroskopie an Membranen
ist, dass sich diese in der flüssigkristallinen Phase befinden müssen, da die stark eingeschränkte
Beweglichkeit der Lipide in der Gel-Phase deren Resonanzen sehr stark verbreitert. Dies ist am
Beispiel der 13C-NMR-Spektren von Dipalmitoyl-Lecithin-Membranen (Phasenumwandlung bei
41° C) gut zu sehen (Abb. 70). Bei tiefen Temperaturen zeigen nur die relativ freien CholinKopfgruppen eine scharfe Resonanzlinie, während die Resonanzen der Fettsäureketten erst bei
höheren Temperaturen scharf werden.
Eine genauere Charakterisierung der unterschiedlichen Beweglichkeit der verschiedenen
Lipidgruppen erlauben Messungen des Ordnungsparameters bei der Anwendung von 2H-NMR oder
der Relaxationszeiten im Fall der 13C-NMR.
Der für 13C-Kerne dominierende Relaxationsmechanismus ist die intramolekulare Dipol-DipolWechselwirkung mit den direkt gebundenen Protonen und ist abhängig von der je nach Gruppe
unterschiedlichen Beweglichkeit (im wesentlichen Rotation um die C-C Bindungen).
Die T1-Messung am Beispiel von Dipalmitoyl-Lecithin-Vesikeln ergibt kurze Relaxationszeiten für
die C-Atome des Glycerin-Rückgrats, aber zunehmende Werte sowohl entlang der Fettsäurekette
als auch zur Cholin-Gruppe hin. Eine Ausnahme bildet die Carbonylgruppe, für die kein direkt
gebundenes H-Atom zur Dipol-Dipol-Relaxation zur Verfügung steht (Abb. 71).
Aus der Temperaturabhängigkeit der gemessenen T1-Zeiten ergibt sich, dass für das untersuchte
System die Näherung ω 2 ⋅τ c2 << 1 gilt, d.h. die Relaxationszeiten sind direkt proportional zur
molekularen Beweglichkeit. Aus der Zunahme der T1-Zeiten folgt daher eine zum Schwanzende der
Lipide zunehmende Beweglichkeit in Lipid-Doppelschichten.
Spektroskopische Methoden zur Strukturaufklärung
67
Dieter Baurecht
Abb. 70: 13C-NMR-Spektren von Dipalmityol-Lecithin-Vesikeln in D2O bei unterschiedlichen
Temperaturen. Zur Nummerierung der C-Atome siehe Abb. 71. Die Skala der Verschiebung ist um 67,4
ppm gegen TMS verschoben (aus 1).
Abb. 71: 13C-T1-Relaxationszeiten von Dipalmityol-Lecithin-Vesikeln bei 52°C in D2O (aus 1).
6.6.6.3 Ortsaufgelöste NMR-Spektroskopie
Methoden zur Gewinnung ortsaufgelöster NMR-Signale werden als Magnetresonanztomographie
(MR, MRT, auch Kernspintomographie und Magnetic Resonance Imaging, MRI) bezeichnet. Mit
deren Hilfe lassen sich zerstörungsfrei Schnittbilder lebender Organismen herstellen. Die Methode
eignet sich im Bereich der Medizin für diagnostische Zwecke. Ihre Anwendung anstelle der
Röntgendiagnostik vermeidet eine unerwünschte Strahlenbelastung und kann auch über das der
Röntgendiagnostik schlecht zugängliche weiche Gewebe Aussagen ergeben.
Ortsaufgelöste NMR-Spektroskopie wird möglich, wenn man statt eines homogenen ein
inhomogenes äußeres Magnetfeld H0 verwendet, das eine solche Form besitzt, dass jedem
Volumenelement der Probe, eindeutig eine Resonanzfrequenz ν0 zugeordnet werden kann (Abb.
72). In der Praxis arbeitet man mit linearen Feldgradienten. Bei der für Ganzkörperaufnahmen am
läufigsten angewandten Technik wird zunächst eine empfindliche Fläche im Objekt erzeugt, z. B.
durch Anlegen eines modulierten Magnetfeldgradienten in z-Richtung. Durch Überlagerung eines
68
Spektroskopische Methoden zur Strukturaufklärung
Biophysik I
zeitlich konstanten Gradienten in der xy-Ebene erhält man Ebenen gleicher Feldstärke, die
senkrecht zur empfindlichen Fläche orientiert sind. Zu einem Signal gleicher Resonanzfrequenz
tragen alle Spins bei, die entlang der jeweiligen Schnittlinien dieser Ebenen mit der empfindlichen
Fläche angeordnet sind. Die Amplituden der erhaltenen Signale bei 1H-NMR an biologischen
Proben - hauptsächlich durch die Konzentration von Wasser gegeben - entsprechen der Projektion
der Spindichte entlang dieser Linien. Diese werden zur Bildrekonstruktion in einer
zweidimensionalen Bildmatrix abgespeichert, und zwar jeweils entlang einer Linie, deren
Orientierung der signalgebenden Linie des Objekts entspricht. Dieser Vorgang wird mehrfach
jeweils nach Drehung des Feldgradienten wiederholt. In der Bildmatrix entsteht dabei durch
Addition der projizierten Intensitäten ein zweidimensionales Schnittbild des Objekts.
Abb. 72: Örtliche Auflösung durch inhomogenes Magnetfeld. Befindet sich ein Objekt in einem nicht
homogenen Magnetfeld, das sich linear mit einer Raumrichtung ändert, so befinden sich die
verschiedenen Teile der Messebene in unterschiedlich starken Magnetfeldern. Somit erfolgt eine
Verknüpfung zwischen Ort des Atomkerns und der dort herrschenden Magnetfeldstärke. Dies führt zu
einer Verbreiterung der Signale. Die Signalintensität bei einer bestimmten Frequenz ν0 im Spektrum
ergibt sich aus der Summe aller Wasserstoffatome der Messebene, deren Resonanzfrequenz mit ν0 gerade
erfüllt wird. Das Spektrum entspricht einer Projektion der Protonendichte der Messebene auf die
Frequenzachse des Spektrums. Auf diesem Prinzip beruht die NMR-Tomographie. (Quelle:
http://www.uni-bayreuth.de/departments/didaktikchemie/umat/nmr/nmr_tomographie.htm)
Da die Intensität der jeweils erhaltenen Signale von den Relaxationszeiten der bildgebenden Kerne
abhängig ist, eignet sich die NMR-Tomografie auch zur Tumorerkennung, denn es konnte gezeigt
werden, dass die Relaxationszeiten von Protonen im Inneren von Karzinomen gegenüber denen im
gesunden Gewebe deutlich verändert sind.
Internet: http://www.cis.rit.edu/htbooks/mri/
Spektroskopische Methoden zur Strukturaufklärung
69
Dieter Baurecht
7 Übungsbeispiele
7.1 pH Wert
Der pKS-Wert der Essigsäure ist 4,8. Man stellt eine Lösung von 0,1 M Essigsäure (CH3-COOH )
und 0,2 M Acetat (CH3-COO-) her. Welcher pH-Wert ergibt sich?
CH3-COOH
⇔
H+ + CH3-COO-
A) Nach der Henderson-Haselbalch-Gleichung ( 17 ) ist der pH:
[Base]
pH = pK S + log
[Säure]
Dabei ist zu beachten, dass [Base] und [Säure] die Konzentrationen im Gleichgewicht sind. Da die
Essigsäure eine schwache Säure ist und daher nicht stark dissoziiert und das Acetat gegenüber dem
OH- eine schwache Base ist und daher nicht protoniert wird, kann man die
Gleichgewichtskonzentration näherungsweise gleich der Anfangskonzentration setzen, und man
erhält:
0,2
pH = 4,8 + log
= 5,1
0,1
B) Exakte Lösung unter Zuhilfenahme der Reaktionslaufzahl ξ:
Hier wollen wir die Änderung der Säure- und Basenkonzentrationen berücksichtigen, die sich nach
Lösung in H2O aufgrund der Dissoziation und der Protonierung ergeben. Dazu wird die
Reaktionslaufzahl ξ eingeführt, welche die umgesetzte Menge an Molekülen (mol/L) während der
Reaktion beschreibt. Dabei wird die Zunahme an Produkten positiv gewertet. Die
Gleichgewichtskonzentrationen der wesentlichen, an der Reaktion
CH3-COOH
⇔
H+ + CH3-COO-
=
=
=
[H+]0 + ξ
[CH3-COO-]0 + ξ
[CH3-COOH]0 - ξ
beteiligten Moleküle werden damit zu:
[H+]eq
[CH3-COO-]eq
[CH3-COOH]eq
KS =
[H + ]eq [CH 3 − COO − ]eq
[CH 3 − COOH]eq
=
([H + ]0 + ξ)([CH 3 − COO − ]0 + ξ)
[CH 3 − COOH]0 − ξ
Nach Umformung erhält man:
ξ 2 + ([H + ]0 + [CH 3 − COO − ]0 + K S )ξ + [CH 3 − COO − ]0 [H + ]0 - K S [CH 3 − COOH]0 = 0
Da das Lösungsmittel reines H2O ist, ist der pH0 = 7 und damit [H+]0 = 10-7. Damit sind alle Größen
bis auf ξ gegeben und man erhält nach Lösen der quadratischen Gleichung:
70
Übungsbeispiele
Biophysik I
ξ1 = 7.825 10-6 M, ξ2 = -0.20002 M
Da mit ξ2, die Konzentrationen der beteiligten Stoffe [H+]eq negativ wären, ist ξ1 die einzige
physikalisch sinnvolle Lösung und man erhält:
[H+]eq = [H+]0 + ξ = 1 10-7 M + 7.825 10-6 M = 7.925 10-6 M, und damit
pHeq = -log [H+]eq = 5.1
was dem Wert entspricht, der mit der Henderson-Haselbalch-Gleichung ebenfalls ermittelt wurde.
Der Grund ist einfach zu erkennen: wenn wir uns den Betrag des Stoffumsatzes ξ = 7.825 10-6 M
ansehen und ihn mit den Anfangskonzentrationen der Base 0.2 M und Säure 0.1M vergleichen,
sehen wir, dass die in der Henderson-Haselbalch-Gleichung zu verwendenden
Gleichgewichtskonzentrationen
der
Säure
und
Base
praktisch
gleich
unseren
Anfangskonzentrationen sind. Dies wäre bei einer starken Säure natürlich nicht der Fall.
7.2 Isoelektrischer Punkt und Ladungsverteilungen
A) Isoelektrischer Punkt von Aminosäuren mit zwei ionisierbaren Gruppen:
Bei einem bestimmten pH-Wert, dem so genannten isoelektrischen Punkt (IEP), sind bei
Aminosäuren exakt gleich viele Säuregruppen negativ geladen, wie Aminogruppen positiv geladen
sind. Am isoelektrischen Punkt wandern Aminosäuren im elektrischen Feld nicht mehr, da die
Summenladung neutral ist. Liegt der pH darunter, nimmt die Dissoziation der Säuregruppe ab, und
die Aminosäure trägt eine positive Summenladung. Liegt der pH darüber, nimmt die Dissoziation
der Säure zu und die Aminogruppe gibt das Wasserstoffion ab, das Molekül trägt eine negative
Summenladung. Diesen Effekt nutzt man z.B. bei der Elektrophorese.
Gegeben sind die pK-Werte der ionisierbaren Gruppe von Glycin, einer Aminosäure mit nicht
ionisierbarer Seitenkette: pKCarboxyl = 2.35, pKAmino = 9.78. Bei welchem pH Wert liegt der
isoelektrische Punkt?
Gesucht: [H+] (-log[H+]) unter der Bedingung, dass die Konzentration positiv geladener
Aminosäuren gleich der Konzentration negativ geladener Aminosäuren ist (isoelektrisch): [COOHNH3+] = [COO--NH2]
Allgemeine Lösung: Aufstellen der Reaktionsgleichungen für die beiden Teilreaktionen
(Deprotonierung der Carboxyl- und der Aminogruppe).
COOH-NH3+
COO--NH3+
I: positiv geladen
II: Zwitterion
⇔
⇔
COO--NH3+ + H+
COO--NH2 + H+
Zwitterion
negativ geladen
Im Gleichgewicht gilt:
+
[H + ][COO − - NH 3 ]
[H + ][COO − - NH 2 ]
KI =
, K II =
+
+
[COOH - NH 3 ]
[COO- - NH 3 ]
+
K I K II =
[H + ][COO − - NH 3 ] [H + ][COO − - NH 2 ] [H + ]2 [COO − - NH 2 ]
=
= [H + ]2
+
+
+
[COOH - NH 3 ]
[COO - NH 3 ]
[COOH - NH 3 ]
Übungsbeispiele
71
Dieter Baurecht
- log(K I ) - log(K II ) = 2(− log[H + ])
- log(K I ) - log(K II )
− log[H + ] =
2
pK I + pK II
pH =
2
Das heißt der pH des isoelektrischen Punkts, pI liegt bei zwei ionisierbaren Gruppen
unterschiedlicher Polarität beim arithmetischen Mittel der beiden pK-Werte.
Für Glycin gilt somit: pI = (2.35 + 9.78)/2 = 6.07
B) Isoelektrischer Punkt von Aminosäuren mit zusätzlicher ionisierbarer Gruppe auf der
Seitenkette:
Aminosäuren, die ionisierbare Gruppen an den Seitenketten besitzen, können eingeteilt werden in
solche, deren Seitenketten zu einer positiven Ladung, und solche, deren Seitenketten zu einer
negativen Ladung beitragen (Tab. 4). Sind die Seitenketten an der positiven Ladung beteiligt
(basische Aminosäuren), müssen die Ladungsbeiträge der α-Aminogruppe und der Seitenkette (R)
zusammen die Ladungsbeiträge der Carboxylgruppe ergeben. Dies ist dann der Fall, wenn der pH
das arithmetische Mittel von pKAmino und pKR ist. Sind die Seitenketten an der negativen Ladung
beteiligt (saure Aminosäuren), müssen die Ladungsbeiträge der α-Carboxylgruppe und der
Seitenkette (R) zusammen die Ladungsbeiträge der Aminogruppe ergeben. Dies ist dann der Fall,
wenn der pH das arithmetische Mittel von pKCarboxyl und pKR ist.
Mit den pK-Werten aus Tab. 5 bekommt man z.B.
pIHistidin = 7.69
pIAsparaginsäure = 2.95
Berechnen Sie die prozentuelle Ladung jeder ionisierbaren Gruppe der Asparaginsäure bei dem pH
der mit dem isoelektrischen Punkt pI identisch ist.
Ionisierbare Gruppen (pK) aus Tab. 5:
α-Carboxylgruppe (pK = 2.0), α-Aminogruppe (pK=10.0), β-Carboxylgruppe (pKR = 3.9).
pI = (2.0+3.9)/2 = 2.95
α-Carboxylgruppe (pK = 2.0):
Henderson-Haselbalch-Gleichung: pH = pK S + log
log
[Base]
[Säure]
[Cα OO- ]
[Cα OO- ]
= pH - pK S = 2.95 − 2.0 = 0.95 ⇒
= 8.9
[Cα OOH]
[Cα OOH]
da [CαOO-] + [CαOOH] = [Asparaginsäure] sein muss folgt:
72
Übungsbeispiele
Biophysik I
[Cα OO- ]
= 8.9 ⇒ [Cα OO- ] = 0.9 ⋅ [Asparaginsäure]
[Asparaginsäure] - [Cα OO- ]
das heißt, bei 90% der Asparaginsäuremolekülen ist die α-Carboxylgruppe bei pH = pI dissoziiert.
Die selbe Rechnung ergibt für die β-Carboxylgruppe (pKR = 3.9)
log
[C β OO - ]
[C β OOH]
= pH - pK R = 2.95 − 3.9 = −0.95 ⇒
[C β OO - ]
[Asparaginsäure] - [C β OO - ]
[C β OO - ]
[C β OOH]
= 0.11
= 0.11 ⇒ [C β OO - ] = 0.1 ⋅ [Asparaginsäure]
das heißt, bei 10% der Asparaginsäuremolekülen ist die α-Carboxylgruppe bei pH = pI dissoziiert.
In Summe sind also genauso viele Gruppen negativ geladen, wie Asparaginsäuremoleküle
vorhanden sind. Da die α-Aminogruppe aller Moleküle bei so kleinem pH 100%ig protoniert
(positiv geladen) ist, ist die Summe der Ladungen gleich Null, was ja den isoelektrischen Punkt
charakterisiert.
Übungsbeispiele
73
Dieter Baurecht
Literatur
1 Hoppe, Lohmann, Markl, Ziegler. Biophysik, Springer-Verlag 1982.
Nienhaus, Skriptum Biophysik, Universität Ulm.
3
Riedel, Anorganische Chemie, deGruyter 1994.
4
Berg JM, Tymoczko JL und Stryer L, Biochemie, 5. Auflage, Spektrum, 2003.
5
Alberts B, Bray D, Lewis J, Raff M, Roberts K und Watson JD, Molekularbiologie der Zelle,
VCH 1995.
6
Stryer L, Biochemie, Spektrum, 1990.
7
Fringeli U.P., Reiter G, und Prossinagg R, 2005/2006, Skriptum Biophysikalische Chemie I, Inst.
f. Biophysikalische Chemie, Universität Wien
8
Zubay G.L., Biochemie, McGraw-Hill 1999.
9
Banwell CN, Fundamentals of Molecular Spectroscopy, 2nd Ed., Mc Graw Hill,1972.
10
Beyer H, Walter W, Lehrbuch der Organischen Chemie, S.Hirzel Verlag, Stuttgart, Leipzig,
2004.
11
Hesse M, Meier H und Zeeh B., Spektroskopische Methoden in der organischen Chemie, 5.
Auflage, 1995.
12
Krimm S und Bandekar J, Vibrational Spectroscopy and Conformation of Peptides,
Polypepdides, and Proteins. Advances in Protein Chemistry 38, 1986.
13
Perkins 1986
14
Fringeli UP 1992, in Mirabella, FM (Ed.), Internal Reflection Spectroscopy, Theory and
Applications, Marcel Dekker 1992, Chpt. 10, 255-324.
2
74
Literatur