pdf - 729 KB
Werbung

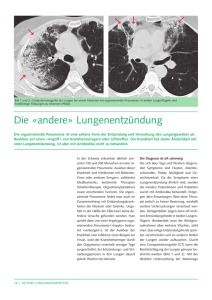
Pneumonie V. Petkov und B. Robibaro AKH-Wien, Universitätsklinik für Innere Medizin IV, Klinische Abteilung für Pulmologie, Leiter: o. Univ.-Prof. Dr. Lutz-Henning Block Definition Die Pneumonie ist eine mikrobiell verursachte entzündliche Erkrankung des Lungenparenchyms. Verschiedene Bakterienspezies, Mykoplasmen, Chlamydien, Rickettsien, Viren, Pilze und Parasiten können Pneumonien verursachen. Somit ist die Pneumonie nicht eine einzelne Krankheit, sondern steht für eine Gruppe von speziellen Infektionen, die sich alle in Epidemiologie, Pathogenese, klinischem Bild und klinischem Verlauf unterscheiden. Epidemiologische Daten - Ambulant erworbene Pneumonie Betrifft in USA ca. 4 Millionen Erwachsene/Jahr (12:1000/a) 600.000 Hospitalisierte/Jahr (USA) Kosten für stationäre Behandlung ca. 20fach teurer im Vergleich zu ambulanter Therapie Kosten ca. 4 Milliarden $ pro Jahr Mortalitätsrate ca. 25% Ambulant erworbene Pneumonie 6.-häufigste Todesursache bzgl. Infektionskrankheiten Respiratorische Infektionen weltweit häufigste Todesursache Klassifikation 1. Pathologisch-anatomisch Lobärpneumonie Bronchopneumonie Interstitielle Pneumonie 2. Klinisch Primäre Pneumonie: beim Gesunden Sekundäre Pneumonie: beim Vorerkrankten (kardiopulmonal, Tumor) 3. Klassifikation nach Ausgangssituation Ambulante Pneumonie: im häuslichen Milieu erworben („community acquired pneumonia“) Nosokomiale Pneumonie: im Krankenhaus erworben („hospital acquired pneumonia“) Pneumonie beim Immunsupprimierten (z.B. HIV, transplantierter Patient) Aspirations-Pneumonie (z.B. nach Bewusstlosigkeit, neurologischen Erkrankungen) 149 4. Klassifikation nach Erreger Pneumonie – Einteilung III Beginn Fieber Tachypnoe (>40/min) Tachykardie (>120/min) Auswurf Thoraxschmerz/Erguss Leukozytose (>15 G/L) C-reaktives Protein Radiologische Infiltrate Typische (bakteriell) akut hoch(>38,5°), Schüttelfrost häufig, schwer krank häufig purulent häufig häufig deutlich erhöht (>10 mg/dl) lobär/segmental Atypische (Viren, Mykoplasmen) über Tage mäßig, langsam steigend selten selten wenig, mukopurulent selten selten wenig erhöht (<10 mg/dl) alveolär/interstitiell/homogen Pneumonie – Symptomatik ♦ ♦ ♦ ♦ ♦ ♦ Husten Auswurf Fieber/Schüttelfrost Dyspnoe, Tachypnoe (Nasenflügelatmen) Zyanose Pleuritische Schmerzen Diagnose Lobärpneumonie Klinik: Inspektion: Perkussion: Auskultation: Thoraxröntgen: Pneumonisches Infiltrat Labor: Entzündungszeichen Leukozytose, Linksverschiebung, ↑ BSG, ↑ CRP, ↑ Fibrinogen Atypische Pneumonie Tachypnoe, Fieber, Zyanose gedämpfter Klopfschall Bronchialatmen (RG‘s) Klinik: Inspektion: Perkussion: Auskultation: Fieber (Thoraxschmerz) Normaler Klopfschall Vereinzelte RG‘s (Bronchitis) Thoraxröntgen: Deutliches, unscharf begrenztes Infiltrat Labor: Entzündungszeichen Leukozytose, oft Lymphopenie, ↑ BSG, CRP gering – mäßig erhöht, Fibrinogen gering – mäßig erhöht 150 Pneumonie – Diagnostik I Thoraxröntgen arterielle Blutgasanalyse Blutbild, Differentialblutbild, Chemie (E-lyte, Niere, Leber), Gerinnung, CRP, BSG Blutkultur Sputum: Gram-Färbung + Kultur ± Ziehl-Neelsen-Färbung + Kultur Bei V.a. atypische Pneumonie: Serologie: Mykoplasmen, Chlamydien, Legionellen, Viren Pneumonie – Diagnostik II HIV-Serologie bei Patienten zwischen 15-54 a Harn: Pneumokokken- und Legionellen-Ag Pleuraerguss (Punktion): LDH, Protein, spez. Gew., pH, Glukose, Gram- + Ziehl-Neelsen-Färbung, Kultur (aerob/anaerob, Mykobakterien) Bronchoskopie/BAL/transbronchiale Biopsie: selten nötig, bei: Vd.a. Pneumocystis c., (Sputum-negative) Tbc, Infiltrat ohne Rückbildungstendenz Pneumonie Richtlinien für die Sputumbakteriologie Mund vor Expektoration spülen Expektorat aus den tiefen Atemwegen (kein Speichel!) ev. induziertes Sputum mittels Inhalation hypertoner NaCl-Lösung bei Verdacht auf Pneumonie durch Mykobakterien oder Pilze, Gewinnung von morgendlichem Sputum an 3 Tagen (Sputum I-III) rasche Verarbeitung (2-5 Std.) Pneumonie - Sputumbakteriologie, Gram-Färbung Qualitative Erfordernisse für untersuchtes Sputum bei 100-facher Vergrößerung: < 10 Epithelzellen/Gesichtsfeld ≥ 25 Leukozyten/Gesichtsfeld Pneumonie – Erregerspektrum in Abhängigkeit von Umgebung bzw. Wirt I. Ambulant erworbene II. Im Krankenhaus erworben (HAP) III. Unter Pneumonie (CAP) Immunsuppression S. pneumoniae M. pneumoniae H. influenzae Legionella S. aureus S. pneumoniae S. aureus H. influenzae E. coli Klebsiellen P. aeruginosa Enterobacter sp. Proteus mirabilis Legionella Anaerobier wie I. und II., zusätzlich Pneumocystis carinii CMV VZV Pilze Atyp. Mykobakterien M. tuberculosis 151 Pneumonie – Erregerspektrum I in Abhängigkeit von Exposition/Risikofaktor Grunderkrankung Erregerspektrum COPD/Raucher S. pneumoniae, H. influenzae, M. catarrhalis, Gram (-) Bakt. Strukturelle Lungenerkrankungen P. aeruginosa, P. cepacia, S. aureus (BE, CF) Alkoholismus S. pneumoniae, Klebsiella p., Anaerobier, M. tuberculosis Influenza (-Epidemie) S. pneumoniae, S. aureus, H. Influenzae, Influenza-V. Aids Pneumocystis c., S. Pneumoniae, H. Influenzae, Cryptococcus, M. Tuberculosis, Rhodococcus equi Aspiration Aerob-anaerobe Mischinfektion Diabetes mellitus S. pneumoniae, S. aureus Organtransplantierte S. pneumoniae, H. Influenzae, Legionella, Pneumocystis c., CMV, Toxoplasma g., Strongyloides stercoralis Pneumonie – Erregerspektrum II in Abhängigkeit von Exposition und Risikofaktor Exposition/Risikofaktor Erregerspektrum Soziales Umfeld Arbeitslosenheime, S. pneumoniae, M. tuberculosis Flüchtlingslager Armeeunterkünfte S. pneumoniae, Chlamydia p., Mycoplasma p. i.v.-Drogen S. aureus, Anaerobier, M. Tuberculosis, Pneumocystis c. Tierkontakt Viehzucht Coxiella b. Kleine Nagetiere Hantavirus Vögel Chlamydia p. Reiseanamnese Osteuropa M. tuberculosis Südostasien Pseudomonas p., Paragonimus w. Mikrobielle Pathogene der ambulant erworbenen Pneumonie Erreger bzw. Ursache Prävalenz (%) Nordamerika Bakterien Streptococcus pneumoniae 20-60 Haemophilus influenzae 3-10 Staphylococcus aureus 3-5 Gram-negative Bakterien 3-10 Mischinfektionen 3-5 Atypische Bakterien Legionella Mycoplasma pneumoniae Chlamydia pneumoniae Viren Aspiration 2-8 1-6 4-6 2-15 6-10 British Thoracic Society 60-75 4-5 1-5 selten 2-5 5-18 8-16 - 152 Vorerkrankungen (Faktoren, die das Auftreten einer Pneumonie begünstigen) Chronisch obstruktive Atemwegserkrankungen/Emphysem Alkoholismus aktive oder passive Immunsuppression Tumorleiden (bes. poststenotische Pneumonie bei N. bronchii) Diabetes mellitus Herz-, Niereninsuffizienz Mangelernährung, Kachexie Rauchen Nosokomiale Pneumonie Risikofaktoren Endogene: Alter, Immundefizienz COPD Bewusstseinslage Exogene: Endotrachealtubus Steroid-/Immunsuppressive Therapie Chirurgischer Eingriff Nasogastrische Sonden Vorausgegangene antibiotische Therapie H2-Antagonisten/Antazida-Therapie Definition 1. Beginn mehr als 72 Std. nach Hospitalisierung 2. ⇐ Radiologisches Lungeninfiltrat/ perk. Dämpfung/ ausk. RG‘s plus zumindest 1 der folgenden Kriterien: ⇐ Eitriges Sputum ⇐ Erregernachweis (Blut, Trachealaspirat, BAL, Biopsie) ⇐ Diagnostischer Antikörpertiter ⇐ Histopathologischer Beweis einer Pneumonie 153 Pathogenese Einteilung nach Krankheitsbeginn „Early onset“, früh einsetzend: Krankheitsbeginn zwischen Tag 1 und 5 ⇐ Überwiegen Gram-positiver Erreger „Late onset“, spät einsetzend: Krankheitsbeginn nach Tag 5 ⇐ Überwiegen Gram-negativer Erreger, Problemkeime Einteilung nach Schweregrad Definition der schweren nosokomialen Pneumonie - Intensiv-pflichtig - Respiratorische Insuffizienz (mechanische Beatmung oder Notwendigkeit für >35% O2 für eine arterielle Sättigung > 90%) - Rapide radiologische Verschlechterung, multilobäre Pneumonie oder Kavitation des Lungeninfiltrates Hinweis für schwere Sepsis: - Hypotension (RRsyst < 90 mmHg, RRdiast >60 mmHg) - Vasopressor-Therapie für > 4 h - Harnmenge < 20 ml/h oder < 80 ml in 4 h - Akute, Dialyse-pflichtige Niereninsuffizienz 154 Mikrobielle Pathogene der nosokomialen Pneumonie Erreger Bakterien Gram-negative Bakterien Pseudomonas aeruginosa Enterobakterien Staphylococcus aureus Anaerobier Haemophilus influenzae Streptococcus pneumoniae Legionella Viren CMV Influenza RSV Pilze Aspergillus Prävalenz (%) 80-90 50-70 15-30 10-30 10-20 10-20 4 10-20 <1 Mikrobielle Pathogene der ambulant erworbenen Pneumonie Erreger bzw. Ursache Bakterien Streptococcus pneumoniae Haemophilus influenzae Staphylococcus aureus Gram-negative Bakterien Mischinfektionen Atypische Bakterien Legionella Mycoplasma pneumoniae Chlamydia pneumoniae Viren Aspiration Nordamerika Prävalenz (%) British Thoracic Society 20-60 3-10 3-5 60-75 4-5 1-5 3-10 3-5 selten - 2-8 1-6 4-6 2-15 6-10 2-5 5-18 8-16 - Therapie Pneumonie – Therapie/Allgemeinmaßnahmen Bettruhe, körperliche Schonung Schonkost, reichlich Flüssigkeit, bes. bei hohem Fieber Thromboseprophylaxe (LMWH s.c.) O2-Therapie nach Blutgasanalyse symptomatische Therapie (Antipyretika) bei Fieber > 39° C symptomatische Therapie (NSAR) bei pleuritischen Schmerzen Physiotherapie (Atemgymnastik, rekonditionierende Therapie) 155 Empirische Therapie Krankenhaus Normalstation Antibiotische Therapie • 3.-Generations-Cephalosporin + Makrolid oder Doyxcyclin • Pneumokokken-wirksames Fluorochinolon • β-Laktam/BLI + Makrolid oder Doyxcyclin Intensivstation (kein Risiko für Pseudomonas aeruginosa-Infektion) • 3.-Generations-Cephalosporin + Pneumokokken-wirksames Fluorochinolon oder Makrolid • β-Laktam/BLI + Pneumokokken-wirksames Fluorochinolon oder Makrolid • Pseudomonas-wirksames β-Laktam + Aminoglykosid + Pneumokokken-wirksames Fluorochinolon oder Makrolid • Pseudomonas-wirksames β-Laktam + Ciprofloxacin Risiko für Pseudomonas aeruginosa-Infektion British Thoracic Society-Richtlinien Erregerspektrum Typische Pathogene: S. pneumoniae, H. influenzae Atypische Pathogene: Mycoplasma p., Legionella spp., Chlamydia p. Wie oben + S. aureus, resistenter S. pneumoniae, Gram-negative Stäbchen Wie oben + P. aeruginosa, Gram-negative Stäbchen zur ambulanten oder stationären Behandlung anhand von Prognosefaktoren 156 Pneumonie – Algorithmus zur Risikostratifizierung PSI (Pneumonia Severity Index) nach Fine Eigenschaften Demograph. Faktoren Altersheim: Begleiterkrankung: Status Labor, Röntgen Lebensalter: Männer Frauen Neoplasie Lebererkrankung Herzinsuffizienz Cerebrovaskuläre Erkrankung Nierenerkrankung Mental alteriert Atemfrequenz ≥ 30/min RRsyst < 90 mmHg Temperatur < 35 oder ≥ 40° C Puls ≥ 125/min arterieller pH < 7,35 BUN > 30 mg/dl (11 mmol/L) Natrium < 130 mmol/L Glukose ≥ 250 mg/dl (14 mmol/L) Hämatokrit < 30% PaO2 < 60 mmHg Pleuraerguss Punkte Alter (Jahre) Alter (Jahre) minus 10 + 10 + 30 + 20 + 10 + 10 + 10 + 20 + 20 + 20 + 15 + 10 + 30 + 20 + 20 + 10 + 10 + 10 + 10 Risikoklasse II (≤ 70), III (71-90), IV (91-130), V (>130)., PORT Study, Fine et al., NEJM 1997; 336:243-50 157 Risikostratifizierung /PORT-Studie Risiko Niedrig Niedrig Niedrig Mittel Hoch Risikoklasse (PSI) I II III IV V Punkte s.Algorithmus ≤ 70 71-90 91-130 > 130 Mortalität (%) 0,1 0,6 0,9 9,3 27 Therapie Ambulant Ambulant Kurz stationär Stationär Stationär Pneumonie – Mortalität nach Patientengruppe Patientengruppe Amb. + hosp. Pat. Hospital. Pat. Höheres Alter Bakteriämie Altersheim Intensivstation Gesamt Studienkohorte 6 84 9 12 6 13 130 Patientenzahl 2097 25629 834 1544 556 788 31448 Therapievorschläge (mod.) der Paul-Ehrlich-Gesellschaft (für die nosokomiale Pneumonie/ 1999) A: Cefotiam, Cefuroxim, Cefotaxim, Cefodizim, Piperacillin/-Tazobactam, Chinolon 4 (Moxifloxacin), Chinolon 2/3 (Ciprofloxacin, Ofloxacin, Levofloxacin) + Clindamycin B: Piperacillin/-Tazobactam, Imipenem, Meropenem, Chinolon 4, Chinolon 2/3 + Clindamycin, ± Fosfomycin C: Cefepim, Cefpirom, Piperacillin/-Tazobactam, Imipenem, Meropenem, ± Chinolon oder Aminoglykosid, ± Fosfomycin, Linezolid, Quinopristin/Dalfopristin 158 Mortalität (%) 5,1 13,6 17,6 19,6 30,8 36,5 13,7