12 Naturstoffe 12.1 Aminosäuren, proteinogene Aminosäuren
Werbung

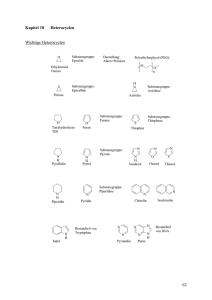
12 12.1 Naturstoffe Aminosäuren, proteinogene Aminosäuren, Seitengruppen, Eigenschaften, Chiralität In der Natur, insbesondere in Peptiden und Proteinen, finden sich fast ausschließlich α-Aminosäuren. Es gibt jedoch auch entsprechende β−, γ−, δ−, etc. Aminosäuren. β δ COOH H2N NH2 COOH COOH α γ β-Alanin (achiral) α-Alanin (chiral) Chemische Eigenschaften von Aminosäuren: Aminosäuren sind meist kristalline Feststoffe und liegen als Zwitterionen vor. Da Aminosäuren eine saure Carboxylatgruppe und eine basische Aminfunktion tragen, können sie pH-abhängig in drei Formen vorliegen. Den pH-Wert, bei dem eine Aminosäure in der (nach außen ungeladenen) zwitterionischen Form vorliegt wird Isoelektrischer Punkt (IP) genannt. Der IP ist für jede Aminosäure charakeristisch. R COOH NH3 -H+ R COO NH3 +H+ "neutral" pH = IP im Sauren -H+ +H+ R COO NH2 im Basischen pKS-Werte und IPs einiger Aminosäuren: die α−Carboxylgruppe von Aminosäuren ist ungewöhnlich sauer. Weitere Carboxalgruppen sind weniger sauer je weiter entfernt sie von Cα sind. allgemein: a-Carboxylgruppe: a-Aminofunktion: pKS = 1,7 – 2,6 (saurer als Ameisensäure!) pKS = 8,9 – 10,6 (als Ammoniumion) andere Grp.: β-Carboxylgruppe (Asp): γ-Carboxylgruppe (Glu): Thiolgruppe –SH (Cys): Hydroxylgrp. –OH (Tyr): ε-Ammonium (Lys): Guanidinogruppe (Arg): Imidazolgruppe (His): pKS = 3,86 (ungefähr wie Ameisensäure) pKS = 4,24 (ungefähr wie Essigsäure) pKS = 8,33 pKS = 10,07 pKS = 8,33 pKS = 12,48 pKS = 6,01 (als Imidazolium) 96 Einteilung der Aminosäuren: Da fast alle Aminosäuren chiral sind (Ausnahme: Glycin) werden AS der L- bzw. DReihe zugeordnet. In der Natur kommen fast ausschließlich nur die L-Formen vor. Von allen möglichen Aminosäuren sind 20 besonders häufig. Sie werden als proteinogene (Protein-bildende) Aminosäuren bezeichnet.Aminosäuren können in „essentielle AS“ und „nicht-essentielle AS“ unterteilt werden. Essentielle AS sind solche, die der menschliche Organismus nicht produzieren kann und die deshalb mit der Nahrung aufgenommen werden müssen. Essentielle Aminosäuren: L-Valin, L-Leucin, L-Isoleucin, L-Phenylalanin, LThreonin, L-Methionin, L-Tryptophan, L-Lysin AS warden “besser” nach ihren chemischen Eigenschaften unterteilt: a) AS mit unpolarem Rest: H H2N COOH L-Glycin (Gly) H CH3 H2N COOH H H2N L-Alanin (Ala) COOH L-Valin (Val) H H H2N H COOH L-Isoleucin (Ile) H2N H2N COOH L-Leucin (Leu) COOH HN COOH L-Prolin (Pro) L-Phenylalanin (Phe) b) AS mit polarem, nicht ionisierbarem Rest: OH OH H H H2N COOH L-Serin (Ser) H2N SH S H COOH L-Threonin (Thr) CH3 H H2N COOH L-Cystein (Cys) H2N COOH L-Methionin (Met) OH O O NH H H2N H H COOH L-Tryptophan (Trp) H2N COOH L-Tyrosin (Tyr) H2N NH2 NH2 H COOH L-Asparagin (Asn) H2N COOH L-Glutamin (Gln) 97 c) polare saure AS mit ionisierbarem Rest: O O OH OH H H H2N COOH H2N L-Asparaginsäure (Asp) COOH L-Glutaminsäure (Glu) d) polare basische AS mit ionisierbarem Rest: H2N NH2 NH NH NH N H H2N H COOH H2N L-Lysin (Lys) H COOH H2N L-Arginin (Arg) COOH L-Histidin (His) 20 der proteinogenen Aminosäuren werden durch Codons des genetischen Materials kodiert. Sie werden daher als kanonische Aminosäuren oder auch als Standardaminosäuren bezeichnet. In Aminosäuresequenzen werden die Aminosäuren meist im Einbuchstabencode oder im Dreibuchstabencode dargestellt. Die 20 kanonischen Aminosäuren Aminosäure Dreibuchstabencode Einbuchstabencode Alanin Ala A Arginin Arg R Asparagin Asn N Asparaginsäure Asp D Cystein Cys C Glutamin Gln Q Glutaminsäure Glu E Glycin Gly G Histidin His H Isoleucin Ile I Leucin Leu L Lysin Lys K Methionin Met M Phenylalanin Phe F Prolin Pro P Serin Ser S Threonin Thr T Tryptophan Trp W Tyrosin Tyr Y Valin Val V Bemerkung nicht-essentiell nicht-essentiell nicht-essentiell nicht-essentiell nicht-essentiell nicht-essentiell nicht-essentiell nicht-essentiell semi-essentiell Essentiell Essentiell Essentiell Essentiell Essentiell nicht-essentiell nicht-essentiell Essentiell Essentiell nicht-essentiell essentiell 98 12.2 Peptide, Proteine, Eigenschaften, Basizität, Konformation, Bildung und Hydrolyse Peptidbindung: Peptide sind Amide aus zwei Aminosäuren: Struktur der Amidbindung: • • • • Die C-N Bindung in Amiden besitzt Doppelbindungscharakter (ca. 40%) Rotation um die C-N Bindung ist gehindert (2 Konformere möglich) Das trans-Konformere ist thermodynamisch stabiler NH ist nicht protonierbar O 1,3 2 7 1,4 O O N 117° N N H 121° 3 1 ,5 OH O N N H 120° trans H H cis Die Peptidgruppe ist fast eben gebaut. In Peptiden stehen die Substituenten der Aminosäuren ober- bzw. unterhalb dieser Ebene H O R' OH H2N N R H H O 99 Einige natürlich vorkommende Peptide NH2 Glutathion (biol. Redoxsystem) O H N HOOC N H O SH Glu Gly Cys H N H2N Carnosin (Neurotransmitter) COOH COOH H N O N β-Ala His HOOC Cys Ocytocin (Hypophysenhormon) Tyr S Ile S Gln Cys Asp Pro Leu Gly NH2 PROTEINE Die Bezeichnung Protein kommt aus dem Griechischen: (proteuo) = „ich nehme den ersten Platz ein“ Einteilung: 1. Skleroproteine (faserartig, Stützstrukturen, wasserunlöslich) z.B.: Keratin (Fingernägel) 2. Sphäroproteine (sphärisch gebaut, wasserlöslich, denaturierbar) z.B.: Eiklarproteine 100 Chemische Struktur: aus einzelnen peptidisch gebundenen Aminosäuren 1 R H2N O R3 O H N R N H 2 N H 4 O R5 O H N R R7 O H N N H 6 O R COOH wegen der Planarität der peptidischen Einheiten und der Rotationsbarriere um die CN Bindung können sich leicht Wasserstoffbrücken zwischen zwei Proteinketten oder intramolekular ausbilden. → Faltblattstruktur oder Helix 1 R O H N H2N O 3 N R R N H R N 6 R β-Faltblatt (antiparallel oder parallel) Beispiel: Kollagenfasern O 5 N H R COOH H 3 R N 4 N R H O R 6 O H 7 O H N N R H O R 4 O H 5 O H N 2 7 HOOC R O O N H R1 H N 2 R NH2 O α-Helix 101 Strukturen von Proteinen: 1. Primärstruktur: Aminosäuresequenz 2. Sekundärstruktur: räumliche Anordnung der Kette (Flatblatt, Helix) nur peptidisches Rückgrat, nicht räuml. Anordnung der AS Seitenketten 3. Tertiärstruktur: Gestalt des Proteins (räuml. Anordnung aller Atome) 4. Quartärstruktur: Aggregate aus mehreren Proteinen (Dimere, Trimere, etc.) Beispiel für Protein mit Quartärstruktur aus 4 Proteinketten (Untereinheiten): Hämoglobulin 102 12.3 Kohlenhydrate, Triosen, Tetrosen, Pentosen, Hexosen, Aldosen, Ketosen, Pyranosen, Furanosen, Aminozucker, Anomere, Onsäuren, Uronsäuren, Schreibweisen: Fischer, Haworth, sterische Schreibweise, Konformation 103 Hexosen D-Allose D-Altrose CHO CHO CHO D-Mannose D-Glucose H H OH OH HO H H OH H HO H OH H OH H OH H OH H H OH CH2OH OH CH2OH OH HO O OH OH OH H H OH OH HO H H OH OH OH H H OH OH OH HO H H OH OH D-Talose HO HO HO H H H H H H H OH OH CH2OH CH2OH HO OH HO OH O HO OH OH CHO OH HO HO HO OH OH O O OH CHO CH2OH HO OH OH OH O HO HO D-Galactose CHO HO H CH2OH OH OH CH2OH O HO HO D-Idose CHO H H OH OH D-Gulose CHO HO H HO H CH2OH OH O HO HO OH H HO OH OH OH O OH OH Furanosen O HO HO HO Fructose OH HO OH O OH HO O OH HO HO HO Ribose Xylose OH O HO HO OH HO Arabinose 104 12.4 Saccharide, Glycoside, 1,4-, 1,6-Verknüpfung, Saccharose, Lactose, Maltose, Isomaltose, Cyclodextrine, Bildung und Hydrolyse von Sacchariden OH Maltose 4-O-(α-D-Glucopyranosyl)-D-glucopyranose O HO HO OH HO O HO O OH HO OH Cellobiose 4-O-(β-D-Glucopyranosyl)-D-glucopyranose OH O HO HO HO HO Lactose (Milchzucker) 4-O-(β-D-Galactopyranosyl)-D-glucopyranose O O HO OH HO OH OH O O O HO HO HO OH HO OH Chitobiose (Chitin) OH O HO HO AcNH HO O O HO OH AcNH OH O HO Melibiose HO O O HO HO HO OH HO HO Saccharose (Rohrzucker) HO OH O HO OH O HO O OH OH OH O HO HO Raffinose (Rübenzucker) O HO HO OH O HO O HO O OH OH 105 Einige Kohlenhydrate aus Nahrungsmitteln und anderen Quellen: OH O HO HO N S O SO3H OH Sinigrin OH O HO HO O O OH HO HO O OH Amygdalin HOOC CN O O O O O HO HO O OH OH Agar-Agar HO HO HO Vitamin C O O OH 106 H2N HN O HO CHO O HO NH OH H N OH NH2 NH HO O O HO HO NHCH3 Streptomycin Palytoxin Herzglycoside 107 12.5 Fette und Lipide, Klassifizierung, Wachse, Sphingolipide, Terpene, Steroide Stoffklassen A. nicht hydrolysierbar • • • • Langkettige Alkane, Carotinoide, Vitamine Terpene, Steroide Fettalkohole >C10 Fettsäuren >C10 108 109 Common Fatty Acids 110 Chemical Names and Descriptions of some Common Fatty Acids Common Name Carbon Double Atoms Bonds Scientific Name Butyric acid Caproic Acid Caprylic Acid Capric Acid Lauric Acid Myristic Acid Palmitic Acid Palmitoleic Acid Stearic Acid Oleic Acid Vaccenic Acid Linoleic Acid Alpha-Linolenic Acid (ALA) Gamma-Linolenic Acid (GLA) 4 6 8 10 12 14 16 16 18 18 18 18 0 0 0 0 0 0 0 1 0 1 1 2 butanoic acid hexanoic acid octanoic acid decanoic acid dodecanoic acid tetradecanoic acid hexadecanoic acid 9-hexadecenoic acid octadecanoic acid 9-octadecenoic acid 11-octadecenoic acid 9,12-octadecadienoic acid 18 3 9,12,15-octadecatrienoic acid 18 3 6,9,12-octadecatrienoic acid Arachidic Acid 20 0 eicosanoic acid Gadoleic Acid Arachidonic Acid (AA) EPA Behenic acid Erucic acid 20 20 20 22 22 1 4 5 0 1 DHA 22 6 Lignoceric acid 24 0 Sources butterfat butterfat coconut oil coconut oil coconut oil palm kernel oil palm oil animal fats animal fats olive oil butterfat safflower oil flaxseed (linseed) oil borage oil peanut oil, fish oil 9-eicosenoic acid fish oil 5,8,11,14-eicosatetraenoic acid liver fats 5,8,11,14,17-eicosapentaenoic acid fish oil docosanoic acid rapeseed oil 13-docosenoic acid rapeseed oil 4,7,10,13,16,19-docosahexaenoic fish oil acid small amounts tetracosanoic acid in most fats B. hydrolysierbar 111 • • • Fette (Fettsäure + Glycerin) Waxe (Fettsäure + Fettalkohol) Sterolester (Fettsäure + Cholesterin s.o.) spermaceti: CH3(CH2)14CO2-(CH2)15CH3 beeswax: CH3(CH2)24CO2-(CH2)29CH3 carnuba wax: CH3(CH2)30CO2-(CH2)33CH3 C. Phospholipide • • Phosphatidsäuren (Fettsäure + Glycerin + Phosphat) Phosphatide (Fettsäure + Glycerin + Cholin) 112 113 D. Prostaglandine, Tromboxane, Leukotriene E. Glycolipide • • Cerebroside (Fettsäure + Sphingosin s.o. + Zucker) Ganglioside (Fettsäure + Sphingosin s.o. + Zucker + Neuraminsäure) 114 12.6 Nucleinsäuren, Purin-, Pyrimidinbasen, Nucleoside, Nucleotide, DNA, RNA 115 116 12.7 Weitere Naturstoffe: Vitamine, Alkaloide, Hormone, Antibiotika Vitamine OH Vitamin A (Retinol) Sehpigment, Immunsystem O N NH O NH2 N N CH2 N N S N OH Vitamin B1 (Thiamin) Vorstufe für Coenzyme Decarboxylasen OH OH Vitamin B2 (Riboflavin) FAD für Oxidoreduktasen OH OH O O O NH2 N Vitamin B3 (Nicotinamid) NAD für Oxidoreductasen N HN H 2N N N COOH N H N H Vitamin B4 (Folsäure) C1-Gruppentransfer COOH 117 R Vitamin B6 Aminosäurestoffwechsel R = CH2OH Pyridoxol R = CHO Pyridoxal R = CH2NH2 Pyridoxamin OH HO N H2NOC R CONH2 H2NOC N N CONH2 Co OH H2NOC OH O O HO N H Vitamin B12 (Cobalamin) Ligasen, Transferasen N Vitamin C (Ascorbinsäure) Radikalfänger Immunsystem O OH CONH2 NH O N OH O N P O O O Vitamin D (Calciferol) Calziumstoffwechsel HO O Vitamin E (Tocoferol) Antioxidans HO HO HO O O Vitamin K (Phyllochinon) Proteinsynthese HO Biotin NH Carboxylasen H H S COOH NH H O H H N CO OH O Pantothensäure Coenzym A Antibiotika N O OH H N H HO OH OH OH Cl Cl HO O Tetracycline HN O O Chloramphenicol O HO HO NH2 HO O HO HO O H H H S N R O O O O Erythromycin O OMe N O COOH OH Penicilline Alkaloide (Wortbildung aus arabisch al qualja: „Pflanzenasche“ und griechisch -oides: „ähnlich“) sind natürlich vorkommende, chemisch heterogene, meist basische, stickstoffhaltige organische Verbindungen des Sekundärstoffwechsels, die auf den tierischen oder menschlichen Organismus wirken. Über 10000 verschiedene pflanzlichen, tierische oder von Mikroorganismen produzierte Substanzen werden dieser Stoffgruppe zugeordnet. Einteilung nach chemischer Struktur Die in der Literatur am häufigsten verwendete Einteilung der Alkaloide ist die Kategorisierung entsprechend ihrer chemischen Struktur. Namensgebend ist der Teil des Moleküls, der einen Stickstoff enthält. • Alkaloide mit heterocyclischem Stickstoff 118 Pyrrolidin-Alkaloide: z. B. Hygrin Steroid-Alkaloide: z. B. Solanin Pyridin-Alkaloide: z. B. Nicotin, Anabasin Tropan-Alkaloide: z. B. Hyoscyamin, Scopolamin, Cocain Chinolin-Alkaloide: z. B. Chinin, Chinidin Isochinolin-Alkaloide: z. B. Morphin, Codein, Papaverin, Berberin, Tubocurarin Indol-Alkaloide: z. B. Ajmalin, Ergotamin, Yohimbin, Reserpin, Strychnin Purin-Alkaloide: z. B. Coffein, Theophyllin, Theobromin Alkaloide mit acyclischem Stickstoff: z. B. Ephedrin, Mescalin o o o o o o o o • Solanin Nikotin Anabasin Cocain Chinin 119 Morphin Papaverin Yohimbin Strychnin Vincristin 120