Title Über die Oxydation von einigen Alkoholen mittels N
Werbung

Title
Author(s)
Citation
Issue Date
URL
Über die Oxydation von einigen Alkoholen mittels NChlorbernsteinsäureimids, besonders über die Entstehung von
N-Phenylbernsteinsäureimid in Benzol als Lösungsmittel
Saigusa, Takeo; Moriga, Hiroyuki; Oda, Ryohei
Bulletin of the Institute for Chemical Research, Kyoto
University (1955), 33(2): 49-57
1955-03-31
http://hdl.handle.net/2433/75502
Right
Type
Textversion
Departmental Bulletin Paper
publisher
Kyoto University
tiber die Oxydation
von einigen
N-Chlorbernsteinsaureimids,
Entstehung
Alkoholen
besonders
mittels
fiber die
von N.Phenylbernsteinsaureimid
in Benzol als Losungsmittel
Takeo SAIGUSA,
HiroyukiMORIGA
and RyoheiODA*
(Oda Laboratorium)
Eingegangen
am20. Januar 1955
C. A. Grobhat neuerdingseine interessanteUntersuchung
iiber die Oxydation
verschiedenen
Alkoholen
mittelsN-Chlorbernsteinsdureimids
(MCS)in dieentsprechenden
Aldehydeoder Ketoneand Ester publiziert. Die Verfasserhaben auch dieselben
Untersuchungen
mit verschiedenen
aliphatis
chenAlkoholen
in Benzolals Losungsmittel
durchgefiihrt
andgefunden,
dassals einReaktionsprodukt
das N-Phenylbernsteinsaureimid
(NPS) ausser den Aldehydenoder Ketonenand Estern entsteht. In Bezugauf die
EntstehungvonNPShabenGroband andereAutorengar nichtbis jetztgeschildert.Fdr
die EntstehungvondiesemNPSmussdasLosungsmittel
Benzolin Reaktionteilnehmen.
Deshalbhabendie Verfasserin diesemPunkteinegrosseInteressegehabtand urnden
Mechanismus
klar zu machen,viele Experimenteunter verschiedenenBedingungen
unternommen.
FUrdieEntstehung
vonAldehyden
oderKetonenausAlkoholen
gibtGrobdie folgenden
Reaktions-Reihen
:
RlRlCH2-CO \
CHOH+ NCS;CHOCI
+ I
'NH
R2`-R./CH2-CO/
R>CHOCI—>R_>C=O
+ HC1
Die Verfasser
di ire
haben zuerst
Entstehung
methoxybutan
von
diesen
Mechanismus
Alkylhypochlorit
durch
aus Buten-2 and ein Gemisch
CH3—CH=CH—CH3
ale richtig
bestatigt,
Nachweisen
der
von NPS haben die Verfasser
denen Aldehyd
gUltig sei.
aus
Benzol
NCS
Entstehung
des
NPS
*
_
and
durch eine
durch
die
Die Verfasser
in Gegenwart
Aldehyd
Art von radikalischer
Zugabe
~:, 1i i rl, y,
von
OCH3
vermutet,
haben experimentell
von
entsteht
Reaktion
Benzoylperoxyd
~J 131j T
( 49 )
von 2-Chlor-3-
bestatigt.
CH3 —CH —CH —CH3I I
CI
Mir die Entstehung
Bildung
von NCS and Methanol
+ NCS + CH3OH--->
d. h. die interme-
bzw.
dass der zuerst
gefunden,
and
verursacht
entstan-
dass das
vermutet,
ist, weil die
durch die Belichtung
dass
NPS
diese
Ausbeute
gesteigert
Takeo SAIGUSA,Hiroyuki MORIGAund Ryohei ODA
wird, im Gegenteil durch Zugabe von Hydrochinon griindsatztlich gehemmt wird. Daraus
haben die Verfasser folgende Reaktions-Schemata fiir die Entstehung von NPS vorgeschlagen :
NCS + Aldehyd
R• (Radikal)
R. + NCS --> R-C1 + CH2-CO\
N.
CH2-0D/
CH,-CO\CI-10-CO\
N. + CGHG -----I-\N-C61-15
CH0-00/CI-11-03/
+ H.
Die Verfasser haben auch gefunden, dass das N-(m-Nitroplieny1)-bernsteinsaureimid
entsteht, wenn das Nitrobenzol statt des Benzols als LOsungsmittelangewandt wird.
Obwohl diese Erscheinung aussehnlich mit der iiblichen Kernitnis der radikalischen
Reaktion nicht iibereinstimmt, doch scheint diese als normal aus den Ansichten von
Dannley und Kooyman, die neuerdings publiziert wurden.
Ziemlich viele Untersuchungen sind schon aber die Oxydation von verschiedenen
Alkoholen mittels N-Chlorbernsteinsaureimids (unten als NCS bezeichnet) publiziert. Grob' hat z. B. den Benzylalkohol, Benzhydrol, Cyclohexanol und Isoamylalkohol mit NCS in Gegenwart von Pyridin behandelt und die entsprechenden
Aldehyde oder Ketone in guten Ausbeuten erhalten.
Die Verfasser haben gemass
den Arbeitsbedingungen von Grob den Methyl-, Athyl-, n-Propyl-, n-Butyl-, Isopropyl-, Isoamylalkohol und Athylenglykol zur Einwirkung von NCS in Benzol unterworfen und ausser den entsprechenden Aldeh.yden oder Ketonen und Estern auch
das N-Phenylbernsteinsaureimid (unten als NPS bezeichnet) in jedern Fall erhalten.
-Ob
er die Entstehung von diesem NPS hat es gar keine Erklarung bis jetzt gegeben.
Far die Entstehung des NPS mtisste das Ltisungsrnittel Benzol in Reaktion teilnehmen.
Deshalb haben die Verfasser diese Reaktion unter -verschiedenen Bedingungen wieder
untersucht, urn den Mechnismus der Entstehung von NPS klar zu machen.
Zuerst mOchten die Verfasser die Arbeitsbedingungen und die Versuchsergebnisse
geben und dann, auf diesen Resultaten stehend, den Reaktionsmechanisrnus erklaren.
VERSUCHSTE/L
Das NCS wurde nach der Methode von Grob dargestellt und nach der Umkrystallisation (Schmp. 150°) zur Untersuchung angewandt.
Alle zur Untersuchung
angewandten Alkohole oder Aldehyde wurden nach gewOhnlichen Methoden gereinigt und getrocknet.
(1)
Einwirkung
von NCS auf Alkohole in Benzol als LOsungsmittel
5g NCS (0.037 M), 3g Pyridin (0.037 M) und verschiedene Menge von Athylalkohol wurden in 20 ml Benzol gelOst und auf einem Wasserbade bei 90-95 unter
Rackfluss wahrencl 2 Stiinden erhitzt.
Die Reaktionsibsung spaltete sich in zwei
( 50 )
Oxidation von einigen Alkoholen
NCS
Schichten, deren obere wurde zur Wasserdampfdestillation unterworfen and der
Riickstand wurde eingeengt. Daraus schied Krystall ab, welch abfiltriert, umkrystallisiert aus heissem Wasser and getrocknet wurde.
Es schmolz bei 153-154°and
wurde als NPS, durch Analyse and Mischprobe mit einem Muster, das anderweitig
aus Anilin and Bernsteinsaure dargestellt wurde, identifiziert. Anderweitig wurden
der Athyl Acetat and der Acetaldehyd (als 2,4-Dinitrophenylhydrazon) aus dem
Destillat der Wasserdampfdestillation, sowie aus der unteren Schicht der Reaktionslosung quantitativ gemessen. Die Resultate, die unter Anwendung von verschiedenen
Mengen von Athylalkohol erhalten wurden, sind in Tabelle 1 wiedergegeben.
Tabelle 1.
Athylalkohol (M)
NCS, (M)NPSAcetaldehydAthyl
Ausbeute (%)'a)
0.53.95.5-1.6.213.71.510.114.446.3
2.010.7'
3.06.913.0----
Acetat
15.034.9
a' Berechnet auf NCS
Nachst wurden die gleichen Versuchungen mit verschiedenen Alkoholen durchgefiihrt. Die Resultate sind in Tabelle 2 'zusammenfassend wiedergegeben.
Tabelle 2.
Versuchsbedingungen
Ausbeute (%) (ber. auf NCS)
Alkohol
Erhitzungs-BernstejnNCS Temp. dauer
NPS Aldehyd Ester saureimid
AlkohoIe
Methylalkohol2
a tbl2
rr lb>
Athylalkohol2
n-Propylalkohol
n-Butylalkohol2
iso-Amylalkohol
Athylenglykol1
iso-Propylalkohol
Benzylalkohol1
^r1
2
2
2
2
90-95°
rr
rr
a
rr
rr
rr
rr
o
rr
60-80°
2.0 Stdn.
rr16.0
1/
a10.7
a6.16.0
rr
2.5
2.0
a
5/6
1/4
12.3
17.4
2.60.8
2.60.8
4.28.8
093.5
085.0
087.0
0
0
0
15.0
45.0
0
0
25.0
39.1
40.8
40.4
0
0
0
0
76.5
--75.8
67,7
89.0
54.0
80.9
94.5
-
(b'.Durchgefuhrt unter Sonnenbestrahlungin Pyrex-I{olben.
Beim Fall von .A.thylenglykol war der erhaltene Aldehyd der Glykolaldehyd,
das als 2,4-Dinitrophenylhydrazon durch Mischprobe mit einem Muster, das anderweitig synthesiert wurde, identifiziert wurde.
Alle obige Versuche wurden in
( 51 )
Takeo SA[GUSA,Hiroyuki MOP.[GAand RyoheiODA
Gegenwart von Pyridin durchgefuhrt.
Bei Abwesenheit des Pyridins findet die
Reaktion gar nicht statt.
Die Verfasser haben z. B. ein Gemisch 5g NCS, von,
3.2g Methanol and 20 ml Benzol 4 Stunden lang unter Riickfluss gekocht, doch
wurde nur das Ausgangsmaterial unverandert zuruckgewonnen.
Die Verfasser
haben auch in dem obigen Fall 0.0242g Benzoylperoxyd zugegeben, aber wurden
weder Aldehyd noch Ester, sondern nur Bernsteinsaureimid erhalten. Die Verfasser
haben auch statt des Pyridins das Pyridinhydrochlorid angewandt, fand aber auch
keine Reaktion statt.
(2)
Reaktion von Buten-2 auf die Losung von NCS in Methanol
40g NCS wurden in 150 ml Methanol gelost and in diese Losung, behaltend
die Temperatur bei 50-55°, wurde Buten-2 innerhaib 8 Stunden eingeleitet.
Das
Buten-2 wurde nach der Methode von David 6' aus 120 ml sek-Butanol hergestellt.
Nach der Einleitung wurde der uberschussige Methanol abgedestilliert. Der Riickstand wurde mit NaHSO3-Losung behandelt, mit Wasser gewaschen, getrocknet and
zur Destillation unterworfen and eine Fraktion, die bei 116-117'ubergeht, abgefangen.
Die Ausbeute dieser Fraktion betrug 5.5g. Dieses Produkt stimmt in allen Eigenschaf ten mit dem 2-Chlor-3-methoxybutan, das Likrosherstov" aus Methylhypochlorit
and Buten-2 erhalten hatte, gut iiberein.
(3)
Reaktion von NCS und Benzol in Gegenwart von Aldehyden
In eine Losung von 5g NCS in 20 ml Benzol wurde Acetaldehyd (bzw. Propionaldehyd oder Aceton) zugefiigt and auf einem Wasserbad unter Riickfluss erwarmt.
Nach die Losung den Punkt erreicht ist,an dem sie nicht mehr das Jod aus Kaliumjodid frei_macht (dieser Punkt wurde gewohnlich nach 2.5-3 Stdn. erreicht), wurde
die Erhitzung noch 30 Minuten fortgesetzt and dann zur Wasserdampfdestillation
unterworfen.
Die Resultate, zusammen mit anderen Versuchsbedingungen, sind in
Tabelle 3 zusammenfassend wiedergegeben.
Tabelle 3.
Aldehd
oder Keton
Acetaldehyd
//6.8
//3.4
a3.4
it6.8
it6.
Propionaldehyd
it4.4
//4.4
Aceton4.5
KomponentenAusbeute
Aldehyd NCS Mol . Verhaltnis BPO Hydro-des
chinon Pyridin
(g)
(g)
Aldehyd/NCS mg(
(g)
3.4
8
4.4//
5.0
a
it
it
//
//
0 .
it
it
20
40
20
220
40
420
20
220
20
20
(52 )
0
0
0
0
0
0
0
0
100
0
3.0
3.0
0
0
0
0
0
0
00
00
NPSauf
(%)
( ber.
\ NCS
1.2
3.8
1.2
2.6
4.1
6. 2
3.5
6.3
Oxidation von einigen Alkoholen mittels NCS
(4)
Reaktion
von N-Brombernsteinsanreimid
6.6 g N-Brombernsteinsaureimid,
mit Alkohol
2.37 g Methanol,
Benzol wurden
gemischt
nachbehandelt,
aber wurde nur Spur von NPS erhalten.
(5)
Reaktion
von NCS mid Benzoylperoxyd
15.6 g NCS wurden
und auf these Losung
3.0 g Pyridin
und 3 Stunden lang unter Riickfluss
in 70 ml Benzol gelost,
wurde eine Losung
gekocht
und 20 mi.
und wie oben
in Benzol
auf 85-8T unter Riickfluss
von Benzoylperoxyd
erwarmt
(14.4 g)
in Benzol
(80 ml) innerhalb 6 Stunden tropfenweise
zugefiigt und weiter 17 Stunden lang
erhitzt.
Dann wurde das Benzol abgetrieben.
der Riickstand wurde mit Wasser,
NaHCO3- und dann NaHS03Wasserdampfdestillation
L6sung,
unterworfen.
wurden
2.2 g 13ersteinsdureimid
Losung
wurde 0.97 g Benzoesdure,
olige Schicht
des Destillates
zuletzt
mit Arnmoniak
zeigte
und nachst
den Schmp.
durch Mischprobe
Fraktion
Wasser
von
mit
zweifellos
anderem
abgefangen
und
dampfdestillation
erhalten.
(6)
wurde ca.
23 g Nitrobenzol,
HC1, erhalten.
Die
wurde
Krystall
mit
wurde
so gereinigte
Deshalb
Destillation
durch
Produkt
ist
die originale
der oligen Schicht
der
die bei 220-250° ubergeht,
Aus dem Riickatand
Extrahieren
der
Wasser-
mit heissem
Wasser
doch wurde daraus
durch
Kochen
mit
wiedergewonnen.
als Liisungsmittel
10 g NCS, 6 g Pyridin
bei 90-97° unter Riickfluss
ubergehende
Wasser
NaHCO3-
als p-Chlorbenzolsulfonsaureamid,
identifiziert.
war teerig,
in Nitrobenzol
mit
mit
Der erzielte
dieses
identifiziert.
Bei der
70 mg NPS
0.98 g Bernsteinsdure
Reaktion
und
und zur
wurde mit CaCl2 getrock-
wurde noch die zweite Fraktion,
diese als Diphenyl
Der letzte Riickstand
konz. HCl ca.
mit
behandelt.
Dies wurde
Muster,
das Chlorbenzol.
Wasserdampfdestillation
Wasch-Losung
die bei 110-136° iibergeht,
umkrystallisiert
143-144%
gewaschen
der Wasch-LOsung
nach der Ansduerung
Chlorsulfonsdure
heissem
Aus
der Wasserdampfdestillation
Eine Fraktion,
aus
Wasser
Aus der ersten
erhalten.
net und wieder destilliert.
viermal
wieder
und 44 g Methanol
erhitzt und zur Destillation
Teil wurde wieder fraktioniert
wurden
unterworfen.
und gab eine Fraktion,
gemischt,
Der unter 100°
30-35° (ca.
1.3
g). Diese wurde als Methyl Format identifiziert.
Der fiber 100° siedende Ted
wurde zur Wasserdampfdestillation
unterworfen und das unveranderte
Nitrobenzol
wurde abgetrieben
(ca. 6 g).
wurde aus Wasser-Alkohol
wurde erhalten.
Schmp.
C 54.20 %, 54.17 %;
Gemisch
129-154°.
feste
Riickstand
umkrystallisiert
der Wasserdampfdestillation
und 0.8 g hellgelbes
Dessen Analysendaten
C 54.54 %, H 3.636 %, N 12.73 9.
stimmen mit den berechneten ziemlich
haben anderweitig
Berechnet
gut
0-, m- und p-Nitrophenylbernsteinsaureimd
( 53 )
Krystall
sind wie folgt
H 3.85 %, 3.87 9;; ; N 13.13 %, 13.03 %.
phenylbernsteinsdureimid
Die gefundenen Werten
Verfasser
Der
als Nitro-
tiberein.
Die
dargestellt
Takeo SAIGMSA,Hiroyuki ,MORIOAund Ryohei ()DA
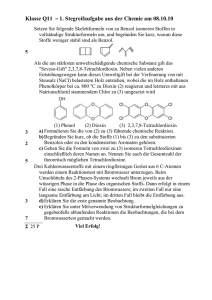
und die Infrarotspektren
gemessen.
des obigen Produktes
Die Ergebnisse
sind in Fig.
and
sowie
der
drei
reinen
Muster
1 wiedergegeben.
30
/".
J
\ -
25
,
7 -.. \
i • \
^I
,
1111
... el.%,.%
,_.,209,
a
.
1\
-......
io
' ./-14.0
I,6._\\A,
,,,i,„`'I%,
.L5•-,,
`1A
„,"
Vf+0‘il
,, \rflO
%%!°AI
0\*3A------------------------.
C-- \
.,
.-
if4.
. ---------------P
,A.'",...111 \+•
./.....,,c.,0 o1pfl
/
1 .:'
E-I
.\
\1
\i/(/
,..•'iji,,--
1 At
1 L, A0-1---;
10------------\------\
"'Q' 7
.•
1
5 ------------------------------------------
11A12p,13p,
Fig. I. Infrarotspektren. (BeckmamIR-2P).
Aus dieser Figur ist ersichtlich, dass das obige Produkt ein Gemisch von 0-,
m- und p-Nitrophenylbernsteinsaureirnidenist und zwar, dass darunter der m-Isomer Oberwiegt. Die Verfasser haben auch bestatigt, dass das reine m-Nitrophenylbernsteinsaureimid durch wiederhohlte Umkrystallisierung des obigen Produktes
aus Alkohol erzielt wird.
DISMISSIONDER VERSUCHSERGEBNISSE
UNDDER ERKLARUNGDER ENTSTEHUNG
VONNPS
Grob hat vermutet, dass diese Dehydrierungsreaktionvon Alkoholen in Aldehyde
oder Ketone mittels NCS nach folgender Weise fortschritt :
(1)
CH-CO
;,CHOH
+ NCS.--' '>CHOC1
-I-CH2I CO )NH
( 54 )
o/
'
Oxidationvon einigenAlkoholenmittels NCS
(2)I\;CHOC'
RI/R2/
--kRi~C=
0 -f-HC1
Nach diesem;Mechanismus soll zuerst das Alkylhypochlorit entstehen. Dies
haben die Verfasser wie folgt bestatigt, d.h. Buten-2 wurde in eine Losung von
NCS in Methanol eingeleitet and als Reaktionsprodukt 2-Chlor-3-methoxybutan
wurde nachgewiesen. 2-Chlor-3-methoxybutanwurde anderweitig nach Likroshers
trov ' durch Einwirkung von Methyl Hypochlorit auf Buten-2 dargestellt. Deshalb
ist es klar, dass die Reaktion (1) wirklich stattfinden kann. Die Verfasser haben
weiter bestatigt, dass die Dehydrierungsreaktion ohne Pyridin gar nicht stattfinden
kann; deshalb ist es wahrscheinlich, class far die Reaktion (2) das Pyridin unbedingt notwendig ist, d.h. dass das Pyridin die Dechlorhydrierung von Alkylhypochlorit beschleunigt. Die Entstehung von Aldehyden oder Ketonen durch Dehydrierung von Alkoholen mittels NCS kann zwar gemass der obigen Weise erklart
werden, doch man kann noch gar nicht die Entstehung von NPS verstehen.
Um die Bedingungen, unter weichen das NPS entsteht, zu bestimmen, haben
die Verfasser die Reaktion unter verschiedenen Bedingungen durchgefuhrt. Die
Resultate sind in'Tabelle 4 zusammenfassend wiedergegeben.
Tabelle
4.
numme-Versuchs-j
ReaktionskomponentenI Entstehung
vonNPS
1
2
3
4
5
6
7
8
9
10
11
12
NCS
NCS
NCS
NCS
NCS
NCS
NCS
NCS
NCS
NCS
NCS
NBS
+ Benzolx
+ Benzol -1- Benzoylperoxydx
+ Benzol + Alkoholx
-I- Benzol + Alkohol ± Benzoylperoxydx
-I- Benzol + Pyridinx
-f- Benzol -I- Pyridin + Pyridin-HClx
-1- Benzol + Alkohol + PyridinO
+ Benzol + Aldehyd + PyridinC)
+ Benzol + Aldehyd0
-f- Benzol + Aldehyd + Hydrochinon
+ Benzol + Acetonx
± Benzol + Alkohol -I- PyridinSpur
Aus dieser Tabelle
von (Alkohol
wendig
ist.
Ohne Pyridm
die Alkohole
ist es denkbar,
in Gegenwart
die Gegenwart
schon in der Tabelle
Ausbeute
dass far die Entstehung
oder von Aldehyden
entseht
beteiligt
von
mittels
ist.
Wie das
3 gezeigt
von NPS zunehmen,
wurde,
obwohl
Experiment
die Zugabe
die Zunahme
(55 )
der
Tatsache
dehydriert
entstandene
die Reaktion
lasst
aus
NCS in Aldehyde
von NPS das
Hydrochinon
von NPS die Gegenwart
ausser NCS and Benzol unbedingt
das NPS gar nicht and
von Pyridin
dass far die Entstehung
der Ausgangsalkohol
hemmt
ersichtlich,
+ Pyridin)
von
class
werden,
Aldehyd,
10 in der Tabelle
grandsatzlich.
nicht
4 zeigt,
Weiter
Benzoylperoxyd
nicht so viel ist.
not-
Ferner,
wie
die
wie
Takeo SAIGUSA,Hiroyuki N1oaiCAund`Ryohei ODA
schon in der Tabelle 2 gezeigt wurde, lasst die Bestrahlung der Reaktionslosung
unter Sonnenlicht auch die Ausbeute des NPS zunehmen. Aus diesen Tatsachen
kann man schliessen, dass die Entstehung von NPS von einer radikalischer Reaktion, die zwischen NCS and Aldehyd, stattfindet, abhangig ist. Beim Fall von Isopropylalkohol entsteht kein NPS. Die Ursache dieser Erscheinung liegt wohl darin,
dass der aus dem Isopropylalkohol entstandene Aceton schwerer teilnehmbar in
radikalischer Reaktion als Aldehyd ist, d.h. der Wasserstoffatom von Aceton schwerer als der von Aldehyden radikalisch entzogen wird.a)-'"
Obwohl ist es schon bekannt, dass keine Reaktion stattfinden kann, wenn das
NCS allein, oder in Gegenwart von Benzoylperoxyd in Benzol erhitzt wird, haben die
Verfasser gefunden, dass die Reaktion wirklich stattfinden kann, wenn das NCS in
Benzol in Gegenwart von aquivalenter Menge von Benzoylperoxyd erhitzt wird and
als Reaktionsprodukte wurden NPS, Chlorbenzol, Bernsteinsaureimid, Diphenyl and
Benzoesaure nachgewiesen.
Gleichzeitig wurde ein teeriges Produkt erhalten,
dessen Konstitution unklar ist. Aber, daraus durch Kochen mit konz. HCl wurde
Bernsteinsteinsaure erhalten. Daraus scheint es sicher, dass dieses teeriges Produkt
ein Produkt, das durch weitere radikalische Reaktion auf den Benzolkern des NPS
entstanden war, ist. Aus den obigen experimentellen Tatsachen kann man vorlaufig
die folgende Reihe von Reaktion schreiben :
0
0
II
II
C;H;C—O—O—C---Cr;H; C6H5. + C6H2000• + CO2
CH2 CO
NCS --> I
`N• + •C1
CH_—CO/
C6H5. + NCS ~
oder
CH2—CO
CH.--00/N—05H;+
Cl.
CH2-CO~
C6H,CI +IN.
CH2—00/
CH2--COCH.--CO
C~;I
IS• + I'N
• ---a• I~N—C;;H;
CH_—CO/
CH2—CO/
C6H2•+ Cl• -----aC;H;CI
Nachst haben die Verfasser das Nitrobenzol statt des Benzols als Losungsmittel
angewandt. Es ist schon wohl bekannt, dass das Nitrobenzol leichter als Benzol in
radikalischen Reaktionen teilnehmen kann and zwar dass, die radikalische Substitution in der o- and besonders in der p-Stellung des Nitrobenzols stattfindet.h1 13)
Die Verfasser deshaib vorher erwartete, das bei diesem Fall das p-Nitrophenylbernsteinsaureimid hauptsachlich erhalten wurde. Aber war das Resultat ganz gegen
Erwartung.
Das Produkt, das dem NPS entspricht, war hauptsachlich das mNitrophenylbernsteinsiureimid.
Dies wurde aus den Infrar•otspektren klar gemacht
( 56 )
Oxidation von einigen Alkoholen mittels NCS
(vergl. Fig. 1).
Die Verfasser haben auch dieses Rohprodukt wiederholt aus
Alkohol umkrystallisiert
and zuletzt das reine m-Nitrophenylbernsteinsaureimid
erhalten. Dieses Produkt stimrnte ganz gut mit einem Muster, das anderweitig
hergestellt wurde, iiberein. Deshalb ist es ganz klar and sicher, dass bei der
Reaktion von NCS auf Alkohole in Nitrobenzol in Gegenwart von Pyridin ausser
den Aldehyden oder Ketonen auch das m-Nitrophenylbernsteinsaureimid
entsteht.
Es scheint aussehnlich denkbar zu sein, dass diese Erscheinung die radikalische
Erklarung, wie oben geschildert wurde, aus Grund vernichten wiirde.
Aber neuerdings hat Dannley") einen Beispiel der radikalischer Substitution am
Benzolkerne, die 100 90ig in die m-Stellung eintritt, gefunden. Dies ist der Fall
von Einwirkung von p-Nitrophenylradikal auf Benzotrichlorid.
Dannley erklart,
dass diese Erscheinung auf polarem Faktor verursachlich ist.
Auch Kooymanl"
zeigte vielen experimentellen Beispiele von radikalischer Substitution, bei denen der
polare Faktor eine grosse Rolle spielt. Kooyman schilderte besonders die Erscheinung, dass der Succinoimdyl-Radikal gegen eine Stelle, wo die Elektronendichte
klein ist, angrifft. Aus diesen Tatsachen kann man ohne weiteres verstehen, dass
die Entstehung von m-Nitrophenylbernsteinsaureimid aus Nitrobenzol and NCS auch
eine radikalische Natur ist.
LITERATUR
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
(10)
(11)
(12)
(13)
(14)
(15)
C. A. Grob, Hely. chin:. Acta., 36, 1763(1953).
C. A. Grob, Experientia, 5, 199 (1949); C. A., 44, 1890(1950).
M. F. Hebbelynck, C. A., 46, 10127(1952).
M. F. Hebbelynck, C. A., 44, 1429 (1950).
M. F. Hebbelynck, C. A., 46, 7051(1952).
H. S. David, J. Am. Chem. Soc., 50, 2779(1928).
M. V. Likrosherstov, C. A., 29, 3306(1935).
W. A. Waters, "The Chemistry of Free Radicals," p. 238 (2 nd Edition).
M. S. Kharasch, J. Org. Chem., 14, 248 (1949).
W. A. Waters, J. Chem. Soc., 1952, 3108.
O. Shimamura, Bull. Chem. Soc., Japan, 23, 205 (1950); 25, 76 (1952).
J. Weiss, J. Chem. Soc., 1949, 2074,3245; 1950, 3265; 1951, 3275.
D. H. Hey, ibid., 1951,2892.
R. L. Dannley, J. Am. Chsm. Soc., 76, 4543(1954).
E. C. Kooyman, Koninkl. Nedel. Akademievan Wetenshappen, Proceeding Series, B.
56, No. 1.
C 57 )