Biochemisch wichtige Komplexe
Werbung
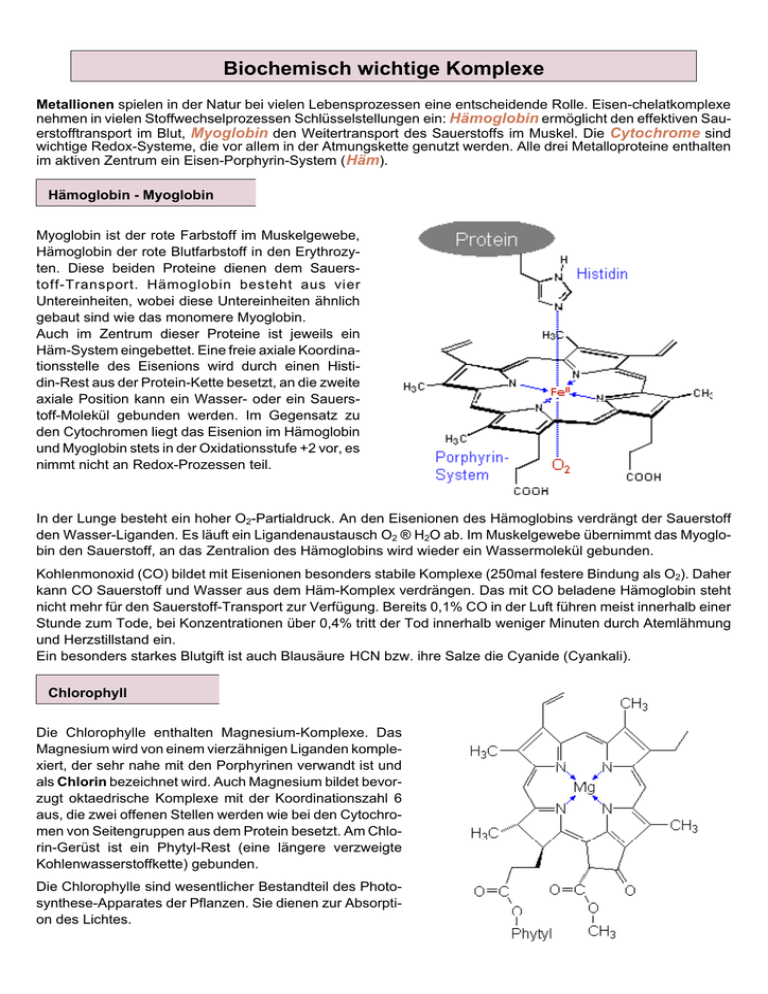
Biochemisch wichtige Komplexe Metallionen spielen in der Natur bei vielen Lebensprozessen eine entscheidende Rolle. Eisen-chelatkomplexe nehmen in vielen Stoffwechselprozessen Schlüsselstellungen ein: Hämoglobin ermöglicht den effektiven Sauerstofftransport im Blut, Myoglobin den Weitertransport des Sauerstoffs im Muskel. Die Cytochrome sind wichtige Redox-Systeme, die vor allem in der Atmungskette genutzt werden. Alle drei Metalloproteine enthalten im aktiven Zentrum ein Eisen-Porphyrin-System ( Häm). Hämoglobin - Myoglobin Myoglobin ist der rote Farbstoff im Muskelgewebe, Hämoglobin der rote Blutfarbstoff in den Erythrozyten. Diese beiden Proteine dienen dem Sauerstoff-Transport. Hämoglobin besteht aus vier Untereinheiten, wobei diese Untereinheiten ähnlich gebaut sind wie das monomere Myoglobin. Auch im Zentrum dieser Proteine ist jeweils ein Häm-System eingebettet. Eine freie axiale Koordinationsstelle des Eisenions wird durch einen Histidin-Rest aus der Protein-Kette besetzt, an die zweite axiale Position kann ein Wasser- oder ein Sauerstoff-Molekül gebunden werden. Im Gegensatz zu den Cytochromen liegt das Eisenion im Hämoglobin und Myoglobin stets in der Oxidationsstufe +2 vor, es nimmt nicht an Redox-Prozessen teil. In der Lunge besteht ein hoher O2-Partialdruck. An den Eisenionen des Hämoglobins verdrängt der Sauerstoff den Wasser-Liganden. Es läuft ein Ligandenaustausch O2 ® H2O ab. Im Muskelgewebe übernimmt das Myoglobin den Sauerstoff, an das Zentralion des Hämoglobins wird wieder ein Wassermolekül gebunden. Kohlenmonoxid (CO) bildet mit Eisenionen besonders stabile Komplexe (250mal festere Bindung als O2). Daher kann CO Sauerstoff und Wasser aus dem Häm-Komplex verdrängen. Das mit CO beladene Hämoglobin steht nicht mehr für den Sauerstoff-Transport zur Verfügung. Bereits 0,1% CO in der Luft führen meist innerhalb einer Stunde zum Tode, bei Konzentrationen über 0,4% tritt der Tod innerhalb weniger Minuten durch Atemlähmung und Herzstillstand ein. Ein besonders starkes Blutgift ist auch Blausäure HCN bzw. ihre Salze die Cyanide (Cyankali). Chlorophyll Die Chlorophylle enthalten Magnesium-Komplexe. Das Magnesium wird von einem vierzähnigen Liganden komplexiert, der sehr nahe mit den Porphyrinen verwandt ist und als Chlorin bezeichnet wird. Auch Magnesium bildet bevorzugt oktaedrische Komplexe mit der Koordinationszahl 6 aus, die zwei offenen Stellen werden wie bei den Cytochromen von Seitengruppen aus dem Protein besetzt. Am Chlorin-Gerüst ist ein Phytyl-Rest (eine längere verzweigte Kohlenwasserstoffkette) gebunden. Die Chlorophylle sind wesentlicher Bestandteil des Photosynthese-Apparates der Pflanzen. Sie dienen zur Absorption des Lichtes.











