Grundlagen der Zellulären Biochemie
Werbung

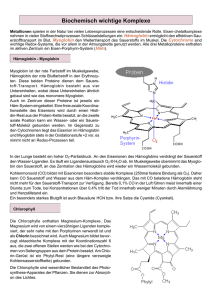
Grundlagen der Zellulären Biochemie Hämoglobin Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie, MHH Hämoglobin das erste gut untersuchte Protein Warum beginnen wir die Diskussion von Enzymen mit Myoglobin und Hämoglobin, die gar keine Enzyme sind? Hämoglobin war das erste Protein von dem Kristalle gezüchtet (1840 Friedrich Hünefeld) und zwischen Spezies verglichen (1909 Edward Reichert und Amos Braun) wurden, dessen Molekulargewicht genau bestimmt wurde, dessen physiologische Funktion herausgefunden wurde, dessen pathogene Veränderung auf eine Punktmutation mit einem Einzelaminosäurenaustausch zurück geführt werden konnte (Sichelzellenanämie), von dem die ersten Röntgenkristallstrukturen (Myoglobin, 1958 John Kendrew, Hämoglobin, 1976 Max Perutz) gelöst werden konnten und somit die ersten molekularen Erklärungen der Mechanismen der Funktion aufgestellt wurden. Speziell die Theorien zur kooperativen Bindung von Liganden und damit die Vorstellungen zu allosteren Beeinflussung von Proteinfunktion und Proteinstruktur wurden am Hämoglobin entwickelt. Außerdem ist die Bindung anderer Moleküle (hier Sauerstoffmoleküle) die Grundlage aller Funktionen, die Proteine übernehmen. Sie ist Voraussetzung für Strukturgebung, Katalyse, Kommunikation und Transport. Aufgaben von Hämoglobin und Myoglobin Beide Proteine sind an der Versorgung des Körpers mit Sauerstoff beteiligt. Das Hämoglobin transportiert den Sauerstoff von den Lungen in das Gewebe. Das Myoglobin in Herz- und Skelettmuskeln übernimmt den Sauerstoff und stellt ihn für die Atmungskette zur Verfügung. Durch die Bindung an die Proteine wird die Menge Sauerstoff pro Liter Flüssigkeit von 4,5 ml physikalisch gelösten Sauerstoff auf 200 ml transportierten Sauerstoff erhöht. Bei kleinen Tieren, in denen Gewebe nie weiter als ungefähr 1 mm von der Oberfläche entfernt ist, reicht die Diffusion des Sauerstoffs zur Versorgung aus. Auch bei uns spielt die Diffusion des Sauerstoffs durch die Haut eine nicht zu vernachlässigende rolle. Sie führt zusätzlich zur Beladung von Hämoglobin, wenn Arterien dicht genug an der Oberfläche verlaufen. Sauerstoffbindung durch Hämoglobin und Myoglobin In der Graphik ist die Sauerstoffsättigung gegen den Partialdruck des Sauerstoffs aufgetragen, der mit der gelösten Sauerstoffkonzentration direkt korreliert. YO2 = [ProtO2] [Prot] + [ProtO2] = pO2 P50 + pO2 Bei dem hohen Sauerstoffpartialdruck (pO2 = 100 Torr = 100 mmHg) in der Lunge wird Hämoglobin mit Sauerstoff beladen. 95 % der Bindungsplätze sind besetzt. Bei dem niedrigen Sauerstoffpartialdruck (pO2 = 30 mmHg) in den Kapillaren des Gewebes gibt Hämoglobin den Sauerstoff ab. 55 % der Bindungsplätze sind besetzt. Myoglobin in den Muskeln kann ihn dort aufnehmen (91 % Besetzung) und für die gleichmäßige Versorgung der Mitochondrien mit Sauerstoff sorgen. Neben der Speicherung von Sauerstoff scheint es dort auch eine Transportfunktion in den Zellen zu haben. Wieso binden die beiden Protein Sauerstoff so unterschiedlich? Häm bindet reversibel Sauerstoff Porphyrine dienen mit unterschiedlichen Metallionen als Liganden (anstelle der H-Atome) vielfältigen Aufgaben. Die Elektronen werden über das gesamte Porphyrinsystem verteilt, sodass die zentralen Stickstoffatome gleichmäßig an das zentrale Metallion koordinativ gebunden sind. Mg2+ ist in Chlorophyllen gebunden, die der Lichtabsorption dienen. Fe3+ ist im Häm der Cytochrome gebunden, die Elektronen aufnehmen und abgeben können (Fe2+ Fe3+). Fe2+ im Häm der Globine kann reversibel O2 anlagern. Dafür ist wichtig, dass eine weitere Koordinationsstelle des zentralen Fe2+-Ions fest durch ein Histidin des Globins besetzt ist, während an der letzten Stelle O2 binden kann. Die Farbe des Hämoglobins wechselt mit der Sauerstoffbeladung von hellrot (arteriell) bis zu dunkel rotviolett (venös). Strukturen von Hämoglobin und Myoglobin Beide Proteine sind evolutionär verwandt, wobei Myoglobin als Monomer beiden Untereinheiten des tetrameren Hämoglobins (22) ähnelt. Identisch in - und -Hb, in beiden und Mb; invariant in Vertebraten-Hb und -Mb Hämoglobin Myoglobin Die Globine gehören zu den all--Proteinen. Die -Helices bilden eine hydrophobe Bindungstasche, in der die Häm-Gruppe gebunden ist. In ihr sind noch zwei Histidine, die auf jeder Seite neben dem Fe2+-Ion stehen. Bindung von Sauerstoff an Myoglobin Desoxy-Myoglobin Animation Oxy-Myoglobin Im sauerstofffreien Myoglobin ist das Eisen kaum zu dem proximalen Histidin aus der Ebene des Häms herausgezogen, obwohl eine Koordinationsstelle gegenüber nicht besetzt ist. Der Sauerstoff wird zwischen dem Fe2+ und dem distalen Histidin gebunden, das eine Wasserstoffbrücke mit dem Sauerstoffmolekül ausbildet. Vergleich Desoxy - Oxy Die Sauerstoffbindung führt aber zu keiner signifikanten Änderung der Myoglobinstruktur. Bindung von Sauerstoff an Hämoglobin Desoxy-Hämoglobin Oxy-Hämoglobin Im sauerstofffreien Hämoglobin ist das Eisen deutlich zu dem proximalen Histidin aus der Ebene des Häms herausgezogen. Der Sauerstoff wird auch hier zwischen dem Fe2+ und dem distalen Histidin gebunden, das eine Wasserstoffbrücke mit dem Sauerstoffmolekül ausbildet. Vergleich Desoxy - Oxy Die Sauerstoffbindung führt aber zu einer signifikanten kooperativen Änderung der Hämoglobinstruktur. Sauerstoff moduliert die lokale Konformation Helix F proximales Histidin Fe2+ Häm Häm Häm Fe2+ Häm O O Die Bindung des ersten Sauerstoffmoleküls an eine Untereinheit führt zu einer Konformationsumwandlung, die sich durch das ganze Tetramer fortsetzt. Die Desoxy-Hämoglobinstruktur wird durch mehrere Salzbrücken in einem gespannten Zustand gehalten. Dies erschwert es dem ersten Sauerstoffmolekül, gebunden zu werden. Dadurch werden Salzbrücken aufgebrochen und umorientiert, sodass das Tetramer in eine relaxiertere Konformation kommt. Weitere Sauerstoffmoleküle können leichter gebunden werden. Kooperativität der Bindung Archibald Hill hat die Kooperativität, die zu der sigmoiden Bindungskurve des Sauerstoffs durch Hämoglobin führt, 1910 zum ersten Mal beschrieben. Dazu hat er in die Gleichungen den Hill-Koeffizienten n (pO2)n eingeführt, der die Kooperativität beschreibt und zwischen YO2 = 1 und der Anzahl der Bindungsplätze liegt. Je größer n ist, (p50)n + (pO2)n desto stärker ist die Kooperativität. Für eine Darstellung kann man die Gleichung auch in eine Geradengleichung umformen: log ( YO2 1 - YO2 ) = n log pO2 - n log p50 Aus Auftragungen nach dieser Gleichung kann man den Hill-Koeffizienten ermitteln. Er liegt für Hämoglobin zwischen 2,8 und 3,0. Das zeigt eine starke Kooperativität an. Beschreibung der Kooperativität Archibald Hill ging im Prinzip davon aus, dass alle Sauerstoffmoleküle auf einmal binden. Tatsächlich aber müsste man mikroskopische Bindungskonstante für das erste, zweite, dritte und vierte gebundene Sauerstoffmolekül bestimmen (Gilbert Adair). Das trägt wiederum nicht der Tatsache Rechnung, dass die Umwandlung von der schlechter bindenden T-Form in die besser bindende R-Form nicht notwendigerweise nach Bindung des ersten Sauerstoffmoleküls erfolgen muss. Entsprechend sind allgemein zwei Modelle für solche allosterischen Aktivierungen von Proteinen entwickelt worden: das Symmetriemodell das Sequenzielle Modell Beide können die Sauerstoffbindung gleich gut beschreiben. pH-Effekt auf die Sauerstoffbindung (Bohr-Effekt) Der pH-Wert hat einen deutlichen Einfluss auf die Sauerstoffbindung durch Hämoglobin: je saurer der pH-Wert desto leichter die Sauerstoffabgabe. Desoxy-Hämoglobin bindet Protonen besser als Oxy-Hämoglobin. In den Erythrozyten werden Protonen frei, wenn im Gewebe das dort produzierte CO2 aufgenommen und in Kohlensäure umgewandelt wird. Das CO2 hat auch direkten Einfluss auf das Hämoglobin, indem es an die N-terminalen Aminogruppen gebunden werden kann. Auch dies geht besser im Desoxy-Hämoglobin. Das gebildete HCO3- wird über die Erythrocytenmembran gegen Cl- ausgetauscht. Auch dieses bindet besser an Desoxy-Hämoglobin. Alle drei Effekte ergänzen sich zum Bohr-Effekt, der den O2-Transport steigert. Effekt von 2,3-Bisphosphoglycerat auf die Sauerstoffbindung In den Erythrozyten kommen hohe Konzentrationen des Metaboliten 2,3Bisphosphoglycerat vor, der in anderen Zellen wenig vorhanden ist. Es wird sogar vermehrt gebildet, wenn zum Beispiel in großen Höhen eine schnelle Anpassung der Transportleistung gefordert ist. 2,3-Bisphosphoglycerat bindet auch wieder besser an Desoxy- als an OxyHämoglobin. So kann in vitro die Sauerstoffbindungskurve des Hämoglobins erst durch entsprechende Konzentrationen von CO2 und 2,3-Bisphosphoglycerat an die von Blut angepasst werden. Methämoglobin Hämoglobin kann Sauerstoff nur transportieren, wenn das Eisen im zweiwertigen Zustand bleibt. Seine Oxidation zum Fe3+ wird aber nicht vollständig unterdrückt, weil es ja direkt mit dem Sauerstoff in Kontakt ist. Es wird zum Methämoglobin. Die Erythrozyten enthalten dafür aber eine Methämoglobin-Reduktase, die die Konzentration von Methämoglobin unter 1 % hält. Ist dieses Enzym defekt, wie bei Familien in Kentucky, die Nachfahren von Martin Fugate sind, dann reichert sich Methämoglobin an und färbt das Blut charakteristisch blau. Neben der Reduktion des Methämoglobins ist für die Erythrozyten auch wichtig, das gebildete Superoxidradikal zu entgiften. Dafür enthalten sie die zwei Enzyme Superoxiddismutase und Katalase. Sichelzellanämie Eine Punktmutation an der Position 6 von Glutamat zu Valin macht das DesoxyHämoglobin anfällig für eine Aggregation. Das kann zu entsprechenden sichelförmigen Veränderungen des Erythrozyten in den Kapillaren des Gewebes führen, die verstopfen können.