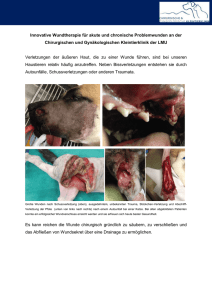
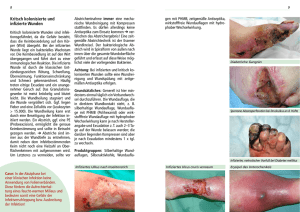
Die infektiöse Wunde (DGKS Marianne Hintner)
Werbung

Die Infektiöse Wunde Bedeutung der Keimbesiedelung für die Wundbehandlung Marianne Hintner „Wenn alle schon jetzt vorhandenen Kenntnisse und Erfahrungen in der Prophylaxe und Therapie von „chronischen Wunden“ konsequent und überall genutzt würden – es könnte vieles an Leid und auch an Kosten gespart werden“ (Assenheimer, 2001, S. 3) Rückblick Hippokrates (460-377 v. Chr.) „primäre Naht für reine Wunden; keine Naht, feuchte Behandlung und Ruhigstellung für verschmutzte Wunden“ Ambroise Pare´ (1510 – 1590) Erste schriftliche Aufzeichnungen über Anwendung von Maden in der Wundtherapie J. Woodall(1617) beschreibt erfolgreiche Behandlung des Ulcus cruris mit einer Lösung aus Silber und Salpetersäure (1:3) Mitte 18. Jhdt.: v.a. in England Kampf gegen Wundinfektionen, Begriffe Sepsis und Antisepsis, Wundreinigung mit Wein oder Alkohol Ende 19. Jhdt.: weltweiter Siegeszug der Antisepsis und Ende des Hospitalbrandes und der Pyämie durch Ignaz Semmelweis (1818-1865) – Händedesinfektion Joseph Lister (1827-1912) – Karbolsäure, „Keime der Luft können Infektionen hervorrufen“ Louis Pasteur (1822-1895) – physikalische Sterilisation chir. Instrumente Robert Koch (1843-1910) – Kampf gegen identifizierte Erreger; Fundament für Sterilisationstechnik 1928 Alexander Fleming: Penicillin 1932 Gerhard Domagk: Sulfonamide Die Entdeckung moderner Antibiotika schlechte Zeiten für die alternativen Methoden Sie verloren ihren Stellenwert in der Wundbehandlung durch Penicillin schien der Sieg über die Infektions-krankheiten näher Anfang 90er Jahre zunehmende Resistenzentwicklung und Vorkommen von Hospitalismuskeimen wie MRSA, ORSA und VRE veranlasste Wissenschaftler dazu, deren Wirkmechanismen systematisch zu erforschen Renaissance alternativer Methoden wie Silber, Maden und Honig Einsatz als topische Wundbehandlungen Kontrolle der Bakterien auf Wunden schnellere Heilung der infizierten Wunden Hautflora = Gesamtheit aller Mikroorganismen auf der Haut • bei unverletzter Haut keine Gefahr, da Epidermis wie mechanische Barriere wirkt • Bei Verletzung können MO in Blutkreislauf und tiefere Gewebeschichten eindringen • Bei kleinen Wunden und immunkompetenten Menschen verhindert dies das Gerinnungssystem und die immunkompetenten Zellen der Haut (z.B. dendritische Zellen, Langerhans-Zellen • Bei großen Wunden mit massiver Keimbelastung und Immungeschwächten kann es zur Infektion kommen Fakten • Auf allen Wunden befinden sich Mikroorganismen Die Anwesenheit von Bakterien in einer Wunde muss nicht bedeuten, dass die Wunde infiziert ist B. Gilchrist Bis heute sind ca. 1600 verschiede Bakterien klassifiziert Kontamination muss nicht zwangsläufig zu Infektion führen Ausschlaggebend ist, neben Art, Anzahl und Virulenz der Erreger, vor allem der Immunsstatus des Patienten Erst wenn Wechselwirkung zwischen Mikroben und Wirt einen Punkt erreicht, bei dem es zu einer Wundheilungsstörung oder Stagnation kommt, ist Intervention angezeigt, um eine Infektion zu verhindern Infektionsquellen: körpereigene Keimflora, ärztliches und pflegerisches Personal, medizinische Ausrüstung Der Weg zur infizierten Wunde Kontamination Nachweis einzelner Keime Bakterielles Gleichgewicht Kolonisation Nachweis einer Keimvermehrung Bakterielles Gleichgewicht Keine antiseptische Therapie (außer bei MRE) Infektion Bakterielles Ungleichgewicht > 105 Mikroorganismen/g Gewebe lokale und/oder systemische Zeichen lokale Antiseptika + systemische Antibiotika Kritische Kolonisation Bakterielles Ungleichgewicht Keine typischen Infektzeichen aber durch Toxinabgabe verzögerte Wundheilung lokale Antiinfektiva Definition der Wundinfektion Unter einer Wundinfektion versteht man den Eintritt von Mikroorganismen in eine Wunde mit den charakteristischen Zeichen einer lokalen Entzündung. Infektion = wesentlicher Eskalationsfaktor • Notwendigkeit von systemischen Gaben von Antibiotika • stationäre Aufnahme • multiresistente Bakterien • Amputationen • Sepsis bis Tod Arten der Wundinfektion Pyogene (eiterbildende) Infektionen lokalisiert, Gewebeeinschmelzungen, Eiterbildung, Abszess, typische Krankenhausinfektion Staphylokokken: rahmig gelblicher geruchsloser Eiter Streptokokken: dünnflüssiger gelbbrauner Eiter Pseudomonas: blaugrünlicher, süßlich riechender Eiter Escherichia coli: bräunlich, fäkulent riechender Eiter Putride (faulig, jauchige) Infektion flächenhaft ausbreitend, nekrotischer Gewebszerfall, faulig-stinkende schmierige Phlegmonen, z.B. Fourniersche Gangrän Fäulniserreger: Proteus vulgaris : stinkende Gase, feuchte Gangrän Anaerobe Infektion häufig unter großflächigen Nekrosen, durch Sauerstoffmangel z.B. Gasbrand, Tetanus, Clostridien Virusinfektion • Sehr selten • bewirken üblicherweise keine Wundinfektionen • z. B. bei Windpocken können Verletzungen bzw. Schädigungen entstehen, Probleme durch spätere Infektion mit Bakterien • Herpes Zoster (Gürtelrose) Pilzinfektion • • • • v.a. an den Füßen Beim diabetischen Fuß schwerwiegende Folgen Pilze können Infektionen auf Hautoberfläche verursachen können in vorhandener Wunde Infektion auslösen Symptome Lokal: Rötung (Rubor), Überwärmung (Calor), Schmerz (Dolor), Schwellung(Tumor), Funktionseinschränkung (Functio laesa); außerdem: verzögerte Wundheilung, Wundranderythem, fragiles ödematöses Granulationsgewebe, neue, zunehmende oder veränderte Schmerzen, Taschenbildung, unangenehmer Geruch, vermehrte Sekretion Systemisch: Lymphangitis CRP-Erhöhung, Leukozytose positive Blutkultur Fieber, Schüttelfrost, Übelkeit Tachykardie, Tachypnoe Diagnose, Wundbeurteilung Fachgerechte Beurteilung der infizierten Wunde ergibt die Behandlungsstrategie, die zur Kontrolle der Bakterienbelastung verfolgt werden kann Checkliste • 5 Kardinalsymptome, aber auch stark zerklüftete Wunden, diffus gerötete Wundränder oder ausgedehnte Wundtaschen • Lokalisation: Wunden im Sakralbereich sind z.B. durch die schlechtere Durchblutung und einer hohen Keimbelastung in diesem Bereich stark infektionsgefährdet • Ätiologie: äußere Einflüsse wie z.B. Stichverletzungen sind grundsätzlich als infektiös zu betrachten, Nekrosen –egal welcher Genese- = idealer Nährboden für Keime • Systemische Faktoren: geschwächtes Immunsystem, schlechter Allgemeinzustand, Malnutrition, maligne Tumoren oder hohes Alter hemmen die Immunantwort • Systemische Symptome: Positive Blutkultur, erhöhte Entzündungswerte oder Lymphangitis sind die häufigsten Zeichen einer manifesten systemischen Infektion Erregernachweis o Sachgemäß durchgeführter tiefer Abstrich und Abstrich vom Wundrand o Probeexcision (genauere Erkenntnis, Konsequenz??) Analyse des Wundkeimes und Erstellung eines Antibiogrammes Differenzierte Beurteilung und Therapie Aussagekraft von Wundabstrichen: Hinsichtlich Genauigkeit der qualitativen und quantitativen Aussagen bedeuten negative Ergebnisse nicht automatisch Keimfreiheit und positive Abstriche nicht zwangsläufig Wundinfektion „Routinemäßige Durchführung von mikrobiologischen Tests wird nicht empfohlen“ WUWHS Durchführung • oberflächliches Sekret und nekrotische oder fibrinöse Beläge mit NaCl entfernen • NICHT mit Desinfektionsmittel Abtötung der Infektionserreger Levine Technik • unter leichtem Druck aus einem ca. 1cm² großen Areal aus dem Zentrum der Wunde • Andruck bewirkt Exprimat von Wundexsudat Essener Kreisel • Entnahme in Spiralform ermöglicht es, die gesamte Oberfläche der Wunde zu untersuchen • Abstrichtupfer wird vom äußeren Wundrand beginnend kreisend unter Ausübung von leichtem Druck bis zum Zentrum der Wunde geführt Goldstandard, weil gesamtes Keimspektrum besser erfasst wird Behandlungsziele Voraussetzungen schaffen für eine erfolgreiche Therapie von infizierten Wunden durch o o o o o Erkennen, Mitbehandeln und Beheben der Ursachen sachgemäß durchgeführte Hygiene Wundbehandler auf aktuellem Kenntnisstand Qualität der verwendeten Produkte Sicherheit in deren Anwendung Prävention und Therapie von Wundinfektionen Die 5 Säulen der Therapie von Wundinfektionen 1. Wundrevision mit Säuberung und Spülung der Wunde, Inzision und Drainage 2. Debridement des nekrotischen Gewebes und Entfernung avitalen Gewebes 3. Nur bei phlegmonöser Ausbreitung systemische Antibiotikagabe kritische Überprüfung der Indikation, gezielte Auswahl nach Antibiogramm, hohe Dosis bei kurzer Dauer 4. Strenge Hygieneregeln „Die Wunde selbst ist nicht steril, deshalb ist steriles Arbeiten nicht nötig“ gilt nicht als Argument Gefahr zusätzliche Keime einzubringen Verbandwechsel mit Wundreinigung und –beobachtung im „non-touch-Prinzip“ physikalischen Therapie, Kompressionsverbände, Hochlagerung und Immobilisierung mit einbeziehen 5. Lokaltherapeutika: Antiseptika • • • • Nur in echter Infektionsphase, nicht langfristig ( 2-6 Tg.), nicht prophylaktisch Risiko einer Allergisierung steigt Wundheilung wird verzögert, Resistenzen Einwirkzeit beachten Silberprodukte • Schnelle Wirkungsentfaltung • Strenge Indikation • Bisher keine relevante Resistenzentwicklung, nicht zelltoxisch Unterdrucktherapie • Physikalisches Prinzip • Das geschlossene System nimmt Bakterien und Keime auf, verhindert Kreuzinfektionen sowie Keimausbreitung und ist deshalb gerade zum Einsatz bei infizierten Wunden gut geeignet Medizinischer Honig Antimikrobielle und wundreinigende Wirkung durch • Hohe Osmolarität • Produktion von WPO in nicht zytotoxischer Konzentration durch Glucoseoxidase • pH – Wert – Senkung • Zuckerabbauprodukt Methylglyoxal Larventherapie • • • • Verdauungssekret der Larven verflüssigt Nekrosen und Fibrinbeläge avitales Gewebe wird aufgesaugt und dient zur Ernährung Larven sondern antiseptische und antibiotische Wirkstoffe ab In larvalen Verdauungssekreten wurden Wachstumsfaktoren gefunden Welche lokalen Antiseptika soll man wann und wie lange verwenden? bei Vorliegen einer Wundinfektion Substanzen mit definierter antimikrobieller Wirkung, zur Reduktion von Mikroorganismen • Bei akuten infizierten bzw. kolonisierten Wunden kurzzeitig PVP-Iod- oder octenidinbasierte Antiseptika • Bei chronischen, schlecht heilenden Wunden Polyhexanide oder wirkstofffreie Wundspüllösungen, auch über längeren Zeitraum • ähnlich wie Antibiotika haben auch Antiseptika zelltoxische Komponente (Niedner 1995, Schopf et al. 1995) • Es besteht bei einigen eine Resorptionsgefahr Nutzen - Risiko - Abwägung Einwirkzeit der Antiseptika Octenisept – 1-2 Minuten ( max. 1 Woche ) (inkompatibel mit Jod!) Betaisodona – 5 Minuten ( max. 1 Woche ) Inaktivierung durch Blut und Eiter (inkompatibel mit Silber) Wundspüllösungen 2 Arten: a) chemisch (mit antibakteriellem Konservierungsmittel) oder b) physikalisch wirksam Zu a): z.B. Octenilin, Prontosan, Lavanid…. • Wirkungseintritt nach 5-20 Min. (!) d.h. Einwirkzeit beachten! • Wirklücken beachten • Keine Kombination mit Enzymen, Ölen… • Nicht an Sehne oder Knorpel, Trommelfell und in Bauchhöhle verwenden • Bessere Reinigungswirkung, da niedrige Oberflächenspannung Zu b) Natriumhypochloritlösungen z.B. Microdacyn • rein natürlicher, physikalischer Prozess: • Hypotone Lösung osmotisches Gefälle (nur bei Einzellern) zum Ausgleich strömt Wasser in die Zelle Platzen der Zellen („bubble burst effect“ – Osmolyse) • Hypochlorige Säure erhöht Zellpermeabilität bei einzelligen MO zerstört die Zellwand • Geruchsreduzierend, pH-neutral, nicht zelltoxisch • Ideale Reinigungswirkung nach mind. 10 Min. • anwendbar bei freiliegenden Gelenken, Knorpeln, Bändern und Sehnen, Innenohr, Bauchhöhle, im Auge • Keine Resistenzen, hypoallergen Hypertone Meersalzlösung Actimaris • Reaktiver Sauerstoff eliminiert Erreger, ohne Gewebe zu schädigen, auch zur Neutralisation von Wundgerüchen • basischer pH - Wert - kontrollierte Freisetzung des reaktiven Sauerstoffs • Meersalz kann günstig Zellmilieu und (Wund-) Stoffwechsel beeinflussen • erhöhter Salzgehalt unterstützt Ausschwemmung von Wundödemen TIPPS - Wundreinigung Mechanisch: • Tupfer, sterile Kompresse, Pinzette, Debrisoft • Wundspüllösung (RLA, NaCl 0,9%, Prontosan….) • Wischrichtung ! egal Nass-Trocken-Phase: • Reduktion und Ausschwemmen von MO, Zuführen von Feuchtigkeit • Lösen von Belägen und Verbandstoffresten Silberauflagen Geschichte Topische Substanz seit Hunderten von Jahren in der Wundversorgung Feste Elementarform - Silberdrähte Silbersalzlösung z.B. Silbernitratlösung - Reinigung Cremes/Salben mit Silberantibiotika (Silbersulfadiazin) = SSD-Creme (z.B. Flammazine) wirkt kurz, mind. 1x/Tag VW, Applikation zeitraubend + unsauber Jetzt: Wundverbände mit elementarem Silber oder Silber freisetzender Verbindung Einfach in Anwendung, können Ag freisetzen, weniger VW, zusätzlicher Vorteil z.B. Exsudatkontrolle….. Silberbestandteil von Verbänden o Als Beschichtung auf einer oder beiden Außenseiten des Verbandes (elementar oder nanokristallin) kommt mit Wunde in Berührung dort antimikrobielle Wirkung o Innerhalb der Verbandstruktur: als Beschichtung, in Zwischenräumen oder als Verbindung, die Teil der Struktur bildet z.B. Alginat Bakterien werden mit Exsudat absorbiert Wirkung im Verband, evtl. Diffusion in die Wunde o Als Kombination Es ist ungeklärt inwiefern Silbergehalt mit der klinischen Leistung zusammenhängt In Laborversuchen wurde gezeigt, dass bereits 1 ppm (Teil pro Millionen) wirksam ist Wirksamkeit Elementar nicht reaktionsfähig, Silberatome (Ag) müssen zu positiv geladenen Silberionen (Ag+) werden ionisieren in Luft schlechter als in wässriger Lösung Silberionen hochreaktiv an mehreren Stellen innerhalb der Bakterienzellen, führen zum Tod dieser durchbrechen bakterielle Zellwand unterbrechen Zellfunktion, indem sie sich an Proteine binden und Energieproduktion, Enzymfunktion und Zellreplikation stören Silberionen (in einer Konzentration von 10-9 bis 10-6 mol/l) wirken bakterizid, fungizid, viruzid und protozoizid ( auch Problemkeime wie MRSA, VRE) Indikationen: Gefährdete, kritisch kolonisierte und infizierte Wunden Als Keimbarriere bei Wunden mit hohem Infektions- oder Reinfektionsrisiko z.B. Verbrennungen Anwendungszeit Empfehlung der Konsensusgruppe: Zweiwöchige „Erprobungsphase“ und dann erneute Beurteilung von Wunde und Behandlungsansatz Wenn nach 2 Wochen: • Besserung zu sehen ist, aber Infektzeichen fortbestehen kann es klinisch gerechtfertigt sein, den Silberverband weiter zu verwenden • Keine Infektzeichen mehr zu sehen sind Absetzen des SV • Keine Besserung Absetzen des SV, Anwendung eines anderen antimikrobiellen Wirkstoffs und evtl. systemisches AB, Pat. auf möglicherweise unbehandelte Begleiterkrankungen untersuchen • Sobald Gesamtkeimzahl unter Kontrolle ist und sich Wunde bessert, sollte ein nicht antimikrobieller Verband in Erwägung gezogen werden DACC (Dialkylcarbamoylchlorid) – Cutimed sorbact • • • • nach dem Prinzip der hydrophoben (wasserabweisenden) Wechselwirkung ohne chemische Substanzen rein physikalisch Bakterien und Pilze sind von Natur aus hydrophob und binden sich deshalb irreversibel an die Wundauflage • mit jedem Verbandwechsel wird die Keimzahl reduziert • besteht aus Acetat- bzw. Baumwollgewebefasern, mit Dialkylcarbamoylchlorid (Fettsäurederivat)beschichtet • • • • keine Resistenzen keine zytotoxischen Nebenwirkungen keine Gegenanzeigen keine bekannten Allergierisiken AcetatKompresse Autolytisches Débridement von Belägen Bakterien werden irreversibel an Bakterien Cutimed Sorbact® gebunden und beim Verbandwechsel entfernt Anwendungsdauer: abhängig von der Indikation, max. 3 Tage Anwendungsempfehlung: • feuchtes Wundmilieu ist Voraussetzung für eine effektive Wirkung • Direkter Wundkontakt ist notwendig für effektive Bindung von Mikroorganismen • Bei tiefen oder kavitösen Wunden Kompressen oder Tamponaden verwenden • grüne Seite muss der Wunde zugewandt sein • Je nach Exsudatmenge mit hydroaktiven sekundären Wundauflagen kombinierbar Maden Larven, Biochirurgie Bei der Madentherapie werden Maden der Goldfliegenart Lucilia sericata dazu eingesetzt, chronische Wunden von nekrotischem Gewebe und Bakterienbefall zu reinigen. Der medizinische Einsatz wird durch die Besonderheit möglich, dass die Goldfliegenmaden sich ausschließlich von abgestorbenem Gewebe ernähren; intaktes Gewebe wird geschont Wirkungsweise Das Verdauungssekret der Larven verflüssigt Nekrosen und Fibrinbeläge avitales Gewebe wird aufgesaugt und dient zur Ernährung Larven sind in der Lage antiseptische und antibiotische Wirkstoffe abzusondern, die eine antimikrobielle Wirkung haben (auch MRSA oder ORSA) In larvalen Verdauungssekreten wurden Wachstumsfaktoren gefunden Enzymatische Wirkung Verschiedene Proteasen z.B. Trypsin, Chemotrypsin, Collagenasen Mechanische Wirkung „Mikrochirurgie“ • mit Hilfe der Mandibeln • Bewegung der Larven im Wundgebiet Antiseptische Wirkung Alkalischer pH Allantoin Aufnahme des Lysats und von Bakterien Antibakterielle Faktoren Applikationsformen BioBag • BioBag-Applikation wie bei einer „normalen“ Wundauflage • jederzeit zu Kontrollzwecken abnehmbar und wieder auflegbar • Biobag: kein Entkommen der Larven BioMonde Larvae - „Freiläufer“ Dosierung: ca. 10 Maden pro cm² Anwendung o Freiläufer mit Hilfe eines Netz-Käfigverbandes ausbruchsicher begrenzt o teebeutelartige Biobags o Wunde mit steriler Kochsalzlösung ausspülen, Maden mit steriler Pinzette auf Wundfläche legen. o Verband mit steriler Kochsalzlösung befeuchten, mit Gaze bedecken und mit durchlässiger Bandage fixieren. Verband soll nicht austrocknen o Sekundärverband soll Luftzirkulation zum Wundbett nicht einschränken. Sauerstoffzufuhr muss gewährleistet sein o Made höchstens 4 Tage auf der Wunde belassen, abnehmen und im Restmüll entsorgen Indikationen • • • • Diabetische Wunden Dekubitus Dehiszente, chirurgische Wunden Venöse Ulzera Therapiedauer: Je Zyklus: 3-4 Tage Entsorgung: im Handschuh zuknüpfen, Restmüll lokale Antibiotika obsolet!!!! Lokale Antibiotika gelangen durch Nekrosen oder andere Beläge nicht in Tiefe der Wunde, wirken deshalb nur oberflächlich führt zu Resistenzen zelltoxische Komponente hemmen Granulation blockieren ribosomale Proteinsynthese der Fibroblasten und Keratinozyten Sensibilisierung des Patienten Superinfektionen mit Pilzen Ausnahme: Gelenkschirurgie, sept. Knochen Zukunft Zunehmende Resistenzen der Bakterien adäquates Management von infizierten Wunden nötig Weitere klinisch-evidente Daten dringend zu fordern sensibler und kontrollierter Umgang mit antimikrobiell wirksamen Substanzen Lokaltherapeutika behalten auch weiterhin ihre Wirksamkeit Die Langzeitanwendung antimikrobieller Substanzen ist zu vermeiden „Die Geschichte lehrt andauernd, doch sie findet keine Schüler“ Ingeborg Bachmann FRAGEN???? DGKS Marianne Hintner Zertif. Wundexperte, VAC-Spezialist [email protected] Universitätsklinik Innsbruck Klin. Abteilung für Allg. und Chir. Intensivmedizin Traumatologische Intensivstation www.wundmanagement-tirol.at