17. Wärme und erster Hauptsatz
Werbung

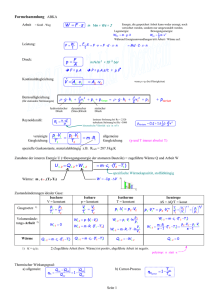
03.04.2014 17. Wärme und erster Hauptsatz 17.1 Wärmekapazität C Wärme war historisch schwer vorstellbar (Transport, ohne Materie ?). Modell: „Calorikum“ bis Mitte 19. Jahrh. Was ist Wärme ? Eine Form der Energie: Die Energie, die von einem System auf ein Anderes aufgrund einer Temperatur-Differenz übertragen wird. keine eigenständige physikalische Größe, sondern nur eine gleichwertige Form von Energie, wie z.B. die mechanische. Einheit: Wärme Q [Joule] [J], (historisch Kalorie [cal]) Beispiel: Abschrecken eines heißen Stahls in kaltem Wasser Q T1 T2 heisser Stahl T1 > T2 kaltes Wasser Im selben System oder 2 Systeme in Kontakt: Temperaturausgleich bis ein thermisches Gleichgewicht erreicht ist, d.h. T1 = T2 Körper 1 gibt Wärmemenge Q1 ab und kühlt dadurch ab; Körper 2 nimmt die Wärmemenge Q2 auf und erwärmt sich: Es muß gelten (Energieerhaltung): Q1 = Q2 = Q Ausgleich über: Wärmeleitung, -strahlung oder Konvektion (siehe 17.8) Welche Wärmemenge Q muss zu- / abgeführt werden um ein ΔT zu erzielen? Q C T vgl. elektrisch: Q C C Wärmekapazität mit Massetransport verbunden bei Wärme auch ohne Stofftransport möglich elektrisches Potential 17-1 03.04.2014 Bezogen auf die Masse: Q c m T mit c C m spezifische Wärme (-kapazität) Beispiel: cW 4,17 1 kg H2O; ΔT = 0°C auf 100°C; kJ kg K Q 1 kg 4,17 kJ 100 K 417 kJ kg K Welche Masse mCu muß ein Kupferblock mit T = 500°C besitzen, um 1 kg H2O von 0°C auf 100°C zu erwärmen? Die gemeinsame Endtemperatur beträgt T = 100°C. cCu 0,382 Q 417 kJ kg K 2,73 kg cCu T 0,382 400 kJ K mCu T 400C 400 K kJ kg K Molare Wärmekapazität, bezogen auf 1 Mol, d.h. konst. Teilchenzahl Wichtig: cm M c M Molmasse C n cm für n Mol c wird entweder bei konst. Druck (cp) oder konst. Volumen (cv) bestimmt. Eine Temperaturänderung hat vor allem bei Gasen auch eine Änderung des Drucks bzw. des Volumens zur Folge. Meisten Körper: Volumenausdehnung für T Q T aber auch V d.h. c p cv mechanische Arbeit (siehe 17.5) für V = const.: nur T für P = const.: V const : V und T, d.h. T ist kleiner als für V = const. mit Q = geg. und c p Q T 17-2 cp 03.04.2014 Für Festkörper und Flüssigkeit: c p cv geringe Volumenausdehnung (siehe 15.4.2) Für Gase : c p cv Tab.17.1: Wärmekapazitäten fester Stoffe bei 20°C und flüssiger Stoffe bei 25°C. cp / J kg-1 K-1 Stoff Beryllium C (Graphit) C (Diamant) Aluminium Eisen Kupfer Zink Molybdän Silber Gold Blei Al2 O3 SiO2(Quarz) CaF2 KCl Benzol (C6 H5 OH) Äthanol (C2 H5 OH) Methanol (CH3 OH) Quecksilber Wasser H2O: 1750 676 502 888 452 382 387 251 235 129 129 764 745 868 682 1740 2420 2550 140 4170 cp / J mol-1 K-1 15,80 8,12 6,03 24,00 25,20 24,30 25,30 24,10 25,30 25,40 26,80 77,20 44,76 67,70 50,80 135,90 111,50 81,71 28,10 75,12 sehr großes c : d.h. die pro kg gespeicherte Energie ist sehr groß Wärmespeicher Milderung von Temperturschwankungen am Meer (Meeresklima) c ist meist = f (T), für H2O jedoch sehr konstant. Nachteil: TDampf niedrig. Tab. 17.2: Spezifische Wärmekapazitäten von Gasen bei 25°C und 1 bar. Stoff He Ar Kr Xe H2 Cl2 N2 O2 CO2 cp [J/(kg K)] 5233 523 248 160 14300 473 1041 917 837 cp [J/(mol K)] cv [J/(mol K)] cp / cv 20,95 20,90 20,78 21,00 28,83 33,54 29,16 29,34 36,84 12,62 12,47 12,30 12,65 20,45 24,84 20,81 21,12 28,49 17-3 1,660 1,676 1,690 1,660 1,410 1,350 1,401 1,389 1,239 cp – cv [J/(mol K)] 8,33 8,43 8,48 8,35 8,38 8,70 8,35 8,22 8,35 03.04.2014 17.2 Latente Wärme, Umwandlungswärme lat.: latere = verbergen Versuch: Schmelzen von Lötzinn reversibel - Bereiche konstanter Temperatur trotz dQ const (konstante Wärmezufuhr) dt - Wärme wird nicht zur Temp.- Erhöhung genutzt, sondern für Phasenübergänge - Phasenübergänge: fest flüssig: Schmelz- energie Erstarrungs- energie flüssig gasförmig: Verdampfungs- energie fest QV [J/kg] Kondensation- energie gasförmig: Sublimations- energie Q m Qi QS [J/kg] QSub [J/kg] Kondensations- energie Qi materialspezifisch i: S, V, Sub fest flüssig gasförmig: Steigender Abstand der Moleküle/Atome Aufbrechen von Bindungen und Überwinden von Anziehungskräften (elektrisch). Keine Umwandlung der Wärme in kin.-Energie (Temp.-Erhöhung) sondern pot.-Energie 17-4 03.04.2014 Tab. 17.3: Schmelzpunkte und Siedepunkte sowie Schmelzwärmen QS und Verdampfungs- wärmen QV einiger Substanzen bei 103 mbar. (Die Werte für Kohlendioxid beziehen sich auf die Sublimation, da flüssiges CO2 bei Atomsphärendruck nicht existent ist). Substanz Schmelzpunkt / K Blei Brom Ethanol Gold Helium Kohlendioxid Kupfer Quecksilber Sauerstoff Schwefel Silber Stickstoff Wasser Zink 600 266 159 1336 1356 234 54,4 388 1234 63 273,15 692 QS / kJ kg-1 Siedepunkt / K QV / kJ kg-1 24,7 67,4 109 62,8 205 11,3 13,8 38,5 105 25,7 333,5 102 2023 332 351 3081 4,2 194,6 2839 630 90,2 717,75 2436 77,35 373,15 1184 858 369 879 1701 21 573 4726 296 213 287 2323 199 2257 1768 Beispiel: 1 kg Eis von T = -20°C in Dampf (T = 100°C) kJ kg K -20°C 0°C: c p 2,05 Q1 1 kg 2,05 fest flüssig : Schmelzwärme: QS = 333,5 kJ/kg 0°C 100 °C: c p 4,17 flüssig gas: Verdampfungswärme: Qv 2257 Eis kJ 20K 41 kJ kgK Q2 m Qs 333,5 kJ kJ kgK Q3 1 kg 4,17 100K 417 kJ kJ kg Q4 m Qv 2257 kJ Viel Energie für Phasenübergänge ! Hinweis: Wasserkühlung durch Verdunsten: Schwitzen des Körpers, Nähe von Gewässern, Spanische Tonkrüge, Ziegenschlauch Kondensation an kalten Körpern: Abgabe von Wärme a. d. kühlere Medium 17-5 03.04.2014 17.3 Innere Energie U Temperaturerhöhung eines Systems Zufuhr von Wärme höhere kin. Energie der Teilchen (Atome, Moleküle) höhere Energie des Systems. Das System bewegt sich jedoch nicht. Wkin = 0. Unterschied: Innere und äußere Energie Äußere Energieformen Wa: Translation - Kinetische Energie Wkin Rotation - Potentielle Energie Wpot z.B.: Bewegung einer Thermoskanne Innere Energieformen Wi: - thermische Energie (Wärme): Translation, Rotation, Schwingungsenergie der Moleküle / Atome (siehe kin. Gastheorie) - chemische Energie: potentielle Energie steckt in den Bindungen: exotherm oder endotherm; Phasenübergänge - nukleare Energie: Bindungsenergie im Kern: (Kernfusion, -spaltung) z.B.: heiße Flüssigkeit in einer Thermoskanne System: Wges Wa Wi Wa Wkin W pot mit Wi U innere Energie U Wges Wa U f (T , P, V , m) = Zustandsgröße wegunabhängig 17-6 03.04.2014 17.4 Erster Hauptsatz Annahme zur Vereinfachung: Geschlossenes System: Austausch von Wärme und Arbeit, kein Austausch von m Beispiel: Joules Experiment W Zufuhr von mechanischer Energie Das Rühren erhöht T und damit U Q Wpot Abgabe von Wärme (schlechte Isolation) Regel: (aus der Sicht des Systems) Zugeführte Energie: positiv Abgeführte Energie: negativ mit Wab 0 und Qab 0 : Bilanz der Arbeit: W Wzu Wab Bilanz der Wärme: Q Qzu Qab Gesamtbilanz: U Wzu Qzu Wab Qab Q W 1. Hauptsatz der Thermodynamik: Satz von der Energieerhaltung - Zufuhr: Sowohl in Form von Q (siehe Kap. 17.1) als auch als W - Im System: Alles wird als innere Energie U gespeichert, nicht als Wärme Q oder als mechanische Energie W. Nicht mehr unterscheidbar. U Wkin n k T 2 als „Temperatur“ gespeichert Annahme: ideales Gas, d.h. keine Chemie, geringer Druck n Anzahl der Freiheitsgrade (1-atomig: n=3) - Abgabe: U kann sowohl in Q oder W umgewandelt werden, hängt vom System ab. 17-7 03.04.2014 17.5 Volumenarbeit Annahme: beweglicher, reibungsfreier Kolben, ideales Gas, m = const. F P A mechanische Arbeit: dW F dx P A dx dV dW P dV aus der Sicht des Systems: Expansion: dV > 0 Arbeit abgeben dW < 0 Kompression: dV < 0 Arbeit aufnehmen dW > 0 Beispiel: Isotherme Expansion / Kompression V2 W12 P (V ) dV Expansion V1 V1 W21 P (V ) dV Kompression V2 Beispiel: Isoth. Expansion ( d.h. W12 < 0): für T = const mit U n k T U = const. 2 mit Wzu = Qab = 0 ΔU = 0 = W12 + Qzu W12 = Qzu Frage: Zufuhr von Wärme für isotherme Expansion wie groß ist Q12 auf dem Weg von 1 nach 2? für ideales Gas: P1 V1 P2 V2 n R T n Anzahl der Mole! 3 mögliche Wege: Sind U12, Q12, W12 wegabhängig? Alternativen 17-8 s.o. 03.04.2014 A) Weg 1: Weg 2: B) Weg 1: Weg 2: Prozeß Abgegebene mechanische Energie W12 Erwärmen für P1 = const: W1 P1 ( V2 V1 ) Isobare Expansion Abkühlen für V = const: W2 0 Isochore Abkühlung Gesamt W A P1 (V2 V1 ) Abkühlen für V = const: W1 0 Isochore Abkühlung Erwärmen für P2 = const: W2 P2 (V2 V1 ) Isobare Expansion Gesamt WB P2 (V2 V1 ) dWC P dV C) Isotherme Expansion: n R T dV V V2 1 V dV n R T ln 2 V V1 V1 dWC n R T Gesamt Ergebnis: Unterschiedliche Wege unterschiedliche Expansionsarbeit W12. Endpunkte gleich heißt keine Temperaturänderung gleiche innere Energie U. U Q W 0 Q W Folgt: unterschiedlich zugeführte Wärmemengen: ΔQA > ΔQC > ΔQB (= Fläche ΔW) W, Q keine Zustandsgrössen ! Wegabhängig ! U Zustandsgröße ! Wegunabhängig ! 17.6 Adiabatische Zustandsänderung Definition: Kein Austausch von Wärme mit der Umgebung (ideale Wärmeisolation). Näherung für sehr schnelle Prozesse ohne Temperaturausgleich (dauert). Q 0 U Q W U W die mechanische Arbeit (Expansion) wird durch Änderung der inneren Energie (d.h. T sinkt) bereitgestellt und umgekehrt. 17-9 03.04.2014 cP cV P V const Adiabatenkoeffizient T V 1 const T const P 1 Poisson Gleichungen vgl: Isotherme: dT = 0 dU = 0 Isochore: dV = 0 dW = 0 Isobare: dP = 0 Adiabate: dQ = 0 dW = dU 17.7 Kreisprozesse Definition: geschlossener Umlauf dU = 0 für ideales Gas da T = const nach einem Umlauf: (für ideales Gas wird U nur in Form von T gespeichert) z.B.: Ottomotor (einfache Näherung) a,c adiabatisch, d.h. dQ = 0 Wab b, d isochor, d.h. dV = 0 ΔW insgesamt abgegebene Arbeit Wzu 1. Rechtsläufig: a) Expansion: im Uhrzeiger im P-V Diagramm Abgabe von Volumenarbeit: c) Kompression: Zufuhr von Volumenarbeit Wab Wa P dV 0 dV 0 Wzu Wc P dV 0 dV 0 Bilanz der mechanischen Arbeit ΔW = Wzu + Wab < 0 : mehr Abgabe als Aufnahme 17-10 03.04.2014 b) Abkühlung: Qab < 0 Bilanz ΔQ > 0: mehr Wärmeaufnahme d) Erwärmung: Qzu > 0 U Wab Wzu Qab Qzu 0 <0 2. Linksläufig: >0 Bilanz: Arbeitsaufnahme und Wärmeabgabe Beispiel: rechtsläufig: linksläufig: 1. Hauptsatz Wärmekraftmaschine: Motoren Kältemaschine: Kühlschrank mit Kompressor Wirkungsgrad W einer Wärmekraftmaschine (Motor): W Nutzen verrichtete Arbeit Aufwand zugeführte Wärme Aufwand = Qzu zugeführte Wärme; insgesamt verrichtete Arbeit = W Wzu Wab abgeführte Qab ist verloren für den Kreisprozess! evtl. andere Nutzung (Kraft – Wärme Kopplung) U 0 W Qzu Qab W 0 verrichtete Arbeit aus der Sicht des Systems W Qzu Qab Q 1 ab Qzu Qzu mit Qab < 0 oder W 1 Qab Qzu W 1 W groß wenn Qab klein, d.h. kein Abkühlen ohne Abkühlen (Qab = 0) aber kein sinnvoller Kreisprozeß möglich: für identischen Rückweg mechanische Arbeit mit W = 0). d.h. W = 1 nicht möglich, d.h. nicht alle zugeführte Wärme Qzu wird in Arbeit W umgesetzt. 17-11 03.04.2014 Wärmereservoir zum Aufheizen (z.B. Benzin) Wärmekraftmaschine Kältereservoir zum Abkühlen (z.B. Kühler) 2. Hauptsatz: Es gibt keine periodische Maschine, die Wärme vollständig in mechanische Arbeit umsetzt. Stets gilt: ηW < 1 Idealfall: Carnot-Prozeß (Wärmekraftmaschine) Vollständig reversibler Prozeß und idealisiert maximal möglicher Wirkungsgrad, d.h. ideale Maschine (geht nicht real) zur Abschätzung des Grenzfalles: 1-2: isotherme Expansion dU = 0 QW WW P dV n R TW ln 3-4: n R TW dV V V2 V1 isotherme Kompression dU = 0 QK WK P dV n R TK ln 2-3: adiabatische Expansion dQ = 0: mit T V 1 const allgemein TW V2 1 TK V3 1 TW V3 TK V2 17-12 1 V3 V4 03.04.2014 4-1: adiabatische Kompression dQ = 0: TK V4 1 TW V1 1 TW V4 TK V1 1 Carnot Wirkungsgrad für reversible Prozesse mit W 1 Qab QZu W max 1 QK T 1 K QW TW in [K] ! = 1 nur für TK = 0 K: geht nicht (siehe Kap. 18.4.3: 3. Hauptsatz)) groß für TK /TW klein real: real Carnot 1 Ursache für nicht reversible Prozesse: z.B. Reibung, Turbulenzen, Nichtgleichgewicht Beispiele: Kohlekraftwerk 25 ... 50 % Dampfmaschine 3 ... 44 % Dieselmotor bis 45 % Ottomotor bis 37 % Elektromotor 20 ... 99,5 % Elektromotor mit Strom aus Kohle: 0,5 · 0,9 = 0,45 Carnot Kältemaschine (ideale Kühlschrank, Klimaanlage): an Umgebung linksläufig: Wärme QK aus dem Bereich mit niedrigerer TK (Kühlschrank innen) abführen QW in einen Bereich höherer Temperatur TW (Umgebung). Dazu muß Arbeit W verrichtet werden (Kompressor). aus Kühlraum 17-13 03.04.2014 Leistungszahl der Kältemaschine: abgeführte Wärme QK verrichtete Arbeit W K abgeführte Wärme aus dem Kühlraum = zugeführte Wärme QK zum Kompressor aus dU 0 W QW QK 0 K 1 QK QW QK QW 1 QK Für Carnot gilt (s.o.): QW TW QK TK K max TK 1 TW 1 TW TK TK Typ. Werte für einen Kühlschrank: ε 5 17.8 Wärmetransport 3 Arten: Wärmeleitung Konvektion Materie gebunden ohne Materietransport Wärmestrahlung ohne Materie mit Materietransport nur Energietransport In der Praxis Mischung aus allen drei Prinzip: Wärme Q strömt immer längs eines Temperaturgefälles = negativer Temperaturgradient 17-14 03.04.2014 17.8.1 Wärmeleitung Definition: Materiegebundener Transport ohne Materietransport. Vorherrschend in Festkörpern TW TK T T Temperaturgradient x Ausgleichsvorgang: Wärmestrom I dQ bis TW TK dt Thermodynamisches Gleichgewicht Es fließt nur Energie keine Materie ! Annahme: Stationärer Zustand oder Fließgleichgewicht: d.h. große Reservoire TW const; TK const z.B. TW = geheizte Wohnung und TK = Umgebung Physikalischer Mechanismus: Energieübertragung durch Atomstöße. In Metallen zusätzlich Unterstützung durch frei bewegliche Ladungen Beschreibung durch empirisches Gesetz: Wärmestrom: I dQ T A dt x Stromdichte: j T I x A W Q ist Wärme nicht elektr. Ladung W m 2 W spez. Wärmeleitfähigkeit m K 17-15 03.04.2014 Tab. 17.4: Spezifische Wärmeleitfähigkeiten bei Raumtemperatur Material W/(m·K) Material W/(m·K) Silber 428 Polyurethanschaum 0,024 Kupfer 400 Wasser 0,6 Stahl 14 - 40 Eis 0,59 Beton 0,19 – 1,3 menschl. Gewebe 0,2 Ziegel 0,84 Wolle 0,04 Holz 0,1 - 1 Daunen 0,025 Glas 0,7 – 0,9 Luft 0,023 = (T) jedoch konstant für Metalle im Bereich 0°C < T < einige 100°C im stationären Zustand gilt: I = const. ≠ f (t) T I damit: R Wärmewiderstand: x I R A x A K W U I R mit R vgl. elektrisch: l A Serienschaltung: T1 T2 T3 1) T1 T2 I R1 2) T2 T3 I R2 1) + 2) T1 T3 I R1 R2 n Rges R1 R2 ... Rn Ri i 1 Beispiel: Wärmedämmung 17-16 03.04.2014 Parallelschaltung: n 1 1 Rges i 1 Ri Beispiel: Thermographie Hausfront dunkel: kalt, hohes R hell: warm, kleines R Haus: T1 1 Fenster T2 aussen 2 Wand RHolz > RZiegel > RFenster + Vorhang > RFenster. Dach schlecht isoliert Frage: Warum ist die Sauna aus Holz und nicht aus Metall? Hohe Wärmeleitfähigkeit von Metall führt schnell Wärme zu (fühlt sich heisser an), Holz hat eine wesentlich niedrigere Leitfähigkeit. Metallische Gegenstände in der Sauna können Verbrennungen hervorrufen. Aufguß erhöht die Leitfähigkeit der Luft, „es wird wärmer“. 17.8.2 Konvektion Definition: Mit Materietransport verbundener Wärmetransport. Vorherrschend in Gasen und Flüssigkeiten. Beispiele: passive: Meeresströmung, Thermik aktive: Ventilator 17-17 03.04.2014 Mathematische Beschreibung sehr komplex und nur näherungsweise möglich. Wärmeübergang: Randschichten an der Grenzfläche fest – gas dort der größte Teil des Temperaturabfalls hängt ab von der Strömungsgeschwindigkeit Beispiele: Glasfenster: Erhöhung von R um bis zu 45% je Seite mit vLuft = 0. d.h. das Glas isoliert nur zu 10% Doppelverglasung: optimaler Abstand zwischen den Scheiben ca. 1 – 2 cm, sonst Konvektion; zusätzlich Vorhänge, Rollos reduzieren vLuft Wind Chill Faktor Vorteil von Daunen, Schäumen (kleine eingeschlossene Luftvolumen) 17.8.3 Wärmestrahlung Definition: Braucht keine Materie. Reiner Energietransport durch elektromagnetische Strahlung Emission: Abgestrahlte Leistung: Stefan – Boltzmann Gesetz PE e A T 4 e Emissionsgrad (materialabhängig) Stefan – Boltzmann Konstante = 5,67·10-8 A abstrahlende effektive Fläche T Temp. des Körpers [K] W m K4 Emission durch Elektronenübergänge im Festkörper Absorption: Leistungsaufnahme aus der Umgebung PA e A T04 T0 Umgebungstemperatur [K] Jeder Körper emittiert und absorbiert gleichzeitig: T > T0 Emission überwiegt T < T0 Absorption überwiegt PN e A T 4 T04 Nettostrahlungsleistung: 17-18 2 03.04.2014 Emissionsgrad: e gilt für Emission und Absorption. Jeder Körper emittiert und absorbiert gleich gut. e = 1: schwarzer Strahler (Körper) oder idealer Strahler e=0 sehr helle, reflektierende Oberflächen e= f (Wellenlänge ) Versuch: Strahlungswürfel Heizen mit heißem Wasser; Messen mit Termoelement 4 Flächen : Spiegel / Metall matt / Heizkörperfarbe / Schwarze Farbe: Meßwerte: 0,38 0,39 2,9 2,9 (gemessene Temp. nicht e) Wellenlängenabhängigkeit für schwarze Strahler: max Wien’sche Verschiebungsgesetz: max mm 2,898 T K (Verteilungsfunktion u(, T) siehe Kap. 19) Beispiele: maximal sichtbare Wellenlänge 800 nm Abstrahlung bei kleiner Temperatur nicht Tsichtbar > 500°C sichtbar, aber meßbar (Thermographie) Körpertemperatur: T 33°C = 306 K max 9,47 μm e (9,47 μm) 1 unabhängig von Hautfarbe d.h auch im sichtbaren Bereich nicht schwarze Strahler können im IR-Bereich schwarze Strahler sein 17-19 03.04.2014 Blau: kalt schlecht durchblutet Rot: warm gut durchblutet vorher Sonne: nach einer Zigarette max 500 nm T 5800 K Mitte des sichtbaren Spektralbereichs – Zufall ? Abgestrahlte Leistung: Pe 1350 J/(m2·s) Klarer Tag: PErde 1000 J/(m2·s) Absorbierte Wärme: Q J 1000 2 e A cos t m s Solarkonstante Aeff A cos Jahreszeiten: Aeff = f (Jahreszeit) 17-20