ZUR BEACHTUNG Aujeszky´sche Krankheit Aujeszky´sche
Werbung
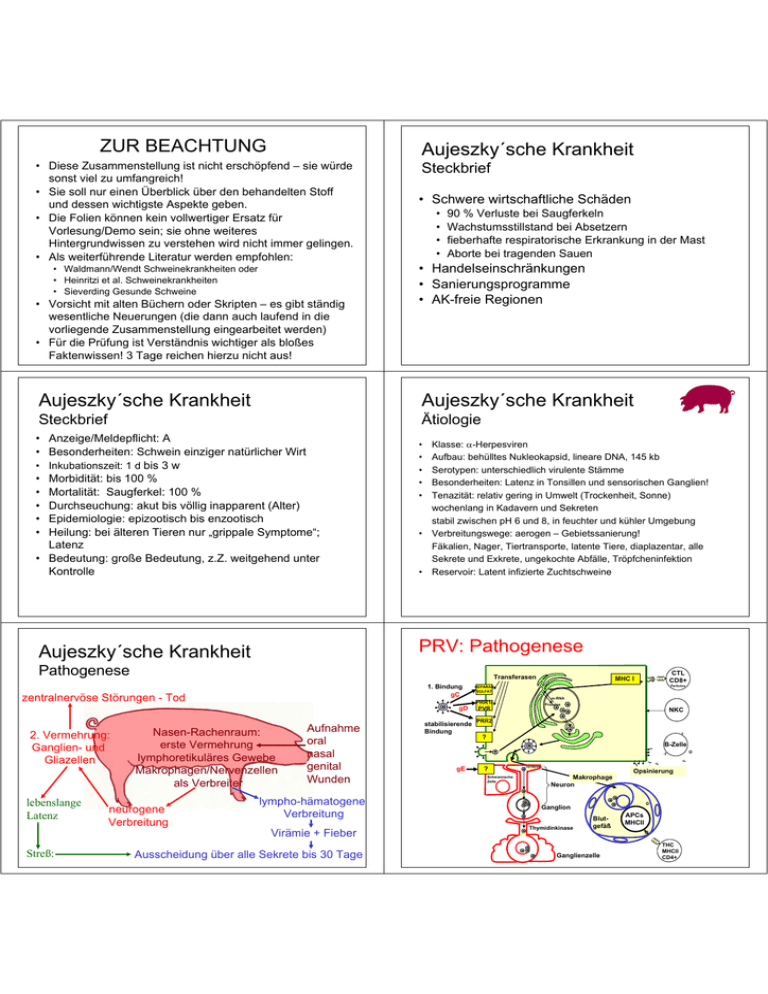
ZUR BEACHTUNG Aujeszky´sche Krankheit • Diese Zusammenstellung ist nicht erschöpfend – sie würde sonst viel zu umfangreich! • Sie soll nur einen Überblick über den behandelten Stoff und dessen wichtigste Aspekte geben. • Die Folien können kein vollwertiger Ersatz für Vorlesung/Demo sein; sie ohne weiteres Hintergrundwissen zu verstehen wird nicht immer gelingen. • Als weiterführende Literatur werden empfohlen: • Waldmann/Wendt Schweinekrankheiten oder • Heinritzi et al. Schweinekrankheiten • Sieverding Gesunde Schweine • Vorsicht mit alten Büchern oder Skripten – es gibt ständig wesentliche Neuerungen (die dann auch laufend in die vorliegende Zusammenstellung eingearbeitet werden) • Für die Prüfung ist Verständnis wichtiger als bloßes Faktenwissen! 3 Tage reichen hierzu nicht aus! Steckbrief • Schwere wirtschaftliche Schäden • • • • 90 % Verluste bei Saugferkeln Wachstumsstillstand bei Absetzern fieberhafte respiratorische Erkrankung in der Mast Aborte bei tragenden Sauen • Handelseinschränkungen • Sanierungsprogramme • AK-freie Regionen Aujeszky´sche Krankheit Aujeszky´sche Krankheit Steckbrief Ätiologie • Anzeige/Meldepflicht: A • Besonderheiten: Schwein einziger natürlicher Wirt • Inkubationszeit: 1 d bis 3 w • Morbidität: bis 100 % • Mortalität: Saugferkel: 100 % • Durchseuchung: akut bis völlig inapparent (Alter) • Epidemiologie: epizootisch bis enzootisch • Heilung: bei älteren Tieren nur „grippale Symptome“; Latenz • Bedeutung: große Bedeutung, z.Z. weitgehend unter Kontrolle • • • • • • • Klasse: α-Herpesviren Aufbau: behülltes Nukleokapsid, lineare DNA, 145 kb Serotypen: unterschiedlich virulente Stämme Besonderheiten: Latenz in Tonsillen und sensorischen Ganglien! Tenazität: relativ gering in Umwelt (Trockenheit, Sonne) wochenlang in Kadavern und Sekreten stabil zwischen pH 6 und 8, in feuchter und kühler Umgebung Verbreitungswege: aerogen – Gebietssanierung! Fäkalien, Nager, Tiertransporte, latente Tiere, diaplazentar, alle Sekrete und Exkrete, ungekochte Abfälle, Tröpfcheninfektion Reservoir: Latent infizierte Zuchtschweine PRV: Pathogenese Pathogenese Transferasen 1. Bindung gC gD neurogene Verbreitung lympho-hämatogene Verbreitung Virämie + Fieber Streß: Ausscheidung über alle Sekrete bis 30 Tage NKC stabilisierende PRR2 Bindung ? Y B-Zelle Y Aufnahme oral nasal genital Wunden Proteine + Y lebenslange Latenz Nasen-Rachenraum: erste Vermehrung lymphoretikuläres Gewebe Makrophagen/Nervenzellen als Verbreiter PRR1/ PVR Y 2. Vermehrung: Ganglien- und Gliazellen Perforine m-RNA gE ? Schwannsche Zelle Y Synapse Makrophage Neuron Opsinierung - Ganglion Thymidinkinase Y zentralnervöse Störungen - Tod CTL CD8+ MHC I HEPARAN SULFAT Y Aujeszky´sche Krankheit Blutgefäß Ganglienzelle APCs MHCII THC MHCII CD4+ PRV-Immunität 2 IL1 Th1 APCs IL4 Th2 Th0 IL2 IL4 Lympfoproliferation B-Zell-Proliferation Memory IFNγ (CD8+/CD4+) CTL (CD8+) humorale Immunität zelluläre Immunität IFNγ AK - klinische Symptomatik Hohe Antikörperproduktion aber unvollständiger Schutz Saugferkel Läufer ältere Tiere akut Tod innerhalb 24-48 Stunden, ohne charakteristische Symptome subakut Fieber, Anorexie, Erbrechen, Durchfall, Inkoordination, Krämpfe mäßiges Fieber,Anorexie, häufig subklinischer Verlauf, leichtes Fieber, respiratorische Symptome, bei tragenden Sauen Aborte,Fruchttod, mumifizerte Früchte bei Ebern Erbrechen, respiratorische Symptome, gering ZNS – Symptome, selten subklinischer Verlauf Inhaltverzeichniss Orchitis Protektive Immunität: CTL-vermittelt Aujeszky´sche Krankheit Klinik • • • • Aujeszky´sche Krankheit Klinik • Ferkel > 4 Wochen: – ähnliche Symptome schwächerer und langsamerer Verlauf – geringere Mortalität • Mastschweine: – – – – – – respiratorische Störungen Niesen, Nasenausfluß, Husten leichte Pneumonie, Dyspnoe Anorexie, Fieber, Verstopfung Hundesitz ungeordnete Bewegungen, Lähmungen, Schluckbeschwerden – Teilnahmslosigkeit! (Schlafkrankheit) • Sauen: – Aborte – Totgeburten/Mumien gleiches Entwicklungsstadium – subklinisch bei nicht Tragenden Neugeborene: Virämische Hyperthermie Zentralnervöse Störungen – unmotivierte Bewegungen mit gleichzeitig gestörtem Sensorium – klonische Krämpfe, Ruderbewegungen in Seitenlage, Ophistotonus – Krämpfe der Kaumuskulatur, Schluckbeschwerden starkes Speicheln – Ausfallerscheinungen, Ataxie, Paralysen Hintergldmße – Tod nach wenigen Tagen Plötzliche Todesfälle Aujeszky´sche Krankheit Aujeszky´sche Krankheit Sektion Histologie • • • • • • • minimale, oft unentdeckte Läsionen nicht-eitrige Meningo-Encephalitis seröse-fibronekrotische Rhinitis, Laryngitis, Tracheitis nekrotische Tonsillitis mit Lymphadenitis Lunge je nach Sek.Erreger - Ödem, fokale Nekrosen - Hämorrhagien miliare Nekrosen (2-3 mm) • Endometritis, nekrotisierende Plazentitis • • Meningo-Panenzephalitis mit perivaskulären mononukleären (nicht-eitrigen) Infiltraten Ganglienzelldegeneration Einschlußkörperchen • • Fokale Nekrosen interstitielle Pneumonie – Ganglien, Epithelien – Lunge, Leber, Milz Aujeszky´sche Krankheit Aujeszky´sche Krankheit Diagnose Erregernachweis • rasche Ausbreitung+hohe Morbidität • Klinik: Ataxie, Krämpfe, gestörtes Sensorium • Sektion: fokale Nekrosen in Organen – nicht-eitrige Meningo-Enzephalitis • Serologie: ELISA • Virusnachweis: zytopathogener Effekt • Bestätigt: • Serologie: AK erst nach 10 Tagen • Virusisolation: – – – – – 2-3 akute Tiere ZNS, Milz, Lunge, Nasentupfer Zellkultur – zytopathischer Effekt –IFZ Dauer: 2 – 5 d; 2 Blindpassagen für neg. Beweis FATS: Dauer 1 h, Tonsillen-Sektion – 1. Klinik + Serologie positiv – 2. Virus- oder Ag-Nachweis – 3. Histologie + Serologie Labordiagnostik AK-ELISA; SNT Feldvirusnegativ; ungeimpft Feldvirusnegativ; gI- -geimpft Feldviruspositiv; ungeimpft Feldviruspositiv; gI- -geimpft AK – Differentialdiagnose AK gI-ELISA Schwein ZNS Störungen + + + + + Inhaltverzeichniss • • • • • • KSP Kolienterotoxämie Kochsalzvergiftung Enterovirus-Enzephalomyelitis (Teschen/Talfan) Ferkelzittern Streptokokkenmeningitis AK – Differentialdiagnose Schwein Respiratorische Symptome • Influenza • andere virale oder bakterielle Infektionen; da die Vermehrung des AK-Virus in der Lunge andere Infektionen begünstigt, ist AK bei allen länger andauernden, schwer therapierbaren respiratorischen Erkrankungen grundsätzlich auszuschließen 4.2.2 AK – Differentialdiagnose III Schwein Reproduktive Störungen • • • • • • KSP PRRS Parvo/Enterovirusinfektion Influenza Brucellose Leptospirose Inhaltverzeichniss Aujeszky´sche Krankheit Aujeszky´sche Krankheit Differentialdiagnostik Therapie • Sensorium meist ungestört: • keine Therapie möglich • • • • • Zitterkrankheit der Ferkel Streptokokkenmeningitis Colienterotoxämie atypische ESP: Paresen Teschener Krankheit: Paresen Hi-Gldmße • Sensorium gestört: • Hypoglykämie der Saugferkel • keine Ausbreitung im Bestand • Kochsalzvergiftung • auch adulte Tiere betroffen • Fruchtbarkeitsstörungen: • PRRS, Brucellose • Leptospirose, Parvo- Enteroviren (SMEDI) Aujeszky´sche Krankheit Immunität und Impfung (Theorie!) • belastungsfähige Immunität in kleinen Beständen • kolostrale AK schützen ca. 12w gegen Klinik • markierter Impfstoff vorhanden - zur Zeit nicht eingesetzt - Impfung nur nach Anordnung durch Vet.Behörde - Suvaxyn AujeszkyBartha - Ingelvac Aujeszky MLV • Schutzimpfung Ferkel erst ab 10. LW (Kolostrum) Mastschweine bei Einstallung impfen • Problem: Impfung kann Infektion kaschieren und Latenz nicht dauerhaft unterdrücken • Impfung verboten!!! Aujeszky´sche Krankheit Sanierung • 1980: AK wird anzeigepflichtig (VO zum Schutz gegen AK) • 1993: 4. VO: Bundesweite Tilgung als Ziel • endemisch verseuchte Gebiete (Kategorie III): Sanierungsprogramm • flächendeckende Schutzimpfung für 2 Jahre: alle Schweine ab 10. LW • Sanierung unter Impfschutz (Impfen + Serologie + Ausmerzen) • Merzung der letzten AK-positiven Tiere (ohne Impfung) • Gebiete mit regionaler AK (Kategorie II): Sanierung durch Merzung seropositiver Tiere evtl. Impfung (Marker: gE) • seuchenfreie Gebiete (Kategorie I): Schutz vor Einschleppung keine Impfung flächendeckende Kontrolluntersuchung • Bei Freiheit (negative Serologie): Impfverbot + Serologie 1 Jahr Beobachtungszeit • Anerkennung als AK-freie Region (Artikel 10 (RL 97/12 EU) : seit April 2003 ganz Deutschland Aujeszky´sche Krankheit Aujeszky´sche Krankheit Sanierung Probenschlüssel Zuchtbetriebe • Maßnahmen zum Erhalt der Artikel-10-Gebiete • • • • • Keine Impfung erlaubt Zukauf nur aus Artikel-10-Gebieten (RL 97/12 EU) Lückenlose Bestandskontrolle (SHHVO) Serumproben bei Verdacht kein Zukauf geimpfter Tiere • Hessen: • Impfverbot seit 1.4.2000 • letzter positiver Reagent: 21.12.1999 • Serumkontrolluntersuchungen 1x/Jahr und Betrieb (Hessen) Betriebsgröße 1 - 20 21 - 25 26 - 100 >100 Probenzahl alle 20 25 30 Aujeszky´sche Krankheit Aujeszky´sche Krankheit Probenschlüssel Mastbetriebe Sanierung Betriebsgröße 1 – 10 Anzahl Poben alle, max. 8 11 – 20 10 21 – 30 11 31 – 60 12 61 – 200 13 >200 14 • 1. Warum mussten positive Sauen im Bestand gemerzt werden, obwohl der Rest geimpft ist? • Impfung = Schutz vor Klinik, nicht vor Infektion! • Spätere Ausscheidung des Feldvirus möglich! • Streß, Krankheit • intra-uterine Infektion: Vermehrung in Früchten, Latenz und Dauerausscheidung der Ferkel • das erklärt auch, daß in Impfbeständen immer wieder AK-positive Tiere gefunden werden • 2. Wie kann der AK-freie Status erhalten werden trotz Zukauf? • JS und JE nur aus amtlich anerkannten AK-freien, bzw. Art.10 Betrieben Aujeszky´sche Krankheit Sanierung • 3. Bringt die Sanierung von Einzelbeständen Erfolg? • Nein! Sehr gute aerogene Übertragbarkeit (mehrere km im Umkreis von Mastställen. Ständige Neuinfektionen • Gebietssanierung! • 4. Problematik der Sanierung im geschlossenen System? • Ständige Reinfektion der Sauen aus dem Mastbereich (JS, Verschleppung) • Empfehlung: zeitweiliger Verkauf aller Ferkel • 5. Nur noch wenige AK-positive Tiere im Betrieb – wie beendet man Sanierung (15 % Marke)? • am besten alle sofort merzen – teuer • strikte Abtrennung der positiven und mit dem Absetzen abschaffen • strikte Impfung so lange diese noch erlaubt ist schützt Restbestand vor Ansteckung Klassische Schweinepest Klassische Schweinepest Steckbrief • hoch variable septikämische Seuche • massive volkswirtschaftliche Schäden – direkte Schäden – Handelsbeschränkungen • 1. hohe Saugferkelverluste • 2. fieberhafte Enteritiden bei älteren Ferkeln • 3. unspezifische Erkrankung älterer Tiere Klassische Schweinepest Ätiologie • Familie: Flaviviridae, Gattung: Pestivirus • behülltes, ikosaedrisches RNA-Virus • Tenazität: • • • • • Monate bei niedriger Temperatur partiell bis 56°C pH stabil zwischen 3 und 11 stabil nach Pökeln und Räuchern wenige Tage bei Fäulnis • Desinfektion mit starken Laugen und organischen Säuren • NaOH (2%), Cresol, Formalin (1%) • atypischer Verlauf! oft nur Einzeltiere betroffen! Klassische Schweinepest KSP-Virusinfektion Klinischer Verlauf W1 W2 W3 W4 W5 W6 Besonderheiten • Inkubationszeit beim Einzeltier ca. 1 Woche Herdeninkubationszeit 3-6 Wochen Wochen nach Infektion 1 INFEKTION 2 3 4 5 6 akute Erkrankung <4 Wochen ANTIKÖRPER Rekonvaleszenz FIEBER VIRÄMIE Inkubation • Virämie schon während der Inkubation (1-4 Tage vor Fieberbeginn) "atypische" Symptome Rekonvaleszenz "typische" Symptome Monate vor Geburt 3 Tod • Klinisches Krankheitsbild ist stark altersabhängig 2 Antikörper >4 Wochen Aborte Totgeburten Frühsterblichkeit Fieber "atypische" Symptome Depner, Mönnig, Liess, 1996 Klassische Schweinepest Klinik Klinik Anorexie, Lethargie, Fieber (41°C) Multifokale Hyperämie + Hämorrhagien Zyanosen der Haut Konjunktivitis Konstipation im Wechsel mit Diarrhoe Husten und Dyspnoe Ataxie, Lähmungen, Krämpfe enge Kontaktsuche Tod nach 5 bis 15 Tagen Mortalität 0 bis 100% Leukopenie Thrombozytopenie ...11 Ak. Klassische Schweinepest – – – – – – – – – – – – 2 VIRÄMIE Inkubation • Akute Form 1 Virämie M1 M2 M3 Monate nach Infektion chronische 1 2Erkrankung 3 • Die vielfältigen klinischen Bilder sind in großem Maße Wirts- und Umweltfaktoren zuzuschreiben und weniger der Erregervirulenz Monate nach Geburt 1 Persistent-virämische Nachkommen • Chronische Form – – – – Lethargie wechselnder Appetit Fieberschübe Diarrhoe • bis zu 1 Monat • therapieresistent • wechselnd mit Fieberobstipation – – – – – – unspezifische Allgemeinsymptomatik Scheinbare Erholung, Rückfall, Tod (152) hohe Aufzuchtverluste Fertilitätsstörungen Leukopenie Thrombozytopenie Klassische Schweinepest Klassische Schweinepest Klinik Klinik • Kongenitale Form – – – – – – – Lebensschwäche Tremor (Ferkelzittern) Kümmern Tod nach Wochen bis (11) Monaten oft auch klinisch normal virämische Dauerausscheider keine Antikörper • Atypische Form – oft symptomlos – v.a. ältere Tiere – vorrübergehend: • Fieber und Inappetenz • Kümmerer – Schlechte Leistung • Resorption, Fruchttod • Totgeburten, SMEDI • selten Aborte – Symptome von Sekundärinfektionen dominieren Klassische Schweinepest Klassische Schweinepest Pathologie Pathologie • Akute Form • Akute Form – Petechien und Ekchymosen • Haut, Lnn, Kehlkopf, • Harnblase, Nierenkapsel – Hämorrhagische Infarzierung • Milzrand – nichteitrige Meningoencephalitis • perivasculäre Infiltration Klassische Schweinepest Klassische Schweinepest Pathologie Pathologie • Chronische Form • Entzündungsanzeichen und Hämorrhagien meist fehlend • „Boutons“ in Colon + Caecum • generalisierter Verlust lymphatischen Gewebes • degenerative Veränderungen: Gefäßwänden und Lymphknoten + nichteitrige Meningoenzephalitis • Lymphozyto- + Thrombozytopenie • Kongenitale Form – – – – – Zentrale Dysmyelinogenese Kleinhirnhypoplasie Microencephalie Hydrops fetalis Mißbildungen Klassische Schweinepest Klassische Schweinepest Differentialdiagnostik Differentialdiagnostik • Septikämie mit Hyperämie und Petechien • ASP: • Salmonellose, Rotlauf, APP, Pasteurellose, Eperythrozoonose, Streptokokken-Infektion, Leptospirose, Cumarin-Vergiftung • keine Unterschiede in Klinik und Sektion Î Erregernachweis • Ink.-Zeit: 5 - 15d • Irido/Poxviren?; • Iberische Halbinsel; Lederzecken, Fleisch 7 M • perakut: hohes Fieber, • Fieber das nicht auf AB anspricht: • AK, Influenza, PRRSV, S.typhimurium DT104 • AK, Colienterotoxämie, Streptokokkenmeningitis, Glässersche Krankheit: • Apathie/Reizerscheinungen, gestörtes Sensorium • Blutungen: Nase und After • 1 - 2d, dann 100 % mortal • erhaltenes Sensorium: • ESP, Teschener Lähmung, Hg, Maulbeerherzkrankheit • akut: 3 - 4d 41°C, Cyanose nach 1w; Dyspnoe, blutiger Durchfall, Erbrechen; 90 - 100 % mortal • chronisch: = ESP • PRRSV • Fieber + Pneumonie + Aborte • weder ZNS-Symptome, noch Leukopenie • Serologie positiv: • Border Disease, MD/BVD Klassische Schweinepest Klassische Schweinepest Differentialdiagnostik Differentialdiagnostik Immunkomplexvermittelte PDNS - Sektion – Gefäßerkrankung und – Glomerulopathie – (Typ III-Hypersensitivität) • • • • Systemische, Gefäßnekrosen! • Petechien auf Organen • Lymphknoten hämorrhagisch infiltriert und angeschwollen • Milzrandinfarkte • Glomerunonephritis! • Lymphozytendepletion • Histiozytose Sektionsbild entspricht ESP max. 1 – 20 % des Bestandes betroffen 11. – 14. LW; 20 – 65 kg KG PDNS - Klinik • Petechien und Ekchymosen • v.a. Perianalbereich und zwischen Hinterschenkeln • nur wenige Tiere betroffen • Blässe, Kümmern, PMWS • hohe Mortalität • Blutharnstoff und Creatiningehalte Klassische Schweinepest Pathogenese II. Virämische Phase Klassische Schweinepest KSPV Ausbreitung zu sekundären Replikationsorten Endothelzellen Pathogenese Endothelzellen Aufnahme, Lymphozyten GALT Makrophagen Knochenmark Milz III. Organphase Thrombozyten primäre Vermehrung in Tonsillen Makrophagen I. Lymphoretikuläre lymphatische Phase Ausbreitung: ausgeprägte Replikation Thrombozyten Lymphozyten Granulozyten Makrophagen Nekrose und Apoptose • Multiorganversagen Herz-KreislaufBlutungen versagen Tod Immunsuppression - Sekundärinfektionen Fieber Endothelschäden Azidose Hypotension Complement -Aktivierung DIC „Kümmern“ - Pneumonien, Diarrhoe Aktivierung überschießende Entzündungskaskade „CytokinSturm“ Pathogenese Teil II Diagnostik Abklärungsuntersuchung Einzeltier AM TNFα • anhaltende, oft geringe Temperaturerhöhung, mehrere Tiere betroffen, AB-Resistent • ZNS-Symptome (Ataxie, Schwanken, Parese) • Durchfall (kariöser Geruch) + Fieber • SMEDI • anhaltende Leukopenie (Neutropenie ohne LiVerschiebung < 10 G/l) • Hautpetechien und Nekrosen (selten, aber typisch) nach Dr. A. Elbers, Wageningen Diagnostik Verdacht auf KSP Abklärungsuntersuchung Bestand weiterführende Unt.suchg. nach §8 SchHalHygV, Anlage 6 • gehäuft Todesfälle innerhalb 7d Großbetriebe Sonstige Ferkel >10 % >20 %(min5) Aufzucht 3% 5 %(min3) • Klinik oder Pathologie oder Serologie lassen Ausbruch der KSP befürchten Mast/Zucht 3% 5 %(min2) • gehäuft Kümmerer Großbetriebe: aufgezogene Ferkel, letzte 10 Würfe, 7% oder 30 Kleinbetriebe: 15 Î ANZEIGEPFLICHT (§ 9 Abs. 1 Tierseuchengesetz) • fieberhafte Erkrankungen ab 40,5°C innerhalb 7d Großbetriebe: mehr als 10 %, mind. 30 Tiere Kleinbetriebe: Mast/Aufzucht: 10 %, (min.10); Zucht: 10 %, (min. 3) • Zuchtbetriebe ab 3 Sauen: innerhalb 4 Wochen: Umrauscher > 20 %; Aborte > 2,5 % Ausbruch der KSP gilt als festgestellt: • Erstausbruch: – durch virologische Untersuchung: Virus-, Antigen- oder Genomnachweis Labordiagnose der KSP Virologische Testverfahren Kriterien Virus Isolierung FAT Antigen ELISA Dauer 3 - 10 Tage 1 Tag 1 Tag 1 Tag Probe Blut, Organe Organe Blut, Organe Blut, Organe Vorteil zuverlässig, hohe Sensitivität schnell schnell schnell, hohe Sensitivität Nachteil zeitaufwendig Interpretation oft schwierig geringe Sensitivität Kontaminationsgefahr Anwendung Bestätigungstest Massen- und EinzeltierUntersuchung MassenUntersuchung Massen- und EinzeltierUntersuchung • Sekundärausbruch: durch – Klinik, Pathologie, und Epidemiologie oder durch – Serologie und Epidemiologie PCR Labordiagnostik KSP Labordiagnostik KSP Virusnachweis (Virämie) Nachweis von Antikörpern • 1-4 Tage vor Fieberbeginn (Inkubationszeit) • ab 3. Infektionswoche • bis zum KSP-bedingten Tod • in und nach Rekonvaleszenz • bis zur Rekonvaleszenz • Terminalphase (3.-5. Infektionswoche) – akut erkrankte Tiere (niedrige Titer) • 3. bis 5. Infektionswoche – chronisch erkrankte Tiere Labordiagnostik KSP Hochrisikoperiode (HRP) Terminierung der Infektion Zeitspanne zwischen dem Eintrag der Infektion in ein KSPV-freies Land bei Hausschweinen und dem Erkennen des ersten Ausbruchs • Virusnachweis +, Antikörper – erste Woche (evtl. Impfstoff [Wildschwein] – frische Infektion Vereinigtes Königreich Niederlande Belgien Deutschland Niederlande Spanien Vereinigtes Königreich Irian Jaya Papua New Guinea Deutschland • Virusnachweis +, Antikörper + – mittelalte Infektion (um 18 Tage) • Virusnachweis -, Antikörper + – Infektion mind. 3 Wochen alt Î weite Verbreitung zu erwarten! Bedeutung der Früherkennung Zuchtbetrieb Ferkelerzeuger KSP-typische Symptome 50 langsame Ausbreitung in Herde erst jetzt auffälliges Bild Î Verdacht 45 40 35 % Infizierte tragende Sau infiziert: selbst unempfindlich geringe Ausscheidung kaum Symptome 30 25 20 15 HPR (in Wochen) 4 6 3 8 6 9 8 > 12 > 16 10 Bedeutung der Früherkennung • KSP oft erst Wochen nach Auftreten erster klinischer Symptome entdeckt • späte Erkennung der Infektion: – Verbreitung des KSP-Virus – Gebiete mit hoher Schweinedichte! 10 5 0 1 6 W später: Geburt Kolostralschutz 1 Tier persistent (1986) (1992) (1993) (1997) (1997) (1997) (2000) (2004) (2004) (2006) 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 Wochen p.i. Î Früherkennung – entscheidendes Element zur • Kontrolle und Eradikation persistentes Ferkel als Absetzer: infektion anderer Tiere (andere Bestände?) Früherkennung der KSP durch aktives Monitoring? serologisches Screening für Frü Früherkennung ungeeignet (Stegemann et al. 1999): • Serokonversion erst ø18 Tage p.i. • Verdoppelung der infizierten Tiere in Zuchtbetrieben alle 6,4 Tage Î Infektion, wenn überhaupt, erst spät erkannt Î Früherkennung KSPV-Infektion • labordiagnostische Abklärung erster klinischer, auf Schweinepest hindeutender Anzeichen Voraussetzungen • sorgfältige Gesamtbestandsuntersuchung • Kenntnisse der klinischen Verlaufsformen • Kenntnisse zur Epidemiologie der KSP Richtungen des Monitoring KSP im Betrieb Früherkennung Virologisches Screening 1. ohne klinische oder epidemiologische Hinweise ungeeignet: • • Nachweissicherheit: Funktion der Prävalenz Prävalenz ohne Klinik/Patho/Epidemiol. zu gering! Î INDIKATORTIERE! 2. Infektion zwar früher erkannt • aber relativ enges Zeitfenster (2 – 3 Wochen) Welche Schweine einbeziehen? • aufgrund des Vorberichtes Verdächtige • „atypisch“ Erkrankte - Spätform (Kümmerer) - chronisch Kranke • Nachbartiere der Erkrankten • Neuzugänge der letzten Wochen • Muttertiere/Zuchteber • Neugeborene Ferkel (bis 2 Tage alt) Klassische Schweinepest Epidemiologie • Reservoir: nur Haus- und Wildschwein • Übertragung: Einschleppung "Rückverfolgung" Verschleppung "Vorwärtsverfolgung" - guter Vorbericht - gründliche Bestandsuntersuchung - richtige Beprobung - Serologie/Virologie - Molekularepidemiologie (Genotypisierung) • direkte Tierkontakte, alle Sekrete und Exkrete • ab 1-2 Tage p.i. bis über Monate (Dauerausscheider möglich) • • • • Personen (Tierarzt!), be- und unbelebte Vektoren Speiseabfälle Transplazental Wildschweine als Reservoir und Überträger • Kontakt über Weide- bzw. Auslaufhaltung • Kontamination von Futtermitteln und Einstreu in Außenlagerung • Jäger als Verbindungsglied zwischen Haus- und Wildschweinen • Entsorgung von Ferkel über den Mist • Speise- und Küchenabfälle • Einfuhr von gefrorenem kontaminiertem Wildschweinefleisch • Jagdabfälle als Kirrung Einschleppung des KSP-Virus in die Seuchenobjekte 1993 - 2007 Primärausbrüche (n = 111) Folgeausbrüche (n = 249) Schwarzwild Tierverkehr unbekannt 60,0 % 28,1 % 23,7 % 24,1 % 18,0 % 8,4 % 22,0 % 15,7 % unbekannt Nachbarschaft Fahrzeugkontakt Speiseabfall Fehler die zu Problemen in der Erkennung und Bekämpfung der KSP führen • Betriebsebene: - Unzulänglichkeiten in der Dokumentation (Bestandsregister) - lückenhafte Tiergesundheitskontrolle - Eigenbehandlungen ohne bzw. mit zu später Heranziehung des Betreuungstierarztes - Missachtung rechtlicher Vorgaben - Abgabe von Tieren trotz Vorliegen ungeklärter klinischer Erkrankungen im Bestand Personenkontakt Fehler die zu Problemen in der Erkennung und Bekämpfung der KSP führen • Tierärztliche Überwachung und Betreuung: - Therapieempfehlung und/oder Arzneimittelabgabe ohne Bestandskontrolle - statt Gesamtbestandskontrolle nur Untersuchung eines Teilbestandes - Diagnostischer Blick Î Unterlassung differentialdiagnostischer Abklärungsuntersuchung bei scheinbar eindeutiger Symptomoatik (z.B. Morbus Glässer) - Überschätzung eines KSPV-negativen Stichprobenergebnisses bei Weiterbestehen des Krankheitsgeschehens - keine Einsendung von Untersuchungsmaterial bei erhöhter Mortalität - ungenügend zielgerichtete Auswahl zu beprobender Tiere KSP-Ausbrüche weltweit 2007 Epidemiologische Screening-Ergebnisse und aktuelle Situation Letzter Stand Hausschweinepest in Deutschland Anzahl Fälle KSP bei Haus- und Wildschweinen in Deutschland (1993 bis 2007) 900 800 700 600 500 400 300 200 100 0 812 100 116 1993 173 52 1995 234 4 208 119 44 11 6 1997 5 2001 11 137 2003 03 024 2005 Hausschwein Morbidität verendet Mortalität 75 19.74 75 100 getötet 305 03.03.2006 Haltern/Reckl. 195 35 17.95 9 25.71 186 46.67 1169 Haltern/Reckl. 81 0 0 0 1183 30 2.54 14 01.04.2006 Raesfeld 242 24 9.92 24 100 218 01.04.2006 Haltern/Reckl. 600 2 0.33 2 100 598 844 12 0 04.05.2006 Borken 2232 0 0 0 2007 09.05.2006 Borken 749 200 26.70 15 7.5 734 Summe/Durchschn. 5662 366 6.46 139 37.98 5523 Zeitraum nach Teuffert und Deppner, LFI erkrankt 380 Haltern/Reckl. 373 2 Tiere Haltern/Reckl. 04.03.2006 174 1999 Ort 01.03.2006 27.03.2006 451 412 289 Ausbruch 81 2232 Wildschwein Letzter Stand Hausschweinepest in Deutschland Anzahl der in Deutschland im Zusammenhang mit dem Seuchengeschehen 1993 bis 30.09.2007 getöteten Schweine Ausbruch Ort Tiere erkrankt Morbidität verendet Mortalität 01.03.2006 Haltern/Reckl. 380 75 19.74 75 100 getötet 305 03.03.2006 Haltern/Reckl. 195 35 17.95 9 25.71 186 04.03.2006 Haltern/Reckl. 81 0 0 0 81 27.03.2006 Haltern/Reckl. 1183 30 2.54 14 46.67 1169 01.04.2006 Raesfeld 242 24 9.92 24 100 218 01.04.2006 Haltern/Reckl. 600 2 0.33 2 100 598 04.05.2006 Borken 2232 0 0 0 09.05.2006 Borken 749 200 26.70 15 7.5 734 Summe/Durchschn. 5662 366 6.46 139 37.98 5523 2232 insgesamt getötete Schweine: 120.000 22 Mio. € direkter Schaden Insgesamt Ø pro Ausbruch Ausbrüche der Schweinepest Anzahl Betriebe Anzahl Schweine 360 425.602 1.182 Prophylaktische Räumungen Anzahl Betriebe Anzahl Schweine 2.493 806.088 6,9 2.339 Abgabe gegen Zahlung von Beihilfen Anzahl Mastschweine Anzahl Ferkel 1.016.276 299.804 2.895 854 Insgesamt 2.547.770 7.077 Rechtliche Grundlagen • Maßnahmen zur Bekämpfung der Schweinepest • • • • • • Richtlinie des Rates der EU vom 23. Oktober 2001 über Maßnahmen der Gemeinschaft zur Bekämpfung der KSP; 2001/89/EG (ABl. Nr. L 316, S. 5 vom 01.12.2001 VO zum Schutz gegen die Schweinepest und die Afrikanische Schweinepest (Schweinepest-Verordnung) vom 20. Dezember 2005 (BGBl. Nr. 74 vom 20.12.2005, S. 3547) Entscheidung der Kommission vom 1. Februar 2002 zur Genehmigung eines Diagnosehandbuchs mit Diagnosemethoden, Probenahmeverfahren und Kriterien für die Auswertung von Laboruntersuchungen zur Bestätigung der KSP 2002/106/EG (EG ABl. Nr. L 39 vom 09.02.2002) Neufassung des Tierseuchengesetzes vom 22. Juni 2004 (BGBl. I S. 3588) Verordnung zum Schutz gegen die Verschleppung von Tierseuchen im Viehverkehr – Viehverkehrsverordnung (ViehVerkV) vom 24. März 2003 (BGBl. I Nr. 11 vom 27. März 2003) Verordnung über Tierkörperbeseitigungsanstalten und Sammelstellen (Tierkörperbeseitigungsanstalten-Verordnung) vom 11. April 2001 (BGBl I S. 552)nnn Verordnung über hygienische Anforderungen beim Halten von Schweinen (Schweinehaltungshygieneverordnung – SchHaltHygV) vom 7. Juni 1999 (BGBl. I, S. 1252) Richtlinie 2001/89/EG • Mitgliedsstaaten müssen Krisenpläne erstellen • Gebiete mit hoher Schweinedichte • Impfstoffbedarf • nationales und lokale Seuchenbekämpfungszentren • Verfütterung von Speiseabfällen endgültig verboten • Untersuchungsmaßnahmen nach Diagnosehandbuch Richtlinie 2001/89/EG • Ausbruch amtlich bestätigt – sämtliche Schweine unverzüglich zu töten (Sperrgebiet 500 m bis 3 km) – alles Material ist zu vernichten oder zu verarbeiten (Hitze) – R+D unter amtlicher Aufsicht – epidemiologische Erhebung mit Fragebögen – Zeitraum, Herkunft, mögliche Ausbreitung • Einheitlichkeit, Vergleichbarkeit – Überwachungszone (10 km) + Schutzzone (min. 3 km) • Verdacht auf KSP in einem Betrieb • amtlicher Überwachung unterstellt • Verbringung von Schweinen untersagt (jede Richtung) • Transportmittel und Betriebszugang desinfizieren Richtlinie 2001/89/EG • Erfassung aller Schweinebetriebe • Stand Still • R+D-Maßnahmen – Wiedereinstellung von Schweinen • frühestens 30 Tage nach Abschluss R+D • Sentinel-Schweine bei Freilandhaltung Keulung • Ausbruch am Schlachthof • atypische Formen Î verlängern HRP • Ausbreitung bei Erstnachweis bereits angelaufen • Î rasche Keulung aller Schweine • alle Tiere sofort töten • Schlachtkörper verarbeiten • 24 h stand still • Wildschweine • Ausweisung eines Seuchengebiets • alle Schweinebetriebe innerhalb – amtliche Überwachung – amtliche Erhebung aller Schweinekategorien – kein Verbringen von Schweinen ohne Genehmigung (beide Richtungen) • • • • • Tilgungsplan innerhalb 90 Tage Informationskampagne für Jäger Abschätzung der WS-Populationen Untersuchung der einzelnen Tiere Entsorgung anfallender Tiere – Seuchenbetrieb – Kontaktbetriebe (30d, 500m) – evtl. Sperrgebiet • Bei hoher Schweinedichte – ethisch und ökonomisch kaum vertretbar • Neuer Ansatzpunkt Realtime RT-PCR: – stand still + Testung betroffener Herden – Keulung nur bei positivem Befund – Zertifizierte Erregerfreiheit durch rt-RT-PCR • Grundsätzliches Impfverbot, aber Notimpfungsplan bei Gefahr im Verzug Impfung • Grundsätzliches Verbot durch EU • 2 Impfstoffe für Notimpfungen ka jd sd ds fbkd ksbv jks ffbk sfjks cbs db asd djb dk fk sd jk bs bk ksdv db ö s jks dd vb – altbewährter (10 Jahre) attenuierter Lebendimpfstoff • Riemser Schweinepestoralvakzine Arzneimittel AG Greifswald-Insel Riems • AK nach 10 Tagen – Subunit-Vakzine Fa. Intervet (Totimpfstoff, Markerimpfstoff) • AK nach 21 Tagen • • • • Persistenz und Rekombination ohne Bedeutung Impfdurchbrüche Schutz vor Klinik aber keine sterile Immunität Zukunft: evtl. in Kombination mit PCR-gestützter Überwachung Î Schlachtung statt Keulung Tierseuchenfrühwarnsystem • Erstes Bundesland: NRW • Pflichtuntersuchungen auf KSP und AK • Abklärungsuntersuchungen als Ausschlussuntersuchungen zwingend! • Finanzierung: TSK – Sektion verendeter Tiere – repräsentative Blutprobenuntersuchung Bekämpfung der Wildschweinepest Genetische Virustypisierung 1993 - 30.09.2007 Grundprobleme • Hausschweinefälle v.a. in Gegenden mit Wildschweinepest • seit 30 Jahren sehr hohe Populationsdichte • erhebliche Schäden auch in Jahren ohne Hausschweinepest: Tierart Wildschwein Hausschwein Typisierung 2.3 Uelzen 2.3 Rostock 2.3 Güstrow 2.3 Spante 2.2 Ringelsdorf 2.1 Paderborn 2.3 Rotenburg 2.3 Warnow 2.3 Spreda • Wildschweinepest gefährdete Bezirke ÎHandelseinschränkungen im Seuchengebiet • ständiges Reservoir für Neuausbrüche Virusnachweis und –typisierung sowie Maßnahmen der Schweinepestbekämpfung bei Wildschweinen Datum letzter genotyp. Meckl.-Vorpommern 01.03.1993 21.07.2000 Virustypisie rung 2.3 Güstrow 2.3 Rostock 2.3 Spante RP Pfalz Brandenburg 1993 14.03.1995 Feb 95 26.04.2000 2.3 Uelzen 2.3 Güstrow Baden-Württemberg 30.09.1998 19.11.1999 2.3 Uelzen RP Pfalz 23.10.1998 12.11.2004 2.3 Uelzen Sachsen-Anhalt 12.10.1999 19.09.2000 Niedersachsen Dez 99 13.06.2002 RP Eifelgebiet Saarland 05.01.1999 26.01.2001 24.03.2003 13.06.2002 Bundesland Erstausbruch Virusnachweis Zeitpunkt der letzten Impfköderauslage Jun 02 keine Impfung Apr 01 Nov 01 31.12.2002 2.3 Uelzen Frühj. 2004 Dez 04 2.3 Rostock 2.3 Rostock Herbst 2004 Herbst 2003 Frühjahr 2004 bis gegenwärtig bis gegenwärtig Mrz 05 Jun 04 NRW 22.04.2002 14.10.2002 2.3 Rostock NRW 07.10.2005 2.3 Rostock RP Eifelgebiet 23.12.2005 03.02.2006 nicht abgeschlossen 2.3 Rostock • Seuchenabriss bei < 1 WS/100 ha in 1 Jahr • Bejagung intensivieren (Sitzjagd) • Freigabe der Hauptempfänglichen Population: Frischlinge bis 1 Jahr • Jagden auch zu Schonzeiten Jan 96 31.12.2002 2.3 Uelzen H H H H H Lösungsansätze 31.12.2002 31.12.2002 W Bekämpfung der Wildschweinepest Tilgung/Aufheb. Sperrmaßnahmen Okt 01 bis gegenwärtig H/W H/W H/W • bejagte Bachen wechseln Reviere • keine Treib- und Drückjagden im Zentrum verseuchter Gebiete; Ausweichen auf Randgebiete • kein Zugang zu Abfällen (Speise, Freizeit, Jagd, Luder) • keine Aufbrüche im Wald zurücklassen (Sammelstelle) • Wildschweinepest gefährdete Bezirke Sep 04 – Intensive Untersuchung von Proben auf KSP • 30% außerhalb gefährdeter Bezirke • alle innerhalb gefährdeter Bezirke • Impfung der Wildschweine Bekämpfung der Wildschweinepest Bekämpfung der Wildschweinepest Impfung Impfung • orale Immunisierung • altbewährter (10 Jahre) attenuierter Lebendimpfstoff: • Riemser Schweinepestoralvakzine Arzneimittel AG Greifswald-Insel Riems. • • • • • Typ C: kein Marker Impfversuch, EU-Ausnahme da Gefahr im Verzug Impfschutz bereits 10 Tage nach Aufnahme Köder in Boden eingebracht oder per Flugzeug auf Felder Maisgrundlage mit Fischmehl; Verletzung der ´Schleimhaut beim Aufbeißen • anfangs 2 Impfkampagnen: Frühjahr und Herbst • Ausrottung der Wildschweinepest in Niedersachsen • heute: 3 Impfkampagnen (hohe Wilddichten in Mecklenburg-Vorpommern und Rheinland-Pfalz) • Ausrottung der Wildschweinepest in Baden-Württemberg 1999-2001 • • • • Auslage jeweils im Abstand von 4 Wochen Frühjahr, Sommer, Herbst Keine Bejagung an Kirreplätzen für 5 Tage Vorteil: Frischlinge können früh erreicht werden • 50% im Alter von 5 Monaten immun • Aber: 5 Monate sehr spät! Kolostrum schützt 3 Monate! • Î Jagdziel: 70% sehr junge Frischlinge Zusammenfassung und Schlussfolgerung • KSP nach wie vor weit verbreitet • erhebliche ökonomische Bedeutung • vordringlichste Aufgaben Maul und Klauenseuche Steckbrief MKS • Gefährlichste Seuche für Klauentiere • Ausschluß vom Welthandel • rasche Ausbreitung + Komplikationen bei Jungtieren – Ausrottung der Wildschweinepest – Verbesserung der Früherkennung • bei sinkenden Prävalenzen: • Bestand und Klinik im Vordergrund Î Herausforderung für Betreuungstierarzt • molekulare Diagnostik: • Reduktion der Keulung Maul und Klauenseuche Steckbrief • MKS Das britische Landwirtschaftsministerium meldet jetzt (19:00 h GMT, Karsamstag 14. April 01) insgesamt 1306 MKS - Fälle. Bisher wurden 1.058.000 Tiere wegen MKS getötet. Hierzu addieren sich weitere 250.000 Schafe in der Grafschaft Cumbria und 45.000 Schafe in der Grafschaft Anglesey, die nicht unmittelbar von MKS betroffen waren. Sie wurden gekeult, um eine weitere Verbreitung des MKS - Virus zu verhindern. In den nächsten Tagen sollen weitere 540.000 Tiere getötet werden. 417.000 Tierkörper sind noch nicht beseitigt. Bis 22.01.02. MKS Steckbrief • Anzeige/Meldepflicht: A • Betroffene Altersstufe: Alle • Besonderheiten: alle Klauentiere betroffen; Impfung bis 91; Serotypen; Erstinfektion kleine Wdk, Schwein; Rind als Indikator; Ausscheidung bereits zur Inkubationszeit • Inkubationszeit: 2 - 3 (12 d) • Morbidität: bis 100 % • Mortalität: 2 – 5 %; Saugferkel 50 – 70 % • Durchseuchung: perakut, rasche Verbreitung über große Gebiete (auch aerogen) • Epidemiologie: epizootisch, rasche Ausbreitung • 1. Tiereinfuhr (Inkubationszeit, Latenz, Erzeugnisse) • 2. Proviantverfütterung aus Drittländern (Reiseverkehr) • 3. Personen aus Drittländern • Heilung: theoretisch ja, 1 - 2 Wochen MKS Erreger • Klasse: Picorna-Viren, Aphtovirus • Aufbau: ss, unbehüllt • Serotypen: 7 Typen + mehrere Varianten A, O, C, Asia, SatI,II,III, • Besonderheiten: Rd>Schw>Schf; andere selten; Einhufer, Mensch praktisch nie • Tenazität: hoch; trocken, kühl, neutral-leicht alkalisch: (Erde, Jauche, Abwasser) monatelang; Gefrierfleisch: Jahre; hohe T, Feuchtigkeit: Stapelmist; Sonne pH<6,0: Fleischreifung; 30´ 60°C: Pasteurisierung • Verbreitungswege: Speiseabfälle, aerogen, Zukauf, Tierkontakt, Personen, alle Sekrete und Exkrete, Aphten! 1 Schwein entspricht aerogen ca. 2000 Rindern • Reservoir: Langzeitausscheider, Tiere in Inkubationszeit • Desinfektion: 2% NaOH; 3% Formalin; 4% Ameisensäure MKS Pathogenese massive Ausscheidung Schmerzen Saugferkel verhungern Abheilung (2w) oro-nasale Aufnahme lokale Immunität (ab d2) Primäraphte Platzen (3Tage) Aphtenbildung nach 1 - 4d Auflösung Gesäuge Herz Klauensaum Ballenbereich Stratum spinosum Virämie cutane Schleimhaut unbehaarte Epidermis Virusvermehrung Fieber MKS MKS Klinik • • • Klinik Fieber + Apathie Aphten: – Klauensaum, Ballen, Zitzen der Sau – Stützbeinlahmheit, Festliegen, Ausschuhen – 1. Rötung (d1) – 2. weißgraue Trübung der Blasendecke (d2) – 3. Platzen: hochrotes Corium+ Str.germ. (d3) 4. Heilung ab d7 oder – eitrige Sek. Infektion Plötzliche Todesfälle – Tigerherz MKS Klinik • • • Fieber + Apathie Aphten: – Klauensaum, Ballen, Zitzen der Sau – Stützbeinlahmheit, Festliegen, Ausschuhen – 1. Rötung (d1) – 2. weißgraue Trübung der Blasendecke (d2) – 3. Platzen: hochrotes Corium+ Str.germ. (d3-5) 4. Heilung ab d7 oder – eitrige Sek. Infektion Plötzliche Todesfälle – Tigerherz MKS Mastbereich Klinik Zuchtbereich - Erste Anzeichen von MKS: Hyporexie, Depression, Lahmheit erschwertes Auftreiben, Festliegen, Beine unter den Körper gestellt - Die Zahl der betroffenen Tiere steigt dramatisch an - Nähere Untersuchung: Blasen im Kronbereich, Ballenbereich, Interdigitalspalt - Erstes Anzeichen in Zuchtherden: hohe Ferkelsterblichkeit - bei Sektion: Tigerherzen bei einigen Ferkeln: multifokale Nekrosen, gelbliche Veränderungen, v.a. Ventrikel MKS MKS Klinik Zuchtbereich Klinik Krankheitsverlauf d1 d3 - Bei den Sauen zeigen sich Blasen auch an den Zitzen - schmerzhaft - Ferkel verhungern d4 d9 d7 d6 MKS Klinik - Läsionen im Mundbereich finden sich an Rüssel, Schnauze, Lippen, Zunge (v.a. dorsal) und Gaumen MKS Sektion • Aphten • Tigerherz MKS Diagnose • Klinik und Virusnachweis • Aphtenmaterial zur BFAV • Serum-AK ab d 5-7 MKS Differentialdiagnostik • alle gehäuften + plötzlichen Lahmheiten • Vesikuläre Stomatitis u. V. exanthem: - nur USA; keine hohen Verlustraten • Bläschenkrankheit (SVD; I66): - Picorna; 5 % Formalin statt NaOH; gleiche Symptomatik an Klauen - hohe Morbidität, keine Sterblichkeit! - gleiche Handhabung • Staph.hyicus: - Ablösung oberflächlicher Schichten Sohlenhaut - ohne Coriumbloßlegung, ohne Lahmheit • Panaritium: - Kronsaumhaut unterminiert • Chron. Se-Vergiftung: • - Klauen und Kronsaum geschädigt, Ballen nicht betroffen • Traumen, Verätzung mit NaOH: - Liegestellen, Zitzen; hohes Fieber und Bläschen fehlen MKS MKS Therapie Immunität und Impfung • keine • bis zur Keulung Sägespäne einstreuen • Impfstoffe vorhanden, aber • fragliche Wirkung, gleichzeitiges Tragen und Ausscheidung von Feldvirus möglich • Serotypen-spezifisch • evtl. Ringimpfung bei Seuchenausbruch • Notimpfung vorbereitet (Impfreserven bei Bayer) 10 Subtypen Typendifferenzierung: 2 Wochen! Sperrmaßnahmen • Impfstopp seit 1991: • Internationaler Handel • Kosteneinsparungen EU-weit: 1 Mrd. DM MKS Salmonellose Prophylaxe Steckbrief • Keulung und Ringimpfung • VO zum Schutz vor MKS (1994) • Sperrung des Seuchengehöfts Kontakt- (letzte 2 w) und Nachbarbetriebe • Sperrbezirk (mind. 3 km Radius) • Beobachtungsgebiet (mind. 10 km Radius) • Schutzzone (mind. 20 km Radius) • Sperrung für Personen und Fahrzeuge, Desinfektionseinrichtungen • Klinische Kontrolluntersuchungen • Blutproben von 30 Schweinen je Betrieb • schwere bakterielle Allgemeinerkrankung subklinisch mit Bedeutung für Fleischhygiene • S. cholerae suis • akute Septikämie, chron. nekrot. Colitis, miliare Lebernekrosen • S. typhimurium • • • • nekrotisierende Colitis+Typhlitis Lebensmittelvergifter, latent im Bestand DT104: Multiresistenzen Zoonose: Enteritis infectiosa • • • • Salmonellose Salmonellose Steckbrief Erreger Erreger: S. cholerae suis, S. typhimurium Anzeige/Meldepflicht: Betroffene Altersstufe: Alle, vorwiegend 4 - 16w Besonderheiten:Plasmidresistenz, Serotyp, Erregermenge (klinisch ab ca. 1 Mio. Keime); Multiresistenzen! Inkubationszeit: 1 - 2d bis Wochen Morbidität: gering Mortalität: gering bis hoch Durchseuchung: langsam, chronisch Epidemiologie: enzootisch Heilung: schwierig, latente Dauerausscheider Bedeutung: Fleischhygiene (subklinisch!); spezifische S. ohne große Bedeutung in Deutschland. • • • • • • • • Klasse: Enterobacteriaceae • Aufbau: gram-negative, bewegliche, fakultativ anaerobe Stäbchen mit Flagellen • Serotypen: >3000 • Besonderheiten: O-Ag (somatisch), H-Ag (Geißel) • Tenazität: hoch; Monate - Jahre, auch gefroren und getrocknet; mehrere Monate in Umwelt, Gülle; Sonne; >70°C; Vermehrung zwischen 5 und 45°C • Verbreitungswege: Ausscheidung mit Kot, Harn, Nasensekret • Reservoir: Darmtrakt; Zukauf latenter Tiere Futtermittel, Schadnager, Fleischfresser, Vögel latente ältere Tiere, Ferkelerzeuger • Desinfektion: Chlor-, Phenol-, Iodbasis (z.B. Sorgene) Salmonellose Pathogenese Salmonella sp. Serotyp, Menge, Resistenzlage Cyanose/Fieber Gefäßschäden Diarrhoe Hypersekretion Enterotoxin (=Coli) Endotoxin Ausscheidung Ak tiv 48h p.i. Septikämie Aktivierung durch 24h p.i. Streß Mesenteriallnn Erregerabwehr Latenz le Makrophage Klinik • Th0 IL12 TNFα IL1 IL6 Salmonellose Klinik Akute Septikämie (S.choleraesuis): Flagellin ie ru Porin ng ss Membranproteine ig LPS na Genexpression MHC-II, NOS NRAMP1 Cytokine Salmonellose • Th1 IL2 Atemwege+oral Eindringen in dendritische Zellen, Enterozyten und Makrophagen IFNγ Salmonellen Enterokolitis (S. typhimurium): – v.a. Absetzer bis 5 M – < 10% der Tiere betroffen – Ausbruch an Streß gekoppelt – evtl. choleraesuis, heidelberg – Absetzen bis 4 M – akut oder chron. – Fieber 40,5 - 42°C, Cyanose (Ohr, Rüsselscheibe, Unterbauch, Gldmß-Innenseite) – matt, Anorexie – plötzliche Todesfälle (hohe Mortalität) – nach 3 – 4 d Durchfall, wäßrig gelb-grau – leichten Husten+Dyspnoe – Aborte – Durchfall+Fieber über 3 – 7 d • wäßrig, gelblich, anfangs ohne Blut und Schleim – fast alle Buchtenmitglieder betroffen – Anorexie, Dehydratation – Blutspuren im Kot – Rückfälle nach scheinbarer Besserung, über Wochen → Kümmerer – Mortalität gering – klinisch geheilt: langjährige Dauerausscheider (mind. 5 M) – Rektalstrikturen Th2 TGFβ hemmen IL4, 10, 13 Salmonellose Salmonellose Sektion • • akute Septikämie: – Cyanosen – Milzschwellung – Mesenteriallnn: ödematös geschwollen – submiliare Lebernekrosen und leichte –schwellung evtl. Ikterus – evtl. Gastritis – Lungen verfestigt, interlobuläre Ödeme und Hämorrhagien – Bronchopneumonie Spitzenlappen – nach 3 – 4d seröse–nekrotisierende Kolitis – evtl. Petechien Nirenrinde und Epicard Histologie: – paratyphoide Knötchen in der Leber Histiozyten nach Leberzellnekrose – Thromben in Magen- und Hautvenen, Glomeruli – Lymphhyoplasie Salmonellose Diagnose • akute Septikämie Sektion • Enterokolitis: – fokale/diffuse nekrotische Enteritis, Colitis, Typhlitis – grau-gelbe Beläge auf der geröteten Schleimhaut – Colon, Caecum, Ilium – Mesenteriallnn (v.a. Iliocaecal) ödematös geschwollen – weder Milz- noch Leberschwellung Salmonellose Differentialdiagnose • akute Septikämie: – Rotlauf • Backsteinblattern, Penicillin – ESP • kleinflächige Hautblutungen – Koliendotoxinschock • Absatzferkel; gleiche Kreislaufsymptomatik • kein Fieber; Verbesserung durch AB – Streptococcus suis – APP – Fieber, Cyanosen – Sektion: Generalisierung, Lebernekrosen – Isolation großer Mengen Salmonellen aus den Geweben auf Selektivnährböden – Lunge, Leber, Milz! • Enterokolitis – Lokalisation im Kolon – Lymphadenitis – Erregerisolation aus Ilium und Ilioceacallnn Salmonellose • Enterokolitis: – Dysenterie • Schleim und rötliche Blutbeimischung • nur Dickdarm; Tiamulin – PIA • Ilium, schwarzbrauner Kot; Tetrazykline – Colienteritis nach dem Absetzen – Rota-, Corona – Trichuris, Kokzidien Salmonellose Erregernachweis Therapie • Anzüchtung aus Geweben bei Septikämie • Selektivmedien bei enteralen Formen • PCR bei latenten Ausscheidern (Kolon, Kot, Tonsillen) • Serologie zur Überwachung (Blut, Fleischsaft) • • • • • intrazellulärer Erreger ! Resistenzen Kümmerer entfernen (Dauerausscheider) Stress reduzieren, Hygiene!!! Behandlung erkrankter Tiere parenteral • Apramycin, Neomycin, Colistinsulfat, Dexamethason • gesamte Tiergruppe über Futter oder Trinkwasser: • Apramycin, Neomycin, Colistinsulfat • Resistenztest • • • • • Ermittlung der Infektionsquelle Schadnager- und Fliegenbekämpfung Rein-Raus! Impfung von Sauen vermindert Eintrag diätetische Maßnahmen in der Mast • gekapselte Futtersäuren (Formyl, Aciprol) • Laktulose • Flüssigfütterung (pH 5!) Salmonellose Salmonellose Immunität und Impfung Prophylaxe • Immunität kann Latenz nicht verhindern, nur reduzieren • Lebendimpfstoffe (zelluläre Immunität) • Impfstoff gegen S. choleraesuis und S. typhimurium stehen zur Verfügung • • • • • Salmonellose Salmonellen VO Haltung optimieren gegenseitige Ansteckung verhindern Erregerkreisläufe! Rein-Raus Fütterung: erhitzte Pellets; Flüssigfutterreste (ansäuern) Fleischhygiene • symptomlos, weit verbreitet, 2-5 % aller Schweine in D, ca. 30% der Bestände • 50 % S. typhimurium • Futtermittel (Nagerkot, Fisch-, Tiermehle) • Transportstreß • Wartezeiten am Schlachthof • Kotkontakt mit Ausscheidern • Aktivierung latenter Infektionen • Kontamination in Schlachtkette (Brühen, Borsten, Tonsillen, Kotaustritt) • alle S. als humanpathogen anzusehen: 20% der Salmonellosen durch Schweinefleisch • QM • Aufbau von Salmonellenkontrollprogrammen Salmonellen VO • Zielsetzung • Verringerung des Eintrages von Salmonellen durch Schlachttiere durch Fleischgewinnung • Prädikat Salmonellen-überwachter Betrieb • Untersuchung • Fleischsaft geschlachteter Mastschweine • AK-Nachweis (O1, O4, O5, O12, O6, O7 = 95% aller relevanter) • Auswertung • Vorlaufzeit 1 Jahr • Probenschlüssel • Kategorien • niedriger Status: < 20 % + • Verdacht auf hohen Status: 20 – 40 % + • hoher Status: > 40 % + • Aktionen • Beratungsgespräch bei zweimaligem Verdacht • Bestandshygienemaßnahmen mit Betreuungstierarzt einleiten • Schlachtung und Kennzeichnung Rotlauf Steckbrief • Probenschlüssel • • • • bis 45 Schlachtschweine/Jahr: alle Tiere bis 100 Schlachtschweine/Jahr: 45 Tiere/a 100 – 200 Schlachtschweine/Jahr: 50 Tiere/a >200 Schlachtschweine/Jahr: 60 Tiere/a • gleichmäßige Verteilung über alle Partien/Jahr • Ersteinstufung frühestens 12 Monate nach Erstuntersuchung • danach rückwirkende Einstufung 2x jährlich • Bakterielle Allgemeinerkrankung • relativ gut therapierbar • chronisch: schlechte Prophylaxe, ungünstige Prognose Rotlauf Rotlauf Steckbrief Erreger • • • • • • • • • • • • • • • • Klasse: gram positiv Aufbau: Stäbchen mit Kapsel Serotypen: 1, 2 Besonderheiten: Tenazität: hoch; mehrere Monate in Umwelt, Jauche, Harn, Kot, Kadavern • Verbreitungswege: Ausscheidung mit Kot, Harn, Nasensekret, Speichel • Reservoir: bei 50 % der gesunden Schweine auf Tonsillen: Ausscheider; Schaf, Nager, Geflügel • Desinfektion: 2% NaOH; 3% Formalin; 4% Ameisensäure Erreger: Erysipelothrix rhusiopathiae/tonsillarium Anzeige/Meldepflicht: Betroffene Altersstufe: Alle > 3 M, < 3 a Besonderheiten: Geflügel, Schaf, Mensch; Wasser, Einstreu, kein Bodenkeim; Inkubationszeit: 3 - 5d Morbidität: gering Mortalität: gering Durchseuchung: Epidemiologie: enzootisch Heilung: gute Aussichten nach rechtzeitiger Behandlung Bedeutung: gering durch milden Verlauf und gute Therapierbarkeit Rotlauf Rotlauf Pathogenese maternale AK BiGe-Zubildung Fibrinaustritt Schutz f. 3 m Herzklappenrotlauf Koagulopathie Immunität Mikrothromben Hämorrhagien fehlende Immunität oro-nasale perkutane Endothelschäden Neuraminidase Septikämie konjunctivale (Haut, Synovial+ Kapsel nach 24h enterale membran) Anheftung+ Hämolyse Phagozytoseschutz Aufnahme proliferative E. Ag-Expression: Knorpelzellen Gelenkknorpelzerstörung periartikuläre Fibrosierung Ankylosen lokale Form „Backsteinblattern“ Klinik • perakut/akut: – Rotlaufseptikämie: absondern, matt, Anorexie – steifer Gang, rasches Hinlegen plötzliche Todesfälle – Schwäche, Fieber (40 - 42°C) → Aborte, Mumien – dunkelrote, konfluierende Flecken (Landkarten), Brust/Ohren d2-3; (heute sehr selten) oder Backsteinblattern (hell/dunkel) – 50 % tot innerhalb 3d subakut: - matt, Anorexie, Fieber, – Bakteriämie – Rote Hautflecken, v.a. Rücken; geometrisch (rund-viereckig), violett, erhabene Erytheme, 2 - 6 cm (Backsteinblattern) – steifer Gang, Gldmß-Schmerzen • massive Erregerausscheidung Gelenksrotlauf Rotlauf Rotlauf Sektion Klinik • chronisch: – nach akutem oder subkl. Verlauf – Herzklappenrotlauf: fibrinöse Auflagerungen, Läufer • starke Dyspnoe und Inappetenz, schwacher Puls, erhöhte Frequenz, Blässe (li) – Zyanose (re) • Brustlage, Hundesitz, Maulatmung, Lungenödem – Gelenksrotlauf: Knie, Ellbogen, Karpal, Tarsal, Wirbels. • Septikämie oder lokal bedingt; Umfangsverm., Verkrümmung • wechselnde Lahmheit, verbessert sich nach paar Schritten • Palpation: schmerzempfindliche, warme Umfangsvermehrung • Fluktuation: Synovialitis • klammer Zehenspitzengang, nicht streckbare Karpalgelenke Ankylose und Tendovaginitis tiefe Beugesehne – Hautnekrosen - komplette Ausheilung in Wochen • evtl. Sek.Infektionen • • perakut: – Petechien Herz, Nieren, Magen – Nieren rötlich, geschwollen punktförmige hyperämische Glomerula – Infarkte – intensive Blutfülle Ma-Da-Trakt – Milz und Lnn stark vergrößert – Milzinfarkte Gelenksrotlauf: – rötliche, serofibrinöse zellreiche Flüssigkeit in Gelenken – eingeklemmte Synovialwucherungen – keine eitrige Einschmelzung – Fibrosen, Ankylosen, Knorpelabbau Rotlauf Diagnose • • • • • • • • • vereinzelte Todesfälle ohne vorhergehende Krankheitszeichen zahlreiche Tiere krank mit Fieber steifer Gang, rege Teilnahme an Umgebung V: >41°C; sichere Penicillinwirkung B: nur durch BU V: Milzhypertrophie Hautform: Backsteinblattern Herzform: Blumenkohlartige Wucherungen Gelenksrotlauf: – gehäuftes, gruppenweises Auftreten – Vor- und Mittelmast – ältere Tiere nur sporadisch • Erregernachweis: Blut, Organe, Gelenke • chron.: – gepaarte Serumproben auf AK : sicheres Ergebnis Rotlauf Differentialdiagnose • Septikämie: – ESP, ASP: Hautblutung punktf. ohne Schwellung – Salmonellose – Penicillin! • Hautform: Backsteinblattern – pathognomonisch – evtl.: Pityriasis, Pocken, lokale Staph.hyicus • Herzform: Blumenkohlartige Wucherungen – Streptokokkenendokarditis – ELISA • Gelenksrotlauf: - Streptokokken • Morbus maculosus: große runde Hautblutungen ohne Fieber Rotlauf Rotlauf Therapie Immunität und Impfung • alle Formen: • Opsonierung zur Phagozytose • Impfung aller Sauen und Zuchtläufer • Penicillin 20 - 30 Mega • Amoxicillin 10 - 20 mg/kg; 250 - 500 ppm oral • • • • Fieberfrei und Besserung in 12 h bislang keine Resistenzen Langzeitpenicillin oder 2 - 3 d hintereinander Metaphylaxe (Kotkontakt) • Depotpenicillin oder Hyperimmunseren • akute Polyarthritis: mind. 3d Penicillin, hohe Dosis • + Phenylbutazon oder Dexamethason • chron. Form/ Endocarditis: infaust • Sauen a.p.: Strophantin(0,02 mg/kg)/Digoxin(0,01mg/kg) • • • • • 1. 12w 2. 20w Auffrischung: 2 - 3w vor Belegen / Bestandsimpfung Erysorb plus; Porcilis Ery Kombination mit Parvo • Immunität für 3-5 M • geringe Effekte auf chronische Formen (intrazellulär) • Keine Lebendimpfstoffe in Rotlauf-freien Beständen Rotlauf PCV-2 Prophylaxe • • • • Auslauf Misthaufen Tiefstreu Impfung • Porzines Circovirus – Typ 2 – – – – – Postweaning Multisystemic Wasting Syndrome Porzines Dermatitis Nephropathie Syndrom Interstitielle Pneumonie Proliferativ Nekrotisierende Pneumonie Reproduktionsstörungen • Zusammengefasst: PCVD (PCV2-Diseases) PCV2 Klinik PCV2 Klinik Entzü Entzündung der Bindehaut und schwarze Trä Tränenspuren als wichtige Symptome Tier palpierbar oder sogar sichtbar) Reine PCV2 Infektion bioScreen, 2000 bioScreen, 2000 Inguinallymphknoten häufig stark vergröß ert (z.T. am lebenden vergrößert Nachweis von PCV2 + PRRSV „PNPPNP-Lunge“ Lunge“ Interstitielle Pneumonie (Proliferativ Nekrotisierende Pneumonie) PMWS - Klinik • Absatzferkel 8.-16. LW • 2-3 Wochen nach Einstallung zur Mast • Therapieresistenz • Genesungsrate sehr gering PMWS - Klinik • • • • • • • • • Respiratorische Symptome 60%* Schlechte Entwicklung33% Ferkelverluste (3-30%)30% Aborte 19% Diarrhoe 18% Blässe 14% Intermittierendes Fieber 14% Nephritis, Lymphadenitis, PDNS Allgemeine Krankheitsanfälligkeit * der Betriebe; nach Ohlinger PMWS Erkrankte Tiere bleiben in der Entwicklung deutlich zurück PMWS - Sektion • Lymphadenitis multiplex • Interstitielle Pneumonie • Lunge gummiartig verfestigt nicht kollabiert • Nephritis, Hepatitis, Enteritis Der Erreger Epidemiologie • Heute weltweit und ubiquitär verbreitet • PCV-2 rückwirkend in Proben aus 1970er Jahren nachgewiesen • PMWS 1991 zum ersten Mal in Kanada 1996 zum ersten Mal in Europa • PMWS/(PDNS): immer PCV-2-Infektion • PCV-2-Infektion führt nicht immer zu PMWS/PDNS ⇒ weitere Faktoren! • Zellen mit hoher Teilungsrate notwendig Bundesland PCV-1 [%] PCV-2 [%] Baden-Württemberg 9.1 54.5 Bayern 26.7 80.0 Berlin 50.0 75.0 Brandenburg 46.7 86.7 Hessen 47.1 76.5 Niedersachsen 44.4 Mecklenburg-Vorpommern 20.0 Nordrhein-Westfalen 13.3 Rheinland-Pfalz * Gewebe PCV-1 positiv [%] PCV-2 positiv [%] 72.2 Tonsillen 26.6 70.4 40.0 Milz 46.9 93.6 46.7 Lunge 21.9 75.2 26.4 68.4 59.4 75.2 Saarland 26.3 63.2 Lymphknoten Sachsen 40.0 70.0 Sachsen-Anhalt 12.5 75.0 Schleswig Holstein 62.5 75.0 Thüringen 16.7 66.7 Durchschnitt 34.4 67.2 * PCR-Ergebnisse; nach Reiner et al., IPVS, 2006, Kopenhagen PMWS - Pathogenese s e ng d vieru stems i t k A unsy Imm PMWS - Histologie Verbreitung im Körper Befall Lymphatischer Gewebe Lymphozytendepletion+ Histiozytäre Infiltration Aborte/Immuntolerante Dauerausscheider Lungeninterstitium Hepatitis/Nephritis chron. therapieresist. Diarrhoe Dyspnoe, interstit. Pneumonie Kümmern PMWS - Pathogenese Aktivierung durch: LPS, Bakterien, Viren, etc. PCV2 Antigen-Präsentation Aktivierung Makrophagen transplazental (bei seronegativen Sauen) Mesenteriallnn Darmwand PMWS - Pathogenese unspezifische IL1 Abwehr TNFα orale/nasale Aufnahme Nasenschleimhäute Makrophagen fäkale Ausscheidung • Massive follikuläre/parafollikuläre Lymphozytendepletion Lymphozytopenie • Infiltration mit Histiozyten Histiozytose • Granulomatöse Entzündung • Synzytiale Makrophagen • Riesenzellen • basophile EK in Makrophagen • Parenchymnekrosen maternale AK? Erregerdichte? IL2 INFγ IL4 CD4+T-Helferzellen Aktivierung Immunevasion zeitlich begrenzte Persistenz ohne Replikation B-Zellen, CD8+-Zellen spezifische Abwehr Aufnahme Verbreitung in allen lymphatischen Organen des Körpers kein PMWS Makrophagen CD4+T-Helferzellen PMWS - Pathogenese Aktivierung durch: LPS, Bakterien, Viren, etc. PMWS - Pathogenese Aktivierung durch: LPS, Bakterien, Viren, etc. PCV2 PCV2 Replikation Aufnahme Antigen-Präsentation unspezifische Abwehr Aktivierung Replikation IL2 ↓ INFγ ↓ Proliferation IL4 ↓ Antigen-Präsentation unspezifische Abwehr Aktivierung CD4+T-Helferzellen Makrophagen CD4+T-Helferzellen Makrophagen Aktivierung IL2 ↓ INFγ ↓ Proliferation IL4 ↓ Aktivierung Replikation Replikation Lymphozytendepletion B-Zellen, CD8+-Zellen B-Zellen, CD8+-Zellen spezifische Abwehr spezifische Abwehr PMWS - Pathogenese PMWS - PathogenesePRRSV Aktivierung durch: LPS, Bakterien, Viren, etc. PCV2 Cytokine Aktivierung MCP1 IL2 ↓ INFγ ↓ S-Phase IL4 ↓ MCP1 Lymphozytendepletion spezifische Abwehr Immundefizienz Sekundärinfektionen bp 1000 900 800 700 600 500 400 300 200 100 – Nur aussagekräftig im Zusammenhang mit Bestandsbefund, klinischem Bild, Sektionsbild – Lunge, Lnn, Milz, Niere Lane 1 Lymphozytendepletion z.B. interst. Pneumonie B-Zellen, CD8+-Zellen spezifische Abwehr Immundefizienz Sekundärinfektionen PCV2: Quantitative Diagnostik • Serologie: keine Aussage, da ubiquitär • Erregernachweis mittels PCR: – Histiozytose, Lymphozytopenie – Einschlusskörperchen, Riesenzellen CD4+T-Helferzellen Histiozytose Riesenzellen „Funktio laesa“ PCV-2 Diagnose - Möglichkeiten • Sektion: Histologisches Bild IL2 ↓ INFγ ↓ S-Phase IL4 ↓ Aktivierung Histiozytose Riesenzellen „Funktio laesa“ B-Zellen, CD8+-Zellen Interleukine Aktivierung Makrophagen Aktivierung z.B. interst. Pneumonie Zelldetritus unspezifische Abwehr CD4+T-Helferzellen Makrophagen 76% H. parasuis 14% Strc., Coli, Corona etc. … Aktivierung durch: LPS, Bakterien, Viren, etc. PCV2 Zelldetritus unspezifische Abwehr Immundefizienz Sekundärinfektionen 2 3 4 5 Beispiel 2: PCV2 70 • PCV2-Nachweis nPCR: flächendeckend • aber: erhebliche quantitative Variabilität • Kopplung PCV2-Kopienzahl / PMWS eng % innerhalb Herkunft 60 50 40 WS HS 30 • Î Umstellung von qualitativer PCR auf quantitative PCR sinnvoll und notwendig! 20 10 0 0 1 2 3 4 5 6 PCV2-Konzentrationsstufe (log) Bedeutung früher PCV2Infektionen Risikofaktoren für PMWS – Niedrige PCV2-Antikörperspiegel der Sau – Unzureichende Kolostrumversorgung – Ungenügende passive Immunität der Ferkel gegen PCV2 – PCV2-Exposition der neugeborenen Ferkel • PCV2-Infektionen im frühen Ferkelleben erhöhen das Risiko für eine spätere PCVDProblematik • Virämie der Sauen ist ein Risikofaktor • Kolostrum und Milch können mit PCV2 kontaminiert sein • intrauterine Infektionen sind möglich Risikofaktor: PCV2-Infektion schon bei jungen Ferkeln PCV2-Infektion im Abferkelbereich über den Kot der Sau PMWS – Risikofaktoren • • • • Koinfektionen (PRRSV, PPV, M. hyo, APP) Kastraten > Sauen Landrasse Risiko ↑ – ↓ maternale Antikörper • • – • Abbau nach 2-4 Wochen 2/3 aller Sauen ohne ausreichende Immunität virämische Sauen Impfungen Risikofaktor - Impfung • Zeitpunkt – – • • ⇒ ⇒ PCV2 gesteigerter Infektionsdruck Risiko durch Stimulation des Immunsystems zum Zeitpunkt aktiver PCV-2 Infektion geringe Gefahr bei Impfung 2-4 Wochen ante PCV-2 infectionem Mineralöl > Pflanzenöl > Carbachol, Al(OH)3 Einfluss von Simultanimpfungen, besonders Kombination Lebend-/Totimpfstoff Impfungen (z.B. M.hyo) < Infektion Impfungen bei hohem PCV-2-Druck: unter maternalem PCV-2 AK-Schutz (bis ca. 4. LW) nicht in florierende PCV-2 Infektion hinein impfen höhere Tierdichte 1. Abferkelmanagement 2. begrenzter Tier-zu-Tier Kontakt (direkt und indirekt) 3. Stress reduzieren 4. Hygienemaßnahmen 5. Gute, hochwertige, altersgerechte Fütterung 6. Muttertierimpfung PMWS – Bekämpfung nach Madec (2000) • Abferkelstall 1. Konsequente Einhaltung Rein-Raus obligatorische Reinigung und Desinfektion (Vircon S?, MennoF Super), Leerzeit 2. Sauen: waschen und Parasitenbehandlung 3. Wurfausgleich auf Minimum beschränken auf maximal 24 Stunden p.p. begrenzen PMWS – Bekämpfung nach Madec (2000) Flatdeck 4. Konsequent Rein-Raus, obligat R+D Leerzeit 5. Haltung in Kleingruppen (< 13 Ferkel) geschlossene Buchten-Trennwände 6. Belegungsdichte reduzieren (≥ 0,35 m2/Ferkel) 7. Troglänge anpassen (≥ 7 cm/Ferkel bei gleichzeitiger Fütterung) 8. Luftqualität optimieren (NH3 < 10 ppm) 9. Lufttemperatur anpassen 10. Kein Zurücksetzen älterer Ferkel verminderte Gewichtszunahme höherer Zeitbedarf bis zum Ausstallen Goldene Regeln gegen PCVD • PMWS Einfluss des Adjuvans – • Risikofaktor - Haltungsdichte PMWS – Bekämpfung nach Madec (2000) • Mast 11. Konsequent Rein-Raus, obligat R+D Leerzeit 12. Haltung in Kleingruppen (< 13 Ferkel) geschlossene Buchten-Trennwände 13. Kein Umstallen innerhalb der Gruppen 14. Kein Zurücksetzen älterer Schweine 15. Belegungsdichte reduzieren (≥ 0,75 m2/Tier) 16. Luftqualität/ -temperatur optimieren PMWS – Bekämpfung nach Madec (2000) • Weitere Maßnahmen 17. Impfzeitpunkte anpassen 18. Tierverkehr im Bestand optimieren 19. Hygienekontrolle (zootechnische Maßnahmen) 20. Kranke Tiere frühzeitig separieren (Krankenstall) PMWS – Bekämpfung Ziel des Madec-Programms • PCV-2-Exposition/Koinfektion denn das PMWS-Risiko Kontrolle - Sauen • Reduktion virämischer Sauen – Screening mit PCR – Reduktion immuntoleranter Ferkel – Senkung des Infektionsdrucks im Wurf und im Bestand • • • • • • Umsetzen von Ferkeln max. 24 Std. p.p. Umsetzen von max. 15 % der Ferkel Umsetzen nur innerhalb des Abteils Absetzalter um 21 Tage Konsequentes Entfernen der Kümmerer Minimierung der Sekundärinfektionen PCV2 - Immunität Serokonversion ca. 2 – 4 Wochen p.i. Erkrankte entwickeln AK erst später Abfall maternaler AK: 2./4. LW Infektion: 4. – 8. LW Antikörper bis ca. 28. LW sinkt mit zunehmendem Alter steigt mit abnehmenden maternalen Antikörpern steigt mit zunehmender Exposition Kontrolle – Management Ferkel – – – • • • • • So spät wie möglich Mit so geringen Erregermengen wie möglich Hygiene Antibiose Impfmaßnahmen PCV-2 - Impfung • • Circovac, Merial Inaktivierter Adjuvans-Impfstoff von Merial – – – – • • Muttertiervakzine, ölig, 2ml i.m. JS: 6 und 3 Wochen a.c. AS: 6 und 3 Wochen ante partum Wiederholung: 3 Wochen a.p. Experimentelle Impfungen seit 2002 erfolgreich Prinzip: – – – passive Immunisierung der Ferkel während der kritischen Phase geschützt + Aufbau eigener aktiver Immunität Senkung des Infektionsdrucks im Bestand Circovac® Impfschema PCV2-Impfstoff, inaktiviert Jungsauen: Grundimmunisierung Maßnahme: ► Aktive Immunisierung des Muttertieres vor dem Abferkeln (JS schon vor dem Belegen) Wirkung: n Wiederholungsimpfung o q p 3-4 Wochen ≥2 ≥2 Wo. Wo. ≥2-4 Wo. Abferkeln Belegung Abferkeln Sauen: ► Passive Immunisierung der Ferkel über die Biestmilch Grundimmunisierung n o Wiederholungs- Wiederholungsimpfung impfung Wochen ≥2 Wo. Abferkeln Vorgehen bei PCVD im Betrieb • Allgemeine Maßnahmen: – Hygiene – Management – Fütterung • Spezifische Maßnahmen: – Muttertierimpfung mit Circovac: Impfung der Jungsauen vor dem ersten Belegen sowie der Jungsauen und Sauen vor jedem Abferkeln – Optimierung des Abferkelmanagements (Kolostrumversorgung!) Î Nachhaltiger Impfschutz der Ferkel über die PCV2-Muttertierimpfung Serologische Verlaufsuntersuchungen Geimpfte Jungsauen entwickeln hohe ELISA-Ak-Titer und geben diese an ihre Ferkel weiter q p 3-4 ≥2-4 Wo. ≥2-4 Wo. Abferkeln Abferkeln Basisinformation: Circovac®: Für Tiere (Schweine). Zusammensetzung: Eine fertig aufbereitete Dosis zu 2 ml enthält: Inaktiviertes porcines Circovirus Typ 2 (PCV2) ≥ 2,1 log10 ELISA-E; Thiomersal 0,20 mg; Adjuvans: dünnflüssiges Paraffin 494 bis 501 mg. Anwendungsgebiete: Passive Immunisierung von Ferkeln durch Aufnahme von Kolostrum nach aktiver Immunisierung von Sauen und Jungsauen, zur Reduktion von Schädigungen des lymphatischen Gewebes infolge der Infektion mit dem porcinen Circovirus Typ 2. Geeignet zur Verminderung der PCV2bedingten Mortalität. Dauer der Immunität: bis zu 5 Wochen nach der passiven Übertragung von Antikörpern durch Aufnahme von Kolostrum. Gegenanzeigen: Keine bekannt. Nebenwirkungen: Leichte vorübergehende Lokalreaktionen, die üblicherweise nach der Verabreichung einer Dosis des Impfstoffes auftreten, sind hauptsächlich Schwellung (durchschnittlich bis zu 2 cm2) und Rötung (durchschnittlich bis zu 3 cm2) und in einigen Fällen Ödeme (durchschnittlich bis zu 17 cm2). Diese Reaktionen bilden sich durchschnittlich innerhalb von maximal 4 Tagen ohne Beeinträchtigung der Gesundheit und Leistung der Sau oder Jungsau von selbst zurück. In klinischen Studien wurden bei post-mortemUntersuchungen der Injektionsstelle nach maximal 50 Tagen nach Impfung begrenzte Läsionen wie Verfärbung und Granulom bei der Mehrzahl der Tiere sowie Nekrose oder Fibrose (bei etwa der Hälfte der Tiere) gefunden. Innerhalb von 2 Tagen nach der Injektion kann es zu einem durchschnittlichen Anstieg der Rektaltemperatur von bis zu 1,4 °C kommen. In seltenen Fällen kann der Anstieg der Rektaltemperatur mehr als 2,5 °C für bis zu 24 Stunden sein. In seltenen Fällen können leichte Apathie oder verminderter Appetit beobachtet werden, die sich in der Regel von selbst normalisieren. Überempfindlichkeitsreaktionen sind ausnahmsweise möglich. In solchen Fällen sollte eine entsprechende symptomatische Behandlung erfolgen. Ausnahmsweise kann es nach der Impfung zum Abort kommen. Falls Sie eine Nebenwirkung bei Ihrem Tier/Ihren Tieren feststellen, die nicht in der Packungsbeilage aufgeführt ist, teilen Sie diese Ihrem Tierarzt oder Apotheker mit. Wartezeit: Null Tage. Besondere Warnhinweise: Eine versehentliche Injektion ist gefährlich - lesen Sie vor der Anwendung die Packungsbeilage. Verschreibungspflichtig. Pharmazeutischer Unternehmer: Merial GmbH, Am Söldnermoos 6, D-85399 Hallbergmoos. PCV2-Muttertierimpfung Quantitative PCR im Serum Nachweis Virus-DNA im Serum von Ferkeln ungeimpfter Kontrollen höher als im Serum von Ferkeln geimpfter Jungsauen 6 Absetzen V3 V2 4 3 V1 2 1 0 0 28 56 84 112 140 168 196 days Ungeimpfte JS Geimpfte JS Kontrollen Ferkel Impflinge 4 PCV2 Inf. Log10 Kopien PCV2/Reaktion PCV2 Antikörpertiter (log10/ml) Abferkeln 5 Kontrollferkel 3 2 1 0 0 10 20 30 Tage nach Challenge Ferkel von Impflingen (Charreyre et al., 0.30-02/-03 IPVS 2006) (Charreyre et al., 0.30-02 IPVS 2006) CircovacMerial – bisherige Erfahrungen • Erfahrungsberichte aus den Impfbetrieben – – – – „Der Virusgehalt bestimmt die Schwere der Erkrankung!“ Kümmerer und Todesfälle im Flatdeck verringert Höhere Zahl verkaufter Ferkel Reduzierter Antibiotikumverbrauch Reduzierte Verluste in der Mast S. Krakowka, Belfast, 09-2005 • • • • von Boehringer Ingelheim Kanadischer Feldversuch 2006 N = 3837 oneone-shot Impfstoff ab einem Alter von 2 Wochen 1 ml/Impfdosis, i.m. Adjuvans: Impran FLEX TM 12 (Polymer, wä wässrig) • Antigen: PCA (purified Circovirus antigen) ntigen) – hochgereinigtes Virus Kapsid (ohne Genom) Mortalität [%] Der CircoCirco-Impfstoff 8 9,6 9,5 8,1 7,6 ungeimpft geimpft 6 4 2,8 2 0 • Die FLEXFLEX-Zukunft: Zukunft: 10,6 10 2,1 3 2,4 0,4 19-22 22-38 38-45 45-59 gesamt Alter bei Impfung [Tage] – Impfstoffe der FLEX-Familie sind untereinander mischbar ø Mortalitä Mortalitätssenkung = 75 % Desrosiers et al. 2006 Deutscher Feldversuch 2006 Reduction of Virem ia 80 Vaccine 70 % PCV2 positive animals Zusammenfassung Placebo • PCV-2 gehört heute zu den ökonomisch bedeutsamsten Krankheitserregern beim Schwein 60 – Interaktion mit anderen Erregern – Potenzierung von Pathogenen 50 40 30 • 10 Jahre in Europa – viele offene Fragen 20 – Pathogenese, Variabilität und Wandel, Genetik 10 • Neuer Impfstoff neue Hoffnung?! Signifikante Reduktion der Dauer und Hö Höhe der Virä Virämie 25 23 21 19 17 15 13 9 11 7 5 3 0 Porcines Dermatitis und Nephropathie Syndrom (PDNS) Steckbrief • Immunkomplexvermittelte Gefäßerkrankung und Glomerulopathie • Sektionsbild entspricht ESP • max. 1 – 20 % des Bestandes betroffen • wahrscheinlich nach chronischem PCV-2-Befall PDNS Steckbrief • Erreger: Beteiligung von Circo-Viren?, PRRS, Influenza, PRCV, Streptos, APP, Pasteurellen • Anzeige/Meldepflicht: • Betroffene Altersstufe: v.a. 40 – 70 kg • Besonderheiten: Tod in 3 - 5 Tagen; Immunkomplexerkrankung, Komplementvermittelt • Inkubationszeit: • Morbidität: bis 25 % aller Tiere • Mortalität: 30 bis 100 % (je älter desto höher) • Durchseuchung: • Epidemiologie: enzootisch • Heilung: Überlebende nach 7 – 10 Tagen • Bedeutung: wachsende Bedeutung PDNS Der Erreger Pathogenese chronische Infektion mit PCV2 und evtl. anderen Erregern Immunantwort Ablagerung von Immunkomplexen in Gefäßen und Glomerula C3 generalis.: Vaskulitis Glomerulonephritis generalisierende Blutungen • Heute weltweit und ubiquitär verbreitet • PCV-2 rückwirkend in Proben aus 1970er Jahren nachgewiesen • PMWS 1991 zum ersten Mal in Kanada 1996 zum ersten Mal in Europa • PMWS/(PDNS): immer PCV-2-Infektion • PCV-2-Infektion führt nicht immer zu PMWS/PDNS ⇒ weitere Faktoren! • Zellen mit hoher Teilungsrate notwendig Befall von Lymphozyten Lymphadenitis Glomerulonephritis Schock Sek.Infektionen Tod durch Nierenversagen PDNS - Pathogenese PCV2-Infektion (oder andere) PDNS • Immunkomplexvermittelte Replikation Zelllyse+ PCV2-Freisetzung Antikörper – Gefäßerkrankung und – Glomerulopathie • Sektionsbild entspricht ESP • max. 1 – 20 % des Bestandes betroffen • wahrscheinlich bei chronischem PCV-2Befall PCV2 chronischer Verlauf „normaler Verlauf“ Vernetzung Vernetzung/ Phagozytose nicht möglich Anlagerung an Epithelzellen + Glomerula Phagozytose PDNS - Pathogenese PCV2-Infektion (oder andere) PCV2 Replikation chronischer Verlauf PDNS - Klinik Zelllyse+ PCV2-Freisetzung Antikörper „normaler Verlauf“ Vernetzung/ Phagozytose nicht möglich Vernetzung Anlagerung an Epithelzellen + Glomerula Phagozytose C3-Aktivierung Vaskulitis Blutungen Glomerulonephritis Schock • Petechiale und ekchymatöse Hautveränderungen • v.a. Perianalbereich und zwischen Hinterschenkeln • Nur wenige Tiere betroffen • Blässe • Evtl. Diarrhoe • Hohe Mortalität Nierenversagen PDNS - Klinik PDNS - Sektion • Petechiale und ekchymatöse Hautveränderungen • v.a. Perianalbereich und zwischen Hinterschenkeln • Nur wenige Tiere betroffen • Blässe • Evtl. Diarrhoe • Hohe Mortalität • Systemische, nekrotisierende Gefäßentzündungen • Petechiale Blutungen auf Organen • Lymphknoten blutig infiltriert und angeschwollen • Milzrandinfarkte • Glomerunonephritis PDNS - Sektion • Systemische, nekrotisierende Gefäßentzündungen • Petechiale Blutungen auf Organen • Lymphknoten blutig infiltriert und angeschwollen • Milzrandinfarkte • Glomerunonephritis PCV-2 Diagnose - Möglichkeiten • Serologie: keine Aussage, da ubiquitär • Erregernachweis mittels PCR: bp 1000 900 800 700 600 500 400 300 200 100 – Nur aussagekräftig im Zusammenhang mit Bestandsbefund, klinischem Bild, Sektionsbild – Lunge, Lnn, Milz, Niere Lane • Sektion: Histologisches Bild – Histiozytose, Lymphozytopenie – Einschlusskörperchen, Riesenzellen 1 2 3 4 5 PDNS - Histologie • • • • generalisierte Glomerulonephritis Fibrin, Neutrophile und Erythrozyten generalisierende nekrotisierende Vaskulitis fibrinoide Nekrose von Tunica, Intima und Media 50%: Lymphozytendepletion+ Histiozytose Mehrkernige Riesenzellen 80%: interstitielle Pneumonie PDNS Diagnose • Im Bestand: einfach und sicher durch Lage der typischen Hautveränderungen • Glomerulonephritis (Fibrinausfällung) • Hohe Blutharnstoff- und Kreatiningehalte • Systemische nekrotisierende Vaskulitis! • Abklärung von ESP! • Erregernachweis in Lnn, Lunge, Milz, Niere - PCR auf Circo-Viren PDNS PDNS Differentialdiagnostik Therapie • ESP • PMWS • keine Therapie möglich PDNS Eperythrozoonose Immunität und Impfung Steckbrief • PCV2-Impfstoff • Prophylaxe = PMWS • Faktorenkrankheit, die in den meisten Beständen subklinisch verläuft • Erreger allein reicht nicht zum Angehen der Erkrankung • Stress durch Haltungsbedingungen! Eperythrozoonose Eperythrozoonose Steckbrief • Erreger: Mycoplasma suis! (Eperythrozoon suis) Erreger: • • • • • • Klasse: Rickettsiales Aufbau: Familie Mycoplasmataceae Serotypen: Besonderheiten: parasitiert in Erythrozyten Tenazität: Vermehrung nur in Zellen möglich Verbreitungswege: Übertragung durch biotechnische Maßnahmen (Spritzen, Schlinge), Läuse • Reservoir: Träger • Desinfektion: - • Anzeige/Meldepflicht: • Betroffene Altersstufe: alle, v.a. Absetzer • Besonderheiten: Einzeltiere nach besonderer Belastung betroffen (Rangordnungskämpfe, Umstallen, Maßnahmen) oder als Begleitsymptom chronischer Krankheiten (PRRS) • Inkubationszeit: 3 – 20 d (7) • • • • • • Morbidität: ? Mortalität: < 1 % Durchseuchung: latent Epidemiologie: enzootisch Heilung: innerhalb weniger Tage Bedeutung: weit verbreitete Faktorenkrankheit Eperythrozoonose Eperythrozoonose Pathogenese Klinik Ohrspitzenverfärbung +-nekrosen Zyanosen Extremitäten Aufnahme über Blut Anlagerung an Erythrozyten Reifungsprozesse Kapillarblutfluß red. Blutungs-Erythrozytendeformation neigung Thrombosierung – Verbr.Koag. Ag auf Erythrozytenoberfläche Kälteagglutination Anämie - Azidose Störung von Wachstum + Fruchtbarkeit • • • • • • • • Abbau in der Milz - Fieber • akut: Fieber bis 42°C Apathie, Anorexie Anämie, vereinzelt Ikterus Zyanose, v.a. Ohrränder Extremitäten fein rötlicher Saum am Ohrrand chronisch: Kümmern, Blässe, allergische Hautreaktionen (Nesselsucht, Unterhautblutungen) Ohrrandnekrosen autoimmune hämolytische Anämie generalisierter hämolytischer Ikterus Eperythrozoonose Eperythrozoonose Hämatologie Diagnose • Blut aus akuter Fieberphase – wässrig, hämolytisch, z.T. ikterisch – Serumüberstand bei ikterischen Tieren deutlich höher als bei normalen – Mikroagglutination am gekühlten Röhrchenrand (Objektträger) – normochrome, normozytäre hämolytische Anämie – Erys, HB, Htkt: paralleler Rückgang – neutrophile Leukozytose – indirektes Bilirubin erhöht – Lichtmikroskopie bei 38°C • Verdacht bei hohem Fieber, Anämie, Ohrrandzyanose, allerg. Hautreaktionen • Erreger im Blutausstrich anfärbbar (38°C) • Akridin-Orange-Färbung Fluoreszenzmikroskop • Splenektomie beim Einzeltier provoziert akuten Anfall • PCR Eperythrozoonose Eperythrozoonose Differentialdiagnostik Therapie • • • • • • • Einzeltierbehandlung mit Langzeit-Oxytetrazyklin (Terramycin LA, 20 - 30 mg/kg) • Metaphylaxe durch orale Behandlung (Chlortetrazyklin [Aureomycin], 500 - 1000 ppm) • Eisengabe an chronisch Kranke und Ferkel • Elimination des Erregers aus dem Körper nicht möglich ESP (Leukopenie) Morbus maculosus Kannibalismus Staphylococcus hyicus Chron. Magengeschwür Eisenmangelanämie (hypochrome Anämie) Eperythrozoonose Eperythrozoonose Immunität und Impfung Prophylaxe • Impfung zur Zeit nicht möglich • nur schwache Immunität (2 – 3 M) • Reinfektion laufend möglich • Äußerste Hygiene bei zootechnichen Maßnahmen • Zwischendesinfektion des Bestecks bei hochgradigem Befall • Sebacil (Phoxim) Ivomec (Ivermectin) gegen Schweineläuse • Vermeidung von Überbelegung und Kannibalismus Leptospirose Leptospirose Steckbrief Steckbrief • Aborte und Fetopathien • in D selten • meist apathogene Formen • • • • • • • • Erreger: Leptospira sp. Anzeige/Meldepflicht: Betroffene Altersstufe: Feten, Sauen Besonderheiten: zahlreiche Spezies, auch Mensch, meist inapparent; Harnorgane besonders betroffen Inkubationszeit: 3 - 4 d Epidemiologie: enzootisch Heilung: Bedeutung: oft subklinisch, Zuchtbestände sollten frei sein Leptospirose Leptospirose Erreger Pathogenese • Klasse: Schraubenbakterien, Leptospiraceae • Aufbau: spiralig, Knopfende, beweglich, 0,1x6-20µm „Kleiderbügel“ • Serotypen: L. pomona, tarassovi, canicola, grippotyphosa, bratislava (oft apathogen), muenchen, australis • Besonderheiten: lokale Genitalinfektion • Tenazität: bis 30 d in Wasserpfützen • Verbreitungswege: Harn oder infiziertes Wasser, Deckakt, Ausscheidung mit Harn über 1 Jahr • Reservoir: Ratte, Hund, andere Haustiere • Desinfektion: Stalosan, gelöschter Kalk Bakteriämie Ansiedlung in Nieren, Plazenta, Fetus Ausscheidung mit Harn SMEDI Leptospirose Leptospirose Klinik • Sauen: Klinik • Bakteriämie: – Fieber bis 40°C – Aborte in letzten 3 w der Gravidität (Plazentation besonders innig) – Totgeburten, Lebensschwache – SMEDI • Ferkel und Mastschweine – leichtes Fieber, Hyporexie, Diarrhoe – selten zentralnervöse Symptome – meist inapparent – Fieber bis 40°C – Ikterus, Haemoglobinurie, Meningitis – Hyporexie, Diarrhoe • Spätere Folgen: – SMEDI – erhöhte perinatale Sterblichkeit Leptospirose Leptospirose Klinik Klinik Leptospiren lieben feuchtes Milieu Aufnahme: Schleimhäute Bindehäute Aborte im letzten Trächtigkeitsdrittel Leptospirose Leptospirose Klinik Sektion • abortierte Feten: – – – – – blutig-sulzige Subkutis braunrote Flüssigkeit in Körperhöhlen häufig herdförmige Lebernekrosen selten Ikterus keine spezifischen Veränderungen an Plazenta • Sauen: – Nieren vergrößert und bräunliche Sprenkelung Auch Mumien können auftreten, bei früher Infektion Leptospirose Diagnose • Erregeranzüchtung gelingt nur selten • Silbefärbung Nieren von Feten • PCR • sicherster Nachweis: AK im Blut 10 d p.i. Leptospirose Differentialdiagnostik • • • • SP (anhaltendes hohes Fieber) AK (hohe Saugferkelverluste, neurologische S.) Parvo Enteroviren Leptospirose Leptospirose Therapie Immunität und Impfung • Problem: latente Träger • Nierengängige Antibiotika • Alle Tiere des Bestandes einbeziehen • kommerzielle Schutzimpfung nicht verfügbar • stallspezifische Vakzine kann eingesetzt werden • parenteral 3 Tage 1x/d Streptomycin 10 mg/kg (Pen Strep 45) • Trimethoprim-Sulfonamid 20 mg/kg (Vetoprim 24) • anschliessend: 14tägige Futtermedikation Chlortetrazyklin 500 - 1000 ppm (Aureomycin) • (Nieren und Feten erreicht) Leptospirose Listeriose Prophylaxe Steckbrief • Nagerbekämpfung innerhalb u. außerhalb Betrieb • Einzeltierhaltung in infizierten Betrieben, um gegenseitige Übertragung zu verhindern • Ausläufe trockenlegen/befestigen • gesamten Stall desinfizieren • Stalosan oder gelöschten Kalk auf den Boden ausbringen • Elimination einzelner positiver Tiere in Zuchtbetrieben • Seltene, nur sporadische Erkrankung bei Schweinen • Zusammenhang mit verdorbener Silage Listeriose Listeriose Steckbrief Erreger • Erreger: Listeria monocytogenes u. innocua • Anzeige/Meldepflicht: M • Betroffene Altersstufe: v.a. Saugferkel und Sauen Mast: nur bei verdorbener Silage/CCM • Besonderheiten: v.a. bei Silagefütterung; sämtliche Tierarten, v.a. Schaf und Rind, keine Tier/Tier-Übertragung • Inkubationszeit: Stunden • Morbidität: • Mortalität: • Durchseuchung: • Epidemiologie: verschwindet bei Futterumstellung • Heilung: rasche Heilung bei Absetzen des Futters • Bedeutung: geringe Bedeutung • • • • • Listeriose Listeriose Pathogenese Klinik Tod bei Saugferkeln Septikämie orale Aufnahme mit verdorbener Silage ZNS-Störung blutige Durchfälle Aufbau: gram-positives Kurzstäbchen Serotypen: Stämme mit unterschiedlicher Hämolyse Besonderheiten: Tenazität: hoch Verbreitungswege: Einschleppung durch Ratten im Herbst; Keine Verbreitung zwischen Schweinen! • Reservoir: Ratten, Ausscheidung mit Kot; verunreinigtes Futter • Desinfektion: Stalosan / Kalk • Saugferkel: – Septikämie mit plötzlichen Todesfällen – Enzephalitis • Zittern, Kopfschiefhalten, Ataxie, Kreislaufen • Parese der Hintergliedmaßen • Sauen: – Aborte 1-2w a.p., Unfruchtbarkeit, Lebensschwache – Allg.Bef. ungestört • Mast: – Septikämie mit blutiger Enteritis – rasches Verenden Listeriose Listeriose Klinik Klinik Ausläufe können bedroht sein; Normalerweise Aufnahme mit dem Futter Listeriose Sektion • Enteritis in Dünn- und Dickdarm • evtl. Blutungen und Nekrosen • Leberzellnekrosen Aborte als häufige Folge Listeriose Diagnose • Erregerisolierung aus – Darminhalt, Leber, Milz, Hirn, Rückenmark • Untersuchung der Futterkomponenten • Serologie ohne Bedeutung Listeriose Listeriose Differentialdiagnostik Therapie • • • • • • • • Saugferkel: Leptospirose Brucellose PRRS AK ESP Kolienterotoxämie Streptokokkenmeningitis Durchfälle in der Mast • 2 - 3x parenteral Trimethoprim-Sulfonamid 25 - 50 mg/kg (Vetoprim 24), Penicillin 30.000 - 50.000 IE (Tardomyocel), Oxytetrazyklin 20 - 50 mg/kg (Terramycin) Listeriose Glässer´sche Krankheit Prophylaxe Steckbrief • • • • • Polyserositis und Arthritis • subklinisch weit verbreitet • Problematisch bei fehlender Immunität Keine Silage an Sauen verfüttern Unbefestigte Ausläufe: Stalosan oder Kalk keine verdorbene Silage in der Mast (Luftzufuhr) Immunprophylaxe nicht möglich Glässer´sche Krankheit Glässer´sche Krankheit Steckbrief Erreger • • • • • • • • • • Erreger: Haemophilus parasuis Anzeige/Meldepflicht: Betroffene Altersstufe: Saugferkel bis Läufer, v.a. Aufzucht Besonderheiten: nur Schwein: Pleuritis, Peritonitis, Pericarditis, Meningitis, Arthritis Inkubationszeit: 5 - 7 d Morbidität: 10 - 30 % Mortalität: 5 - 10 % Durchseuchung: perakut bis chronisch Epidemiologie: enzootisch Bedeutung: wirtschaftliche Verluste Haemophilus parasuis • Klasse: Pasteurellaceae • Aufbau: kleine gramnegative Stäbchen, Kapsel • Serotypen: min. 15 Serotypen: 1,5,10,12-14 besonders pathogen • Besonderheiten: v.a. im Alter von 3 - 8 w; • Tenazität: gering • Verbreitungswege: Tierkontakt • Reservoir: oberer Respirationstrakt nur bei Resistenzminderung: Polyserositis Glässer´sche Krankheit Pathogenese Infektion an der Muttersau Ansiedlung in Nasenhöhle bei schlechter Immunität Septikämie Fieber, Blutungen Ödeme, Pneumonie Systemische Organbesiedlung Glässer´sche KH Polyserositis (70 %) Polyarthritis (70 %) Meningitis (80 %) Fibrinausschwitzung Verklebungen symptomfrei eitrige Rhinitis PRRS, NH3 nasale Aufnahme fokale Zilienverluste Schleimhautschwellung Ansiedlung in Nasenhöhle (12 h) Petechien+Ekchymosen (Leber, Niere, Meningen) selten Zyanosen, Ödeme Polyserositis (70 %) Polyarthritis (70 %) Meningitis (80 %) Septikämie (36 h) Systemische Organbesiedlung Exsudatausschwitzung (Fibrin, Neurophile, Makrophagen) Glässer´sche Krankheit Glässer´sche Krankheit Klinik • Sporadisch 2 W bis 4 M, Akut: SPF-Bestand – Plötzliches Auftreten, rascher, schwerer Verlauf: Zyanosen, Septikämie • • Fieber bis 42°C, Apathie, Anorexie Peritonitis, Pleuritis, Arthritis – gekrümmter Rücken, Bauchdecke aufgezogen, Bauchdecke und Rippen schmerzempfindlich – flache Atmung, etwas Husten, Kopfstrecken – Lahmheit, leichte Bewegungsstörungen – Gelenksschwellungen – Herzbeutelentzündung: Herzrhythmusstörungen, Reibegeräusche – Ataxie und Seitenlage (Meningitis) • • Sektion • • • • • • • • Herzbeutelentzündungen u. -Verklebungen Brustfellentzündungen u. -Verklebungen Bronchopneumonie Vergrößerung von Milz und Leber Petechien auf Niere Gelenke mit dickflüssiger, gelb-grünlicher, fibrinöser Flüssigkeit Meningitis fibrinöse Verklebungen der Bauchhöhle nach einigen Tagen Tod oder Kümmern Überlebende oft mit - chron. Arthritiden - Verdauungsstörungen durch Darmverklebung Glässer´sche Krankheit Glässer´sche Krankheit Diagnose Erregernachweis • Verdacht aufgrund ausgeprägter Gelenksentzündungen • Typisches Sektionsbild (akute Phase) • Erregerisolation trotz eindeutiger Befunde oft nicht möglich Î PCR • höhere Inzidenz als vermutet • Nasentupfer, Serosen, seröse Flüssigkeiten Glässer´sche Krankheit Glässer´sche Krankheit Differentialdiagnostik Therapie • Streptococcus suis hBehandlung vor Fibrinausschwitzung erfolgreich hsofort ganze Tiergruppe behandeln • Enzephalitis+Polyarthritis, ohne Peritonitis und Pleuritis • Erysipelothrix rhusiopathiae • Hautrotlauf • Actinobacillus suis • Salmonella choleraesuis • Septikaemie • Escherichia coli • M.hyorhinis • Polyarthritis und Polyserositis bei Absetzern • ohne ZNS-Symptome und Todesfälle • Pasteurellose • Pneumonien mit Pleuritis h2 mal 7-tägige Trinkwasser/Futtermedikation hAmoxicillin 10 -20 mg oder 500 ppm hTrimethoprim/Sulfonamid 500 - 1000 ppm hUnterstützung durch Dexamethason hoft Resistenzen gegen Tetrazykline, Penicillin Glässer´sche Krankheit Immunprophylaxe Therapie Porcillis Glässer Intervet ka jd sd ds fbkd ksbv jks ffbk sfjk cbs db asd sdjb dk fk sd jk bs bk ksd db ö s v jks dd vb Immunologie und Immunprophylaxe z.B Amoxicillin Penicillin Pulmotil Trimetoprim/ Sulfonamide • stallspezifische Vakzine verhindert klinische Symptome • Sauen 6 und 3 w a.p. • Impfung der Ferkel während Aufzucht • kommerzielle Vakzine: Porcilis Glässer Glässer´sche Krankheit Streptococcus suis Prophylaxe Steckbrief • • • • Ferkel infizieren sich bereits in 1. LW immunologisches Gleichgewicht einstellen Jungsauenüberhang abbauen Kein Mischen unterschiedlicher Altersstufen und Herkünfte • Quarantänemaßnahmen • Verlustreiche Erkrankung von Ferkeln und Absetzern mit: Streptococcus suis Streptococcus suis Steckbrief Erreger • Erreger: Streptococcus suis • Anzeige/Meldepflicht: • Betroffene Altersstufe: Saugferkel (Typ 1); Absatz- und Mastschweine (Typ 2); • Besonderheiten: Zoonoseerreger • Inkubationszeit: 1d – 2w • Morbidität: meist < 5 %, trotz 100 % Träger • Mortalität: je nach Organsystem • Durchseuchung: schleichend • Epidemiologie: enzootisch • Heilung: bei früh einsetzender AB-Therapie • Bedeutung: sehr große Bedeutung • Aufbau: grampositive Kokken α-hämolytisch • Serotypen: 35 Typen; Typ 1: v.a. Saugferkel, seltener; Typ 2: v.a. Absatz- und Mastschweine • Besonderheiten: Zoonose-Erreger • Tenazität: mäßig • Verbreitungswege: Kot, Tierkörper, infizierte Tiere, Fliegen, Schadnager • Reservoir: Latent infizierte Sauen; Tonsillen; Infektion der Ferkel unmittelbar p.p.; dichte Stallbelegung, Absetzstress • Desinfektion: Formalin • Meningitis • Arthritis • Pneumonie Streptococcus suis Streptococcus sp. (+ dysgalactiae) Pathogenese Krankheitsbilder Gelenke Pneumonien in Aufzucht/Mast Endocarditis Septikämie Streptokokken- Saugferkel RespiraMenigitis tionstrakt Aufnahme: Durchdringen der Blut-Hirn-Schranke Genitaltrakt Sau abortierte Foeten Ansiedlung in Makrophagen Trojanisches Pferd Verstärkt durch PRRS Influenza Schleimhaut Nabel, Zahnfleischverletzungen Hautscheuerstellen Kastrieren • • • • • • Streptococcus suis Streptococcus suis Sektion Klinik • • • • • • • Absetzer von 5 bis 8 W Saugferkel ab 1. Woche perakut plötzliche Todesfälle Septikämie mit Fieber (42,5°C) – sonst zunächst symptomlos – Inappetenz, matt, lustlos Streptokokkenmeningitis – Zittern, Ataxie, Seitenlage, Ruderbewegungen, Ophistotonus, Kopfschiefhaltung, Nystagmus – starrer Blick, hochrote Konjunktiven Arthritis – Lahmheit, Gelenksentzündung Pneumonie – Husten, Dyspnoe • Enzootische Streptokokkenmeningitis Arthritis purulenta Polyarthritis bei Saugferkeln Pericarditis, Endocarditis Cystitis, Endometritis, Mastitis Paraplegie durch Rückenmarksabszesse • • • eitrige Meningitis eitrige Gelenksentzündung Pneumonie – Pleuritis, Pericarditis – hochgradige Bronchopneumonie • • • • Erweiterung von Subduralraum und Ventrikeln grau-weiße bis gelblichrote trübe Exsudatfüllung Hyperämie fibrinopurulente oder lympholeukozytäre Infiltrate in Meningen und Ventrikel Hirnödeme Exsudat: grampositive Diplokokken fibrinöse – fibrinopurulente Bronchopneumonie mit Pleuritis • • • – primär oder sekundär, Bronchopneumonie Polyserositis, Endocarditis Streptococcus suis Diagnose • Klinik und Erregernachweis • Tupferproben – von sezierten Ferkeln (Hirn, Lunge) – aus Gelenkspunktaten – aus Lungenspülproben • Serum-AK ab d5 Streptococcus suis Differentialdiagnostik • ZNS: • Ödemkrankheit • AK • Kochsalzvergiftung • Gelenke und Lunge: • Hämophilus parasuis • Mycoplasmen • Rotlauf Streptococcus suis Streptococcus suis Therapie Immunität und Impfung • Streptokokken-Meningitis • Stallspezifische Vakzine • parenteral Penicillin • in frühem Stadium erfolgreich • einmalige Antiphlogistika-Gabe (Voren, Finadyne) • Grundimmunisierung des Sauenbestandes 2 x Abstand 3 - 4 Wochen • Auffrischungsimpfung, spätestens 2w a.p. oder 3 x/a • einzugliedernde Jungsauen mit einbeziehen • spezifische Vakzine regelmäßig aktualisieren • Streptokokken-Infektion Aufzuchtferkel • mehrmalige Gabe von Amoxycillin (Clamoxyl, Duphamox) • Metaphylaxe der Wurfgeschwister • Atemwege und Gelenke betroffen: • Einzeltierbehandlung • Metaphylaxe über Trinkwasser mit Amoxicillin ZNS-Störungen beim Schwein Streptococcus suis Prophylaxe Ätiologie • Waschung der Sauen vor dem Einstallen • Zwischendesinfektion 1x/w • Hygiene beim Abnabeln, Zähneabschleifen, Kastrieren, Schwanzkupieren • Haltungsdichte • Abteilweise Rein-Raus • gründliche R+D • Fußbodenbeschaffenheit • Nabeldesinfektion Hypoglykämie Zitterferkel Eisenvergiftung Organophosphate NaCl-Vergiftung AK ESP VW Tollwut Tetanus Ödem Listeriose Strc.-Meningitis Neurologische Störungen beim Schwein Tollwut AK, NaCl, Hypoglycämie Strc.Meningitis, Listeriose, Hämophp. Kochsalzvergiftung + respirator. + Gelenke + Diarrhoe + Fruchtbarkeitspr. + Fieber Paralyse Parese Motorischer Ausfall Ataxie Ferkelzittern Norm • ZNS-Symptomatik – Muskelzittern – klonische Krämpfe, Speicheln, – Zwangsbewegungen – Histo: perivaskuläre eosinophile Granulozyten im ZNS, Ödematisierung • Durchfall • Tod in Seitenlage innerhalb weniger Stunden möglich • Nierenversagen, harnpflichtige Stoffe Ödem ESP Saugferkel Saugferkel Saugferkel ZNS, ganzer Bestand, ... mehrere Tiere, jedes Alter Altersklassen, mehrere Tiere seuchenhaft, atypisch Magen selten, Freiland selten, Sägebock Absetzen, Ödeme Futterfehler Einzeltiere, Abszesse, Husten Diagnose Sensorium gestört SE Teschen Abweichung Klonisch Tetanus Tonisch Motorische Reizung Enterovirus-Enzephalomyelitis (Teschen/Talfan) Steckbrief • Enteroviren ubiquitär verbreitet • unterschiedliche Virulenz • Teschen: ansteckende Schweinelähme (PEV1) • schweineadaptierte Viruserkrankung mit Neurotropismus • Poliomyelitis • Talfan • gutartige Variante • Myelitis Teschen/Talfan Steckbrief • Erreger: Picorna-Virus • Anzeige/Meldepflicht: A (Teschen) • Betroffene Altersstufe: Saugferkel lethal, Läuferstadium inapparent • Besonderheiten: analog zur menschlichen Poliomyelitis kann SMEDI auslösen • Inkubationszeit: 8 - 30 d • • • • • • Morbidität: niedrig Mortalität: niedrig bis hoch Durchseuchung: endemisch Epidemiologie: Sporadisch Heilung: Talfan kommt zur Ausheilung Bedeutung: D: seit Jahrzehnten nicht mehr nachgewiesen Teschen/Talfan Teschen/Talfan Erreger Pathogenese • • • • • • • • Klasse: Picorna-Viren Aufbau: RNA-Virus, extrem klein Serotypen: Teschen – Talfan, PEV 1-13 Besonderheiten: entspricht Kinderlähmung des Menschen Tenazität: Verbreitungswege: Eintritt über Verdauungskanal Reservoir: Latent infizierte ältere Schweine Desinfektion: schwierig weitgehende Durchseuchung in D meist subklinische Ausscheider Lähmungen Fieberhafte Allgemeinerkrankung immunogen Vermehrung neurovirulenter Stämme im ZNS Virämie Teschen/Talfan Klinik • Akut: Teschen (Hirn-Rückenmarksform) – v.a. Ferkel – kurzer Fieberschub, 40 - 41°C – danach nervöse Anzeichen • • • • Zittern der Nierenpartie beim Gehen Fallen auf die Hinterhand beim Umdrehen vollst. Festliegen nach 1 - 2 d Sensorium ungestört! – jetzt massive Enzephalitis: • • • • • • • • Zittern des Kopfes, Zähneknirschen, Nystagmus Schlundkopflähmung - heissere Schreie weder Wasser- noch Futteraufnahme möglich Muskeltremor, tonisch-klonische Krämpfe Ophistotonus, Nystagmus Hinterhandlähmung hohe Mortalität und Morbidität Tod unter Dyspnoe und Herzinsuffizienz orale/nasale Aufnahme Vermehrung im Verdauungstrakt Ausscheidung mit dem Kot Teschen/Talfan Klinik • Perakut: Teschen – sehr selten – sofortiges Festliegen und vollständige Lähmung – Tod 2 d nach ersten Symptomen • Chronisch: Teschen – bei ausgewachsenen Tieren – Enzephalitis bleibt aus Teschen/Talfan Teschen/Talfan Klinik Klinik • Gutartige Form: Talfan (Myelitis) – – – – Fieberanfall mit Schwäche d. Hinterhand torkelnder Gang, Extremitäten gekreuzt Allgemeinzustand ungestört, Anorexie nur wenige Tiere aus einer Gruppe • Schwere Form: Talfan – – – – – Lähmung der Hinterhand Hinterteil beim Laufen nachgezogen Lähmungssymptome können bestehen bleiben geringe Mortalität, Allgemeinbefinden bleibt o.k. Sensibilität bleibt erhalten (evtl. Hyperästhesie) Lähmung bei voll erhaltenem Sensorium Teschen/Talfan Teschen/Talfan Klinik Sektion • Ganglienzelldegenerationen in Kleinhirn, Hirnstamm, RM • vaskuläre und perivaskuläre Infiltrate • = nichteitrige Polioenzephalomyelitis Mastschwein mit Schwäche der Hintergliedmaße Teschen/Talfan Diagnose • Klinischer Verdacht + Virusnachweis aus Gehirn u. Rückenmark (bis 2 d nach Auftreten neurologischer Symptome) • Serologie unsicher durch Kreuzreaktion mit Enteroviren • Verlaufsserologie Teschen/Talfan Differentialdiagnostik • • • • • • AK Kolienterotoxämie ESP Arsanilsre-Vergiftung Se, Hg-Vergiftung Rückenmarksabszesse Teschen/Talfan Teschen/Talfan Therapie Immunität und Impfung • keine • umfangreiche, stille Durchseuchung in D Teschen/Talfan Pityriasis rosea Prophylaxe Steckbrief • keine Besonderheiten • Abschaffung der Anzeigepflicht erwartet. - Unbekannte Ätiologie Evtl. genetische Komponente (autosomal) Einzeltiere bis mehrere Tiere Hautveränderungen ab 2 - 4 w - 2- 3 cm, rötliche Flecken Flankengegend - konfluieren zu großflächigen Arealen, v.a. im Bauchbereich - geröteter Rand, Zentrum unauffällig - Vollständige Abheilung nach 8 w Nicht infektiös Keine Behandlung notwendig oder möglich Keine Wachstumsbehinderung Pityriasis rosea Parakeratose Klinik Steckbrief - Zinkmangel führt zu mangelhafter Verhornung der Epidermis Parakeratose Parakeratose Steckbrief - Klinik Verstärte Bildung unausgereifter Epithelzellen klebrige, panzerartig eintrocknende Borken v.a. bei Läuferschweinen, aber auch ältere Tiere hofeigene Futtermischung - > 0,5 % Kalzium - reichlich Phytin - weniger als 30 ppm Zn - Selbstheilung 6 - 12 w nach Krankheitsbeginn, auch ohne Zn-Zusatz • 1. Hautrötungen, Innenseite Beine, Bauch, Brustunterseite, Ohrgegend, Perianalbereich • 2. Bildung von Knötchen • 3. Zusammenfließen zu braun-schwarz klebrigen Borken • Juckreiz! Scheuern im Sitzen • Abheilung Unterbauch und Gldmaßen zuletzt • Auch Klauenschäden können vorkommen Parakeratose Parakeratose Klinik Vorbeuge und Bekämpung • • • • 0,5 g ZnCO3 je Läufer und Tag Allgemeinbefinden und FA verbessert 2. Woche: Rückbildung der Hautsymptome 3 Wochen lang behandeln (Rezidive) Beine sind besonders stark betroffen Pocken Pocken Steckbrief Erreger - - Klasse: Poxviridae Erreger: Suipox-Virus Anzeige/Meldepflicht: M Betroffene Altersstufe: Alle, besonders 4. - 12. LW Besonderheiten: lokal bis generalisiert Inkubationszeit: 4 - 7d (Haut); 12 - 24 d (Nasen-Rachen) Morbidität: bis 100 % Mortalität: 3 - 5% Durchseuchung: Epidemiologie: epizootisch Heilung: ja Bedeutung: Durch Hautschäden keine Qualitätsferkel - Tenazität: in Krusten über Monate infektiös - Verbreitungswege: Läuse, Zukauf Pocken Pocken Pathogenese Klinik • klassisches Pockenexanthem • kleine Knötchen mit gerötetem Zentrum oro-nasale Aufnahme Primärpocke – Blasenbildung in der Mitte (Blasenstadium) – Pusteln trocknen ein - Pfennig-große Kruste (Krustenstadium) • Perakute septikämische Form bei Neugeborenen – – – – Fehlen der typischen Pusteln lediglich Durchblutungsstörung der Haut krank geborene verenden nach wenigen Stunden Totgeborene Virusvermehrung Fieber Pocken Pocken Klinik Diagnose • Klinisches Bild reicht aus durch typische Hautveränderungen • Erregernachweis nicht notwendig - Pocken Pocken Therapie Immunität und Impfung - Keine direkte Behandlungsmöglichkeit - Sebacil-Lsg auf Haut aufsprühen gegen Sek. Inf. - Stabile Immunität - mit Kolostrum auf die Ferkel übertragen - Vakzine steht nicht zur Verfügung Pocken Aktinomykose Prophylaxe Steckbrief - Läusebekämpfung - R+D unterbricht Infektionskette - Strahlenpilz - Häufige Abgangsursache für Sauen Aktinomykose Aktinomykose Steckbrief Erreger - - Klasse: Actinomyceten - Aufbau: grampositives Bakterium - Besonderheiten: Drusenbildung mit pilzmycelartiger Struktur im Eiter - Verbreitungswege: Ausgehend von Mundflora der Ferkel Bißverletzungen - Reservoir: bei gesunden Schweinen: Tonsillen, Mundflora; Fistelmaterial erkrankter Tiere! - Erreger: Actinomycis suis Anzeige/Meldepflicht: Betroffene Altersstufe: Sauen Besonderheiten: Regelmäßige Begleitkeime: Coli, Staphys, Streptos, Corynebakterien Inkubationszeit: bis mehrere Wochen Morbidität: bis 50 % Mortalität: 0 % Durchseuchung: Epidemiologie: enzootisch Heilung: Bedeutung: kann Hauptabgangsursache von Sauen sein Aktinomykose Aktinomykose Klinik Klinik • Bildung einzelner oder multipler Knoten im infizierten Gesäugekomplex • Erbsen- bis Gänseeigroß • Bi-Ge-Ummantelung, zentraler Eiterherd • Fistelöffnungen mit Eiterentleerung • Durchbruch als blutende Geschwüre nach außen • Endphase: gestielte, pendelnde Aktinomykome • Allgemeinbefinden ungestört • keine Hinweise auf Schmerzen häufiger bei Strohhaltung Aktinomykose Sektion • Typische Aktinomykome Aktinomykose Diagnose • Charakteristisch: – derbe Aktinomykome mit deutlicher Größenzunahme, Abzess- und Fistelbildung – Erregernachweis aus sandkorngroßen Drusen im Eiterinhalt Aktinomykose Aktinomykose Therapie Immunität und Impfung - Parenterale Behandlung - Immunität nicht ausreichend - keine Impfung möglich - Penicillin Tardomyocel, Amoxytetracyclin, Baytril - 4 - 5 mal im Abstand von 2 - 3 Tagen - Bestandsbehandlung bei gehäuftem Auftreten zur Eindämmung der Ausbreitung - über 2 - 3 w - Amoxicillin 500 - 1000 ppm - Chlortetracyclin 500 - 1000 ppm - Neuerkrankungen und Rückfälle Aktinomykose Aktinobazillose Prophylaxe Steckbrief - Schlachten erkrankter Tiere nach Absetzen, da Ansteckungsquelle - Abschleifen der Eckzähne - Infektions-begünstignde Puerperalerkrankungen behandeln - Harmloser Erreger, der in Herden mit sehr hohem Hygienestatus zum Problem werden kann Aktinobazillose Aktinobazillose Steckbrief Pathogenese Infektion über Hautverletzungen - Erreger: Actinobaculum suis Anzeige/Meldepflicht: Betroffene Altersstufe: Alle Epidemiologie: enzootisch Bedeutung: bei hohem Hygienestatus immunologische Lücken - Reservoir: bei gesunden Schweinen: Haut, Genitalschleimhaut, Tonsillen fehlende Immunität Septikämie Aktinobazillose Aktinobazillose Klinik Klinik Ansiedlung • Infektion 1. - 6. LW – Gelenksentzündungen – Herzklappenentzündungen – Septikämie mit plötzlichen Todesfällen • Mast: – Hautrötungen, ähnlich Rotlauf – Hautnekrosen Nacken/Ohrbereich Vormastschwein mit fleckigen Hautläsionen Aktinobazillose Aktinobazillose Klinik Sektion • Gelenksentzündungen • Herzklappenentzündungen Vormastschwein mit fleckigen Hautläsionen Aktinobazillose Diagnose • Klinik und Sektion nicht sehr typisch • Erregeranzüchtung notwendig Aktinobazillose Differentialdiagnostik - entspricht weitgehend Rotlauf Aktinobazillose Aktinobazillose Therapie Immunität und Impfung - Einmalige Injektionsbehandlung aller Ferkel des Wurfes mit Penicillin ist ausreichend - Bei gehäuftem Auftreten Bestandbehandlung mit - Stabile Immunität - Kolostralschutz für 8 w - Amoxicillin 250 - 500 ppm - Tetracyclin 500 - 1000 ppm - Tilmicosin 400 ppm Exsudative Epidermitis Steckbrief - Ferkelruß Pechräude Nässendes Ekzem seborrhöisches Ekzem - akute lebensbedrohliche Situation für Saugferkel - leichte Fälle bei älteren Ferkeln - sporadisch oder Bestandsproblem Exsudative Epidermitis Epidemiologie - Grossbetriebe Frühes Absetzen Hohe Besatzdichte Uneinheitliche Immunität (JS) - verschiedene Serovare Symptome über 2-3 Mo zahlreiche Würfe betroffen bis 70 % Mortalität Exsudative Epidermitis Exsudative Epidermitis Erreger Pathogenese - Staphylococcus hyicus - Grampositive Kokken - 8 Serovare; virulente/avirulente Typen nicht unterscheidbar - bei Gesunden: Exfoliatives Toxin Separation des Str. germinativum und corneum - Nasenschleimhaut, Konjunktiven, Haut, - Vagina: Besiedlung der Ferkel bei Geburt - hohe Tenazität (wochenlang im Stall) - aerogene Übertragung möglich; Läuse - Schäden durch ein Stoffwechselprodukt (exfoliative Substanz); Schäden an Haut, Niere, Harnleiter und Gehirn (Spätfolgen) Exsudative Epidermitis Infektion über Hautverletzungen Hautrötung Exsudation Ansiedlung fehlende Immunität Entzündung Dehydratation (Neutrophile) Hyperplasie Exfoliatives Toxin Lnn Septikämie Exsudative Epid. Pathogenese Opsonierung Antikörper Protein A (Fc) Adhäsion durch Fibronectin bindendes Protein Klinik • Generalisierte Form Makrophagen Hautbarriere Kapsel Aggregation Katalase Exfoliatives Toxin Kapsel Fibronektin bindendes Protein Staph hyicus Exsudative Epid. Klinik • Generalisierte Form – Saugferkel, Ende 1. LW bis 5./6. LW – gesamter Körper mit abgestoßenem Epithel + Exsudat – Haut krustig verdickt, von Rissen durchzogen – leichter Verlauf: nur dünner bräunlicher Belag ohne Erosionen, kein Juckreiz, meist ohne Fieber – Überlebende kümmern – Blasen/Geschwüre am Maul – Hornablösung am Ballen – Tod in 24 h bis 10 d möglich – Saugferkel, Ende 1. LW bis 5./6. LW – gesamter Körper mit abgestoßenem Epithel + Exsudat – Haut krustig verdickt, von Rissen durchzogen – leichter Verlauf: nur dünner bräunlicher Belag ohne Erosionen, kein Juckreiz, meist ohne Fieber – Überlebende kümmern – Blasen/Geschwüre am Maul – Hornablösung am Ballen – Tod in 24 h bis 10 d möglich Exsudative Epidermitis Klinik • Lokale Form: – dunkle runde Flecken, unterschiedliche Größe und Anzahl – ganzer Körper, vorwiegend jedoch haarlose Stellen Nasenrücken, Ohrgrund, Ohren – kein Juckreiz – v.a bei älteren Saugferkeln, Absetzern und Läufern Exsudative Epidermitis Klinik • Lokale Form: – dunkle runde Flecken, unterschiedliche Größe und Anzahl – ganzer Körper, vorwiegend jedoch haarlose Stellen Nasenrücken, Ohrgrund, Ohren – kein Juckreiz – v.a bei älteren Saugferkeln, Absetzern und Läufern Exsudative Epidermitis Sektion • Lokale Form: – keine Organveränderungen feststellbar • Generalisierte Form: – – – – – – Hautentzündung mit Ablösung der Oberhaut klares Exsudat schmierige, stinkende Krusten weißliche Urat-Ausfällungen in der Niere Verdickung des Harnleiters Lebervergrößerung, vollkommen leerer Magen – intraepidermale Pusteln und Bläschen – perivaskuläre Entzündung – Kulturen in verhornten Schichten Exsudative Epidermitis Exsudative Epidermitis Differentialdiagnostik Therapie - Pocken: linsengrosse, erhabene Pusteln, lokalisiert - Parakeratose: Juckreiz - Toxinwirkungen therapeutisch nicht zu beheben - AB Behandlung der generalisierten Form oft unbefriedigend - Sulfonamide, Lincomycin - Auch wirksame AB (Resistenztest) oft ohne Erfolg - Corticosteroide, Immunseren, Desinfektionsbäder/-Salben lindern - Stallspezifische Vakzine als Mittel der Wahl Exsudative Epidermitis Exsudative Epidermitis Immunität und Impfung Prophylaxe - Stabile Immunität - mit Kolostrum auf die Ferkel übertragen - bei nachlassen des maternalen AK-Schutzes in immunen Beständen: enzootische, mildere, lokale Form bei Absetzern - Vakzine steht nicht zur Verfügung - Stallspezifische Vakzine als Mittel der Wahl - Zähne abschleifen - AB-haltige Sebacil-Lsg beim Absetzen und Einstallen zur Mast, zur Versorgung von Rangordnungs-Wunden - Haltung verbessern - Sauen waschen - alle JS + AS 6 und 3w a.p. - Auffrischung alle 4 -5 Monate oder vor nächstem Wurf - Serotypen beachten! Sarcoptes Sarcoptes Steckbrief Erreger - - Erreger: Sarcoptes scabiei var. suis Anzeige/Meldepflicht: Betroffene Altersstufe: Alle Besonderheiten: Inkubationszeit: 2 - 8 d Morbidität: 40 bis 80 % Mortalität: 10 - 80 % Durchseuchung: Epidemiologie: enzootisch Heilung: ja Bedeutung: klinisch heute selten, subklinisch weit verbreitet; große wirtschaftliche Einbußen Klasse: Sarcoptes Aufbau: 0,25 - 0,5 mm Serotypen: Besonderheiten: Tenazität: hoch Verbreitungswege: Übertragung Sau - Ferkel; Eber Sauen - Reservoir: latente Träger, Altsauen Sarcoptes Sarcoptes Pathogenese Klinik Weibchen in Gängen tieferer Hautschichten nach 21 d Männchen auf Hautoberfläche nach 14 d Paarung Einbohren in tiefere Schichten Eiablage 2 saugende Nymphenstadien • • • • • Schlupf der Larven nach 2 - 4 d • • • • • • • Beginn am Kopf Innenseite der Ohren! Umgebung der Augen, Nasenrücken Ausbreitung über gesamten Körper Fesseln, Bauchunterseite, Hüfthöcker, Schenkelinnenseiten zunächst pustelartige Hautrötungen Juckreiz ab 2 - 3w p.i. - dauerhaftes Scheuern Hautverdickungen, Falten, Borken Hautareale Eintrittsstellen für Bakterien und Viren starke Unruhe verminderte Leistung Verminderte Fruchtbarkeit Aggressivität der Eber Sarcoptes Sarcoptes Klinik Klinik • wirtschaftliche Schäden (klinisch + subklinisch) – – – – reduzierte Futterverwertung reduzierte Zunahmen geringere Aufzuchtleistung gestörte Fruchtbarkeit Eber als Überträger im Bestand: Nacken/Kopfbereich, Hodensack Sarcoptes Sarcoptes Klinik Diagnose • Rubbing Index RI – Anzahl Kratzeinheiten/10 Sauen/15 Minuten – >1=bestätigt; <0,4 o.k. • Mikroskopischer Erregernachweis aus Hautgeschabsel (Gehörgang) – geringste Empfindlichkeit • Digestionsmethode aus Hautgeschabsel – 35%ige Sicherheit • Serologie ELISA – AK 6w - 9m p.i. nachweisbar – Sensitivität: 60 - 80 % • Dermatitis score am Schlachthof frühes Stadium, Schenkelinnenseite Sarcoptes Sarcoptes Differentialdiagnostik Therapie - Pocken - Parakeratose - Exsudative Epidermitis - Bei Waschung alle Stellen erreichen (Ohr, Innenschenkel) - Wiederholung nach 7 - 10 Tagen - Systemisch: zweimalig - Ivermectin (Ivomes-S oder I.-Prämix [7 d]) - einmalig: Dectomax (Doramectin) Sarcoptes Sarcoptes Immunität und Impfung Prophylaxe - nur klinische Symptome unterdrückt - Sauen regelmäßig waschen und behandeln Demodikose Steckbrief - Demodikose Klinik In D sehr seltene Haarbalgmilbe Ei, ein Larven, 2 Nymphenstadien dauert 4 w befruchtete Weibchen bohren sich in die Haut Ablage der Eier in den Bohrgängen Übertragung durch Körperkontakt Tier/Tier Tenazität: bis 2w Faktorenkrankheit - Stoffwechselstörung, Mangelernährung, Allgemeininfektionen • bevorzugt: Augenlider, Rüssel, Backen, Halsbereich • bei starkem Befall + Unterbauch, GldmßInnenflächen, Beugeflächen der Gelenke • Milben in Unterhaut und Haarbälgen • bis erbsengroße Knötchen und Pusteln • bei starkem Befall: Haarausfall und Hautverdickung mit leichtem Juckreiz • Diagnose: Milbennachweis in Pustelinhalt / Hautgeschabsel Demodikose Demodikose Klinik Klinik Pusteln und Knötchen Augenbereich Knötchen im Brustbereich Demodikose Schweinelaus Behandlung und Vorbeuge Steckbrief - Bei Waschung alle Stellen erreichen (Ohr, Innenschenkel) - Wiederholung nach 7 - 10 Tagen - Systemisch: einmalig reicht - Faktorenkrankheit bei Abwehrschwäche mit wirtschaftlichen Einbußen durch Unruhe und Juckreiz - Ivermectin (Ivomes-S oder I.-Prämix [7 d]) - Phoxim (Sebacil oder S.Pour-on) Schweinelaus Schweinelaus Steckbrief Erreger - - Klasse: Insekten - Aufbau: 5 - 6 mm, braun, breiter Körper, schmaler Kopf - Eier 1 mm, an Borsten angeklebt - Serotypen: - Besonderheiten: bevorzugt Nacken, Kopfbereich, Schultern, Flanken, Ernährung vom Blut des Wirts - Tenazität: nur wenige Tage - Verbreitungswege: Übertragung: direkter Tierkontakt - Erreger: Haematopinus suis Anzeige/Meldepflicht: Betroffene Altersstufe: Alle Besonderheiten: nur bei schlechter Haltung/Mangelfütterung, Abwehrschwäche Faktoren: Vitamin/Mineralstoffmangel, unausgeglichenes Ca/P-Verhältnis, Lichtarmut Durchseuchung: Epidemiologie: enzootisch Heilung: ja Bedeutung: klinisch heute selten, subklinisch verbreitet große wirtschaftliche Einbußen Schweinelaus Schweinelaus Pathogenese Klinik erwachsene Läuse Paarung nach 3 - 4w Eiablage • • • • • Blutaufnahme 6 x /Tag - Einstich + Umherwandern Juckreiz, Unruhe, Scheuern und Kratzen Entzündliche Hautveränderungen Störung des Allgemeinbefindens Jungtiere mit starkem Befall: – Blutarmut (Porzellanferkel), Eisenmangelanämie – schlechte Zunahmen und Futterverwertung – verlängerte Mastdauer • Überträger von ESP, Pocken und Eperythrozoonose 3 saugende Nymphenstadien Schlupf der Larven Schweinelaus Schweinelaus Klinik Klinik Läuse sind mit bloßem Auge zu entdecken An den Borsten finden sich Nissen Schweinelaus Schweinelaus Diagnose Therapie • mit bloßem Auge zu stellen – adulte Tiere – Nissen - Therapie zusammen mit Räudebekämpfung - Bei Waschung alle Stellen erreichen (Ohr, Innenschenkel) - Wiederholung nach 7 - 10 Tagen - Systemisch: einmalig reicht - Ivermectin (Ivomes-S oder I.-Prämix [7 d]) - Phoxim (Sebacil oder S.Pour-on) Schweinelaus Schweinelaus Immunität und Impfung Prophylaxe - klinische Symptome unterdrückt - Sauen regelmäßig waschen und behandeln PRRS PRRS Steckbrief • Porzines Reproduktives und Respiratorisches Syndrom • chronisch-rezidivierende Pneumonien bei Absetzern und in der Mast • geringe eigene Valenz aber Wegbereiter für Sekundärinfektionen • Seuchenhafter Spätabort • Seit 1990 Steckbrief • • • • • • • • • • • Erreger: Arterivirus Anzeige/Meldepflicht: Betroffene Altersstufe: alle Besonderheiten: Befall und Reduktion der Lungenmakrophagen Inkubationszeit: 1-3d Morbidität: 0 - 100 % Mortalität: 0 - 15 % Durchseuchung: Monate bis Jahre im Bestand Epidemiologie: enzootisch Heilung: gute Haltungsbedingungen: nach 3 - 5w Bedeutung: weit verbreitet; Sekundär-Erreger! Porcines Reproductives und Respiratorisches Syndrom PRRS Erreger PRRS • Klasse: Arteriviren • Aufbau: behülltes RNA-Virus, 15 kb • Serotypen: unterschiedlicher Virulenz; europäischer/amerikanischer Typ • Besonderheiten: Persistenz für ca. 6 M • Tenazität: gering (37°C, Trockenheit), lang bei Minusgraden; bis 1 w bei RT; pH 6,5 – 7,5 • Desinfektion: Detergentien • Verbreitungswege: Tierhandel!!!; aerogen (Mastbetriebe!: 3 km); Transportfahrzeuge, Sperma, Harn, Gülle Ausscheidung über alle Körpersekrete ab 2d p.i. für mind. 1 Monat; intrauterin • Epidemiologie: neg. JS in persistente Herde Absatzferkel 6. – 9. LW • Reservoir: latent infizierte Tiere • Erhebliche ökonomische Einbußen • Wellenförmiger Infektions- und klinischer Verlauf mit Herdenpersistenz • Neutralisierende Antikörper nach 4-8 Wochen, Abbau innerhalb ca. 5 Monaten • Virusausscheidung über alle Sekrete und Exkrete, oft über Monate. • Brennpunkte im Bereich Ferkelaufzucht und Jungsaueneingliederung • Interaktion mit Co-Erregern: PCV2! PRRS – Klinik/Pathologie PRRS – Klinik/Pathologie • Reproduktionsstörungen bei Neuausbruch • Klinisches Bild sehr variabel – Spätabort, Totgeburten, Lebensschwache – Tieralter – Resistenzlage und Immunität – Virustyp und Sekundärerreger • Endemisch: Respiratorische Störungen PRRS PRRS Klinik • • • • • • • • • Pneumonie wechselndes Fieber hochrote Konjunktiven blaurote Ohren, Gesäuge Lidödem, Augenausfluß, Rhinitis Krankheitsbeginn völlig asynchron wellenförmiger Verlauf Sauen: Anorexie, reproduktive Störungen: Spätabort (um 110. d) erneute Erkrankung wenige Tage nach scheinbar erfolgreicher ABTherapie Klinik • Mast – FA vermindert, Auseinanderwachsen – Leistungsdepression um ca. 20 % – höhere Totalverluste, Anfälligkeit – Zunahmen um 30 -150 g/d vermindert – Bindehautentzündung bei > 5 % – Rhinitis bei mind. 5 % – vereinzelt Brüllhusten – vereinzelt Fieber > 39,5°C – Hirnhautentzündungen (sek. Erreger) – blaurote Ohren – va. Vormastschweine 30 bis 60 kg – Erkrankungsdauer mind. 3 Wochen PRRS PRRS Klinik Klinik • Sauen • Absatzferkel – akut: • > 5 % Verluste, vermehrt Kümmerer • Atemwegserkrankungen, Bindehautentzündungen – chronisch: • > 3 % Verluste, vermehrt Kümmerer • Atemwegserkrankungen (Bindehautentzündungen) • vermehrt Infektionen durch Sek.-Erreger • rezidivierendes Aufflackern von Bestandsproblemen – akut: • Aborte 105.-113. Tag, • Totgeburten, Lebensschwache, • Plötzliche Todesfälle bei Sauen, • Anorexie, Fieber bis 41°C/ Untertemperatur • Zyanosen Ohren und Unterbauch – chronisch: • < 10,5 leb.geb.Ferkel/Wurf • > 0,7 tot geb. Ferkel/Wurf • > 5 % Frühgeburten • > 3 % Würfe mit < 7 Ferkel • Umrauscher > 15 %, verzögertes Umrauschen • verlängerte Trächtigkeit bis 120 d • hohe Saugferkelverluste (lebensschwache Ferkel) PRRS PRRS - Verlauf Sektion 120 Persistenz Virämie 100 % /R e la t iv • hochgradig proliferative interstitielle Pneumonie • gesamte Lunge betroffen • je nach Begleitkeimen 80 60 AK 40 T-Zellen Klinik 20 0 0 3 7 14 21 30 50 70 90 100 110 120 135 Tage p.i. nach Murtaugh 2004 Pathogenese: - Infektion PRRS - Verlauf LPS, Bakterien, Viren, etc. • lang andauernde Virämie nach Abklingen klinischer Symptome • Lymphatische Persistenz über Monate Î latente Ausscheider Î Übertragung innerhalb und zwischen Betrieben Î Circulus vitiosus durch Erregerzirkulation und Reinfektion • ineffiziente Immunantwort gp5 HeparinRezeptoren PRRSV aktivierte Makrophagen Pathogenese:- Ausbreitung LPS, Bakterien, Viren, etc. „direkte Zellkontakte“ LPS, Bakterien, Viren, etc. unspezifische Abwehr IL1 TNF IFNα gp5 HeparinRezeptoren IL10 ?Mx1/Ubp/NFKB? Zelltod extrazellulär PRRSV aktivierte Makrophagen Immunität und Prophylaxe PRRSV aktivierte Makrophagen Pförtnereffekt •Immunsuppressiv •TH1ÎTH2 •Inhibition von •NK-Zellen • Zytokinen • T-, B-Zellen • MHC-Expression↓ „Immune-Escape“ PRRS Verluste • Immunität läuft synchron mit Persistenz und Ausscheidung – lediglich Eindämmung klinischer Symptome • Lebend- > Totimpfstoffe – Schutzwirkung zeitlich begrenzt (3-4 Mo) – Wirkung nicht voraussagbar (Kreuzimmunität) – Übertragung des Impfvirus möglich – unentbehrliches Produktionsinstrument • erhebliche ökonomische Belastung • keine nachhaltige Problemlösung! PRRS Diagnose • Serologie – – – – – – 5-10 Blutproben je Alterstufe ELISA (ab 1-2 W. p.i. für ca. 6 Mo nachweisbar) + beginnende oder abnehmende Serokonversion /Impftiter ++ wahrscheinlich Feldvirus +++ Viruskontakt kurz zuvor: sicher akutes Geschehen ursächlich v.a. bei gleichzeitigem Vorliegen seropositiver und negativer Reagenten – Doppelbestimmung (3-4 Wochen Abstand) • Virusnachweis – sicherste Methode – PCR: Lnn, Tonsillen, Lunge, Milz, Rachentupfer, Blut Abortmaterial, Lebensschwache, Sperma, akut erkrankte, frisch verendete Ferkel PRRS Differentialdiagnostik • PCV2 • +Husten und Dyspnoe • Influenza • +hohes Fieber, akutes Auftreten im Bestand • AK, ESP • +neurologische Symptome, +hohes Fieber • PPV • Mumien • Bordetellen, Pasteurellen, NH3 PRRS PRRS Immunität und Impfung Impfungsvoraussetzungen • • • • • • • Reduziert Dauer und Grad der Virämie nach Feldinfektion kein vollständiger Infektionsschutz maternale AK für 4 - 12w (Schutz vor Infektion / Klinik) Immunität hält homolog mind. 2 Jahre humorale und zelluläre Immunität! Reinfektion: Boosterung ohne Virämie keine Viruselimination aus dem Bestand Ferkel und JS: ständig akut! • 3 – 4 M nach Absetzen der Impfung: Rückkehr zu klinischen PRRS-Symptomen im Bestand • Klinik + Serokonversion im Bestand • Impfung mind. 3 w vor zu erwartender Infektion • vollständige Impfung aller, auch gesunder Tiere PRRS PRRS Impfung Impfung • Impfstoffe – Ingelvac PRRS MLV (Boehringer): • • • • Bestandsimpfung Sauen Frühe Ferkelimpfung nur in PRRS-pos. Betrieben (Virusausscheidung) sehr gute Immunität, sehr bewährt – Porcilis PRRS (Intervet): • nur für Mastschweine, einmalige Impfung 6.-9.LW • Impfvirusausscheidung – Ingelvac PRRS KV/Progressis (Boehringer/Merial): • • • • • seit Sept. 01, reproduktionsorientiert Totimpfstoff: alle Kategorien, einschl. Tragende Grundimmunisierung 2 x Abstand 3 –4 W für PRRS-freie Betriebe Jungsaueneingliederung • Ferkelerzeuger – alle Sauen gleichzeitig impfen, unabhängig vom Trächtigkeitsstadium (Bestandsimpfung)! – Sauenimpfung schützt nur Sauen! – alle klinisch unauffälligen Saug- (ab 3 Wochen) und Absatzferkel (kontinuierlich)! – Zweitimpfung aller Sauen nach 4 – 6 W. – Folgeimpfungen: im Abstand von 3 bis 4 Monaten PRRS PRRS Impfung Impfung • Mastbetriebe – geimpfte Ferkel einstallen – oder alle Ferkel bei Einstallung impfen – ältere Tiere bei kontinuierlicher Belegung mitimpfen (Bestandsimmunität) • Systemferkel – alle im Alter von 3 W beim Erzeuger geimpft – oder: alle Ferkel direkt bei Einstallung impfen – kontinuierlich: alle älteren Ferkel mitimpfen • geschlossene Betriebe – Bestandsimpfung: alle Sauen, Ferkel ab 3 W und Mastschweine – Alle Sauen nach 4-6 W nachimpfen – Folgeimpfungen alle 3 bis 4 Monate – kontinuierlich alle Ferkel im Alter von 3 W impfen PRRS PRRS Impfung Impfung • Jungsaueneingliederung • Jungsaueneingliederung • Probleme: – Tot- oder Lebendimpfstoff? • Positive JS: Lebendvakzine – Infektion PRRS negativer Herden durch positive JS (offene Produktion) – schlechte Fruchtbarkeit PRRS-negativer in pos. Herden (Impfung) – Destabilisierung pos. Herden durch Eingliederung neg. JS (Impfung) PRRS • mit 3 W, Nachimpfen nach 4 M • Empfängerbetrieb: – PRRS-stabile Herde: einmalige Impfung bei Anlieferung – PRRS-Klinik: Erstimpfung + Wdh.-Impfung – kein Kontakt mit PRRS-Ausscheidern während Eingliederungsphase • Negative JS: Totvakzine – Einsatz im PRRS-negativen Vermehrungsbetrieb möglich – Impfung 6 + 3 W vor Auslieferung – Nachimpfung beim PRRS-instabilen Empfänger PRRS Bestandsproblematik Quarantäne – Stammsauen: Bestandsimpfung Abstand 3-4 M – JS: JS Sauen Bestandsproblematik PRRS-negative Herde: - nur PRRS-freies Sperma - nur PRRS-freie JS - keine Impfung - Hygiene u. Management optimieren Quarantäne + Impfung JS Sauen maternale AK Saugferkel Absetzer Absetzer Mast Mast PRRS JS Sauen maternale AK Impfung Saugferkel Absetzer Mast Erst Serologie, dann Impfung 90 % pos: alle Sauen impfen 70 % pos: aller außer HT 6 pp – 60 pc 50 % pos: erst Todimpfstoff später Lebendimpfstoff PRRS Bestandsproblematik Quarantäne + Impfung Saugferkel Impfung PRRS-positive Herde: - JS-Eingliederung - Quarantäne - Durchseuchung/Impfung - Hygiene u. Management optimieren - Absetzer geimpft! PRRS-Eradikation: -Erstinfektion vor mind. 1a -Aufbau Zuchtläufer -JS-Stopp für 1/2a -Stabilisierung der Herde - keine Symptomatik - geringe Serologie -vollst. Räumung ab Flatdeck (3-4 W) -Management -negatives Sperma + JS -Überwachungsdiagnostik Prophylaxe • Aufbau stabiler Immunität und Unterbrechung von Infektionsketten durch: • • • • • • Konsequentes Rein-Raus gründliche Zwischendesinfektion Abschirmen des Bestandes Personenverkehr einschränken Strikte Trennung der Altersklassen! Jungsaueneingliederung! • Quarantäne von 8 W mit gezielter Infektion/Impfung • Immun und nicht Ausscheider bei Eingliederung • keine Mischung von Herkünften! • hohe Stallhygiene • So wenig Zukäufe wie möglich • • • • PRRS-freie Besamungsstation Ferkelumsetzen nur innerhalb Abteil und innerhalb 24 h Absetzen mit 21 Tagen Euthanasie von Problemferkeln • Impfung bei klinischer Symptomatik PRRS PRRS Sanierung Sanierung • Grundlage: • Durchführung (DK, F) • • • • • 1. Infektion = Schutz vor Reinfektion! 2. Tenazität gering! 3. Infektion v.a. über Tierkontakte! 4. Herdenimmunität in 6 – 12 M! 5. kritisch sind: a) JS; b) Absetzer (6. – 9. LW) • Voraussetzung: • ab 6 M vor Sanierungsbeginn kein JS-Zukauf mehr • Serologie nach AK-Probenschlüssel • alle Herdenteile mit infizierten Tieren räumen • keine Tiere < 10 M • 1 abferkelfreies Interval • Beispiel aus Deutschland • Betrieb mehrere Jahre geimpft • Mai 2001: Einstellung von • keine Klinik mehr im Bestand • Einschleppung vor 1 a; Durchseuchung aller Zuchtschweine erreicht • • • • • Impfung, JS-Zukauf • + vollständige Räumung der Flatdecks keine aktuelle Viruszirkulation im Bestand (Klinik, Serologie) kontrolliert negative JS und Sperma stehen zur Verfügung geringes Reinfektionsrisiko (Bestandsabstand min. 1000 m) Prävalenz serolog. positiver max. 25 % • Wiederbelegung Ende September • Indikatorschweine mit aufgestallt (PRRS-frei!) • ELISA, PCR • rechtzeitige Einstellung aller Vakzinationsmaßnahmen Schweineinfluenza Schweineinfluenza Steckbrief Steckbrief • Akute, plötzlich auftretende und rasch durchseuchende Erkrankung • Zoonose • Saugferkel kaum betroffen Schweineinfluenza • • • • • • • • • • • • Erreger: Influenza-Virus Typ A Anzeige/Meldepflicht: Betroffene Altersstufe: ab Aufzucht, v.a. Mastbetriebe Besonderheiten: Bronchien und Bronchioli kalte Jahreszeit vermehrt Inkubationszeit: 1-3 d Morbidität: bis 100 % Mortalität: 2 - 3 % Ausscheidung: 5 Wochen! Durchseuchung: sehr rasch und plötzlich, alle Tiere Epidemiologie: epizootisch Heilung: gute Haltungsbedingungen: nach 1w Bedeutung: Sekundär-Erreger! Reinfektionen Schweineinfluenza Erreger Erreger • Klasse: Orthomyxoviridae • Aufbau: RNA-Virus, 8 RNA-Stränge • Serotypen: (15Hn 9N-Typen) A/New Jersey/76; H1N1; H3N2; H1N2 • Besonderheiten: 1918 USA, Grippewelle; D: 76 H Antigendrift! Antigenshift (Rekombination: H1N2) • Tenazität: gering • Verbreitungswege: aerogen (Mastbetriebe!) Transportfahrzeuge, Zukauf, Menschen • Reservoir: latent infizierte Tiere, Lungenwurmlarven in Regenwürmern, wildlebende Wasservögel • EU: seit 1979 • D: seit 1980 • H1N2: seit 2000 • 71% Betriebe Norddeutschlands: H1N1 Bakum98 • 50%: H3N2 Bakum 93 Schweineinfluenza Pathogenese akute BronchoBefall ges.resp.Epithel pneumonie: blaurote, herdförmig verdichtete Spitzenlappen interst.Pneumonie später auch Zwerchfellappen • • • • • • • Schweineinfluenza aerogene Aufnahme Klinik Ziliarepithel Clearance-Verlust Sekundärinfektionen: - APP! - Bordetellen - Pasteurellen - Mycoplasmen - PRRS! • akute Bronchopneumonie – meist lokalisiert – selten generalisiert Î tödlich • • • hohes Fieber (41-42°C; Aborte, Infertilitäten), Dyspnoe, schmerzhafter Husten Atemnot • • • Depression, Myalgien Anorexie, Apathie, Gewichtsverluste Dauer: 3d, dann setzt Heilung ein • • nur milder Verlauf bei Saugferkeln stärkere Klinik: Ältere + Belastung Schweineinfluenza Schweineinfluenza Sektion Diagnose Je nach bakteriellem Sekundärerreger 24h p.i.: Blaurote herdförmige Verdichtung Spitzenlappen bis d4: auch Zwerchfellappen betroffen Herde gegenüber emphysematösem Rest eingesunken Bronchien: fibrinöse, schleimig-eitrige Füllung Mediastinallnn: vergrößert, ödematös, hyperämisch Histo: wenige h: Hyperämie und Zellinfiltration – interstitielle Pneumonie – fokale Nekrosen im Bronchialepithel – d3: Alveolen und Bronchioli mit Exsudat und Neutros – ab d4: mononukleäre Leukos: Heilung • Erregernachweis – sofort: Nasen-/Rachentupfer, 5 Tiere → Virusnachweis • nach 5 Tagen kein Virusnachweis mehr möglich – gepaarte Serumprobe: HAH; Positiv: +4 Stufen in 14d – Immunfluoreszenz an Lungenschnitten – PCR, RT-PCR (Subtyp) • Schocklunge: cardiogener Schock (Hypoxie, Verlegung der Bronchioli) Schweineinfluenza Schweineinfluenza Differentialdiagnostik Therapie • alle anderen Pneumonien • • • • Fiebersenkung: Acetylsalicylsäure Schleimlösung: Bromhexin (Bisolvon) Sekundärerreger: AB, z.B. Tylosin Kreislaufkollaps: Kortikosteroide • Stalltemperatur erhöhen • Einstreu • Lüftung verbessern Schweineinfluenza Schweineinfluenza Immunität und Impfung Immunität und Impfung • Sauen zum Schutz gegen Aborte • Suvaxyn Flu: H1N1+ H3N2- Komponenten • Zuchttiere: 2 x 4 Wochen vor Belegung • Ferkel: 10. + 12. Lebenswoche • Mastschweine: Kosten/Nutzen-Analyse • 1malig: verhindert Klinik • 2malig: relativer Infektionsschutz • keine Masteinbußen • Schutz durch neutralisierende AK 7.d bis 6m nachweisbar. • belastbare Immunität: ca. ½ Jahr; lebenslang bei Infektion nach 9. Lebensmonat • Kolostrum: Schutz vor Klinik/Infektion • CAVE: Ältere Impfstoffe oft wenig wirksam aufgrund starker Antigendrift • Ingelvac® Flu, neuer Influenza- Impfstoff für Schweine, inaktiviert • enthält aktuelle, in den 90er Jahren vom Schwein isolierte Influenzastämme • schützt gegen die in Deutschland dominierenden Stämme der Subtypen H1N1 und H3N2. • Suvaxyn Flu, Fort Dodge, Infl.A H1N1+H3N2 • Viraflu, Merial, Infl.A H1N1+H3N2 Schweineinfluenza Schweineinfluenza Prophylaxe Neu • Abschirmen des Bestandes • Personenverkehr einschränken • zunehmend auch bei schleichendem Verlauf Î endemisch: • H1N1: weniger virulent, größte Varianz, Regionen geringer Dichte • auch subklinisch möglich • Belegungsdichte • Lüftung, Raumtemperatur • H3N2, H1N2: schweinedichte Gebiete abwechselnd alle 6 Monate Rhinitis atrophicans Rhinitis atrophicans Schnüffelkrankheit Schnüffelkrankheit toxinbildende Bordetella bronchiseptica toxinbildende Pasteurella multocida nicht-progressive Rhinitis atrophicans progressive Rhinitis atrophicans Conchenhypoplasie ökonomisch ökonomisch uneingeschränkte eingeschränkte Mastleistung Mastleistung toxinbildende Bordetella bronchiseptica toxinbildende Pasteurella multocida progressive Rhinitis atrophicans Umwelt Virulenz Immunität Begleiterreger Conchenhypoplasie ökonomisch ökonomisch uneingeschränkte eingeschränkte Mastleistung Mastleistung nicht-progressive Rhinitis atrophicans Rhinitis atrophicans Progressive Rhinitis atrophicans Schnüffelkrankheit toxinbildende Bordetella bronchiseptica Steckbrief • Zerstörung der Nasenmuscheln durch toxinbildende Pasteurella multocida-Stämme begünstigt durch Vorschädigung der Schleimhäute → Schnüffelkrankheit toxinbildende Pasteurella multocida progressive Rhinitis atrophicans Haltungsdichte kontinuierlich hoher JS Anteil schlechte Luft Conchenhypoplasie Trockenfütterung ökonomisch ökonomisch uneingeschränkte eingeschränkte Mastleistung Mastleistung nicht-progressive Rhinitis atrophicans Progressive Rhinitis atrophicans Progressive Rhinitis atrophicans Steckbrief Erreger • Erreger: toxinbildende Pasteurella multocida • Anzeige/Meldepflicht: • Betroffene Altersstufe: Infektion ab 1.LT, Klinik nicht vor 1 bis 3 Monate • Besonderheiten: Überwachungsprogramme • Inkubationszeit: Tage bis Wochen; Einschleppung bis Klinik: Monate - Jahre • Morbidität: bis 90 % • Mortalität: bis 10 % • Durchseuchung: langsam, chronisch • Epidemiologie: enzootisch, jahrelang Teil der Ferkel betroffen • Bedeutung: starke wirtschaftliche Schäden durch Wachstumsstillstand; Winterwürfe • Klasse: kurze gramnegative Stäbchen; bipolar, aerob, • Aufbau: toxinbildender Stamm • Serotypen: TypD • Besonderheiten: wächst im Nasenschleim – Toxinabgabe - Symptome • Tenazität: gering • Verbreitungswege: Zukauf subklinischer Tiere • Reservoir: Schweine bleiben jahrelang Träger Progressive Rhinitis atrophicans Progressive Rhinitis atrophicans Pathogenese Klinik belebte Ursachen Viren -EKR -Influenza -PRRS -AK Bakterien -Mycoplasmen -Streptokokken -Bordetellen Schleimhautschäden Schleimansammlung unbelebte Ursachen -Staub toxinbildende -Schadgase Pasteurellen -trockene Luft katarrhalisch-eitrige Rhinitis -kalte Luft Hemmung der Osteoblasten -Temperaturschwankungen • • • • • • • • Hypoplasie der ventralen Conchen oft subklinisch, ungestörter Verlauf Niessen, Schniefen seröser Nasenausfluß Pneumonieanfälligkeit OK-Deformation und Nasenbluten Verformung des Oberkiefers – kurznasige Rassen: Brachygnathia superior+Faltenlegung – langnasige Rassen: Verbiegung braune Krusten im inneren Augenwinkel Mastleistung stark reduziert! Ausschluß vom Zuchttierverkauf! Progressive Rhinitis atrophicans Progressive Rhinitis atrophicans Sektion Sektion • Nasenquerschnitt kurz vor P1 Progressive Rhinitis atrophicans Progressive Rhinitis atrophicans Diagnose Erregernachweis • V: Klinik: schiefe und blutige Nase D: Nasentupferprobe – Erregeranzüchtung toxinbildende Pasteurellen! 10 - 20 kg Ferkel, gekühltes Transportmedium • Messen der ventralen Naseneingangshöhe • Frei-Anerkennung: • Nasentupfer: 8-14 / Betrieb, 2 x pro Jahr – bakteriologische Untersuchung – PCR • Toxinnachweis! – Zytopathogenitätstest – PCR • Serologie auf Ak gegen toxinbildende Pasteurellen: 10 – 20 Proben, 2 x pro Jahr • Keine Impfung in Zuchtbetrieben • Behandlung verschleiert Symptomatik – 6 - 9 Bestandsprüfungen in 2 - 3 Jahren – bei 300 Sauen: 24 Nasentupfer Pasteurella multocida Pasteurella multocida Steckbrief Steckbrief • Pneumonien in der Mastphase durch nicht toxinbildende Pasteurellen • • • • • • • • • • • Erreger: Pasteurella multocida Anzeige/Meldepflicht: Betroffene Altersstufe: Läufer bis Jungsauen Besonderheiten: Inkubationszeit: 1 - 2d Morbidität: bis 50 % Mortalität: bis 100 % Durchseuchung: rasch, perakut bis akut Epidemiologie: enzootisch Heilung: selten Bedeutung: ubiquitär, fast alle Betriebe nicht toxinbildende Pasteurella multocida Klinik • • • • • • • • • • • • a) selten perakute Septikämie b) akute Broncho- u. Pleuropneumonie c) am häufigsten als Sek. Erreger Dyspnoerinne Fruchtbarkeitsstörungen bei der Sau eitrig-fibrinöse Laryngitis nicht toxinbildende Pasteurella multocida Klinik • • a) selten perakute Septikämie b) akute Broncho- u. Pleuropneumonie c) am häufigsten als Sek. Erreger Dyspnoerinne Fruchtbarkeitsstörungen bei der Sau eitrig-fibrinöse Laryngitis • • • • nicht toxinbildende Pasteurella multocida Klinik nicht toxinbildende Pasteurella multocida Diagnose a) selten perakute Septikämie b) akute Broncho- u. Pleuropneumonie c) am häufigsten als Sek. Erreger Dyspnoerinne Fruchtbarkeitsstörungen bei der Sau eitrig-fibrinöse Laryngitis • V: Sektion • D: Erregerisolation aus Lungenspülprobe oder Lunge in Reinkultur • PCR Bordetella bronchiseptica Bordetella bronchiseptica Steckbrief Steckbrief • Keuchhusten bei Saugferkeln, häufig in kalter Jahreszeit • häufig bei Atemwegserkrankungen und RA beteiligt, aber nur untergeordnete Rolle • toxinbildende Stämme: npRA • kaum Einfluß auf Wachstum • • • • • • • • • • • Erreger: Bordetella bronchiseptica Anzeige/Meldepflicht: Betroffene Altersstufe: Saugferkel bis Aufzuchtende Besonderheiten: npRA nur bei Infektion 3. - 6. LW Resistenz ab 6. Woche Inkubationszeit: 2 - 3 d Morbidität: bis 50 % Mortalität: bis 10 % Durchseuchung: rasch, akut bis chronisch Epidemiologie: enzootisch Heilung: oft vollständig 4w p.i. Bedeutung: Wegbereiter für toxinbildende Pasteurellen weit verbreitet Bordetella bronchiseptica Bordetella bronchiseptica Erreger Pathogenese Lunge • Aufbau: bewegliche gramnegative Stäbchen, aerob • Serotypen: • Besonderheiten: Lebenslange Latenz! nur hohe Dosen können, nur bei sehr jungen Tieren ohne Immunschutz zur Conchenatrophie führen • Tenazität: gering • Verbreitungswege: Zukauf latent infizierter • Reservoir: latent infizierte Jungsauen, Nager • • • • • Bronchopneumonie Atemwegs-Epithelien aerogene Aufnahme bei Toxinbildung Conchen nicht progressive Rhinitis atrophicans Wegbereiter für toxinbildende Pasteurellen Bordetella bronchiseptica Bordetella bronchiseptica Klinik Sektion Anfangs: heißerer sehr heftiger Husten Rasche Ausbreitung Niesen, Dyspnoe, Tränenfluß, Tränenringe Syptome gehen 2 M p.i. zurück Wachstumsverzögerung bei npRA Bordetella bronchiseptica Diagnose • V: Klinik • D: Erregerisolation aus Nasentupfer/Lunge/ Lungenspülprobe Ferkel 10d - 10w • PCR • • • Entspricht makroskopisch und mikroskopisch EP Schädigung der Blutgefäße: Hamorrhagien+interlobuläre Ödeme BiGe-Zubildung - Schrumpfung fissurartige Einschnürungen Therapie beim Ferkelerzeuger • Sauenbestandsbehandlung 14d • Einzeltier: Amoxicillin, Enrofloxacin, Oxytetracyclin • oral: 500 - 1000 ppm Trim.Sulf. oder Tetracycline 500 ppm Amoxicillin 400 ppm Tilmicosin • Injektion aller Saugferkel: d1, d5, d10, Absetzen • Langzeit-AB (s.o.) • Futtermedikation aller Ferkel bis 25 kg (s.o.) Herdbuchbetriebe ausmerzen Muttertiervakzinierung nach Krankheitsausbruch Immunität und Impfung • Kaum immunogen - jahrelange Träger • Impfstoffe: nur gesunde Tiere! • Porcilis AR-T (Intervet) Prophylaxe • 1. Fütterung- u. Haltungsbedingungen optimieren • • • • • Bordetella bronchiseptica • Pasteurella m. Typ D Toxoid • Porcilis Atrinord (Intervet) • Deletionsderivat des P.m.-Toxins (Protein d0) • Respiporc (IDT) • • • • • • • • • Bordetella bronchiseptica Pasteurella multocida A Toxoid von P.m. D Sauen: 2 x 4 ml s.c. 5. und 2. Woche a.p. Absetzer: 5. und 8. LW je 1 ml s.c. Grundimmunisierung aller Bestandssauen Auffrischung jeweils 4 - 5w a.p. Kolostrum schützt! Positive Reagenten erst nach Jahren reduziert Trennung Absatzferkel und Abferkelstall Unterteilung der Ställe Rein-Raus Belegungsdichte • 2. Aufbau einer homogenen Bestandsimmunität • Jungsauenintegration • 3. Infektionsdruck senken durch Rein-Raus • 4. Verbesserung des Stallklimas • Luftfeuchtigkeit, Staubgehalt, NH3 • • • • • echte Sanierung nur durch Räumung geschlossener Bestand Zukauf nur aus kontrolliert pRA-freien Beständen Quarantäne keine Impfung in überwachten Betrieben!!! Enzootische Pneumonie Enzootische Pneumonie Steckbrief Steckbrief • Bestandsproblem mit erheblichen wirtschaftlichen Schäden durch Auseinanderwachsen • Flimmerepithelien geschädigt • Wegbereiter für Sekundärinfektionen • • • • • • • • • • • Enzootische Pneumonie Erreger • • • • Klasse: Mycoplasmataceae Aufbau: keine Zellwand – vielgestaltig, 0,1µm Serotypen: Besonderheiten: extrem resistent geg. Penicillin, Ampicillin hohe Keimzahl für Infektion notwendig • Tenazität: sehr gering, Detergenzien • Verbreitungswege: aerogen (Mastbetriebe!) Transportfahrzeuge, Zukauf, KB, Sektio! Tröpfcheninfektion im Betrieb • Reservoir: Trägersauen → Ferkel (vertikal!) Einstallen latent infizierter Jungsauen in fast allen Beständen endemisch Erreger: Mycoplasma hyopneumoniae Anzeige/Meldepflicht: Betroffene Altersstufe: alle bis einschließlich Jungsauen Besonderheiten: Zerstörung des Ziliarepithels Stillstand bei 60 kg; frühe Infektion, Manifestation in Mastphase; Syn. Ferkelgrippe!? Inkubationszeit: 3 - 4w (Monate) Morbidität: 30 - 100 % Mortalität: 1 - 10 % Durchseuchung: langsam, akut bis chronisch Epidemiologie: enzootisch Heilung: je nach Umwelt und Sek.-Erreger; Komplikation durch: Besatzdichte, Kälte, schlechte Belüftung, Sek.Err. Bedeutung: einer der wichtigsten Erreger Sekundär-Erreger: MIRD, PRDC, PRRS Enzootische Pneumonie Pathogenese Clearance-Verlust Ziliarepithel aerogene Aufnahme Anreicherung von Schleim und Keimen Spitzenlappenpneumonie Husten trocken, unproduktiv Sekundärinfektionen: - APP! - Bordetellen Husten produktiv - Pasteurellen Fieber - PRRS! Pförtnereffekt MIRD Erreger Hygiene/Management Hygiene/Management Mycoplasma hyopneumoniae Zilien↓ Abwehr Abwehr Cytokine -TNF -IL10 T-Killer -zellen Makrophagen igernd pathogenitätsste hemmt Makrophagen T-Helfer -zellen Abwehrzellen Zilien↓ Makrophagen Klinik BP T-Killer -zellen T-Helfer -zellen • • • • • • • • • Enzootische Pneumonie Clearance ↓ igernd pathogenitätsste hemmt • • • • • Ab 2-4w p.i. trockener, chron. unproduktiver Husten durch Auftreiben provozierbar weder Fieber noch Dyspnoe schwere Form: hundesitzig, Tachypnoe, Dyspnoe, Hypoxie, Cyanose, bis 10% Verluste + Sek.Inf.: Fieber, produktiver Husten oft klinisch stumm Enzootische Pneumonie Enzootische Pneumonie Sektion Diagnose Geringer Befall: nur Spitzenlappenpneumonie lobuläre/lobulär-konfluierende Pneumonie anfangs graurote Schwellung später Einziehungen braunroter Farbe vielgestaltig durch Sek.Inf. Pleura und andere Organe meist o.b.B. Histo: katarrh. Bronchitis u. Bronchopneumonie peribronchuläre u. perivasculäre Lymphozyten Hyperplasie des Alveolar- und Bronchialepithels T-Killer -zellen T-Helfer -zellen Co-Erreger Abwehr Cytokine -TNF -IL10 BP Immunzellen Hygiene/Management Mycoplasma hyopneumoniae Co-Erreger Clearance ↓ • V: Husten im Bestand, frisch abgesetzte Ferkel und junge Mastschweine – 2-4w nach Wegfall kolostraler AK – v.a Würfe von JS • D: sehr schwierig – – – – problematische Erregerisolation Dauer mehrere Wochen heute PCR Sektion: Spitzenlappenpneumonie Enzootische Pneumonie Enzootische Pneumonie Erregernachweis Differentialdiagnostik • Serologie unzuverlässig • alle Pneumonien • chron. APP: – – – – kaum humorale Reaktion, erst ab 60 kg am besten aus Kolostralmilch 5-10 Blutproben/Alterstufe ELISA • Erregeranzüchtung schwierig • PCR • Pleuritis, Nekroseherde in Lunge • Erregernachweis, Serologie • Chlamydien: • Serumtiteranstieg, mikroskop. Erregernachweis Lunge • Ascaridenlarven: • massive Einwanderung = EP (klinisch) • Lungenläsionen+Punktblutungen Zwerchfellappen • Influenza: • Virusisolation aus Nasensekret, Serologie, Lungenhisto Enzootische Pneumonie Enzootische Pneumonie Differentialdiagnostik Therapie • Bordetella bronchiseptica: • Bronchosekretolytika: Bromhexin (Bisolvon) • Kortikosteroide: Entzündungshemmung • schon bei 3 - 4d alten Ferkeln • Lungenhisto: Hämorrhagien, Erregernachweis • zukaufende Mastbetriebe: Fütterungsprophylaxe aller Zukäufe • chron. Infiz. Betriebe: Futtermedikation über 2 - 3 w während Mast mindern Verluste • AK = EP (klinisch): • Somnolenz (ZNS) • Fremdkörperpneumonie: • meist rechter Spitzenlappen • Einzeltiere • Fremdkörperriesenzellen Enzootische Pneumonie • Sekundärerreger: AB • Enrofloxacin (Baytril), Marbofloxacin (Marbocyl) • Oxytetracycline (Terramycin), Tylosin (Tylan), Tiamulin • oral: 400 ppm Tilmicosin, 250 ppm Tylosin • Ferkel: 1.LT 50 mg Tylosin 2 weitere Inj. 1.+2.Lw Impfstoffe für Schweine Immunität und Impfung • Immunität bei Altsauen • Ferkel: • inaktivierte Mykoplasmenimpfstoffe • d7 + d21 (z.Z. Absetzen) = Two Shot • nicht vor d7 (Streß, Colidruck, Eisenbeladung der Makrophagen) • oder einmalig (One-Shot) • nicht in florierende PCV2-Infektion hineinimpfen • EP – – – – – – Hyoresp Multiporc M.hyo Stellamune Mycoplasma Suvaxyn M.hyo 1-Shot Stellamune 1-Shot Merial M.hyo IDT M.hyo Pfizer M.hyo Fort Dodge M.hyo Boehringer Pfizer i i i i i i wäßrig wäßrig Öl/W wäßrig W/Öl Öl/W Actinobacillus pleuropneumoniae (APP) Enzootische Pneumonie Prophylaxe • • • • • • • Steckbrief Maximale Schwankung der Stalltemperaturen: 4°C Luftfeuchte 60-80 % >3m3/Tier Rein-Raus Quarantäne Parasitenbekämpfung Schadgase • Pleuropneumonie • Bedeutsame und schwerwiegende Pneumonieerkrankung beim Schwein • häufiger Sekundär-Erreger • NH3 < 10 ppm • H2S < 5 ppm • Teilsanierung: 14d nur Sauen im Bestand halten + Chemotherapie APP APP Steckbrief Erreger • Erreger: Actinobacillus pleuropneumoniae • Anzeige/Meldepflicht: • Betroffene Altersstufe: Aufzucht bis Jungsauen, va. 9. - 16.w • Besonderheiten: besonders schlimmer Verlauf mit PRRS • Inkubationszeit: 1 - 5 d • Morbidität: 30 - 100 % • Mortalität: 20 - 50 % • Durchseuchung: perakut bis akut • Epidemiologie: enzootisch • Bedeutung: hohe wirtschaftliche Verluste • Klasse: Pasteurellaceae, gramnegative Kokken • Aufbau: Kapselpolysaccharide; Zytotoxine: ApxI-III • Serotypen: 2 Biotypen:1Nad+=virulent; 12 Serotypen EU: 1,2,3,5,6,7,9 • Besonderheiten: Virulenzfaktoren: ApxI+II (+III): hämolytisch und zytotoxisch; 100 Keime reichen für erfolgreiche Infektion • Tenazität: überleben 4 Jahre in Regenwürmern • Verbreitungswege: Zukauf stumm infizierter, Stiefel, Kleider; im Betrieb aerogen • Reservoir: Latenz in Tonsillen, Respirationstrakt APP Pathogenese APP aerogene Aufnahme Befall der Alveolen Klinik • Resistenzfaktoren Kapsel LPS OMPs TBPs Proteasen Apx-toxine! Adhäsion! Hämolytisch und PhagozytoseEisenentzug IgA-, Rezeptorzytotoxisch für Complementermöglicht durch Hb-Abbau Interaktion Lungenmakroschutz Transferrinbindung am unteren phagen und Neutrophile respiraAK: SerotypSchweinespezifisch Porenbildner spezifischer Schutz torischen ApxI>ApxII Epithel Lipid als Endotoxin ApxIII: zytotoxisch Adhäsion Endothelzellen Steigerung der Oxidative Burst in MPs Toxizität Gram neg. Bakterien AK: kein Schutz • • perakut: Husten, Dyspnoe, giemende Atemgeräusche Apathie, Anorexie, Vomitus, Fieber 42,5°C, Zyanose, blutiger, schaumiger Nasenausfluß Maulatmung, Herz-KreislaufKollaps Tod in 12 - 24h: sudden death akut: Dyspnoe, stoßweiser, schmerzhafter Husten Fieber 41°C, Inappetenz, Apathie, ohne Beh. Tod in wenigen Tagen oder chronisch beide: sehr schmerzhafte Pleuritis und Pericarditis - hundesitzige Stellung, kein Flankenschlagen APP APP Klinik Sektion • • chronisch: kein bis schwaches Fieber, Fieberschübe Husten, Dyspnoe nach Bewegung Inappetenz, Wachstumsreduktion, Zahl der Kümmerer erhöht sich auch in geschlossenen Betrieben vermehrt blasse Tiere im Bestand • subklinisch: Zuchtbetriebe mit günstigen Umweltbedingungen latente Phase nach kurzer akuter Phase • • • hämorrhagisch-nekrotisierende Pneumonie Akut: dunkelrote Pneumonieherde (1-3 cm) in Zwerchfellslappen beetartiges vorragen (Rest emphysematös) fibrinöse Beläge auf Pleura perakut: zahlreiche solche Herde serösblutige Flüssigkeit in der Brusthöhle chron: adhäsive Pleuritis; Pneumonieherde: graurote bis weiße Schnittfläche mit Nekrosezentrum; selten Arthritis, Endoc.valv. APP APP Diagnose Erregernachweis • Klinik: Verdacht = Sek.Inf. Nach EP • Sektion charakteristisch • bei akuter Form ohne Behandlung gut möglich • Serologie: Blut: KBR, ELISA, Kolostrum: ELISA = Methode der Wahl bei subklinischer und chronischer Form APP APP Differentialdiagnostik Therapie • • • • hakut: parenterale Einzeltierbehandlung Penicilline 20.000 IE über 3d oral: Chlortetrazyklin, Tylosin, Sulfonamide Influenza Mikroangiopathie Herz-Kreislauf-Erkrankung EP = chronische Form APP Metastrongylose Immunologie und Immunprophylaxe Steckbrief • Stabile Immunität lokal+humoral nach Überstehen • latente Infektion bleibt erhalten (v.a. Mast) • Meist subklinisch verlaufende Erkrankung, nur bei Weidehaltung • Regenwürmer als Zwischenwirt und Reservoir • Impfung: Toxoid-Impfstoff • APP – Haeppovac – Hyactin – Porcilis App IDT APP Serotyp 2 Merial APP Serotyp 1,6 Intervet Toxoide + OMP i i i wäßrig wäßrig wäßrig Metastrongylose Metastrongylose Steckbrief Erreger • • • • • • • • • • • • • • • • Erreger: Metastrongylus apri (Haus) pudendofectus (Wild) Anzeige/Meldepflicht: Betroffene Altersstufe: Läufer und Mast Besonderheiten: nur bei Weidehaltung Inkubationszeit: 10 - 12d; Präpatenz: 4w Morbidität: bis 100 % Mortalität: 1 - 5 % Durchseuchung: chronisch Epidemiologie: enzootisch Bedeutung: Wegbereiter für Sekundärinfektionen, Reservoir für Influenza Klasse: Rundwürmer Aufbau: 1,5 cm lang, weiss Serotypen: Besonderheiten: Tenazität: überleben 4 Jahre in Regenwürmern Verbreitungswege: Zukauf, mind. 7 m im Schwein lebensfähig • Reservoir: Ausläufe und Weiden, Wildschweine Metastrongylose Metastrongylose Pathogenese Klinik Infektiöse Larven nach 18 - 30d Regenwurm durchbohren der Darmwand Kot Lymp-/ Blutweg Abschlucken Lunge orale Aufnahme Entzündungen und Blutungen Sek.Inf. - EP Flimmerepithel Eier Ansiedeln in Bronchien Geschlechtsreife 3. Larve • • • • Husten, Dyspnoe, Nasenausfluß Entwicklungsstörungen nur bei jungen Schweinen apparent meist subklinisch bis chronisch Metastrongylose Metastrongylose Sektion Diagnose • • • • • Kotuntersuchung • Eier: dicke, dunkelgraue Schale, leicht runzelige Oberfläche Larve 1 im Innern • ZnCl/NaCl 1:2 • oft nur geringe Eiproduktion! • Sektion Petechiale Blutungen an Lungenoberfläche grauweiße Knötchen + lobuläre Emphyseme v.a. caudo-ventral am Zwerchfellrand Schleim + 1,5 cm lange Würmer in Bronchioli Metastrongylose Metastrongylose Differentialdiagnostik Therapie • Ascaris suum hConcurat (Tetramisol) 10 mg/kg oral hwirkt auch gegen ältere Larven • Leber + Darm • Strongyloides • Haut + Darm Metastrongylose Atemwegserkrankungen Prophylaxe Therapie • Stallhaltung • regelmäßige Kontrolle und Entwurmung • Impfprogramme • Mycoplasmen • PRRS • Verbessertes Management und Hygiene • Rein-Raus • Funktionstrennung • Effizienter Erhalt der Leistung • Exakt eingehaltenes Schlachtgewicht • Wartezeit Atemwegserkrankungen Atemwegserkrankungen Therapie Therapie • Unumgänglich bei (typische Symptomatik) • Anforderungen an die Therapie • • • • • • Fieber bis 42°C Atemnot (Maulatmung im Hundesitz) verschärfte Atmung durch verkrampfte Bronchien Bauchschlagen Fressunlust und Abgeschlagenheit starker Husten • rascher Therapieerfolg • sofortiger Einsatz, da Bakterien in der Vermehrungsphase am besten getötet werden (Teilung) • Wirkungsweise: • Bindung an Bakterienoberfläche • Einströmen ins Bakterium • rasche Wirkung: AB mit bakterizidem Effekt (körpereigene Abwehr nebensächlich) • keine vorangegangene Behandlung mit bakteriostatischer Wirkung • optimale Dosierung und Behandlungsdauer • optimale Konzentration am Wirkort (Bronchialschleim); Futtermedikation?! • Mittel: Penicillin, Ceftiofur, Streptomycin, Neomycin, Ampicillin, Amoxicillin, Kanamycin, Gentamycin, Enrofloxacin Therapie von Atemwegserkrankungen • Früher Einzelkrankheiten – ein Medikament war oft ausreichend • Heute multiple Ätiologien – Behandlung in der Reihenfolge der Bedeutung – Kombination mit Immunprophylaxe • Resistenzlage ist oft sehr ungünstig • Haltungs- und Hygieneprobleme führen zu verstärkter Ausprägung der Grunderkrankung Therapie von Atemwegserkrankungen • Grundlage jeder Behandlung sind: – Bestandsuntersuchung • regelmässig mind. alle 7 Tage (AB) • alle 31 Tage (BB + nAB): unter Einbeziehung ALLER Bestandsfaktoren – Resistenztest – Altersgruppen, Belegdichte, R. u. D Schema – Therapieerfolg gefährdet Therapie von Atemwegserkrankungen • Anforderungen an die Therapie • rascher Therapieerfolg • günstige Wartezeit • sofortiger Einsatz, da Bakterien in der Vermehrungsphase am besten getötet werden (Teilung) • optimale Dosierung und Behandlungsdauer (Reduktion verhindert Wirkung und fördert Resistenzen) • optimale Konzentration • am Wirkort (Bronchialschleim); Futtermedikation?! • Anreicherung im Lungengewebe • Anreicherung Intrazellulär Therapie von Atemwegserkrankungen • Antibiotika mit bakterizidem Effekt • körpereigene Abwehr nebensächlich • Penicillin, Ceftiofur, Streptomycin, Neomycin, Ampicillin, Amoxicillin, Kanamycin, Gentamycin, Enrofloxacin • Antibiotika mit bakteriostatischem Effekt • Behandlung über mehrere Tage notwendig (> 5 Tage) • Keimbeseitigung allein durch das Immunsystem • Tetracyclin, Chlortetrazyklin, Oxytetrazyklin, Tylosin, Erythromycin, Tiamulin • Niemals bakteriostatische und bakterizide Medikamente gemeinsam einsetzen Therapie von Atemwegserkrankungen • Hohe Konzentration in der Lunge • starke Verschleimung der Atemwege hemmt Austritt der Medikamente zum Wirkort • Verfestigter Schleim als Schutzpanzer für die Bakterien • Unterstützung durch Sekretolytika (Bisolvon) Bromhexin „Einschleussungseffekt“ Therapie von Atemwegserkrankungen • Hohe Konzentration in der Lunge Zielgewebe: Lunge BlutSpiegel ß-Lactame; Tetrazykline Makrolide; z.B. Pulmotil Atemwegserkrankungen Atemwegserkrankungen Therapie Therapie • Welcher Erreger und Resistenzen • Injektionsschäden • oft nicht genug Zeit für Resistenztests in der Praxis • Amoxicillin: ölige Lösung 18 – 30 d WZ wässrige Lsg. 10 d WZ oral 3 d WZ • Cephalosporin-AB: Umwidmung: 28 d WZ • Gewebsfreundlich: • Proc.-Penicillin, Pen.-Strep, Ceftiofur, Ampicillin • Gewebsreizend: • Tetrazyklin, Tylosintartrat, Erythromycin, SulfonamidTrimetoprim • Excenel, wässrig: 3 d WZ • Excenel RTU, ölig, 5 d WZ • Cave: Pen-Strep: 45 d WZ, Gentamycin: 60 d WZ Therapie • Empfehlung • deutlich erkrankte Tiere mit Excenel RTU (5 d WZ) + Bisolvon (0 d WZ) • am nächsten Tag fressen die Tiere wieder • jetzt Amoxicillin und Bisolvon übers Futter (3 d lang), danach 3 d WZ • Tiere, die noch nicht fressen, nachinjizieren (wässriges Excenel) Colon Caecum Ileum Jejunum Atemwegserkrankungen Differentialdiagnostik Durchfallerkrankungen Saugferkel Absatzferkel Läufer Mast Zucht Rota! TGE EVD Kolidiarrhoe! Clostridium C! Clostridium A Ödemkrankheit Salmonellose Kokzidiose! Strongyloidose PIA Dysenterie! Transmissible Gastro-Enteritis Transmissible Gastro-Enteritis Steckbrief Steckbrief • • • • • • • • • • • Ferkel zukaufende Mastbetriebe nur in der kalten Jahreszeit hoch ansteckend 100%ige Mortalität bei Saugferkeln explosionsartige Ausbreitung alle Alterstufen heute nur noch geringe Bedeutung • hohe Durchseuchung mit dem schwach pathogenen Porcinen Respiratorischen Corona Virus (einer TGEVariante mit verändertem Tropismus) • • • • • • Erreger: TGE-Virus (Corona) Anzeige/Meldepflicht: M Betroffene Altersstufe: Jede! Besonderheiten: nur in kalter Jahreszeit! Ferkel zukaufender Mastbetriebe, kontinuierliche Belegung Inkubationszeit: 0,5 - 4d Morbidität: Saugferkel bis 2w: bis 100 % Mortalität: Saugferkel bis 10.LT: 90 - 100 % Durchseuchung: explosionsartig, akute Erkrankung Epidemiologie: epizootisch/enzootisch Heilung: Regenerationsbeginn nach 7d/2w Transmissible Gastro-Enteritis Transmissible Gastro-Enteritis Erreger Pathogenese • • • • • • • • Klasse: Coronaviren Aufbau: behülltes DNA-Virus Serotypen: Besonderheiten: Kreuzreaktion mit PRCV Tenazität: RT: 10 d; -20°C: 6M-Jahre; Sonne: 6h Verbreitungswege: Transporter, Zukauf Reservoir: chron. infiz. Herden; subklinische Ausscheider (Schw, Katze, Fuchs, Hund, Star) Desinfektion: Formalin Transmissible Gastro-Enteritis Pathogenese orale Aufnahme Mikrokanalikuli/ Makropinozytose Mastschweine 10.000 x LD50 Empfindlichkeit ab 3. LW Transmissible Gastro-Enteritis Pathogenese Diar- Maldigestion Exsikkose rhoe Malabsorption (Osmose) reflektorischer Pylorusverschluß Darmreizung Erbrechen orale Aufnahme orale Aufnahme Befall + vollständige Zerstörung der Zotten in Jejunum + Ileum Mikrokanalikuli/ Makropinozytose Mastschweine 10.000 x LD50 Empfindlichkeit ab 3. LW Befall + vollständige Zerstörung der Zotten in Jejunum + Ileum Mikrokanalikuli/ Makropinozytose Mastschweine 10.000 x LD50 Empfindlichkeit ab 3. LW Infektionsdruck Transmissible Gastro-Enteritis Transmissible Gastro-Enteritis Pathogenese Klinik Diarrhoe Schutz/Heilung Maldigestion Exsikkose Malabsorption Darmreizung reflektorischer Pylorusverschluß IgA Kreuzimmunität PRCV 1. Erbrechen Erbrechen orale Aufnahme lokale Immunität Befall + vollständige Zerstörung der Zotten in Jejunum + Ileum Krypten verschont Mikrokanalikuli/ Makropinozytose UV/ Hitze Mastschweine 10.000 x LD50 Regeneration ab d7 Empfindlichkeit ab 3. LW Mast/Sauen Saugferkel 2. Durchfall graugelbübelriechend 1. 1./2.d: Apathie, Anorexie 40,5°C 2. 3.-6.d: Kot graugelb, futterdurchsetzt, übelriechend 3. Verminderte Mastleistung 4. Sterilität bei Sau möglich 3. Exsikkose + Schwäche - Hypoglykämie, akutes Nierenversagen/ chron.Niereninsuffizienz Infektionsdruck Transmissible Gastro-Enteritis Transmissible Gastro-Enteritis Klinik Klinik TGE-Kot der Sau Kot: grau-grün, wäßrig + weicher weißer Milchfettkot erste Tage weiterer Verlauf Transmissible Gastro-Enteritis Transmissible Gastro-Enteritis Klinik Klinik Abferkelbereich Transmissible Gastro-Enteritis Transmissible Gastro-Enteritis Klinik Klinik in der Mast in der Mast Transmissible Gastro-Enteritis Transmissible Gastro-Enteritis Sektion Diagnose • Transparenter Darm vollständige Atrophie des Zottenepithels (Saugferkel bis 10d; Stereolupe) • Magen und Dünndarm leicht gebläht • geronnene Milch in Magen und Darm • Klinik + Verlauf • Sektion • Atrophie der Dünndarmzotten • Milchkoagula im Magen • Transparenter Darm • plötzlicher und rascher Verlauf • jede Altersgruppe, Ferkel besonders stark betroffen • Saugferkel bis 10 d: 100 % Mortalität • Virusnachweis (Darm+Kot) • AK-Nachweis 14d p.i. Transmissible Gastro-Enteritis Erregernachweis • Immunfluoreszenz des Virus-Ag (Darmschleimhaut/Kot) • Anzüchtung Zellkultur • PCR Transmissible Gastro-Enteritis Differentialdiagnostik • Rota-Viren: - gleiches Bild, schwächerer Verlauf, Zotten nur verkürzt - Kot breiig-pastös; geringe Sterblichkeit; 1.-8.LW • EVD: - gleiches Bild, aber Mast >> Saugferkel - Saugferkel d 4 - 7: Mortalität 20 - 30 % - ganzjährig • Colidiarrhoe: - nur Neugeborene und Absetzer, Chemotherapie! • Dysenterie: - weniger akut, Kotfarbe, Chemotherapie! - max. 30 % eines Mastbestandes befallen • Chron. Schweinepest: - langanhaltendes Fieber! Transmissible Gastro-Enteritis Transmissible Gastro-Enteritis Therapie Immunität und Impfung • Saugferkel: • • • • reichlich klares Wasser Volumenauffüllung (Niere):5 g NaCl + 50 g Glucose/l evtl. parenteral 1,2% NaHCO3 + 5% Glucose Baytril, Apralan, Neodiar-Doser (Sek.Erreger) • Mast: • Futterentzug bzw. reizarme Diät • Einzeltierbehandlg (Inj.): Enrofloxacin, Gentamycinsulfat, Trimethoprim-Sulfonamid • Futtermedikation (Sek.Erreger): Neomycinsulfat, Colistinsulfat (je 250 ppm) • • • • Zuchtsau: 2J Virusneutralisierende AK: 5d p.i. - 9w p.i. Passive Immunität für 12w (Kolostrum) bislang keine zuverlässige Vakzinierung möglich • Stalltemperatur erhöhen! • Liegeflächen trocken halten! Transmissible Gastro-Enteritis Epizootische Virusdiarrhoe Prophylaxe Steckbrief • • • • • • • hochansteckende, ganzjährige Viruserkrankung • Freßunlust, Erbrechen und Diarrhoe • Endmastschweine am stärksten Betroffen • • • • ständige AK-Versorgung der Saugferkel Eingliederung der Jungsauen Mast: Rein-Raus-Verfahren Futterentzug für 3-4 Tage Keine Milchprodukte (Osmose) Hygiene (Personen, Geräte, Tiertransporter, Zuchtviehmärkte) wochenlange Ausscheidung nach Heilung! (bis 8M Ferkel) Kot als Hauptinfektionsquelle v.a. im Winter! Seuchenzüge alle 3-4 Jahre Großbetriebe als Reservoir (Kümmerer als Dauerausscheider) Epizootische Virusdiarrhoe EVD Steckbrief Erreger • Erreger: EVD-Virus (Corona) • Anzeige/Meldepflicht: • Betroffene Altersstufe: Absetzer bis Sauen, Unterschiede! Mastschweine (60 - 70 kg!) Belastungsmyopthie • Besonderheiten: ganzjährig Ferkel zukaufender Mastbetriebe, kontinuierliche Belegung • Inkubationszeit: 1- 4d • Morbidität: Saugferkel kaum betroffen, Rest 30-80% • Mortalität: Saugferkel bis 3.LT: 90 - 100 %, dann 20-30 % Mast bis 10 % • Durchseuchung: schleppend • Epidemiologie: enzootisch • Heilung: langsam nach 3w • Bedeutung: groß, aber sinkend • • • • • • • Klasse: Coronaviren Aufbau: behülltes DNA-Virus Serotypen: Besonderheiten: Tenazität: RT: 10 d; -20°C: 6M-Jahre; Sonne: 6h Verbreitungswege: Reservoir: chron. infiz. Herden; subklinische Ausscheider (Schw, Katze, Fuchs, Hund, Star) • Desinfektion: Formalin Epizootische Virusdiarrhoe Epizootische Virusdiarrhoe Pathogenese Pathogenese Diar- Maldigestion Exsikkose rhoe Malabsorption (Osmose) reflektorischer Pylorusverschluß Darmreizung Diarrhoe reflektorischer Pylorusverschluß Darmreizung Erbrechen orale Aufnahme Rezeptoren Befall + vollständige Zerstörung der Zotten in Jejunum + Ileum Schutz/Heilung Maldigestion Exsikkose Malabsorption lokale Immunität kaum ausgeprägt Befall + vollständige IgA Erbrechen orale Aufnahme Rezeptoren Hitzeresistent Zerstörung der Zotten in Jejunum + Ileum Krypten verschont Regeneration ab w3 Infektionsdruck Infektionsdruck Epizootische Virusdiarrhoe Epizootische Virusdiarrhoe Klinik Klinik 1. Erbrechen 2. Durchfall evtl. perakute Todesfälle durch Belastungsmyopathie ab Endmast wäßrig grünlich gelb übelriechend 3. Exsikkose + Schwäche Schweine kotbeschmutzt Epizootische Virusdiarrhoe Epizootische Virusdiarrhoe Klinik Klinik Abmagern und Durchfall erste Tage Eindickung im weiteren Verlauf Epizootische Virusdiarrhoe Epizootische Virusdiarrhoe Klinik Sektion • akute katarrhalisch-eitrige Entzündung der Dünndarmschleimhaut • transparenter Darm vollständige Atrophie des Zottenepithels (Stereolupe) • evtl. Herz-Kreislaufversagen + akute Rückenmuskelnekrose Dackelohren durch Exsikkose Epizootische Virusdiarrhoe Epizootische Virusdiarrhoe Sektion Diagnose Schwellung der Darmlymphknoten • Klinik + Verlauf • Sektion • Atrophie der Dünndarmzotten • Transparenter Darm • schleppender Verlauf, Reinfektionen • jede Altersgruppe, Ferkel kaum betroffen • Saugferkel ab d4: 20-30 % Mortalität • Virusnachweis (Darm+Kot) • AK-Nachweis 14d p.i. nach Heilung! Epizootische Virusdiarrhoe Erregernachweis • Immunfluoreszenz des Virus-Ag (Darmschleimhaut/Kot) • Serologie: AK-Max 2.-5.w • humorale AK bis 2 Jahre nachweisbar, aber ohne Schutz! • Anzüchtung Zellkultur • PCR Epizootische Virusdiarrhoe Differentialdiagnostik • TGE: - gleiches Bild, aber Mast << Saugferkel - Saugferkel d 4 - 7: Mortalität 90 - 100 % - nur im Winter, Inkubationszeit kürzer, höhere Morbidität, kürzere Krankheitsdauer • Rota-Viren: - gleiches Bild, schwächerer Verlauf, Zotten nur verkürzt - Kot breiig-pastös; geringe Sterblichkeit; 1.-8.LW • Colidiarrhoe: - nur Neugeborene und Absetzer, Chemotherapie! • Dysenterie: - weniger akut, Kotfarbe, Chemotherapie! - max. 30 % eines Mastbestandes befallen • Chron. Schweinepest: - langanhaltendes Fieber! Epizootische Virusdiarrhoe Epizootische Virusdiarrhoe Therapie Immunität und Impfung • Ferkel: • • • • reichlich klares Wasser Volumenauffüllung (Niere):5 g NaCl + 50 g Glucose/l evtl. parenteral 1,2% NaHCO3 + 5% Glucose, Amynin Baytril, Apralan, Neodiar-Doser (Sek.Erreger) • Mast: • Futterentzug 4-5d, dann halbe Ration • Einzeltierbehandlung (Inj.): Enrofloxacin, Gentamycinsulfat, Trimethoprim-Sulfonamid • Futtermedikation (Sek.Erreger): Neomycinsulfat, Colistinsulfat (je 250 ppm) über 14d • Vitaminisierung (Malabsorption) • Keine dauerhaft belastbare Immunität • Beginn: 4-5w, Ende 5m • mehrfache Reinfektion im Mastabschnitt möglich bei kontinuierlicher Belegung • bislang keine zuverlässige Vakzinierung möglich • Stalltemperatur erhöhen! • Liegeflächen trocken halten! Epizootische Virusdiarrhoe Vomiting und Wasting Disease Prophylaxe Steckbrief • Eingliederung der Jungsauen • Mast: Rein-Raus-Verfahren! Elimination aus Bestand Durchseuchung des Gesamtbestandes, sonst erkrankt jede neu eingestallte Gruppe • Kontaktsuppe für gesamten Bestand • Futterentzug für 3-4 Tage • Keine Milchprodukte (Osmose) • Hygiene (Personen, Geräte, Tiertransporter, Zuchtviehmärkte) • Kot als Hauptinfektionsquelle - Erreger: Haemagglutinierendes Encephalomyelitis-Virus (Corona) - Anzeige/Meldepflicht: - Betroffene Altersstufe: 1.- 3. LW - Besonderheiten: Erbrechen und Kümmern - VW in Europa; Nordamerika: Ontario Encephalomyelitis - Inkubationszeit: 4 - 5d - Morbidität: bis 10 % Mortalität: 100 % - Epidemiologie: epizootisch/enzootisch - Heilung: keine Heilung möglich - Bedeutung: gering Vomiting und Wasting Disease Vomiting und Wasting Disease Steckbrief Pathogenese - Erbrechen und Kümmern der Saugferkel - keine Heilung möglich 4-5d Magenwandganglien Stammhirn Bulbus olfactorius nasale Aufnahme N.vagus Vomiting und Wasting Disease Vomiting und Wasting Disease Pathogenese Klinik keine Diarrhoe Lähmung der Magenwand d5 Magenerweiterung Magenwandganglien Saugferkel erste 3 LW milde Hirnsymptome Stammhirn Bulbus olfactorius nasale Aufnahme Anorexie Erbrechen 1. Erbrechen kurz nach Saugakt 2. Auftreibung der Magengegend 3. Kümmern über mehrere Wochen maternale AK Vomiting und Wasting Disease Vomiting und Wasting Disease Sektion Sektion - starke Abmagerung - blaß-graue Haut, struppig - prall mit Milchbrei gefüllter Magen - stark geweitet Ferkel, kümmernd mit aufgetriebener Magengegend - Histologie: entzündliche Infiltration der Nerven der Magenwand (v.a. Pylorusregion) - oft nichteitrige Enzephalitis Vomiting und Wasting Disease Vomiting und Wasting Disease Diagnose Differentialdiagnostik - Klinik + Bestandssituation - Sektion - - Abmagerung - Magenerweiterung - Histo: milde Enzephalitis + Ganglienzelldegeneration - jede Altersgruppe, Ferkel besonders stark betroffen - Saugferkel bis 10 d: 100 % Mortalität - Virusisolation (Tonsillen, Hirn, Lunge) nur bei extrem frisch klinischen Tieren; selten nötig Anfangsstadien akuter Gastro-Enteritiden TGE und EVD Colidiarrhoe Clostridium perfringens Typ C - stets Diarrhoe nach dem Erbrechen, nie Verstopfung Vomiting und Wasting Disease Vomiting und Wasting Disease Therapie Immunität und Impfung - keine Therapie möglich - stumme Durchseuchung mancher Bestände - Immunisierung der Sau mit Teilen erkrankter Ferkel - Schutz der Ferkel durch Kolostrum - Virusneutralisierende AK ab d7-12p.i. - keine Vakzinierung möglich Vomiting und Wasting Disease Rota-Virus-Infektion Prophylaxe Steckbrief - • • • • • ständige AK-Versorgung der Saugferkel Kontaktsuppe für Zuchtsauen (spätestens 14 d a.p.) Eingliederung der Jungsauen Hygiene (Personen, Geräte, Tiertransporte) Rota-Virus-Infektion Appetitlosigkeit gelegentliches Erbrechen nachfolgend Durchfall milder Verlauf 2-Wochendurchfall (+Coli) Rota-Virus-Infektion Steckbrief Erreger • • • • • • • • • • • • • • • • • • Erreger: Rota-Virus (Serotyp A) Anzeige/Meldepflicht: Betroffene Altersstufe: zwischen 10. und 20. LT Besonderheiten: wenig wirtsspezifisch (Jungtiere + Kinder) Inkubationszeit: 0,5 - 2d Morbidität: bis 100 % Mortalität: bis 50 % Durchseuchung: rasch Epidemiologie: enzootisch Heilung: wenige Tage Dauer Bedeutung: häufig mit Coli vergesellschaftet Klasse: Rota, Serotyp A Aufbau: behülltes DNA-Virus, Reoviren Serotypen: Besonderheiten: Tenazität: RT 9m; schwer desinfizierbar Verbreitung: ubiquitär verbreitet Reservoir: subklinische Ausscheider (Ferkel, Sauen, Katze, Hund, Nager, ...) • Desinfektion: Formalin Rota-Virus-Infektion Rota-Virus-Infektion Pathogenese Klinik Exsikkation 1-7d massenhafte Ausscheidung mit dem Durchfall -kot Resorptionsstörung Steatorrhoe Reizung Anorexie Erbrechen Apathie orale Aufnahme Zottenverkürzung Jejunum Ileum Ausbreitung bei fehlendem Kolostralschutz 1. Erbrechen, Apathie, Anorexie 2. Durchfall hellgelb-pastös - dunkelbraun übelriechend, Nahrungsreste, molkeähnlich wenige Tage Dauer (1-7) 3. Exsikkose + Schwäche - Hypoglykämie, Gewichtsverluste bis 30 % 4. evtl. Kümmern Rota-Virus-Infektion Rota-Virus-Infektion Sektion Diagnose • akute katarrhalische Enteritis • Histologisch: Zottenverkürzung • Klinik • Sektion: Absterben der Zottenspitzen • Virusnachweis: • Elektronenmikroskopie, ELISA, PCR (Durchfallkot) • Immunfluoreszenz (Darmschleimhaut) • AK-Nachweis: max. 2-4w p.i. sinnlos wegen hohem Durchseuchungsgrad Rota-Virus-Infektion Rota-Virus-Infektion Differentialdiagnostik Therapie • TGE und EVD in chron. teildurchseuchten Großbeständen • • • • • Erregernachweis • Kokzidiose • Therapieversuch • Strongyloidose • Therapieversuch • Kolidiarrhoe • Nahrungsfreier, dünner Kot • Clostridieninfektion Zweiwochendurchfall! Koliwirksame Mittel: Heilung in 24 h Elektrolyt-Glucose-Lsg. ad. lib. Starterfutter absetzen (osmotische Belastung) Rota-Virus-Infektion Rota-Virus-Infektion Immunität und Impfung Prophylaxe • Immunisierung der tragenden Sauen durch Kotkontakt • Jungsauen eingliedern • • • • • • • genügende AK-Versorgung der Saugferkel Eingliederung der Jungsauen Futterentzug Hygiene (Personen, Geräte, Tiertransporte) Kot als Hauptinfektionsquelle Reinigung und Desinfektion der Abferkelställe Rein-Raus! Coliruhr (5) Colienterotoxämie/ Ödemkrankheit nein Fimbrien ja F18 (Rez ab d21) (6) Coliendotoxämie (7) Colidiarrhoe Absetzer Toxine: SLT, Endotoxin+Mast F4,5,6 ST, LT (Rez ab Geburt) (1) Colidiarrhoe der Neugeborenen ja maternale AK nein (2) Colisepsis wenig (3) 3-Wochendurchfall Steckbrief • • • • weitverbreitete, verlustreiche Durchfallerkrankung Geburt bis Absetzen 80 % aller Ferkeldurchfälle 50 % aller Ferkelverluste Futterumstellung (4) Colidiarrhoe der Absetzferkel atypische Stämme: (8) MMA, Zystitis, ... Coliruhr Coliruhr Steckbrief Erreger • • • • • • • • • • • • Klasse: ETEC (Enterotoxinbildende Stämme) • Aufbau: gramnegative Stäbchen • Serotypen: -O8, 138, 139, 141, 147, 149, 157 • Virulenzfaktoren: Fimbrien: F4, F5, F6, F41 Enterotoxine: Sta (hitzestabil) Lt (hitzelabil): nur sekretionssteigernd! • Tenazität: RT: 10 d; -20°C: 6M-Jahre; Sonne: 6h • Verbreitungswege: • Reservoir: ubiquitär verbreitet • Desinfektion: Formalin Erreger: Escherichia coli Anzeige/Meldepflicht: Betroffene Altersstufe: Geburt bis Absetzen Besonderheiten: Neugeborene / 3.-4. LW / Absetzen Inkubationszeit: 0,5 - 4d Morbidität: bis 100 % Mortalität: bis 100 % Durchseuchung: akute Erkrankung Epidemiologie: enzootisch Heilung: ohne Medikation kaum Aussichten Bedeutung: groß Coliruhr Coliruhr Erreger Pathogenese Milchmangel keine Immunität geringe Aufnahme Exsikkose wässriger, nahrungsfreier Durchfall zu wenige AK orale Aufnahme aus Umgebung Elektrolyt- und Wasserverluste Anheften und massenhafte Vermehrung durch Fimbrien Freisetzung von Enterotoxinen Beeinträchtigung der Enterozytentransportfunktion Anheften von E.Coli an der Zottenoberfläche Coliruhr Coliruhr Virulenzfaktoren Virulenzfaktoren • Fimbrien F4, F5 • Enterotoxine • Fehlen serotypischer AK in Kolostrum • • • • Zukauf Absetzen von stark immunen Sauen MMA, Agalaktie, Futterumstellung Genetik: kein F4-Ag bei der Sau Coliruhr Coliruhr Klinik Klinik Coliruhr beim Saugferkel Coliruhr Coliruhr Sektion Klinik • Dünndarm gering hyperämisch oder o.B. • Darminhalt wäßrig mit Milchflocken Coliruhr nach dem Absetzen Coliruhr Coliruhr Diagnose Erregernachweis • enzootisches Auftreten wäßrigen Durchfalls • Neugeborene, 3./4. LW oder kurz nach Absetzen • BU: hoher Gehalt an ETEC im oberen Dünndarmbereich (frisch tote Tiere verwenden) • Pathogene Serotypen im Kot • Sektion • Immunfluoreszenz des Virus-Ag (Darmschleimhaut/Kot) • Anzüchtung Zellkultur • PCR • nur geringe Hyperämie des Dünndarms • Serotyp? Impfung! • Resistenztest! Chemotherapie Coliruhr Differentialdiagnostik • TGE: - akuter Verlauf, keine Altersbeschränkung - totaler Zottenverlust - transparenter Darm - Chemotherapieresistent - Immunfluoreszenz, Virusneutralisierende AK • Strongyloidose: - Diarrhoe frühestens ab d3, meist Ende 1.LW - keine plötzlichen Todesfälle - Anämie - Anthelmintika wirksam - Parasitol. Untersuchung • Nekrotisierende Enteritis: - 1. und 2. LW, nie in ersten 12 h - Kot gelb-schaumig, blutgefärbt, übelriechend - Chemotherapie wirkungslos - mehrere cm lange Nekrose pathognomonisch Coliruhr Differentialdiagnostik • Kokzidiose: - v.a. ab 2. LW - gelb-pastöser bis grau-wäßriger, übelriechender Durchfall - Zottenatrophie - Sporozoiten in Enterozyten - Kotuntersuchung erst nach 5 Tagen positiv! • Rota: - gelblich-pastös - 3.LW, ungestörtes Allgemeinbefinden - spontane Heilung nach einigen Tagen • Dysenterie: - Absatzferkel - dunkel-schleimiger Kot, Blutspuren - Dickdarm! • S. typhimurium: - diphteroid bis ulzerierende Enteritis - Östrus - Milchüberschuß - Futterwechsel Coliruhr Coliruhr Therapie Immunität und Impfung • frisches Trinkwasser • tägliche Chemotherapie bis Heilung, oral/parenteral • • • • • Doser: Apralan, Neodiar, Baytril, Floracid • • • • • ältere Ferkel: Trinkwasserzusatz Absetzer, Fütterungs-AB orale Rehydratation mit Glucose-Elektrolyt-Lsg. Stalltemperatur erhöhen! Liegeflächen trocken halten! Zuchtsau oral vakzinieren! Grundimmunisierung Abstand von 3-4w vor jeder Abferkelung wiederholen Impfstoffe mit • Zellwandantigen, Toxin, Fimbrien (Enterisol, Coli3Plus, ColiporcPlus) • evtl. Stallvakzine nach vorheriger Typisierung • Metaphylaxe: Futtermedikation der Sau um Geburtstermin Coliruhr E. coli F4-Rezeptoren Prophylaxe SSC13 • Rein-Raus-Verfahren im Abferkelstall • • • • • • Waschen der Sauen vor Abferkeln gründliche R+D vor jedem Neubelegen: Stalosan F evtl. Zwischendesinfektionen Wärmestrahler rechtzeitig vorbereiten Sau rechtzeitig in Abferkelstall bringen - AK gründliche Kotbeseitigung zur Säugezeit MUC-4 • Coli-Immunität verbessern durch Kontaktsuppe an tragende Sauen; Jungsauen: 3w vor Belegen + 3w vor Geburt • MMA-Vorbeuge: • • • • ? F4ac F Duroc (17) Hampshire (9) Landrace (126) Yorkshire (111) % Empfindlich % Resistent 12,00 0,00 99,00 80,00 88,00 100,00 1,00 20,00 % Resistenzallele (1992) E D C B 10,00 (36,00) 45,00 (41,00) Dia zur Verfügung gestellt von Jorgensen, 2006 Autosomal rezessiver Erbgang (Gibbons et al., 1977) • F4ab/ac: Kopplung mit Transferrin-Locus (Guerrin et al., 1993) • Kartierung auf SSC13 (EdforsLilja et al., 1995) • Feinkartierung: Mucin-4 als Kandidatengen, Gentest patentiert (Joergensen et al., 2003) A F4R Estimated effects in Danish pigs Breed Genotype Breedin gIndex 94,00 (100,00) 100,00 (100,00) • F4ad • Genetik: SSC13: F4! • Sauen impfen mit Coliporc, Enterisol Coli, Porcovac o.ä. Rasse (n) Resistente und empfindliche Phänotypen bezüglich ETEC F4 unterscheidbar (Sellwood, 1975) F4ab 3d a.p. vor bis 3d p.p. 2x täglich 15g Glaubersalz evtl. pH-senkende Futterzusätze, z.B. Calci-Cap evtl. Fütterungsantibiotikum zu dieser Zeit rechtzeitige Gebärmutterbehandlung MUC4-Frequenzen in Dänemark • Subindex LG5 Landrace RR SR SS pvalue Yorkshir RR SR e SS pvalue Daily gain 30-100 kg 16,6 Strength Meat % Slaugther loss Piglets born 0,476 Daily gain 0-30 kg 3,27 Feed 115,3 -0,0387 0,073 0,064 0,172 3,93 113,0 0,373 2,92 21,3 -0,0453 0,0485 0,111 0,169 111,1 0,086 < *** 0,0001 0,157 2,49 19,3 -0,0441 0,0342 0,186 0,074 ** 0,0002 107,3 105,6 0,095 103,5 -0,025 *** < 0,0001 + ** 0,0003 + NS 0,44 1,53 1,06 0,49 NS 0,12 NS 0,28 4,2 7,9 11,2 ** 0,0020 (-) NS * 0,51 0,044 -0,0081 0,0696 -0,0134 0,0674 -0,0176 0,0617 *** < 0,0001 NS 0,75 ** 4,02 4,03 *** 0,0008 < 0,0001 -0,01 0,086 0,016 0,035 NS 0,09 (-) (+) (-) 0,036 -0,007 ** 0,0003 - NS 0,23 2,53 2,38 2,46 *** < 0,0001 (+) Maria Johannsen, Bjarne Nielsen, Danish Slaughterhouses Coli bei Absetzern Colienterotoxämie Steckbrief Steckbrief • 3 Erkrankungsformen nach dem Absetzen der Ferkel, abhängig vom gebildeten Toxin • darmeigene E.Coli als Ursache • • • • • • • • • • • Erreger: Escherichia coli Anzeige/Meldepflicht: Betroffene Altersstufe: Absetzer, Vormast Besonderheiten: Das Toxin bestimmt die Erkrankung Inkubationszeit: 1w (Tage bis 2w nach Absetzen) Morbidität: bis 50 %, beste Tiere Mortalität: Enteritis bis 30 %, Ödem 95 % Durchseuchung: endemisch im Bestand Epidemiologie: endemisch Heilung: Enteritis: gut, Ödem: kaum Aussichten Bedeutung: 50 % der Ferkelverluste Coli bei Absetzern Coli bei Absetzern Erreger Pathogenese • • • • Klasse: Enterobacteriaceae Aufbau: gramnegative Stäbchen Serotypen: O138, O139, O141, O157, ... Besonderheiten: Virulenzfaktoren: Fimbrienantigene: F18 Toxine: SLTIIv (Neuro bzw. Vasotoxin) • • • • Tenazität: hoch Verbreitungswege: ubiquitär, Sauenkot Reservoir: Sauen Desinfektion: z.B. Lomasept Übererregbar Krämpfe Seitenlage Radfahren Kümmern verminderte E.Coli: apathogene Peristaltik und pathogene Maldigestion Formen im Dickdarm Malabsorption explosionsartige Vermehrung innerhalb 1 Woche Hypoxie Dyspnoe ZNS Lunge Resorptionsumkehr Ödeme Plasmaaustritt Dünndarmbesiedlung durch Fimbrien Blutkreislauf Coli bei Absetzern Colienterotoxämie Klinik Klinik • 1. Colienteritis • Diarrhoe wäßrig, graubraun evtl. blutig-schleimig • Austrocknung, evtl. Kümmern • 2. Ödemkrankheit (Colienterotoxämie) generalisierte Ödeme Nasenrücken, Augenlider ZNS (Krämpfe, Lähmungen, Seitenlage, Ruderbewegungen) Dyspnoe verwaschene Lidbindehäute Standardfutter, die best entwickelten Tiere • 3. Schock • völlig gesunde Tiere, plötzlicher Tod im Schock • Zyanosen, verwaschene rote Konjunktiven • Hackfrucht-Getreide Schock Futterumstellung Wasser + Elektrolytverlust Ad lib.-Fütterung Magenüberladung Diarrhoe Freisetzung von Toxinen: Enterotoxin • • • • • • Tod in 24 h Lidödem Vasotoxin Endotoxin Blutdruckabfall Histamin Cytokine Colienterotoxämie Colienterotoxämie Klinik Klinik Ödemkot Colienteritiskot Coli bei Absetzern Colienterotoxämie Sektion Sektion • 1. Ödemkrankheit • Ödeme in Magenwand, Dickdarmgekröse, Lunge, ZNS • Fibrinöse Ergüsse Herzbeutel, Brust- u. Bauchhöhle • ZNS Histo: perivasculäre Ödeme Enzephalomalazie Zysten • 2. Colischock • Darmhyperämie • serofibrinöse Ergüsse in die Körperhöhlen Magenwandödem Colienterotoxämie Colienterotoxämie Sektion Sektion Kolonödem Fibrinausschwitzung bei Ödemkrankheit Colienterotoxämie Colienterotoxämie Sektion Sektion Meningitis bei Ödemkrankheit Nasenrückenödem Colienterotoxämie Colienterotoxämie Diagnose Erregernachweis • Klinik und Sektion • BU: Bestimmung der Serotypen aus Darm und Hirn, F18, SLT • Resistenztest • nicht fieberhaft • Immunfluoreszenz Darm und Hirn • Darm-BU+Molekulargenetik Coli bei Absetzern Coli bei Absetzern Differentialdiagnostik Therapie • Colienteritis: • Ödem: praktisch nicht möglich • Ausschwemmen gelingt nicht wegen Kreislaufschwäche • Metaphylaxe: • Dysenterie - Dickdarm betroffen • Salmonellose • 48 h hungern • frisches Wasser • 1w Trinkwasser-/Futtermedikation, evtl. Injektion Apramycin, Colistin, Neomycinsulfat (200 ppm) - generalisierte Symptomatik • Ödemkrankheit: • • • • Nervöse Form der AK ESP Streptokockenmeningitis Arsanilsre-Vergiftung alle ohne Ödem • Schock: nicht möglich • Versuch mit Amynin, Enrofloxacin, Gentamycinsulfat Coli bei Absetzern Coli bei Absetzern Immunität und Impfung Prophylaxe • aktiv: Herstellung einer stallspezifischen Vakzine Verabreichung oral über 1 Woche - kaum praktikabel. • passiv: IgGs ins Futter einmischen (Eiklar mit AK gegen F4, F18, Rota (steht in Deutschland nicht zur Verfügung) • • • • • • • • • viel frisches Trinkwasser Nippelkontrolle (800 ml/Min) Futter rationieren Rohfaser auf > 6 % für 14 d RP auf < 16 % für 14 d Futtersäuren z.B. Aciprol Probiotika (Paciflor) evtl. AB.Futtermedikation für 14 d Genetik SSC13: F4 - sofort exprimiert - Ferkeldurchfall (ETEC) SSC6: F18 - erst ab d 20 exprimiert - Enterotoxämie (STEC) dominante Vererbung E. coli F18-Rezeptoren Voraussetzungen für eine Erkrankung durch E.coli SSC6 α-Fucosyltransferase FUT-1 ? 307 • F18-Rezeptor als Einfachgenort (Bertschinger et al., 1993) • F18 Kopplung mit MHS-Genort auf SSC6 (Vögeli et al., 1996) • Feinkartierung: FUT-1; Gentest patentiert (Meijerink et al., 1997) • Heute: Praxiseinsatz Schweiz, PIC 307 CTG ACG CAG CTG GCG CAG Leu Thr Kolonisation des Dünndarms über Fimbrien an Rezeptoren der Dünndarmschleimhaut F18R MAS gegen Enterotoxämie ACGC GCGC Cfol Leu Ala F18 F18R ab/ac Restriktionsmuster des α1FUT-Gens Glu Glu F18 F18R FUT1: Allelfrequenzen Rasse AA AG GG Large White 11% 45% 44% Schweizer Landrasse 1% 13% 86% Clostridium perfringens Typ A-Infektion Praxisanwendung Steckbrief • FUT1 und MHS eng gekoppelt – MHS-negative Schweine oft empfindlich gegen E. coli F18 – Co-Selektion notwendig • milde katarrhalische Enteritis • vorübergehende Beeinträchtigung des Allgemeinbefindens • Verluste bei Neueinschleppung • Integration in Zuchtprogramme – Schweiz – PIC (USA, DK, nicht in Deutschland) – Patente! Clostridium Typ A Clostridium Typ A Steckbrief Erreger • • • • • • • • • • • Klasse: Clostridium perfringens TypA • Aufbau: grampositiv, Stäbchen, Sporenbildner, anaerob • Serotypen: • Besonderheiten: α-Toxin • Tenazität: sehr resistent • Verbreitungswege: Zukauf • Reservoir: chron. infiz. Sauen-Herden; subklinische Ausscheider • Desinfektion: Formalin Erreger: Clostridium perfringens Anzeige/Meldepflicht: Betroffene Altersstufe: erste Lebenstage Besonderheiten: Verluste bei Neueinschleppung Inkubationszeit: 0,5 - 4d Morbidität: gering Mortalität: gering Epidemiologie: epizootisch Heilung: nach Tagen Bedeutung: zunehmend Clostridium Typ A Clostridium Typ A Pathogenese 1. Apathie, Anorexie, gesträubtes Haarkleid, Tod wäßriger gelblicher schleimiger Durchfall Trypsininhibitor aus Kolostrum leichte Resorptionsstörungen orale Aufnahme durch Kotkontakt Besiedlung Besalmembran im Jejunum Reizung d. Darmschleimhaut α-Toxin-Produktion (trypsinempfindlich) Klinik • perakut: Tod innerhalb 2d • sonst: – eingefallene Flanken – gelblich verschmierter After – wäßrig, schleimig, gelblicher Durchfall Clostridium Typ A Clostridium Typ A Klinik Sektion • • • • cremig-wäßriger nicht blutiger Inhalt geringe Enteritis keine Nekrosen Clostridium Typ A Clostridium Typ A Diagnose Therapie • Erregeranzüchtung mit Typisierung • perorale Penicillin-Gabe (Aviapen) • 2-3d Clostridium Typ A Clostridium Typ A Immunität und Impfung Prophylaxe • stallspezifischer Impfstoff kann hergestellt werden • am besten in Kombination mit E.Coli • Sauen regelmäßig waschen • Vakzinierung: stallspezifisch oder Toxoidimpfstoff C • Reinigung und Desinfektion oft unbefriedigend! • für Neugeborene: - Antibiotische Metaphylaxe: • magensaftresistentes Penicillin: Aviapen (40-80.000 IE) 1.+2.LT Nekrotisierende Enteritis der Saugferkel Steckbrief • • • • NE Clostridium perfringens TypC tödliche Darmerkrankung der Saugferkel hochgradige Störung des Allgemeinbefindens Blut im Ferkelkot, erste Lebenstage! Clostridium Typ C Steckbrief • • • • • • • • • • • Erreger: Clostridium perfringens (Typ C) Anzeige/Meldepflicht: Betroffene Altersstufe: erste LT bis max. 4 W Besonderheiten: anaerober Keim; hohe Verluste hoher Magensaft pH; Trypsininhibitoren Inkubationszeit: Stunden bis Tage Morbidität: 15 - 80 % Mortalität: 100 % Durchseuchung: rasch, perakuter Verlauf Epidemiologie: enzootisch: Monate bis Jahre im Bestand Heilung: keine Bedeutung: hohe Ferkelverluste Clostridium Typ C Clostridium Typ C Erreger Pathogenese • Klasse: • Aufbau: anaerob grampos. Stäbchen, Sporenbildner • Serotypen: Typ C • Besonderheiten: • Tenazität: extrem widerstandsfähig • Verbreitungswege: • Reservoir: chron. infiz. Sauen-Herden, Großbestände, verminderte Hygiene • Desinfektion: sehr schwierig Abhilfe: Hyperimmunserum 1. Apathie, Anorexie, gesträubtes Haarkleid, Tod 2. ab d2: gelblich-rötlicher schaumiger Durchfall Trypsininhibitor aus Kolostrum orale Aufnahme durch Kotkontakt irreversible Resorptionsstörungen Nekrosen Blutungen Emphyseme Besiedlung Besalmembran im Jejunum Ablösung der Basalmembran Clostridium Typ C Clostridium Typ C Klinik Sektion Verlauf abhängig von ß1-Toxin-Menge 1. perakut: plötzliche Todesfälle, noch kein Durchfall 2. akut: evtl. Erbrechen rötlich-brauner Durchfall Tod nach 24 h 3. chronisch: schaumiger, übelriechender, graugelblicher,grießiger Durchfall Tod durch Exsikkose und Elektrolytmangel • • • • • • ß1-Toxin-Produktion (trypsinempfindlich) akut - chronisch hämorrhagisch-nekrotisierende Jejunitis Darm äußerlich bandartig gestreift (Tigerstreifung) Nekrotische Membranen im Dünndarm Emphysem der Muskelschicht ringförmige Zonen, nur Teile betroffen akut: dünnflüssiger Kot rotbraun, übelriechend • chron.: graugelb grießiger Kot Clostridium Typ C Clostridium Typ C Sektion Sektion akut hämorrhagischer Darm Fibrin(Tiger-)streifung Clostridium Typ C Clostridium Typ C Sektion Sektion nur Teilbereiche betroffen evtl. mit Emphysem Fibrin(Tiger-)streifung Clostridium Typ C Diagnose • Blut im Ferkelkot erste LT: pathognomonisch • ß1-Toxin-Nachweis: Darminhalt, Peritonealflüssigkeit • PCR Clostridium Typ C Erregernachweis • monoklonale AK gegen ß1-Toxin = beweisend • evtl. Erregeranzüchtung zur Typisierung • PCR Clostridium Typ C Clostridium Typ C Differentialdiagnostik Therapie • Strongyloides: - im späteren Verlauf - ungestörtes Allgemeinbefinden - ab 4. LT, alle erkranken Antibiotische Therapie und Metaphylaxe: • magensaftresistentes Penicillin: Aviapen (40-80.000 IE) 1.+2.LT • TGE: - plötzlich im Bestand, alle Altersstufen - Kot gelblich-grünlich • Colidiarrhoe: - ungestörtes Allgemeinbefinden - Kot wäßrig weißlich-gelb • Isospora suis: - ähnlich Clostridium Typ C Clostridium Typ C Immunität und Impfung Prophylaxe • Impfstoffe: • Sauen regelmäßig waschen • Vakzinierung • Reinigung und Desinfektion oft unbefriedigend! • • • • Per-C-Porc Covexin 8 Clostricol Enterisol Coli Clost • für Neugeborene: - Hyperimmunserum für frisch geborene Ferkel - Antibiotische Prophylaxe: • magensaftresistentes Penicillin: Aviapen (40-80.000 IE) 1.+2.LT Durchfallerkrankungen und Leistungseinbußen im Mastbestand Leistungseinbußen und Diarrhoe im Mastbestand Tieralter; Resistenz/Immunität; Erregervirulenz; Begleit- und Mischinfektionen; Hygiene; Stressoren (Haltung, Fütterung, ...) Erreger Typische Bestandsproblematik Beteiligte Erreger deutliche Leistungsdepression Salmonellen; Nematoden; PCV2; E.coli; Clostridien; Verderbniskeime, ... Diarrhoe Brachyspiren; Lawsonien ⊗ ⊗ ⊗ ⊗ Diagnostik erschwert durch: Brachyspira hyodysenteriae ? Überlappende klinische Bilder Anzüchtung schwierig bis sehr schwierig Empfindlichkeit der Keime beim Transport Überwucherung durch Begleitkeime Brachyspira pilosicoli ? Lawsonia intracellularis ? Mischinfektion ? ⇒ Molekulare Methoden oft hilfreich Weiterführende Diagnostik ist essentiell ! • • • • Klinisches Bild und Sektionsbild oft nicht eindeutig Brachyspiren und Lawsonien weit verbreitet Mischinfektionen kommen regelmäßig vor Therapie und Prophylaxe auf Erreger abzustimmen • Diagnostik als Grundlage jeder Behandlung! Brachyspiren • Weite Verbreitung: jeder 3. Mastbetrieb betroffen • Signifikante ökonomische Verluste durch – Zurückbleiben im Wachstum/Auseinanderwachsen • Tägliche Zunahmen (minus 50 – 400 g = 1bis 8 €) • Futterverwertung (minus 0,6 = 7 €) – Futtermedikation (2-8 €) – Tierverluste (0-30 % = bis 33 €) – Milder endemischer Verlauf: • Gesamtverlust min. 5 € Brachyspiren • • B. hyodysenteriae B. pilosicoli • B. intermedia Schwein, Vögel • • • • B. innocens B. murdochii B. aalborgi B. alvinipulli Schwein, andere Dysenterie Schwein, Vögel, Mensch andere Intestinale Spirochätose Intestinale Spirochätose/ apathogen Schwein, andere apathogen Schwein, andere apathogen Mensch, Tiere Diarrhoe Vögel Intestinale Spirochätose Brachyspiren - Klinik • • • • Variabel! Leistungsminderung Anorexie, Apathie Kot – zunächst weich, • braun – später schleimig, • braun • blutigrot • zementfarben • Eingefallene Flanken • Blässe • Todesfälle Brachyspiren - Sektion • Herdförmige Typhlitis und Colitis Diagnostik - Grundproblem • Intermittierende Ausscheidung • insbesondere bei subklinischen Verlauf – akut: hämorrhagisch nekrotisierend – chronisch: herdförmig fibrinös nekrotisierend Diagnostik - Möglichkeiten • Brachyspiren – kultureller Nachweis • Resistenztest • Nachweisgrenze: 100 Keime/g Kot • Vitalität / Transport! – Serologie • Lawsonien Dysenterie Pathogenese – praktisch nicht möglich nekrotisierende Enteritis mit Vasculitis – IFAT, IPMA, ELISA • Zeitpunkt, Grad • rel. unzuverlässig – PCR – „einfacher Nachweis“ • Vitalität ohne Bedeutung • Differenzierung der Arten • (Resistenzen?) • 10.000 Keime/g Kot resistenzmindernde Faktoren: Umstallung, Futterwechsel, Transport, Stallklima Synchroner Nachweis nur mittels PCR möglich Brachyspiren - Klinik • • • • Brachyspiren - Klinik Variabel! Leistungsminderung Anorexie, Apathie, Fieber 39,5-40°C Kot: Dehydratation, Kreislaufversagen – zunächst weich, • braun – später schleimig, • braun • blutigrot • zementfarben • Entleerung des Dickdarms – eingefallene Flanken • Sickerblutungen - Blässe • Todesfälle blutiger Kot: erste Tage der Dysenterie zementfarben nach einigen Tagen Brachyspiren - Sektion Dysenterie Klinik • Herdförmige Typhlitis und Colitis – akut: hämorrhagisch nekrotisierend Fibrinbeimengungen • chronisch: herdförmig fibrinös nekrotisierend akut Hyperämie und Resorptionsstörung, Schleimbildung Schleimhautödem fibrinös herdförmig nekrotisierende hämorrhagische (Vasculitis) Kolitis/Caecitis mit Diarrhoe Dysenterie Bekämpfung auf Erreger abstimmen (Resistenzen!) Sektion • Dickdarmschleimhaut Ileitis Valnemulin Lincomycin 3-4 mg/kg 10 mg/kg ? 10 mg/kg 10 mg/kg 2,2 - 3,3 mg/kg 2,2 – 3,3 mg/kg ?? 2,2 – 3,3 mg/kg ?? 5 - 10 mg/kg - - 21 Tage 14 Tage 14 Tage Enterisol® Ileitis - - Behandlungsdauer Impfung Silberfärbung B. hyo: Erregermenge im Chymus korreliert mit Erkrankungsgrad* Nachteile der klassischen PCR 16 100000000 • Nachweisgrenze: 10.000 Keime/g Kot • Fehlende Quantifizierbarkeit: schlechte Korrelation mit Klinik/Sektion • Keine quantitative Gegenüberstellung der Einzelerreger bei Mischinfektionen • Gleiche Gewichtung trotz extremer Anteilsunterschiede 12 B. hyo per g Chymus • Folgeschritt nach PCR zur Darstellung der Produkte notwendig 14 10000000 10 1000000 8 100000 6 4 10000 2 1000 0 1 2 3 Tiere-Nr. * nach Davies et al., 2005 4 5 KlinScore Fibrinausfällung B. pilosicoli 3-4 mg/kg Tylosin chronisch B. hyo - Tiamulin akut chronisch n B. hyo KlinScore q-PCR q-PCR • Direkter Nachweis des genetischen Material des Erregers • unabhängig von Qualität der Probe! • Quantifizierung des Erregers Proben • Korrelation zum Befalls-/Erkrankungsgrad DNA-Extraktion • Steigerung der Sensitivität (ca. 1000 Keime/g Kot) • Amplifikation und Auswertung in einem Schritt RT-PCR ansetzen Lauf im Thermo-Cycler Messprinzip: Fluoreszenzsignal ~ Menge doppelsträngiger DNA • spart Zeit für Gelelektrophorese • reduziert Amplifikationsschritte • Aufwendige Etablierung, rel. teure Geräte • Hohe Präzision und hoher Durchsatz oder Mit Taq-man® Sonden CYBR®-Green Zusammenfassung q-PCR • Brachyspiren und Lawsonien sind • weit verbreitet und • von enormer ökonomischer Relevanz • Probleme für Prognose, Therapie und Prophylaxe: Proben DNA-Extraktion RT-PCR ansetzen Lauf im Thermo-Cycler Zeitpunkt Anstieg Fluoreszenzsignal ~ n Kopien Ausgangs-DNA • Klinische Bilder austauschbar • Mischinfektionen weit verbreitet • Bekämpfung erregerspezifisch • exakte weiterführende Diagnostik • qualitativ (welche[r] Erreger?) • quantitativ (Haupt- oder Nebenbefund?) • q-PCR als effiziente Unterstützung von • Bestandsbefunden • Klinik und Sektionsbefunde Zum Erreger Lawsonia intracellularis • obligat intrazelluläres Bakterium – gram-negativ, gekrümmt, mikroaerophil, nicht begeisselt, nicht sporenbildend, schwer anzüchtbar – 1931/1974/1995(McOrist et al., 1995) • weltweite Verbreitung • Zieltierarten – Schwein, Hamster, Blaufuchs, Pferd, Hirsch, Ratiten • keine Neigung zu Antibiotikaresistenz (McOrist 2000) Zum Erreger 4 Verlaufsformen 1) Porcine Intestinale Adenomatose • • • • • bakteriell nicht verkomplizierte Form kaum entzündliche Veränderungen Verdickung der Dünndarm-Schleimhaut Wucherung des Drüsenepithels Absetzer, auch ältere Tiere (6. - 20. LW) • • • tiefe, koagulierende Nekrosen durch bakterielle Komplikation graugelbe verkäsende Massen, Pseudomembranen Absetzer bis Endmast • • Beschränkung auf Ileum (Therapie von 3) „Wasserschlauch“, Hypertrophie der Muskulatur 2) Nekrotisierende Enteritis 3) Regionale Ileitis 4) Proliferat. Haemorrh. Enteropathie • • • • massive Blutungen aus adenomatöser Schleimhaut Ausfüllung des Dünndarms mit Blutgerinnseln 4. - 12. LM (Mast/Jungsauen) perakute/protrahierte Todesfälle PIA hat viele Gesichter. . . EUROPÄISCHE SEROPRÄVALENZ Prozent positiver Betriebe 93% 95% (PCR) 70% 100% 71% Weicher, blutiger oder schwarzer Kot Deutliche Größenunterschiede pro Bucht Wässriger Durchfall 62% 52% 57% . . . und kein Bestand ist vor PIA sicher 67% 73% EUROPÄISCHE SERO-PRÄVALENZ Prozent positiver Schweine Verbreitung hauptsä hauptsächlich orooro-fäkal 63% Vögel 54% 48% 33% 38% 31% Personal Sau -> Ferkel Gülle Horizontal 31% 31% Hauptsä Hauptsächliche Übertragung Nagetiere 31% Träger Auswirkungen der PIA Auseinanderwachsen Wässriger Durchfall Ungleiche Marktreife Fressen ohne zu wachsen Abmagerung mit Verlängerung der Mastperiode Plötzliche Todesfälle, besonders bei Jungsauen • PIA Chron. PIA – Diarrhoe, – Niedergeschlagenheit – Blässe – Tage bis Wochen – zunächst keine Anorexie – dennoch Auseinanderwachsen, Kümmern • NE/RI – Verschlechterter Allgemeinzustand – evtl Peritonitis – 1 % Todesfälle Akute PIA • PHE – blutige Durchfälle – teerartiger Kot – plötzliche Todesfälle (über Nacht) – JS Subklinische PIA Bleibt die subklinische PIA unbehandelt, geht sie häufig in die chronische Form über Subklinische PIA • Wird selten erkannt, weil sie häufig unauffällig verläuft • Sporadische Durchfälle, Größenunterschiede und Auseinanderwachsen können die einzigen Symptome sein. • Könnte eine Möglichkeit für eine frühe Diagnose und rechtzeitiges Einschreiten sein. Pathologie • Ileum, Caecum, Beginn Colon • hirnwindungsart verdickte Schleimhaut • Hämorrhagien • schwarzer, teerartiger Kot im Dickdarm (PHE) • graugelbe verkäsende Massen (NE) Subklinische PIA Diarrhoe Malabsorption Eindringpforte Ansiedlung im hinteren Dünndarmbereich Pathogenese I Schleimhautwucherungen Nekrosen Hämorrhagien orale Aufnahme Faktoren: Frühabsetzen, Umstallen, hohe Belegungsdichte, Futterumstellung, Pilzgifte, ... Zum Erreger Aufnahme in proliferative Kryptenzellen Pathogenese II -komplexe Darmflora notwendig Pathogenese III -Immunsystem entscheidend -Aufnahme in Vakuole Extrazelluläre Faktoren Rezeptoren + Intrazelluläre Faktoren Epithelzelle Differenzierung Transkriptionsfaktoren Krankheitsverlauf -Immunsystem entscheidend -Abgabe infizierter Zellen ins Darmlumen Proliferation -Austritt aus Vakuole -Umschaltung des Zellzyklus -Proliferation vs. Differenz. -Transkriptionsfaktoren unbekannt G0 interner Zeitgeber (p27) Stammzelle Zum Erreger Zum Erreger Pathogenese III Pathogenese III Extrazelluläre Faktoren Rezeptoren + Intrazelluläre Faktoren Epithelzelle Extrazelluläre Faktoren Rezeptoren + Intrazelluläre Faktoren Epithelzelle Differenzierung Differenzierung Transkriptionsfaktoren Proliferation G0 Stammzelle Transkriptionsfaktoren Proliferation interner Zeitgeber (p27) Immunität • • • • • Lawsonien Hauptsächlich IgM Maternale AK bis 3. Lebenswoche Serokonversion : 7 bis 24 Wochen Antikörperpersistenz < 2 Monate humorale Antwort > zelluläre Antwort G0 interner Zeitgeber (p27) Stammzelle Ileitis: aufgenommene Erregermenge korreliert mit Erkrankungsgrad* Kontrolle 5,4*108 5,4*109 5,4*1010 0 0 6,3 25 TZUN (g) 440 259 186 91 Futteraufnahme (g) 762 628 539 456 FVW (kg/kg) 1,7 2,4 2,9 5 Anteil mit Diarrhoe (%) 16 39 50 63 Länge der Läsionen (cm) 0 73 85 171 Mortalität (%) * nach Guedes et al., 2003 D u rc h sc h n ittlic h e T a g e sz u n ah m e (g ) Jeder Zentimeter Läsion = Reduktion der Tageszunahme von 1,6 g* Diagnose Diagnosemöglichkeiten von PIA 240 200 160 120 80 60 80 100 120 140 160 Schlachthof Makroskopisch Histologisch Labordiagnostik • Polymerase Chain Reaction • Immun - Floureszenz Test Läsionenlänge (cm) * nach McOrist 2002 Diagnose q-PCR • Direkter Nachweis des genetischen Material des Erregers • unabhängig von Qualität der Probe! Labordiagnostik von PIA ELISA: wenig aussagekräftig, starke indiv. Unterschiede IFAT: Antikörpernachweis aus Serumproben IFT: Erregernachweis in Gewebe/Kot PCR: 16S rRNA; 103/g Kot • Quantifizierung des Erregers • Korrelation zum Befalls-/Erkrankungsgrad • Steigerung der Sensitivität (ca. 1000 Keime/g Kot) • Amplifikation und Auswertung in einem Schritt • spart Zeit für Gelelektrophorese • reduziert Amplifikationsschritte • Aufwendige Etablierung, rel. teure Geräte • Hohe Präzision und hoher Durchsatz q-PCR Proben DNA-Extraktion q-PCR RT-PCR ansetzen Lauf im Thermo-Cycler Messprinzip: Fluoreszenzsignal ~ Menge doppelsträngiger DNA oder Mit Taq-man® Sonden CYBR®-Green Proben DNA-Extraktion RT-PCR ansetzen Lauf im Thermo-Cycler Zeitpunkt Anstieg Fluoreszenzsignal ~ n Kopien Ausgangs-DNA Lawsonia Serologie – Querschnittsstudie Krankheitsausbruch Sensitivität/Spezifität Behandlung • Untersuchung mehrerer Kotproben aus positiven Betrieben: – 84,6 % der Proben positiv • Übereinstimmung zwischen zwei Untersuchungsstellen: – Kotproben: 3 von 3 – Organproben: 10 von 11 – Kot-/Organproben: 3 von 4 Bekämpfung auf Erreger abstimmen (Resistenzen!) Ileitis Valnemulin Tiamulin Lincomycin Tylosin Behandlungsdauer Impfung B. hyo B. pilosicoli - 3-4 mg/kg 3-4 mg/kg 10 mg/kg ?? 10 mg/kg 10 mg/kg 2,2 - 3,3 mg/kg 2,2 – 3,3 mg/kg ?? 2,2 – 3,3 mg/kg ?? 5 - 10 mg/kg - - 21 Tage 14 Tage 14 Tage Enterisol® Ileitis - - Warum Tylosin bei PIA • Tylan Soluble ist derzeit das einzige Produkt, dass speziell für die Behandlung von Lawsonia intracellularis zugelassen ist. • Es hat in klinischen Zulassungsstudien seine Wirksamkeit bewiesen • Trotz 40 Jahren Einsatz von Tylan gibt es keine Resistenzen der Lawsonien Warum Tylosin bei PIA? • Die Gruppe der Makrolide reichern sich nachgewiesenermaßen intrazellulär an. • Dementsprechend liegt es nahe, dass sich auch Tylan Soluble in den Epithelzellen des Darms anreichert, wo Lawsonia intracellularis angreift • Die intrazelluläre Anreicherung ist wichtig, um PIA vorzubeugen und zu behandeln. Alternative Medikation • Chlortetrazykline 500 ppm • Tiamulin 200 ppm • Lincospectin 100 ppm Impfung • • • • Enterisol Ileitis (Boehringer, Ingelheim) per Drench orale Eingabe Absatzferkel mind. 14 tage vor Auftreten erster klinischer Symptome Prophylaxemassnahmen • Zukauf • • • • eine Herkunft Überprüfung der Herkünfte vertikale Integration, Rückmeldung Selbst jahrelang frei erscheinende Bestände können betroffen sein! • Einstallquarantäne: Klinik kurz nach Einstallung Prophylaxemassnahmen Epidemiologie • Mortalität durch NE/RI: 1 % • Leistungseinbussen: 2,5 – 20 % • Ausscheidung ab 1 Woche p.i. bis min. 12 Wochen • Absetzer > Mast > Sauen • Herdengrösse als Risikofaktor • Kontakt Sauen - Flatdeck Prophylaxemassnahmen • Haltung • geschlossenes System • Rein-Raus • Keine Mischung von Tieren/Altersstufen • Nagerkontrolle Ileitis - Wirtschaftliche Auswirkungen • Bei Ausbruch: • • • • • Impfprophylaxe nicht möglich Abschottung erkrankter Tiere Kotkontamination! Kotbeseitigung und Desinfektion gründliche und vollständige Reinigung • evtl. Einstallprophylaxe Der negative Einfluss der Ileitis auf den Deckungsbeitrag reicht von 1,44 € pro Schwein bei milder bis zu 17,09 € bei schwerer Verlaufsform, bei einem Schlachtpreis von 1,29 €. Zusammenfassung internationaler Studien: milde Ileitis schwere Ileitis Futterverwertung -6% - 25 % Tageszunahmen -9% - 21 % Mortalität (Steigerung) 1-2 % Ausfälle (Steigerung) • Tylan 200 ppm über 3 x 7 d Quelle : Estimates of the Economic Impact of Porcine Proliferative Enteropathy; A Hypothetical Evaluation. Fleck Veenhuizen, et al., 2002. 3– 6% 2 – 17 % Parasitosen des Schweins Übersicht Spulwurm Steckbrief Name 1. Ort 2. Orte Schäden Klinik Hyostrongylus rubidus Roter Magenwurm Magen - Blutsauger Anämie, Leistungsminderung Ascaris suum Spulwurm Dünndarm Leber Lunge Wanderstadien Nahrungskonkurrenz Fieber, Husten, Dyspnoe, Sek.Inf. Strongyloides ransomi Zwergfadenwurm Dünndarm Haut Lunge Wanderstadien Blutsauger Diarrhoe 2.LW Quaddeln, Kümmern Oesophagostomum Knötchenwurm Dickdarm - Darmepithelschäden Sek. Inf., blutige Diarr. Leistungsminderung Trichuris suis Peitschenwurm Dickdarm Darm Wanderstadien Blutsauger Anämie, Diarrhoe Leistungsminderung Metastrongylus sp. Lungenwurm Lunge Darm Entzündung, Sek.Inf. Dyspnoe, Husten Sarcoptes suis Räude Haut - Juckreiz, Unruhe Leistungsminderung • erhebliche Schäden bei Mastschweinen • Milchflecken auf der Leber Spulwurm Spulwurm Steckbrief Erreger • • • • • • • • • Erreger: Ascaris suum Anzeige/Meldepflicht: Betroffene Altersstufe: Alle Besonderheiten: 3 Organe: Darm, Leber, Lunge Inkubationszeit: Präpatenz 8 - 9 w Morbidität: 100 % Mortalität: 0 % Durchseuchung, Epidemiologie: endemisch Bedeutung: Wegbereiter für Sek.Inf., Leistungsrückgang schwerste wirtschaftliche Verluste: Mast kontinuierlich Spulwurm Pathogenese Mastleistung Kümmern Anämie Blutungen, Entzündungen Stoffwechselstörungen Eier 10 Jahre infektiös Außenentwicklung Mai - Sept. • Aufbau: gelblich-weiß bis blaß-rötlich m: 15-25 cm x 3-4 mm w: 20-30 cm x 5-6 mm • Verbreitungswege: Kot • Reservoir: Jungsauen bis 1. Geburt • Desinfektion: Schwefelkohlenstoff-haltige Mittel; Sodalösung; Feuer Erdausläufe praktisch nicht möglich Spulwurm Klinik Blutungen in Alveolen Husten Wurmknötchen Adulte im Dünndarm: Nährstoffentzug 0,1-1,5 Mio Eier/d • Klasse: Rundwürmer orale Aufnahme Milchflecken Wanderstadium Leber - 4. Larve 5 Tage Einbohren in Blutgefäße - Ileum, Caecum, Kolon Schlupf 3. Larve 3. Larve im Ei infektiös nach 30-40 d • v.a. Ferkel und Vormast betroffen • Blutarmut, Wachstumsrückgang, Kümmern • Wanderstadien bewirken bei massiver Eiaufnahme: – Fieber, Husten, Dyspnoe mit ausgeprägter Bauchatmung – Anorexie, Wachstumsstillstand, Kümmern, blaßgraue Haut • Lunge: Eintrittspforte für Sek. Erreger (EP, Influenza) • Darmkatarrh durch Reizung, – evtl. Darmverschluß Spulwurm Spulwurm Klinik Sektion • katarrhalische Enteritis • Spulwürmer im Darm • Leber: Schwellung und Blutungen • später Milchflecken • Lunge: punktförmige Blutungen Spulwürmer im Darm Spulwurm Spulwurm Sektion Diagnose • Rückmeldung vom Schlachthof • Kotuntersuchung Flotation • Eier dickschalig+höckrig Spulwürmer im Darm Milchflecken Spulwurm Spulwurm Therapie Immunität und Impfung • Sauen: – 10 d a.p. (Umstallen) gründlich waschen – regelmäßige Bestandsbehandlung 2 x/ Jahr 4 Wochen Abstand (Wanderstadien)! • Mastläufer zu Beginn der Vormast • relative Immunität bei älteren Tieren Spulwurm Knötchenwurm Prophylaxe Steckbrief • sehr schwer desinfizierbar • Weidegang und Auslauf • Befallsrate steigt mit dem Alter an • Dickdarm befallen • Schwefelkohlenstoffe • heiße Sodalösung • Hitze • • • • • Hygiene regelmäßige und gründliche Kotbeseitigung Ferkel nur in saubere Bereiche einbringen regelmäßige Bestandsbehandlung Mast: Rein-Raus-System Knötchenwurm Knötchenwurm Steckbrief Erreger • • • • • • • • • • • Klasse: Nematoden • Aufbau: weißlich 1-1,5 cm lang • Serotypen: • Besonderheiten: K • Tenazität: mehrere Monate, Überwinterung • Verbreitungswege: Kot • Reservoir: Verschmutze Einstreu, Ausläufe • Desinfektion: Endosan, Lomasept Erreger: Oesophagostomum dentatum/quadrispinulatum Anzeige/Meldepflicht: Betroffene Altersstufe: Läufer bis Sauen Besonderheiten: Knötchen im Dickdarm Präpatenz: bis 5 Wochen Morbidität: hoch Mortalität: gering Durchseuchung: chronisch Epidemiologie: endemisch Bedeutung: Sek.Inf. Knötchenwurm Knötchenwurm Pathogenese Abwehr schwere Durchfälle bei Jungtieren Klinik Entwicklungsstörungen Mastleistung Todesfälle Ansiedlung Dickund Blinddarm Eier Larven Knötchenbildung 2x Häutung evtl. Geschwüre 7-14d p.i. ins Darmlumen orale Aufnahme Eiablage Gipfel zur Säugezeit Aktivierung Sek.Inf. ansteckungsfähige 3.Larve verschmutzte Einstreu, Auslauf • • • • • • schleimig-blutige Durchfälle bei Jungtieren Entwicklungsstörungen Sauen: Gewichtsverluste Milchrückgang Rausche vermindert Wurfleistung vermindert Knötchenwurm Knötchenwurm Sektion Sektion • Knötchen in Blind- und Dickdarmschleimhaut bis erbsengroß • Schrumpfung des Blinddarms durch Faltenbildung • Rückbildung der Knötchen nur bei Erstinfektion Dickdarmschleimhaut Knötchenwurm Knötchenwurm Sektion Diagnose • Eier im Kot, Flotation Knötchen in Dickdarmschleimhaut Knötchenwurm Knötchenwurm Therapie Prophylaxe • Zuchtsauen: 10d a.p. • Mastläufer Vormastbeginn • strohlose Stallhaltung • wirkungsvolle Kotbeseitigung • Langzeitentwurmung • Kurzzeitentwurmung Abstand 5-6w Peitschenwurm Peitschenwurm Steckbrief Steckbrief • Sauen mit Auslauf • Wurm spiralig aufgerollt • Blutsauger an Dickdarmschleimhaut • • • • • • • • • • Erreger: Trichuris suis Anzeige/Meldepflicht: Betroffene Altersstufe: Läufer bis Sauen Besonderheiten: Präpatenz: 50 d Morbidität: hoch Mortalität: gering Durchseuchung: chronisch Epidemiologie: endemisch Bedeutung: Sek. Erreger Peitschenwurm Peitschenwurm Erreger Pathogenese • • • • • Durchfall Klasse: Rundwürmer Aufbau: schlank, 35-55 mm Serotypen: Besonderheiten: Spikulum, spiralig eingerollt Tenazität: jahrelang im Freien; stirbt bei Trockenheit und Sonne ab; • Verbreitungswege: Kot • Reservoir: Schweine, Ausläufe • Desinfektion: Endosan, Lomasept Mastleistung Colitis+Typhlitis Sek.Erreger (Balant.) erhebliche Schadwirkung bei starkem Befall Eier 37°C: 3w draußen: 60-90d Eingraben + Blutsaugen ins Lumen ab d16 orale Aufnahme der Eier Schlupf Eindringen über Darmdrüsen Gewebepassage 13 Tage Embryonierung Peitschenwurm Peitschenwurm Klinik Sektion • Anämie • Diarrhoe – stinkend, dünnbreiig – Schleim- und Blutbeimengungen • Mastleistung, evtl. Todesfälle • Würmer an Schleimhaut con Caecum und Colon Peitschenwurm Peitschenwurm Diagnose Differentialdiagnostik • Kotprobe, Flotationsverfahren • zitronenförmige Eier • durchsichtige Polpfropfen • Dysenterie • Chemotherapie Peitschenwurm Peitschenwurm Therapie Prophylaxe • Ivermectin wirkt nicht! • Flubenol (Flubendazol) • Hygiene • Ausläufe • regelmäßige Entwurmung Roter Magenwurm Roter Magenwurm Steckbrief Steckbrief • Sauen mit Auslauf magern ab, werden anämisch und milcharm, rauschen schlecht • Magenfundusdrüsen betroffen • • • • • • • • • • Erreger: Hyostrongylus rubidus Anzeige/Meldepflicht: Betroffene Altersstufe: junge Läufer bis Sauen Besonderheiten: Blutsauger Präpatenz: 3 w Morbidität: bis 100 % Mortalität: gering Durchseuchung: chronisch Epidemiologie: endemisch Bedeutung: Fruchtbarkeit Roter Magenwurm Roter Magenwurm Erreger Pathogenese • Klasse: Nematoden • Aufbau: schlank, rötlich m: 4-7 mm; w: 5-11 mm • Serotypen: • Besonderheiten: schmarotzt in Magenschleimhaut • Tenazität: hoch • Verbreitungswege: feuchte Weiden, Tiefställe • Reservoir: feuchte Weiden, Tiefställe • Desinfektion: z.B. Endosan, Lomasept Einwandern in Fundusdrüsen 3./4.Häutung ab d 20 in Magenhöhle Eier orale Aufnahme Schlupf 7.d Infektiöse 3. Larve feuchte Einstreu Tiefstall 2 M lebensfähig Blutsaugen Anämie Gastritis Plasmaeiweißverlust Verdauungsstörung FVW reduziert Roter Magenwurm Roter Magenwurm Klinik Sektion • Sau: – Anämie, evtl. dunkler Kot – Abmagerung, Milchmangel, schlechte Rausche • jüngere Tiere Milchmangel Rauschestörung • Magenschleimhaut pflastersteinartig • Entzündung + flache, schleimgefüllte Geschwüre • gelbliche Beläge, Würmer an deren Grund • linsen- bis haselnußgroße Knötchen • gelegentlich Todesfälle mit Magenblutungen – Anämie, Blässe, FVW, FA, Zun Roter Magenwurm Roter Magenwurm Sektion Diagnose • Flotationsverfahren • Ei entspricht Knötchenwurm Larvenanzüchtung nötig • Sektion: Magenbefunde Würmer als dunkelrote Striche Fundusdrüse mit Drittlarve Abmagerung Roter Magenwurm Roter Magenwurm Differentialdiagnostik Therapie • Magengeschwür – Sektion • mehrmalige Behandlung notwendig, da Larve 4 Ruhephasen einlegen kann • Langzeitentwurmung empfohlen Roter Magenwurm Roter Magenwurm Immunität und Impfung Prophylaxe • mit steigender Immunität sinken • halbjährliche Bestandskontrolle + Entwurmung • Zuchtstall vor Umstallung behandeln • Gründliche Kotbeseitigung • Wurmgröße • Eiausstoß Zwergfadenwurm Zwergfadenwurm Steckbrief Steckbrief • Kümmern und Anämie bei Saugferkeln • Befall des Dünndarms • • • • • • • • • Erreger: Strongyloides ransomi Anzeige/Meldepflicht: Betroffene Altersstufe: Alle, Ferkel besonders betroffen Besonderheiten: Sek.Inf. von Darm und Lunge (Körperwanderung) Präpatenz: 6d Morbidität: bis 100 % Mortalität: $ Durchseuchung, Epidemiologie: endemisch Bedeutung: weit verbreitet Zwergfadenwurm Zwergfadenwurm Erreger Pathogenese Einbohren vorderer • • • • • • • • Klasse: Nematoden Aufbau: haarfein, 3-5 mm lang Serotypen: Besonderheiten: parasitische und nichtparasitische Phase beim weiblichen Wurm Tenazität: hoch Verbreitungswege: Kot, Schmutz, Kolostrum! Reservoir: Sauen, Schmutz Desinfektion: z.B. Endosan, Lomasept Dünndarm: Dünndarm; nach 4d Einwandern in Beginn Eiablage Darmwandgefäße Ferkel: orale Aufnahme mit Kolostrum Entwicklung im Kot 4-6d 20°C Sau: perkutane Aufnahme der Larven auch perkutane Aufnahme Über Blutgefäße, Herz und Lunge: Unterhautfettgewebe Östrogenwirkung: Einwandern in Milch Zwergfadenwurm Zwergfadenwurm Klinik Sektion • • • • • • Durchfall ab Ende 1. LW gelblich-weiß Abmagerung struppiges Haarkleid, Blässe Kümmern hochrote flohstichartige Quaddeln • heftiger Juckreiz Anämie Reizung: Appetitmangel Durchfall Gewichtsrückstand Körperwanderung über Lunge + Schlund • 3 Organe betroffen: • Darm • Haut • Lunge • katarrhalische Enteritis Zwergfadenwurm Zwergfadenwurm Diagnose Erregernachweis • Auseinanderwachsen des Wurfes • Durchfälle 2. LW • Flotation: U-Larve in Eiern • • • • • dünnschalige Eier 25 x 50µm U-förmige Larve Flotationsverfahren ab d6 p.i. Schlupf im Ferkelkot bei 20°C nach 6-8h! • Trichinenkompressorium Dünndarmschleimhaut frisch toter Ferkel Zwergfadenwurm Zwergfadenwurm Differentialdiagnostik Therapie • Coliruhr: • Saugferkel: • erster Schub meist vor d 4-5 • Paste/Injektion d3, d6, d9 • 2. Schub (Haut) 4.w • Pechräude: • nur im Anfangsstadium • Sauen: • a) einmalige Injektion 10d a.p. (alle Stadien erfaßt) Ivermectin: 1 ml Ivomec auf 33 kg KG • b) oral über 5-10d 2 x jährlich gesamter Bestand Ivomec Prämix 2 ppm Ivermectin = 350 g/to über 7d Panacur (Fenbendazol) 250-500 g/to 5-10d Zwergfadenwurm Zwergfadenwurm Immunität und Impfung Prophylaxe • relative Immunität bei älteren Tieren • zuverlässige Kotbeseitigung • Entwurmung der Sau vor dem Umstallen Spulwurmwirksame Desinfektionsmittel Antiparasitika Wirkstoff Präparat Dosis Verabrei -chung WZ Ekto Para Spul Roter Magen Zwerg faden Knöt chen Peitschen Lungenwurm Doramectin Dectomax S 0,3 mg 1xi 49 +++ +++ +++ +++ +++ - +++ Febantel Rintal 5 mg 2xo 6 - +++ +++ ++ +++ ++ ++ Fenbendazol Panacur 5 mg 5-10o 5 - +++ +++ ++ +++ ++ Name Einsatz (%) Wirkzeit (h) IDT DES special N 2 2 Schaumann Endosan forte S 2 2 Interhygiene Lomasept L20 5 2 Noak DES-Endo 2 2 +++ Flubendazol Flubenol 5 mg 5-10o 14 - +++ +++ +++ +++ +++ +++ Ivermectin Ivomec S 0,3 mg 1xi 28 +++ +++ +++ +++ +++ - +++ I.Prämix 0,1 mg 7o 7 +++ +++ +++ +++ +++ - +++ Levamisol Hersteller Citarin-L 5 mg 1xi 8 - +++ ++ ++ ++ + +++ ConcuratL 7,5 mg 2xo 5 - +++ ++ ++ ++ + +++ Magengeschwüre Magengeschwüre Steckbrief Klinik • „Berufskrankheit“ intensiv gefütterter Mastschweine • Ösophagogastrische Geschwüre: drüsenlose Speiseröhrenschleimhaut größte Bedeutung • Magenfundusgeschwüre: extremer Streß, Heilung • Ursache weder genetisch noch infektiös • Disposition: fein gemahlenes, faserarmes Getreide (>20% <0,2 mm) • Hitzebehandlung des Getreides • CCM mit hohen Essigsäureanteilen • Streß: • Überbelegung der Buchten • Kämpfe um Freßplätze • Transport und Umstallung • perakut: – plötzliche Todesfälle, bester Ernährungszustand – blasse Hautfarbe – alle Altersklassen betroffen, aber v.a 20-40 kg + Sauen peri partum • chronisch-subklinisch – Anorexie, Wachstumsverzögerung, Kümmern – Blässe, Zähneknirschen, Temperatur herabgesetzt – Kot: dunkel bis teerfarben, weich • Blutarmut und Immunsuppression → häufig Folgeinfektionen (Lunge) • Morbidität: bis 50 %; Mortalität bis 5 % Magengeschwüre Magengeschwüre Klinik Sektion • Tierkörper + Organe auffallend blaß • akut: – eng begrenzt im Eingangsbereich des Magens: Geschwür – Magen gefüllt mit geronnenem Blut – Dünndarm blutdurchsetzt – Enddarminhalt teerfarben • chronisch: – Sickerblutung, eingegrabenes, vernarbtes Geschwür – Strikturen → Kümmern • bei Durchbruch: schwere Peritonitis Blasse Tiere Tod durch Verbluten in den Darm Magengeschwüre Magengeschwüre Sektion Sektion akutes Magengeschwür chronisches Magengeschwür Magengeschwüre Magengeschwüre Diagnose Differentialdiagnostik • teerfarbener, geformter Kot • blasse Haut und Schleimhäute • kein Fieber • teerfarbener Kot durch zu hohe Kupfergehalte im Futter • Eperythrozoonose: Blutarmut • Furazolidon-Vergiftung • Kupfervergiftung Magengeschwüre Magengeschwüre Therapie Prophylaxe • • • • • Streß ausschalten • Buchten gleichmäßig zusammenstellen • Rohfaser! Primärstreß abstellen Eisenpräparate Vitamin K Kalzium Enterohämorrhagisches Syndrom, EHS Steckbrief • • • • • • Darmverdrehung unter Gasbildung im Dickdarm plötzliche Todesfälle v.a Mittel- u. Endmast; Sauen starke Gärung durch hohen Hefebefall (z.B. Molke) auch Clostridium Typ A Fusarien-befallenes CCM EHS Klinik • Tod innerhalb weniger h • aufgeblähter Bauch, Bauchschmerzen • gut bis sehr gut entwickelte Tiere EHS EHS Sektion Sektion • • • • Auftreibung des Abdomens hochgradige Blässe von Haut und Organen Aufgasung des MaDa-Traktes Verlagerung der Blinddarmspitze nach vorn unter den Rippenbogen • Drehen des Darmkegels um mind. 180° um Gekrösewurzel • Stauungshyperämie; hämorrhagische Infarzierung • rötliche seröse Ansammlungen in Bauchhöhle EHS EHS Therapie Prophylaxe • nicht möglich • Futterhygiene • Untersuchung auf Hefen im Futter • Bei Clostridienbeteiligung: Impfung Fütterungsbedingte Erkrankungen Erkrankungen durch verdorbene Futtermittel Gewinnung Lagerung Zubereitung Mischung Fütterungsmanagement Mischfehler Wassergehalt Futterration DosierungsFehlgärung Fütterungstechnik fehler Schadnager Fütterungshygiene Sauberkeit Verarbeitungsfehler (Hitze, Mahlung) Verderbnis durch: Bakterien Pilze Milben Toxine Geschmacksstoffe Vergiftungen verminderte FA Wasserversorgung Nippel Fließgeschwindigkeit Wasserqualität Futterkomponenten verminderte Futtermenge Wasseraufnahme Futterverderb KochsalzKeimbelastung vergiftung Keimbelastung • Erhöhter/veränderter Keimgehalt • unspezifisch: Verdauungsstörungen, Stase, Colivermehrung Durchfälle, geringe FA • spezifisch: Salmonellen: Allg. Erkrankung, Verdauungsstörungen Listerien: Allg.Erkrankung, Durchfälle, Aborte, ZNS Clostridien: Allg. Vergiftungserscheinungen, Diarrhoe • Pilze, Pilzsporen und Hefe: Tympanien, Blähungen, Durchfall • Mycotoxine: Komplexe Krankheitserscheinungen hitzestabil! mischbar • Milben: blutige Ferkeldurchfälle schlechte FA bei Mastschweinen • Fehlgärung: Essig- und Buttersäure: Magenverätzung, FA (pH<4,2) Fäulnis • Verarbeitungsfehler: feine Vermahlung, Hitze: Magenulzera Staub: Schleimhautreizung, FA Erkrankungen durch fehlerhafte Futterrationen Erkrankungen durch fehlerhafte Fütterungstechnik • Schwer verdauliche Komponenten • Übergang • Ferkel: • Stärke • Kuhmilch (Laktose) • überhitztes Eiweiß (Sojaschrot, Milchpulver) • Mast: • Molke, Magermilch (Laktose) • rohe Kartoffelstärke • Wirkung: schlecht verdaulich • Nährboden für Darmbakterien • osmotisch wirksam - dünnflüssiger wasserreicher Kot • Darmreizung - schnellere Passage • • • • • rationiert - ad libitum fest - flüssig längere Transporte besonders schmackhaftes Futter • Überfütterung • Streptokokken und Laktobazillen • Laktat • pH 7 - pH 6 • 12h später dünnbreiiger-dünnflüssiger Kot Erkrankungen durch fehlerhafte Fütterungshygiene Erkrankungen durch fehlerhafte Fütterung der Sau • Überhöhte Keimgehalte - Toxine • ante partum • FA • Verdauungsstörungen • Durchfälle • Wasser • Nitratbelastung • Coli-Gehalt • Energie-Überversorgung + Eiweiß-, Ca-, P-Unterversorgung: → Reduzierte Menge und Qualität des Kolostrums • Vitamin A-Unterversorgung: → geringe Reserven der Ferkel • starke Unterversorgung mit Energie, B2, Mn: → kleine, lebensschwache Ferkel • post partum • Futterwechsel → Änderung der Milchzusammensetzung • zu energiereich u. eiweißarm → Milchfettgehalt ↑ → fettige Durchfälle Erkrankungen durch fehlerhafte Fütterung der Ferkel Erkrankungen durch Mykotoxine z z z z z z z z • Aflatoxine RP: >22-25 % RF: < 3 % Zucker: >10 % Fischmehl: Salmonellen oder NaCl Magermilch: ansauer → Tympanien plötzlicher Futterwechsel → Coli Überfütterung nach dem Absetzen → Coli Milchmangel, unzureichende Beifütterung → Streuaufnahme z Wasserversorgung unzureichend → Harnsaufen z zu hoher Spelzenanteil → Magenulzera • Aspergillus flavus; Erdnüsse! Baumwollsaat, Hirse, Bohnen, Brot • frei: Getreide und Soja • akut: Lebernekrose; chronisch: hepatotox.+cancerogen ASAT, ALT, AP • Körperhöhlen- und Darmblutungen, Petechien • Gewichtsverluste, Kümmern, häufig Todesfälle • immunsuppresiv • Aborte ohne Folgeschäden für Sau • Diagnose: Leberschäden + Aflatoxinbestimmung • Th.: Zusatz von Tonerde Erkrankungen durch Mykotoxine Mutterkorn • Ochratoxin • Penicilien und Aspergillen • Leber- und Nierenschäden Gewichtsverluste, Kümmern, vermehrte Trinkwasseraufnahme und Harnabsatz • Stachybotryotoxine • • • • Stachybotrys atra Blutungen: Nase, Maul hohe Ferkelsterblichkeit Aborte Ergotismus Ergotismus Danach war die Universität Giessen in den Genuß eines Hauptteils des Klostervermögens gelangt und Rechtsnachfolgerin des Antoniterklosters von Grünberg geworden. Der Orden selbst unterhielt im 14. Jahrhundert über 350 Hospitäler in ganz Europa ausschließlich für Ergotismuskranke. So lag es nahe, das Antoniterkreuz als Zeichen eines Hospitalsordens auch als Wappen einer Universität zu übernehmen, deren Medizinische Fakultät sich der gleichen Aufgabe verpflichtet wußte. Außerdem wurde das Ordenskreuz auch in die 1896 gestiftete und jetzt einhundert Jahre alte Universitätsfahne aufgenommen. Ergotismus Eine der letzten Ergotismusepidemien in Deutschland hatte noch 1879 im Grünberg-Giessener Raum gewütet. Die Medizinische Fakultät Giessen hatte sich daher besonders dieser Umweltseuche angenommen, die als Ignis sacer, Antoniusfeuer [dargestellt an der brennenden linken Hand des Kranken in Abb. 2; Vergrößerung mit Mausklick], "mal des ardents" und Kriebelkrankheit imponierte und vor allem unter der Landbevölkerung (Morbus ruralis) grassierte. So hieß es in einem Gutachten der Medizinischen Fakultät Giessen vom 19.9.1770, das den Zusammenhang zwischen dem Mutterkorn und dem Ergotismus postulierte: "So zweiffeln wir nicht, daß gedachtes Secale cornutum die Ursache erwähnter Krankheit seye." Seitens der Obrigkeit wurde daher befohlen, den Roggen vor dem Mahlen durch Sieben vom Mutterkorn zu trennen. Diese Präventionsmaßnahme wurde jedoch nicht befolgt und so sollte sich die alte Erfahrung bestätigen, daß das Erkennen der Ursache einer Krankheit allein nicht genügt, um eine Krankheit zum Erlöschen zu bringen. Mykotoxine Fusarium Toxine Fusarium Toxine • Feldpilze: – Fusarium graminearum – F. culmorum – F. avenaceum • häufigste Pilze der Nordhalbkugel • Getreide und Mais • besonders empfindlich: – Weichweizen, Triticale, Hafer – Sortenunterschiede! • stabiler: – Roggen – Wintergerste • • • • • Befall aus Boden, Strohresten, Saatgut Askosporen – Wind – Ähren von Weizen und Mais Verbreitung mit Getreidesporen v.a. bei hoher Temperatur und Luftfeuchte Fruchtfolge – nach CCM kein Weizen – nie 2 mal hintereinander Weizen – kein Triticale nach Weizen • D: einzelne aufgehellte Ähren, evtl. rosa Pilzmycel • mehr Toxine bei – intensivem Fungizideinsatz – starker N-Düngung • Anbau: infektiöses Maisstroh!!! • pfluglose Bearbeitung (v.a. nach Körnermais) Fusarium Toxine • weniger empfindlich: – längere Halmsorten – lockerere Ähren (trocknen besser) • Überragender Faktor: Witterung zur Blüte • Separierung befallener Körner im Mähdrescher möglich Energiegetreide Fusarium Toxine • 3 Toxingruppen mit Leittoxinen – Trichothecene – Fumonisine – Zearalenon Fusarium Toxine • Trichothecene – F. graminearum – T2-Toxin: Fusarium Toxine • DON – Hemmung der Eiweißsynthese = Makrolide; zytotoxisch – Schleimhautreizung u. Entzündung, v.a. Verdauungstrakt • Hautläsionen, Hi-Hand Paresen, Tremor, Speicheln, Erbrechen, Apathie – DAS (Deacetoxyscirpenol) • Panzytopenie, Schleimhauttoxisch (Bindet an DNA, stört Eiweißsynthese) – DON (Deoxynivalenol) Vomitoxin • Fumonisine – F. moniliforme – Hemmung Ceramid-Synthetase (Sphingosin-Anschoppung) • Porcines pulmonales Ödem, Herzinsuffizienz, Leberenzyme > • Rezeptoren//Erreger! • Zearalenon – F. graminearum, culmorum – Lactonring mit Östrogenwirkung • blutige Diarrhoe möglich – – – – – – – – – – – Area postrema: Brechreiz (Vomitoxin) Zytokinfreisetzung, Immunsuppression, Aborte, embryotoxisch < Uteruselongation Depression der Fruchtbarkeit im Herdenmaß Umrauscher (Uterusmilieu), Wurfgröße <, Vitalität < Spreizferkel, Schwanznekrosen Endometritis – Puerperium verzögert Selektive Schäden im Dickdarm – Dysbakterie, Clostridientoxine FA reduziert, Mastleistung reduziert, Milchleistung reduziert D: Futter 500µg/kg; Galle: 80 µg/kg; Blut 10-15 µg/kg Th: Mycofix Biomin – 15%; Bierhefe, Fischmehl (Reparation) Fusarium Toxine • ZEA – – – – – F. graminearum, culmorum; Lacton -> Östrogenwirkung präpubertäre JS am empfindlichsten geschwollene Vulva (Ö) ohne Duldungsreflex (LH) Pseudogravidität: d13 – d30 vorgetäuschtes Nidationssignal!!! Verschiebung Ö:P = Uterine Histiotrophe unangepasst = Embryotoxisch – azyklische Östrogenwirkung: pos. feed back auf LH peak bleibt aus -> Zysten – GnRH-Blockade durch Ö = verzögerte Pubertät – D: Futter 50µg/kg; Galle 10µg/kg; • Uterus: Hyperämie, Ödeme, Eosinophilie, Gewichtssteigerung – TH: Biomin Mycofix -30%; 2% Bierhefe; Fischmehl – nach Futterwechsel: Mastdarmvorfall Steckbrief • Mastschweine ab 12. LW, Sauen um Geburt • Ursachen • starker Husten im Bestand • Durchfall mit Reizung der Schleimhaut→Drängen auf Kot • starker Hefebefall bei Flüssigfütterung →Druck durch Magenaufgasung • Zearalenongehalte →Östrogenwirkung lockert auf (Sauen) • hinten tiefer stehende hochtragende Sauen • Tylosin und Erythromycingaben (Darmreizung) • z.T. spontane Reponierung • z.T. angefressen • z.T. Mastdarmstenose durch narbige Striktur • Einzeltier in 4 Wo o.k. • Bestand in 3-4 Monaten o.k. Mastdarmvorfall Mastdarmvorfall Klinik Klinik Mastdarmstenose: selbständig oder in Folge Rektumulzera bzw. rückgebildetem Mastdarmvorfall Mastdarmvorfall Mastdarmvorfall Klinik Therapie und Prophylaxe • • • • • Mastdarmstenose: selbständig oder in Folge Rektumulzera bzw. rückgebildetem Mastdarmvorfall a) Absondern der Tiere b) Reposition von Hand, Tabaksbeutelnaht c) chirurgische Amputation - Strikturgefahr d) Antibiotische Abdeckung (z.B. Tardomyocel) Primärursache bekämpfen! Erbliche Krankheiten Bruchferkel Bruchferkel Therapie und Prophylaxe • Hernia umbilicalis und inguinalis • die häufigste angeborene Mißbildung (0,5 - 1,5 %) • doppelt rezessiver Erbgang • Heritabilität 0,3 • a) Eber überprüfen • b) Saugferkel kennzeichnen • c) Bruchferkel-OP mit 7-10w Wundantibiose mit Penicillin-Puder • Gefahr durch • Inkarzerierung des Darmes im Bruchspalt • Verletzung nach Schleifen am Boden • Austreten von Darm nach dem Kastrieren Erbliche Krankheiten Atresia ani Atresia ani Klinik • Rektumverschluß • • • • angeborene Mißbildung (0,5 - 1 %) polygene Vererbung Tod der männlichen Ferkel nach 3d bis Aufnahme festen Futters 50 % der weiblichen: Recto-Vaginal-Fistel Trächtigkeiten möglich (unerwünscht) • evtl. OP: Kreuzschnitt und Vernähen des Darms • Überprüfung des Ebers Atresia ani Klinik











