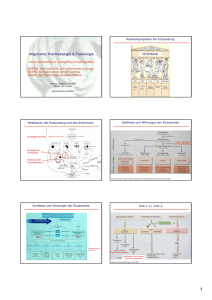
Mukosaschädigung im Gastrointestinaltrakt der Ratte : Rolle von
Werbung

84 5. Zusammenfassung Zwei Isoenzyme der Cyclooxygenase (COX-1 und COX-2) katalysieren den ersten Schritt der Biosynthese von Prostaglandinen und Thromboxan aus Arachidonsäure. COX-1 wird in den meisten Geweben konstitutiv exprimiert. Im Gegensatz dazu ist die Expression von COX-2 unter basalen Bedingungen gering. Eine schnelle Hochregulation der COX-2 Expression findet bei Entzündung statt. Herkömmliche nichtsteroidale Antiphlogistika (NSA) inhibieren beide Cyclooxygenasen und induzieren Nebenwirkungen am Gastrointestinaltrakt und der Niere. Selektive COX-2 Inhibitoren zeigen verglichen mit herkömmlichen NSA geringere gastrointestinale Nebenwirkungen bei Versuchstieren unter basalen Bedingungen und beim Menschen. Es wurde postuliert, daß NSA induzierte Nebenwirkungen auf der Inhibition der COX-1 beruhen, während die Inhibition der COX-2 die antiinflammatorischen, antipyretischen und analgetischen Effekte bewirkt. Die Synthese von Prostaglandinen in der Magenmukosa ist ein Faktor für die Resistenz der Mukosa gegen Ulzerogene und die Hemmung der Prostaglandinsynthese mit nichtselektiven Cyclooxygenase Inhibitoren führt zur Gewebeschädigung. Ziel der Arbeit war, die Effekte der selektiven COX-2 Inhibitoren (NS-398, DFU, Rofecoxib, Celecoxib), des COX-1 Inhibitors (SC-560) und des Inhibitors der COX-2 Induktion (Dexamethason) mit den Effekten des nichtselektiven Cyclooxygenase Inhibitors (Indometacin) auf die Magen-und Dünndarmmukosa in drei experimentellen Modellen für akute Schädigung zu vergleichen und die Enzyme zu ermitteln, die für die Protektion wichtig sind. Methoden: Im Ischämie-Reperfusions-Modell wurde die A. coeliaka für 30 min abgeklemmt um Ischämie des Magens zu bewirken bzw. die A. mesenterica superior wurde abgeklemmt um Ischämie des Dünndarms zu bewirken. Die Reperfusion erfolgte für 60 min. Untersucht wurde die makroskopische Schädigung der Magenmukosa und die Zunahme der Permeabilität des Dünndarms für „Evans blue“. Die Synthese von gastralem PGE2 und 6-Keto-PGF1α und des Thrombozyten TXB2 im Blut wurde mittels Radioimmunassay quantifiziert sowie die Spiegel von COX-1 und COX-2 mRNA in der Magenmukosa wurden durch Northern Blot analysiert. Die nichtselektive Inhibition der NO-Synthetase durch L-NAME und die selektive Inhibition der induzierbaren NO-Synthetase durch 1400W wurde durchgeführt, um die Rolle von NO für die Magenprotektion zu untersuchen. In einem zweiten Modell diente die Instillation von 0,3 N HCl in den Rattenmagen und Inhibition der NO-Synthetase durch L-NAME zur Schädigung der Mukosa und Effekte der selektiven Cyclooxygenase Inhibition wurden getestet. In einem dritten Modell wurde die Denervierung von Capsaicin-sensitiven afferenten Neuronen durch hohen Dosen Capsaicin angewendet, um Neuropeptide zu dezimieren und Effekte der selektiven Cyclooxygenase Inhibition wurden ermittelt. Die Experimente führten zu folgenden Ergebnissen: 1. Ischämie-Reperfusion des Magens allein induzierte nur geringe Schäden der Mukosa. Alle hochselektiven COX-2 Inhibitoren, der Inhibitor der COX-2 Induktion und der selektive COX-1 Inhibitor induzierten schwere Schäden der Magenmukosa nach Ischämie-Reperfusion, im gleichen Ausmaß wie der nichtselektive Cyclooxygenase Inhibitor Indometacin. 2. Obwohl eine Zunahme der Synthese von 6-Keto-PGF1α und PGE2 nach IschämieReperfusion in der Magenmukosa nicht dargestellt werden konnte, wurde eine Induktion der COX-2 mRNA nach 1 h Reperfusion mittels Northern Blot gezeigt. Ischämie-Reperfusion hatte keinen Effekt auf die Spiegel der COX-1 mRNA. 3. Nur Indometacin hemmte die Synthese von 6-Keto-PGF1α und PGE2 in der Magenmukosa oder TXB2 in Serum, während kein selektiver COX-2 Inhibitor meßbare Hemmung zeigte. 85 4. Der nichtselektive Inhibitor der NO-Synthetase L-NAME verstärkte dosisabhängig Schäden der Magenmukosa durch Ischämie-Reperfusion, jedoch nicht das Enantiomer D-NAME. Verstärkung der Schäden durch L-NAME konnte verhindert werden durch L-Arginin, aber nicht durch D-Arginin oder 16,16-DMPGE2. Die Schädigung der Magenmukosa durch Indometacin oder DFU in Kombination mit L-NAME war additiv. 5. Die selektive Hemmung der induzierbaren NO-Synthetase durch 1400W bewirkte keine Verstärkung des gastralen Ischämie-Reperfusionsschadens. Das NSA Amtolmetinguacyl (AMG) induzierte nach Ischämie-Reperfusion keine Magenschäden bei der Ratte, trotz antiinflammatorischer Aktivität und signifikanter Hemmung des 6-Keto-PGF1α im Magen und des Thrombozyten TXB2, während die kombinierte Gabe von AMG und 1400W schwere Schäden der Mukosa bewirkte. 6. Ischämie-Reperfusion allein induzierte keine meßbare Zunahme der Permeabilität des Dünndarms. Während Indometacin keine Zunahme der Permeabilität des Dünndarms bei Ratten mit Schein-Operation induzierte, verstärkten Indometacin, Dexamethason und selektive COX-2 Inhibitoren die intestinale Permeabilität bei Ratten mit IschämieReperfusion. SC-560 erhöhte nur gering die intestinale Permeabilität, aber steigerte die durch Rofecoxib induzierte Permeabilität. 7. Während die Instillation von 0,3 N HCl in den Magen und alleinige Behandlung mit dem nichtselektiven Inhibitor der NO-Synthetase L-NAME, den selektiven COX-2 Inhibitoren oder Dexamethason geringe Magenschäden induzierte, verstärkte die Behandlung mit selektiven COX-2 Inhibitoren oder Dexamethason die Mukosaschäden bei kombinierter Behandlung mit L-NAME. Selektive COX-1 Inhibition und Instillation von 0,3 N HCl induzierte dosisabhängig Magenschäden, welche zusätzlich durch Behandlung mit L-NAME gesteigert wurden. 8. Behandlung mit DFU, NS-398, Dexamethason oder SC-560 induzierte schwere Mukosaschäden, wenn Capsaicin-sensitive afferente Neurone mit hohen Dosen Capsaicin denerviert wurden. 9. Die Zunahme der Magenmukosaschäden in allen Modellen und die Zunahme der intestinalen Permeabilität nach Ischämie-Reperfusion durch selektive COX-2 Inhibitoren, den selektiven COX-1 Inhibitor und Dexamethason konnte durch Verabreichung von sehr niedrigen Dosen des Prostaglandin Analogons 16,16-DMPGE2 verhindert werden. Die Behandlung mit Indometacin oder SC-560 erforderte höhere Dosen an 16,16-DMPGE2 als die Behandlung mit selektiven COX-2 Inhibitoren für die Verhinderung von Magenschäden oder der intestinalen Permeabilitätssteigerung. Diskussion: Während neue Untersuchungen ergaben, daß unter basalen Bedingungen nur die Inhibition beider Cyclooxygenasen Läsionen am Magen induziert, zeigt die vorliegende Arbeit, daß bei Ischämie-Reperfusion Schäden am Magen oder Dünndarm entstehen, wenn nur das COX-1 oder COX-2 Enzym inhibiert wird oder die Induktion von COX-2 gehemmt wird. Ischämie-Reperfusion bewirkt schnell die Expression von COX-2 mRNA und COX-2 vermittelte Prostaglandine wirken zusammen mit COX-1 vermittelten Prostaglandinen bei der Minimierung von Schäden. Unter Ischämie-Reperfusion ist COX-2 besonders wichtig für die Protektion, denn COX-2 Inhibitoren schädigten die Mukosa von Magen und Dünndarm in niedrigeren Dosen als der COX-1 Inhibitor. Dies liegt offenbar an einer Hemmung der Leukozytenadhärenz an das Gefäßendothel nur durch COX-2 aber nicht durch COX-1 synthetisierte Prostaglandine. Die Bildung von reaktiven Sauerstoff-Metaboliten und Peroxidation von Membranlipiden durch adhärente Leukozyten führt zu erhöhter Permeabilität der gastrointestinalen Mukosa und ist ein wichtiger Faktor bei der Schädigung 86 durch Ischämie-Reperfusion. Inhibition der COX-1 bei Ischämie-Reperfusion induziert ebenfalls Schäden an Magen und Dünndarm, aber in geringerem Ausmaß als COX-2 Inhibition, möglicherweise durch Verzögerung der Normalisierung der Mukosadurchblutung in der Reperfusionsphase. Durch die konstitutive NO-Synthetase aus L-Arginin gebildetes NO ist ein wichtiger Faktor für die Protektion bei Ischämie-Reperfusion, während die induzierbare NO-Synthetase diesbezüglich nur eine geringe Funktion erfüllt. NO wirkt protektiv aufgrund von Vasodilatation, Inhibition der Leuozytenadhärenz und Minimierung oxidativer Schäden. Im Schädigungsmodell durch Säure schädigten selektive COX-2 Inhibitoren und Dexamethason die Magenmukosa nur, wenn gleichzeitig die NO Synthese inhibiert wurde. Im Gegensatz dazu bewirkte der selektive COX-1 Inhibitor Schäden ohne gleichzeitige Inhibition der NO Synthese. Unter diesen Bedingungen ist die Inhibition der Durchblutung der Magenmukosa durch Inhibition der COX-1 von größerer Bedeutung, als die Zunahme der Leukozytenadhärenz durch Inhibition der COX-2. Bei Ratten mit Dezimierung von Neuropeptiden aus Capsaicin-sensitiven afferenten Neuronen induziert die selektive COX-1 oder COX-2 Inhibition ebenso wie die Inhibition der COX-2 Induktion schwere Schäden der Magenmukosa. NO dient in afferenten Neuronen als „second messenger“, daher wirkt die funktionelle Denervierung wie die Inhibition der NO-Synthetase. Diese Arbeit zeigt, daß, obwohl selektive COX-2 Inhibitoren unter normalen Bedingungen bei Versuchstieren und beim Menschen geringere Gastrotoxizität als herkömmliche NSA aufweisen, unter speziellen Bedingungen wie Ischämie-Reperfusion, erhöhter Azidität im Magen und gestörter NO-Synthese diese Inhibitoren Schäden am Magen und Dünndarm im gleichen Maße induzieren wie NSA. Unter diesen Bedingungen wird die COX-2 schnell induziert und COX-2 synthetisierte Prostaglandine wirken bei der Minimierung von Schäden des Gastrointestinaltrakts zusammen mit COX-1 synthetisierten Prostaglandinen. COX-2 Inhibitoren verzögern die Heilung von Magenulzera bei Versuchstieren und es wurden physiologische Funktionen der COX-2 in einigen Organen, insbesondere der Niere identifiziert. Daher sind die Vorteile von selektiven COX-2 Inhibitoren begrenzt und bei Vorliegen von gastrointestinalen Schäden und Heilungsprozessen können sie Schäden wie herkömmliche NSA hervorrufen.