Aktuell - BIOspektrum
Werbung
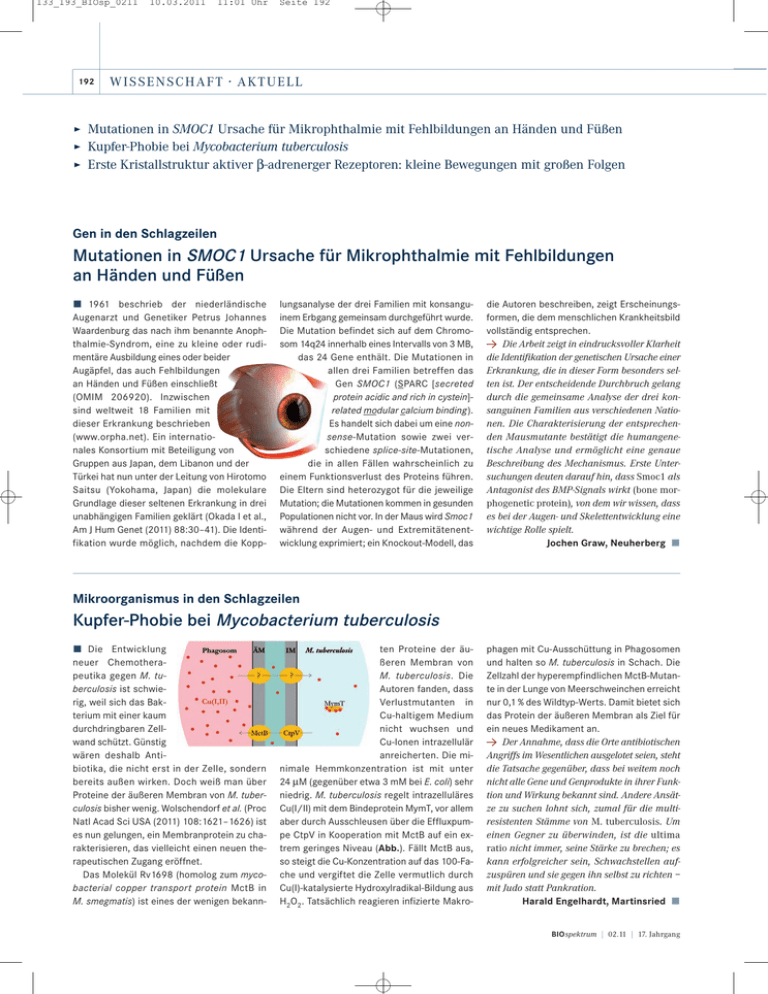
133_193_BIOsp_0211 192 10.03.2011 11:01 Uhr Seite 192 W I S S E N SCH AFT · AKTU E LL ÿ Mutationen in SMOC1 Ursache für Mikrophthalmie mit Fehlbildungen an Händen und Füßen ÿ Kupfer-Phobie bei Mycobacterium tuberculosis ÿ Erste Kristallstruktur aktiver β-adrenerger Rezeptoren: kleine Bewegungen mit großen Folgen Gen in den Schlagzeilen Mutationen in SMOC1 Ursache für Mikrophthalmie mit Fehlbildungen an Händen und Füßen ó 1961 beschrieb der niederländische Augenarzt und Genetiker Petrus Johannes Waardenburg das nach ihm benannte Anophthalmie-Syndrom, eine zu kleine oder rudimentäre Ausbildung eines oder beider Augäpfel, das auch Fehlbildungen an Händen und Füßen einschließt (OMIM 206920). Inzwischen sind weltweit 18 Familien mit dieser Erkrankung beschrieben (www.orpha.net). Ein internationales Konsortium mit Beteiligung von Gruppen aus Japan, dem Libanon und der Türkei hat nun unter der Leitung von Hirotomo Saitsu (Yokohama, Japan) die molekulare Grundlage dieser seltenen Erkrankung in drei unabhängigen Familien geklärt (Okada I et al., Am J Hum Genet (2011) 88:30–41). Die Identifikation wurde möglich, nachdem die Kopp- lungsanalyse der drei Familien mit konsanguinem Erbgang gemeinsam durchgeführt wurde. Die Mutation befindet sich auf dem Chromosom 14q24 innerhalb eines Intervalls von 3 MB, das 24 Gene enthält. Die Mutationen in allen drei Familien betreffen das Gen SMOC1 (SPARC [secreted protein acidic and rich in cystein]related modular calcium binding ). Es handelt sich dabei um eine nonsense-Mutation sowie zwei verschiedene splice-site-Mutationen, die in allen Fällen wahrscheinlich zu einem Funktionsverlust des Proteins führen. Die Eltern sind heterozygot für die jeweilige Mutation; die Mutationen kommen in gesunden Populationen nicht vor. In der Maus wird Smoc1 während der Augen- und Extremitätenentwicklung exprimiert; ein Knockout-Modell, das die Autoren beschreiben, zeigt Erscheinungsformen, die dem menschlichen Krankheitsbild vollständig entsprechen. Y Die Arbeit zeigt in eindrucksvoller Klarheit die Identifikation der genetischen Ursache einer Erkrankung, die in dieser Form besonders selten ist. Der entscheidende Durchbruch gelang durch die gemeinsame Analyse der drei konsanguinen Familien aus verschiedenen Nationen. Die Charakterisierung der entsprechenden Mausmutante bestätigt die humangenetische Analyse und ermöglicht eine genaue Beschreibung des Mechanismus. Erste Untersuchungen deuten darauf hin, dass Smoc1 als Antagonist des BMP-Signals wirkt (bone morphogenetic protein), von dem wir wissen, dass es bei der Augen- und Skelettentwicklung eine wichtige Rolle spielt. Jochen Graw, Neuherberg ó Mikroorganismus in den Schlagzeilen Kupfer-Phobie bei Mycobacterium tuberculosis ó Die Entwicklung neuer Chemotherapeutika gegen M. tuberculosis ist schwierig, weil sich das Bakterium mit einer kaum durchdringbaren Zellwand schützt. Günstig wären deshalb Antibiotika, die nicht erst in der Zelle, sondern bereits außen wirken. Doch weiß man über Proteine der äußeren Membran von M. tuberculosis bisher wenig. Wolschendorf et al. (Proc Natl Acad Sci USA (2011) 108:1621–1626) ist es nun gelungen, ein Membranprotein zu charakterisieren, das vielleicht einen neuen therapeutischen Zugang eröffnet. Das Molekül Rv1698 (homolog zum mycobacterial copper transport protein MctB in M. smegmatis) ist eines der wenigen bekann- ten Proteine der äußeren Membran von M. tuberculosis. Die Autoren fanden, dass Verlustmutanten in Cu-haltigem Medium nicht wuchsen und Cu-Ionen intrazellulär anreicherten. Die minimale Hemmkonzentration ist mit unter 24 µM (gegenüber etwa 3 mM bei E. coli) sehr niedrig. M. tuberculosis regelt intrazelluläres Cu(I/II) mit dem Bindeprotein MymT, vor allem aber durch Ausschleusen über die Effluxpumpe CtpV in Kooperation mit MctB auf ein extrem geringes Niveau (Abb.). Fällt MctB aus, so steigt die Cu-Konzentration auf das 100-Fache und vergiftet die Zelle vermutlich durch Cu(I)-katalysierte Hydroxylradikal-Bildung aus H2O2. Tatsächlich reagieren infizierte Makro- phagen mit Cu-Ausschüttung in Phagosomen und halten so M. tuberculosis in Schach. Die Zellzahl der hyperempfindlichen MctB-Mutante in der Lunge von Meerschweinchen erreicht nur 0,1 % des Wildtyp-Werts. Damit bietet sich das Protein der äußeren Membran als Ziel für ein neues Medikament an. Y Der Annahme, dass die Orte antibiotischen Angriffs im Wesentlichen ausgelotet seien, steht die Tatsache gegenüber, dass bei weitem noch nicht alle Gene und Genprodukte in ihrer Funktion und Wirkung bekannt sind. Andere Ansätze zu suchen lohnt sich, zumal für die multiresistenten Stämme von M. tuberculosis. Um einen Gegner zu überwinden, ist die ultima ratio nicht immer, seine Stärke zu brechen; es kann erfolgreicher sein, Schwachstellen aufzuspüren und sie gegen ihn selbst zu richten – mit Judo statt Pankration. Harald Engelhardt, Martinsried ó BIOspektrum | 02.11 | 17. Jahrgang 133_193_BIOsp_0211 10.03.2011 11:01 Uhr Seite 193 Arzneimittel in den Schlagzeilen Erste Kristallstruktur aktiver β-adrenerger Rezeptoren: kleine Bewegungen mit großen Folgen (Bild: Rasmussen et al., Nature (2011) 469: 175–180) ó G-Protein-gekoppelte Rezeptoren (GPCR) zählen zu den wichtigsten Zielmolekülen von Arzneistoffen. Seit der Klonierung des β2-adrenergen Rezeptors 1986 wurden bis heute im humanen Genom über 800 GPCRs entdeckt. Bereits kurz nach der Klonierung begannen mehrere Arbeitsgruppen mit der in vitro-Produktion und Reinigung von Rezeptorproteinen, um ihre dreidimensionale Struktur aufzuklären. Erst 2007 konnten erstmalig β-adrenerge und Adenosin-Rezeptorstrukturen aufgedeckt werden. Die bisher bekannten Strukturen hatten jedoch einen gravierenden Nachteil: Sie zeigten die Rezeptoren nur im inaktiven Zustand, da die Proteine zur Kristallisierung durch inverse Agonisten oder Antagonisten stabilisiert werden mussten. Nun ist es den Arbeitsgruppen von Kobilka sowie Tate und Schertler gelungen, aktive β-adrenerge Rezeptoren zu kristallisieren (Rasmussen SG et al., Nature (2011) 469:175–180; Rosenbaum DM et al., l. c. 236–240; Warne T et al., l. c. 241–244). Schlüssel zum Erfolg waren zum einen neue Agonisten, die sich mit sehr hoher Affinität bzw. irreversibel an die Rezeptoren binden, sowie Antikörper, die aus Lamas gewonnen wurden. Lamas und einige andere BIOspektrum | 02.11 | 17. Jahrgang Kamelarten synthetisieren Antikörper, die keine leichten Ketten enthalten, sodass es gelingen konnte, minimale Antigen-bindende Fragmente zu erhalten, die nur ein Viertel der Größe eines Fab-Fragments ausmachen. Diese Nanokörper (nanobody) zeigten G-Protein-ähnliche Eigenschaften, sodass gereinigtes β2-Rezeptorprotein durch einen hochaffinen Agonisten und einen Nanokörper ausreichend stabilisiert und im aktiven Zustand eingefangen werden konnte. Die Veränderungen des Rezeptorproteins vom inaktiven in den aktiven Zustand waren erstaunlicherweise sehr gering (Abb.). In der Bindungstasche der Agonisten wurden nur kleine Bewegungen festgestellt, die sich aber wie über einen Hebelmechanismus zu deutlichen größeren Ausschlägen (bis zu 11,4 Å) der zytoplasmatischen Regionen der Transmembrandomänen TM3, TM5, TM6 und TM7 entwickelten. Y Wird es nun gelingen, gezielt Liganden zu entwickeln, die diese Rezeptoren spezifisch aktivieren oder inaktivieren? Die vorgestellten Arbeiten sind sicher bedeutende Meilensteine auf diesem Weg. Lutz Hein, Freiburg ó