Onkologische Welt 2/2011 Kapitel: Serie urologische Onkologie
Werbung

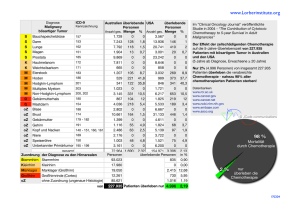
Serie urologische Onkologie 94 Keimzelltumore des Hodens Risikofaktoren und Langzeittoxizität Die Inzidenz von Keimzelltumoren des Hodens nimmt seit den vergangenen 50 Jahren kontinuierlich zu. In Deutschland sind jährlich etwa 4700 Männer betroffen. Bei mehr als 95% der Hodentumore handelt es sich um Malignome. Heute können rund 80% der Männer dauerhaft geheilt werden. Daher ist es wichtig, prognostisch wichtige Faktoren zu identifizieren, um die Inzidenz und die tumorassoziierte Mortalität senken zu können. Obwohl maligne Hodentumoren nur rund 2% der Krebserkrankungen der Männer ausmachen, handelt es sich um den häufigsten soliden Tumor bei Männern zwischen dem 25. und 45. Lebensjahr. Über einem Alter von 50 Jahren treten weniger als 20% dieser Tumore auf. Über die Gründe für die seit Jahrzehnten steigende Inzidenz gibt es nur Spekulationen, die vor allem um negative Umweltfaktoren kreisen. Folgende, als gesichert geltende Risikofaktoren begünstigen die Entstehung eines malignen Keimzelltumors: Kryptorchismus, positive Familienanamnese, intratubuläre Keimzellneoplasie in der Biopsie des Gegenhodens, HIV-Infektion, Down- oder Klinefelter-Syndrom. Ungefähr 10% der Hodentumoren sind mit einem Kryptorchismus assoziiert. Eine Orchidopexie im 2. Lebensjahr gewährleistet eine normale Hodenentwicklung und senkt das Risiko einer malignen Transformation (10). Eine Fall-Kontroll-Studie zeigte für Männer >185cm eine erhöhte Hazard Ratio (HR) von 2,11 (95% KI 1,25–3,55) für die Entwicklung eines Hodentumors im Vergleich zu Männer mit einer Körpergröße von 175–179 cm (3). Eine aktuelle populationsbasierte Studie mit 27 948 Teilnehmern (4) weist darauf als ungünstigen prognostischen Faktor für das Hodenkrebs-spezifische Überleben hin. Dort war die Mortalität von Seminom- bzw. Nicht-Seminom-Patienten im Alter über 40 Jahre bei Diagnosestellung im Vergleich zu jüngeren Patienten doppelt so hoch. Dies galt auch bei Berücksichtigung der Erstbehandlung und dem Ausmaß der Erkrankung. Bei Nicht-Seminom-Patienten führen nicht-weiße Ethnizität und ein niedrigerer sozioökonomischer Status ebenfalls zu einem signifikanten Anstieg der tumorsspezifischen Mortalität. In der Studie wurde die Hazard-Ratio (HR) für die tumorspezifische 10-Jahres-Mortalität anhand derjenigen Patienten berechnet, die zwischen 1978 und 2006 in das SEER (Surveillance, Epidemiology and End Results Program) eingegangen waren (n = 27 948). Als unabhängige Prädiktoren wurden dabei das Alter bei Diagnosestellung, sozioökonomischer Status, Familienstand, Ausmaß der Erkrankung, Radiotherapie und retroperitoneale Lymphknotendissektion identifiziert. Im Vergleich zu jüngeren Patienten, war ein Diagnosealter über 40 Jahre mit einer signifikant erhöhten Mortalität assoziiert (Seminom: HR 2,00; p<0,001; Nicht-Seminom: HR 2,09; p<0,001). Das Risiko war in der metastasierten Situation deutlich höher (HR 8,62; p<0,001 bzw. HR 6,35; p<0,001). Nicht verheiratete Männer wiesen im Vergleich zu Verheirateten eine zwei- bis dreifach höhere Mortalität auf (HR 2,97; p<0,001 bzw. HR 1,54; p<0,001). Bei Nicht-Seminom-Patienten führten ein geringerer sozioökonomischer Status (p<0,001) und nicht-weiße Ethnizität (HR: 2,11; p<0,001) zu einer erhöhten Mortalität. Patienten, deren Tumor nach 1987 diagnostiziert wurde, hatten eine signifikant geringere Mortalität (HR: 0,58; p = 0,001 bzw. HR: 0,74; p = 0,001). Eine nicht durchgeführte retroperitoneale Lymphknotendissektion war mit einem siebenfach erhöhten Mortalitätsrisiko assoziiert (p<0,001). Inzwischen mehren sich auch die Hinweise, dass Marijuana-Konsum mit einem häufigeren Auftreten von Hodentumoren assoziiert ist (2, 11). Eine US-Arbeitsgruppe testete 187 Männer, bei denen zwischen 1990 und 1996 ein Hodentumor diagnostiziert worden war, auf den Konsum von Marijuana. Im Vergleich zu 148 gesunden Kontrollen konsumierten die Tumorpatienten häufiger und öfter Marijuana als die Kontrollen (OR 2,2). Insbesondere Patienten mit Nicht-Seminomen wurden signifkant öfter als häufige (täglich oder öfter: OR 3,1) und langjährige Konsumenten (≥10 Jahre: OR 2,4) identifiziert (11). Patienten mit Nicht-Semino- men und gemischten Histologien konsumierten in einer zweiten Studie ebenfalls häufiger Marijuana (OR 2,3). Auch ein Alter <18 Jahre bei Beginn der Drogeneinnahme war mit einem erhöhten Risiko von Hodentumoren assoziiert (OR 2,2). Sekundärtumoren nach Chemo-/Radiotherapie Bereits ein bis zwei Jahre nach Chemotherapie kann eine Leukämie, i.d.R. eine akute myeloische Leukämie auftreten. Die kumulative Leukämie-Inzidenz nach 5 Jahren beträgt aber weniger als 0,5%. Solide Tumoren treten meist erst mit einer Latenz von mehr als 10 Jahren nach Abschluss der Bestrahlung auf. Hier handelt es sich um Karzinome von Magen, Harnblase, Kolon, Rektum und Pankreas. Die Auswertung der Daten von 2703 Überlebenden nach adjuvanter Bestrahlung bei Seminomen im Stadium I ergab nach einer medianen Nachbeobachtungszeit von 18 Jahren insgesamt 385 Zweitmalignome (354/2703 Patienten, 13%). Im Vergleich zu den jeweiligen Länder-, Alters- und Geschlechts-spezifischen Tumorraten in der Normalbevölkerung zeigte sich eine insgesamt erhöhte Rate an Zweitmalignomen (SIR 1,31), vor allem für Tumoren des Magens (SIR 1,63), des Pankreas (SIR 2,35) und der Blase (SIR 2,14) (7). Aufgrund der hier bestätigten erhöhten Inzidenz von Zweitmalignomen nach infradiaphragmaler Radiatio wird diese Intervention beim Seminom im Stadium I zunehmend verlassen zugunsten einer risikoadaptierten Surveillance-Strategie oder einer adjuvanten Chemotherapie (1). Auch eine aktuelle große schwedische Studie fand bei 5533 Überlebenden von Keimzelltumoren (Seminome und Nicht-Seminome) über alle Histologien und Stadien ein erhöhtes Risiko für Zweitmalignome von 6,7% (6). Auffällig ist auch das Risiko für Blasenkarzinome bei Nichtseminomen von 8%. Weitere Studien sollen auch die Rolle von Ifosfamid-haltigen Regimen prüfen (1). Epidemiologische und klinische Studien weisen darauf hin, dass die erfolgreiche Therapie von Hodentumoren einige Langzeitfolgen hervorrufen kann. Die Chemotherapie mit Cisplatin ist danach im Stadium 1 eines Seminoms so wirksam wie eine Strahlentherapie und weniger toxisch, sodass die Patienten schneller wieder in den Beruf zurückkehren können. Trotz Onkologische Welt 2/2011 © Schattauer 2011 Downloaded from www.onkologische-welt.de on 2017-06-03 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. Serie urologische Onkologie 95 solcher Fortschritte muss man im Auge behalten, dass bei den Patienten nach Strahlen- und Chemotherapie etwas häufiger ein zweiter Tumor auftritt als allgemein zu erwarten ist. Das relative Risiko einer Leukämie ist nach Therapie mit Etoposid um 2% erhöht, bei hohen kumulativen Dosen steigt es auf 4%. Bei einem auf Cisplatin basierenden Therapieregime scheint zumindest das Risiko eines Zweittumors im verbliebenen Hoden reduziert zu sein. Allerdings begünstigt nicht nur Cisplatin chronische endotheliale Entzündungsprozesse, was einer vorzeitigen Koronararteriosklerose Vorschub leisten kann. Eine norwegische Studie verglich das Risiko kardiovaskulärer Erkrankungen von 990 Keimzelltumorpatienten (nur OP: n = 206; Radiatio: n = 386; Chemotherapie: n = 364; Radio plus Chemotherapie: n = 34) mit demjenigen der altersgematchen Normalbevölkerung. Der mediane Follow-Up betrug 19 Jahre. Dabei ergab sich für beide Chemotherapie-Subgruppen einer Gebrauch von Antihypertensiva und die Diagnose eines Diabetes mellitus (Chemotherapie: OR 2,3; Radio plus Chemotherapie: OR 3,9). Arteriosklerotische Veränderungen wurden in allen Gruppen mit Radiatio bzw. Chemotherapie gehäuft festgestellt (Radiatio: OR 2,3; Chemotherapie: OR 2,6; Radio plus Chemotherapie: OR 4,8), die Inzidenz betrug insgesamt 8%. Patienten nach PEB-haltiger Chemotherapie zeigten ein 5,7-fach erhöhtes Risiko kardiovaskulärer Erkrankungen, das Myokardinfarkt-Risiko war um das 3,1-fache erhöht (5). Insgesamt muss man daher heute davon ausgehen, dass das kardiovaskuläre Risiko bei Patienten mit Keimzelltumoren nach einer Radiatio oder einer Chemotherapie, vor allem aber bei einer kombinierten Radiochemotherapie, signifikant erhöht ist. Internistische Verlaufskontrollen müssen bei diesen Patienten lebenslang erfolgen (1). Spättoxizität Da Patienten mit Hodenkrebs eine sehr günstige Langzeitprognose besitzen, ist die Spättoxizität der Chemotherapie besonders zu beachten. Die wichtigsten langfristigen Nebenwirkungen sind gonadale Dysfunktion mit Infertilität, Ototoxizität, Störungen der Lungen- und Nierenfunktion mit Abfall der Kreatinin-Clearance um rund 15% sowie Sekundärtumoren nach Chemo- oder Radiotherapie. Sexualfunktion und Fertilität Neuropsychiatrische Störungen Zur Sexualfunktion liegen zahlreiche Untersuchungen vor, die Ergebnisse sind aber widersprüchlich. Einer großen norwegischen Studie zufolge haben Männer nach überstandenem Hodenkrebs etwas häufiger Erektions- und Ejakulationsprobleme. Dies könnte teilweise durch den Hypogonadismus erklärt werden. Wahrscheinlicher ist jedoch eine Schädigung parasympathischer Nervenfasern nach retroperitonealer Lymphknotendissektion. Ein wichtiger Faktor sind auch depressive und Angstsymptome, die bei diesen Patienten gehäuft gefunden werden (8). Ein anderes Problem ist die Fertilität. Rund die Hälfte der Patienten mit Hodenkrebs weisen schon vor Beginn der Chemotherapie quantitative und qualitative Störungen der Spermatogenese auf, von welcher sie sich nur teilweise wieder erholen. Nach retroperitonealer Strahlentherapie kann durch Streustrahlung trotz Abschirmung des kontralateralen Hodens die Spermatogenese meist nur passager beeinträchtigt werden. Wichtig ist, die Patienten vor Beginn der Therapie auf die Möglichkeit einer Kryopräservation hinzuweisen (8). Unmittelbar nach einer Cisplatin-haltigen Therapie sind nahezu alle Patienten infertil (9). In diesen Fällen sowie anderen Standardtherapien erholt sich die Spermatogenese aber in bis zu 80% wieder. Entsprechend hoch ist die Zahl der Männer, die nach erfolgreicher Behandlung Vater werden. Dennoch sollte auch an einen therapieinduzierten Hypogonadismus gedacht werden. Das Ausmaß behandlungsassoziierter psychiatrischer und kognitiver Störungen wird unterschätzt. So treten nicht nur nach erfolgreicher Therapie gehäuft Angststörungen und depressive Symptome auf. Eine aktuelle Studie fand bei 46% von 69 Patienten mit einem neu diagnostizierten nicht-seminomatösen Keimzelltumor (51% Stadium I, 33% Stadium II, 15% Stadium III) nach Orchiektomie, aber noch vor einer Chemotherapie, deutliche Beeinträchtigungen der Konzentrations- und Lernfähigkeit, der Exekutivfunktionen sowie der sprachlichen und motorischen Fähigkeiten (p<0,0001 im Vergleich zur Normalbevölkerung) (12). Daher ist eine engmaschige Kontrolle der kognitiven Funktionen während und nach einer Chemotherapie zu empfehlen (1). Oto- und Neurotxozität Eine andere Langzeitfolge ist die Cisplatin-assoziierte periphere sensorische Neuropathie bei dem Regime Cisplatin/Vinblastin/Bleomycin (PVB), unter der 10–30% der Patienten leiden. Mit dem Wechsel auf das Standardregime Cisplatin/Etoposid/Bleomycin (PEB) konnte die Toxizität deutlich gesenkt werden. Hörstörungen wie Hochfrequenzverlust oder Tinnitus treten nach einer Chemotherapie (PEB) in 15–25% der Fälle auf, da Cisplatin kumulativ toxisch auf die Haarzellen im Innenohr einwirkt. Dr. Alexander Kretzschmar, München Literatur 1. Bokemayer C et al. Tumore des Urogenitaltraktes. Onko-Update 2011 vom 28. bis 29. Januar 2011, Berlin. 2. Daling JR et al. Association of marijuana use and the incidence of testicular germ cell tumors. Cancer 2009; 115(6): 1215–1223. 3. Dieckmann KP et al. Is risk of testicular cancer related to body size? Eur Urol 2002; 42(6): 564–569. 4. Fossa SD et al. Adverse prognostic factors for testicular cancer–specific survival: A population-based study of 27 948 patients. JCO 2011; 29: 963–970. 5. Haugnes HS et al. Cardiovascular risk factors and morbidity in long-term survivors of testicular cancer: a 20-year follow-up study. J Clin Oncol 2010; 28(30): 4649–4657. 6. Hemminki K et al. Second cancers after testicular cancer diagnosed after 1980 in Sweden. Ann Oncol 2010; 21(7): 1546-1551. 7. Horwich A et al. Risk of second cancers among a cohort of 2703 long-term survivors of testicular semonoma teated with radiotherapy. J Clin Oncol 2010; 28: 15s (Abstract 4538). 8. Oldenburg J et al. Spättoxizität nach Hodentumortherapie unter besonderer Berücksichtigung sexueller Störungen. Urologe A 2009; 48: 372–376. 9. Pottek TS et al. Nachsorge und Spättoxizitäten bei Hodentumoren. Dtsch Ärzteblatt 2005; 102: 3342–3348. 10. Schefer H et al. Hodentumore. Schweiz Med Forum 2003; 3: 950–959. 11. Trabert B et al. Marijuana use and testicular germ cell tumors. Cancer 2011; 117(4): 848–853. 12. Wefel JS et al. Cognitive impairment in men with testicular cancer prior to adjuvant therapy. Cancer 2011; 117(1): 190–196. © Schattauer 2011 Onkologische Welt 2/2011 Downloaded from www.onkologische-welt.de on 2017-06-03 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. UroOnkologie 96 Metastasiertes hormonrefraktäres Prostatakarzinom Neue Therapieoption zur Zweilinientherapie nach DocetaxelVersagen Mit Cabazitaxel (Jevtana®) steht ein Taxan der neuesten Generation demnächst zur europaweiten Zulassung zur Zweitlinientherapie des metastasierten hormonrefraktären Prostatakarzinoms (mHRPC) in Kombination mit Prednison an. Die Erwartungen im Hinblick auf eine Überlebensverbesserung sind hoch, denn die Alternativen nach Docetaxel-Versagen sind sehr begrenzt. Derzeit ist Docetaxel (Taxotere®) zur First-lineTherapie des mHRPC zugelassen. Allerdings dauert es in vielen Fällen sehr lang, bis man sich überhaupt zur Second-line-Therapie entschließt, so Priv.-Doz Peter J. Goebell, Erlangen. Die meisten Männer wurden mit Mitoxantron/Prednison weiterbehandelt. Zwar ließen sich damit Schmerzkontrolle und bessere Lebensqualität umsetzen, jedoch ohne Überlebensverlängerung. Cabazitaxel wurde in den USA im FastTrack-Verfahren zugelassen. Basis dafür waren Daten der TROPIC-Studie. 755 Männer mit mHRPC wurden nach Docetaxel-Versagen alternativ mit Cabazitaxel /Prednison bzw. Mitoxantron/Prednison behandelt. Dabei reduzierte Cabazitaxel das relative Sterberisiko nach einer medianen Nachbeobachtungszeit von 12,8 Monaten statistisch signifikant um 30% (HR = 0,70; p<0,0001) bei einer medianen Gesamt- überlebenszeit von 15,1 Monaten unter Cabazitaxel und 12,7 Monaten im Kontrollarm. Der mediane Überlebensvorteil bestätigte sich in allen Subgruppen. Cabazitaxel ist ein neuartiges Taxan und stabilisiert wie Docetaxel die Mikrotubuli in der Zelle. Es passiert die Blut-Hirn-Schranke. Die häufigsten (>5%) unerwünschten Wirkungen waren Neutropenie, Leukopenie, Anämie, febrile Neutropenie, Diarrhö, Müdigkeit und Asthenie. Als Prophylaxe gegen Übelkeit und Erbrechen empfahl Dr. Götz Geiges, Berlin, etwa 30 Minuten vor der Gabe von Cabazitaxel eine Prämedikation (i.v.) aus einem Antihistaminikum, beispielsweise Dexchlorpheniramin 5 mg, einem Kortikosteroid (Dexamethason 8 mg), einem H2-Antagonist (Ranitidin 50 mg) und einem Antiemetikum. Dr. med. Nana Mosler, Leipzig Quelle: Fach-Pressekonferenz „Die Krebstherapie verändern: Jevtana® – Neuzulassung beim metastasierten hormonrefraktären/kastrationsresistenten Prostatakarzinom“ am 22. Februar 2011, Berlin. Veranstalter: Sanofi-Aventis Deutschland, Berlin. Onkologische Welt 2/2011 © Schattauer 2011 Downloaded from www.onkologische-welt.de on 2017-06-03 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved.