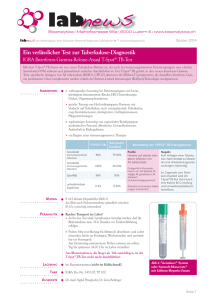
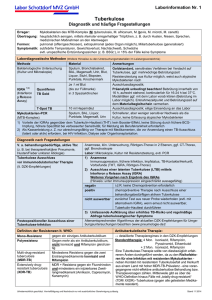
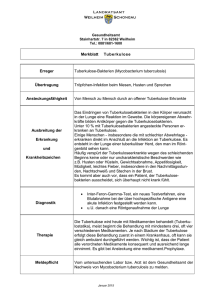
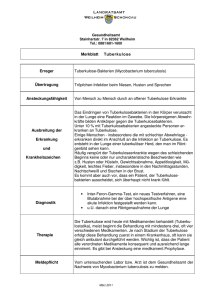
Tuberkulose Im Anhang (Seiten 9-15): Diagnostik
Werbung

Tuberkulose (TB, Tbc) Tuberkulose Definition Durch Erreger des Mycobacterium tuberculosis-Komplexes Dr. Macé Schuurmans, Oberarzt Pneumologie Universitätspital Zürich 18.5.2011 verursachte Infektionskrankheit, die durch Ausbildung eines spezifischen Granulomgewebes (zentral verkäsend) gekennzeichnet ist. Im Anhang (Seiten 9-15): Diagnostik der Tuberkulose Macé M. Schuurmans Klinik für Pneumologie, Universitätsspital Zürich Therapeutische Umschau 2011; 68 (7) Tuberkulose Mycobacterium tuberculosis-Komplex Mycobacterium tuberculosis Mycobacterium bovis The greatest infectious killer of all time Mycobacterium africanum Die WHO hat 1993 einen globalen Tuberkulosenotstand Mycobacterium microti ausgerufen. Mycobacterium canetti Ubiquitäre Mykobakterien und BCG gelten nicht als Erreger der Tbc • Epidemiologie Geschichte 1839 wurde diese Erkrankung wegen der Vielfalt der •1/3 der Weltbevölkerung ist infiziert Symptome als einheitlich erkannt und Tuberkulose • Jährlich erkranken 8-9 Millionen Menschen neu genannt (Johann Lukas Schönlein) • 5-10% der Infizierten erkranken an aktiver Tbc • Jeder Erkrankte infiziert jährlich 10-15 weitere Personen Armut, Migration, medizinische Unterversorgung und HIV fördern die Ausbreitung 1882 Entdeckung des Erregers durch Robert Koch 1921 erste Impfung an Menschen (BCG) Erreger der Tuberkulose BCG-Impfung • Unbewegliche, aerobe Stäbchenbakterien Bacille Calmette-Guérin = attenuierter Lebendimpfstoff • Schwach grampositiv Nicht mehr empfohlen in Ländern mit niedriger Prävalenz • Intrazelluläre Persistenz in mononukleären Phagozyten Umgehung des humoralen Abwehrmechanismus • Mycolsäuren der Zellwand bedingen die Säurefestigkeit Infektionswege der Tuberkulose Klinik der Lungentuberkulose Die Symptomatik der Tuberkulose ist uncharakteristisch • Mensch zu Mensch-Übertragung infektiöser Aerosole Trias: Husten, Auswurf, Nachtschweiss • Endogene Reinfektion Abgeschlagenheit, Müdigkeit • Orale Infektion mit rohen Milchprodukten infizierter Appetitlosigkeit, Gewichtsverlust Rinder ( Pasteurisieren!) subfebrile Temperaturen, Hämoptoe Tuberculin-Skintest (TST) =Mantoux Test Intrakutane Injektion 2E PPD* am volaren Vorderarm: Quaddel muss entstehen Querdurchmesser ablesen nach 48-72 h *PPD=Purified Protein Derivative 12 21.07.2011 T-Zell Antigene (Mykobakterien) Mantoux Test- Limitationen Ältester diagnostischer Test Mantoux C. Presse Med 1910;18:10-13 RD1 Gen-Region: Niedrige Spezifität (60%) PPD als Antigen: Kreuzreaktivität mit BCG- Impfstamm u. atyp.Mykobakterien (falsch pos) Tuberculosis complex Niedrige Sensitivität (60%) In 20-50% bei aktiver TB negativ, vor allem bei Immunsuppression und Mangelernährung ESAT-6: Early Secreted Antigenic Target (6kDa) CFP-10: Culture Filtrate Protein (10kDa) ESAT-6 CFP 10 Environmental strains ESAT-6 CFP 10 M kansasii + + M tuberculosis + + M marinum + + M africanum + + M szulgai + + M bovis + + M M M M M M M - - BCG - - M leprae + + Untersucher-abhängig abcessus, M avium, branderi, M celatum, chelonae, M fortuitum, gordonii, M intracellulare, malmoense, M oenavense, scrofulaceum, M smegmatis terrae, M vaccae, M xenopi Nicht reproduzierbar Zwei Zeitpunkte notwendig (Ablesen) Andersen P, Lancet 2000;356:1099-104 13 21.07.2011 14 Immunologische TB Tests Antigenpräsentierende Zelle PPD Tuberkulin-Hauttest (Mantoux) TNF IFN IFN Incubation at 37ºC for 16-24 hours Centrifuge tubes for 15 min Röhrchen wiederholt nach Blutentnahme“Ueberkopfdrehen” (nicht schütteln!) 16 Lymph/Mono +Antigen IFN- Anti-IFN- 21.07.2011 3x1mL blood collection Keine Aufbewahrung im Kühlschrank! T SPOT-TB 17 IFN- stable refrigerated for at least 4 weeks. Messung der Interferon- Aktivität 21.07.2011 Plasma Lymph/Mono Gel Ec+Granulo Stufe 1 – Blutentnahme und Probenvorbereitung Nil Mitogen TB IL-8 IL-8 Messung der Induration 15 ESAT 6 CFP-10 Memory-T-Zellen von TBinfizierten Personen werden aktiviert, wenn sie mit dem Antigen in Kontakt kommen In vitro Bluttest TNF QuantiFERON®-Gold In Tube Wirkprinzip T-GedächtnisZelle MykobakterienAntigene 21.07.2011 markierte Anti-IFN- 21.07.2011 Primärinfektion postprimäre Tuberkulose Umgebungsuntersuchung 22 Tuberkulose: aktiv oder latent? 21.07.2011 Immun-Antwort bei TB Infektion und Erkrankung ANTWORT Nur 10% der mit M. Tbc infizierten erkrankt klinisch (=aktive TB) früh nach Ansteckung Zellvermittelte Immunität 90% der Infizierten bleiben klinisch gesund, es kommt zu einer klinisch stummen Immunantwort (latente TB) - mögliche spätere Aktivierung der TB in ca. 10% im Verlaufe des Lebens - Immunsuppresion begünstigt die Aktivierung: z.B. HIV-Infektion, immunsuppressive Medikamente (Steroide), Diabetes, Silikose “Mycobacterial Load” Latente TB Infektion 23 21.07.2011 24 21.07.2011 Erkrankung ZEIT Latente Infektion Erkrankung? Endogene Reinfektion Resistenzmindernde Faktoren • Malnutrition • Hohes Lebensalter • Alkoholismus, Drogenabhängigkeit • Diabetes • Kortikosteroide, Immunsuppressiva, Zytostatika • Masern, Keuchhusten • Silikose • AIDS • Maligne konsumierende Erkrankungen Zusätzliche Risikofaktoren: 26 Tuberkulosestadien • Primärtuberkulose: Alle Krankheitserscheinungen im Rahmen der Erstinfektion mit Tb 21.07.2011 Horsburgh CR. NEJM 2004;350:2060-7 Formen der Primärtuberkulose • Primäraffekt oder Primärherd • Primärkomplex • Primärherdphthise (Phthisis = Schwund Schwindsucht) • Postprimärtuberkulose: Alle Krankheits• Progressiver Primärkomplex/ Hiluslymphknoten-Tbc verläufe, die sich nach vorübergehender Kontrolle • Lymphonoduläre Perforationsphthise der Infektion durch das Immunsystem entwickeln • Miliar-Tuberkulose Primäraffekt und Primärkomplex Hiluslymphknotentuberkulose • Erreger werden eingeatmet Lymphogene Ausbreitung der Erreger über die • Typische granulomatöse Gewebereaktion in dem regionären Lymphknoten hinaus auf die nachgebetroffenen meist subpleural gelegenen Lungen- schalteten paratrachealen und tracheobronchialen areal (= Primäraffekt) Lymphknoten • Miteinbezug des regionären Lymphknotens durch lymphogene Verschleppung der Erreger (= Primärkomplex) Komplikation: Stenosen von Bronchien Miliar-Tuberkulose Postprimärtuberkulose Hämatogene Streuung der Erreger, meist in folgende Organe: Manifestation - Lunge (sog. Simon-Spitzenherde) - Meningen - Leber/Milz • Pulmonale Tbc, ca. 85% der Fälle • Extrapulmonale Tbc, ca. 15% der Fälle - Nieren - Nebennieren - Chorioidea der Augen 1. Periphere Lymphknoten 2. Urogenitaltrakt 3. Knochen/Gelenke Komplikation: Sepsis Landouzy bei fehlender Abwehr Tuberkulöse Kaverne Komplikationen der Kavernösen LungenTbc • Bronchogene Streuungsgefahr für den Patienten Erhält ein eingeschmolzenes käsiges Lungenareal • Lungenblutung ( mykotisches Aneurysma) Anschluß an einen Brochus, so kann sich der • Spontanpneumothorax, Pleuraempyem Inhalt nach aussen entleeren: zurück bleibt ein • Sekundäre Erregerbesiedlung (z.B. Aspergillus) luftgefüllter Hohlraum (Kaverne). • Kavernenwandkarzinom Hochinfektiöse offene Lungen-Tbc • Respiratorische Insuffizienz und Cor pulmonale • Sekundäre Amyloidose Mikroskopischer Nachweis: Anreicherung Ziehl-Neelsen-Färbung, Auramin-Färbung Kultureller Nachweis es müssen mindestens 104 Keime/ml vorhanden sein, um ein positives Ergebnis Anzucht auf festen Nährböden (Nachweis nach 3-4 zu erhalten zwischen Tuberkulosebakterien und ubiquitären Mykobakterien kann nicht unterschieden werden ein positiver Befund aus dem Sputum ist trotzdem nach dem Infektionsschutzgesetz meldepflichtig! Wochen) Anzucht in Flüssigmedium mit Fluoreszenzsystem (Nachweis nach 1-2 Wochen) Nukleinsäure-Nachweis: Polymerase-chain-reaction (PCR) innerhalb von 1-2 Tagen Immer nur in Ergänzung zur Mikroskopie und Kultur Materialgewinnung bei V. a. Lungentuberkulose: Sputum (3x morgens nüchtern) Reizsputum (nach Inhalation mit 3,0% NaCl- Lösung) Bronchialsekret Restriktionfragmentlängen-Polymorphismus (DNAFingerprinting): Infektionsketten aufgeklärt Magensaft (Kinder) 2-5 ml nativ Therapie 2+4 Monate: „2HRZE/4HR“ Materialgewinnung bei V. a. extrapulmonale TBC: Biopsien, OP-Präparate (in NaCl-Lösung) Punktate, Sekrete (20 ml nativ) Liquor (2-3 ml, nativ) Stuhl nativ Blut (nur bei HIV, nativ) Wiederholungtherapie (empirisch) MDR-Tbc: Daran denken bei... Annahme einer SDR oder MDR TB: 2 Monate: H - R - E - Z + S dann 1 Monat H - R - E - Z, dann 5 Monate H - R – E Kurz: „2HRZES/1HRZE/5HRE“ Resistenzprüfung! 1. Patienten, die nach 4 Monaten Therapie positiv bleiben oder wieder werden 2. Patienten die eine TB Vortherapie hatten 3. Patienten mit Kontakt zu MDR TB Patienten 4. Patienten mit Kontakt zu Patienten, die unter DOT Therapie an TB starben 5. medizinisches Personal 6. HIV-Patienten 7. Patienten aus Gefängnissen mit hoher MDR TB Rate Therapie der MDR-TB Die Therapie basiert auf 5 Standardmedikamenten Man kann auch mit mehr als 5 Medikamenten beginnen Maximal Dosis muss angewendet werden Parenterale Madikamente werden noch 6 Monate nach Kulturnegativität gegeben Dauer der Therapie 18 – 24 Monate und dann noch 18 Monate nach Kulturkonversion Nebenwirkungen / Isolation bei Hepatitis oder anderen NW: Absetzen der gesamten Therapie bei Anstieg der Transaminasen um das 3-fache warten bis Werte normalisiert erneuter Start mit H in halber Dosis unter Laborkontrolle, nach 3d volle Dosis, genauso weiter mit anderen Tuberkulostatika Infektiosität / Isolierung: gering, Schwebeteilchen 1-5 µm bis zu 23 Tagen in Luft Lüften FFP 3 Masken, bei Untersuchung Patient mit Mundschutz ohne Husten keine Keimverbreitung DOT Tuberkulose: Diagnostik-Zusammenfassung V.a. aktive Tuberkulose: Erreger-Nachweis baldmöglichst (Sputum, Bronchoskopie, Biopsie, Direktpraeparat, Kultur, PCR) Erregernachweis-> Erreger-Typ, Resistenzprüfung, rechtfertigt langdauerned Therapie (NW!) Interferon-Test: kein diagnostisches Instrument für aktive TB, kein guter Ausschluss-Test (kann neg sein bei aktiver TB!) Kontaktpersonen bei offener TB: Umgebungsuntersuchung: 8 Wochen nach Kontakt: Mantoux-Test, wenn unklar Interferon-Bluttest: Dokumentation der Konversion (Basisinformation für prophylakt. Behandlung mit INH für 9 Monate) 45 21.07.2011 TB or not-TB? That is the question! DANKE! Referenzen: Ther Umsch. 2011 Jul;68(7):369-375 Kriterien für Aufhebung der Isolation © 2011 by Verlag Hans Huber, Hogrefe AG, Bern Therapeutische Umschau 2011; 68 (7): DOI 10.1024/0040-5930/a000179 Übersichtsarbeit Klinik für Pneumologie, Universitätsspital Zürich Macé M. Schuurmans Diagnostik der Tuberkulose Unerklärter Husten von mehr als 2 – 3 Wochen oder Patienten mit einem hohen Risiko für eine Tuberkulose (TB) sollten zeitnah im Hinblick auf eine mögliche Tuberkulose-Erkrankung abgeklärt werden: Thoraxröntgenbild, 3 Sputumproben für Direktnachweis und TB-Kultur sind die ersten diagnostischen Schritte. Bei fehlendem Ansprechen auf eine Antibiotikatherapie und negativem Direktpräparat sind weitere diagnostische Schritte zu erwägen, insbesondere die Sputumprovokation mit hypertoner Kochsalzlösung oder die bronchoskopische Probegewinnung. Immunologische und molekulare Diagnosemöglichkeiten ergänzen die Basisdiagnostik besonders bei positivem Direktpräparat oder hohem Ver- steckend ist. Eine Reaktivierung der Infektion erfolgt bei Immunkompetenten in zirka 10 % der Betroffenen zeitlebens, wobei diverse Krankheitszeichen auftreten und die Patienten als ansteckend gelten (postprimäre Tuberkulose; Tab. 1). Bei Immundefekten ist die Reaktivierungsrate erheblich erhöht, so zum Beispiel bei HIV-Infektion in 10 – 15 % der Betroffenen pro Jahr. dacht auf TB bei negativen Sputumproben. Dabei kann einerseits eine Typendifferenzierung der Mykobakterien erfolgen, anderseits können in gewissen Situa- Ärztliche Primär-Diagnostik tionen Antibiotikaresistenzen rasch identifiziert werden. Die Schutzmaßnahmen bei vermuteter oder bestätigter TB sind sowohl für Kontaktpersonen als auch für das medizinische Personal entscheidend, da die Infektion beim Husten durch Aerosolbildung übertragen wird. Gewisse Kriterien sollten erfüllt sein damit im Spital die Isolationsmaßnahmen aufgehoben werden können. Einleitung Hochrechnungen ergeben, dass ein Drittel der Weltbevölkerung mit Tuberkulosebakterien infiziert ist. Dabei ist die Mehrheit ohne Symptome, d. h. es handelt sich um eine latente Tuberkulose-Infektion. Davon zu unterscheiden ist die eigentliche TuberkuloseErkrankung, welche bei Lungenbeteiligung mit Husten zur Infektions-Übertragung führen kann. Die frühe Diagnose und Behandlung einer pulmonalen Tuberkulose-Erkrankung (kurz Tuberkulose oder TB) ist ein entscheidender Beitrag zur Reduktion der Tuberkulose-Infektionen und deren Ausbreitung. Die TB ist eine bakterielle Infektionskrankheit, welche durch Mykobakterien hervorgerufen wird: Mycobacterium (M.) tuberculosis, M. bovis, M. africanum und M. microti werden zusammengefasst als „Mycobacterium tuberculosis complex“ bezeichnet. Am häufigsten beteiligt ist jedoch das Mycobacterium tuberculosis (MTB), welches vorzugsweise die Lunge befällt, in der Regel Husten verursacht und durch Inhalation eines Aerosols übertragen wird (Tröpfcheninfektion). Nur eine Minderheit (5 – 10 %) der Personen entwickelt nach Aufnahme des MTB eine manifeste Tuberkulose-Erkrankung. In der Regel verläuft die Primärinfektion unbemerkt (asymptomatisch) oder mit geringen unspezifischen Symptomen (oligosymptomatisch, Tab. 1), wobei das Immunsystem auf den intrazellulären Erreger reagiert und die Ausbreitung der Erreger durch eine entsprechende immunologische Reaktion begrenzt wird. Es kommt zu einer lokalen Kontrolle des Infektgeschehens, wobei die Erreger entweder ganz eliminiert werden oder eine immunologische Kontrolle der Ausbreitung stattfindet. Dabei gehen die MTB meist in einen metabolischen Ruhezustand über. Bei fehlenden Krankheitszeichen und unauffälligem Thoraxröntgenbild wird dann von einer latenten Tuberkuloseinfektion (LTBI) gesprochen, welche als solche nicht an- Aus epidemiologischer Sicht ist bei niedriger TB-Inzidenz (Schweiz: 500 – 600 Neuerkrankungen /Jahr) und dem Verzicht auf ein allgemeines Screeningprogramm (keine Schirmbildkontrollen mehr) die Frühdiagnose und Frühbehandlung besonders wichtig [2]. Die Frühdiagnose ist nur dann möglich, wenn die Verdachtsdiagnose „TB“ überhaupt gestellt wird und dann entsprechende Abklärungschritte zeitnah eingeleitet werden (Sputumuntersuchungen, Thoraxröntgenbild, siehe unten). Die Diagnostik bei TB-Verdacht sollte möglichst rasch erfolgen. Die Weltgesundheitorganisation (WHO) empfiehlt für die TB-Diagnostik ein standardisiertes Vorgehen (Tab. 2) [3]. Für die Schweiz sind Empfehlungen im „Handbuch Tuberkulose“ festgehalten, welches von der Lungenliga Schweiz und dem Bundesamt für Gesundheitswesen herausgegeben wird [4]. Zudem betreibt die Lungenliga Schweiz ein TB-Beratungstelefon, welches Ärzten einen erleichterten Zugang zu TB-Spezialisten ermöglicht. Die Diagnose einer TB ist erst dann möglich, wenn im klinischen Kontext der Verdacht einer Tuberkulose-Erkrankung geschöpft und aktiv danach gesucht wird. Hinweisend auf eine TB können anamnestische Angaben, klinische Symptome und radiologische Befunde sein. 369 Macé M. Schuurmans 370 Diagnostik der Tuberkulose Übersichtsarbeit Tabelle 1 Klinisches Bild der Tuberkulose [1] Primärinfektionen Postprimär Tuberkulose (Lunge) Beschwerden +++ Husten Müdigkeit/Unwohlsein + Gewichtsverlust + ++ ++ Nachtschweiß ++ Hämoptyse + Thoraxschmerzen + + ++ ++ Befunde Fieber Rasselgeräusche + Dämpfung, Pleurareiben + Tuberkulinreaktion +++ (nach 4 – 8 Wochen) +++ (in 85 % der Fälle) + die Infekt-, Familien- und Reiseanamnese erhoben werden, sowie das Herkunftsland des Patienten bekannt sein. Diese Informationen helfen, das Risiko für eine TB besser abzuschätzen: Bei Patienten mit hohem Risiko für eine Tuberkulose (Tab. 3) sollte auch bei unklaren respiratorischen oder AllgemeinSymptomen von weniger als 3 Wochen Dauer und/oder unauffälligem Thoraxröntgenbild eine TB-Diagnostik veranlasst werden, da gerade bei Immunsuppression (z. B. HIV-Infektion) sowohl die Klinik als auch die radiologischen Zeichen fehlen können. Nachdem die ärztliche Primär-Diagnostik zur Verdachtsdiagnose „TB“ geführt hat erfolgt die Labordiagnostik mit dem primären Ziel mittels direktem Erregernachweis im Sputum laborchemisch und klinisch die Diagnose zu bestätigen. Thoraxaufnahme Infiltrate der Lungenspitzen +++ Kavernen +++ Infiltration der Lungenbasen ++ Hilusvergrößerung ++ Probegewinnung für Direktnachweis und TB-Kultur + + + = oft (> 50 %), + + gelegentlich, + selten Anamnese, Symptome, klinische Zeichen und das Thoraxröntgenbild Husten ist das Kardinalsymptom der Tuberkulose (Tab. 1). Wenn der Husten für mehr als 2 – 3 Wochen andauert und mindestens ein zusätzliches Symptom vorhanden ist (Fieber, Nachtschweiß, Gewichtsverlust oder Auswurf mit oder ohne Blut), dann sollte ein Thoraxröntgenbild angefertigt werden. Bei einem pathologischen Röntgenbefund (z. B. lokalisierte Transparenzminderung im Bereich der Oberlappen oder apikalen Unterlappen mit oder ohne Kavität), sollte die Verdachtsdiagnose TB gestellt und die TB-Diagnostik eingeleitet werden. Radiologische Labordiagnostik Befunde können bei der TB vielfältig sein und lassen zahlreiche Differentialdiagnosen zu. Trotzdem ist das Thoraxröntgenbild von großer Bedeutung: Bei suggestiven Veränderungen ist die TB-Diagnostik zu rechtfertigen und bei unklaren radiologischen Pathologien sind weiterführende diagnostische Schritte möglich, wie z. B. eine Computertomographie bei Tumorverdacht oder eine sonographisch-gesteuerte Punktion bei Pleuraerguss. Auch in der TB-Diagnostik sind Vergleiche mit früheren Thoraxröntgenbildern nicht selten hilfreich, um vorbestehende Veränderungen zu verifizieren. Da die Symptome und klinischen Zeichen der Lungentuberkulose oft uncharakteristisch sind, sollte besonders Bei Verdacht auf Tuberkulose sollten die diagnostischen Schritte ohne Verzug veranlasst werde, wobei der KeimNachweis mittels Kultur nach wie vor der Gold-Standard ist und daher immer angestrebt werden sollte. Dazu sollten primär eine sofortige Sputumprobe (unabhängig von der Tageszeit) und anschließend 2 morgendliche Sputumproben abgenommen und als Direktpräparat und TB-Kultur im Labor untersucht werden. Bei fehlender Sputumproduktion ist eine Sputum-Provokation durch Inhalation von hypertoner (3 %) Kochsalzlösung möglich, dabei muss aber beachtet werden, dass für anwesende Personen im Falle einer aktiven TB eine Übertragungsgefahr besteht und entsprechende Schutzmaßnahmen einzuhalten sind [4]. Alternativ könnten bronchoskopische Proben (broncho- Therapeutische Umschau 2011; 68 (7): 369 – 375 Übersichtsarbeit Tabelle 2 Internationale Standards für die Tuberkulosediagnostik [gekürzt aus 3, 4] 1. Bei nicht anders erklärbarem Husten länger als 2 – 3 Wochen an Tuberkulose denken! 2. Immer mindestens 2, besser 3 Sputumproben auf Tuberkulose einschicken, mindestens eine davon aus Morgensputum 3. Bei Verdacht auf extrapulmonale Tuberkulose Präparat nicht nur für Zytologie/Histologie, sondern auch für Tuberkulosekultur entnehmen. 4. Bei tuberkuloseverdächtigem Thoraxröntgenbild immer Sputumkulturen auf Tuberkulose veranlassen. 5. Die Verdachtsdiagnose Tuberkulose soll auch bei negativem Sputumdirektpräparat bei verdächtigem Röntgenbild und Nichtansprechen auf eine antibiotische Therapie während 1 – 2 Wochen (nicht mit Fluorochinolonen!) aufrechterhalten und eine Tuberkulosetherapie eingeleitet werden, insbesondere bei HIV/AIDS-Patienten. 6. Bei Kindern mit positivem Tuberkulosehaut- oder allenfalls -bluttest und/oder Expositions- Anamnese und Röntgenbefunden: Kultur aus Sputum, Magensaft oder Bronchialsekret veranlassen. alveoläre Lavage; BAL) gewonnen werden. Gelegentlich ist eine zusätzliche Bildgebung mittels Computertomographie zur Lokalisationsdiagnostik notwendig, dies wird aber vom Lungenspezialisten veranlasst. Manchmal haben die tuberkulösen Gewebeveränderungen keinen Anschluss an das Bronchialsystem. Dann kann eine Probeentnahme mittels Nadel- punktion (z. B. Computertomographiegesteuerte) oder eine chirurgische Gewebebiopsie (z. B. videothorakoskopisch) notwendig sein. Die Probe sollte dann nicht nur der Pathologie sondern auch an das TB-Labor für Direktnachweis und Kultur verschickt werden. Die Zusammenarbeit mit einem Labor mit entsprechender Erfahrung und Expertise in der TB-Diagnostik ist sehr zu empfehlen. Die SputumprobenVerarbeitung (Anreicherung, Dekontamination, Färbungen und diverse Kulturmethoden), die Beurteilung und die erzielten Resultate sind auch davon abhängig, welche apparativen Möglichkeiten zur Verfügung stehen für die Weiterverarbeitung der Proben im Falle eines positiven Direktnachweises. Tabelle 3 Risikofaktoren und prädisponierende Faktoren bei Tuberkulose [modifiziert nach 1] Risikofaktoren (Faktoren, welche das Risiko für eine Ansteckung erhöhen) Kontakt zu einem kontagiösen Tuberkulosepatienten, Tuberkulintest von > 15 mm Immigranten aus Ländern mit hoher Tuberkulose-Inzidenz (Asien, Afrika, Lateinamerika, Russische Föderation) Insassen von Institutionen, Randgruppen Medizinisches Personal Prädisponierende Faktoren für eine Tuberkulose (d. h. Erhöhung des Risikos, bei gegebener Ansteckung die Krankheit zu entwickeln) HIV-Infektion kürzliche Konversion des Tuberkulintests Silikose Diabetes Chronische Niereninsuffizienz maligne Erkrankungen (Kopf, Hals, Lungen, Lymphom) Gastrektomie Alkoholismus Kachexie Behandlung mit Steroiden oder Immunsuppressiva alte unbehandelte Tuberkulose (Folgen) IV-Drogen-Abusus TNF-alpha-Hemmer 371 Macé M. Schuurmans Diagnostik der Tuberkulose 372 Übersichtsarbeit Direktnachweis und TB-Kultur Der mikroskopische Direktnachweis im Sputum ist eine Schlüsseluntersuchung, da sie eine rasche Erkennung einer potentiell ansteckenden Infektion ermöglicht. Dabei wird Ziehl-Neelsen-Färbung oder Auramin-RhodaminFärbung angewendet. Die Färbung verbleibt auch nach Behandlung mit einer sauren Lösung, daher kommt der Begriff „säurefeste Stäbchen“. Mit Vorteil erfolgt die Beurteilung des Direktpräparates unter Einsatz der Fluoreszenzmikroskopie (bessere Sensitivität als konventionelle Mikroskopie). Mindestens 10 000 Keime/ml müssen im Sputum vorhanden sein damit der Direktnachweis positiv wird. Patienten mit niedriger Keimzahl im Sputum werden mit dieser Methode häufig übersehen, was insbesondere bei Patienten mit HIV-Infektion die Diagnostik erschwert. Wird der Erregernachweis mittels einer TB-Kultur des Sputums erbracht, ist die Diagnose einer Tuberkulose gesichert und damit auch die Infektiosität dokumentiert. Die Gramfärbung stellt die Mykobakterien ungenügend dar, wobei sie als schwach grampositiv zur Darstellung kommen. Bei positivem Direktnachweis sollte eine Polymerase-Chain-Reaction (PCR)-Untersuchung für den raschen Nachweis des MykobakteriumTyps (positiver Nachweis von MTB) erfolgen, damit eine Therapie rasch eingeleitet werden kann (möglich im Sputum und in der BAL). Die gleichzeitig angelegte TB-Kultur des Sputums wird entweder konventionell verarbeitet (Löwenstein-Jensen oder Ogawa Nährmedium, Resultat innert 2 Monaten) oder mittels automatisierter Methode unter Einsatz eines Flüssigmediums kultiviert (BACTEC MGIT = mycobacteria growth indicator tube), Resultat innert 2 Wochen). Die Sputumkultur wird zur Bestäti- gung des Bakteriumwachstums (viable und teilungsfähige Mykobakterien) und zur Resistenzprüfung verwendet. Erforderlich sind 50 – 100 Keime/ml im Sputum für den positiven Nachweis mittels TB-Kultur. Bei positiver Kultur kann die Art des Mykobakteriums identifiziert werden. Die Empfindlichkeitsprüfung des Erregers auf die wichtigsten Antituberkulotika sollte unbedingt verlangt werden. Bei dem ohnehin schon zeitaufwendigen kulturellen Nachweis lohnt es sich, mit einem spezialisierten Labor zusammen zu arbeiten, welches u. a. die automatisierte Methode anbietet. Kultur-negative Tuberkulose Bei fehlendem kulturellen Nachweis kann von einem wahrscheinlichen Tuberkulosefall gesprochen werden, wenn (a) die Identifikation von MTB mittels DNA-Sonde (siehe unten) erfolgt ist, oder (b) Mykobakterien im Direktnachweis erfolgt sind, oder (c) bei ärztlichem Entscheid, eine vollständige antituberkulöse Therapie durchzuführen wenn zusätzlich bei diesen 3 Situationen die klinischen und radiologischen Befunde mit einer TB vereinbar sind. Man spricht dann von einer Diagnosestellung ohne bakteriologische Bestätigung und man sollte in solchen Fälle erst nach Rücksprache mit einem TB-Spezialisten eine antituberkulöse Therapie durchführen bzw. den Patienten für ergänzende Untersuchungen zur Diagnosesicherung überweisen [4]. Immunologische Tests Es gibt immunologische Tests, welche eine Immunantwort auf Bestandteile von Mykobakterien anzeigen. Zu diesen Tests gehören der TuberkulinHauttest und der Interferon-GammaRelease Assay (IGRA). Beide Tests können zur Diagnostik einer latenten Tuberkuloseinfektion eingesetzt werden, wobei bei einem positiven Testresultat stets klinisch und radiologisch eine aktive Tuberkulose ausgeschlossen werden muss. Der Tuberkulin-Hauttest (THT, synonym: Mantoux-Test) ist ein in vivo Test, bei dem eine definierte Menge gereinigter Antigene aus Mykobakterien in die Haut gespritzt wird. Bei Personen mit vorhergehendem Kontakt mit Mykobakterien kommt es innerhalb von 48 – 72h zu einer spezifischen T-Zellaktivierung (verzögerte Überempfindlichkeitsreaktion) mit einer tastbaren Verdickung der Haut (= Induration) und oft auch zu einer lokalen Rötung. Die Induration wird zur Testinterpretation ausgemessen und wird als positiv bezeichnet, wenn eine definierte Indurationsgröße überschritten wird. Ab welchem Durchmesser ein Test als positiv zu bewerten ist hängt ab vom relativen Infektionsrisiko der Bevölkerungsgruppe, welcher der Patient angehört, z. B. nicht-BCG-geimpfte Normalbevölkerung ≥ 10 mm, BCG-geimpfte Normalbevölkerung ≥ 15 mm und Personen mit eingeschränkter Immunität (z. B. HIV-Infektion) ≥ 5 mm [1, 5]. Ein positiver THT ist lediglich ein Hinweis für den vorausgegangenen Kontakt mit Mykobakterien (d. h. durchgemachte Primärinfektion vor ≥ 8 Wochen). Er kann nicht unterscheiden zwischen einer latenten Infektion und einer aktiven Tuberkulose-Erkrankung. Die Verlässlichkeit des Tests ist zudem eingeschränkt durch die Anfälligkeit auf Fehler bei der Durchführung (Injektion) und Ablesung, sowie durch falsch-negative Testresultate bei schweren TBKrankheitsverläufen, wie z. B. einer Miliartuberkulose (eingeschränkte Sensitivität). Eine Tuberkulose-Schutzimpfung mit BCG und Kontakt mit atypischen Mykobakterien können auch zu einem positiven Testresultat führen (einge- Therapeutische Umschau 2011; 68 (7): 369 – 375 Übersichtsarbeit schränkte Spezifität). Bleibt bei einem korrekt durchgeführten THT bei einer immunkompetenten Person die Induration aus oder ist die Haut lediglich gerötet ist eine Tuberkulose-Erkrankung unwahrscheinlich, aber nicht ausgeschlossen. Zusammenfassend ist der THT bei Erwachsenen für die Diagnostik der latenten Tuberkuloseinfektion einsetzbar. Bei Kindern hingegen ist die Chance eines früheren Kontakts mit MTB als gering einzustufen, sodass ein neu dokumentierter positiver THT durchaus einer frischen Infektion entsprechen kann. Da ein größerer Anteil der Infektionen im Kindesalter zur eigentlichen TB-Erkrankung führt und schwere Verläufe ebenfalls häufiger zu beobachten sind, ist ein positiver Tuberkulintest bis zum Beweis des Gegenteils eine TBErkrankung. In entwickelten Ländern hat der THT bei Erwachsenen wegen oben-genannter Limitationen zunehmend an Bedeutung verloren, weil mit den in vitroTests eine neuere Methode vorliegt, welche den Kontakt mit MTB zuverlässiger nachweist und somit zur Diagnostik der latenten Tuberkuloseinfektion geeignet ist. Beim Interferon-Gamma-Release Assay (IGRA) handelt es sich um einen in vitro-Test bei dem Abwehrzellen im Blut mit einer Mischung von Antigenen von MTB stimuliert werden. Ein vorausgegangener Kontakt mit MBT führt zu einer vermehrten Produktion von Interferon Gamma, welches im Test mengenmäßig nachweisbar ist und sich quantitativ von einer Negativ-Kontrolle unterscheidet. Innerhalb von 24 h nach Antigenkontakt lassen sich sowohl im ELISA (Quantiferon-Gold-Test in tube; (QFT-G-IT), Cellestis, Carnegie, Australien) als auch im ELISPOT (T-SPOT.TB; Oxford Immunotec, Abingdon, UK) MTB-spezifische T-Zellen als Ausdruck eines rasch aktivierbaren immunologischen Gedächtnisses ge- genüber MTB nachweisen. Zur Anwendung in beiden Testverfahren kommen Antigene aus der RD-(„region of difference“-)1 im Genom von MTB [6]. Diese Region unterscheidet MTB von anderen Mykobakterien (mit Ausnahme von M. kansasii, M. marinum, M. szulgai) und von den für die Impfung verwendeten BCG-Stämmen. Daher bleibt der Test durch atypische Mykobakterien und die BCG-Impfantwort unbeinflusst, ein Vorteil gegenüber dem THT. Zugelassen ist der Test für die Diagnostik der latenten Tuberkuloseinfektion. Da der IGRA-Test ähnlich dem THT lediglich einen vorausgangenen Kontakt mit Mykobakterien nachweisen kann und das Ausmaß der Interferon-Gamma-Ausschüttung nicht ein verlässliches Maß zur Unterscheidung einer latenten oder aktiven Tuberkuloseinfektion ist, muss eine ergänzende Diagnostik mit radiologischen Veränderungen und Keim-Nachweis zur Diagnostik der Tuberkulose-Erkrankung erfolgen. Obwohl die diagnostische Sensitivität des IGRAs dem des THT überlegen ist, ist die Sensitivität nicht ausreichend hoch, damit er als Ausschlusstest für eine Tuberkulose dienen kann [7]. Ein negatives IGRATestresultat kann somit eine aktive Tuberkulose nicht mit genügender Sicherheit ausschließen. Bei HIV-Infektion ist die Immunreaktion im THT und QFT-G-IT stark abhängig von der Anzahl CD4pos-Zellen, was sich in einer erhöhten Anzahl falsch negativer Resultate äußert. Der T-Spot.TB-Test hingegen scheint aufgrund des Testverfahrens auch bei tiefen CD4pos-Zellzahlen diagnostisch einsetzbar zu sein [8]. Molekulare Nachweismethoden Verschiedene molekulare Nachweismethoden haben sich in der TB-Diagnostik der letzten Jahre für die Erre- ger-Identifikation und Erfassung von Antibiotikaresistenzen etabliert. Der molekularbiologische Direktnachweis von MTB mittels PCR erlaubt die Abgrenzung des Erregers gegenüber anderen säurefesten Stäbchen wie Nichttuberkulöse Mykobakterien oder Nocardia, wobei das Testresultat meist innert eines Tages vorliegt. Wenn eine Therapie bei hohem Verdacht auf TB rasch eingeleitet werden muss, dann ist diese Unterscheidung sehr wichtig. Bei einem positiven Direktpräparat ist die Sensitivität im Falle von MTB nahezu 100 %, bei einem negativen Direktpräparat mit später nachgewiesener Tuberkulose ist die Sensitivität von PCR im Direktpräparat lediglich 60 – 70 % [1]. In der Regel ist diese Methode dann sinnvoll einsetzbar, wenn ein positives Direktpräparat vorliegt. Ist jedoch bei einem negativen Direktpräparat der Verdacht auf eine Tuberkulose sehr hoch (Risikogruppe), dann kann ein positives PCR-Resultat therapeutisch richtungsweisend sein und eine entsprechende Zusatzdiagnostik ermöglichen. Zu den Nachteilen dieser Methode gehören die fehlende Aussage, ob die Nukleinsäuren von toten oder lebenden Mykobakterien stammen und gelegentlich falsch positive Resultate aufgrund von Kontamination der Proben. Weiterführenden Diagnostik in Speziallabors für TB-Diagnostik und zukünftige Entwicklungen Mittels einer Gen-Sonde ist eine Typendifferenzierung (von z. B. M. tuberculosis, M. avium intracellulare, M. kansasii und M. gordonae) in wenigen Stunden möglich, wobei eine speziesspezifische Hybridisierung von ribosomaler RNA von Flüssig- und Festmedienkulturen möglich ist. Bei einem TB-Verdachtsfall aus einem Land mit hoher Resistenzhäufigkeit und/oder 373 Macé M. Schuurmans Diagnostik der Tuberkulose 374 Übersichtsarbeit Tabelle 4 Aufhebung der Isolierung von Patienten mit offener Tuberkulose [10] 1. Adäquat dosierte Behandlung mit klinischer Besserung während mindestens zwei Wochen 2. Kein Husten mehr oder mindestens zweimalige konsekutive negative Sputummikroskopie 3. Keine anamnestischen, klinischen, epidemiologischen oder bakteriologischen Hinweise auf resistente Tuberkulosestämme 4. Gewährleistete Weiterbehandlung (kontrollierte Medikamenteneinnahme oder keine Zweifel an der Compliance und gesicherte medizinische Nachbetreuung) 5. Rückkehr in ein Milieu ohne Risikopersonen (keine abwehrgeschwächten Personen oder Kleinkinder) nach bereits früher durchgeführter TBBehandlung kann die direkte Bestimmung des für eine Resistenz auf Rifampicin (RIF) verantwortlichen Gens (rpoB-Gen) innert weniger Stunden den entscheidenden Hinweis auf resistente Mykobakterien liefern. Da eine RIF-Resistenz meist mit einer Isoniazid-Resistenz einhergeht, kann die Verdachtsdiagnose MDR (multi-drug-resistente, auf Isoniazid und RIF resistente) TB frühzeitig gestellt und eine Behandlung mit Reserveantibiotika eingeleitet werden (4). Ein fast vollständig automatisiertes System (GeneXpert der Firma Cepheid) mit einer Einmalkartusche "XpertMTB/RIF" kann innert 2 Stunden mittels PCR-Technik sowohl das MTB als auch eine RIF-Resistenz in einer Sputumprobe detektieren. Schließlich ist bei unklarer Typendifferenzierung auch die Sequenzierung des Erregers möglich, wobei die DNA-Sequenz zur Identifikation dient. Auch diese Methode ist speziellen Situationen vorbehalten. Serologische Testverfahren zum Nachweis von Antikörpern gegen Mykobakterien haben bisher keinen Stellenwert in der Klinik. Andere diagnostische Verfahren, z. B. der Nachweis einer TB durch einen molekularen „Fingerabdruck“ unterschiedlicher Antigene oder Serumproteine bzw. Zytokine befinden sich in der klinischen Entwicklung. Schutzmaßnahmen bei vermuteter oder bestätigter Tuberkulose Zum Schutz des medizinischen Personals und der Mitpatienten müssen infektiöse TB-Patienten in einem Isolierzimmer initial behandelt werden. Zu den Schutzmaßnahmen gehören auch die Kennzeichnung der Infektionsbereiche und Masken für die Patienten, die die Aerosolproduktion beim Husten verhindern. Für die Arbeitnehmer sind persönliche Schutzmasken der Schutzklassen FFP2 und FFP3 bereitzustellen. Die Schutzmaßnahmen beim Umgang mit Patienten mit vermuteter oder bestätigter ansteckender Tuberkulose (Früherkennung und Abklärung von Patienten mit Verdacht auf ansteckende Tuberkulose; Isolierung von Patienten im stationären Bereich; generell technische, organisatorische und personenbezogene Schutzmaßnahmen) sind in der Publikation der SchweizerischenUnfall-Versicherungs-Anstalt (SUVA) detailliert beschrieben [9]. Nicht nur im stationären Bereich sondern auch bei ambulanten Patienten sollten bei Symptomen einer schweren respiratorischen Infektionskrankheit eine einfache, aber höchst wirkungsvolle Maßnahme getroffen werden: der kranken Person eine Gesichtsmaske abgeben, welche vor den Mund und Nase getragen wird. Tuberkulosekranke, welche eine korrekte Behandlung einnehmen und nicht mehr husten sind für Nicht-immunsupprimierte Umgebungspersonen als nicht ansteckend zu betrachten [2]. Die Aufhebung von Isolationsmaßnahmen im stationären Bereich sollte gemäß Swiss Noso-Publikation nach gewissen Grundsätzen erfolgen (Tab. 4) [10]. Die Punkte 1 – 4 gelten für alle Patienten. Punkt 5 muss erfüllt sein, falls initial eine sehr hohe Bakterienlast im Sputum vorhanden war, kavitäre Lungenläsionen vorliegen, oder bei Aufhebung der Isolierung noch vereinzelte säurefeste Stäbchen im Direktpräparat sichtbar sind. Diagnosing pulmonary tuberculosis Unexplained cough for more than 2 – 3 weeks or patients considered to be at high risk for tuberculosis (TB) should be investigated in a timely manner: Chest radiography and 3 sputum examinations for detection acidfast bacilli and TB cultures are essential first diagnostic steps. Pending sputum results an antibiotic trial (avoiding fluorochinolones) is warranted and if symptoms do not resolve and the diagnosis remains unclear then additional investigations are required to confirm or rule out pulmonary tuberculosis: sputum provocation by inhalation of hypertonic saline or alternatively bronchoscopy may provide samples to confirm TB or lead to an alternative diagnosis. Immunologic and molecular tests are useful in specific situations to identify previous contact with specific mycobacteria or identify drug-resistant strains. Prompt diagnosis and treatment are important epidemiologic measures to prevent transmission of Therapeutische Umschau 2011; 68 (7): 369 – 375 Übersichtsarbeit mycobacteria to contacts including the medical personnel. Isolation measures take into account the transmission by aerosol and the viability of the 4. mycobacteria and specific criteria need to be met before these precautions can be abandoned. 5. Literatur 1. Brändli O, Prod'hom G, Rochat T, Zellweger JP. Klinik und Diagnose der Tuberkulose, Schweiz Med Forum 2003; 5: 492 – 7. www.medicalforum.ch 2. Handbuch Tuberkulose (Herausgegeben von der Lungenliga Schweiz und dem Bundesamt für Gesundheit BAG, 2007). 3. Hopewell PC, Pai M, Maher D, Uplekar M, Raviglione MC.Interna- 6. 7. tional standards for tuberculosis care. Lancet Infect Dis. 2006 Nov; 6: 710 – 25. Brändli O. Wie diagnostiziere ich 2008 eine Tuberkulose? Schweiz Med Forum 2008; 8: 564 – 568. www.medicalforum.ch Rieder H, Zellweger JP, Quadri F, Desgrandchamps D. Früherfassung und Behandlung der Tuberkuloseinfekion-BCG-Impfung. Schweiz Med Forum, 2003; 3: 531 – 9. www.medicalforum.ch Strassburg A, Jafari C, Greinert U, Lange C. Klinische Diagnostik der pulmonalen Tuberkulose. Med Klin 2007; 102: 665 – 75. Sester M, Sotgiu G, Lange C, Giehl C, Girardi E, Migliori GB, et a. Interferon-γ release assays for the diagnosis of active tuberculosis: a systematic review and meta-analysis. Eur Respir J. 2011 Jan; 37: 100 – 11. 8. Leidl L, Mayanja-Kizza H, Sotgiu G, Baseke J, Ernst M, Hirsch C, et al. Relationship of immunodiagnostic assays for tuberculosis and numbers of circulating CD4 + T-cells in HIV infection. Eur Respir J. 2010 Mar; 35: 619 – 26. 9. «Tuberkulose am Arbeitsplatz: Gefährdung und Prävention», Suva Publikation, 1999; 2869/35. 10. Swiss Noso Band 5, Nummer 1, März 1998. Korrespondenzadresse Dr. med. Macé Schuurmans Klinik für Pneumologie C-HOER 27 Rämistraße 100 CH - 8091 Zürich [email protected] 375