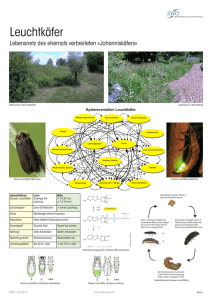
Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger
Werbung

Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Lektion 1 Grundlagen 1 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Thermodynamik mit Mechanik, Optik, Elektrodynamik Ist klassisches Teilgebiet der Physik (daneben noch Quantenmechanik) Das Teilgebiet hat eigenen Charakter Getragen von sehr vielen Molekülen Statistische Mittelungen 2 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Viele neue Begriffe System Zustand Zustandsgrößen: Temperatur, Druck, Volumen, Masse… Gleichgewicht 3 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Beispiel Gleichgewicht Bewegung schnell langsam 4 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Ursprüngliche Ansicht: Wärme = eigenständiges Phänomen Untersuchen von Zusammenhängen: Druck, Temperatur, Volumen, Masse,… Dies führt auf die sog. Phänomenologische Thermodynamik 5 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Beispiel: Temperatur-Ausgleich T2 T1 T2 T2 > T1 T1 T2 > T2 = T1 > T1 Umkehrung unmöglich! Richtung der Zeit! 0. Hauptsatz der Thermodynamik 6 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 1842 Robert Mayer (Heilbronn!): sagt Wärme = Arbeit = Energie! 1 cal = 4,185 Joule Später: Wärme = kinet. Energie von Molekülen Maxwell und Boltzmann : Statistik 7 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Zwei Arten der Beschreibung 1. Makroskopische Betrachtung = phänomenologische Thermodynamik Zustandsgrößen p, T, V, m, r… 2. Mikroskopische Betrachtung = Beschreibung mit mathem. Statistik Thermodynamische Potentiale U, H, S, 8 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Modell eines Moleküls 9 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 10 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 11 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 12 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger p 1 B T 2 A V 13 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 14 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger T O 373.15 K 100 C 273.15 K 0C Temperatur Gefrierpunkt abs T=0 Siedepunkt Temperatur Tripelp. Siedep. 15 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 16 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Fixpunkt Wasserstoff Neon Sauerstoff Wasser Gallium Aluminium Silber Gold T/K 13,8033 24,5561 54,3584 273,16 302,9146 933,473 1234,93 1337,33 oC -259,3467 -248,5939 -218,7916 0,01 29,7646 660,323 961,78 1064,18 17 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Aufgaben 18 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Lektion 2 Ideale Gase 19 1 273,15 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 1. Phänomenologische Thermodynamik Die Zustandsgleichung für ideale Gase a) Gesetz von Gay-Lussac V V01 bei p = const in °C. Ideale Gase: 1 273,15 20 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger b) Boyle-Mariotte p V const bei T const. 21 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger b) Boyle-Mariotte p V const bei T const. Kombination Gay_Lussac und Boyle-Mariotte: p V = n Rm T Mit: n = Stoffmenge in mol Rm = universelle molare Gaskonstante T = absolute Temperatur in Kelvin p = Druck in Pascal:1 Pa = 1 N/m2) 22 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Da m n MG Mit m = Masse des Gases MG = Molekulargewicht folgt: Rm m p V Rm T m T m Ri T MG MG mit Rm Ri MG = individuelle Gaskonstante 23 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Weitere Schreibweise: Da Mit Rm N A k B 1 N A 6,023 10 Avogadro Konstan te mol 23 J k B 1,38 10 Boltzmann Konstan te K J fo lg t Rm 8,315 K mol 23 24 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Wir benutzen die Gleichung für ideale Gase in der Form: p V = n Rm T Mit p in Pa, V in m3 und T in K Und Rm = 8,315 J/K mol 25 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Beispiel: • Wasserdampf bei 200°C lässt sich bei Atmosphärendruck oder weniger Druck mit guter Näherung als ideales Gas beschreiben. Wie viel Liter Wasserdampf entstehen aus m = 54 g Wasser bei T = 525 K und p = 506 mb absolut? 26 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 2. Mikroskopische Beschreibung Die kinetische Gastheorie – Ein Modellgas Molekül Nr. i in einem Würfel der Kantenlänge a 27 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Grundannahmen: • Das Eigenvolumen der Teilchen ist vernachlässigbar 28 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Grundannahmen: • • Das Eigenvolumen der Teilchen ist vernachlässigbar Zwischen den Teilchen wirken keine Kräfte 29 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Grundannahmen: • • • Das Eigenvolumen der Teilchen ist vernachlässigbar Zwischen den Teilchen wirken keine Kräfte Die Stöße zwischen Teilchen und zwischen Teilchen und Gefäßwand sind rein elastisch (d.h. Impuls- und Energieerhaltung sind gültig). 30 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Impulsübertrag an die Wand: p 2 m v xi 31 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Impulsübertrag an die Wand: p 2 m v xi Laufzeit hin + rück: 2a t v xi 32 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Impulsübertrag an die Wand: p 2 m v xi Laufzeit hin + rück: Mittlere Kraft: 2a t v xi ~ pi 2 m v xi m v xi2 Fi 2 a t a v xi 33 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Impulsübertrag an die Wand: p 2 m v xi Laufzeit hin + rück: Mittlere Kraft: 2a t v xi ~ pi 2 m v xi m v xi2 Fi 2a t a v xi Fi Fi m v xi2 m v xi2 Druck durch Teilchen i: pi 2 3 A a V a 34 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Impulsübertrag an die Wand: p 2 m v xi Laufzeit hin + rück: 2a t v xi Mittlere Kraft: Druck durch Teilchen i: Alle N Moleküle: ~ pi 2 m v xi m v xi2 Fi 2a t a v xi Fi Fi m v xi2 m v xi2 pi 2 3 A a V a m p N v xi2 V 35 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Alle N Moleküle: p 1 N m N v xi2 V x Wegen Mittelwert (allgemein): x Mittlere quadr. Geschwindigk. v x2 1 v xi2 N N Mittlerer Druck: p Nm 2 vx V Über alle 3 Richtungen x,y,z: p 1 Nm 2 v 3 V i i 36 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Mit der Gasdichte: Folgt: Und schließlich: N m M ges V V 1 p v 2 3 vmittel v 2 3p 37 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Phänom. Thermodyn.: • Kinet. Gastheorie: p V n Rm T n N A kB T N kB T 1 p V N m v 2 3 • Vergleich ergibt: 1 m v 2 kB T 3 • Also: 3 1 3 2 m v Wkin k B T 2 3 2 • Für Moleküle mit 3 Freiheitsgraden! 38 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Für f Freiheitsgrade: f Wkin k B T 2 Freiheitsgrade: 1-at. 2-at,starr verb. 2-at.federnd verb. 3-at.starr verb. Translat. Rotat. Schwing. 3 0 0 3 2 0 3 2 2 3 3 0 f 3 5 7 6 39 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Lektion 3 Der 1. Hauptsatz 40 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Verteilung der Geschwindigkeiten nach Maxwell 41 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Temperatur 42 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Neu: Der erste Hauptsatz der Thermodynamik: Bekannt: Wärme Q = Energie! Zu- bzw. Abfuhr von Wärme: dQ = C dT C = Wärmekapazität (allgemein) 43 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Der erste Hauptsatz der Thermodynamik: Wärme Q = Energie! dQ = C dT C = Wärmekapazität 44 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger C = Wärmekapazität = f ( Material , Masse , T ) 45 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger C = Wärmekapazität = spezifische Wärme f ( Material , Masse , T ) C c f ( Material , T ) m 46 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger C = Wärmekapazität = spezifische Wärme Molare Wärme f ( Material , Masse , T ) C c f ( Material , T ) m C C MG Cm c MG n m 47 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Molare Wärme = f(Material,T) T2 Q n Cm (T ) dT T1 48 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger dQ = Cp,m dT dQ = Cv,m dT 49 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Messung der Wärmekapazität: Kalorimeter Qabgegeben = Qaufgenommen m2 c2 (T2 - Tm) = m1 c1 (Tm - T1) m1 c1 ( Tm T1 ) c2 m2 (T2 Tm ) Messung gegen Wasser 50 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Wasser: c = 1 cal/g · K Mechanisches Wärme-Äquivalent: 1 cal = 4,185 J 51 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 1. Hauptsatz: In einem abgeschlossenen System bleibt der Gesamtbetrag der Energie konstant. Die verschiedenen Energieformen wandeln sich nur ineinander um. 52 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 1. Hauptsatz: In einem abgeschlossenen System bleibt der Gesamtbetrag der Energie konstant. Die verschiedenen Energieformen wandeln sich nur ineinander um. Oder: dU = dQ + dW 53 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 1. Hauptsatz: In einem abgeschlossenen System bleibt der Gesamtbetrag der Energie konstant. Die verschiedenen Energieformen wandeln sich nur ineinander um. Oder: bzw. dU = dQ + dW dU = dQ - pdV 54 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Lektion 4 Zustandsänderungen 55 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Zustandsänderungen Fläche unter der Kurve = mechanische Arbeit 56 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Wie groß ist die mechanische Arbeit (= Fläche zwischen Kurve und V-Achse?) V2 W12 p(V , T ) dV V1 Bei idealem Gas: n RT p V , T V 57 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Darstellung im p-VDiagramm (p über V): n Rm T p V ergibt eine Hyperbel für ein bestimmtes T Vergleiche const . y x 58 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Es gibt 4 fundamentale Zustandsänderungen A) Isotherme Zustandsänderung 59 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz: a) Innere Energie U: Mit T = const ist dT = 0 → dU = 0 → Mit dU = dQ + dW folgt: f dU n Rm dT 2 dQ = - dW 60 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz: b) Mechanische Arbeit: dW = - pdV V2 W12 pV dV V1 ergibt sich mit p (V ) n Rm T V V1 W12 n Rm T ln V2 Beachte: W12 > 0 da V1 > V2 61 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz: c) Wärme dQ = - dW → Q12 = - W12 Also V1 Q12 n Rm T ln V2 62 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger B) Isochore Zustandsänderung 63 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz: a) Innere Energie U: dU = n · Cv,m · dT U12 = U2 – U1 = n Cv,m (T2 – T1) 64 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz b) Mechanische Arbeit: Mit V = const ist dV = 0, also dW = - pdV = 0 → W12 = 0 65 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz c) Wärme Q Wegen dU = dQ + dW Und dW = 0 Ist dQ = dU = n · Cv,m · dT Q12 = n · Cv,m · (T2 – T1) 66 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger C) Isobare Zustandsänderung 67 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz a) Innere Energie U U12 = U2 – U1 = n · Cv,m · (T2 – T1) 68 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz b) Mechanische Arbeit W V2 W12 pV dV V1 Mit p = const folgt: W12 p V1 V2 0 69 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz c) Wärme Q Wegen dQ = dU - dW gilt: Q12 = n · Cv,m · (T2 – T1) + p (V2 – V1) und Q12 = n · Cp,m · (T2 – T1) 70 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Aus dem Vergleich: n · Cp,m · (T2 – T1) = n · Cv,m · (T2 – T1) + p (V2 – V1) folgt mit p(V2 – V1) = n Rm (T2 – T1): Cp,m = Cv,m + Rm 71 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger D) Adiabate Zustandsänderung 72 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz a) Innere Energie U: U12 = n · Cv,m · (T2 – T1) 73 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz b) Mechanische Arbeit W Adiabat heißt: Kein Wärmeübergang: dQ = 0, also dU = dW → W12 V2 p dV n C T v ,m 2 T1 V1 74 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz Mit Hilfe der Gleichung für ideale Gase findet man nach längerer Rechnung: 1 p1 V1 V1 W12 1 V2 1 75 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Bilanz c) Wärme Q Da dQ = 0 (adiabat!) folgt Q12 = 0 76 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Adiabate Zustandsänderung Weitere Ergebnisse (1) f Cv ,m Rm 2 f C p ,m 1 Rm 2 C p ,m 2 1 C v ,m f 77 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Adiabate Zustandsänderung Weitere Ergebnisse(2): Auf einer Adiabaten gilt : T V 1 const1 p V const 2 T 1 p const 3 78 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Polytrope Zustandsänderung: n p V const Isobare Isotherme Adiabate Isochore n=0 n=1 n= n=∞ 79 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Zusammenfassung: Isotherme ZÄ: U12 = 0 V1 W12 n Rm T ln V2 V1 Q12 n Rm T ln V2 80 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Zusammenfassung: Isochore ZÄ: U12 = U2 – U1 = n Cv,m (T2 – T1) W12 = 0 Q12 = n · Cv,m · (T2 – T1) 81 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Zusammenfassung: Isobare ZÄ: U12 = U2 – U1 = n · Cv,m · (T2 – T1) W12 p V1 V2 0 Q12 = n · Cv,m · (T2 – T1) + p (V2 – V1) und Q12 = n · Cp,m · (T2 – T1) Cp,m = Cv,m + Rm 82 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Zusammenfassung: Adiabate ZÄ: U12 = n · Cv,m · (T2 – T1) W12 V2 p dV n C T v ,m 2 T1 V1 1 p1 V1 V1 W12 1 1 V2 Q12 = 0 83 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Adiabate Zustandsänderung Weitere Ergebnisse(2): Auf einer Adiabaten gilt : T V 1 const1 p V const 2 T 1 p const 3 84 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Adiabate Zustandsänderung Weitere Ergebnisse (1) f Cv ,m Rm 2 f C p ,m 1 Rm 2 C p ,m 2 1 C v ,m f 85 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Lektion 5 Kreisprozesse 86 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Kreisprozesse Schema: Mechan. Arbeit a V2 W p V dV V1 Entspricht der Fläche unter der Kurve 87 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 88 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Rechtsläufiger Prozess → Wärmekraftmaschine (Motor) 89 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Wärme-Kraftmaschine Verbrennung Antrieb Kühler 90 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Wirkungsgrad Wärmekraftmaschine T1 W M 1 T2 91 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Linksläufiger Prozess → Wärmepumpe und Kühlschrank 92 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Kühlschrank Umgebung (Küche) Kompressor Kühlgut 93 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Wärmepumpe Wohnraum Pumpe Boden, Luft (außen) 94 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Leistungszahl ε a) Kühlschrank: b) Wärmepumpe: T1 T2 T1 T2 T2 T1 95 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Otto-Motor Otto-Motor 96 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Technisch wichtige Kreisprozesse Seiliger-Prozess 97 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Technisch wichtige Kreisprozesse Otto-Prozess 98 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Technisch wichtige Kreisprozesse Diesel-Prozess 99 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Technisch wichtige Kreisprozesse Stirling-Prozess 100 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Technisch wichtige Kreisprozesse Joule-Prozess 101 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Technisch wichtige Kreisprozesse Ericsson-Prozess 102 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Technisch-wichtige Kreisprozesse Clausius-Rankine-Prozess 103 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger • Technisch wichtige Kreisprozesse 104 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger Aufgabe 4: Kreisprozess 105 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 106 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 107 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 108 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 109 Verfahrens- und Umwelttechnik Prof. Dr. Freudenberger 110