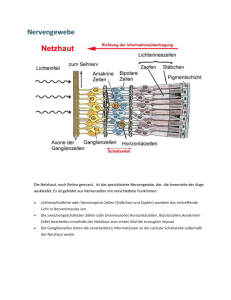
13 N e tzhaut und Glask örper
Werbung

178 Der Zentralvenenverschluss (ZVV) ist die zweithäufigste vaskuläre Erkrankung der Netzhaut nach der diabetischen Retinopathie. Netzhautblutungen sowie eine Erweiterung und vermehrte Schlängelung der Netzhautvenen zeigen sich in allen 4 Quadranten. Ätiologie/Pathogenese. Die arterielle Hypertonie ist die wichtigste prädisponierende Systemerkrankung. Diabetes mellitus, kardiovaskuläre Erkrankungen, Hyperviskositätssyndrome und ein erhöhter Augeninnendruck sind weitere Risikofaktoren. Histopathologisch zeigen sich Thrombosen innerhalb der Vena centralis retinae auf Höhe der Lamina cribrosa. Epidemiologie. Der ZVV zeigt sich gehäuft zwischen der 5. und 7. Lebensdekade. Klinik. Die Perfusion der Netzhaut bestimmt die Klinik des ZVV (s. unten). Nichtischämischer ZVV (venöse Stase- Retinopathie, nichthämorrhagischer ZVV, perfundierter ZVV, Aa u. b). Das kapilläre Nicht-Perfusionsareal der Netzhaut ist kleiner als 10 Papillenflächen. Die Visusminderung wird durch das Ödem oder Hämorrhagien in der Makula verursacht. Wenn die zentrale Sehschärfe bei der Erstpräsentation 0,5 oder besser ist, ist die Visusprognose bei über 67 % der Patienten günstig. Dennoch können bis zur 34 % der nichtischämischen ZVV innerhalb von 32 Monaten in einen ischämischen ZVV konvertieren. Ischämischer ZVV (hämorrhagischer ZVV, nichtperfundierter ZVV, Ac). Das kapilläre Nicht-Perfusionsareal ist größer als 10 Papillenflächen. Es finden sich ausgedehnte Netzhautblutungen, Cotton-Wool-Herde am Papillenrand und im Bereich des hinteren Pols. Eine ausgeprägte Papillenschwellung ist im akuten Stadium häufig. Ursachen für die Visusminderung sind Ödeme, Blutungen und eine Ischämie in der Makula, das Neovaskularisationsglaukom, die Glaskörperblutung und eine exsudative oder traktive Netzhautablösung. Zwei schwerwiegende Komplikationen eines ischämischen ZVV sind die Rubeosis iridis und das Neovaskularisationsglaukom. Diagnostik. Das klinische Bild ist für die Diagnose oft ausreichend. Die Fluoreszenzangiographie ermöglicht die Messung des Ischämieareals der Netzhaut, sodass die Einteilung des ZVV möglich wird. Afferente Pupillenstörung und die Elektroretinographie sind zusätzliche diagnostische Methoden zur Beurteilung der Netzhautischämie im akuten Stadium des ZVV. Therapie. Beobachten: Bei nichtischämischem ZVV ohne Makulaödem monatliche Kontrollen, um das Auftreten oder die Zunahme einer Netzhautischämie früh zu diagnostizieren. Neben der Ophthalmoskopie unbedingt Spaltlampenuntersuchung des vorderen Segments und Tonometrie, um die am meisten gefürchteten Komplikationen (Rubeosis iridis, Kammerwinkelneovaskularisation, Neovaskularisationsglaukom) rechtzeitig zu erkennen. Medikamentös: Die Regulierung eines erhöhten Blutdrucks und die Behandlung von Risikofaktoren wirken sich günstig auf die Prognose aus. Die Anwendung von Thrombozytenaggregationshemmern, isovolemische Hämodilution und systemische Kortikosteroidgabe finden unterschiedliche Akzeptanz. Laserfotokoagulation: Eine panretinale Laserfotokoagulation wird nach der „Central Retinal Vein Occlusion Study Group“ bei folgenden Befunden empfohlen: ● Netzhautischämie über 10 Papillenflächen, ● Neovaskularisationen der Netzhaut, ● Neovaskularisation der Iris über 2 Stunden, ● Kammerwinkelneovaskularisation. Chirurgisch: Radiäre Optikusneurotomie, intravitreale Kortisoninjektion. Diese neuen chirurgischen Verfahren sind bis jetzt nicht durch prospektive randomisierte Studien evaluiert worden. B. Venenastverschluss (VAV) Es finden sich Hämorrhagien und ein Ödem der Retina im Bereich der betroffenen Netzhautvenen (Ba). Die okkludierte Netzhautvene ist peripher der arteriovenösen Kreuzungsstelle dilatiert. Visusminderung und sektorielle Gesichtsfeldausfälle resultieren aus Hämorrhagien, Ödem oder Netzhautischämie (Bb, c). Bei perfundierter Makula mit Ödem ist die Gridlaserfotokoagulation indiziert. Eine sektorielle Laserkoagulation wird bei retinaler Neovaskularisation, einer Ischämie über 5 Papillenflächen oder bei Rubeosis iridis empfohlen. Dieses Dokument ist nur für den persönlichen Gebrauch bestimmt und darf in keiner Form an Dritte weitergegeben werden! Aus T. Schlote u.a.: Taschenatlas Augenheilkunde (ISBN 3-13-131481-8) © 2004 Georg Thieme Verlag, Stuttgart Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 13 Netzhaut und Glaskörper A. Zentralvenenverschluss (ZVV) a Venöse Stase-Retinopathie (nichtischämischer ZVV) a Frischer Verschluss der Vena temporalis inferior b Venöse Stase-Retinopathie nach 12 Monaten mit Rückgang der Hämorrhagien und des Ödems b Fluoreszenzangiographisch zeigt sich ein perfundiertes Makulaödem bei Verschluss der Vena temporalis superior c Ischämischer ZVV (hämorrhagischer ZVV) mit ausgeprägten Hämorrhagien und Ödem c Fluoreszenzangiographisch zeigt sich eine Netzhautischämie unterhalb der Makula bei Verschluss der Vena temporalis inferior 179 Dieses Dokument ist nur für den persönlichen Gebrauch bestimmt und darf in keiner Form an Dritte weitergegeben werden! Aus T. Schlote u.a.: Taschenatlas Augenheilkunde (ISBN 3-13-131481-8) © 2004 Georg Thieme Verlag, Stuttgart Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. B. Venenastverschluss (VAV) Vaskuläre Erkrankungen der Netzhaut A. Zentralvenenverschluss (ZVV) B. Arterienastverschluss (AAV) Der Zentralarterienverschluss wird durch die Okklusion der Arteria centralis retinae hervorgerufen. Leitsymptom ist die schmerzlose, plötzliche Sehminderung. Ätiologie/Pathogenese. Meist handelt es sich um einen Embolus oder Thrombus. Ein gelber Cholesterin-Embolus (Hollenhorst-Plaque) auf dem Sehnervkopf oder in einer Astarterie der Netzhaut sichert die Diagnose. Wichtigste Ursachen für die Embolien sind atherosklerotische Plaques der Karotisarterien, arterielle Hypertonie und Herzklappenfehler. Epidemiologie. Die Prävalenz des ZAV beträgt 0,85/100 000 der Bevölkerung in einem Jahr. Es ist eine Erkrankung des Erwachsenenalters (im Durchschnitt 6. Lebensdekade). Bilateraler Befall in 1–2 %, mit Ausnahme der Arteriitis temporalis und anderer systemischer Vaskulitiden. Klinik. Sichtbare Embolien in den NetzhautArterien und kirschroter Reflex (dunkelroter Foveareflex umgeben von weißlichem Netzhautödem am hinteren Pol, Aa, b) ist pathognomonisch für einen Zentralarterienverschluss der Netzhaut. Die Arterien sind dünn und der segmentierte Blutfluss in den Netzhautarterien kann in den akuten Stadien der Erkrankung beobachtet werden (Ac). Diagnose. Die Klinik (s. unten) und durch die Fluoreszenzangiographie kann die Diagnose gesichert werden. Diffenzialdiagnose. Die Differenzierung zwischen arteriitischen (Morbus Horton) und nichtarteriitischen ZAV ist sehr wichtig, weil beim Morbus Horton ohne entsprechende Therapie ein Befall des Partnerauges innerhalb weniger Tage eintreten kann. Therapie. Zurzeit besteht kein Konsens über die Effektivität verschiedener Behandlungsformen. ● Konservative Behandlung: Bulbusmassage, Vorderkammerparazentese, Infusionsbehandlung mit Pentoxifyllin, hyperbarer Sauerstoff, rheologische Maßnahmen, intravenöse rTPAoder Kortikosteroidinjektion. ● Invasive Behandlung: Selektive Katheterisation der Arteria ophthalmica mit Applikation fibrinolytischer Medikamente. Entsprechend der okkludierten Astarterie zeigt sich betont am hinteren Pol ein Netzhautödem (Ba). Die Patienten berichten über einen sektorförmigen Gesichtsfeldausfall. Der Abfall der zentralen Sehschärfe ist von der Perfusion der Fovea abhängig (Bb). Neben dem weißlichen Netzhautödem sind gelbliche intraarterielle Embolien und die Verengung der Arterien wichtige klinische Befunde. Eine internistische Abklärung kardiovaskulärer Risikofaktoren und eine konservative Therapie (s. ZAV) wird empfohlen. Die Prognose für das zentrale Sehvermögen ist gut. Gesichtsfeldausfälle können aber persistieren. C. Okuläres Ischämiesyndrom Hierbei handelt es sich um eine chronische Insuffizienz der Arteria ophthalmica, die zur Minderdurchblutung des gesamten Auges führt. Die häufigste Ursache ist dabei eine Karotisstenose. Die zentrale Sehschärfe ist in fortgeschrittenen Stadien reduziert. Klinisch zeigen sich verengte Netzhautarterien, punktund fleckförmige Blutungen in der Peripherie der Netzhaut. Dilatationen und Tortuositas der Netzhautvenen fehlen (Differenzialdiagnose venöse Stase-Retinopathie). Rubeosis iridis und Tyndalleffekt der Vorderkammer sind häufig. Die retinalen Neovaskularisationen entwickeln sich häufig nach der Rubeosis iridis. Die pathologisch verlängerte Arm-NetzhautFüllungszeit bei der Fluoreszenzangiographie ist pathognomonisch. Die Karotis-DopplerUntersuchung kann das Ausmaß der Stenose darstellen. Die betroffenen Patienten zeigen meistens ein hohes Risikoprofil bezüglich kardiovaskulärer Erkrankungen. Die Mortalität beträgt ca. 50 % innerhalb von 5 Jahren nach Diagnosestellung. Eine internistische Abklärung ist daher dringend zu empfehlen. Die panretinale Laserfotokoagulation wird bei ausgedehnten Netzhautischämien sowie bei Vorhandensein einer Rubeosis iridis und retinaler Neovaskularisationen durchgeführt. Prognose. Die Sehschärfe bei der Erstpräsentation entscheidet im Allgemeinen über die Prognose. Spontane Besserungen sind in bis zu 15 % zu beobachten. Dieses Dokument ist nur für den persönlichen Gebrauch bestimmt und darf in keiner Form an Dritte weitergegeben werden! Aus T. Schlote u.a.: Taschenatlas Augenheilkunde (ISBN 3-13-131481-8) © 2004 Georg Thieme Verlag, Stuttgart Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 13 Netzhaut und Glaskörper 180 A. Zentralarterienverschluss (ZAV) a ZAV mit Netzhautödem durch die Ischämie; umschriebene Netzhautperfusion temporal der Papille ist bedingt durch die patente A. zilioretinalis a AAV mit Netzhautödem entsprechend dem Versorgungsgebiet der A. temporalis superior; Netzhautblutung am Rand der Papille, Dilatation und Anschlängelung der Venen deutet auf kombinierten arteriovenösen Verschluss der Netzhaut hin b ZAV mit kirschrotem Fleck in der Fovea b Die Fluoreszenzangiographie zeigt die Nichtperfusion der Netzhaut c Die Fluoreszenzangiographie mit nichtperfundiertem Areal der Netzhaut und segmentiertem Blutfluss 181 Dieses Dokument ist nur für den persönlichen Gebrauch bestimmt und darf in keiner Form an Dritte weitergegeben werden! Aus T. Schlote u.a.: Taschenatlas Augenheilkunde (ISBN 3-13-131481-8) © 2004 Georg Thieme Verlag, Stuttgart Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. B. Arterienastverschluss (AAV) Vaskuläre Erkrankungen der Netzhaut A. Zentralarterienverschluss (ZAV) Runde Dilatationen der retinalen Arteriolen innerhalb der ersten arteriolaren Bifurkation werden als erworbene arterielle Makroaneurysmen bezeichnet. Arterielle Hypertonie und Atherosklerose sind die wichtigsten Ursachen. In der Regel ist der Befall einseitig und bei Frauen häufiger. Eine Visusminderung oder ein Gesichtsfeldausfall tritt auf, wenn eine Leckage oder Hämorrhagie im Bereich der Makula auftritt. Hämorrhagien können in unterschiedlichen Schichten der Netzhaut und im Glaskörperraum auftreten. Subpigmentepitheliale Hämorrhagien zeigen sich als dunkelrote Läsionen und erfordern die differenzialdiagnostische Abgrenzung zu pigmentierten Aderhauttumoren. Finden sich multiple Makroaneurysmen, Entzündungszellen im Glaskörper oder Kollateralgefäße, ist die präzise Diagnosestellung von Bedeutung, weil die Prognose und die Behandlung der arteriellen Makroaneurysma unterschiedlich sein kann (s. Morbus Coats, Venenastverschluss). Mittels IndocyaningrünAngiographie können arterielle Makroaneurysmata oft trotz epiretinaler Hämorrhagien dargestellt werden. Die Hämorrhagien sind fast immer reversibel. Besteht eine Visusminderung nach der Resorption der Hämorrhagien empfiehlt sich eine Fluoreszenzangiographie zur Darstellung einer Leckage des Makroaneurysmas. Eine Laserfotokoagulation des Makroaneurysmas kann dann zur Zurückbildung der Leckage führen. B. Morbus Coats 182 Der Morbus Coats ist eine kongenitale retinale Gefäßerkrankung, die durch retinale Teleangiektasien, Mikroaneurysmen und kapilläre Minderperfusionsareale in der Peripherie der Netzhaut charakterisiert ist. Leber-Miliaraneurysmen und gewisse Formen der idiopathischen juxtafovealen Teleangiektasien werden als Varianten des Morbus Coats angesehen. Histopathologisch zeigt sich ein Verlust an Endothelzellen und Perizyten der retinalen Gefäßwände. Das männliche Geschlecht wird bevorzugt befallen. 80 % der Manifestationen sind unilateral. Die Erkrankung tritt gehäuft in der ersten und fünften Lebensdekade auf. Periphere retinale Gefäßanomalien verursachen eine Leckage, die sich in fortgeschrittenem Stadium am hinteren Pol als Makulaödem und subretinale Lipidablagerungen präsentiert (Ba, b). Der Morbus Coats ist eine chronische, langsam fortschreitende Erkrankung. I. d. R. wird die Diagnose durch die Exsudation am hinteren Pol gestellt. Komplikationen sind Netzhautablösung, vasoproliferativer Tumor der Netzhaut, Katarakt, Glaukom und Phthisis bulbi. Die Diagnose wird durch die Klinik, demographische Auffälligkeiten (Geschlecht, Alter) und die fluoreszenzangiographischen Befunde in der Netzhautperipherie gestellt (Bc). Diffenzialdiagnostisch kommen im Kindesalter andere Ursachen der Leukokorie und im Erwachsenenalter periphere retinale Vaskulopathien in Betracht. Die Therapie des Morbus Coats basiert auf der Destruktion der avaskulären Netzhautareale und leckenden Mikroaneurysmen. Therapie der Wahl ist die Laserfotokoagulation. Bei Versagen der Lasertherapie, Lage der Läsionen in der extremen Peripherie der Netzhaut oder bei Zunahme der subretinaler Exsudationen wird die Kryotherapie angewendet. Im fortgeschrittenen Stadium des Morbus Coats (exsudative Netzhautablösung, vasoproliferative Tumorbildung) kommen auch vitreoretinale Verfahren in Frage. C. Fundus hypertonicus Die chronische arterielle Hypertonie führt zu einer Verengung retinaler Arteriolen und zu einer Störung der inneren Blut-Retina-Schranke. Als Folge entwickeln sich Exsudationen, Blutungen, Cotton-Wool-Herde, Lipidablagerungen mit Bevorzugung des hinteren Pols der Netzhaut. Stadien des Fundus hypertonicus (nach Scheie) sind: Stadium 0: Normaler Netzhautbefund. Stadium I: Diffuse arteriolare Verengung. Keine Kaliberschwankungen der Arteriolen. Stadium II: Ausgeprägte arterioläre Verengung mit zusätzlichen fokalen Konstriktionen (Ca). Stadium III: Ausgeprägte diffuse und fokale arteriolare Verengungen mit retinalen Hämorrhagien. Stadium IV: Zusätzlich zu den genannten Befunden zeigen sich ein retinales Ödem, harte Exsudate und eine Papillenschwellung (Cb). Dieses Dokument ist nur für den persönlichen Gebrauch bestimmt und darf in keiner Form an Dritte weitergegeben werden! Aus T. Schlote u.a.: Taschenatlas Augenheilkunde (ISBN 3-13-131481-8) © 2004 Georg Thieme Verlag, Stuttgart Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 13 Netzhaut und Glaskörper A. Arterielles Makroaneurysma Arterielles Makroaneurysma im Verlauf der A. temporalis superior; es zeigen sich retinale, subretinale und subpigmentepitheliale Hämorrhagien a Makulaödem mit Lipidablagerungen verursacht durch arterielles Mikroaneurysma b Submakulärer Cholesterinplaque bei Morbus Coats c Fluoreszenzangiographie bei Morbus Coats: retinale Teleangiektasien, Mikroaneurysmen, Kapillarabbrüche mit Leckage in der Peripherie C. Fundus hypertonicus 183 a Fundus hypertonicus Stadium II b Fundus hypertonicus Stadium IV mit Papillenödem und Makulastar Dieses Dokument ist nur für den persönlichen Gebrauch bestimmt und darf in keiner Form an Dritte weitergegeben werden! Aus T. Schlote u.a.: Taschenatlas Augenheilkunde (ISBN 3-13-131481-8) © 2004 Georg Thieme Verlag, Stuttgart Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. B. Morbus Coats Vaskuläre Erkrankungen der Netzhaut A. Arterielles Makroaneurysma