Regulatorische Netzwerke bei der Embryonalentwicklung der Säuger
Werbung

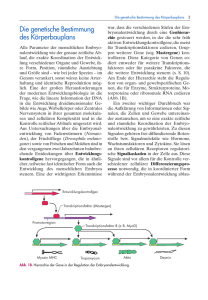
Herrmann, Bernhard G. | Regulatorische Netzwerke bei der Embryonalentwicklung der ... Tätigkeitsbericht 2004 Entwicklungs- und Evolutionsbiologie/Genetik Regulatorische Netzwerke bei der Embryonalentwicklung der Säuger Herrmann, Bernhard G. Max-Planck-Institut für molekulare Genetik, Berlin Korrespondierender Autor: Herrmann, Bernhard G. E-Mail: [email protected] Zusammenfassung Die Entwicklung der Körperanlage mit ihren Organen wird durch eine Vielzahl komplexer Regelmechanismen gesteuert, die einem streng kontrollierten Ablauf folgen. Am Anfang dieser Ereigneisse steht die Mesenchymbildung, ein Vorgang, der Ähnlichkeiten zur Metastasierung von Tumoren aufweist. Mithilfe neuer Verfahren sollen regulatorische Netzwerke aufgedeckt werden, die Mesenchymbildung und Gewebedifferenzierung kontrollieren. Abstract The development of the body anlage with its organs is controlled by a multitude of complex regulatory mechanisms which follow a strict order. On top of these processes is the formation of mesenchyme, an event with similarities to metastasis formation of tumors. Novel methods are utilized to unravel regulatory networks controlling mesenchyme formation and tissue differentiation. Die Entwicklung eines Embryos beginnt mit der Verschmelzung von Eizelle und Spermium. Der einzellige Embryo fängt an, sich zu teilen und bildet einen Zellhaufen. Damit jedoch ein überlebensfähiger Organismus heranwachsen kann, müssen sich die neuen Zellen in unterschiedlicher Weise entwickeln und innerhalb des entstehenden Körpers organisieren. Dies basiert auf einer Vielzahl komplexer Prozesse, die einem räumlich und zeitlich streng kontrollierten Ablauf folgen. Ein wichtiger Schritt bei der Entstehung des neuen Organismus ist die Bildung der embryonalen Rumpfanlage. Sie entsteht aus einem mehrschichtigen primitiven Epithel aus pluripotenten, sich teilenden Stammzellen. Unter dem Einfluss verschiedener Signalmoleküle (Wnt/β-Catenin, FGF oder TGFβ1/BMP) wird ein Teil der Zellen angeregt (induziert), sich aus dem Zellverband zu lösen und mesenchymale Eigenschaften anzunehmen, d.h., sie verlieren ihre abgerundete, epitheliale Form, werden beweglich und in die Lage versetzt, sich zu unterschiedlichen Zelltypen zu entwickeln (differenzieren). Auch die Differenzierung der mesenchymalen Zellen wird durch die Art der Signalmoleküle bestimmt, die auf sie einwirken. Einige entwickeln sich zu paraxialen Zellen, die später u.a. Wirbelsäule und Muskulatur von Skelett und Extremitäten bilden. Aus anderen entstehen z. B. Nieren und Gonaden, wieder andere bilden Bauchdecke, Bauchfell und Bauchmuskulatur. Aus den im ursprünglichen Epithelverband zurückbleibenden Zellen entstehen die Oberhaut und das Rückenmark. © 2004 Max-Planck-Gesellschaft www.mpg.de 2531 Tätigkeitsbericht 2004 Herrmann, Bernhard G. | Regulatorische Netzwerke bei der Embryonalentwicklung der ... Abb. 1 : Epithelial-mesenchymale Transition (EMT) bei der Bildung der Körperanlage. Unter dem Einfluss von Signalmolekülen werden proliferierende epitheliale Stammzellen angeregt, Mesenchym zu bilden, nach festgelegten Mustern zu differenzieren und Gewebe und Organe zu bilden. Tumore entstehen häufig durch unkontrolliertes Wachstum einzelner Epithelzellen, in denen die gleichen Signalwege konstitutiv aktiviert wurden. Aus solchen epithelialen Tumoren können sich einzelne Zellen durch EMT lösen und an anderer Stelle im Körper Metastasen bilden. Dabei sind häufig wiederum die gleichen Genprodukte beteilt, wie bei der EMT im Embryo. Bild : Bernhard G. Herrmann, MPIMG Das Interesse der Abteilung Entwicklungsgenetik am Max-Planck-Institut für molekulare Genetik gilt der Regulation der frühen Ereignisse bei der Rumpfbildung. Zurzeit ist noch ungeklärt, wie das Umschalten der epithelialen Stammzellen vom Zellteilungs- in ein Differenzierungsprogramm kontrolliert wird. Auch die Gestaltänderung vom epithelialen zum mesenchymalen, motilen Zelltyp ist molekular nur ansatzweise bekannt, ebenso sind die Grundlagen für die Steuerung unterschiedlicher Differenzierungsprogramme und der Übertragung von Positionsinformation auf die Zellen zu klären. Alle diese Prozesse finden gleichzeitig statt und werden von ein paar wenigen Signalkaskaden gesteuert. 2254 www.mpg.de © 2004 Max-Planck-Gesellschaft Herrmann, Bernhard G. | Regulatorische Netzwerke bei der Embryonalentwicklung der ... Tätigkeitsbericht 2004 Epithelial-mesenchymale Transition im Embryo versus Tumor Wie beschrieben, wird der Übergang vom epithelialen in den mesenchymalen Zustand bei der Bildung der Rumpfanlage durch verschiedene Signalmoleküle gesteuert. Diese aktivieren die Wnt/β-Catenin, FGF- und TGFβ1/BMP-Signalketten. Ein wichtiges Zielgen dieser Signalwege ist Brachyury, ein T-BoxTranskriptionsfaktor. Außerdem ist das Produkt des Snail-Gens beteiligt, welches als Transkriptionsrepressor agiert. Snail unterdrückt die Expression (Bildung) von E-Cadherin, einem Zelladhäsionsprotein, das wesentlich an der Aufrechterhaltung der epithelialen Struktur vieler Zellverbände beteiligt ist. Die Unterdrückung von E-Cadherin durch Snail spielt daher eine wichtige Rolle bei der Bildung von Mesenchym aus epithelialen Zellverbänden. Die Rolle von Brachyury bei diesem Prozess ist nur zum Teil verstanden, eine Beteiligung an der Kontrolle von Snail gilt als wahrscheinlich. Die Identifizierung der Zielgene beider Regulatoren wird wesentlich zum Verständnis der epithelial-mesenchymalen Transition (EMT) beitragen. Über das Verständnis der embryonalen Vorgänge hinaus erwarten die Wissenschaftler von diesen Untersuchungen wichtige Hinweise über die Entstehung und Metastasierung von Tumoren epithelialen Ursprungs. Tumore entstehen durch unkontrolliertes Wachstum, das bedeutet, Zellen gehen aus einem differenzierten, ruhenden Zustand in einen wachsenden (proliferierenden) Zustand über. Die gleichen Signalketten, welche die Mesenchymbildung im Embryo regulieren, sind auch bei vielen Tumoren konstitutiv aktiv. Es besteht also eine deutliche molekulare Verbindung zwischen beiden Prozessen. Die Verbreitung von Tumoren im Organismus (Metastasierung) weist ebenfalls Gemeinsamkeiten mit den Vorgängen während der Embryonalentwicklung auf. Metastasen entstehen durch das Herauslösen weniger Zellen aus einem epithelialen Tumor. Die Zellen verbreiten sich über Blut- oder Lymphsystem im Körper, siedeln sich an anderen Stellen neu an und bilden neue Tumore. Das Herauslösen von Zellen aus einem Tumor kann von Genen gesteuert werden, die auch bei der Mesenchymbildung im Embryo wesentliche Bedeutung haben, wie z.B. Snail. Da dieser Prozess im Patienten kaum untersucht werden kann, soll der Mausembryo als In-vivo-Modell zur Untersuchung der Metastasierung dienen. Die Segmentierung der Rumpfanlage, Voraussetzung für die Bildung der Wirbelsäule Wie erwähnt, legt bereits die Qualität der Signale bei der Induktion von Mesenchym während der Rumpfbildung den weiteren Differenzierungsweg der Zellen fest. Aus den Zellen, die beiderseits des Neuralrohrs, des späteren Rückenmarks, zu liegen kommen, entstehen die Vorläufer der Wirbelsäule. Dazu müssen die zunächst in zwei Strängen vorliegenden Zellen segmental unterteilt werden. In regelmäßiger periodischer Abfolge entlang der Längsachse des Körpers entstehen die Somiten, epitheliale, fast kugelförmige Strukturen mit anterior-posteriorer und dorso-ventraler Polarität. Aus der hinteren Hälfte eines und der vorderen Hälfte des dahinterliegenden Somitenpaares geht jeweils ein Wirbel hervor. Dazu wird nur der ventrale Anteil der Somiten, das so genannte Sklerotom verwendet. Aus dem dorsalen Teil entstehen Muskeln und Unterhaut. Die Entstehung der Somiten wird durch das Zusammenspiel eines Oszillators (oder Segmentationsuhr) und eines Gradienten kontrolliert. Der Oszillator besteht aus zwei miteinander gekoppelten Signalkaskaden (Wnt- und Notch-Signalketten). Sie werden durch negative Rückkopplungsmechanismen und schnellen Zerfall zentraler Steuerungskomponenten einmal pro Segmentationszyklus (alle 90 - 120 Minuten) aktiviert und inaktiviert. Da die Zielgene der Signalwege dem Aktivierungs- / Inaktivierungsrhythmus entsprechend "an- und ausgeschaltet" werden, entsteht in regelmäßigen Abständen eine Grenzfläche zwischen den Zellen, in denen der Oszillator aktiv ist, und © 2004 Max-Planck-Gesellschaft www.mpg.de 2553 Tätigkeitsbericht 2004 Herrmann, Bernhard G. | Regulatorische Netzwerke bei der Embryonalentwicklung der ... denen, in denen der Oszillator bereits abgeschaltet ist. An dieser Stelle wird eine Segmentgrenze induziert. Die Aktivität des Oszillators ist von einem Signalmolekül (Wnt3a) abhängig. Dieses wird am kaudalen Ende des Embryo gebildet und schwindet mit der Zeit in den präsomitischen Zellen, während sich gleichzeitig die Signalquelle durch kaudales Wachstum von den gebildeten Zellen entfernt. Der entstehende Konzentrationsabfall im "Gewebefeld" wird als Gradient bezeichnet. Während eines Segmentationszyklus "wandert" der Schwellenwert des Wnt3a-Signals in Richtung des kaudalen Embryoendes. Der Abstand zwischen Segmentgrenzen wird also durch die Dauer eines Segmentationszyklus und die Zerfallsgeschwindigkeit des Wnt3a-Signals bestimmt. Abb. 2 : 9,5 Tage alter Mausembryo: Kopf und Rumpf sind bereits angelegt, der Schwanz wird aus der Schwanzknospe (SK) durch kaudale Verlängerung (Pfeil) gebildet. Die Segmentation ist anhand der Somiten erkennbar (Pfeile); das präsomitische Mesoderm (PSM) am kaudalen Ende des Embryo zeigt an, dass der lumbosakrale Bereich des Rumpfes noch nicht vollständig segmentiert ist. Bild : Bernhard G. Herrmann, MPIMG - 4256 www.mpg.de © 2004 Max-Planck-Gesellschaft Herrmann, Bernhard G. | Regulatorische Netzwerke bei der Embryonalentwicklung der ... Tätigkeitsbericht 2004 Werkzeuge zur Erforschung regulatorischer Netzwerke der Embryonalentwicklung 1) Die Sichtbarmachung der Genaktivität im Embryo Gene, die maßgeblich an regulatorischen Netzwerken beteiligt sind und wichtige Vorgänge bei der Embryonalentwicklung steuern, können durch verschiedene Ansätze identifiziert werden. Als Hauptansatz der Abteilung Entwicklungsgenetik wurde die Genexpressionsanalyse gewählt. Regulatorische Gene sind sehr oft gewebespezifisch exprimiert, werden also nur in bestimmten Zellgruppen oder Organanlagen aktiv. Die restriktive Expression ergibt ein spezifisches Muster, das durch so genannte In-situ-Hybridisierung dargestellt werden kann. Dabei wird die Boten-RNA, die von einem aktivierten Gen abgeschrieben wird, im Embryo sichtbar gemacht. Durch Expressionsanalyse tausender, idealerweise aller Gene im Genom lässt sich die Anatomie des Embryos auf molekularer Ebene widerspiegeln. So kann die Beteiligung der meisten Gene, die maßgeblich an der Kontrolle der Embryonalentwicklung beteiligt sind, dargestellt werden. Aus den Daten können Gengruppen erstellt werden, die an Teilprozessen wie Musterbildung, Gewebedifferenzierung oder Organbildung beteiligt sind und in regulatorische Netzwerke eingeflochten werden. Durch Hochdurchsatzverfahren, die im Labor der Abteilung entwickelt wurden, konnten etwa 10.000 Mausgene auf Aktivität im Embryo geprüft werden. Sie stehen jetzt unmittelbar für eine Vielzahl funktioneller Untersuchungen zur Verfügung (siehe unten). Unter anderem hat die Abteilung die Mausorthologen der Gene, die sich auf dem Chromosom 21 des Menschen befinden, untersucht. Patienten, die das Chromosom 21 in dreifacher Form tragen (Trisomie 21), entwickeln das Down-Dyndrom. Es ist durch eine Vielzahl von Fehlbildungen und Prädispositionen für Krankheiten gekennzeichnet. Durch Expressionsanalyse der Chromosom 21-Gene in der Maus (Kooperation mit Dr. Yaspo, Abt. Lehrach) konnten eine Reihe von Genen identifiziert werden, die möglicherweise ursächlich mit der Pathogenese des Down-Syndrom in Beziehung stehen. Diese Kandidatengene werden nun gezielt weiteren Funktionsanalysen unterzogen. 2) Promoteranalysen - in silico und in vivo Die Ergründung regulatorischer Netzwerke bei Teilprozessen der Embryonalentwicklung setzt voraus, dass zumindest ein wesentlicher Teil der daran beteiligten Gene bekannt ist. In dem hier beschriebenen Ansatz dient die Expressionsanalyse embryonal exprimierter Gene, aus denen an Teilprozessen beteiligte Gengruppen erstellt werden, als Grundlage für die Analysen. Mitglieder von Gengruppen stehen in einer hierarchischen Beziehung zueinander. Sie können zunächst in regulatorische Gene und potenzielle Zielgene eingeteilt werden. Dies kann mithilfe von bereits bekannten biochemischen Eigenschaften vieler Genfamilien geschehen. Regulator/Zielgen-Beziehungen können mit bioinformatischen Programmen (Kooperation mit Abt. Vingron) untersucht werden, mit denen Promotersequenzen, also regulatorische Gensequenzen, auf Bindungsstellen für regulatorische Proteine durchsucht werden. Diese bioinformatischen Werkzeuge werden zurzeit noch erprobt. Durch In-silico-Verfahren vorhergesagte Netzwerke müssen durch funktionelle Analysen in vivo verifiziert werden. Dazu werden sowohl Reportergenkonstrukte auf Aktivität der regulatorischen Gensequenzen - wildtyp bzw. in einzelnen Bindestellen mutiert - im Embryo getestet, als auch Gensubgruppen auf Abhängigkeit von bestimmten regulatorischen Proteinen untersucht. Für letztgenannte Untersuchungen ist die Entfernung der betreffenden Regulatoren durch Mutagenese nötig. 3) Mutagenese durch RNA-Interferenz Technologie Die Funktion einzelner Gene in biologischen Prozessen kann nur durch Mutagenese-Verfahren ergründet werden. Dabei wird z.B. untersucht, wie sich der Verlust eines Gens auf den gesamten Organismus auswirkt. Die Entfernung einzelner Genfunktionen aus dem Gesamtorganismus mittels so genannter © 2004 Max-Planck-Gesellschaft www.mpg.de 2575 Tätigkeitsbericht 2004 Herrmann, Bernhard G. | Regulatorische Netzwerke bei der Embryonalentwicklung der ... "Knock-out"-Mutagenese in der Maus ist aufwändig und langwierig. Vor kurzem wurden jedoch neue Verfahren entdeckt, mit deren Hilfe die Boten-RNA, die von einem aktiven Gen abgeschrieben wird, selektiv zerstört werden kann. Auf diese Art ist es möglich, die Gesamtzeit der Analyse einzelner Gene von mehreren Monaten auf wenige Wochen zu verkürzen. Das Verfahren wird gegenwärtig für die Anwendung an Mäusen und Mausembryonen etabliert und getestet. Abb. 3 : Genaktivität im 9,5 Tage alten Mausembryo: Die Boten-RNA einzelner Gene wurde durch das In- situHybridisierungsverfahren sichtbar gemacht. Die Hauptexpressionsorte sind: A) Schwanzknospe und Chorda dorsalis, B) präsomitisches Mesoderm und Neuralrohr einschließlich Gehirn, C) die posterioren Hälften der Somiten, D) der skelettbildende Anteil der Somiten und drüsenbildende Teile des Vorderdarms, E) der muskelbildende Anteil der Somiten und das Herz, F) das Herz, G) Blutgefäße, H) Blutzellen, I) Hinterhirn und Rumpf, K) Neuralleistenzellen, L) Zellen des zentralen und peripheren Nervensystems, M) der dorsale Anteil von Hinterhirn und Rückenmark, N) die Anlagen der vorderen Gliedmaßen, O) die Urogenitalleisten (Anlagen für Nieren und Gonaden) und Septum transversum (Epicard), P) Mesothelium (Vorläufer von Bauchfell, Zwerchfell, Herzbeutel etc.), Q) Darm und Ohrbläschen. Bild : Neidhardt et al (2000), Mech Dev 98(1-2):77-94 6258 www.mpg.de © 2004 Max-Planck-Gesellschaft