Die genetische Bestimmung des Körperbauplans
Werbung

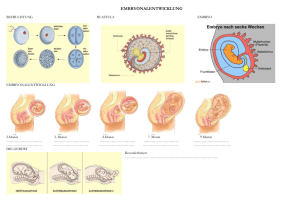
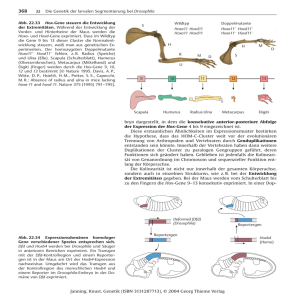
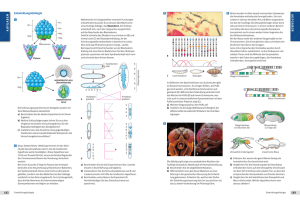
Die genetische Bestimmung des Körperbauplans Die genetische Bestimmung des Körperbauplans Alle Parameter der menschlichen Embryonalentwicklung wie der genaue zeitliche Ablauf, die exakte Koordination der Entwicklung verschiedener Organe und Gewebe, ihre Form, Position, räumliche Ausrichtung und Größe sind – wie bei jeder Spezies – im Genom verankert, sonst wären keine Arterhaltung und identische Reproduktion möglich. Eine der großen Herausforderungen der modernen Entwicklungsbiologie ist die Frage, wie die lineare Information der DNA in die Entwicklung dreidimensionaler Gebilde wie Auge, Wirbelkörper oder Zentrales Nervensystem in ihrer gesamten molekularen und zellulären Komplexität und in die Kontrolle zeitlicher Abläufe umgesetzt wird. Aus Untersuchungen über die Embryonalentwicklung von Fadenwürmern (Nematoden), der Fruchtfliege (Drosophila melanogaster) sowie von Fröschen und Molchen sind in den vergangenen zwei Jahrzehnten bahnbrechende Entdeckungen über Entwicklungskontrollgene hervorgegangen, die in ähnlicher, teilweise fast identischer Form auch die Entwicklung des menschlichen Embryos steuern. Eine der wichtigsten Erkenntnisse war, dass die verschiedenen Stufen der Embryonalentwicklung durch eine Genhierarchie gesteuert werden, in der die sehr früh aktiven Entwicklungskontrollgene, die meist für Transkriptionsfaktoren codieren, Gruppen weiterer Gene (sog. Mastergene) kontrollieren. Diese Kategorie von Genen codiert entweder für weitere Transkriptionsfaktoren oder für parakrine Faktoren, die die weitere Entwicklung steuern (s. S. 10). Am Ende der Hierarchie steht die Regulation von organ- und gewebspezifischen Genen, die für Enzyme, Strukturproteine, Motorproteine oder ribosomale RNA codieren (Abb. 1B). Ein zweiter wichtiger Durchbruch war die Aufklärung von Informationen oder Signalen, die Zellen und Gewebe untereinander austauschen, um so eine exakte zeitliche und räumliche Koordination der Embryonalentwicklung zu gewährleisten. Zu diesen Signalen gehören frei diffundierende Botenstoffe bzw. Signalmoleküle wie Hormone, Wachstumsfaktoren und Zytokine. Sie lösen an ihren zellulären Rezeptoren regulatorische Signalkaskaden in der Zelle aus. Diese Signale sind vor allem für die Kontrolle verschiedener zellulärer Differenzierungsprozesse notwendig, die in koordinierter Form während der Embryonalentwicklung ablau- Entwicklungskontrollgen Transkriptionsfaktor (Mastergen) Promotorregion Myosin MHC Transkriptionsfaktor B (z. B. MyoD) Tropomyosin 3 Aktin Abb. 1B. Hierarchie der Gene in der Regulation der Embryonalentwicklung. Desmin 4 Einleitung fen müssen. Das Gleiche gilt für stationäre Signale, die von Zelloberflächenmolekülen und extrazellulären Matrixmolekülen ausgehen und ebenfalls über spezifische Rezeptoren von benachbarten Zellen erkannt und verarbeitet werden. Obwohl wir noch weit davon entfernt sind, die gesamte Regulationskette während der Entwicklung auch nur eines Organs auf molekularer und zellulärer Ebene lückenlos zu verstehen, gibt es für bestimmte Schlüsselprozesse der Embryonalentwicklung doch schon sehr genaue Modelle, von denen hier exemplarisch einige vorgestellt werden sollen. Ziel ist es, die Wirkungsweise von Entwicklungskontrollgenen, die von ihnen codierten Transkriptionsfaktoren und die spezifischen Funktionen von Wachstumsfaktoren sowie andere extrazelluläre Signale zu entschlüsseln. Dieses Wissen wird unser Verständnis der komplexen morphologischen Veränderungen und Differenzierungsprozesse während der Embryonalentwicklung erleichtern und es uns schließlich ermöglichen, genetisch bedingte Fehlbildungen und andere Erbkrankheiten besser zu verstehen. Hox-Gene bestimmen den Körperbauplan von Insekten und Wirbeltieren Die genetische Analyse von DrosophilaMutanten mit einem extra Beinpaar am Kopf anstelle von Fühlern (Antennapedia) oder einer Mutante mit zwei Paar Flügeln anstelle von einem Paar Flügel und einem Paar Halteren (Bithorax) hat mit zu der bahnbrechenden Entdeckung der homöotischen Gene (Hox-Gene) beigetragen. Sie sind nicht nur für die spezifischen Merkmale der Körpersegmente von Insekten, sondern auch für die von Wirbeltieren verantwortlich. Das Ungewöhnliche an den homöotischen Genen ist, dass sie in der Reihenfolge auf dem Chromosom aneinandergereiht sind, die der Reihenfolge ihrer Expression in den aufeinanderfolgenden Körpersegmenten entspricht, also z. B. den Wirbeln bei den Vertebraten (Abb. 1C). Das bedeutet, dass Hox-Gene, die in terminalen Körpersegmenten exprimiert sind, auch am Ende dieser Gengruppe auf dem Chromosom liegen. Das Neue daran ist auch, dass sich diese Gene, die für Transkriptionsfaktoren codieren, in einer hierarchischen Reihenfolge gegenseitig regulieren. Das hat zur Folge, dass bei Ausfall eines Hox-Gens (z. B. durch Mutation) die benachbarten Hox-Gene auch ausfallen oder geringer aktiviert werden, so dass die betreffenden Körpersegmente die Merkmale eines anderen Segments annehmen können. So führt z. B. die Mutation im HoxGen Ubx bei Drosophila zum Austausch des thorakalen Segments T3 (Merkmal: Stummelflügel oder Haltere) durch T2 (Merkmal: Flügel). Ebenso kann man z. B. in der Maus durch Überexpression des Hox-b3-Gens ein 14. Paar Rippen induzieren. Dieses 14. Paar ist eine Verdoppelung von Paar 13 und kommt durch eine Umwandlung des Lendenwirbels L1 in einen Thorakalwirbel (T14) zustande. Solche Umwandlungen werden homöotische Transformationen genannt. Viele Polysyndaktylien (sechs und mehr Finger) entstehen nicht durch Bildung eines neuen, andersartigen Fingers, sondern durch Verdoppelung eines der fünf Finger. Sie sind auf Mutationen in den Hox-d(9–13)-Genen zurückzuführen, die für die unterschiedlichen Merkmale der fünf Finger bzw. Zehen verantwortlich sind. Im Laufe der Evolution haben sich die zehn Hox-Gene von Drosophila, die auf einem Chromosom liegen, beim Menschen zu vier Hox-Clustern mit je 9–11 Hox-Genen pro Cluster vervielfacht, die jedoch untereinander homolog sind (Abb. 1C). Wie bei Drosophila, sind die am 3’-Ende gelegenen Gene für die anterioren (Kopf-)Segmente verantwortlich, während die am 5’-Ende gelegenen Gene die spezifischen Merkmale der kaudalen Körpersegmente und der Finger bzw. Zehen festlegen. Wie aus Abb. 1D c5 b5 a5 scr c6 b6 a6 ftz b7 a7 Antp d8 c8 b8 Ubx d9 c9 b9 a9 d10 c10 a10 Abda c12 c13 b13 a13 5’ d11 d12 d13 c11 a11 Abdb Posterior Mensch Drosophila Abb. 1C. Hox-Gene bestimmen den Körperbauplan. In der Fruchtfliege Drosophila melanogaster wurden als Erstes die Hox-Gene entdeckt, die in einem Cluster auf einem Chromosom in der gleichen Reihenfolge (von 3‘ nach 5‘) angeordnet sind, in der sie von anterior nach posterior – von den Kopfsegmenten zu den Abdominalsegmenten – exprimiert sind. In den Vertebraten gibt es vier homologe Hox-Cluster auf vier verschiedenen Chromosomen, die in ihrer Gesamtheit die Identität der Körpersegmente (Wirbel, Neuralrohr- und Gehirnsegmente, Glieder der Extremitäten) festlegen. Hox-Gene regulieren sich gegenseitig in einer hierarchischen Reihenfolge von 3‘ nach 5‘ (modifiziert nach B. Alberts et al., 2002). Paraloge Gruppen d3 b4 d4 d1 b3 a4 Dfd Hox-d Chrom. 2 b2 a3 bcd c4 b1 Hox-b Chrom. 11 a2 pb Hox-c Chrom. 15 a1 lab Anterior Hox-a Chrom. 6 3’ Wirbelsäule Neuralrohr Die genetische Bestimmung des Körperbauplans 5