Onkologische Welt 3/2011 Kapitel: Neuro
Werbung

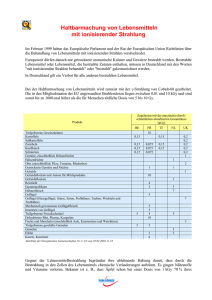
Kongressnachlese DGNC 2011 120 Trends in der Behandlung von Gliompatienten Biomarker geben die Richtung an „Wenn man die letzten 25 Jahre unseres Faches Revue passieren lässt, hat sich in der jüngsten Vergangenheit gerade auf dem Gebiet der Hirntumorerkrankungen die rascheste Entwicklung vollzogen“, meinte Prof. Jörg-Christian Tonn, München, auf der 62. Jahrestagung der Deutschen Gesellschaft für Neurochirurgie (DGNC). Hier sind Gliome besonders interessante „Targets“ für die Tumorforschung, weil sie sich aufgrund ihrer molekularen Eigenheiten als „Modell“ für grundlegende Mechanismen des Tumorwachstums eignen. Tonns besonderes Interesse gilt den Gliomen. Denn diese vom Nervenstützgewebe ausgehenden Tumore sind nicht nur die häufigsten primären Neoplasien im Gehirn, sondern weisen auch ein breites Malignitätsspektrum auf – von den kurablen/selten progressiven pilozytischen Astrozytomen (WHO-Grad 1) bis zu den hochaggressiven Glioblastomen (WHO-Grad IV) mit einer mittleren Überlebenswahrscheinlichkeit von 15 Monaten. moren, betonte Tonn. Das helfe dabei, besser zu verstehen, warum von zwei Patienten mit gleichem Tumor, gleicher Operation und gleicher Histologie der eine nach 12 Monaten stirbt und der andere nach 3 Jahren noch lebt. Fortschritte bei Bildgebung und der Neurochirurgie Im interdisziplinären Verbund von Grundlagenforschern, Neuropathologen und Klinikern konnten an großen Serien Gene identifiziert werden, die eine Vorhersage zum Krankheitsverlauf oder zum Ansprechen auf verschiedene chemotherapeutischen Regime erlauben. Relativ gut ist hier der Wissenstand zur Bedeutung von Mutationen der IDH1- und IDH2-Gene (Isocitrat Dehydrogenase). Gliome mit dieser Charakteristik scheinen hinsichtlich ihrer metabolischen und klinischen Eigenschaften einen Tumorsubtyp zu repräsentieren, der für die Patienten mit besseren Überlebenschancen einhergeht. Als ein valider Marker für das Ansprechen maligner Gliome auf eine Chemotherapie – vor allen mit Alkylantien – gilt inzwischen der Methylierungsstatus des MGMT-Promotors (Methylguaninmethyltransferase) (씰Kasten „ALDH1-Hemmung überwindet TemozolomidResistenz“). Ebenfalls als Zielstrukturen für maßgeschneiderte Therapiekonzepte bieten sich Moleküle an, die entweder von der Oberfläche der Tumorzellen aus wie Integrine oder mutierte EGF-Rezeptoren (Epidermal Growth Faktor) oder vom Tumor freigesetzt wie VEGF (Vascular Endothelial Growth Faktor) die Angiopoese an- Als einen wichtigen Baustein führte Tonn die Fortschritte im Bereich der bildgebenden Diagnostik an. Dank der inzwischen sehr hohen Auflösung von Magnetresonanztomographie (MRT) und Computertomographie (CT) lässt sich nicht nur die Lokalisation der Gliome, sondern auch ihre Ausdehnung heute viel exakter bestimmen als noch vor wenigen Jahren. Mit ergänzenden Verfahren wie Positronenemissionstomographie (PET), Singlephotonenemissionstomographie (SPECT) und Magnetresonanzspektroskopie können auch kleinste Herde besonders malignen Gewebes im Tumorinneren identifiziert und Informationen zum Tumorstoffwechsel erlangt werden. Dazu kommt die verfeinerte neurochirurgische Technik, aufgrund derer sich heute Gliome sehr viel vollständiger, aber gleichzeitig auch schonender operieren lassen. Das verbessert nicht nur die Chancen auf Funktionserhalt, sondern auch für einen möglichst raschen Beginn der in der Regel postoperativ erforderlichen Radio- oder Chemotherapie. Viel gelernt in den vergangenen Jahren habe man aber vor allem über die Biologie der Tu- Genetische Informationen zu Prognose und Therapieresponse ALDH1-Hemmung überwindet TemozolomidResistenz Ein Beispiel, wie man sich die molekulargenetischen Erkenntnisse im klinischen Alltag zu Nutze machen könnte, lassen Untersuchungen einer Arbeitsgruppe am Klinikum rechts der Isar in München erkennen (1). Die Prognose von Patienten mit Glioblastom gilt als besonders schlecht, wenn der positive Status des MGMT-Promotors (Methylguaninmethyltransferase) ein Ansprechen auf eine adjuvante Therapie mit Temozolomid verhindert. Einen wichtigen Beitrag für das aggressive Wachstum der Tumorzellen scheint die Überexpression von ALDH1 (Aldehyddehydrogenase) zu leisten. Die immunohistochemischen Analysen von Glioblastomgewebeproben mit positivem MGMT-Status ergab eine signifikante Korrelation von hohen ALDH1-Spiegeln und Resistenz auf Temozolomid. Wurde jedoch das Zytostatikum in Kombination mit den ALDH1-Hemmern 4-Diethylaminobenzaldehyd (DEAB) oder Tetraethylthiuramdisulfid (DSF) verabreicht kam es zu Resensitivierung für Temozolomid und zur Verlangsamung des Wachstums der Gliomzellen. Quelle: 1. Ringel F et al. Targeting the prognostic marker ALDH1 overcomes temozolomide resistance in human glioblastoma patients with unfavourable MGMT status. Vortrag auf der 62. Jahrestagung der Deutschen Gesellschaft für Neurochirurgie (DGNC) vom 7. bis 11. Mai, Hamburg. regen. Studien, in denen versucht wird, diese Vorgänge zu unterbrechen und damit den Tumor auszuhungern, sind angelaufen. Verfeinerte Analysemethoden Die Biomarker werden bisher vornehmlich aus Operationspräparaten bestimmt. Das reicht nach Aussage von Tonn in den meisten Fällen aus, weil die Chemotherapie der chirurgischen Intervention nachgeschaltet ist. Zeitlich früher lässt sich Untersuchungsmaterial mit der stereotaktischen Serienbiopsie gewinnen. Diese Gewebeproben, deren Volumen sehr viel klei- Onkologische Welt 3/2011 © Schattauer 2011 Downloaded from www.onkologische-welt.de on 2017-08-20 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. Kongressnachlese DGNC 2011 122 ner ist als ein Streichholzkopf, können nicht nur Auskunft über die Histologie, sondern auch über molekulare Besonderheiten des Tumors geben. Biomarker aus dem Blut zu bestimmen, sei im Moment noch Zukunftsmusik, stellte Tonn klar. Aber die Entwicklung der dafür erforderlichen Technologien mache große Fortschritte. In einem weiteren Ansatz werde versucht, die biologische Charakteristik der Tumoren mit Hilfe der nuklearmedizinischen Diagnostik im Gehirn der Patienten sichtbar zu machen. Der Wissenszuwachs kommt nach Überzeugung von Tonn nicht nur der Behandlung von Gliompatienten zugute. Sondern mit den Ergebnissen der Verbundforschung schreite man auch konzeptionell auf dem Gebiet der personalisierten Tumortherapie voran. Da viele der molekulargenetischen Charakteristika auch für andere Tumore von Belang seien, diene das Gliom gewissermaßen als Modell und ließen sich bisherige und zukünftiger Erkenntnisgewinne möglicherweise auch für die Behandlung anderen Krebspatienten nutzen. Gabriele Kiel, Hamburg Quelle: Pressekonferenz bei der 62. Jahrestagung der Deutschen Gesellschaft für Neurochirurgie (DGNC) am 9. Mai 2011, Hamburg. Onkologische Welt 3/2011 © Schattauer 2011 Downloaded from www.onkologische-welt.de on 2017-08-20 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. Internationale Literatur 123 Neue Erkenntnisse aus der Tumorbiologie Komplexe Mechanismen der Strahlenresistenz Eine Radiotherapie kann zur Selektion strahlenresistenter Tumorstammzellen führen, aus denen sich im weiteren Verlauf ein Rezidiv oder Metastasen entwickeln. Ursächlich ist die Überexpression des MET-Onkogens, das die Zellinvasion begünstigt und Zellen vor der Apoptose schützt. Gezielt gegen MET gerichtete Substanzen erhöhen die Radiosensibilität und verhindern den strahleninduzierten Tumorprogress. Die Arbeitsgruppe um Prof. Francesca de Bacco, Turin, untersuchte den komplexen Prozess der Strahlenresistenz in Zelllinien mehrerer Tumoren nach Bestrahlung in therapeutischen Dosen bis 10 Gy (1). 24 Stunden nach Radiatio maßen sie deutlich erhöhte Spiegel des c-MET-Proteins, der als Rezeptor für HGF (Hepatocyte Growth Factor) fungiert. Dabei fiel ein biphasisches Profil mit einem frühen Gipfel 1–2 Stunden und einem späten Gipfel bzw. einem Plateau 24 Stunden nach Bestrahlung auf. Auch die vom c-MET-Rezeptor ausgehende intrazelluläre Signalkaskade wurde durch die Bestrahlung aktiviert, wie die Phosphorylierung von c-MET und nachgeschalteter Proteine belegt. Der überexprimierte Rezeptor wird nach Bestrahlung auch ohne Ligandenbindung aktiviert und ist zudem sensibler gegenüber einer Stimulierung durch HGF. Die Bestrahlung induziert die vermehrte Synthese des c-MET-Protein auf der Ebene der Transkription. Verantwortlich dafür ist der durch Strahlung aktivierte Transkriptionsfaktor NF-κB, dem bei der Ausbildung einer Strahlenresistenz eine wichtige Rolle zukommt. Die NFκB-Aktivierung ist abhängig von der Proteinkinase ATM (Ataxia Teleangiectasia Mutated) als Sensor für DNA-Schäden. Zudem induziert die Strahlung eine HGF-Synthese in Stromazellen, was auf einen parakrinen Signalaustausch zwischen Tumor und Stroma hindeutet und die MET-Expression und Aktivierung weiter steigert. HGF wiederum stimuliert einen komplexen, Zellmigration, Proliferation und räumliche Reorganisation umfassenden physiologischen Prozess. Insgesamt fördert der von c-MET ausgehende Signalweg einen epithelial-mesenchymalen Phänotyp mit erhöhter Motilität und vermehrtem invasiven Potenzial, erläuterten O. Guryanova und S. Bao in einem Kommentar zu der kürzlich publizierten Arbeit (2). Dieser Mechanismus ist in gesundem Gewebe für die Heilung von Strahlenschäden verantwortlich, begünstigt in Krebszellen jedoch die Progression zur Malignitiät. c-MET- Inhibition als therapeutisches Target Im Mausmodell mit Tumor-Xenografts führte die Gabe eines selektiven MET-Inhibitors zu einer erheblich stärkeren Tumorschrumpfung als eine Bestrahlung, die lediglich das Tumorwachstum stoppte. Kombinierte man eine sehr niedrig dosierte und daher ineffektive Bestrahlung (4,5 Gy fraktioniert) mit dem MET-Inhibitor, so ließ sich das Tumorvolumen um im Mittel 75% reduzieren. Die Inhibition von c-MET könnte sich damit künftig als attraktives Target für pharmakologische Strategien erweisen, resümieren die Kommentatoren. Von besonderem Interesse ist das z. B. beim Glioblastom, bei dem die verabreichten Strahlendosen aufgrund der strahlenbedingten Toxizität limitiert sind. Die MET-Inhibition könnte hier die Effektivität der niedrig dosierten Ganzhirnbestrahlung verstärken. Dr. Katharina Arnheim, Freiburg Literatur 1. de Bacco F et al. J Natl Cancer Inst 2011; 103: 645−661. 2. Guryanova OA, Bao S. J Natl Cancer Inst 2011; DOI:10.1093/jnci/djr103. © Schattauer 2011 Onkologische Welt 3/2011 Downloaded from www.onkologische-welt.de on 2017-08-20 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. Forum NeuroOnkologie 124 Thermo-Therapie mit magnetischen Nanopartikeln Neuer Ansatz in der Krebstherapie Tumorgewebe ist im Vergleich zu Normalgewebe aufgrund seiner schlechteren Thermoregulation wesentlich empfindlicher gegenüber einer Wärmebehandlung. Die Kombination aus Re-Bestrahlung und intratumoraler Thermotherapie mit magnetischen Nanopartikeln wurde im Rahmen einer klinischen Phase-II-Studie an 59 Patienten mit einem Glioblastom-Rezidiv untersucht (Abb. 1). Neben der direkten Thermoablation von Tumorzellen bewirkt die NanoTherm® Therapie eine Verstärkung der begleitenden Strahlentherapie im Temperaturbereich von 40–44°C. Als medianes Überleben wurden in einer Studie 13,4 Monate „Overall Survival“ nach Diagnose des ersten Tumorrezidivs ermittelt (1). Damit zeigt sich die Nanopartikel-vermittelte Tumortherapie im Magnetfeld als neuer Ansatz in der Krebstherapie. Erste Indikation Gehirntumore stellen die erste zugelassene Indikation dar. Besonders Patienten mit einem Glioblastom-Rezidiv könnten wegen der begrenzten Zahl an Behandlungsalternativen von dieser neuen Technologie profitieren. Pro Jahr treten ca. 2800 Glioblastom-Neuerkrankungen in Deutschland auf. Nach DGN-Leitlinie sind die bestehenden Optionen für die Primär- und Rezidivtherapie die Resektion sowie Strahlen- und Chemothe- Mittleres Überleben (Monate) Primärer Studienendpunkt 30 25 rapie. Mit diesen Verfahren konnte in den vergangenen zwei Jahrzehnten nur eine unbefriedigende Verbesserung bei der Lebenserwartung erreicht werden. Das Ziel dieser Nanopartikel-vermittelten Thermo-Therapie ist, einen zusätzlichen, positiven Einfluss auf die Überlebenszeit der Patienten mit Hirntumoren zu nehmen. In einer klinischen Phase-II-Studie wurden Rezidive des Glioblastoms behandelt, wobei die Therapie in Kombination mit stereotaktischer Bestrahlung eingesetzt wurde. Der primäre Studienendpunkt „Gesamtüberleben ab Diagnose des 1. Tumorrezidivs“ wurde mit einem Ergebnis von 13,4 Monaten (Median) Gesamtüberleben bei 59 ausgewerteten Patienten mit Glioblastom-Rezidiv erreicht. Diese Studien- Sekundärer Studienendpunkt NanoTherm® Therapie * Historische Kontrolle **, *** 95% Konfidenzintervall 20 15 0 Funktionsweise der Behandlung Bei dem neuartigen Verfahren zur lokalen Tumorbehandlung werden superparamagnetische Eisenoxid-Partikel in kolloidaler Dispersion mit einer Eisen-Konzentration von 112 mg/ml sowie einer Umhüllung aus Aminosilanen nach vorheriger Planung mit konventionellen Techniken direkt in einen soliden Tumor eingebracht. Anschließend werden die Partikel in einem magnetischen Wechselfeld erwärmt. Durch den Verbleib der Nanopartikel am Ort der Applikation sind wiederholte Behandlungen möglich. Umliegendes, gesundes Gewebe wird bei der Behandlung geschont, da die Wärmeerzeugung aus dem Tumorinneren erfolgt. Die gewünschte Behandlungstemperatur und dazu erforderliche Magnetfeldstärke werden vom behandelnden Arzt (Neurochirurg, Strahlentherapeut) vor Therapiebeginn im Rahmen einer Postimplantationsanalyse (PIA) auf Basis der Dichteverteilung der Nanopartikel im postoperativen CT geplant. Er wird dabei durch die Software NanoPlan® unterstützt, welche die Temperaturverteilung im Zielgebiet simuliert. Grundlage für den Einsatz sind ein präoperatives MRT (씰Abb. 2) sowie ein postoperatives CT (씰Abb. 3), welche Lage und Konzentration der applizierten Nanopartikel ermitteln. Die eingebrachten Nanopartikel werden mittels eines Magnetwechselfeldapplikators (NanoActivator®) von außen aktiviert. Sie wandeln dabei die Energie des Magnetfelds durch Relaxationsprozesse in Wärme um. Dabei können Behandlungstemperaturen von bis zu 80°C erreicht werden (씰Abb. 4). 23,2 10 5 ergebnisse (1) waren Basis der europäischen Zulassung der Therapie zur Behandlung von Gehirntumoren. 14,6 13,4 Effekt und Nutzen 6,2 Nach Diagnose des ersten Tumorrezidivs * Maier-Hauff et al. (2010), J Neurooncol Sep 16. [Epub ahead of print] Nach Diagnose des Primärtumors ** Stupp et al. (2009) Lancet Oncology 10:459–466 *** Stupp et al. (2005), N Engl J Med 352: 987–996 Abb. 1 Überlebenszeiten nach kombinierter NanoTherm®-/Strahlentherapie vs. historischem Vergleichskollektiv bei 59 Patienten mit Glioblastom-Rezidiv. Primärer Endpunkt: Gesamtüberleben ab Diagnose des 1. Tumorrezidivs (OS 2) 13,4 Monate* vs. 6,2** Monate; sekundärer Endpunkt: Gesamtüberleben ab Diagnose des Primärtumors (OS 1) 23,2* Monate vs. 14,6*** Monate. Temperaturen zwischen 40°C und 44°C verstärken die Wirkung von parallelen Strahlen- oder Chemotherapien und machen die so behandelten Zellen angreifbarer für körpereigene Abwehrmechanismen. Ab einem Schwellenwert von 43°C, appliziert über einen Zeitraum von 60 Minuten, entstehen nicht reversible Schäden in den Tumorzellen. Auf diese schonende Weise werden hypertherme und thermoablative Tem- Onkologische Welt 3/2011 © Schattauer 2011 Downloaded from www.onkologische-welt.de on 2017-08-20 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. Forum NeuroOnkologie 125 Abb. 2 Präoperatives MRT Abb. 3 CT nach Applikation der Nanopartikel Abb. 4 Isothermen zur Simulation im Zielgebiet peraturen in soliden Tumoren erreicht. Die Therapie dauert drei Wochen, in denen der Patient zweimal pro Woche für jeweils 60 Minuten im Magnetfeldapplikator behandelt wird. Welche Patienten profitieren? Die Therapie ist für alle Gehirntumoren zugelassen. In der klinischen Studie wurden Patienten mit einem Glioblastom-Rezidiv behandelt. Ausgeschlossen von der Behandlung wurden Patienten mit Infiltration des Balkens, der Ventrikel und des Hirnstamms sowie beim Vorliegen von Schmetterlingsglioblastomen. Schwangere und Patienten mit Herzschrittmachern oder implantierten Defibrillatoren sowie mit nicht entfernbaren, metallischen Gegenständen im Behandlungsgebiet (Abstand von weniger als 40 cm zum Tumor) konnten ebenfalls nicht behandelt werden. Metallische Zahnfüllungen, Kronen, Brücken wurden für die Dauer der Therapie entfernt, da sie sich wie die Nanopartikel im Magnetfeld erhitzen könnten. MRT-Untersuchungen zur Diagnostik weiteren Tumorwachstums können nach Einbringen der Nanopartikel wegen Artefakten in der Bildgebung nicht mehr eingesetzt werden. Für Körperpartien außerhalb der Zielregion eignet sich das MRT nach wie vor uneingeschränkt. Positronen-Emissions-Tomographie (PET) Untersuchungen oder Computertomografie (CT) sind uneingeschränkt möglich. laufen zurzeit klinische Studien zur Behandlung des Pankreas- sowie des Prostatakarzinoms. Darüber hinaus wird an der Erweiterung des therapeutischen Einsatzes des Verfahrens durch Kopplung der Nanopartikel an Radiound Chemotherapeutika oder biologischer Wirkstoffe gearbeitet. Die Markteinführung der Therapie in Deutschland erfolgte im 1. Quartal 2011. Das erste Behandlungszentrum befindet sich in der Charité –Universitätsmedizin Berlin. Jörg Camp, Fürstenfeldbruck Literatur Ausblick Die guten Perspektiven dieser neuen und für den Patienten gut verträglichen Behandlungsform konnten in der klinischen Studie anhand der vielversprechenden Überlebensdaten aufgezeigt werden. Zur Erweiterung der Indikation 1. Maier-Hauff et al. Efficacy and safety of intratumoral thermotherapy using magnetic iron-oxide nanoparticles combined with external beam radiotherapy on patients with recurrent glioblastoma multiforme. J Neurooncol 2010; Sep 16. [Epub ahead of print] Hinweis: Mit freundl. Unterstützung der MagForce Nanotechnologie AG, Berlin © Schattauer 2011 Onkologische Welt 3/2011 Downloaded from www.onkologische-welt.de on 2017-08-20 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved.