Newsletter Q2 2015
Werbung
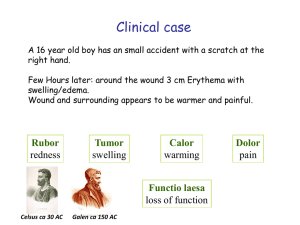
Wissenschaftliche Gesellschaft zur Forschung und Weiterbildung im Bereich nahrungsmittelbedingter Intoleranzen Newsletter Q2/2015 The english version of this text starts at page 9. Teil 2: Das erworbene (spezifische) Immunsystem Als Einleitung in das erworbene Immunsystem möchte ich noch einmal auf die Unterschiede zwischen angeborenen und erworbenen Immunsystem eingehen: Angeborenes Immunsystem Erworbenes Immunsystem Evolutionär alt Evolutionär jung Reagiert schnell Braucht Anlaufzeit Unspezifisch da Erkennung von Mustern Erkennung sehr spezifischer Strukturen Mustererkennende Rezeptoren (pattern recognition receptors) Große Anzahl verschiedener spezifischer Antigen-erkennender Rezeptoren Kein Gedächtnis Immunologisches Gedächtnis Ähnlich dem angeborenen Immunsystem kann man auch das erworbene Immunsystem in eine zelluläre Komponente, die T- und B-Zellen und eine lösliche (humorale) Komponente, die so genannten Antikörper, auch Immunglobuline genannt, einteilen. Um ein besseres Verständnis von der Funktion von T- und B-Zellen zu bekommen, werfen wir einen Blick auf die Entwicklung dieser Zellen. Beiden gemeinsam ist, dass sie im Knochenmark gebildet werden aus einer gemeinsamen lymphozytischen Vorläuferzelle. Während die B-Zellen für Ihre Entwicklung im Knochenmark verbleiben, wandern die T-Zellen für ihre weitere Entwicklung in den Thymus. Deshalb auch die Bezeichnung B-Zellen für bone-marrow (bei Vögeln Bursa Fabricii) und TZellen für Thymus. Während der Entwicklung beider Zelltypen kommt es zur Expression – zur Hochregulierung – der spezifischen Zell Rezeptoren: dem B-Zellrezeptor und dem T-Zellrezeptor. Diese neu gebildeten Rezeptoren werden danach in der Zellentwicklung intensiv darauf getestet, dass sie einerseits funktionell sind, d.h. dass sie Signale in das Zellinnere weiterleiten können und andrerseits keine körpereigenen Strukturen erkennen. Das Testen der Rezeptoren ist von immenser Bedeutung, da beide Zellrezeptoren zufällig aus einer Vielzahl von DNA-Vorlagen gebildet werden und dadurch an praktisch jede beliebige (Protein-) Struktur binden können. Darunter eben auch an körpereigene Strukturen, was zur Ausbildung einer Autoimmunität, wie z.B. bei der Zöliakie, führen würde mit fatalen Folgen für den Organismus. Ein Unterscheidungsmerkmal der beiden Rezeptortypen ist, das der B-Zellrezeptor seinen Bindungspartner, das so genannte Antigen, in löslicher Form binden kann, während der T-Zellrezeptor sein Antigen nur erkennt, wenn es ihm speziell präsentiert wird. Diese Präsentation erfolgt von spezialisierten Zellen, den sogenannten Antigen präsentierenden Zellen, durch spezielle Moleküle den Haupthistokompatibilitätskomplexmolekülen Klasse I und II (major histocompatibility complex clas I und dem major histability complex clas II), kurz MHCI und MHCII. Schauen wir uns nun im Detail die T-Zellentwicklung an. T-Zell Entwicklung im Thymus Wie oben bereits erwähnt findet die Entwicklung der T-zellen im Thymus, auch Bries genannt, statt. In der Thymusarchitektur kann man einen Cortex (Rinde) von einer Medulla (Mark) unterscheiden. Unreife Vorläufer T-Zellen aus dem Knochenmark werden nachdem sie in den Thymus eingewandert sind als Thymozyten bezeichnet. Während der Entwicklung im Thymus kommt es nicht nur zur Neuarrangierung des T-Zellrezeptors sondern auch zu einem bestimmten Expressionsmuster an Ko-rezeptoren, mit deren Hilfe man verschiedene Arten von T-Zellen und bestimmte Entwicklungsstadien unterscheiden kann. In der ersten Phase der Entwicklung spricht man von doppelt negativen (DN) T-Zellen. Doppelt negativ deshalb, weil diese Thymozyten weder den Korezeptor CD4 noch den Korezeptor CD8 exprimieren. Des Weiteren kommt es zu einer geregelten Expression von CD44 und CD25, sodass man innerhalb der DN-Phase 4 weitere Phasen unterscheiden kann. In dieser Zeit kommt es zum Rearrangement von DNA Stücken, der sogenannten somatischen Rekombination, des DNA Abschnitts, der den T-Zellrezeptor bildet. Der TZellrezeptor selbst besteht aus einer alpha und einer beta Kette. Die beiden Ketten bestehen wiederum aus einem konstanten Teil (C) und einem variablen Teil, der sich wiederum aus V (variable), D (diversity) und J (joining) Elementen zusammensetzt. Tabelle 2 gibt einen Überblick über die Anzahl der Segmente im T-Zellrezeptor Segment Alpha Kette Beta Kette Variable (V) Ca. 70 52 Diversity (D) 0 2 Joining (J) 61 13 Neben dieser Kombinatorischen Diversität kommt es auch noch durch Hinzufügen von DNABausteinen während der Rekombination der VDJ-Segmente zu einer so genannten junctional Diversity. Im Endeffekt kann man berechnen, dass es zu 1016 unterschiedlichen Kombinationen an T-Zellrezeptoren kommen kann. Zum Vergleich der menschliche Körper besteht aus ca. 1014 Zellen. In der DN3 Phase wird nun zum ersten Mal in der Entwicklung der T-Zelle eine funktionierende beta-T-Zellrezeptor Kette an der Oberfläche exprimiert. Gleichzeitig findet zu diesem Zeitpunkt auch die Erste Überprüfung statt. Im Prozess der beta-Selektion wird getestet, ob die Neuarrangierung der beta-Kette erfolgreich war. Falls es zu keiner erfolgreich arrangierten betaKette kommt, bekommt die T-Zelle eine 2te Chance und rekombiniert eine beta Kette am 2ten DNA-Strang. Kommt es auch dann nicht zur erfolgreichen Rekombination stirbt die T-Zelle einen geregelten Zelltod, d.h. sie geht in Apoptose. Ist alles erfolgreich verlaufen, paart die beta-Kette mit einer Surrogat alpha-Kette und bildet einen pre T-Zellrezeptor. Die Bildung dieses Komplexes führt zum Überleben, zur Proliferation und zur weiteren Differenzierung der T-Zelle, was zur Hochregulierung der Korezeptoren CD4 und CD8 führt und zur Rearangierung der alpha Kette. Die Thymocyten treten dann in die Phase der doppelt positiven (DP), da sie CD4 und CD8 exprimieren, Thymocyten ein. Nach der erfolgreichen Produktion der alpha Kette kommt es zur positiven Selektion. In der positiven Selektion wird überprüft, ob der Neugebildete T-Zellrezeptor an körpereigene Peptide (kurze Proteinsequenzen) die wiederum an MHC Klasse I oder MHC Klasse II Moleküle gebunden sind, bindet. Bindet der T-Zellrezeptor und leitet ein Signal weiter, führt das zum Überleben der T-Zelle. Bindet er nicht, kommt es zur Apoptose. Nun wird die Produktion eines der beiden Ko-rezeptoren – CD4 oder CD8 – eingestellt. Wie genau es zur Entscheidung für den Einen oder den Andren kommt, ist noch nicht vollständig geklärt. Dadurch treten die Thymocyten in die Phase der single positiven (SP) Zellen ein und treten nun auch physisch von der Rinde in das Mark des Thymus über. Im Mark kommt es dann zur negativen Selektion. In der negativen Selektion werden jene Zellen ausgesiebt, die zu stark an körpereigene Peptide binden würden und dadurch zu Reaktionen des Immunsystems gegen den eigenen Körper führen würden. Übersteht der Thymozyt die drei Kontrollpunkte: beta-Selektion, positive Selektion und negative Selektion verlässt er den Thymus und ist bereit seine Aufgaben in der Verteidigung gegen unerwünschte Eindringlinge auszuüben. So werden innerhalb von ca. 2 Wochen von 60 Millionen T-Zellen, die in den Thymus pro Tag einwandern nur 2 Millionen selektioniert, dies entspricht etwas mehr als 3%. Man sieht also dass es zu einer rigorosen „Qualitätskontrolle“ kommt um falsch reagierende T-Zellen auf jeden Fall zu eliminieren. Figur 1 T Zellentwicklung im Thymus. Doppelt negative T Zellen (DN) beginnen nach erfolgreicher beta Selektion mit der Expression von CD4 und CD8 und werden dadurch zu doppelt positiven Zellen (DP) In diesem Stadium untergehen sie der positiven Selektion im Thymus Cortex und der negativen Selektion in der Thymus Medulla. Erfolgreich Selektionierte T Zellen verlassen den Thymus entweder als einfach positive CD4 oder CD8 Zellen (SP). Abbildung unter Creative Commons license aus PLoS Pathog 2(6): e62. doi:10.1371/journal.ppat.0020062 B-Zell Entwicklung Analog der T-Zell Entwicklung kommt es zur B-Zell Entwicklung im Knochenmark. Auch hier gibt es verschiedene Kontrollpunkte um sicherzustellen, dass die reifen B-Zellen einen funktionierenden BZellrezeptor besitzen. Beim B-Zellrezeptor spricht man allerdings nicht von einer alpha und beta Kette sondern von einer schweren und einer leichten Kette. Der B-Zellrezeptor wird auch als Immunglobulin betitelt, da er wenn er sezerniert wird, das heißt nicht in der Membran einer B-Zelle verankert ist, nichts anderem als einem Antikörper, d.h. einem Immunglobulin entspricht. Was also wiederum bedeutet, dass B-Zellen für die Antikörperproduktion im Körper verantwortlich zeichnen. Die spezifische Immunantwort Da wir nun die Entwicklung aller Komponenten des spezifischen Immunsystems besprochen haben können wir uns ansehen, was bei einer Infektion passiert. Manche Pathogene können allein vom angeborenen Immunsystem eliminiert werden. Dies passiert ohne oder nur mit geringen Symptomen. Wird das angeborene Immunsystem aber von einem Pathogen überwältigt, merken wir die Beteiligung des spezifischen Immunsystems. Nachdem die T-Zellen ihre Reifung im Thymus abgeschlossen haben, zirkulieren sie im Blut. Erreichen sie ein peripheres lymphatisches Organ, z.B. einen Lymphknoten oder die Milz, verlassen sie das Blutsystem und zirkulieren nun im lymphatischen System, solange bis sie wieder ins Blutsystem zurückkehren. Reife T-Zellen, die im Blut- und Lymphsystem zirkulieren, aber noch nicht in Kontakt mit ihrem spezifischen Antigen waren nennt man naive T-Zellen. Um aktiviert zu werden, muss eine T-Zelle mit ihren T-Zellrezeptor ihren spezifischen peptid:MHC Komplex auf einer Antigen präsentierenden Zelle binden. Antigen präsentierende Zellen können Macrophagen, B-Zellen oder der für den Beginn einer Immunantwort wahrscheinlich wichtigste Vertreter die dendritische Zelle sein. Die dendritische Zelle bildet das Bindeglied zwischen angeborener und erworbener Immunität. Verletzt man sich z.B. an der Haut fällt der Schutz durch die Barriere Haut und Bakterien können relativ leicht in den Körper eindringen. Dendritische Zellen, die in großer Figur 2 Überblick über die spezifische Immunantwort. Antigen präsentierende Zellen (APC) aktivieren CD4 positive oder CD8 positive T Zellen. Dies führt zur Elimination von virusbefallenen Zellen durch zytotoxische T-Zellen (CTL), oder zur T-Zellhilfe an z.B. B-Zellen, welche dann Antikörper produzieren. Sowohl T-Zellen als auch BZellen sind befähigt langlebige Gedächtniszellen zu bilden (Memory) die bei einer erneuten Infektion rascher reagieren können. Abbildung unter Creative Commons license von van de Sandt, C.E.; Kreijtz, J.H.C.M.; Rimmelzwaan, G.F. Evasion of Influenza A Viruses from Innate and Adaptive Immune Responses. Viruses 2012, 4, 1438-1476. Zahl gleich unter der Haut, oder auch unter Schleimhäuten sitzen, fressen ähnlich wie die Macrophagen die Bakterien auf. Sie haben aber nicht das Ziel diese zu eliminieren, sondern sie prozessieren die Bakterien und präsentieren Teile (Peptide) davon wieder an Ihrer Zelloberfläche gebunden an den MHC Klasse II Komplex. Dieser Vorgang des Prozessierens findet während der Wanderung der dendritischen Zelle von der Haut in den nächstgelegenen Lymphknoten statt. Während dieser Wanderung verändert sie auch ihr Aussehen und wird zur reifen dendritischen Zelle die jetzt nicht mehr so gut im Auffressen von Bakterien ist, aber eine sehr große Oberfläche bildet, an der sie viel vom peptid:MHC Komplex präsentiert. Die Lymphknoten sind praktisch die Marktplätze des Immunsystems, indem viele Immunzellen auf kleinstem Raum aufeinander treffen. Trifft nun der Verkäufer, die dendritische Zelle, auf ihren passenden Käufer, die für das präsentierte Peptid passende T-Zelle, kommt es zur Aktivierung der T-Zelle. Je nachdem welcher Typ von T-Zelle aktiviert wurde, können verschiedene Effektormechanismen in Kraft treten. T-Zell Typ CD8+ zytotoxische T-Zellen CD4+ Th1-Zellen CD4+ Th2Zellen CD4+ Th17Zellen CD4+ TregZellen Funktion Abtöten von Virus infizierten Zelle Aktivierung Makrophagen. Hilfe für B – Zellen zur IgG Produktion Hilfe für BZellen zur IgE Produktion Hilfe für Neutrophile Unterdrückung der Immunantwort Zielpathogen Viren, bestimmte intrazelluläre Bakterien Intramakrophage Parasiten, Bakterien: z.B. Allergie Mycobacteria, Listeria. Extrazelluläre Bakterien Extrazelluläre Bakterien Bevor wir uns aber mit den verschiedenen Typen der T Helfer Zellen (Th) beschäftigen, müssen wir noch eine grundsätzliche Unterscheidung zwischen Cytotoxischen T-Zellen und eben den Th Zellen treffen. Wie wir bereits bei der T-Zellreifung besprochen haben, gibt es T-Zellen, die den Korezeptor CD4 oder den Korezeptor CD8 exprimieren. Exprimieren T- Zellen den Korezeptor CD4 erkennen sie Peptid, dass mit Hilfe des MHC Klasse II präsentiert wird und man spricht von T Helfer Zellen. Exprimieren T-Zellen den Korezeptor CD8 erkennen sie Peptid, dass mittels MHC Klasse I präsentiert wird. Jede Zelle im Körper mit Zellkern (d.h. Rote Blutkörperchen nicht) exprimiert MHC Klasse I – warum? Mit Hilfe des MHC Klasse I Moleküls werden Virale Peptide präsentiert. Viren brauchen aber für Ihre Vermehrung die zelleigene Maschinerie zur Verdoppelung des genetischen Codes, der wiederum nur in Zellen mit Zellkern enthalten ist. D.h. mit Hilfe des MHC Klasse I und der zytotoxischen T-Zellen kann das Immunsystem jede Körperzelle auf Virusbefall überprüfen. Wird Funktion IgM IgD IgG IgA IgE Neutralisation + - ++ ++ - Opsonierung + - ++ + - Sensibilisierung Mastzellen - - - - +++ - ++ + - Aktivierung +++ Komplementsystem nun eine CD8 positive zytotoxische T-Zelle durch ihr spezifisches Peptid im MHC Klasse I Komplex einer virusbefallenen Zelle aktiviert, schüttet die T-Zelle bestimmte zellschädigende Botenstoffe aus und killt damit die Zielzelle. Deshalb werden CD8 positive T-Zellen auch T Killer Zellen genannt. Kommen wir aber nun zurück zu den CD4 positiven T Helfer Zellen. Warum T Helfer Zellen? Weil diese Zellen nicht selbst Pathogene eliminieren sondern anderen Zellen z.B. B-Zellen oder Macrophagen bei der Pathogeneliminierung helfen. Wie gesagt gibt es auch hier verschiedene Unterklassen und je nach dem welcher Unterklasse die aktivierte T-Zelle angehört ist der Effekt ein anderer. Th1 Zellen z.B. sind verantwortlich für die sogenannte zellvermittelte Immunität indem sie Macrophagen aktivieren oder Hilfe für B-Zellen liefern, wodurch diese den Prozess der Affinitymaturation durchlaufen und zu Plasmazellen werden und beginnen ihren B-Zellrezeptor zu sezernieren, d.h. Antikörper zu produzieren. Es gibt verschiedene Klassen von Antikörpern, die auch wieder verschiedene Effektorfunktionen erfüllen. Immunglobulin M (IgM) ist die Basisform eines Antikörpers, wie er zu Beginn einer B-Zellantwort bevor es zu dem sogenannten class switching kommt produziert wird. IgM bindet im Vergleich zu anderen Antikörpern relativ schlecht an sein Antigen, hat aber 5 Bindungsstellen. Dies macht ihn um einiges größer als andere Antikörper und dadurch sind IgM Antikörper hauptsächlich im Blut zu finden. Seine Funktion ist Pathogene zu opsonieren, d.h. sie besser sichtbar zu machen und dadurch v.a. das Komplementsystem, eine Komponente des angeborenen Immunsystems, zu aktivieren. Man sieht also auch hier wieder die Wechselwirkung angeborenes – erworbenes Immunsystem. Durch die T-Zellhilfe werden die BZellen aktiviert und es kommt zur Affinitätsreifung und zum class switch. Dies bedeutet, es werden andere Antikörperklassen, die relativ besser als IgM ihr Antigen binden, gebildet. Bekommen BZellen durch Th1 Zellen Hilfe wird hauptsächlich IgG Antikörper produziert. IgG ist der Antikörper mit der höchsten Serumkonzentration. Er kann dazu dienen Toxine zu neutralisieren oder Pathogene für die Aufnahme durch Fresszellen zu opsonieren. Eine weitere Antikörperklasse sind die IgA-Antikörper. Diese werden hauptsächlich durch die epitheliale Zellschicht sezerniert und dienen im Dünndarm oder der Lunge als neutralisierende Antikörper. Bekommt eine B-Zelle Hilfe von einer Th2 Zelle produziert diese hauptsächlich IgE Antikörper. Dies ist der ursprüngliche Weg um eine Immunantwort gegen Parasiten einzuleiten. Berühmter ist der IgE Antikörper eher für seine Wirkung in der Allergie. IgE bindet an Mastzellen und aktiviert diese zur Histaminausschüttung sobald das Allergen an den an die Mastzelle gebundenen IgE Antikörper bindet. Eine andere wichtige Klasse von T-Zellen sind die regulatorischen T-Zellen Treg, die Immunantworten abschwächen und unterbinden können und dadurch ein unkontrolliertes Ausbreiten einer Immunantwort verhindern. Daneben gibt es noch eine Reihe von neu identifizierten Subklassen (Th17, Th9, Th22), die unterschiedliche Botenstoffe produzieren und wichtige Funktionen in autoimmun Erkrankungen oder im mukosalen Immunsystem ausüben. Kommt es nun zur Elimination des Pathogens durch das Zusammenspiel all der genannten zellulären und humoralen Komponenten des angeborenen und des erworbenen Immunsystems werden besonders langlebige T und B-Zellen gebildet, die sogenannten T und B memory cells. Diese Zellen überleben oft Jahre bis Jahrzehnte lang und benötigen bei einer wiederholten Infektion mit dem gleichen Pathogen keine Aktivierung mehr durch Antigen präsentierende Zellen bzw. produzieren sie hoch affine, d.h. sehr stark bindende Antikörper. Dies ist der Effekt, den man bei Impfungen ausnützt. Alles in allem sehen sie wie komplex aber gleichzeitig faszinierend das Immunsystem ist, und wie wichtig es ist, es bestmöglich durch z.B. ausgewogene Ernährung zu unterstützen und nicht überzustrapazieren. Literatur: PLoS Pathog 2(6): e62. doi:10.1371/journal.ppat.0020062 van de Sandt, C.E.; Kreijtz, J.H.C.M.; Rimmelzwaan, G.F. Evasion of Influenza A Viruses from Innate and Adaptive Immune Responses. Viruses 2012, 4, 1438-1476 Weiterführende Literatur: Lerne dein Immunsystem kennen (in Englisch): http://www.interactive-immunity.net/ Eine Interaktive Reise durch das Immunsystem: http://www.inside-immunity.org/de#explication 2 Standardwerke zur Immunbiologie: Charles A. Janeway: Immunologie. Spektrum Akademischer Verlag; 5. Auflage (2002) ISBN 3-82741079-7 Abul K. Abbas: Cellular and Molecular Immunology (engl.). W.B. saunders Company; 5th update (2005) ISBN 1-4160-2389-5 Part 2: The adaptive immune system As an introduction into the adaptive immune system I want to recapitulate the differences between the adaptive and the innate immune system. Innate immune system Evolutionary old Reacts fast Unspecific because it recognizes recurring patterns Pattern recognition receptors No memory Adaptive immune system Evolutionary young Needs time for reaction Recognizes very specific structures A big number of different very specific antigen recognizing receptors Memory Like the innate immune system the adaptive immune system can be categorized in a cellular part, the T- and B-cells, and a humoral part, the antibodies or also called immune globulins (Ig). For a better understanding of the function of T- and B-cells, we will have a closer look at the development of these cells. Both cell types origin in the bone marrow from a common lymphoid progenitor cell. The B-cells stay in the bone marrow during their development. T-cells migrate in the thymus for further development. That’s why they are called B-cells for bone marrow (in birds Bursa Fabricii) and T-cells for thymus. During the development of both cell types they start to express their specific receptors. The newly expressed receptors are rigorously tested for their functionality – so that they can transduce a signal from outside the cell inside the cell - and their safety, which means that they do not recognize structures from the own body. Testing of the receptors is very important because both receptors are built randomly from a high number of DNA blueprints and therefore they can recognize almost any protein structure. This includes body’s own structures, which would lead to autoimmunity reactions like coeliac disease. A difference between B- and T-cell receptors is that the B-cell receptor can bind to soluble antigen, whereas the T-cell receptor recognizes its antigen only if it’s special presented. The presentation is done by special cells the so called antigen presenting cells (APC), by special molecules the major histocompatibility complex class I and class II (MHCI and MHCII). Now we will have a closer look at the T-cell development T cell development in the thymus T-cell development takes place in the thymus. In the thymus one can discriminate distinct areas the cortex and the medulla. Immature T-cells from the bone marrow, are called thymocytes after they enter the thymus. During the development in the thymus not only the T-cell receptor is newly arranged but also expression of Co-receptors starts. With the help of the expression of the Coreceptors different developmental phases are distinguishable. In the first phase of development thymocytes are called double negative because they lack the expression of the co-receptors CD4 and CD8. Moreover there is an ordered expression of CD44 and CD25, which leads to the discrimination of 4 phases within the DN-phase. During this phase the somatic recombination of the DNA parts encoding the T-cell receptors takes place. The T-cell receptor consists of an alpha and a beta chain. Both chains consist of a constant part (C) and a variable part, which in turn consists of a variable number of variable (V), diversity (D) and joining (J) elements. In the following table you see an overview of the different elements in the alpha and beta chain. Segment Variable (V) Diversity (D) Joining (J) Alpha chain Ca. 70 0 61 Beta chain 52 2 13 Besides the combinatorial diversity, a junctional diversity happens by adding DNA elements during the recombination process. In the end you can get 1016 different combinations of T-cell receptors. For comparison the human body consists of 1014 cells. In the DN3 phase for the first time during the development of a T-cell a recombined beta chain of the T-cell receptor is expressed. Simultaneously the first check for a functional T-cell receptor takes place. A process called beta selection. In case the newly arranged beta chain is not functional the T-cell gets a second chance and recombines a beta chain on the 2nd DNA strain. Does the second beta chain again fail to successfully transduce a signal the cell undergoes an ordered cell death in a process called apoptosis. If the T-cell successfully passes the beta selection the beta chain binds to a surrogate alpha chain to build up the pre T-cell receptor. Expressing a pre T-cell receptor leads to survival, proliferation and differentiation of the T cell, which leads to the upregulation of the co-receptors CD4 and CD8 and to the rearrangement of the alpha chain. The thymocytes enter now the phase of double positive thymocytes, because they express both CD4 and CD8. After the successful production of the alpha chain the positive selection takes place. The positive selection selects those T-cells which are able to bind to peptides (small parts of proteins) within the context of MHC class I or II. Is the T-cell receptor able to bind to the peptide MHC complex, the T-cell survives. If the T-cell receptor doesn’t bind the T-cell undergoes apoptosis. Now the production of one of the two co receptors – CD4 or CD8 – is terminated. Therefore the cells enter the stage of single positive SP thymocytes and leave the cortex and enter the medulla. In the medulla the process of negative selection takes place. In the negative selection all cells undergo apoptosis, which bind too strong to self-peptide in the context of MHC I or II and therefore would lead to an auto immune reaction. If the thymocyte survives the three control points: beta selection, positive – and negative selection, it is ready to fulfil its duty in the body defence. Within two weeks just 2 million T cells survive the selection from 60 million, which enter the thymus in the beginning. That’s a little bit more than 3%. One can understand that there is a rigorous quality control so that wrong reacting T-cells are for sure eliminated. Figure 1: T cell development in the thymus. Double negative T cells (DN) start after successful beta selection with the expression of CD4 and CD8 and become double positive cells. In this stage they undergo positive selection in the cortex of the thymus and negative selection in the medulla. Successful selected T cells leave the thymus as single positive CD4 or CD8 cells. Picture under creative commons license from PLoS Pathog 2(6): e62. doi:10.1371/journal.ppat.0020062 B-cell development Similar to the T-cell development the B-cell development takes place in the bone marrow. Again they have to pass several control points to make sure that the mature B-cell has a functional B-cell receptor. The B-cell receptor consists of a heavy and a light chain. It’s also called immune globulin, because if the B-cell receptor is secreted, it’s nothing else than an antibody or also called immune globulin. This means that B cells are responsible for the production of antibodies in the body. The adaptive immune response Now that we know the development of all components of the adaptive immune system we can have a closer look at what is happening during an infection. Some pathogens are eliminated from the innate immune system without or with just little symptoms. Is the innate immune system overwhelmed from the pathogen we realize the involvement of the adaptive immune response. After the T-cells finish their development in the thymus they are circulating in the blood. If they enter a peripheral lymphatic organ, like a lymph node or the spleen, they leave the blood system and enter the lymphatic system. Mature T-cells, which are recirculating between the blood- and the lymphsystem and haven’t encountered there antigen yet are called naïve T-cells. To get activated a T-cell has to bind with its T-cell receptor its specific peptide:MHC complex on an antigen presenting cell. Antigen presenting cells are Macrophages, B-cells or the most important cell type for the initiation of an immune response the dendritic cells. The dendritic cell is the linker between the innate and the adaptive immune system. If you get hurt in the skin, which means you don’t have a barrier protection any longer, it’s easy for pathogens to enter the body. Beneath the skin and mucosal barriers a lot of dendritic cells are located. Dendritic cells phagocytize like macrophages bacteria but they don’t have the goal to eliminate them but they process them and present parts thereof (peptides) on their surface in the context of MHC class II. The processing takes place during the way from the skin (or mucosa) to the nearby lymph node. During this time the dendritic cells also changes its shape and becomes a mature dendritic cells which is no longer a good phagocytizing cell but because of a very large surface is very good in presenting peptides of pathogens and activating T-cells. The lymph nodes are the bazaars of the immune system. A lot of immune cells are meeting each other and if a seller, the dendritic cell, meets it suitable buyer, the T-cell, activation of this T-cell takes place. Depending on which type of T-cell gets activated, different effector mechanism take place. Figure 2: Overview of the specific immune response. Antigen presenting cells (APC) activate CD4 or CD8 positive T cells. This leads to elimination of a virus bearing cell through cytotoxic T cells (CTL), or to the help of B-cells, which afterwards start to produce antibodies. T and B-cells are able to generate long lived memory cells, which react much faster after a new infection with the same pathogen. Picture under Creative Commons license from van de Sandt, C.E.; Kreijtz, J.H.C.M.; Rimmelzwaan, G.F. Evasion of Influenza A Viruses from Innate and Adaptive Immune Responses. Viruses 2012, 4, 14381476. T-cell type Function Target CD8+ cytotoxic Tcell Killing of virus infected cells Virus, special intracellular bacteria CD4+ Th1-cells CD4+ Th2cells CD4+ Th17cells CD4+ Tregcells Activation of macrophages. Help B-cells for IgG production Intramacrophageal bacteria: Mycobacteria, Listeria. Extracellular bacteria Help B-cells for IgE production Help neutrophils Suppress immune reaction Parasites, allergy Extracellular bacteria Before we start with the different types of T-helper cells we have to distinguish between CD8 positive cytotoxic T-cells and CD4 positive T-helper cells. Express T-cells the co receptor CD8 they recognize peptide only if it is presented in the context of MHC class I. Every body cell with a nucleus is expressing the MHC class I molecule for the presentation of intracellular proteins. If a cell is now attacked by a virus, the virus starts to produce its own proteins in the cell. These newly expressed viral proteins are, like the cell own proteins, presented on the cell surface within the MHC class I complex. This means that with the help of the MHC class I and the cytotoxic T-cells every body cell can be checked for virus infection. If a CD8 positive cell gets now activated from a virus infected cell it kills this cell by the production of cytotoxic substances. That’s why cytotoxic T cells are also called T killer cells. But let’s come back to the T helper cells. As already mentioned they express the co receptor CD4 and therefore recognize peptides only if presented in the context of MHC class II. Why are they called T helper cells? Because these cells don’t eliminate pathogens on their own but they help other cells like macrophages or B-cells, to do so. There are several subtypes of T-helper cells and depending which subtype gets activated different effector mechanism take place. Th1 cells are responsible for the cell mediated immunity, by activating macrophages or by helping Bcells. If a B-cell gets help from a T–cell they start the process of affinity maturation and become plasma cells which secrete their B-cell receptor, which means they produce antibodies. Different classes of antibodies fulfil different effector functions. Immune globulin M (IgM) is the first produced basic form of an antibody before it comes to the process of class switching. IgM binds in comparison to other antibody classes weak but has 5 binding sites. Therefore it is bigger than other antibodies and it is mainly found in the blood. Its function is to opsonize pathogens and thereby activate mainly the complement system. So you can again see the interplay between the innate and the adaptive immune system. With the help of T-cells B-cells get activated and the process of affinity maturation and class switching starts. During these processes other antibody classes, which bind better to their antigen than IgM are formed. Funktion Neutralisation Opsonisation Sensibilization of mast cells Activation complement system IgM + + - IgD - IgG ++ ++ - IgA ++ + - IgE +++ +++ - ++ + - If a B-cell gets help from a Th1 cell it will produce mainly IgG antibodies. IgG is the antibody with the highest serum concentration. It can neutralize toxins or opsonize pathogens for a better phagocytosis by phagocytising cells. Another antibody class are IgA antibodies. They are secreted through epithelial cell layers and neutralize pathogens in the small intestine or the lung. If a B-cell gets help from a Th2 cell it start to produce IgE antibodies. They were originally important to fight against parasites. However nowadays they are “famous” for their role in allergy. IgE binds to mast cells and activate them to secrete histamine as soon as an allergen binds to the IgE. Another important class of T-cells are regulatory T cells (Treg). Tregs can dampen and suppress an immune response and therefore prevent an uncontrolled immune reaction. Besides the well described long known Th subsets newly discovered substes like Th17, Th9 and Th22 are described. They produce different messengers (cytokines) and play an important role in auto immune diseases or in the mucosal immunity. If the pathogen gets eliminated by the interaction of the cellular and humoral components of the innate and adaptive immune system special cell types the long lived memory T- and B-cells are formed. These cells survive for years or even decades and react much faster if a new infection with the same pathogen takes place. The reason is that they do not need the help of antigen presenting cells to get activated and they produce high affine strongly binding antibodies. That’s the effect which is used in the vaccination. In summary one can see how complex but fascinating the immune system works and how important it is to support it, by for instance balanced food, and not to stress it. Literature PLoS Pathog 2(6): e62. doi:10.1371/journal.ppat.0020062 van de Sandt, C.E.; Kreijtz, J.H.C.M.; Rimmelzwaan, G.F. Evasion of Influenza A Viruses from Innate and Adaptive Immune Responses. Viruses 2012, 4, 1438-1476 get to know your immune system: http://www.interactive-immunity.net/ Eine Interaktive Reise durch das Immunsystem (in german): http://www.insideimmunity.org/de#explication Very good text books: Charles A. Janeway: Immunology. Spektrum Akademischer Verlag; 5. Auflage (2002) ISBN 3-82741079-7 Abul K. Abbas: Cellular and Molecular Immunology (engl.). W.B. saunders Company; 5th update (2005) ISBN 1-4160-2389-5