Ganzen Artikel lesen
Werbung

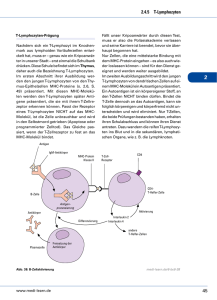
EINSICHTEN 2009 NEWSLETTER 03 lebenswissenschaften S usa n n e W edli c h Gefährliche Bodyguards Fremd vom Eigenen zu unterscheiden, ist eine der wichtigsten Aufgaben des Immunsystems. Wenn statt Krankheitserregern körpereigene Strukturen angegriffen werden, können gefährliche Autoimmunkrankheiten entstehen. In ihren Arbeiten konnten die Immunologen Professor Ludger Klein, Professor Thomas Brocker und Privatdozent Dr. David Vöhringer neue Mechanismen nachweisen, die eine derartige Entgleisung der Immunabwehr verhindern. Typ-1-Diabetes, Schuppenflechte, Multiple Sklerose und selbst bestimmte Formen des Haarausfalls: Die Liste der Autoimmunerkrankungen des Menschen ließe sich lange fortsetzen. In all diesen Fällen richtet sich die Abwehrreaktion des Organismus gegen körpereigene Zellen oder Gewebe. Unbehandelt können diese Leiden zur Zerstörung von Organen oder sogar zum Tod des Patienten führen. Als Ursache der fehlgeleiteten Immunreaktion werden genetische Defekte in Kombination mit Umweltfaktoren vermutet. Verantwortlich für viele solcher Angriffe auf körpereigene Strukturen sind die für die Immunabwehr wichtigen T-Lymphozyten. Sie entwickeln sich im Thymus, einem Organ im oberen Brustkorb. In dieser „T-Zell-Schule“ wird jede der Zellen mit einem individuellen Rezeptor an ihrer Oberfläche ausgestattet, der spezifisch ein Antigen eines pathogenen Erregers erkennen soll. Antigene sind molekulare Strukturen, meist Bruchstücke von Proteinen. Weil jeder T-Lymphozyt über einen spezifischen Rezeptor verfügt, ergibt sich eine ungeheure Vielfalt an T-Zell-Rezeptoren – und das Immunsystem kann auf nahezu jeden Krankheitserreger reagieren. Die Konstruktion der T-Zell-Rezeptoren erfolgt nach dem Zufallsprinzip, so dass im Thymus immer auch T-Lymphozyten entstehen, die auf körpereigene Strukturen reagieren und diese attackieren könnten. Schutz vor Autoimmunerkrankungen bietet nur die Vernichtung oder Entschärfung dieser autoreaktiven Immunzellen – die sogenannte immunologische Toleranz. Eine wichtige Voraussetzung dafür ist die negative Selektion. Dabei werden die gefährlichen T-Zellen einzeln aussortiert und in den Zelltod getrieben, bevor sie den Thymus verlassen können. Die verbleibenden T-Lymphozyten werden allerdings noch einem zweiten Ausleseverfahren unterzogen. Diese Prüfung findet in anderen Geweben des Immunsystems statt, den peripheren lymphatischen Organen. August 01 Es sind vor allem die Lymphknoten und die Milz, in denen diese zusätzliche Qualitätskontrolle abläuft. Zuständig dafür sind, wie eine internationale Kooperation unter der Leitung des LMUImmunologen Professor Thomas Brocker zeigen konnte, die sogenannten Dendritischen Zellen. Zu deren vorrangigen Aufgaben gehört eine wichtige Interaktion: Weil T-Lymphozyten nicht an freie Antigene andocken können, sind sie auf die Präsentation der Proteinfragmente durch andere Immunzellen angewiesen. Meistens, wenn auch nicht ausschließlich, bieten die Dendritischen Zellen den T-Lymphozyten verschiedene Strukturen zur Prüfung an. Ist das passende Antigen dabei, löst die betreffende T-Zelle eine Abwehrreaktion des Körpers aus. wie A utoimmu n reaktio n e n verhi n dert werde n k ö n n te n Wie Thomas Brocker und sein Team zeigen konnten, wandern die Dendritischen Zellen aber auch aus Geweben und Organen, etwa Magen, Darm, Bauchspeicheldrüse, Lunge und Haut, kontinuierlich in die Lymphknoten ein. Im Gepäck haben sie körpereigenes Material zur Prüfung durch die T-Zellen. Möglich ist dies unter anderem dank der Fähigkeit der Dendritischen Zellen zur Kreuzpräsentation: Sie können also mit Hilfe spezieller Mechanismen körpereigene Gewebsproteine aufnehmen, diese von den Geweben in die Lymphorgane transportieren und dort den T-Lymphozyten präsentieren. „Wenn ein T-Lymphozyt dann eines dieser körpereigenen Proteine erkennen kann, droht eine Autoimmunreaktion“, sagt Thomas Brocker. „Solche autoreaktiven T-Lymphozyten sind also potentiell gefährlich und werden während dieses Erkennungsprozesses inaktiviert und abgetötet. Auf diesem Weg wird die lebenswichtige periphere Toleranz etabliert.“ Für die vorliegende Arbeit erzeugten die Forscher genetisch veränderte Mäuse, deren Dendritische Zellen gezielte Defekte bei der Aufnahme und Kreuzpräsentation von Proteinen zeigen. „In diesen Tieren blieb die periphere Toleranzinduktion aus“, berichtet Thomas Brocker. „Damit konnten autoreaktive T-Zellen akkumulieren und Autoimmunerkrankungen induzieren.“ Die Ergebnisse zeigen erstmals, dass dieser aktive Prozess im Optimalfall autoreaktive T-Lymphozyten entschärft und so das Entstehen von Autoimmunerkrankungen verhindert – und dass Dendritische Zellen dabei eine zentrale Rolle spielen. Andererseits erklärt dies auch, warum es für den Organismus und auch in therapeutischen Ansätzen so schwer ist, eine Immunantwort gegen Krebs zu erzeugen. Schließlich bestehen die Tumoren vornehmlich aus körpereigenem Material, und Immunzellen, die darauf reagieren, werden systematisch eliminiert. Basierend auf diesen Resultaten, zeigte eine Studie unter der Leitung von Privatdozent Dr. David Vöhringer, dass die Rolle der Dendritischen Zellen nicht auf die Etablierung peripherer Toleranz beschränkt ist. „Unsere Arbeit an Mäusen hat den Nachweis geliefert, dass ohne Dendritische Zellen auch die erste und zentrale Selektion der T-Lymhozyten im Thymus nur noch ineffizient funktioniert“, berichtet der LMU-Immunologe. „Bei diesen Tieren verlassen auch autoreaktive Zellen den Thymus. Sie werden dann in den peripheren Organen aktiviert – und lösen Autoimmunität aus.“ Damit sind die Dendritischen Zellen für die Körperabwehr und die gesamte immunologische Toleranz des Körpers essentiell. Angesichts der vielen zentralen Aufgaben, die diese Zellen übernehmen, stellt sich eine Frage: Wie kann ohne Dendritische Zellen überhaupt Autoimmunität ausgelöst werden? „Die Zellen sind unter anderem darauf spezialisiert, Antigene zu präsentieren, was überhaupt erst eine Reaktion der Körperabwehr ermöglicht“, sagt David Vöhringer. „Es bleibt August 02 also zu klären, welcher Zelltyp die autoreaktiven T-Zellen aktiviert, wenn mit den Dendritischen Zellen die vermutlich wichtigsten Antigen-präsentierenden Zellen des Immunsystems fehlen. Dafür gibt es bereits ein paar Kandidaten, deren Funktion wir jetzt genauer untersuchen werden.“ Einen weiteren Typ Antigen-präsentierender Zellen, der aber nur unter bestimmten Umständen aktiv wird, konnte Professor Ludger Klein vom Institut für Immunologie der LMU identifizieren. Die Antigene liefert hier das Recycling alter und funktionsuntüchtiger Proteine, die sogenannte Autophagie („sich selbst essen“). Bei Nährstoffmangel wird dieser Prozess angeschaltet, um Zellstrukturen wieder zu verwenden und dadurch Immunfluoreszenz-Aufnahme von histologischen Schnitten der Haut: Bei fehlender peripherer Toleranzinduktion infiltrieren autoreaktive T Zellen (grün) unterschiedliche Hautschichten und induzieren Schuppenflechte-ähnliche Symptome. Zellkerne sind dem Körper Brennstoffe zur Energiegewinnung zu liefern. Wie die Forscher um Ludger Klein zeigen violett und Haarfollikel rot angefärbt. konnten, spielt die Autophagie aber wider Erwar- Quelle: LMU ten nicht nur in dieser extremen Situation eine Rolle. Die Zerstückelung körpereigenen Materials scheint vielmehr auch bei der Auslese autoreaktiver T-Lymphozyten wichtig zu sein. So kapern wohl die Epithelzellen der Thymusdrüse diesen Mechanismus: Sie bilden den einzigen Zelltyp im Organismus, der auch ohne verstärkten Energiebedarf eine konstant hohe Rate von Autophagie aufweist. Die Epithelzellen des Thymus präsentieren den heranreifenden T-Lymphozyten mit Hilfe der körpereigenen Antigene in gewisser Weise ein immunologisches Spiegelbild aller Proteine des Organismus. Autoreaktive T-Zellen können auf diese Weise ausgesiebt werden. „Wir wussten, dass eben diese Zellen bei der Entschärfung autoreaktiver T-Zellen wichtig sind“, berichtet Ludger Klein. „Die thymischen Epithelzellen sind durch einen immer noch rätselhaften Mechanismus in der Lage, praktisch jedes Protein des Körpers zu produzieren und für die T-Lymphozyten auf ihrer Oberfläche zu präsentieren.“ Lieferant für das Material könnte, vermuten die Forscher, die zweckentfremdete Autophagie sein. So könnte es dieser Prozess den thymischen Epithelzellen ermöglichen, die körpereigenen Proteine klein genug zu häckseln und auf ihre eigene Oberfläche zu schleusen. Die Untersuchung selbst wurde im Tiermodell durchgeführt. Im entscheidenden Experiment schalteten die Forscher gezielt den Mechanismus der Autophagie in den thymischen Epithelzellen aus. „Nach fünf Wochen sah man bereits mit bloßem Auge, dass es den betroffenen Mäusen nicht gut ging“, sagt Jelena Jedjic, eine Koautorin der Studie. „Die Tiere hatten massiv an Gewicht verloren und ihre Haut war schuppig.“ Die immunologische Analyse der Organe zeigte drastisch die Auswirkungen des Defekts: T-Lymphozyten hatten Blut und Lymphe verlassen, waren in Organe gewandert und hatten dort Gewebeschäden verursacht. „Allerdings wissen wir nicht, warum die TLymphozyten nur einzelne Organe befallen haben“, meint Ludger Klein. „Für uns war jedenfalls sehr August 03 interessant, dass vor allem der Darm so stark geschädigt wurde. Denn dieses Krankheitsbild erinnert stark an Morbus Crohn.“ Tatsächlich wurde in zwei unabhängigen Studien gezeigt, dass eine genetische Verbindung zwischen dieser Autoimmunerkrankung des MenAutoimmunität als Folge experimentell ausgeschalteter Autophagie: Links ist ein histologischer schen, einer chronischen Schnitt durch gesundes Drüsengewebe (Hardersche Drüse) dargestellt, rechts ist ein durch au- Darmentzündung, und einer toaggressive T-Zellen teilweise zerstörtes Organ abgebildet. Die Pfeile deuten auf Anhäufungen von eingewanderten T-Zellen. Autophagie-Komponente Quelle: LMU besteht. Der molekulare Zusammenhang ist allerdings noch nicht geklärt. Die Forscher wollen jetzt herausfinden, wie autoreaktive T-Zellen der Selektion im Thymus entkommen können, und wie sich eine defekte Autophagie im Thymus auswirken kann. Diese Ergebnisse sollen auch Einblicke in die Entstehung von Autoimmunerkrankungen liefern und könnten so möglicherweise helfen, diese zu verhindern oder zu therapieren. Einen möglichen Verbündeten in diesem Kampf hat Ludger Klein schon identifiziert: die regulatorischen T-Zellen. Das sind jene autoreaktiven T-Zellen, die zwar enttarnt, aber nicht in den Zelltod getrieben werden. Einige der gefährlichen Einzelgänger werden zu sogenannten regulatorischen T-Zellen „umerzogen“. Sie besitzen dann zwar immer noch einen T-Zell-Rezeptor, der auf körpereigene Strukturen reagiert. Dank einer Umprogrammierung im Thymus können regulatorische T-Zellen aber keinen Schaden mehr anrichten. „Ganz im Gegenteil“, sagt der Immunologe. „Sie halten sogar andere, aus dem Ruder gelaufene T-Zellen in ihrer Nachbarschaft unter Kontrolle. Damit sind die Mechanismen der Entstehung regulatorischer T-Zellen von großem praktischem Interesse.“ In einer Studie beschäftigten sich der Immunologe und seine Mitarbeiter deshalb mit einigen ungeklärten Aspekten der regulatorischen T-Zellen: Wie können sowohl die negative Selektion, also der induzierte Zelltod, als auch die Umprogrammierung zu regulatorischen T-Zellen in der Thymusdrüse und damit am selben Ort stattfinden? Warum treibt der scheinbar selbe Auslöser manche Zellen in den „Selbstmord“, während er bei anderen einen „Umerziehungsprozess“ auslöst? „Eine unter Immunologen weit verbreitete Hypothese zur Beantwortung dieser Fragen beruht darauf, dass T-Zellen ihre Zielstrukturen nur erkennen können, wenn diese von bestimmten anderen Immunzellen präsentiert werden“, sagt Gerald Wirnsberger, Erstautor der Studie. „Da es im Thymus verschiedene Unterarten solcher antigen-präsentierenden Zellen gibt, haben wir getestet, ob ein Teil davon möglicherweise darauf spezialisiert ist, das eine oder andere T-Zell-Schicksal zu steuern – mit negativem Ergebnis.“ Stattdessen stellte sich heraus, dass das Entwicklungsstadium – gewissermaßen das „Alter“ – der T-Zellen eine entscheidende Rolle spielt. Selbst im Reagenzglas ließ sich dies beobachten: Junge T-Zellen können sehr gut in regulatorische T-Zellen umerzogen werden, August 04 während ältere T-Zellen unter identischen Bedingungen weitgehend „erziehungsresistent“ sind. „Für uns ist entscheidend, diese ‚Erziehbarkeit’ auf molekularer Ebene zu verstehen“, meint Ludger Klein. Dann könnten möglicherweise auch erwachsene, nicht-autoreaktive T-Zellen entsprechend manipuliert werden, die leicht und zu Millionen aus dem Blut von Patienten gewonnen werden können. Junge T-Zellen sind dagegen nur im Thymus vorhanden. „Wir werden jetzt untersuchen, ob es sowohl für die negative Selektion als auch für die Umprogrammierung in regulatorische TZellen im Leben einer jungen T-Zelle spezielle Zeitfenster gibt“, berichtet er. „Außerdem versuchen wir, die molekularen Schalter innerhalb der T-Zellen zu entschlüsseln, die diese zellautonome Umschaltung als Antwort auf externe Signale steuert.“ Prof. Dr. Thomas Brocker ist seit 2000 Professor für Immunologie an der LMU. 2002 übernahm er zunächst kommissarisch die Leitung des Instituts für Immunologie. Seit 2004 hat er den Lehrstuhl für Immunologie inne. http://immuno.web.med.uni-muenchen.de/research/ag_brocker/index.html [email protected] Prof. Dr. Ludger Klein ist seit 2007 Professor für Immunologie. Zuvor war er Arbeitsgruppenleiter „T Zell Toleranz“ am Forschungsinstitut für Molekulare Pathologie in Wien. http://immuno.web.med.uni-muenchen.de/research/ag_klein/index.html [email protected] Privatdozent Dr. David Vöhringer leitet seit 2005 eine Emmy-Noether-Forschungsgruppe am Institut für Immunologie. http://immuno.web.med.uni-muenchen.de/research/ag_voehringer/index.html [email protected] August 05