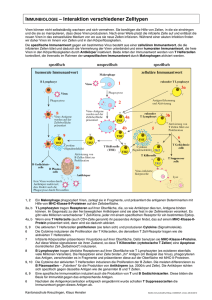
Der Einfluß früher Komplementfaktoren auf die Apoptose von B
Werbung

Aus dem Institut für Immunologie und Transfusionsmedizin der Universität zu Lübeck Direktor: Prof. Dr. med. H. Kirchner Der Einfluß früher Komplementfaktoren auf die Apoptose von B-Zellen im Rahmen der peripheren Toleranzinduktion Inauguraldissertation zur Erlangung der Doktorwürde der Universität zu Lübeck - aus der medizinischen Fakultät Vorgelegt von Kirstin Faust, geb. Lüddecke aus Ludwigshafen am Rhein Lübeck 2005 1. Berichterstatter: Priv.-Doz. Dr. med. Siegfried Görg 2. Berichterstatter: Prof. Dr. univ. (Univ. Budapest) Tamás Laskay Tag der mündlichen Prüfung: 13.7.2007 Zum Druck genehmigt Lübeck, den 13.7.2007 gez. Prof. Dr. med. Werner Solbach Dekan der Medizinischen Fakultät 2 für Dierk 3 Inhaltsverzeichnis Abkürzungen 6 1 Einleitung 8 1.1 Das Immunsystem und Autoimmunität 8 1.2 B-Lymphozyten 9 1.2.1 Entwicklung der B-Lymphozyten 1.2.2 Effektorfunktionen der B-Lymphozyten: die adaptive humorale Immunantwort 1.2.3 Produkte der B-Lymphozyten: Immunglobuline 1.3 Das Komplementsystem: Bindeglied zwischen angeborener und adaptiver Immunantwort 1.3.1 1.3.2 1.4 9 11 13 14 Allgemeine Funktionen des Komplementsystems Frühe Komplementkomponenten: Funktionen im Rahmen der erworbenen Immunität und der Toleranzinduktion 14 15 Toleranzentwicklung 19 1.4.1 Toleranzentwicklung der B-Zellen 1.4.2 Apoptose, ein Mechanismus der Toleranzinduktion 1.5 19 21 Systemischer Lupus Erythematodes (SLE) 1.5.1 23 Theorien zur Entstehung des SLE 24 1.6 Zielsetzung, Begründung der Fragestellung 27 2 Material und Methoden 28 2.1 Material 28 2.1.1 Mäuse 2.1.2 Zellinien (der in vitro Experimente) 2.1.3 Antigen 2.1.4 Antikörper (Ak) 2.2 28 28 29 29 Methoden 2.2.1 2.2.2 2.2.3 2.2.4 2.2.5 2.2.6 2.2.7 2.2.8 2.2.9 2.2.10 31 Immunisierung der Mäuse und Alumpräzipitation des Antigens Induktion von Apoptose Isolierung von Milzlymphozyten Durchflußfluoreszenzzytometrie TUNEL (TdT mediated dUTP nick end labeling) Immunhistochemie Blutentnahme ELISA zum Nachweis Np-spezifischer Antikörper Kopplung von Antikörpern an Biotin Statistik 31 31 32 34 35 36 39 39 42 42 4 3 Ergebnisse 43 3.1 Beeinflussung Antigeninduzierter Apoptose durch den Mangel früher Komplementkomponenten: Versuche in vivo 43 3.1.1 Immunhistochemische Färbungen 3.1.2 Analyse am Durchflußfluoreszenzzytometer 3.1.3 Antikörperbestimmung mittels ELISA 3.1.4 Beeinflussung des immunologischen Gedächtnisses durch Komplementmangel 3.2 45 47 48 55 Beeinflussung der Fas (CD95)-induzierten Apoptose durch frühe Komplementkomponenten: Versuche in vitro 61 3.2.1 Vorversuch 1: Phänotypische Eigenschaften der WEHI-Zellinien 3.2.2 Vorversuch 2: Apoptoseinduktion bei WEHI-Zellen 3.2.3 Der Einfluß von Komplement auf die Fas (CD95)-induzierte Apoptose von WEHI-Zellen 3.2.4 Vorversuch 3: Phänotypische Eigenschaften aufgereinigter Splenozyten 3.2.5 Der Einfluß von Komplement auf die Fas (CD95)-induzierte Apoptose von BLymphozyten der Milz 61 63 65 66 69 4 Diskussion 73 4.1 Antigeninduzierte Apoptose: Versuche in vivo 74 4.1.1 Die Humorale Immunantwort gegen Np 4.1.2 Hochdosis-Toleranz 4.1.3 Die Antigeninduzierte Apoptose 4.1.4 Beeinflussung des immunologischen Gedächtnisses durch die Antigeninduzierte Apoptose 4.2 74 77 78 84 Fas (CD95)-induzierte Apoptose: Versuche in vitro 89 4.2.1 Der Einfluß von Komplement auf die Fas (CD95)-induzierte Apoptose von Zellen der WEHI 231- und 279-Zellinien 4.2.2 Der Einfluß von Komplement auf die Fas (CD95)-induzierte Apoptose von BLymphozyten der Milz 4.3 5 90 94 Bedeutung der Ergebnisse für die periphere Toleranzinduktion der BLymphozyten und für die Entwicklung der Autoimmunerkrankung Systemischer Lupus Erythematodes (SLE) Zusammenfassung 99 102 Literatur 103 Danksagung 117 Kongressbeiträge und Veröffentlichungen 118 Lebenslauf 119 5 Abkürzungen aqua dest.: AEC: Ag: AI: Ak: Alum: AP: BE: BSA: BZR: c: C4: C4-/-: CD: CGG: CR2: Cr2-/DMSO: ELISA: Fas: FCS: FDC: Fitc: FS: GC HRP: IgG: Inj: i.p.: IDC: IL: KLH: Np: PBS: PE: PNA pNpP: rpm: destilliertes Wasser 3-Amino-9-Ethyl-Carbazole (Substrat für Immunhistochemie) Antigen Apoptoseinduzierende Injektion (Injektion einer hohen Dosis eines Antigens in die etablierte Immunantwort gegen jenes Antigen hinein) Antikörper Aluminumkaliumsulphat Alkaline Phosphatase (Enzym) Blutentnahme Bovines Serum Albumin (Trägerprotein) B-Zell-Rezeptor Konzentration Komplementfaktor 4 Knock-out-Mäuse, denen das Gen für den Komplementfaktor 4 fehlt Cluster of Differentiation (Oberflächenantigene) Chicken Gamma Globulin (Immunglobulin vom Huhn, Trägerprotein) Komplementrezeptor 2 Knock-out-Mäuse, denen das Gen für die Komplementrezeptoren 2/1 fehlt Dimethylsulfoxid (C20H16N2OH) Enzyme-linked immunosorbent assay (Enzym-Immuno-Assay) Apoptose induzierender Rezeptor (Apo-1, CD95), bindet TNF-ähnlichen FasLiganden (CD95L) Fetal Calf Serum (Fetales Kälberserum) Follikuläre Dendritische Zelle Fluoresceinisothiocyanat (Fluoreszenzfarbstoff) Forward Scatter (gebrochenes Licht im Durchflußfluoreszenzzytometer, Maß für Größe der Zelle) Germinal Centre (Keimzentrum) Horse Radish Peroxidase (Enzym) Immunglobulin der Klasse G Injektion intraperitoneal Interdigitierende Retikuläre Zelle Interleukin Keyhole Limpets Hemocyanin (Trägerprotein) 4-Hydroxy-3-Nitrophenylacetyl (Antigen) Phosphate Buffered Saline (phosphatgepufferte Kochsalzlösung) Phycoerythrin (Fluoreszenzfarbstoff) Peanut-Agglutinin (Selectin der Erdnuss) p-Nitrophenyl Phosphat (Substrat der Alkaline Phosphatase) Umdrehungen pro Minute 6 RT: SLE: SS: TdT: TNF: Tnp: TUNEL: w:m: wt: Raumtemperatur, ca. 22°C Systemischer Lupus Erythematodes (Autoimmunerkrankung) Sideward Scatter (seitlich weggebrochenes Licht im Durchflußfluoreszenzzytometer, Maß für Granularität der Zelle) Terminale Desoxynukleotidyltransferase (Enzym) Tumor Nekrose Faktor 2,4,6-Trinitrophenyl (Antigen) TdT mediated dUTP nick end labeling (Verfahren zum Nachweis apoptotischer Zellen) Verhältnis der von einer bestimmten Krankheit befallenen weiblichen zu den an der selben Erkrankung leidenden männlichen Patienten Wildtypmäuse 7 1 Einleitung 1.1 Das Immunsystem und Autoimmunität Das Immunsystem dient dem Schutz eines Körpers gegen fremde, potentiell schädigende Reize von außen. Es muß in der Lage sein, Fremdes von eigenem zu unterscheiden und die Reaktion daraufhin anzupassen, d.h. Körpereigenes zu tolerieren und Körperfremdes wirksam zu bekämpfen1. Das Immunsystem läßt sich einteilen in angeborene und erworbene Immunität. Die Komponenten des angeborenen Immunsystems, wie z.B. die phagozytären Zellen, sind in der Lage, eine große Gruppe eindringende Erreger anhand bestimmter, feststehender Erkennungsmoleküle als fremd zu identifizieren und diese schnell unschädlich zu machen. Die Komponenten des sog. erworbenen Immunsystems, deren Reaktion man auch als adaptive („anpassungsfähige“) Immunantwort bezeichnet, sind in der Lage, neue Strukturen auf potentiell schädlichen „Eindringlingen“ zu erkennen und zu bekämpfen. Jede der Zellen des adaptiven Immunsystems (wie B- oder T-Lymphozyten) erwirbt während ihrer Entwicklung die Fähigkeit eine definierte Struktur, das „Antigen“, mit Hilfe bestimmter Rezeptoren (T-Zell-Rezeptor, Immunglobuline der B-Zellen) zu erkennen und eine Immunantwort gegen diese einzuleiten. (Tab.1) Merkmale der adaptiven (erworbenen) Immunantwort Erkennungsmoleküle der Wirbeltiere werden in jedem Individuum neu entwickelt Rezeptoren und Antikörper (Immunglobuline) haben eine hohe Variabilität (Diversität) Verstärkung beim zweiten Kontakt Gedächtnis neuentwickelte Antikörper sind potentiell autoreaktiv Tabelle 1: Merkmale der adaptiven Immunantwort Dabei besteht die Gefahr, daß Zellen entstehen, die körpereigene Antigene fälschlicherweise als fremd erkennen und bekämpfen. Verschiedene Mechanismen, wie die Induktion des Zelltods („Apoptose“) oder die Inaktivierung („Anergie“) solcher autoreaktiver Zellen, sorgen physiologischerweise für die Toleranz des Immunsystems dem eigenen Körper gegenüber. Diese Toleranzinduktion ist sehr effektiv und wird durch ein komplexes System reguliert, das bis heute nicht ganz verstanden ist. Dennoch kommt 8 es immer wieder vor, daß Zellen des Immunsystems, deren Aufgabe es eigentlich ist, einen Organismus schützen, diesen angreifen. Es kommt zur Autoimmunität. Ein Beispiel für das Versagen der Toleranzerhaltung ist die Autoimmunerkrankung Systemischer Lupus Erythematodes (SLE), bei der antigenspezifische Proteine (Antikörper) gegen körpereigene Antigene von autoreaktiven B-Lymphozyten (Zellen des erworbenen Immunsystems) gebildet werden. Der wichtigste genetische Risikofaktor für diese Erkrankung ist der Mangel an frühen Komplementkomponenten (C1, C4 und C2). Das Komplementsystem besteht aus einer Gruppe von Serumproteinen, die verschiedene Funktionen sowohl in der angeborenen als auch in der erworbenen Immunität erfüllen. In dieser Arbeit möchte ich auf den Zusammenhang zwischen dem Mangel an frühen Komplementkomponenten und der Entstehung von autoreaktiven B-Lymphozyten, deren Produkte dann pathogenetisch für die Autoimmunerkrankung SLE bedeutsam sind, eingehen. Dazu wird der Einfluß des Komplementmangels auf einen bestimmten Schritt der peripheren Toleranzentwicklung untersucht: die Apoptose von potentiell autoreaktiven B-Zellen im Keimzentrum. 1.2 B-Lymphozyten 1.2.1 Entwicklung der B-Lymphozyten Die Bildung der B-Lymphozyten beginnt bei Säugetieren in der fetalen Leber. Nach der Geburt setzt sich dieser Prozeß im Knochenmark fort. (Abb.1, S.10) Dort entwickeln sie sich von frühen Pro-B-Zellen (Vorläuferzellen, die von pluripotenten hämatopoetischen Stammzellen abstammen) über verschiedene weitere Stadien zu naiven B-Zellen, die das Knochenmark verlassen und in die peripheren Lymphorgane auswandern. Zu diesem Zeitpunkt tragen die B-Lymphozyten schon charakteristische Merkmale: sie exprimieren auf ihrer Oberfläche den B-Zell-Rezeptor (ein membranständiges Immunglobulin der Klasse M) und den noch unvollständigen Korezeptorkomplex bestehend aus CD19 und TAPA-1 (CD81). (Abb.2, S.10) Außerdem tragen sie weitere Rezeptoren, wie CD45R (B220), CD40, CD20 und MHC-Moleküle der Klasse II. 9 Zentral: Knochenmark Entwicklung Stammzelle Pro- Prä- Peripher: Milz, Lymphknoten, ... unreife reife/ Zentroblast Zentrozyt Plasmazelle naive m-IgM, s-IgM, s-IgG, ss-IgM m-IgD s-IgG IgA, s-IgE vollständiger Korezeptorkomplex (CD19, CD21/35, CD81...) Keimzentrum: Proliferation/ somatische Mutation/IgKlassenwechsel m-µm-IgM Kette wenig CD19 Korezeptoren CD19 Rekombination unterschiedlicher Immunität/ V-D-J Kopplung schwerer und Diversität leichter Ketten Antigeninduzierte Apoptose (jedes follikuläre Antigen), Anergie, RezeptorToleranzinduktion Exklusion Editierung Immunglobuline Abbildung 1: Antigeninduzierte Apoptose (hohe Konz.), Fas-induzierte Apoptose Entwicklung der B-Lymphozyten2 Nachdem die B-Zellen das Knochenmark verlassen haben, zirkulieren sie mit dem Blut und der Lymphe durch die sekundären lymphatischen Organe des Körpers, wie Milz, Lymphknoten, oder die lymphatischen Gewebe der Schleimhäute. Dort findet man die BZellen vor allem in abgegrenzten Regionen, den Follikeln. Ruhende reife B-Zellen scheinen das spezielle Mikromilieu, das von den dortigen Stromazellen und den Follikulären Dendritischen Zellen (FDC) gebildet wird, zum Überleben zu benötigen3-5. Diese reifen B-Zellen unterscheiden sich von den unreifen B-Zellen des Knochenmarkes durch einige Oberflächenmoleküle. Sie exprimieren zusätzlich zu dem Immunglobulin der Klasse M eines der Klasse D (IgD), sowie einen vollständigen Korezeptorkomplex inkl. des Komplementrezeptors 2 (CD21)6. (Abb.2) Abbildung 2: B-Zellrezeptor (BZR) und Korezeptorkomplex (CD81/TAPA,CD19,CD21/CR2) (Quelle:www.immunology.klimov.tom.ru/fig35.gif) 10 1.2.2 Effektorfunktionen der B-Lymphozyten: die adaptive humorale Immunantwort Ein wichtiger Bestandteil der adaptiven humoralen Immunantwort (humoral von lat. humor, Flüssigkeit, d.h. den nicht zellulären Anteilen) sind die Antikörper oder Immunglobuline, welche von den B-Lymphozyten produziert werden. Um Antikörper gegen ein bestimmtes Antigen produzieren zu können, muß die reife, für das spezielle Antigen spezifische B-Zelle aktiviert werden. Bei der Immunantwort gegen T-Zellabhängige Antigene, wie z.B. Proteinstrukturen auf Bakterien, geschieht dies durch Interaktion der B-Zellen mit anderen Zellen des Immunsystems, wie beispielsweise antigenpräsentierenden Zellen oder T-Lymphozten, die für das gleiche Antigen spezifisch sind7. Dringt ein Antigen in den Körper ein, so wird es von Zellen des phagozytären Systems aufgenommen und in die T-Zell-Zone der sekundären lymphatischen Organe transportiert4. Dort wird es von Interdigitierenden Retikulären Zellen (IDC) festgehalten, verarbeitet, und zirkulierenden B- und T-Lymphozyten präsentiert. Zellen mit für dieses Antigen spezifischen Rezeptoren werden in dieser Zone festgehalten und können interagieren und proliferieren8. T-Helferzellen, eine Unterart der T-Lymphozyten, regen B-Zellen wahrscheinlich über Interaktion mit dem Rezeptor CD40 der B-Zellen und eine Reihe von Zytokinen wie IL-4, 5 und 6 zur Proliferation an9-11 und bilden zusammen mit diesen sog. primäre oder extrafollikuläre Foci12. In diesen Foci reifen einige der B-Zellen weiter aus8 und beginnen die Produktion erster Antikörper gegen das Antigen8 noch mit niedriger Affiniät13. Die Foci in der T-Zell-Zone bleiben bis ca. zum zehnten Tag nach dem ersten Kontakt mit dem Antigen bestehen. Sie sind verantwortlich für den ersten Teil der adaptiven Immunantwort. Etwa vier Tage nach Kontakt mit dem Antigen wandern einige der aktivierten, aber noch nicht ausgereiften B-Zellen zusammen mit den T-Zellen, von denen sie aktiviert wurden, in die Follikel der B-Zell-Zone der lymphatischen Organe aus8,14,15. Dort bilden sie zusammen mit den dort ansässigen FDCs sog. Keimzentren (GC), hochkomplexe Strukturen weiterer Reifung und Proliferation von B-Lymphozyten8. (Abb.3, S.12) 11 Abbildung 3: Schematischer Aufbau eines Keimzentrums im lymphatischen Gewebe umgeben von ruhenden Lymphozyten der Follikel In der „dunklen“ Zone des Keimzentrum machen die B-Zellen, nun Zentroblasten genannt, eine Phase intensiver Proliferation durch. Dabei kommt es verstärkt zu Punktmutationen innerhalb der Gene für die Immunglobuline16. Durch diesen Prozeß, der als Somatische Hypermutation bezeichnet wird, entstehen B-Zell-Klone mit leicht modifizierten Rezeptoren17. Diese Klone können das zu bekämpfende Antigen entweder mit höherer, niedrigerer oder derselben Affinität erkennen als der Ausgangsklon. In der „hellen“ Zone des Keimzentrums konkurrieren die so entstandenen B-Zellen, Zentrozyten, untereinander um das auf den dortigen FDCs in Form von Antikörper-Antigen-Komplement-Komplexen gebundene Antigen8. Nur Zellen, die das Antigen mit höherer Affinität binden, erhalten kostimulatorische Signale, die für Ihr Überleben notwendig sind18. Die anderen sterben ab oder werden anergisch15. Durch diesen Selektionsprozeß, den man auch als Affinitätsreifung bezeichnet, wird sichergestellt, daß B-Zellen mit immer höherer Spezifität für das Antigen entstehen8,9. Diese hochaffinen Zentrozyten reifen unter dem Einfluß von T-Helferzellen19 weiter aus und wechseln die Immunglobulinklasse20, wobei sich ein Teil von ihnen zu langlebigen BGedächtniszellen differenziert, und der Großteil als antikörpersezernierende Plasmazellen ins Knochenmark wandert21-23. Die Gedächtniszellen (erkennbar an einigen Oberflächenmarkern wie CD3824, CD4425 und IgD20) sorgen im Rahmen einer zweiten Immunreaktion gegen das gleiche Antigen für eine schnellere und gerichtetere Immunantwort26. 12 1.2.3 Produkte der B-Lymphozyten: Immunglobuline Immunglobuline sind die antigenspezifischen Produkte von B-Lymphozyten. Sezerniert tragen sie als Antikörper entscheidend zum Erfolg der adaptiven Immunantwort bei, membranständig beeinflussen sie als B-Zell-Rezeptor (oder Antigenrezeptor) das Schicksal der Zelle. Alle von einer bestimmten Zelle produzierten Antikörper (membrangebunden oder in löslicher Form) weisen dieselbe Struktur ihrer variablen Region auf, d.h. sie sind zunächst für dasselbe Antigen spezifisch. (Abb.4) Beispielhaft seien hier einige der Funktionen von Antikörpern genannt: Markierung von Fremdkörper wie Bakterien für das Immunsystem („Opsonisierung“), Neutralisation von Toxinen oder Viren, und das Auslösen der Komplementkaskade. Abbildung 4: Aufbau eines Immunglobulins Das Antikörpermolekül selbst besteht aus vier Aminosäureketten, zwei schweren (H) und zwei leichten (L), die jeweils aus zwei Teilen bestehen: der antigenbindenden Region, die von Antikörper zu Antikörper sehr unterschiedlich ist, und deshalb als variable Region bezeichnet wird, und der konstanten Region, die die Effektormechanismen des Immunsystems auslöst, von der es nur fünf Hauptformen oder Isotypen gibt. Dabei kann eine variable Region zusammen mit jeder beliebigen konstanten Region exprimiert werden, dies erfolgt durch den Klassenwechsel. Die fünf Hauptformen oder Isotypen der Immunglobuline sind IgM, IgG, IgD, IgA und IgE, wobei beim Menschen noch die Unterklassen IgA1 und IgA2 sowie IgG1-4 unterschieden werden. Bei Mäusen werden die Unterklassen IgG1, IgG2a, IgG2b und IgG3 unterschieden27. Unreife B-Zellen exprimieren zunächst IgM, nach Ausreifung auch IgD. Nach ihrer vollständigen Reifung zu Plasmazellen sezernieren sie zunächst auch nur Antikörper der Klasse IgM. Somit sind die ersten Antikörper, die im Laufe einer Immunantwort gegen ein Antigen gebildet werden, IgM-Antikörper. Erst später, nach weiterer Aktivierung der Zellen in Keimzentren, erfolgt der Klassenwechsel zu einem der anderen Isotypen. Je nach Art der Infektion bilden die Zellen dann IgG-, IgA- oder IgE-Antikörper. Dabei kommt beispielsweise IgA beim Schutz der Schleimhäute, IgE bei der Mastzellaktivierung zur Abwehr parasitärer Infektionen, IgG1 und IgG3 (IgG2b bei der Maus) in der Abwehr 13 bakterieller7 und IgG2 (IgG2a bei der Maus) in der Abwehr viraler Infektionen7,28 besondere Bedeutung zu. Über die Funktion des IgG4 (IgG3 der Maus) ist noch wenig bekannt. Diese unterschiedliche Differenzierung der B-Lymphozyten wird durch verschiedene Zytokine, die von zwei unterschiedliche Untergruppen der T-Helferzellen (TH-1- und TH-2-Zellen) sezerniert werden, induziert. So wird die Immunantwort gegen eine Proteinantigen oder ein proteingebundenes Hapten über die Ausschüttung von IL-4 durch TH-1-Zellen ebenfalls IgG1-dominiert7. 1.3 Das Komplementsystem: Bindeglied zwischen angeborener und adaptiver Immunantwort 1.3.1 Allgemeine Funktionen des Komplementsystems Eine Gruppe von ca. 30 verschiedenen Plasmaproteinen, die nach der Reihenfolge ihrer Entdeckung mit C1-9 sowie einigen Buchstabenkombinationen benannt werden, wird als Komplementsystem bezeichnet29,30. Komplement spielt eine zentrale Rolle in vielen Bereichen des Immunsystems wie bei der Abwehr von bakteriellen Erregern, bei der Modulation von Entzündungsreaktionen, bei der Eliminierung von Immunkomplexen und bei der Regulation der Antikörperproduktion. Derzeit sind drei Möglichkeiten zur Aktivierung der Effektorfunktionen von Komplement bekannt: der klassische, der alternative und der Mannose-bindendes-Lektin (MBL)-Weg. Beim klassischen Weg erfolgt die Komplementaktivierung durch Immunkomplexe, bestehend aus Antigenen (z.B. Epitopen auf Krankheitserregern) und Antikörpern wie IgM und IgG. Über die Komplementfaktoren C1q, r und s wird C4 gespalten und damit aktiviert. Das größere Spaltprodukt von C4, C4b (das kleinere wird als C4a bezeichnet) bindet an eine Zieloberfläche und bildet gemeinsam mit C2 eine C3-Konvertase. Beim alternativen Weg wird die spontan aktivierte Komplementkomponente C3 direkt an die Pathogenoberfläche gebunden und bildet mit weiteren Faktoren ebenfalls eine C3Konvertase. Ein relativ neu entdeckter weiterer Aktivierungsweg erfolgt über MBL, eine Serumkomponente, welche an Mannose- oder N-acetylglukosaminhaltige Proteine oder Kohlenhydrate auf teilweise verkapselten Bakterien bindet und dort eine Komplementaktivierung ermöglicht. Die gemeinsame Endstrecke aller drei Wege verläuft über die C3-Konvertase, die in der Lage ist, C3 zu spalten und so zu aktivieren. C3b induziert dann die Aktivierung weiterer 14 Komplementfaktoren wie C5-C9. Diese bilden den Membranangriffskomplex (MAC), einen Komplex aus mehreren Proteinen, der eine Pore in der Membran bildet. (Abb.5) Das Durchbrechen der Membran führt dann zu Verlust der zellulären Homöostase und schließlich zur Zerstörung der Zelle /des Pathogens. Abbildung 5: Funktionen der verschiedenen Komplementspaltprodukte Komplementspaltprodukte wie C3b, C3a, C4a oder C5a haben noch weitere Funktionen im Rahmen der angeborenen 31 Analphylatoxine , d.h. Immunität: sie wirken Entzündungsmediatoren, die auch als u.a. Opsonine oder Vasopermeabilität, Mastzelldegranulation und Leukozytenchemotaxis beeinflussen. (Abb.5) Des weiteren spielen Komplementfaktoren in der Beseitigung von zirkulierenden Immunkomplexen sowie von apoptotischem Zellmaterial eine Rolle32,33. C1, C4 und C3 binden an die Immunkomplexe, wobei C1q die Löslichkeit von solchen zirkulierenden Komplexen erhöht, und deren Präzipitation in Geweben verhindert34. C3b und C4d fördern wahrscheinlich die Aufnahme der Immunkomplexe über zugehörige Rezeptoren auf Zellen des phagozytären Systems35. (Abb.5) 1.3.2 Frühe Komplementkomponenten: Funktionen im Rahmen der erworbenen Immunität und der Toleranzinduktion Die Bedeutung des Komplementsystems für die adaptive humorale Immunantwort konnte bereits 1972 durch die Anwendung des Cobra Venum Factor (Dekomplementierung) gezeigt werden36. Seitdem wurde diese Beobachtung in verschiedenen Modellen bestätigt (Übersicht37-39). In späteren Arbeiten konnte unter Verwendung von Knock-out-Mäusen 15 die Bedeutung einzelner Komponenten des klassischen Aktivierungsweges (C1q40, C2, C336,39 und C439) für die humorale Immunantwort präzisiert werden. Vor allem diese „frühen“ Komponenten des klassischen Aktivierungsweges beeinflussen die Antikörperbildung. Im Verlauf der Komplementaktivierung kommt es dabei zur Integration von C3d in Immunkomplexe41. (Abb.5, S.15) Ihre Wirkung auf die humorale Immunantwort entfalten die Komplementkomponenten über die spezifische Bindung an Komplementrezeptoren42-44. (Tab.2) In der vorliegenden Arbeit wird vor allem auf die Bedeutung des für die B-Zell-Funktion wichtigen Komplementrezeptors 2 (CR2, CD21) eingegangen. Dieser Rezeptor wird bei Mäusen auf dem gleichen Gen codiert wie der Komplementrezeptor 1 (CR1, CD35). Durch alternatives „Splicen“ entstehen die beiden Rezeptoren, die einen sehr ähnlichen Aufbau haben. Vor allem im murinen System ist es bis jetzt nicht möglich, alle Funktionen der beiden Rezeptoren klar zu unterscheiden45, weshalb diese in vielen Veröffentlichungen zu CD21/35 (CR2/1) zusammengefaßt werden. Name Liganden Vorkommen Auswahl von bekannten / vermuteten Funktionen stimuliert Phagozytose, CR1 (CD35) C3b, C4b, B-Zellen, FDCs, Granulozyten, Transport von Immunkomplexen C3d, iC3b, Monozyten/ Makrophagen, durch Erythrozyten46 C3dg, C4d Erythrozyten Verstärkung der Immunantwort Toleranzentwicklung? CR2 (CD21) C3dg,C4d, iC3b CD18) CR4 (CD11c/ CD18) Tabelle 2: reife B-Zellen, FDCs CD23 CR3 (CD11b/ Teil des B-Zell- C3d, iC3b, C3dg, iC3b Korezeptorkomplexes Verstärkung der Immunantwort Toleranzentwicklung? Monozyten /Makrophagen, NKZellen, Granulozyten stimuliert Phagozytose Monozyten /Makrophagen, aktivierte B-Zellen, Granulozyten, stimuliert Phagozytose Thrombozyten Komplementrezeptoren, deren Nomenklatur und Liganden im murinen System10,47-49 (Die kleinen Buchstaben kennzeichnen die unterschiedlichen Spaltprodukte der Komplementkomponenten) 16 Ein Fehlen der Rezeptoren (CR2/1, CD21/35) wie bei Knock-out-Mäusen (Cr2-/-) macht sich in einer reduzierten Antikörperantwort auf T-Zell-abhängige Antigene bemerkbar43,5054 . Vor allem die Bildung von Keimzentren zur Produktion hochaffiner Antikörper und Gedächtniszellen scheint durch den Mangel oder die Blockade von Komplement oder Komplementrezeptoren gestört39,55-57. Die Immunantwort gegen T-Zell-unabhängige Antigene und bekapselte Bakterien ist bei Cr2-/-Mäusen ebenfalls stark eingeschränkt54. Man findet diese Rezeptoren vor allem auf zwei für die Etablierung der Antikörperantwort wichtigen Zellpopulationen: auf den B-Lymphozyten, wobei der Komplementrezeptor 2 (CD21) Teil des Korezeptorkomplexes ist58,59 (im Gegensatz zu CD3553), und auf den Follikulären Dendritischen Zellen (FDC) der B-Zell-Zonen in den peripheren lymphatischen Organen58. Auf beiden Zellpopulationen hat eine Stimulation von CD21/35 Auswirkungen auf den Verlauf einer Immunantwort. Dabei können frühe Komplementkomponenten direkt oder indirekt über C3 (klassischer Aktivierungsweg) als Liganden der Rezeptoren CD21 oder der alternativen Spliceform CD35 wirken. Die Stimulation des Korezeptorkomplexes, zu dem auch CD21 gehört, zusammen mit der Stimulation des B-Zell-Rezeptors verstärkt dessen Signal innerhalb der B-Zelle60,61, sodaß man, falls das Antigen mit Komplement (C3d) besetzt ist, eine geringere Dosis des Antigens benötigt, um eine humorale Immunantwort auszulösen62. (Abb.5, S.15) Die Stimulation des Korezeptorkomplexes zusammen mit dem B-Zellrezeptor scheint die Schwelle, die für die Reaktion der Zelle auf den Stimulus „Antigen“ notwendig ist, zu senken59. Die Funktion von CD21 auf B-Zellen ist nicht auf die Aufgaben als Teil des Korezeptorkomplexes beschränkt43,62,63. Die alleinige Kreuzvernetzung von CD21/35 kann B-Zellen aktivieren61,64. Um innerhalb eines Keimzentrums zu überleben benötigt eine BZelle die Stimulation von CD21/35, z.B. über die Bindung von CD23, einem sowohl löslich als auch membranös vorliegendem Liganden von CR2/158,65. B-Zellen von Komplementrezeptor-Knock-out-Mäuse (Cr2-/-) verlieren den Konkurrenzkampf mit normalen B-Zellen um follikuläre Retention und damit um das Überleben im Keimzentrum66. Die Bedeutung von CD21/35 für die humorale Immunantwort liegt nicht nur in dessen Präsenz auf B-Zellen, sondern begründet sich auch in seiner Funktion auf Follikulären Dendritischen Zellen (FDC) des Keimzentrums. Dort kann der Komplementrezeptor 2/1 komplementbehaftete Immunkomplexe festhalten, und damit den proliferierenden B-Zellen 17 das Antigen wirksamer präsentieren43,67,68. Dies scheint insbesondere für die Entwicklung einer Gedächtniszellfunktion vonnöten zu sein69. Neben der Bedeutung des Komplementsystems für die humorale Immunantwort (positive Regulation von B-Zellen) gibt es viele Hinweise darauf, daß auch die Toleranzinduktion (negative B-Zell-Regulation, Kapitel 1.4.1) von Komplement beeinflußt wird54,70,71. Es konnte gezeigt werden, daß CD21 und CD35 (CD21/35) einen Einfluß auf die Toleranzinduktion von B-Zellen haben70,72,73. Zudem gibt es Hinweise auf einen Zusammenhang von CD21/35-Defizienz und der Autoimmunerkrankung SLE45,48,63,70. (Kapitel 1.5.1) Auch eine CD21/35-unabhängige Regulation der Toleranzentwicklung durch Komplementfaktoren ist denkbar. Verschiedene Ergebnisse zeigen die Notwendigkeit der frühen Komplementkomponenten C1q und C4 für die Aufrechterhaltung der Selbsttoleranz unabhängig von C3 und den bekannten Komplementrezeptoren4,58,74. Auf welche Strukturen C1q und C4 direkt wirken sollen, und über welche Mechanismen eine Reaktion ausgelöst wird, ist jedoch noch nicht bekannt, und wird in dieser Arbeit diskutiert. Komplement in der erworbenen Immunität Komplementrezeptoren auf reifen naiven (ruhenden) B-Zellen ermöglichen das Überleben im Follikel Komplementrezeptoren auf reifen B-Zellen reduzieren den für deren Aktivierung nötigen Schwellenwert und erleichtern damit eine Immunantwort bei suboptimalen Antigenkonzentrationen43 Komplementrezeptoren auf Follikulären Dendritischen Zellen (FDC) im Keimzentrum werden für die effektive Präsentation des Antigens benötigt Bedeutung in der Toleranzinduktion von B-Zellen Tabelle 3: Funktionen früher Komplementkomponenten im Rahmen der adaptiven (erworbenen) Immunantwort Zusammenfassend läßt sich sagen, daß vor allem frühe Komplementkomponenten wie C1, C2, C3 und C4 eine wichtige Rolle im Ablauf der adaptiven Immunantwort sowie der Toleranzinduktion spielen. (Tab.3) 18 1.4 Toleranzentwicklung 1.4.1 Toleranzentwicklung der B-Zellen Bei der Entwicklung der B-Lymphozyten entstehen Zellen, von denen jede ein bestimmtes Antigen aus einer Vielzahl von möglichen Antigenen erkennt. Darunter können auch Selbstantigene, d.h. Merkmale körpereigener Zellen, sein. Um solche selbstreaktiven Zellen zu identifizieren und unschädlich zu machen, haben sich im Laufe der Evolution verschiedene Mechanismen herausgebildet, deren Gesamtheit als Toleranzentwicklung bezeichnet wird. Nach dem Ort, an dem sich diese Selektion abspielt, unterscheidet man zentrale und periphere Toleranzinduktion75. Da im Knochenmark, dem Ort der zentralen Toleranzentwicklung, in der Regel nur körpereigene Antigene präsent sind, werden bei der zentralen Toleranzentwicklung alle Zellen, die im Knochenmark Antigen binden, in ihrer Entwicklung unterdrückt76. So können unreife B-Lymphozyten, deren Immunglobulingene zu einem autoreaktiven IgMRezeptor rekombiniert wurden, entweder absterben77, inaktiviert überleben („anergisch“ werden)77,78 oder ihre Immunglobulingene neu arrangieren79. Ziel ist es, nur selbsttolerante Zellen in die Peripherie zu entlassen. (Tab.4) Zentrale Toleranz von B-Zellen negative Selektion: jedes Antigen im Knochenmark induziert in unreifen B-Zellen Toleranz: hohe Affinität des B-Zell-Rezeptors zu dem präsentierten Antigen/ membrangebundenes Antigen: Rezeptoreditierung (Austausch eines Teiles des Rezeptors, „zweite Chance“) oder Apoptose (programmierter Zelltod) niedrige Affinität des B-Zell-Rezeptors zu dem präsentierten Antigen/ lösliches Antigen: Anergie (Reduzierte Lebensdauer, reduzierte Aktivierbarkeit) Tabelle 4: Mechanismen der zentralen Toleranzentwicklung von B-Zellen6 Autoreaktive Zellen, die den zentralen Selektionsprozeß überlebt haben (anergische Zellen oder Zellen, die einen Rezeptor für ein nicht im Knochenmark präsentes Selbstantigen tragen), können auch später noch im Rahmen der peripheren Toleranzinduktion8,76 durch mangelnde Aktivierung in den peripheren lymphatischen Geweben (follikuläre Exklusion)3,5,78 oder direkt über zytotoxische T-Lymphozyten78 abgetötet werden. 19 Auch bei dem Prozeß der somatischen Hypermutation der B-Zellen in den Keimzentren der peripheren lymphatischen Gewebe können autoreaktive B-Zellen entstehen8,17,80. Die Elimination dieser Zellen ist ebenfalls ein Teil der peripheren Toleranzinduktion81. (Tab.5) Periphere Toleranz von B-Zellen im Keimzentrum Überleben im Keimzentrum nur mit Hilfe kostimulatorischer Signale, bei fehlender Stimulation =>Apoptose der B-Zelle Keine T-Zelle mit einem für das Autoantigen passenden Rezeptor => keine Kostimulation der autoreaktiven B-Zelle =>Apoptose der autoreaktiven B-Zelle Antigeninduzierte Apoptose durch hohe Konzentrationen an Antigen (Besetzung der B-Zell-Rezeptoren mit Antigen => dadurch keine kostimulatorischen Signale von FDC => Apoptose der B-Zellen) Fas (CD95)-induzierte Apoptose durch zytotoxische T-Zellen verschiedene Einflußfaktoren auf die Apoptose im Keimzentrum Einfluß von Komplement? Tabelle 5: Modell der peripheren Toleranzinduktion Ein Teil der so entstandenen autoreaktiven B-Zellen wird durch fehlende Kostimulation eliminiert: die im Keimzentrum proliferierenden B-Zellen (Zentrozyten) können nur mit Hilfe kostimulatorischer Signale von T-Lymphozyten (CD 154/CD40) oder antigenpräsentierenden FDC (B-Zell-Rezeptor) überleben82. Es sollte aufgrund der Toleranzinduktion in der Entwicklung der T-Lymphozyten keine T-Helferzelle geben, die dasselbe Antigen wie eine potentiell autoreaktive B-Zelle erkennt und die weitere Entwicklung dieser Zelle fördert9,83. Einer solchen B-Zelle fehlt somit die Stimulation von CD40 durch T-Zellen. Dazu kommt, daß eine B-Zelle, die in der somatischen Hypermutation ihren Rezeptor so verändert, daß dieser nun Selbstantigen erkennt, das auf den FDCs präsentierte Fremdantigen wahrscheinlich schlechter als konkurrierende Zentrozyten erkennt. Diese autoreaktive Zelle erhält somit keine kostimulatorischen Signale von den FDCs9. Da die Signale von FDCs und T-Helferzellen für das Überleben der B-Lymphozyten im Keimzentrum notwendig sind, wird eine solche B-Zelle in den meisten Fällen apoptotisch13,76, d.h. sie stirbt ab und wird von umliegenden Makrophagen phagozytiert. Ein weiterer Mechanismus der Selektion soll den Körper wahrscheinlich vor der Entstehung von Autoantikörpern gegen lösliche, in den Keimzentren in großer Zahl 20 vorhandenen Antigenen -wie beispielsweise den Serumproteinen- schützen: eine extrem hohe Konzentration an löslichem Antigen in einem Keimzentrum löst in einer für dieses Antigen spezifischen B-Zelle Apoptose aus (Antigeninduzierte Apoptose). (Tab.5, S.20) Auch im Keimzentrum töten zytotoxische T-Lymphozyten autoreaktive B-Zellen über Stimulation von deren Fas-Rezeptors (CD95)8,47,78,84,85. Auf welche Signale hin diese Selektion geschieht, ist nicht abschließend geklärt. Sicher ist, daß eine Vielzahl regulierender Faktoren (z.B. IL-4) einen Einfluß auf das Schicksal einer potentiell autoreaktiven B-Zellen hat86. Ob Komplementkomponenten die Apoptose von potentiell autoreaktiven B-Zellen im Keimzentrum beeinflussen können, wird in dieser Arbeit untersucht. Obwohl verschiedene Mechanismen der peripheren Toleranzinduktion bekannt sind, ist bislang nicht erforscht, welche bei der Entstehung von Autoimmunerkrankungen versagen, oder ob möglicherweise noch unbekannte Toleranzmechanismen einer Rolle spielen. 1.4.2 Apoptose, ein Mechanismus der Toleranzinduktion Apoptose, eine Form des programmierten Zelltodes87, ist einer der wichtigsten Mechanismen der Toleranzinduktion. Man beschreibt seit 1972 mit diesem Begriff ein Programm von aktiven Vorgängen in einer Zelle, die letztendlich zum Tod derselben führen. Verantwortlich für diesen Prozeß sind eine Reihe von intrazellulären Enzymen wie die Caspasen, die für den korrekten Ablauf der Apoptose sorgen76. Apoptose im Rahmen der B-Zellentwicklung Im Knochenmark: Apoptose von unreifen B-Lymphozyten, die Selbstantigen erkennen oder einen inaktiven B-Zell-Rezeptor präsentieren In der Peripherie: Apoptose bei follikulärer Exklusion Im Keimzentrum: vermutlich Apoptose von B-Zellen mit autoreaktiven und niedrigaffinen Rezeptoren Nach abgelaufener Immunantwort: Apoptose der nicht mehr benötigten antikörpersezernierenden Zellen vermutlich Regulation der B-Gedächtniszellen und Plasmazellen Tabelle 6: Beispiele für Apoptose im Rahmen der B-Zellentwicklung6 21 Ein funktionsfähiger Apoptosemechanismus ist für den physiologischen Ablauf der Immunantwort und vor allem für die Entwicklung der Selbsttoleranz von großer Bedeutung. Dies zeigt sich eindrücklich an transgenen Tiermodellen, die Defekte in verschiedenen für die Apoptose wichtigen Proteinen haben76. So entwickeln beispielsweise lpr-Mäuse, denen ein funktionsfähiger Fas-Rezeptor (CD95) fehlt, oder gld-Mäuse, die den dazugehörigen Liganden Fas-L (CD95L) nicht exprimieren, Zeichen der Autoimmunerkrankung SLE76,88,89. (Tab.6, S.21) Es können zwei verschiedene Formen der Apoptose unterschieden werden, die durch unterschiedliche Faktoren induziert werden. Auch regulieren unterschiedliche intrazelluläre Proteine (u.a. bcl-2, bax) den Ablauf der beiden Apoptoseformen76,90,91. Eine Form der Apoptose (intrinsische oder mitochondriale Apoptose), wird bei BLymphozyten durch Zellgifte, ionisierende Strahlung, Nährstoffmangel oder ein starkes Signal des Antigenrezeptors ohne gleichzeitige T-Zell-Hilfe92-94 ausgelöst, und beginnt mit dem Abfall des transmembranen Potentials der Mitochondrien. Dadurch werden verschiedene Moleküle wie Cytochrom C freigesetzt, die ihrerseits über intrazelluläre Proteine (z.B. der bcl-2-Familie) die Bildung der Caspasen induzieren6,76. Die zweite Form der Apoptose (extrinsische oder TNF-Rezeptor-assoziierte Apoptose) wird durch die Stimulation von Oberflächenrezeptoren ansonsten intakter Zellen ausgelöst. Diese Rezeptoren, wie der Fas-Rezeptor (CD95), aktivieren die Caspasen direkt6,76. Sind die Caspasen aktiviert, so ist bei beiden Formen der weitere Ablauf sehr ähnlich. Eine Zelle, die über einen der auslösenden Faktoren ein Signal zur Einleitung der Apoptose erhalten hat, zeigt deutliche Zeichen der Dehydratation: sie wird kleiner und schmaler und intrazelluläres Kalzium wird mobilisiert95. Zusätzlich wird der Zellkerninhalt kondensiert und die nukleäre DNA durch endogene Nukleasen fragmentiert, während der Zellkern und mikrotubuläre Strukturen aufgelöst werden. Obwohl das transmembrane Potential der Mitochondrien dabei deutlich erniedrigt ist, bleiben diese und andere Zellorganellen zunächst intakt und funktionsfähig96. Gegen Ende des apoptotischen Programms werden Teile des Zytoplasmas zusammen mit den Zellorganellen und den DNA-Stücken in Vesikel „verpackt“ und ausgeschleust. In vivo werden diese sog. apoptotische Körperchen dann von umliegenden Makrophagen an Oberflächenstrukturveränderungen (z.B. dem Erscheinen von Phosphatidylserin33) erkannt und phagozytiert, ohne daß entzündungserregende Zellbestandteile in den Extrazellulärraum dringen können97. Dies unterscheidet die aktiv ablaufende Apoptose 22 normalerweise von anderen, passiven Formen des Zelltodes wie der Nekrose98. Dennoch kann auch bei dem Prozeß der Apoptose eine Immunreaktion gegen Zellbestandteile ausgelöst werden99. Das schematisiert ablaufende Programm des aktiven Zelltodes ermöglicht es, apoptotische Zellen mittels verschiedene Testverfahren kenntlich zu machen, was teilweise auch in dieser Arbeit genutzt wurde. (Tab.7) Merkmal Testverfahren Schrumpfung der Zelle Lichtmikroskopische Auszählung DNA-Fragmentierung (sog. Laddering) PCR, TUNEL-Test Oberflächenstrukturveränderung, Phosphatidylserin auf Zellmembran Aktivierung von Enzymen Zellkernkondensation Nachweis mittels Annexin V in der Fluoreszenzmikroskopie /Durchflußfluoreszenzzytometrie Caspasen-Nachweis (z.B. mittels Durchflußfluoreszenzzytometrie) Propidiumiodid u. a. Zellkernfarbstoffe Tabelle 7: Auswahl von Testverfahren zur Erkennung apoptotischer Zellen zusammen mit dem Merkmal, auf dem das Testverfahren beruht 1.5 Systemischer Lupus Erythematodes (SLE) Der Systemische Lupus Erythematodes ist eine Autoimmunerkrankung, die durch die Ablagerung von Immunkomplexen im Bindegewebe von Haut und Gefäßen verschiedener Organe mit konsekutiver chronischer Entzündung der Gefäßwände charakterisiert wird. Es erkranken überwiegend Frauen im gebärfähigen Alter (w:m = 10:1), wobei das klinische Bild in Abhängigkeit von der Organbeteiligung wechselt, und von Patient zu Patient sehr unterschiedlich ist. Die Erkrankung kann plötzlich beginnen, sie kann sich aber auch schleichend über einen Zeitraum von Monaten bis Jahren entwickeln. Prinzipiell kann jedes Organsystem Krankheitsmanifestationen aufweisen. Typischerweise findet man die Beteiligung von Haut, Gelenken, Muskeln, Nieren, der Lunge, dem Zentralen Nervensystem und serösem Gewebe (Pleura und Perikard)100. Häufige Symptome sind, neben unspezifischen Allgemeinbeschwerden wie Fieber, Schwäche und Gewichtsverlust, 23 Muskel- und Gelenkbeschwerden, charakteristische Hautveränderungen wie das schmetterlingsförmige Erythem an Wangen und Nasenrücken, oronasale Ulzerationen oder die erhöhte Photosensibilität der Haut. Die Klassifikation der Krankheit erfolgt anhand der ACR-Kriterien (American College of Rheumatology)101 bei denen auch bestimmte Marker im Serum Beachtung finden. So kann man im Serum von Patienten mit SLE Autoantikörper gegen verschiedene Zellkernantigene102 (Antinukleäre Antikörper, ANA) wie doppelsträngige DNA, Sm, Ro, La, Jo-1 oder Histone, sowie gegen diverse andere zytoplasmatische Antigene102, gegen den Komplementfaktor C1q103, gegen Phospholipide102 und gegen verschiedene Blutzellen nachweisen102. Zudem sind im entzündlichen Schub die Komplementfaktoren meist erniedrigt102. 1.5.1 Theorien zur Entstehung des SLE Der pathophysiologische Entstehungsmechanismus des SLE ist bis heute nicht endgültig verstanden. Sicher ist, daß es zur Bildung von Autoantikörpern kommt, die zusammen mit dem komplementären Antigenen Immunkomplexe bilden. Diese Immunkomplexe bestehen zumeist aus DNA als Antigen, Anti-DNA Antikörper, Komplement und Fibrin41. Sie lagern sich im Gewebe ab und lösen dort, u.a. über den klassischen Weg der Komplementaktivierung46, eine Entzündungsreaktion aus78,104. Man nimmt an, das sowohl genetische und hormonelle als auch Umweltfaktoren bei der Entstehung der Krankheit eine Rolle spielen105. Ein Zusammenhang zwischen SLE und dem Komplementsystem wurde erstmals identifiziert, als Untersuchungen den reaktiv erniedrigte Komplementspiegel bei SLEPatienten nachwiesen. Später konnte wiederholt gezeigt werden, daß der häufigste genetisch bedingte Risikofaktor für die Entstehung des SLE beim Menschen die Defizienz einer frühen Komplementkomponente (C1, C4 und C2) ist37,106-112. Dabei ist die Assoziation zwischen C1- oder C4-Defizienz und dem Auftreten von SLE besonders stark113,114. Auch erworbene Komplementdefizienz begünstigt die Entwicklung von SLE37,115,116. Dieser Zusammenhang zwischen dem Mangel an frühen Komplementkomponenten und dem Auftreten von SLE konnte auch im Tiermodell nachgewiesen werden. So wurden bei C1q- und C4-Knock-Out Mäusen117,118 als auch bei C2- bzw. C4-defizienten Meerschweinchen119 Zeichen eine Immunkomplexerkrankung wie erhöhte Autoantikörper oder Glomerulonephritiden festgestellt. Nach neuen 24 Ergebnissen läßt sich auch eine Beteiligung der Komplementrezeptoren (CR2/1) über eine direkte Interaktion von C4 mit CD21/35 (unabhängig von C3) in der Pathogenese des SLE nicht mehr ausschließen48,63. Im Gegensatz dazu sind beim Menschen wie auch bei der Maus C3-Defizienz und der Mangel an Komplementkomponenten des Membranangriffskomplexes (C5-9) nicht mit dem Auftreten von SLE assoziiert43,118. Zudem spielt die aktivierte Komplementkaskade in der Entzündungsvermittlung und Verstärkung der Antikörperproduktion eine bedeutende Rolle und wirkt dadurch krankheitsverstärkend120. Der protektive Effekt einiger früher Komplementkomponenten scheint somit unabhängig von C3 und dessen Rolle in der Entzündungsvermittlung zu sein118. Es werden verschiedene Hypothesen für den pathogenetischen Wirkmechanismus der Entstehung des SLE beim Mangel an frühen Komplementkomponenten postuliert. Die erste Theorie geht von der Beobachtung aus, daß der B-Zell-abhängige Teil der Immunantwort, der ja zur Produktion der für die Entwicklung des SLE pathogenetisch wichtigen Antikörpern führt, über verschiedene Komplementkomponenten reguliert wird36,58. Ein Komplementmangel könnte somit über eine gestörte Toleranzentwicklung der B-Zellen die Krankheit initiieren46,58,71. Dabei können sowohl die zentrale als auch die periphere Toleranzentwicklung betroffen sein. Da es vor allem zur Bildung von Immunglobulinen der Klasse G kommt, die größtenteils erst nach dem Prozeß der somatischen Hypermutation von B-Zellen im Keimzentrum gebildet werden, ist es wahrscheinlich, daß die periphere Toleranzentwicklung betroffen ist47,121-123. Auch läuft die bisher bekannte Regulation der B-Zellen über den Komplementrezeptor 2 (CD21), (Kapitel 1.3.2) der erst auf reifen B-Zellen in der Peripherie des Immunsystems exprimiert wird. (Kapitel 1.2.1) Somit könnte eine durch Komplementmangel bedingte Störung der peripheren Toleranzentwicklung eine Ursache für die Entwicklung des SLE sein. Als Folge des Komplementmangels könnte ein Apoptosedefekt die periphere Toleranzentwicklung stören, da auch Mäuse, die einen defekten Fas-Rezeptors (CD95) aufweisen (lpr/lpr-Mäuse), zu einer SLE-ähnlichen Erkrankung neigen, und dies bei zusätzlicher Defizienz von Komplement C4 verstärkt wird47,70,124. Wenngleich naheliegend, so wurde dieser Zusammenhang (Apoptosedefekt durch C4-Defizienz) bislang allerdings nicht hinreichend untersucht. Dies soll deshalb Ziel dieser Arbeit sein. 25 Die zweite bedeutende Hypothese über die Entstehung des SLE basiert auf den Beobachtungen, dass intraperitoneal (i.p.) applizierte apoptotische Körperchen als Quelle für lupustypische Autoantigene weniger gut phagozytiert werden können, wenn C1q103,125 oder C4A35 fehlt47, und daß nicht phagozytierte apoptotische Zellen immunogen wirken können99,126,127. Der Komplementmangel könnte somit durch Beeinflussung der Phagozytose die Krankheit initiieren33,47,128. Dafür spricht auch, daß in Patienten mit SLE die Aufnahme apoptotischer Zellen durch Makrophagen im Germinalen Zentrum gestört ist129. Allerdings spricht gegen diese Theorie, daß die komplementvermittelte Phagozytose zumindest teilweise auch C3b benötigt, der Mangel an C3 allerdings nicht mit einem SLE assoziiert ist. 26 1.6 Zielsetzung, Begründung der Fragestellung Die Hauptaufgabe des Immunsystem ist es, effektiv körperfremde, potentiell gefährliche Infektionserreger zu bekämpfen. Gleichzeitig muß es sicherstellen, daß körpereigene Substanzen toleriert werden. Versagt diese Diskriminierung, kommt es zur Autoimmunität. Ein wichtiger Bestandteil der erworbenen Immunabwehr sind die B-Lymphozyten, die Antikörper produzieren. Ihre Entwicklung unterliegt einer strengen Regulation, um die Entstehung von autoreaktiven Zellen und damit von Autoimmunerkrankungen zu vermeiden. Dieser Prozeß wird auch als Toleranzinduktion bezeichnet. Ein bedeutender Mechanismus zur Erhaltung der Selbsttoleranz während der Reifung der B-Lymphozyten ist der programmierte Zelltod, der auch als Apoptose bezeichnet wird. Dennoch kommt es bei manchen Menschen zum Verlust der Toleranz und zur Ausprägung von Autoimmunerkrankungen. Ein besonderes Beispiel hierfür stellt der Systemische Lupus Erythematodes (SLE) dar, eine Krankheit, bei der es zur Bildung von hochaffinen Autoantikörpern gegen nukleäre Antigene durch B-Lymphozyten kommt. Diese Antikörper werden als Auslöser von Entzündungsreaktionen in diversen Organen angesehen. Ursächlich für die Entstehung der Erkrankung könnte somit eine Störung in der Toleranzentwicklung von B-Lymphozyten sein. Autoreaktive B-Zellen, die eigentlich absterben sollten, könnten dann überleben und ein Reaktion gegen körpereigene Antigene auslösen. Der genaue pathophysiologische Entstehungsmechanismus des SLE ist aber bis heute nicht endgültig verstanden. Bekannt ist, daß ein Mangel an frühen Komplementkomponenten wie C1q, C2 oder C4 die Entstehung des SLE begünstigt, und daß diese Komplementkomponenten einen regulierenden Einfluß auf die B-Zell-Immunität über den Komplementrezeptor CD21 entfalten. In dieser Arbeit wurde daher die Hypothese untersucht, ob der Mangel an frühen Komplementkomponenten über einen veränderten Apoptosemechanismus die periphere Toleranzentwicklung der B-Zellen stört, und damit die Entstehung eines SLE begünstigt. Diese Hypothese sollte in zwei unabhängigen Verfahren überprüft werden. Zum einen wurde in vivo die Antigeninduzierte Apoptose in Abhängigkeit von Komplement C4 unter Verwendung von C4-defizenten Knock-out-Mäusen mit Hilfe der TUNEL-Methode und der spezifischen Antikörperproduktion untersucht. Zum anderen wurde in vitro die Fas (CD95)-induzierte Apoptose in Abhängigkeit von der Stimulation des Komplementrezeptors CD21 durchflußfluoreszenzzytometrisch analysiert. 27 2 Material und Methoden 2.1 Material 2.1.1 Mäuse Als Wildtypkontrolle wurden Mäuse vom Stamm C57BL/6 (Charles River Laboratories, Wilmington, USA) verwendet. Als komplementdefiziente Mäuse wurden C4-/-Mäuse vom Stamm C57BL/6 eingesetzt (freundlicherweise von Prof. Michael C. Carroll [Harvard Medical School Boston, USA] zur Verfügung gestellt). Für die Versuche wurden zwischen 6 und zehn Wochen alte Weibchen verwendet. Der Tierversuchsantrag für dieses Projekt vom 28.08.1998 wurde durch das Ministerium für Natur und Umwelt des Landes Schleswig-Holstein bis zum 31.12.2000 bewilligt und bis zum 31.03.2004 verlängert (Kennziffer 29/b/99). Die Einwilligung der Ethikkommission der Universität zu Lübeck liegt ebenfalls vor. 2.1.2 Zellinien (der in vitro Experimente) WEHI 231: Zellen eines B-Zell-Lymphoms der Maus [(BALB/c xNZB) F1], induziert durch Mineralölinjektion, lymphoblastische Morphologie Center for applied Microbiology& research (CAMR, ECACC, Salisbury, UK) WEHI 279: Zellen eines B-Zell-Lymphoms der Maus [NZC], induziert durch Bestrahlung, lymphoblastische Morphologie Center for applied Microbiology & research (CAMR, ECACC, Salisbury, UK) Beide Zellinien wurden in einem miniPERM-Bioreaktor (Heraeus Instruments IN VITRO Systems & Services GmbH, Osterode) bei 37°C und 5% CO2 kultiviert. Das Nährmedium bestand aus IMDM (BioWittaker, Cambrex, Belgien) dem 10% FCS (PAA Laboratories GmbH, Österreich), 1% L-Glutamin (Biochrom, Berlin), 1% essentielle Aminosäuren (BioWittaker, Cambrex, Belgien), 1% Natrium-Pyruvat (BioWittaker, Cambrex, Belgien), 1% Penicillin-Streptomycin (Biochrom, Berlin) und 2µl 2Mercaptoethanol (Sigma, Steinheim) pro 500ml zugefügt wurden. Zwei mal pro Woche wurden die Zellen im Verhältnis 1:2 mit frischem Medium versetzt, und die Zellinien wurden nie länger als sechs Monate in Kultur gehalten. 28 2.1.3 Antigen Np-(36)-CGG (Biosearch Technologies, Novato, USA) Np-(24)-BSA (Biosearch Technologies, Novato, USA) Np-(29)-KLH (Biosearch Technologies, Novato, USA) Np-(24)-Ficoll (Biosearch Technologies, Novato, USA) Bei dem für die Versuche verwendeten Antigen handelt es sich um 4-Hydroxy-3Nitrophenylacetyl (Np). Es ist ein Hapten und demzufolge nicht ausreichend immunogen, deshalb wurde es an Trägerproteine (BSA [Bovines Serumalbumin], KLH [Keyhole Limpets Hemocyanin] und CGG [Chicken Gamma Globulin]) gekoppelt verwendet. Es wirkt so als T-Zell-abhängiges Antigen. Wird Np an den Zucker Ficoll gekoppelt, wirkt es als T-Zell unabhängiges Antigen. Um eine Np-spezifische Antikörperantwort zu induzieren und zu messen (unabhängig von der Immunantwort gegen Strukturen der Trägerproteine) wurden verschiedene Trägerproteine verwendet. Das Hapten Np ist über eine Amidbindung mit dem Trägerprotein konjugiert, hierbei liegen soviele Np-Gruppen pro Proteinmolekül vor, wie die Zahl in der Klammer angibt (z.B. 24 Np-Gruppen pro Molekül BSA bei Np-(24)-BSA). 2.1.4 Antikörper (Ak) Antikörper gegen (Anti-) Maus IgM Maus IgG2a Gekoppelt Hersteller Konzentramit tion Alkalischer Sigma 4,2mg/ml Phosphatase (AP) AP Pharmingen, San Diego AP Pharmingen Maus IgG2b AP Pharmingen Maus IgG3 AP Pharmingen Isotyp Fluorescein Pharmingen isothiocyanat (Fitc) Fitc Pharmingen Maus IgG1 Maus CR1/ CR2 (CD21/35) 0,5mg/ml 0,5mg/ml Art des Antikörpers IgM der Ziege IgG1 der Ratte (kappa) IgG1 der Ratte (kappa) IgG2a der Ratte (kappa) IgG2a der Ratte (kappa) IgG2a der Ratte IgG2b der Ratte (kappa) 29 Antikörper gegen (Anti-) Maus B220 (CD45) Maus CD19 Gekoppelt Hersteller mit Fitc Pharmingen Fitc Pharmingen Maus Fas (CD95) Maus IgD Fitc Pharmingen Konzentra- Art des Antikörpers tion 0,5mg/ml IgG2a der Ratte (kappa) 0,5mg/ml IgG2a der Ratte (kappa) 0,5mg/ml IgG2 des Hamsters Fitc eBioscience 0,5mg/ml Maus CD3 Fitc Pharmingen 0,5mg/ml IgG2a der Ratte (kappa) IgG2 des Hamsters Maus CD90.2 (Thy1.2) Maus Gr1 (LY 6G) Isotyp Fitc Pharmingen 0,5mg/ml IgG2a der Ratte Fitc Pharmingen 0,5mg/ml IgG2b der Ratte Phycoerythrin (PE) PE Pharmingen 0,2mg/ml IgG2a der Ratte Pharmingen 0,2mg/ml IgG2 des Hamsters PE eBioscience 0,2mg/ml - Pharmingen 1mg/ml - Pharmingen 0,5mg/ml - Pharmingen 1mg/ml IgG2a der Ratte (kappa) IgG2 des Hamsters (kappa) IgG2b der Ratte (kappa) IgG2 des Hamsters - Pharmingen 0,5mg/ml IgM des Hamsters Maus Fas (CD95) Maus IgM Isotyp (anti-KLH) Maus CR1/ CR2 (CD21/35) Maus Fas (CD95) Maus CD40 Tabelle 8: Im Rahmen dieser Arbeit verwendete Antikörper 30 2.2 Methoden 2.2.1 Immunisierung der Mäuse und Alumpräzipitation des Antigens Die Applikation des Antignes erfolgte im Rahmen dieser Arbeit ausschließlich intraperitoneal. Dazu wurde die zu injizierende Dosis des Antigens in ca. 200µl sterilem „Phosphate Buffered Saline“ (PBS) gelöst und mit einer spitzen Kanüle direkt in den Bauchraum der Mäuse gespritzt. Dieses Verfahren traumatisierte die Mäuse relativ wenig. Wird ein Antigen in den Intraperitonealraum injiziert, so läuft ein Großteil der so induzierten Immunantwort in der Milz und den Lymphknoten des Bauchraumes ab. In dieser Arbeit wurden die so induzierten Vorgänge in der Milz und im Serum untersucht. Um die Immunantwort gegen ein bestimmtes Antigen zu steigern kann man dieses vor intraperitonealer Injektion in die Mäuse in Alum [Aluminiumkaliumsulphat, AlK(SO4)2] präzipitieren. Das so im Intraperitonealraum gebundene Antigen bildet dort eine Art Depot von dem ein starker Entzündungsreiz ausgeht. Dazu wird 1mg des Antigens in 2ml sterilem PBS gelöst (c=0,5mg/ml) und mit 4ml 10%Alum [1g AlK(SO4)2 in 10ml aqua dest.] vermischt. Durch tropfenweise Zugabe von 1M Kaliumhydroxidlösung (5,61g KOH in 100ml aqua dest.) wird der pH-Wert der Lösung von 3 auf 6,5 angehoben. Dabei bildet sich ein milchiger Niederschlag, der sich bei zu starker Alkalisierung der Suspension gelblich verfärbt. Nach Zentrifugation der weißlichen Suspension (Zentrifuge: CentrikonT-324, Kontron Instruments) über 15min bei 2500rpm und 4°C und dreimaligem Waschen des Niederschlages in sterilem PBS wird das präzipitierte Antigen in 3ml sterilem PBS resuspendiert. 2.2.2 Induktion von Apoptose In vitro wurden verschiedene Verfahren zur Induktion von Apoptose verwendet: Nährstoffentzug (Inkubation von 4*106 Zellen in 1ml PBS über 20h bei 37°C im Brutschrank), Inkubation mit dem Zellgift Camptothecin (4*106Zellen in 1ml DMSO (Merck, Darmstadt) mit 8µl 1mM Camptothecin in DMSO 4h bei RT), und Stimulation des Fas-Rezeptors (CD95) (4*106Zellen in 1ml Medium mit 5µg AntiMaus CD95 über 10h bei 37°C im Brutschrank). 31 Um eine größere Menge an apopotischen Zellen in vivo untersuchen zu können, wurde in dieser Arbeit eine bereits etablierte Methode gewählt: die Antigeninduzierte Apoptose92. Die Injektion einer großen Dosis löslichen Antigens in eine etablierte Immunantwort hinein läßt eine große Menge vorher gebildeter antigenspezifischer B-Zellen apoptotisch werden92-94. Aufgrund der großen Zahl an apoptotische Zellen wird dieser Versuchsaufbau auch als „Suicide-Versuch“ (engl. suicide, Selbstmord) bezeichnet. Wird das Antigen den Versuchtieren intraperitoeal injiziert, so läuft ein Großteil der so ausgelösten Prozesse intraperitoneal ab. In dieser Arbeit wurde als Antigen das Hapten Np (4-Hydroxy-3-Nitrophenylacetyl) an CGG oder BSA gekoppelt verwendet. Zur Etablierung der Immunantwort gegen Np wurde den Versuchstieren 50µg in Alum präzipitiertes Np-CGG zusammen mit 150µg Isoprotenerolhydrochlorid intraperitoneal (i.p.) gespritzt. Neun Tage danach wurde ihnen als zweite Injektion erneut Np, um Einflüsse des Trägerproteins auszuschließen diesmal an BSA gekoppelt (Np-BSA), in einer Dosis von 4mg i.p. injiziert92. 2.2.3 Isolierung von Milzlymphozyten 2.2.3.1 1. Schritt: Extraktion der Splenozyten Die in einem festen Gewebe wie der Milz enthaltenen Lymphozyten wurden mit Hilfe eines Dichtegradienten isoliert. Das Prinzip dieser Aufreinigung besteht in der Zentrifugation der Zellsuspension auf einer Lösung, welche dieselbe Dichte hat wie die zu isolierende Zellart, in diesem Fall Lymphozyten. Dichtere Zellen wie Erythrozyten und große Bindegewebspartikel sinken beim Zentrifugieren ab, die Lymphozyten dagegen sammeln sich am Übergang Zellsuspension - Isolierungslösung an. Beim nachfolgenden Waschen der gewonnenen Zellen lassen sich weniger dichte Zellen wie Thrombozyten größtenteils entfernen. Puffer und Lösungen: Waschpuffer: PBS (phosphatgepufferte Kochsalzlösung) Lymphozytenseparationsmedium: PAA Laboratories, Pasching, Österreich Protokoll: Milz der Maus vorsichtig zwischen zwei Objektträgern zerreiben, in 5ml PBS suspendieren, Suspension filtern (Cellstainer 40µm BD Bioscience, Belgien) 32 5ml Lymphozytenseparationsmedium in ein Falcon-Tube (BD Bioscience, Belgien) füllen, vorsichtig mit derselben Menge an Zellsuspension überschichten in einer auf 15°C vorgekühlter Zentrifuge (Varifuge3.2RS, Heraeus, Osterode) 20min bei 600g zentrifugieren, dabei auf langsames Beschleunigen und Bremsen der Zentrifuge achten von den drei voneinander abgrenzbaren Schichten die mittlere (Interphase) großzügig abnehmen, Rest verwerfen so gewonnene Zellen in PBS bei RT waschen 1210rpm, 10min 2.2.3.2 2.Schritt: Isolierung von B-Lymphozyten Zur spezifischen Isolierung von B-Lymphozyten wurden mittels eines weiteren Isolierungsverfahrens T-Lymphozyten sowie eventuell noch in der Suspension enthaltene Makrophagen und dendritische Zellen anhand ihrer spezifischen Oberflächenmarker entfernt. Dazu wurden zu den Zellen mit magnetischen Partikeln (sog. „Beads“) gekoppelte Antikörper gegeben, welche spezifisch Antigene auf T-Zellen und Makrophagen erkennen. Die wie oben beschrieben gewonnenen Zellen wurden dann über eine Säule gegeben, die mit einem starken Magneten gekoppelt war, wodurch mit Antikörpern behaftete Zellen in der Säule festgehalten wurden. Puffer und Lösungen: Waschpuffer: 1% humanes Albumin (DRK, Deutschland) mit 0,4% Natriumzitrat (Baxter, Frankreich) in 500ml PBS MicroBeads: Anti-CD11b, Anti-CD90 (Tyh1.2), Anti-CD11c (Miltenyi Biotec) Nährmedium: RPMI (BioWittaker, Cambrex, Belgien) je 500ml versetzt mit: 5% FCS (PAA Laboratories GmbH, Österreich) 1% L-Glutamin (Biochrom, Berlin) 1% Penicillin-Streptomycin (Biochrom, Berlin) 2µl 2-Mercaptoethanol (Sigma, Steinheim) Protokoll: Zellen waschen: Zellen in Waschpuffer suspendieren, bei 1600rpm 10min zentrifugieren, Überstand verwerfen 33 Zellen in 100µl Waschpuffer suspendieren und mit pro 107Zellen je 10µl der verschiedenen „Beads“ 15min bei 10°C inkubieren Zellen in Waschpuffer bei RT waschen Zellen in 500µl Waschpuffer aufnehmen und Suspension auf eine mit 500µl Waschpuffer gespülte Säule (SuperMACS, Milteny Biotec, Bergisch-Gladbach) geben Säule mit 1ml Waschpuffer nachspülen, Eluat auffangen so gewonnene Zellen über eine zweite Säule geben, erneut mit 1ml Waschpuffer nachspülen, Eluat auffangen („Positivfraktion“), beide Säulen aus dem Magneten entfernen, mit 1ml Waschpuffer spülen, Eluat auffangen („Negativfraktion“) Kontrolle der Reinheit der Zellen am Durchflußfluoreszenzzytometer 4*106Zellen der Positivfraktion in 1ml Nährmedium aufnehmen, bei 37°C und 5%CO2 kultivieren im Brutschrank (miniPERM-Bioreaktor, Heraeus Instruments IN VITRO Systems & Services GmbH, Osterode) kultivieren 2.2.4 Durchflußfluoreszenzzytometrie Am Durchflußfluoreszenzzytometer können durch Fluoreszenzfarbstoffe markierte Antigene, die sich auf oder in einzelnen Zellen befinden nachgewiesen werden. Dazu werden diese Antigene mit Antikörpern markiert, an welche ein Fluoreszenzfarbstoff gekoppelt ist. Fällt ein Laserstrahl auf die zu untersuchende Zelle, so wird das Farbstoffmolekül angeregt und emmitiert Licht einer bestimmten, vom Laserstrahl unterscheidbaren Wellenlänge, welches vom Durchflußfluoreszenzzytometer analysiert wird. Zusätzlich können anhand von zwei weiteren optischen Parametern, Forward Scatter (FS) und Sideward Scatter (SS) (die Brechung des Laserstrahles durch die Zelle), die Größe (FS) und die intra- bzw. extrazellulären Bestandteile der Zelle (Granularität, SS) abgeschätzt werden. In der vorliegenden Arbeit wurde ein Coulter EPICSXL verwendet, welches mit einem Laser der Wellenlänge 488nm arbeitet, und Messungen mit bis zu vier Farbstoffen 34 gleichzeitig erlaubt. In den hier beschriebenen Untersuchungen wurden nur die Farbstoffe Fluoresceinisothiocyanat (Fitc, Fluoreszenz: 575nm) und Phycoerythrin (R-PE, Fluoreszenz: 525nm) verwendet. 2.2.4.1 Untersuchung des Phänotypes von Zellen Zur Darstellung verschiedener Antigene auf der Zelloberfläche der verwendeten Zellinien und Milzlymphozyten wurden je 1*106 Zellen mit 0,5µg des betreffenden Antikörpers in einem Volumen von ca. 100µl PBS für 10-15min bei RT inkubiert. Danach wurden die Zellen in 1ml PBS gewaschen, und im Durchflußzytometer untersucht. Um nur die spezifisch an die zu untersuchenden Rezeptoren gebundenen Antikörper zu messen wurden alle Messungen mit einer sog. Isotypkontrolle (ein Kontrollantikörper des selben Isotyps, der keine der auf der Zelle verfügbaren Strukturen spezifisch bindet) verglichen. 2.2.5 TUNEL (TdT mediated dUTP nick end labeling) In dieser Arbeit erfolgte der Nachweis apoptotischer Zellen mittels eines Testverfahrens der Firma Boehringer Mannheim. Dieses Verfahren erlaubt den Nachweis von durch Strangbrüche entstandenen freien DNA-Enden. Ein Enzym, Terminale Desoxynukleotidyltransferase (TdT), markiert diese freien 3’OH-Enden mit an dUTP (Desoxyuridintriphosphat) gekoppeltem Durchflußfluoreszenzzytometer direkt Markierungsschrittes mit gemessen, Alkalischer Flourescein, oder Phosphatase mit (AP) welches im eines zweiten Hilfe und Substrat für die Lichtmikroskopie sichtbar gemacht wurde. Für die Negativkontrolle wurde das spezifisch koppelnde Enzym (TdT) weggelassen, um unspezifisch gebundenes Flourescein darstellen zu können. In dieser Arbeit wurde das Protokoll des Herstellers leicht verändert für Zellsuspensionen und Gewebeschnitte verwendet. Puffer und Lösungen: 4% PFA: 4mg Paraformaldehyd in 100ml PBS Triton X 100: 1g Natriumcitrat + 1ml Triton X 100 in 1l aqua dest. TUNEL Boehringer Kit; Enzym : Labelsolution = 1:9 35 Protokoll: Zellen in PBS waschen. Pellet von ca. 4*106 Zellen in einem EppendorffReaktionsgefäß in 1ml PBS suspendieren, 10min bei 4000 Umdrehungen pro min (rpm) zentrifugieren, Überstand verwerfen oder Gewebeschnitt (s.u.) 15min an der Luft trocknen lassen, mit PAP-Pen (Ted Pella Inc., USA) Gewebe umfahren, erneut ca. 15min trocknen lassen zur Fixierung Zellen in 1ml 4% PFA suspendieren /Gewebeschnitt mit 1ml 4% PFA überschichten und bei Raumtemperatur 10min einwirken lassen Zellen /Gewebe zwei mal je 10min mit 1ml PBS waschen Zellen /Gewebe 2min auf Eis mit je 100µl Triton X 100 behandeln (Pellet in angegebenem Volumen suspendieren /Gewebe mit Lösung überschichten) Zellen /Gewebe erst einmal 5min, danach 10min mit 1ml PBS waschen Zellen /Gewebe bei 37°C 1h mit Boehringer TUNEL-Reagenz inkubieren Analyse der Zellen im Durchflußfluoreszenzzytometer oder Gegenfärbung des Gewebes mit weiteren Markern (s.u.) 2.2.6 Immunhistochemie Zur Darstellung von Antigenen auf Gewebeschnitten können verschiedene Methoden angewendet werden. In dieser Arbeit wurden Antigene direkt und indirekt nachgewiesen. Beim direkten Nachweis bindet ein enzymgekoppelter Antikörper/ Marker (Horseradish Peroxidase (HRP) oder Alkalische Phosphatase (AP)) unmittelbar an das Antigen, beim indirekten Nachweis ist erst ein Sekundärantikörper, der den Primärantikörper/ -marker auf dem Antigen erkennt, an ein Enzym gekoppelt. Bei beiden Arten des Nachweises setzt das Enzym ein Substrat zu einem farbigen und damit meßbaren Endprodukt um. Werden für eine Zweifarbenfärbung zwei verschiedene Enzyme verwendet, so ist immer das AP – abhängige Substrat vor dem HRP – abhängigen Substrat zu entwickeln. 36 Objektträger beschichten Die Objektträger (Super Fast, Menzel) wurden vor Gebrauch 10min bei RT in 4°C kaltes Aceton getaucht, 10min an der Luft getrocknet, und schließlich 10min bei RT in ebenfalls 4°C kaltem 0,01% Poly-L-Lysin (in aqua dest.) getaucht. Danach wurden sie über Nacht bei RT getrocknet. Gewebe vorbereiten Das frisch aus der Maus entnommene Gewebe wurde in Einbettmedium (Jung Tissue medium, Leica, Nusslach) eingebettet, und bei -80°C eingefroren. Vor dem Färben wurde das gefrorene Gewebe bei -20°C mittels des Mikrotoms (LEICA CM 1850, Leica) in einer Schichtdicke von 5-8µm geschnitten und auf die beschichteten Objektträger aufgebracht. Anschließend wurden die Schnitte 1h luftgetrocknet, 10min in 4°C kaltem Aceton dehydriert und wiederum 1h luftgetrocknet. Die Lagerung erfolgte bei -20°C. Zweifarben-Färbung: TUNEL-PNA Puffer und Lösungen: Waschpuffer: PBS Einbettmedium: Crystal/Mount (Biomeda Corp., USA) Marker I: dUTP-Fitc (Boehringer TUNEL-Reagenz) (s.o.) Sekundärantikörper I: anti-Fluorescein Antikörper gekoppelt an AP (Boehringer Converter AP ) Substrat I: Fast Blue BB Base (Detektion von AP, Farbe: blau): Naphthol AS-MX Phosphate (Sigma-Aldrich, Steinheim) N,N-Dimethylformamid (Sigma-Aldrich, Steinheim) Tris-Puffer (0,1 M): 12,1 g Tris-[hydroxymethyl]aminomethan in 1l aqua dest., pH=8,5 Fast Blue BB Base (Sigma-Aldrich, Steinheim) 2 M HCl 4% Natriumnitrat Levamisole (Sigma-Aldrich, Steinheim) Marker II: PNA gekoppelt an HRP (Lectin from Arachis Hypogaea (Erdnuss), Peroxidase labeled, Sigma-Aldrich, Steinheim) 37 Substrat II: AEC (Detektion von HRP, Farbe: rotbraun): AEC-Lösung: 400 mg 3-Amino-9-Ethyl-Carbazole (Sigma-Aldrich, Steinheim) in 25 ml N,N Dimethylformamid (lichtgeschützt aufbewahren!) Natriumacetat-Puffer (0,05 M): 3,4 g Natriumacetat in 500 ml aqua dest.; pH 5,0 Hydrogenperoxid, 30% (w/v)(Sigma-Aldrich, Steinheim) Protokoll: Gewebeschnitte 15min an der Luft trocknen lassen, mit PAP-Pen (Ted Pella Inc., USA) Gewebe umfahren, erneut ca. 15min trocknen lassen nach dem TUNEL-Protokoll (2.2.5.) als ersten Antikörper (I) Boehringer TUNELReagenz einwirken lassen mit Waschpuffer abspülen als zweiten Antikörper 2,5µl PNA-HRP, und als Sekundärantikörper I 37,5µl Converter AP zusammen mit 10µl PBS über jeden Schnitt schichten, bei 37°C abgedunkelt in einer feuchten Kammer 1h inkubieren mit Waschpuffer abspülen als Substrat der Alkalischen Phosphatase (AP) 5mg Naphthol AS-MX Phosphate bei RT in 250µl N,N-Dimethylformamid lösen, und dazu 40ml Tris Puffer geben 10mg Fast BB Blue base bei RT in 250µl 4°C kalte HCl (2M) geben, danach 250µl 4°C kaltes Natriumnitrit dazugeben, und diese Lösung tropfenweise zu dem TrisPuffer hinzufügen schließlich 10mg Levamisole bei RT dazugeben, um die endogene Alkalische Phosphatase-Aktivität zu inhibieren die Lösung filtern (Filter mit 0,45 µm Porengröße, Schleicher & Schuell, Dassel) und über die Schnitte schichten bei RT abgedunkelt in einer feuchten Kammer 1-2h inkubieren mit Waschpuffer abspülen 38 als Substrat der Horseradish Peroxidase (HRP) 250µl AEC-Lösung zu 9,75ml Natriumacetat-Puffer geben, und die Lösung filtern (Filter mit 0,45 µm Porengröße, Schleicher & Schuell, Dassel), vor Licht schützen! 5µl Hydrogenperoxid dazugeben, gut mischen und über die Schnitte schichten bei RT in einer dunklen und feuchten Kammer ca.1h inkubieren, bis die Schnitte makroskopisch eine deutliche rotbraune Färbung zeigen mit Waschpuffer abspülen mit 3-5 Tropfen Einbettmedium (Crystal/Mount, Biomeda, Forster City) überschichten, über Nacht bei RT trocknen 2.2.7 Blutentnahme Zur Serumgewinnung wurde aus der Schwanzvenen der Maus mittels einer Kanüle 100400µl Blut entnommen. Dieses wurde bei RT ca. 1h in einem Eppendorff-Reaktionsgefäß ruhen gelassen und danach 10min mit 4000 rpm zentrifugiert. Der Überstand wurde abgenommen und bei -80°C gelagert. 2.2.8 ELISA zum Nachweis Np-spezifischer Antikörper Mit diesem Verfahren können im Mausserum enthaltene Antigen (Np)-spezifische Antikörper halbquantitativ gemessen werden. Die verschiedenen Immunglobulinsubklassen wurden unabhängig von einander bestimmt. Als Standard wurde aus mit 200µg Np-BSA oder mit 50µg Tnp-Ficoll (jeweils in Alum präzipitiert) immunisierten Mäusen gewonnenes Serum verwendet, welches als Verdünnungsreihe mit Waschpuffer im Verhältnis 1:1 drei mal weiterverdünnt wurde. Der Korrelationskoeffizient des Standards lag bei allen Messungen zwischen 0,997 und 0,999. Da die genaue Konzentration der Np-spezifischen Antikörper im Standardserum nicht bekannt ist, können die Immunglobulinsubklassen untereinander nicht verglichen werden. Alle Proben und Standards wurden im Doppelansatz gemessen. 39 2.2.8.1 ELISA zum Nachweis von Np-spezifischem IgM Puffer und Lösungen: Waschpuffer: 19,1g Dulbecco’s + 1ml Tween 20 in 2l aqua dest. Block-Puffer: 1mg Cytochrom C in 1ml Waschpuffer (s.o.) Coating-Puffer: 1 Karbonat-Bikarbonatpuffer-Kapsel (Sigma-Aldrich, Steinheim) in 100ml aqua dest. Antigen: Np-(29)-KLH Standard: Poly-IgM-Serum (B1-8), erste Verdünnung: 10µl auf 190µl Waschpuffer Sekundärantikörper: Substrat: anti-Maus IgM-AP 1:2500 pNpP (SIGMA FASTTM pNpP-Substrattabletten (Sigma-Aldrich, Steinheim) Stopp-Puffer: 3M NaOH Protokoll: Mikrotiterplatte (Costar® 96 well EIA/RIA plate, (no lid, medium binding, Polystyrene) Corning Incoperated Nr.9017) mit je 100µl Np-(29)-KLH in einer Konzentration von 5µg pro ml Coating-Puffer pro Vertiefung beschichten, bei 4°C über Nacht inkubieren drei mal mit je 300µl Waschpuffer pro Vertiefung waschen, Platte ausklopfen zum Blocken mit je 100µl Block-Puffer pro Vertiefung, 1h bei 37°C inkubieren drei mal waschen (s.o.) Proben und Standard in verschiedenen Verdünnungen pipettieren, jeweils 100µl pro Vertiefung, bei 4°C über Nacht, danach 1h bei 37°C inkubieren drei mal waschen (s.o.) je 100µl Sekundärantikörper in die Vertiefungen der Mikrotiterplatte pipettieren, 1h bei 37°C inkubieren drei mal waschen (s.o.) 40 in jede Vertiefung 200µl Substrat geben, 30 min im Dunkeln bei RT inkubieren pro Vertiefung 50µl Stopp-Puffer dazugeben, kurz auf dem Schüttler mischen bei 405nm (Referenz 620nm) im Spektralphotometer (Hitachi U-3000, Hitachi, Tokyo/Japan) die Extinktion messen 2.2.8.2 ELISA zum Nachweis von Np-spezifischem IgG Für diese Messungen wurden bis auf die unten genannten Unterschiede die gleichen Puffer und Lösungen verwendet, und auch der Ablauf unterschied sich nur in den unten aufgeführten Punkten. Es gelang nicht, einen Standard zur Messung der IgG2a-Subklasse zu etablieren, was höchst wahrscheinlich auf den verwendeten Sekundärantikörper (Anti-Maus IgG2a-AP, Pharmingen, SanDiego) zurückzuführen ist130. Puffer und Lösungen: Standard: IgG1: poly-Np IgG-Serum, erste Verdünnung: von einer 1:100 Vorverdünnung 10µl auf 190µl Waschpuffer IgG2b: poly-Np IgG-Serum, erste Verdünnung: von einer 1:100 Vorverdünnung 100µl auf 100µl Waschpuffer IgG3: poly-Tnp-Serum, erste Verdünnung: 10µl auf 190µl Waschpuffer Sekundärantikörper: IgG1: anti-Maus IgG1-AP, Verdünnung: 1:10 000 IgG2b: anti-Maus IgG2b-AP, Verdünnung: 1:5 000 IgG3: anti-Maus IgG3-AP, Verdünnung: 1:2 500 Protokoll: Inkubationszeit des Substrates (pNpP, s.o.): IgG1: 50min IgG2b: 50min IgG3: 4h 41 2.2.9 Kopplung von Antikörpern an Biotin Da Antikörper gegen CD21/35 (CR2/1) der Maus im Handel nicht an Biotin gekoppelt verfügbar sind, wurde dieser Schritt mit aufgereinigtem Anti-CD21/35 nachvollzogen. Puffer und Lösungen: Borat-Puffer: 1,24g Borsäure + 7,62g Di-Natriumtetraborat in 200ml aqua dest. Waschpuffer: PBS Biotin: 10mg Biotin-amidocoproatanhydroxysuccinidester in 1ml DMSO (c=10mg/ml) Antikörper: purified Anti-Maus-CD21/35 (Pharmingen), c=0,5mg/ml Stoppreagenz: 1M Ammoniumchlorid (NH4Cl) Salzsäure (HCl), Natriumhydroxid (NaOH) Protokoll: 0,5mg (1ml) Antikörper mit 1ml Borat-Puffer vermischen, und 50µg (5µl) Biotinester dazugeben. Die Lösung bei RT inkubieren. nach 2h 10µl Stoppreagenz hinzupipettieren und 10min bei RT inkubieren Lösung auf vier Eppendorff-Reaktionsgefäße verteilen (je 500ml pro Reaktionsgefäß), diese mit Dialyseschlauch (Sigma, Steinheim) verschließen und drei Tage im Waschpuffer bei 4°C dialysieren. Täglich den Waschpuffer wechseln. 2.2.10 Statistik Die statistische Analyse der Ergebnisse sowie die Berechnungen der Mittelwerte und Standardabweichungen wurden mit Excel−Analyse-it für Windows durchgeführt. Die Signifikanzen wurden mit dem nicht parametrischen Mann-Withney-Test für zwei unabhängige Stichproben ermittelt. α wurde kleiner als 0,05 gewählt. Statistisch signifikante Unterschiede (p<0,05) zwischen den einzelnen Versuchsgruppen wurden in den Abbildungen mit einem Stern (*) gekennzeichnet. 42 3 Ergebnisse 3.1 Beeinflussung Antigeninduzierter Apoptose durch den Mangel früher Komplementkomponenten: Versuche in vivo Das hier verwendete Modell zur Untersuchung der peripheren Toleranzentwicklung in vivo basiert auf der Erkenntnis, daß die Injektion einer großen Dosis löslichen Antigens in eine etablierte Immunantwort hinein eine große Menge vorher gebildeter antigenspezifischer BZellen apoptotisch werden läßt. Aufgrund der großen Zahl apoptotischer Zellen wird dieser Versuchsaufbau auch als „Suicide-Versuch“ (engl. suicide, Selbstmord) bezeichnet. In diesem Versuch sollte der Einfluß von C4 auf die Antigeninduzierte Apoptose von BZellen in vivo untersucht werden. Dazu wurde in den Versuchstieren (Mäusen) zunächst eine Immunantwort gegen ein Antigen, 4-Hydroxy-3-Nitrophenylacetyl (Np), ausgelöst. Die Injektion des Antigens intraperitoneal (i.p.) hat zur Folge, daß der Hauptteil der Immunantwort gegen dieses Antigen in der Milz abläuft. Durch die zusätzliche Injektion einer großen Dosis des Antigens wurde dann bei den für dieses Antigen spezifischen BLymphozyten Apoptose induziert. (Abb.6) Mit Hilfe verschiedener Methoden wurde untersucht, ob die C4-Defizienz der Versuchstiere einen Einfluß auf die Apoptose der Zellen oder auf die weitere Entwicklung der antigenspezifischen Immunantwort hat. Abbildung 6:Versuchsaufbau zur Untersuchung der Antigeninduzierten Apoptose (BE:Blutentnahme) 43 Einer Gruppe von Wildtyp (wt)- (Gruppe A) und C4-/-Mäusen (Gruppe E) wurden entsprechend der Abb.6 (S.43) zunächst 50µg des in Alum präzipitierten Haptens Np an CGG gekoppelt (Np-CGG) intraperitoneal (i.p.) injiziert. Neun Tage später, nach Etablierung der Immunantwort, wurde ihnen als zweite Injektion erneut Np, diesmal an BSA gekoppelt (Np-BSA), in einer Dosis von 4mg zusammen mit 150µg/kg KG Isoprotenerolhydrochlorid (zur Vermeidung eines anaphylaktischen Schocks) i.p. gespritzt. (Das Trägerprotein wurde gewechselt, um nur die Np-spezifische Immunantwort und nicht die gegen das Trägerprotein (CGG) zu beeinflussen.) Zusätzlich wurden verschiedene Gruppen von Mäusen (wt und C4-/-) als Kontrollen mitgeführt. Einige Mäuse bekamen nur am Tag 0 die erste Injektion [Gruppen B (wt) und F (C4-/-)], einige nur am Tag 9 die zweite Injektion [Gruppen C (wt) und G (C4-/-)]. Die letzten Gruppen von Mäusen erhielten keinerlei Injektionen [Gruppen D (wt) und H (C4-/)]. (Tab.8) Tabelle 8: Einteilung der verschiedenen Versuchsgruppen (zur Untersuchung der Antigeninduzierte Apoptose) Vor der ersten Injektion am Tag 0 wurde allen Mäusen Blut abgenommen, ebenso am Tag 8, am Tag 9 acht Stunden nach der zweiten Injektion, und an den Tagen 16, 23 und 30 nach der ersten Injektion. In den gewonnenen Seren wurde der Titer Np-spezifischer Antikörper mittels ELISA bestimmt, um den Verlauf der Immunantwort gegen Np zu untersuchen. (Kapitel 3.1.3) Acht Stunden nach der zweiten Injektion wurden aus jeder der Gruppen einige Mäuse getötet, deren Milzen entnommen und mit Hilfe eines scharfen Skalpells geteilt. Für die spätere immunhistochemische Aufarbeitung wurde ein Teil 44 eingebettet und bei -80°C eingefroren. (Kapitel 3.1.1) Aus dem kleineren Teil der Milz wurden die Lymphozyten isoliert und im Durchflußfluoreszenzzytometer analysiert. (Kapitel 3.1.2) 3.1.1 Immunhistochemische Färbungen Die immunhistochemischen Färbungen der Milzgefrierschnitte erfolgten mit PNA (PeanutAgglutinin), einem Marker zur Darstellung der Keimzentren, sowie der TUNEL-Methode zur Markierung der apoptotischen Zellen. Abbildung 7: Immunhistochemische Färbungen von Milzgefrierschnitten PNA (GC-Marker, braun) / TUNEL (Apoptose-Markierung, blau) A,B,C: Wildtypmäuse E,F,G: C4-/-Mäuse A,E: Erstinjektion (50µg Np-CGG) und Zweitinjektion (4mg Np-BSA) B,F: nur Erstinjektion (50µgNp-CGG) C,G: nur Zweitinjektion (4mg Np-BSA) 45 Bei allen Mäusen, die eine niedrige Dosis Np-CGG erhalten hatten (Gruppen A, B, E und F), ließen sich PNA pos. Keimzentren in der weißen Pulpa der Milz nachweisen, nicht dagegen bei Mäusen, die keine oder nur eine hohe Dosis des Antigens 8h vor Entnahme der Milzen erhalten hatten. Die absolute oder relative Anzahl der Keimzentren in den Milzen waren schlecht vergleichbar, da zur Analyse nur ein Teil der Milz zur Verfügung stand. Dabei muß bemerkt werden, daß aufgrund der recht aggressiven Schritte zur intrazellulären Darstellung der DNA-Strangbrüche (TUNEL-Test) die Oberflächenfärbung PNA schwach, aber doch erkennbar ausfiel. (Abb.7, S.45) Antigeninduzierte Apoptose Anzahl apoptotischer Zellen in der Milz (Immunhisochemische Analyse) A: Wt, beide Inj. (n=8) 16 14 12 10 8 6 4 2 0 B: Wt, nur 1.Inj. (n=4) C: Wt, nur 2. Inj. (n=4) D: Wt, keine Inj. (n=2) E: C4-/-, beide Inj. (n=8) F: C4-/-, nur 1. Inj. (n=4) Anzahl der TUNEL pos. Zellnester pro GC Anzahl der TUNEL pos. Zellen in weißer Pulpa pro Gesichtsfeld G: C4-/-, nur 2. Inj. (n=4) H: C4-/-, keine Inj. (n=2) Abbildung 8: Anzahl apoptotischer Zellen in der Milz, Analyse Immunhistochemischer Färbungen von Milzgefrierschnitten: TUNEL/PNA (mit Standardabweichung, Gruppen A vs. E und C vs. G: *p<0,05) Bei den Mäusen, die beide Injektionen erhalten hatten (A und E), fanden sich innerhalb der Keimzentren gehäuft apoptotische Zellen, die in Gruppen von fünf bis zehn TUNEL pos. Zellen zusammenlagen. Diese „Zellnester“ waren sowohl bei Wildtypmäusen (Gruppe A), als auch bei deren C4-/-Pendant (Gruppe E) zu erkennen. Dabei fand sich kein signifikanter Unterschied in der Frequenz oder der Größe der Zellnester pro Keimzentrum zwischen den beiden Gruppen. Subjektiv scheinen C4-/-Mäusen jedoch etwas mehr apoptotische Zellgrüppchen pro Keimzentrum zu haben. (Abb.7, S.45 und Abb.8) Bei den Mäusen, die lediglich mit 50µg des Antigens (1.Inj.) immunisiert worden waren (Gruppen B und F), fanden sich ebenfalls solche „Zellnester“ apoptotischer Zellen in den Keimzentren, allerdings waren diese deutlich kleiner und seltener. Auch hier war kein Unterschied zwischen Wildtyp- und C4-/-Mäusen nachweisbar. 46 In den Milzen der Kontrollmäuse, die keinerlei Injektion erhalten hatten, fanden sich nur vereinzelt apoptotische Zellen. Auffällig waren die Färbungen der Mäuse, die nur eine hohe Dosis des Antigens injiziert bekommen hatten: hier fanden sich wenige Keimzentren, aber über die gesamte Milz verstreut einzelne TUNEL pos. Zellen. Dieser Befund war bei den Wildtypmäusen (Gruppe C) weniger stark ausgeprägt (nicht signifikant) als bei den C4-/-Mäusen (Gruppe G). (Abb.8, S.46) 3.1.2 Analyse am Durchflußfluoreszenzzytometer Ein Teil der Milzen der Wildtyp- und C4-/-Mäuse wurde zerrieben, und die Splenozyten wurden isoliert. (Kapitel 2.2.3) Die nach dem ersten Schritt der Lymphozytenaufreinigung gewonnenen Zellen (Kapitel 2.2.3.1) wurden im Durchflußfluoreszenzzytometer analysiert. Dabei zeigte sich, daß diese Splenozyten zu ca. 67% (+/-10%) B-Lymphozyten waren, erkennbar an den Oberflächenmarkern B220 (CD45) und CD19. Die restliche Zellpopulation setzte sich überwiegend aus T-Lymphozyten und Makrophagen zusammen. Diese Verteilung war für alle Versuchsgruppen gleich. Ohne weitere Aufreinigung (d.h. ohne spezifische Isolierung der B-Lymphozyten) wurden die Zellen auf das Vorhandensein von apoptotischen Merkmalen hin untersucht. Die Gesamtzahl apoptotischer, d.h. TUNEL pos. Zellen war allerdings sehr klein (um 1% der untersuchten Zellen), so daß sich mit dieser Methode keine signifikanten Unterschiede zwischen den einzelnen Versuchsgruppen feststellen ließ. (Abb.9) Antigeninduzierte Apoptose Anzahl apoptotischer Zellen in der Milz (Durchflußfluoreszenzzytometrische Analyse) Prozent TUNEL pos. Zellen 8 A: Wt, beide Inj. (n=8) 7 B: Wt, nur 1.Inj. (n=4) 6 C: Wt, nur 2. Inj. (n=4) 5 4 D: Wt, keine Inj. (n=2) 3 E: C4-/-, beide Inj. (n=8) Abbildung 9: 2 F: C4-/-, nur 1. Inj. (n=4) 1 G: C4-/-, nur 2. Inj. (n=4) Anzahl apoptotischer Zellen in der Milz (mit Standardabweichung) 0 Versuchsgruppe H: C4-/-, keine Inj. (n=2) Analyse aufgereinigter Splenozyten im Durchflußfluoreszenzzytometer 47 3.1.3 Antikörperbestimmung mittels ELISA Um eine Aussage über die Stärke der Immunantwort der Mäuse gegen Np, und damit indirekt über die Aktivität der spezifischen B-Lymphozyten, treffen zu können, wurde der Titer Np-spezifischer Antikörper im Serum mittels ELISA bestimmt. Betrachtet man den Verlauf der Immunantwort, so war in allen behandelten Versuchsgruppen (Gruppen A und E) nach Injektion der ersten Dosis von 50µg des Antigens ein unterschiedlich starker Anstieg der Np-spezifischen Antikörper zu beobachten. Mit Injektion der hohen Dosis, 4mg des Antigens, fiel der Antikörperspiegel wieder ab, um danach langsam wieder anzusteigen. Blieb diese Injektion aus (Gruppen B und F), so sank der Antikörperspiegel auch nicht ab. Unbehandelte Mäuse (Gruppen D und H) oder Mäuse, die nur am Tag 9 4mg des Antigens injiziert bekommen hatten (Gruppen C und G), zeigten keinen Anstieg Np-spezifischer Antikörper. (Abb.10a, S.49) Im einzelnen variierten die Antikörperantworten in den verschiedenen Immunglobulinsubklassen jedoch deutlich, und wichen teilweise auch von dem oben zusammengefaßt wiedergegebenen Ablauf ab. Auf diese individuellen Unterschiede wird in den Unterkapiteln der Subklassen näher eingegangen werden. Des weiteren fiel auf, daß vor allem unter den C4-/-Mäusen einige Mäuse nicht in allen Subklassen eine Immunantwort entwickelten. Da bekannt ist, daß C4-/-Mäuse im Schnitt eine schwächere Immunantwort ausprägen, wurden diese Mäuse nicht aus der Wertung genommen. Allgemein läßt sich zusammenfassen, daß die einzelnen Mäuse sehr unterschiedlich auf das injizierte Antigen reagierten, d.h. verschieden hohe Antikörperspiegel entwickelten, und somit der Standardfehler oft groß war. Aufgrund der begrenzten Anzahl an zur Verfügung stehenden Versuchstieren wurde nur die Unterschiede zwischen den eigentlichen Versuchsgruppen (A vs. E) statistisch ausgewertet. Somit läßt sich über die Signifikanz der in den Kontrollgruppen (B, C, D, F, G, und H) gefundenen Trends nur begrenzt eine Aussage treffen. 3.1.3.1 IgM Alle Mäuse, die am Tag 0 50µg des Antigens injiziert bekommen hatten (Gruppen A,B,E,F) zeigten am Tag 8 nach dieser Injektion eine IgM-Antwort gegen selbiges. In dieser primären Immunantwort zeigte sich zu Beginn (Tag8) kein signifikanter Unterschied 48 zwischen C4-/- (Gruppen E und F) und Wildtypmäusen (Gruppen A und B), und auch im weiteren Verlauf der unbeeinflußten Immunantwort bis zum Tag 30 (Gruppen B und F) unterschieden sich Wildtyp- und C4-/-Mäuse nicht. (Abb.10c) Eine einzelne Dosis von 4mg Np löste bei beiden Mausstämmen keinen Anstieg der Anti- 300 350 250 300 IgM-Spiegel (1000 arb. U) IgM-Spiegel (1000 arb. U) Np IgM-Antikörper im Serum aus (Gruppen C und G). (Abb.10a und b) 200 150 100 50 250 200 150 100 50 0 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 T age nach erster Injektion a: Wt A: beide Inj. (n=12) C: nur zweite Inj. (n=5) 0 30 4 6 B: nur erste Inj. (n=5) D: keine Inj. (n=3) 8 10 12 14 16 18 20 22 24 26 28 30 T age nach erster Injektion b: C4-/- E: beide Inj. (n=12) G: nur zweite Inj. (n=4) F: nur erste Inj. (n=4) H: keine Inj. (n=3) 150% IgM-Spiegel in Prozent des Wertes von Tag 8 350 300 IgM-Spiegel (1000 arb. U) 2 250 200 150 100 50 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 30 T age nach erster Injektion 50% 0% 0 8 9 16 23 30 T age nach erster Injektion d: Vergleich Wt mit C4-/- c: Vergleich Wt mit C4-/A:wt,beide Inj.(n=12) B:wt,nur erste Inj.(n=5) 100% E:C4-/-,beide Inj.(n=12) F:C4-/-,nur erste Inj.(n=4) A: wt, beide Inj. (n=12) E: C4-/-, beide Inj. (n=12) Abbildung 10: IgM-Immunantwort gegen Np a: IgM im Serum der Wildtypmäuse (Gruppen A-D), (Gruppe A mit Standardfehler) b: IgM im Serum der C4-/-Mäuse (Gruppen E-H), (Gruppe E mit Standardfehler) c: IgM im Serum von Wildtyp- und C4-/-Mäusen (Gruppen A,B vs. E,F), (A vs. E: *p<0,05) d: IgM in Prozent des Serumspiegels von Tag 8 von Wildtyp- und C4-/-Mäusen (Mittelwerte von Tag 8 der jeweiligen Versuchsgruppe sind auf 100% gesetzt), (Gruppen A vs. E), zur Darstellung des Wiederanstiegs nach dem Antigeninduzierten Abfall am Tag 9 (mit Standardfehler, *p<0,05) Acht Stunden nach der 2. Injektion von 4mg des gleichen Antigens gekoppelt an ein anderes Protein (BSA) war der IgM-Antikörperspiegel bei Wildtyp- (Gruppe A) und C4-/Mäusen (Gruppe E) bis auf das Ausgangsniveau abgefallen. Eine Woche später fanden sich jedoch erneut spezifische IgM-Antikörper im Serum, bei den Wildtypmäusen etwa 49 50% einer normalen, ungestörten Immunantwort, bei den C4-/-Mäusen etwa 70%. Dieser Antikörperspiegel blieb auch über die nächsten beiden Wochen konstant. (Abb.10c, S.49) Vergleicht man den Wiederanstieg der Antikörper im Serum nach dem antigeninduzierten Abfall am Tag 9 (Tage 16-30) mit den Antikörperspiegeln am Tag 8 (einem Maß für die unbeeinflußte Immunantwort gegen Np), so zeigt sich, daß C4-/-Mäuse einen signifikant stärkeren Wiederanstieg haben als Wildtypmäuse. (Abb.10d, S.49) Interessanterweise zeigte ein Großteil der C4-/-Mäuse einen erhöhten Anti-Np IgMSpiegel im Blut, (Abb.10b, S.49) ohne vorher mit dem Antigen in Kontakt gekommen zu sein (Gruppen F,G und H). Dieser erhöhte Grundtiter konnte bei Wildtypmäusen nicht gefunden werden (Gruppen D). 3.1.3.2 IgG1 Auch die Immunantwort in der IgG1-Subklasse schien nach einer Woche schon voll etabliert zu sein (Gruppen A und B (wt), E und F (C4-/-)). Allerdings zeigten die C4-/Mäuse der Gruppe F eine deutlich reduzierte Antwort gegenüber den am Tag 8 noch gleich behandelten Mäusen der Gruppe E. Im Vergleich mit der IgG1-Immunantwort von Wildtypmäusen (Gruppen A,B) war der IgG1-Spiegel im Serum der C4-/-Mäuse zu allen Zeiten deutlich erniedrigt (Gruppen E,F), wobei der Unterschied nur an den Tagen 16-30 signifikant war. (Abb.11c, S.51) Um den Wiederanstieg der Np-spezifischen IgG1-Antikörper im Serum nach Injektion der zweiten, hohen, Dosis des Antigens trotz der unterschiedlich starken Immunantwort von C4-/- und Wildtypmäusen vergleichen zu können, wurden die Werte wiederum zu dem IgG1-Spiegel der jeweiligen Versuchsgruppe am Tag 8 in Bezug gesetzt. Dabei zeigte sich, daß sich bei Wildtypmäusen schon am Tag 16, also eine Woche nach der zweiten Injektion, 85% des IgG1-Spiegels der unbeeinflußten Immunantwort finden, wogegen C4/-Mäuse nach dem antigeninduzierten Abfall des Antikörperspiegels nur bis zu 44% des am Tag 8 gemessenen IgG1-Spiegels wieder produzieren können. Dieser Unterschied ist am Tag 16 signifikant, scheint sich aber bis zum Tag 30 abzuschwächen. (Abb.11d, S.51) 50 2.500 1.400 1.200 IgG1-Spiegel (1000 arb. U) IgG1-Spiegel (1000 arb. U) 2.000 1.500 1.000 1.000 800 600 400 500 200 0 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 30 T age nach erster Injektion a: Wt A: beide Inj. (n=12) C: nur zweite Inj. (n=5) 0 B: nur erste Inj. (n=5) D: keine Inj. (n=3) IgG1-Spiegel (1000 arb. U) 1.400 1.200 1.000 800 600 400 200 0 4 6 8 10 12 14 16 18 20 22 24 26 28 30 T age nach erster Injektion c: Vergleich Wt mit C4-/A:wt,beide Inj.(n=12) B:wt,nur erste Inj.(n=5) 6 8 10 12 14 16 18 20 22 24 26 28 30 T age nach erster Injektion E: beide Inj. (n=12) G: nur zweite Inj. (n=4) IgG1-Spiegel in Prozent des Wertes von Tag 8 1.600 2 4 b: C4-/- 1.800 0 2 F: nur erste Inj. (n=4) H: keine Inj. (n=3) 140% 120% 100% 80% 60% 40% 20% 0% 0 8 9 16 23 30 T age nach erster Injektion d: Vergleich Wt mit C4-/E:C4-/-,beide Inj.(n=12) F:C4-/-,nur erste Inj.(n=4) A: wt, beide Inj. (n=12) E: C4-/-, beide Inj. (n=12) Abbildung 11: IgG1-Immunantwort gegen Np a:IgG1 im Serum der Wildtypmäuse (Gruppen A-D), (Gruppe A mit Standardfehler) b: IgG1 im Serum der C4-/-Mäuse (Gruppen E-H), (Gruppe E mit Standardfehler) c: IgG1 im Serum von Wildtyp- und C4-/-Mäusen (Gruppen A,B vs. E,F), (A vs. E: *p<0,05) d: IgG1 in Prozent des Serumspiegels von Tag 8 von Wildtyp- und C4-/-Mäusen (Mittelwerte von Tag 8 der jeweiligen Versuchsgruppe sind auf 100% gesetzt), (Gruppen A vs. E), zur Darstellung des Wiederanstiegs nach dem Antigeninduzierten Abfall am Tag 9 (mit Standardfehler, *p<0,05) 3.1.3.3 IgG2a Ein Standard zur Messung der Immunantwort in der IgG2a-Subklasse ließ sich nicht etablieren, und eine Immunantwort in dieser Subklasse ließ sich somit nicht messen. Die Ursachen und Konsequenzen werden im Kapitel 4.1.1.1 abgehandelt. 3.1.3.4 IgG2b Die Injektion von 50µg Np-CGG in Alum löste auch die Bildung von Anti-NpAntikörpern der IgG2b-Subklasse aus: an den Tagen 8, 9 und 16 nach der Injektion finden sich in Wildtyp- (Gruppe B) und C4-/-Mäusen (Gruppe F) deutlich erhöhte IgG2b-Titer. Diese sind bei den Wildtypmäusen noch ca. viermal höher als bei den C4-/-Mäusen, wobei 51 dieser Unterschied zwischen den Gruppen A (wt) und E (C4-/-) auch signifikant ist. Interessanterweise beginnt der Antikörperspiegel bei beiden Mausstämmen nach 2 Wochen wieder abzufallen bis er am Tag 30 fast das Ursprungsniveau erreicht. (Abb.12c) Auch in dieser Subklasse werden eine Woche nach dem antigeninduzierten Abfall des IgG2b-Spiegels (Gruppen A und E), am Tag 16, wieder Antikörper im Serum gefunden. Bei den Wildtypmäusen (Gruppe A) ist die Antikörperantwort im Vergleich zu Tag 8 um etwa 50% reduziert, bei den C4-/-Mäusen um etwa 60% (Gruppe E). In beiden Gruppen ist die Relation des weiteren Anstiegs schlecht zu beurteilen, da ab dem Tage 16 auch die unbeeinflußte Immunantwort stark zurückgeht. Es läßt sich jedoch zu keinem Zeitpunkt ein signifikanter Unterschied zwischen der Stärke des Wiederanstiegs der C4-/-(E) und Wildtypgruppe (A) zeigen. (Abb.12d) 300 90 80 250 IgG2b-Spiegel (1000 arb. U) IgG2b-Spiegel (1000 arb. U) 70 200 150 100 50 60 50 40 30 20 10 0 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 T age nach erster Injektion a: Wt A: beide Inj. (n=12) C: nur zweite Inj. (n=5) 0 30 2 4 6 10 12 14 16 18 20 22 24 26 28 30 T age nach erster Injektion b: C4-/- B: nur erste Inj. (n=5) D: keine Inj. (n=3) 8 E: beide Inj. (n=12) G: nur zweite Inj. (n=4) F: nur erste Inj. (n=4) H: keine Inj. (n=3) IgG2b-Spiegel in Prozent des Wertes von Tag 8 300 IgG2b-Spiegel (1000 arb. U) 250 200 150 100 50 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 30 T age nach erster Injektion c: Vergleich Wt mit C4-/A:wt,beide Inj.(n=12) B:wt,nur erste Inj.(n=5) 140% 120% 100% 80% 60% 40% 20% 0% 0 8 9 16 23 30 T age nach erster Injektion d: Vergleich Wt mit C4-/E:C4-/-,beide Inj.(n=12) F:C4-/-,nur erste Inj.(n=4) A: wt, beide Inj. (n=12) E: C4-/-, beide Inj. (n=12) Abbildung 12: IgG2b-Immunantwort gegen Np a: IgG2b im Serum der Wildtypmäuse (Gruppen A-D), (Gruppe A mit Standardfehler) b: IgG2b im Serum der C4-/-Mäuse (Gruppen E-H), (Gruppe E mit Standardfehler) c: IgG2b im Serum von Wildtyp- und C4-/-Mäusen (Gruppen A,B vs. E,F), (A vs. E: *p<0,05) d: IgG2b in Prozent des Serumspiegels von Tag 8 von Wildtyp- und C4-/-Mäusen (Gruppen A vs. E), (mit Standardfehler, *p<0,05) (Mittelwerte von Tag 8 der jeweiligen Versuchsgruppe sind auf 100% gesetzt) zur Darstellung des Wiederanstiegs nach dem Antigeninduzierten Abfall am Tag 9 52 3.1.3.5 IgG3 Bei der Beurteilung der IgG3-Immunantwort ist zu beachten, daß die Kontrollgruppen (BD, F-H) in diesem Fall mangels auswertbarem Untersuchungsmaterial aus nur sehr wenigen Mäusen (z.T.n=2) bestanden und somit Ausreißer stärker ins Gewicht fallen. (Abb.13a und b, S.54) Dementsprechend ist der Verlauf der unbeeinflußten IgG3-Immunantwort der Wildtypmäuse gegen Np (Gruppe B) nicht sicher aus den Daten zu bestimmen. Es scheint, daß der IgG3-Spiegel bei Wildtypmäusen erst nach einer Woche zu steigen beginnt, um am Tag 16 seinen Höhepunkt zu erreichen und dann wieder abzufallen. Dagegen zeigten die Mäuse der Gruppe A, die am Tag 0 ebenfalls eine Injektion von 50µg des Antigens erhalten hatten, also bis dahin gleich behandelt worden waren, schon nach einer Woche einen deutlichen Anstieg des IgG3-Spiegels im Serum. (Abb.13a, S.54) Auch bei den C4-/-Tieren zeigen sich am Tag 8 zwischen den bis dahin eigentlich gleich behandelten Gruppen E und F ein Unterschied, nur daß in diesem Fall mehr IgG3Antikörper im Serum der Mäuse der Kontrollgruppe (F) zu finden war. Die Mäuse der Gruppe E zeigten nur einen sehr schwachen Anstieg der Anti-Np IgG3-Antikörper, sowohl am Tag 8 nach der ersten Immunisierung als auch an den Tagen 16-30, nach der zweiten Injektion von 4mg des Antigens. (Abb.13b, S.54) Bei dem Vergleich der unbeeinflußt ablaufenden Immunantwort von C4-/-Mäusen (Gruppe E) mit der der Wildtypmäuse (Gruppe A) scheint die der C4-defizienten Tiere wesentlich geringer auszufallen. Dieser Unterschied war jedoch zu keinem Zeitpunkt signifikant. (Abb.13c, S.54) Bei den Wildtypmäusen (Gruppe A) fallen die Antikörper nach der zweiten Injektion des Antigens bis auf das Ausgangsniveau ab, und steigen eine Woche später wieder an, ohne jedoch den Höchstwert wieder zu erreichen. (Abb.13a, S.54) Da bei den C4-/-Mäusen die Immunantwort sehr schwach und uneinheitlich auszufallen scheint, wurde auf eine weitere Analyse der Daten (Analyse des Wiederanstiegs der Antikörperspiegel nach Tag 9) verzichtet. 53 100 16 90 14 70 IgG3-Spiegel (1000 arb. U) IgG3-Spiegel (1000 arb. U) 80 60 50 40 30 20 12 10 8 6 4 2 10 0 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 30 T age nach erster Injektion a: Wt A: beide Inj. (n=6) C: nur zweite Inj. (n=3) 0 b: C4-/- B: nur erste Inj. (n=2) D: keine Inj. (n=2) 2 4 6 8 10 12 14 16 18 20 22 24 26 28 T age nach erster Injektion E: beide Inj. (n=6) G: nur zweite Inj. (n=3) F: nur erste Inj. (n=3) H: keine Inj. (n=2) 50 45 IgG3-Spiegel (1000 arb. U) 40 35 30 Abbildung 13: IgG3-Immunantwort gegen Np 25 20 a: IgG3 im Serum der Wildtypmäuse (Gruppen A-D), (Gruppe A mit Standardfehler) 15 10 5 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 30 T age nach erster Injektion c: Vergleich Wt mit C4-/A:wt,beide Inj.(n=6) B:wt,nur erste Inj.(n=2) E:C4-/-,beide Inj.(n=6) F:C4-/-,nur erste Inj.(n=3) 30 b: IgG3 im Serum der C4-/-Mäuse (Gruppen EH), (Gruppe E mit Standardfehler) c: IgG3 im Serum von Wildtyp- und C4-/Mäusen (Gruppen A,B vs. E,F), (A vs. E: *p<0,05) Zusammenfassend läßt sich sagen, daß die normale Immunantwort gegen Np in allen untersuchten IgG-Subklassen bei C4-/-Mäusen signifikant geringer ausfällt als bei Wildtypmäusen, die IgM-Produktion nach Immunisierung der Mäuse durch C4-Mangel jedoch unbeeinflußt scheint. Auch der Wiederanstieg der Antikörperspiegel nach dem durch die zweite, hohe Dosis an injiziertem Antigen provozierten Abfall des Antikörperspiegels fällt, soweit beurteilbar, in den IgG-Subklassen bei C4-/-Mäusen schwächer aus als in der vergleichbaren Gruppe von Wildtypmäusen. Dieser Unterschied ist jedoch nur in einer Subklasse signifikant. Der Wiederanstieg des IgM-Antikörperspiegels ist dagegen bei C4-/-Mäusen signifikant stärker ausgeprägt als bei Wildtypmäusen. 54 3.1.4 Beeinflussung des immunologischen Gedächtnisses durch Komplementmangel Auch die Funktion des immunologischen Gedächtnisses kann einen Hinweis auf die Effektivität der Apoptose im Rahmen der Keimzentrumsreaktion geben. Sollten durch Injektion einer hohen Dosis des Antigens in eine etablierte Immunantwort hinein ein Großteil der im Keimzentrum befindlichen B-Zellen absterben, so wäre die Bildung der Gedächtniszellen gestört und der Ablauf einer zweiten Immunantwort gegen das Antigen verändert. Um zu überprüfen, ob die Gedächtniszellbildung durch Komplementmangel beeinflußt wird, wurde Mäusen aller Versuchsgruppen sechs Monate nach den oben beschriebenen Versuchen (am Tag 180) erneut eine niedrige Dosis des Antigens an ein anderes Protein gebunden (100µg Np-BSA) ohne weitere Adjuvantien intraperitoneal appliziert. (Tab.9) Im Verlauf wurde den Mäusen an den Tagen 183,187,194 und 201 Blut entnommen, und in dem daraus gewonnenen Serum wurden mittels ELISA die Konzentration der Np-spezifischen Antikörper bestimmt. Ein Vorversuch hatte gezeigt, daß diese Dosis des Antigens ohne weitere Adjuvantien bei vorher unbehandelten Mäusen die Bildung von Immunglobulinen der Klasse M (IgM), aber nicht von Immunglobulinen der Klasse G (IgG) induziert. Somit konnte anhand der Bildung von Immunglobulinen der Klasse G bei den unterschiedlich vorbehandelten Mäusen des Suicide-Versuches eine primäre von einer sekundären Immunantwort gegen Np unterschieden werden. Tabelle 9: Übersicht über den Versuchsaufbau zur Untersuchung immunologischen Gedächtnisses bei Komplementmangel des 55 3.1.4.1 Antikörperbestimmung mittels ELISA Auch in diesem Versuch wurde wieder deutlich, daß die einzelnen Werte der Immunglobulinkonzentrationen innerhalb der einzelnen Versuchsgruppen zum Teil sehr stark differierten. Der Standardfehler war dementsprechend z.T. sehr groß. (Abb.16b, S.59) Außerdem ist festzustellen, daß zwei der C4-/-Mäuse der Versuchsgruppe F noch am Tag 180 einen vergleichsweise hohen Spiegel an Np-spezifischen IgM- und IgG1-Antikörpern aufwiesen, obwohl in allen andern Mäusen die primäre Immunantwort schon wieder abgeklungen war. Diese Mäuse wurden nicht aus der Wertung genommen. 3.1.4.2 IgM Alle Mäuse zeigten am siebten Tag nach der erneuten Injektion des Antigens (Tag 187) eine spezifische IgM-Produktion. Innerhalb der Gruppe der Wildtypmäuse war der IgM-Spiegel im Serum in den Gruppen A (alle drei Injektion) und B (nur erste und dritte Injektion), bei denen 6 Monate zuvor schon eine Np-spezifische Immunantwort abgelaufen war, etwa doppelt so hoch wie in den Kontrollgruppen C (nur zweite und dritte Injektion) und D (nur dritte Injektion). Nach zwei Wochen begann dieser Titer wieder abzufallen. (Abb.14a, S.57) Auch die C4-/-Mäuse entwickelten nach einer Woche Np-spezifische IgM-Antikörper, die in den Versuchsgruppen E, G und H auch ähnlich hohe Titer erreichten wie die der Wildtypmäuse. (Abb.14b, S.57) Auffällig ist, daß in der Gruppe F, d.h. der C4-defizienten Tiere, die 6 Monate zuvor nur einmal mit 50µg Np-CGG in Alum immunisiert worden waren, zwei Mäuse schon am Tag 180 einen hohen Antikörperspiegel hatten, der 7 Tage nach der erneuten Injektion von 100µg Np-BSA noch weiter anstieg. Da diese Mäuse nicht aus der Wertung genommen wurden, lag der IgM-Spiegel in dieser Versuchsgruppe deutlich höher als in den anderen Gruppen C4-/-Mäuse. (Abb.14b, S.57) Zwischen den Wildtypmäusen der Gruppe A und den C4-/-Mäusen der Gruppe E ließ sich kein signifikanter Unterschied in der Stärke dieser zweiten Immunreaktion feststellen. (Abb.14c, S.57) 56 400 700 600 300 IgM-Spiegel (1000 arb. U) IgM-Spiegel (1000 arb. U) 350 250 200 150 100 500 400 300 200 100 50 0 0 180 182 184 186 188 190 192 194 196 198 180 200 T age nach erster Injektion a: Wt A: alle drei Inj. (n=9) C: nur 2. und 3. Inj. (n=3) 182 186 188 190 192 194 196 198 200 T age nach erster Injektion b: C4-/- B: nur 1. und 3. Inj. (n=4) D: nur 3. Inj. (n=3) 184 E: alle drei Inj. (n=9) G: nur 2. und 3. Inj. (n=4) F: nur 1. und 3. Inj. (n=3) H: nur 3. Inj. (n=3) 700 IgM-Spiegel (1000 arb. U) 600 500 Abbildung 14: 400 IgM-Produktion im Rahmen einer sekundären Immunantwort gegen Np 300 200 a: IgM im Serum der Wildtypmäuse (Gruppen A-D), (Gruppe A mit Standardfehler) 100 0 180 182 184 186 188 190 192 194 196 198 b: IgM im Serum der C4-/-Mäuse (Gruppen EH), (Gruppe E mit Standardfehler) 200 T age nach erster Injektion c: Vergleich Wt mit C4-/A:wt,alle drei Inj. (n=9) B:wt, nur 1.u.3.Inj. (n=4) E:C4-/-,alle drei Inj. (n=9) F:C4-/-nur 1.u.3.Inj. (n=3) c: IgM im Serum von Wildtyp- und C4-/Mäusen (Gruppen A,B vs. E,F), (A vs. E: *p<0,05) 3.1.4.3 IgG Die Mäuse, die vorher noch keine Immunantwort gegen Np entwickelt hatten, produzierten nach der Injektion von 100µg Np-BSA i.p. keine Antikörper der IgG-Subklassen. Dabei machte es keinen Unterschied, ob die Mäuse noch nie mit dem Antigen in Berührung gekommen waren (Gruppen D und H) oder aber 6 Monate zuvor die hohe Dosis Np (4mg) injiziert bekommen hatten, und daraufhin keine Immunantwort entwickelt hatten (Gruppen C und G). (Abb.15a und b, S.58) Die jeweilige Immunantwort in den einzelnen IgG-Subklassen der anderen Versuchsgruppen (Gruppen A, B, E und F) wird im Folgenden dargestellt. 3.1.4.3.1 IgG1 Die Titer der Np-spezifischen IgG1-Antikörper unterscheiden sich bei Wildtyp- und C4-/Mäusen nicht. Bei beiden Stämmen reagierten Mäuse, die sechs Monate zuvor mit 50µg des Antigens in Alum immunisiert worden waren (Gruppen B und F), d.h. schon eine 57 normale Immunantwort gegen Np durchlaufen hatten, nach einer Woche mit der Bildung von Np-spezifischen IgG1-Antikörpern. (Abb.15c) Auch bei Mäusen, die in diese etablierte Immunantwort hinein zusätzliche 4mg des Antigens injiziert bekommen hatten (Gruppen A und E), fanden sich ab dem Tag 187 IgG1-Antikörper im Serum. Allerdings war der IgG1-Titer im Serum dieser Mäuse deutlich niedriger als der der Mäuse, die eine unbeeinflußte primäre Immunantwort durchlaufen hatten (etwa 25% des IgG1-Spiegels der Gruppe B bei den Wildtypmäusen der Gruppe A und ca. 35% des IgG1-Spiegels der Gruppe F bei den C4-defizienten Mäusen der Gruppe E). Dieser Unterschied war bei den Wildtypmäusen ab dem Tag 187, 1.000 1.000 900 900 800 800 700 700 IgG1-Spiegel (1000 arb. U) IgG1-Spiegel (1000 arb. U) (Abb.15a) bei den C4-/-Mäusen erst am Tag 201 signifikant. (Abb.15b) 600 500 400 300 600 500 400 300 200 200 100 100 0 0 180 182 184 186 188 190 192 194 196 198 200 T age nach erster Injektion a: Wt A: alle drei Inj. (n=9) C: nur 2. und 3. Inj. (n=3) 180 182 184 b: C4-/- B: nur 1. und 3. Inj. (n=4) D: nur 3. Inj. (n=3) 186 188 190 192 194 196 198 200 T age nach erster Injektion E: alle drei Inj. (n=9) G: nur 2. und 3. Inj. (n=4) F: nur 1. und 3. Inj. (n=3) H: nur 3. Inj. (n=3) 900 800 Abbildung 15: IgG1-Spiegel (1000 arb. U) 700 IgG1-Produktion im Rahmen einer sekundären Immunantwort gegen Np 600 500 400 a: IgG1 im Serum der Wildtypmäuse (Gruppen A-D), (Gruppen A und B mit Standardfehler, A vs. B: *p<0,05) 300 200 100 0 180 182 184 186 188 190 192 194 196 198 200 T age nach erster Injektion c: Vergleich Wt mit C4-/A:wt,alle drei Inj. (n=9) B:wt, nur 1.u.3.Inj. (n=4) E:C4-/-,alle drei Inj. (n=9) F:C4-/-nur 1.u.3.Inj. (n=3) b: IgG1 im Serum der C4-/-Mäuse (Gruppen EH), (Gruppen E und F mit Standardfehler, E vs. F: *p<0,05) c: IgG1 im Serum von Wildtyp- und C4-/Mäusen (Gruppen A,B vs. E,F), (A vs. E: *p<0,05) 3.1.4.3.2 IgG2a Ein Standard zur Messung der Immunantwort in der IgG2a-Subklasse ließ sich, wie schon beim „Suicide-Versuch“ nicht etablieren, und eine Immunantwort in dieser Subklasse ließ sich nicht messen. Dies wird in Kapitel 4.1.1.1 genauer erörtert. 58 3.1.4.3.3 IgG2b In der IgG2b-Subklasse zeigte sich der Unterschied zwischen Mäusen, die 6 Monate zuvor eine ungestörte Immunantwort gegen Np durchlaufen hatten, und den Mäusen, die am Tag 9 eine zusätzliche Injektion des Antigens (4mg NP-BSA) erhalten hatten, noch deutlicher. Nur Mäuse der erstgenannten Gruppen (B und F) entwickelten nach der Injektion von 100µg Np-BSA eine nennenswerte IgG2b-Antwort. Bei den Wildtypmäusen war dieser Unterschied (Gruppe A vs. Gruppe B) an den Tagen 194 bis 201 signifikant, (Abb.16a) im Gegensatz zu den C4-/-Mäusen, bei denen keine signifikanten Unterschiede zwischen den 350 80 300 70 250 IgG2b-Spiegel (1000 arb. U) IgG2b-Spiegel (1000 arb. U) Gruppen E und F nachgewiesen werden konnten. (Abb.16b) 200 150 100 50 60 50 40 30 20 10 0 0 180 182 184 186 188 190 192 194 196 198 200 T age nach erster Injektion a: Wt A: alle drei Inj. (n=9) C: nur 2. und 3. Inj. (n=3) 180 182 184 188 190 192 194 196 198 200 T age erster nach Injektion b: C4-/- B: nur 1. und 3. Inj. (n=4) D: nur 3. Inj. (n=3) 186 E: alle drei Inj. (n=9) G: nur 2. und 3. Inj. (n=4) F: nur 1. und 3. Inj. (n=3) H: nur 3. Inj. (n=3) 18 350 16 300 IgG2b-Spiegel (1000 arb. U) IgG2b-Spiegel (1000 arb. U) 14 250 200 150 100 50 12 10 8 6 4 2 0 0 180 182 184 186 188 190 192 194 196 198 200 T age nach erster Injektion c: Vergleich Wt mit C4-/A:wt,alle drei Inj. (n=9) B:wt, nur 1.u.3.Inj. (n=4) E:C4-/-,alle drei Inj. (n=9) F:C4-/-nur 1.u.3.Inj. (n=3) 180 182 184 186 188 190 192 194 196 198 200 T age nach erster Injektion d: Vergleich Wt mit C4-/A:wt,alle drei Inj. (n=9) E:C4-/-,alle drei Inj. (n=9) Abbildung 16: IgG2b-Produktion im Rahmen einer sekundären Immunantwort a: IgG2b im Serum der Wildtypmäuse (Gruppen A-D), (Gruppen A und B mit Standardfehler, A vs. B: *p<0,05) b: IgG2b im Serum der C4-/-Mäuse (Gruppen E-H), (Gruppen E und F mit Standardfehler, E vs. F: *p<0,05) c: IgG2b im Serum von Wildtyp- und C4-/-Mäusen, (Gruppen A,B vs. E,F), (Gruppen B und F mit Standartfehler, B vs. F: *p<0,05) d: IgG2b im Serum von Wildtyp- und C4-/-Mäusen, (Gruppe A vs. E), (mit Standardfehler, *p<0,05) 59 Im Vergleich der C4-/-Mäuse mit den Wildtypmäusen fiel die „normale“ sekundäre Immunantwort fiel bei den Wildtypmäusen (Gruppe B) signifikant stärker aus als bei den C4-/-Mäusen (Gruppe F). (Abb.16c, S.59) Vergleicht man die Versuchsgruppen der beiden Mausstämme, deren primäre Immunantwort durch die Injektion von 4mg Np am Tag 9 unterbrochen wurde, so findet sich auch hier einen signifikanter Unterschied: die C4-/-Mäuse (Gruppe E) haben ab Tag 187 signifikant weniger Antikörper im Serum als die Wildtypmäuse (Gruppe A) der Vergleichsgruppe. (Abb.16d, S.59) 3.1.4.3.4 IgG3 Es konnte in dem untersuchten Zeitraum (Tag 180-201) in keiner der Versuchsgruppen ein nennenswerter Anstieg von IgG3-Antikörpern gegen Np nachgewiesen werden. Zusammenfassend kann man sagen, daß die IgM-Bildung einer sekundären Immunantwort durch eine zweite, hohe Dosis des Antigens während der ersten Immunantwort bei Wildtyp- und C4-/-Mäusen nicht verringert wird. Die Bildung von Antikörpern der Klasse G (IgG1 und IgG2b) im Rahmen einer sekundären Immunantwort wird dagegen bei beiden Mausstämmen durch eine Störung des Ablaufes der primären Immunantwort wie die Injektion von 4mg des Antigens stark abgeschwächt. Diese Verringerung des Antikörperspiegels war jedoch nur bei Wildtypmäusen signifikant. Unterschiede in der Stärke der sekundären IgG-Immunantwort zwischen Wildtyp- und C4defizienten Mäusen konnten bei den Mäusen des Suicide-Versuches (als Maß für die Effektivität der Antigeninduzierten Apoptose in diesem Versuch) nur in einer Subklasse gefunden werden. Die C4-defizienten Mäuse der Gruppe E wiesen signifikant niedrigere IgG2b-Spiegel als deren Wildtyp-Vergleichsgruppe A auf. 60 3.2 Beeinflussung der Fas (CD95)-induzierten Apoptose durch frühe Komplementkomponenten: Versuche in vitro Mit Hilfe dieser Versuchsreihe sollte der Einfluß früher Komplementfaktoren vermittelt über den Komplementrezeptors 2/1 (CD21/35) auf die Fas (CD95)-induzierte Apoptose von B-Lymphozyten untersucht werden. Dazu wurde zum einen mit aus der Milz von Wildtypmäusen isolierten B-Lymphozyten, und zum anderen mit zwei murinen BZellinien (WEHI 231 und 279) gearbeitet. Apoptotische Zellen wurden mit Hilfe des TUNEL-Verfahrens nachgewiesen. 3.2.1 Vorversuch 1: Phänotypische Eigenschaften der WEHI-Zellinien Die beiden murinen Zellinien WEHI 231 und 279 wurden über mehrere Wochen mit Hilfe des Durchflußfluoreszenzzytometer auf das Vorhandensein verschiedener Oberflächenmoleküle hin untersucht. Abstammend von B-Lymphozyten der Maus sollten beide Zellinien CD45R (B220) sowie CD19, Teil des B-Zell-Korezeptorkomplexes, exprimieren. Um das Entwicklungsstadium der Zellen abschätzen zu können, wurden sie außerdem auf das Vorhandensein von membranständigem IgD, IgM und Peanut-Agglutinin (PNA) untersucht. (Abb.17) Auch der Prozentsatz CD95 (Fas)- und CD21/35 (CR2/1)-tragender Zellen wurde über mehrere Monate hin bestimmt. (Abb.17) Oberflächenstruktur der WEHI-Zelllinien Prozent pos. Zellen 100 80 60 WEHI 231 40 WEHI 279 20 0 Isotyp (1) B220 (2) CD19 (3) FAS (4) CR2/1 (5) IgM (7) IgD (6) Oberflächenmarker Abbildung 17: Expression von Oberflächenmarkern der beiden Zellinien WEHI 231 und 279 gemessen im Durchflußfluoreszenzzytometer angegeben mit der Standardabweichung (n=9) 61 Am deutlichsten unterscheiden sich die beiden Zellinien in der CD19-Expression: ca. 95% aller lebenden WEHI 231-Zellen tragen CD19, im Gegensatz zu ca. 41% der lebenden WEHI 279-Zellen. Auch Immunglobulin der Klasse D (IgD) findet sich bei der WEHI 231-Zellinie in ausgeprägterem Maße. 40% der WEHI 231-Zellen tragen IgD, bei den WEHI 279-Zellen ist es dagegen nur bei ca.10% zu finden. (Abb.17, S.61) Die restlichen Oberflächenmarker sind bei beiden Zellinien in ähnlichem Maße ausgeprägt. So tragen fast alle Zellen beider Zellinien membranständiges IgM, 26% der lebenden WEHI 231-Zellen (36% der lebenden WEHI 279-Zellen) sind für CD45R (B220), positiv, 42% der lebenden WEHI 231-Zellen (51% der lebenden WEHI 279-Zellen) exprimieren die Komplementrezeptoren 2 und 1 (CD21/35) und 68% der WEHI 231-Zellen (79% der lebenden WEHI 279-Zellen) tragen den Fas-Rezeptor (CD95). (Abb.17, S.61) Beide Zellinien tragen kein Peanut-Agglutinin (PNA), ein Oberflächenmerkmal von BZellen des Keimzentrums. Abbildung 18: Darstellung von Größe und Granularität (FS/SS) der WEHI 231Zellinie als Densitogramm im Durchflußfluoreszenzzytometer Abbildung 19: Darstellung von Größe und Granularität (FS/SS) der WEHI 231Zellinie im Durchflußfluoreszenzzytometer braun: apoptotische Zellen (TUNEL pos.) grau: lebendige Zellen (TUNEL neg.) Bei allen Messungen fanden sich in der Darstellung der Größe und Granularität (FS/SS) zwei verschiedene, deutlich voneinander getrennte Populationen, die hier beispielhaft für die Zellinie WEHI 231 mit A und B bezeichnet werden. (Abb.18) Sie scheinen sich deutlich im Oberflächenmolekülmuster zu unterscheiden. (Abb.20, S.63) Die Zellen der Population B sind zum größten Teil TUNEL pos., also tote oder sterbende Zellen. (Abb.19) Daher beziehen sich die Angaben in Abbildung 17 auf die Population A. 62 Prozent der für den Marker pos. Zellen Oberflächenstruktur der WEHI-Zelllinien Population A vs. B 100 80 60 40 20 0 Isotyp CD19 FAS WEHI 231 Population A WEHI 231 Population B WEHI 279 Population A WEHI 279 Population Abbildung 20: Expression der Oberflächenmarker CD19 und Fas (CD95) in den beiden verschiedenen Zellpopulationen von WEHI 231 und 279 (Population A und B), angegeben mit der Standardabweichung (n=9) 3.2.2 Vorversuch 2: Apoptoseinduktion bei WEHI-Zellen Um in den beiden Zellinien Apoptose zu induzieren, wurden verschiedene Verfahren getestet: Entzug des Mediums durch Inkubation in PBS über 20h, Behandlung mit dem Zellgift Camptothecin (Sigma) über 4h, und Stimulation des Fas-Rezeptors (CD95) mit Anti-Maus CD95 (Pharmingen) über 10h. Danach wurde jeweils der Prozentsatz apoptotischer, d.h. TUNEL pos. Zellen im Durchflußfluoreszenzzytometer bestimmt. (Abb.21) Abbildung 21: Darstellung von apoptotischen Zellen mit Hilfe des TUNEL-Testes (Histogramm des Durchflußfluoreszenzzytometers) dunkelblau: neg. Kontrolle violett: WEHI 231 20h Mediumsentzug Dabei zeigte sich, daß in beiden Zellinien schon unter normalen Kulturbedingungen ein bestimmter Prozentsatz apoptotischer, d.h. TUNEL pos. Zellen vorlag, der leicht, aber 63 nicht signifikant unterschiedlich war (5% der WEHI 231-Zellen, 14% der WEHI 279Zellen). Dies waren zum größten Teil Zellen der Population B. (Abb.22) Nach Entzug des Nährmediums über 20h zeigten fast alle WEHI 231-Zellen (95%) apoptotisch fragmentierte DNA, im Gegensatz zu den Zellen der WEHI 279-Zellinie, von denen nur 23% pos. für TUNEL wurden. (Abb.22) Nach Behandlung mit Camptothecin wurden von beiden Zellinien ca. 80% der Zellen apoptotisch. (Abb.22) Obwohl beide Zellinien Fas (CD95) exprimieren, ließen sich nur WEHI 279-, nicht aber WEHI 231-Zellen durch Stimulation des Rezeptors zur Apoptose anregen. Nach Behandlung mit 5µg Anti-Maus CD95 über 10h waren nur 2% der WEHI 231-, aber 56% der WEHI 279-Zellen apoptotisch. Auch der Versuch das Signal durch Kreuzvernetzung der an CD95 (Fas) gebundenen Antikörper mittels Protein G (Sigma) zu verstärken, mißlang. Wurde zu den über Fas stimulierten Zellen zusätzlich Protein G dazugegeben (1µg pro 4*106 Zellen in 1ml Medium), zeigten sich nur 2% der WEHI 231-Zellen und 44% der untersuchten WEHI 279-Zellen positiv im TUNEL-Test. (Abb.22) Prozent TUNEL pos. Zellen Apoptoseinduktion bei WEHI-Zellen 100% 80% 60% WEHI 231 40% WEHI 279 20% 0% neg.Kontrolle Mediumsentzug Campthotecin Anti-FAS Ak Anti-FAS Ak und Prot.G Isotyp Ha 4/8 Abbildung 22: Apoptoseinduktion mittels verschiedener Methoden bei zwei WEHI-Zellinien Prozent TUNEL pos. Zellen, angegeben mit der Standardabweichung (n=8) neg. Kontrolle: Zellen 20h in Medium bei 37°C Mediumsentzug: Zellen 20h in PBS bei 37°C Campthothecin: Zellen 4h in DMSO mit Campthothecin bei RT Fas: Zellen 10h in Medium mit 5µg Anti-Maus CD95 bei 37°C (Brutschrank) Fas+Prot.G: Zellen 10h in Medium mit Anti-Maus CD95 und Prot.G bei 37°C In den weiteren Versuchen wurde die WEHI 231-Zellinie nur noch für die Positiv- und Negativkontrolle des Apoptosenachweises verwendet, alle anderen Versuche wurden mit der Fas (CD95)-sensiblen Zellinie WEHI 279 durchgeführt. 64 3.2.3 Der Einfluß von Komplement auf die Fas (CD95)-induzierte Apoptose von WEHI-Zellen Um den Einfluß von Komplement auf die Fas-induzierte Apoptose zu untersuchen, wurden die Zellen wie im vorigen Absatz beschrieben 10h mit 5µg Anti-Fas (CD95) Antikörper stimuliert und dann im Durchflußfluoreszenzzytometer auf das Vorhandensein von charakteristischen Merkmalen der Apoptose hin untersucht. Je nach Versuchsgruppe waren die Zellen vorher 10h mit Anti-Maus CD21/35, einem Antikörper gegen die Komplementrezeptoren 2 und 1 der Maus oder N1G9 (ein IgG der Maus gegen ein künstliches Antigen, Np) als Kontrolle behandelt worden. (Tab.10) Dafür wurden jeweils 4*106 Zellen in 1ml Medium aufgenommen, und mit 2µg des mit Biotin gekoppelten Antikörpers bei 37°C im Brutschrank 1h inkubiert. Nach Zugabe von je ca. 0,02µg ExtrAvidin (Sigma) zum Kreuzvernetzen der Antikörper wurden die Zellen nochmals 10h bei 37°C inkubiert. Vor der Induktion der Apoptose mittels Anti-Fas (CD95) Antikörper wurden die Zellen zwei mal in PBS gewaschen. Zusätzlich wurden WEHI 231-Zellen, die 20h in PBS inkubiert hatten, als Positivkontrolle, und gleichbehandelte WEHI 231-Zellen ohne spezifisch koppelndes Enzym (TdT des TUNEL-Testes) als Negativkontrolle mitgeführt. (Abb.23, S.66) Eine weitere Gruppe wurde 11h mit rekombinanten IL-4 (300 Units) (Pharmingen, Nr.550067) stimuliert. (Tab.10) Schließlich wurde die Anzahl apoptotischer Zellen mittels des TUNEL-Testes und der Durchflußfluoreszenzzytometrie bestimmt. Tabelle 10: Übersicht über den Versuchsaufbau zur Untersuchung der Fas (CD95)-induzierten Apoptose an WEHI-Zellen 65 FAS-induzierte Apoptose von WEHI 279-Zellen Prozent TUNEL pos. Zellen 100% 80% 60% 40% 20% 0% Versuchsgruppen pos. Kontrolle (Gruppe 1) neg. Kontrolle (Gruppe 2) unstimulierte Zellen (Gruppe 3) Anti-CD21/35 Ak (ohne Anti-Fas Ak) (Gruppe 4) Anti-Fas Ak (Gruppe 5) Anti-Fas Ak und N1G9 (Gruppe 6) Anti-Fas Ak und AntiCD21/35 Ak (Gruppe 7) Anti-Fas Ak und IL-4 (Gruppe 8) Abbildung 23: Fas (CD95)-induzierte Apoptose an WEHI-Zellen im Durchflußfluoreszenzzytometer Prozent TUNEL pos. Zellen, (mit Standardabweichung (n=3)) pos. Kontrolle (Gruppe 1): 20h in PBS Mediumsentzug (WEHI 231) neg. Kontrolle (Gruppe 2): 20h in PBS Mediumsentzug, TUNEL Boehringer Kit ohne spezifisch Koppelndes Enzym verwendet (WEHI 231) Wie man auf obenstehender Grafik (Abb.23) erkennen kann, überleben ein Großteil aller unstimulierten oder nur mit Anti-CD21/35 Antikörper behandelten Zellen. Nur 14% der Zellen unter Kulturbedingungen (Gruppe3) und 12% der Zellen die mit Anti-CR2/1 (CD21/35) Antikörper behandelt worden waren (Gruppe 4), zeigten Zeichen der Apoptose. Von den Zellen, die mit Fas (CD95) stimuliert worden waren (Gruppe5) starben. Durch vorhergehende Stimulation mit Anti-CD21/35 Antikörper (Gruppe 7) oder dem unspezifischen Antikörper N1G9 (Gruppe 6) ließ sich die Rate TUNEL pos. Zellen nicht senken, sie blieb mit 57% bei der Gruppe 7 und 61% der Gruppe 6 praktisch unverändert. Auch die vorhergehende Stimulation mit IL-4 (Gruppe 8) „rettete“ die Zellen nicht vor der Fas (CD95)-induzierten Apoptose (58% TUNEL pos. Zellen im Durchflußfluoreszenzzytometer). (Abb.23) 3.2.4 Vorversuch 3: Phänotypische Eigenschaften aufgereinigter Splenozyten Aus den Milzen von pro Versuch je drei Wildtypmäusen wurden zunächst Splenozyten über einen Dichtegradienten isoliert. (Kapitel 2.2.3.1) Die so gewonnenen Zellen wurden dann anhand spezifischer Oberflächenmarker weiter aufgereinigt. (Kapitel 2.2.3.2) Dies erfolgte mit Antikörpern, an welche sogenannte magnetische Beads gekoppelt sind und die verschiedene Epitope auf T-Lymphozyten oder Makrophagen wie CD11b, CD90 (Tyh1.2) 66 und CD11c erkennen. Mittels eines Magneten wurden dann die mit Beads behafteten Zellen (die Negativfraktion) entfernt. Die Reinheit der so gewonnenen Zellen (Positivfraktion) wurde dann zusammen mit dem Profil der Oberflächenmarkern der Zellen im Durchflußfluoreszenzzytometer untersucht. Dabei zeigte sich, daß diese Zellen („Positivfraktion“) im Durchschnitt zu ca. 80% B220 (CD45) und CD19, beides Marker von B-Zellen trugen. Allerdings wurde B220 wesentlich stärker exprimiert als CD19, d.h. die durchschnittliche Fluoreszenzintensität, ein Maß für die Ausprägung eines Merkmals auf einer einzelnen Zelle, lag für B220 deutlich höher (20 vs. 4). (Abb.24) Auch waren die Zellen fast vollständig für membranständiges IgM und IgD, (Abb.25) sowie für den Komplementrezeptor 2/1 (CD21/35) positiv. Abbildung 24: Darstellung der Expression verschiedener Oberflächenmoleküle aufgereinigter Splenozyten im Durchflußfluoreszenzzytometer (Histogramm des Durchflußfluoreszenzzytometers) dunkelblau: violett: Isotypkontrolle, B220, türkis: CD19 Abbildung 25: Darstellung der Expression von IgD auf isolierten Splenozyten (Histogramm des Durchflußfluoreszenzzytometers) dunkelblau: Isotypkontrolle, violett: IgD Wurden im Durchflußfluoreszenzzytometer nur die der Größe und Granularität von Lymphozyten entsprechenden Zellen (FS/SS) untersucht („gegatet“), so zeigte diese Untergruppe der Positivfraktion eine B-Zell-Reinheit von über 90%, d.h. über 90% der Zellen exprimierten B220, CD19, CD21/35, IgM und IgD. (Abb.26, S.68) 67 Oberflächenstruktur aufgereinigter Splenozyten "Positivfraktion" Prozent der für den untersuchten Marker pos. Zellen 100% 80% 60% 40% 20% 0% Isotyp B220 CD19 CR2/1 IgD IgM FAS CD3 CD90.2 Gr-1 F4/80 untersuchter Oberflächenmarker Abbildung 26: Expression von Oberflächenmarkern auf aufgereinigten Splenozyten (der „Positivfraktion“) gemessen im Durchflußfluoreszenzzytometer, mit Standardabweichung (n=4) Nur 60% der aufgereinigten B-Lymphozyten trugen den Fas-Rezeptor (CD95). (Abb.26) Dieser Prozentsatz ließ sich nicht durch Stimulation der Zellen mit Anti-CD40 oder AntiCD40 und Anti-CD8α über 48h variieren. (Kapitel 3.2.5) Die Zellen, die Fas exprimierten, trugen zu ca. 90% auch den Komplementrezeptor 2/1. Die mit Anti-CD40 stimulierten Zellen veränderten sich jedoch phänotypisch: sie wurden, erkennbar im Durchflußfluoreszenzzytometer, etwas größer und zeigten eine veränderte Granularität. (Abb.27) Abbildung 27: Größe (FS) und Granularität (SS) aufgereinigter Lymphozyten im Durchflußfluoreszenzzytometer nach Stimulation mit Anti-CD40 Antikörper über 49h Population B: B-Lymphozyten, die durch Stimulation des CD40-Rezeptors Größe und Granularität veränderten BL: größtenteils lebendige B-Zellen BT: apoptotische (TUNEL pos. B-Zellen) Population T: T-Lymphozyten (Größe und Granularität unstimulierter Lymphozyten) Die im zweiten Schritt der Aufreinigung (Kapitel 2.2.3.2) herausgefilterten Zellen der Negativfraktion, die für die Versuche nicht verwendet wurden, trugen zu 60% CD3 und 68 CD90.2, beides Marker von T-Lymphozyten, und zu 15% B220 und CD19. Zusätzlich fanden sich Zellen, die Gr-1 (ein Oberflächenmolekül von Granulozyten) oder F4/80 (ein Oberflächenmolekül von Makrophagen) exprimierten. (Abb.28) In einem anderen Versuchsansatz wurde auf den zweiten Schrittes der Aufreinigung, die Negativselektion anhand spezifischer Oberflächenmarker verzichtet und lediglich über einen Dichtegradienten aufgereinigt. In diesem Versuchsansatz lag der Prozentsatz der TLymphozyten, erkennbar an den Markern CD3 und CD90.2 (Thy-1) bei ca. 25%. Die restlichen Zellen waren zu 65% B220 pos., also wahrscheinlich B-Zellen, und weniger als 3% trugen Gr-1 oder F4/80. (Abb.29) 100% 80% 60% 40% 20% 0% untersuchter Oberflächenmarker Oberflächenstruktur aufgereinigter Splenozyten mit T-Zellen Isotyp B220 CD19 CD3 CD90.2 CD8 Gr1 F4/80 Abbildung 28: Oberflächestruktur der im Zuge der Aufreinigung herausgefilterten Zellen („Negativfraktion“) 3.2.5 Prozent der für den untersuchten Marker pos. Zellen Prozent der für den untersuchten Marker pos. Zellen Oberflächenstruktur aufgereinigter Splenozyten Negativfraktion 100% 80% Isotyp 60% B220 40% CD3 20% Gr1 0% untersuchter Oberflächenmarker F4/80 Abbildung 29: Oberflächestruktur aufgereinigter Splenozyten ohne Entfernung der T-Zellen Der Einfluß von Komplement auf die Fas (CD95)-induzierte Apoptose von BLymphozyten der Milz Um an den aus der Milz isolierten B-Lymphozyten den Einfluß von Komplement zu untersuchen, wurden die Zellen in Nährmedium (Kapitel 2.2.3.2) bei 37°C und 5% CO2 kultiviert. Nach 5h wurde der schon mit WEHI 279-Zellen durchgeführte Versuch (Kapitel 3.2.3) wiederholt. Je 4*106 isolierte B-Zellen wurden über 10h mit 300 Units IL-4, 2µg AntiCD21/35 Antikörper oder 2µg des unspezifischen Antikörpers (N1G9) und 0,02µg ExtrAvidin inkubiert, um dann über 10h mit 5µg Anti-Fas Antikörper stimuliert zu werden. Danach wurden sie im Durchflußfluoreszenzzytometer bezüglich der Apoptoserate untersucht. 69 Dabei zeigte sich, daß schon unstimulierte Kontrollzellen zu ca. 30% apoptotisch waren. Eine Stimulation des Fas-Rezeptors (CD95) konnte diese Rate weder mit noch ohne vorhergehende IL-4 oder Anti-CD21/35 Behandlung signifikant erhöhen. Die Applikation von IL-4 schien die Apoptoserate leicht, allerdings nicht signifikant zu erniedrigen. (Abb.30) Fas-induzierte Apoptose von aufgereinigten B-Zellen der Milz pos. Kontrolle neg. Kontrolle Prozent TUNEL pos. Zellen 100% unstimulierte Zellen Anti-Fas Ak 80% 60% 40% 20% 0% Versuchsgruppe Abbildung 30: N1G9 und AntiFas Ak Anti-CD21/35 Ak und Anti-Fas Ak IL-4 und Anti-Fas Ak Fas (CD95)-induzierte Apoptose an aufgereinigten B-Zellen der Milz im Durchflußfluoreszenzzytometer in Prozent TUNEL pos. Zellen, (mit Standardabweichung (n=3)) pos. Kontrolle: 20h in PBS Mediumsentzug (WEHI 231-Zellen) neg. Kontrolle: 20h in PBS Mediumsentzug, TUNEL Boehringer Kit ohne spezifisch Koppelndes Enzym verwendet (WEHI 231-Zellen) 3.2.5.1 Der Einfluß von Komplement auf die Fas (CD95)-induzierte Apoptose von vorstimulierten B-Lymphozyten der Milz Um eine gesteigerte Sensitivität der Zellen für Fas zu erreichen wurden in einem neuen Versuchsansatz nach der Aufreinigung je 2*106 Zellen 48h lang mit 10µg Anti-CD40 Antikörper, 10µg Anti-CD40 Antikörper zusammen mit 10µg Anti-CD8α Antikörper oder 10µg Anti-CD40 Antikörper zusammen mit isolierten T-Zellen der Milz bei 37°C im Brutschrank inkubiert. Danach wurden die Zellen gewaschen, die entsprechenden Mengen IL-4 (300Units bzw. 1200Units) oder CD21/35 (2µg) dazugegeben, erneut 1h inkubiert, und 0,02µg ExtrAvidin hinzugefügt. Nach weiteren 9h im Brutschrank wurden die Zellen gewaschen, in neuem Nährmedium gelöst und mit 5µg Anti-Fas Antikörper versetzt, woraufhin sie wiederum 10h bei 37°C im Brutschrank inkubierten. Auch hier wurde die Rate apoptotischer Zellen nach Behandlung und diversen Kontrollen mit Hilfe des TUNEL-Testes im Durchflußfluoreszenzzytometer bestimmt. (Abb.31, S.71) 70 Abbildung 31: Übersicht über den Versuchsaufbau zur Untersuchung des Einflusses von frühen Komplementfaktoren auf die Fas-induzierte Apoptose aufgereinigter Splenozyten Dabei zeigte sich, daß alle Zellen, die keine CD40-Stimulation erhalten hatten nach 3 Tagen im Nährmedium zu ca. 90% abgestorben waren. (Abb.32, S.72, Gruppe0) Wurden die Zellen mit Anti-CD40 Antikörper stimuliert, so veränderten sie Größe und Granularität (Abb.27, S.68) und nur ca. 40% wurden TUNEL pos. (Abb.32, S.72, Gruppe1) Die Gabe von Anti-CD8α Antikörper oder isolierten T-Lymphozyten zum Nährmedium zusätzlich zu Anti-CD40 Antikörper änderte nichts am Aussehen oder der Überlebensrate der Zellen. Nach 3 Tagen waren in diesen Versuchsgruppen ebenfalls etwa 40% der Zellen TUNEL pos.. Die Zellen, die zusätzlich zu der Vorbehandlung mittels des Anti-CD40 Antikörper über den Fas-Rezeptor (CD95) stimuliert worden waren, zeigten zu 95% Zeichen der Apoptose. (Abb.32, S.72, Gruppe2) Auch in diesem Versuchsaufbau änderte die Zugabe von AntiCD8α Antikörper oder isolierten T-Lymphozyten zum Nährmedium die Apoptoserate nicht. In diesem Modell der durch Anti-CD40, Anti-CD40 und Anti-CD8α oder Anti-CD40 und T-Zellen vorstimulierten B-Lymphozyten veränderte die Behandlung der Zellen mit IL-4 (Abb.32, S.72, Gruppen 4, 7 und 9) oder Anti-CD21/35 Antikörper (Abb.32, S.72, Gruppen 3, 6 und 8) die Rate der Fas-induzierten Apoptose nicht signifikant. Ein Trend zu weniger TUNEL pos. Zellen ließ sich nur bei hoher IL-4 (1200 Units) Dosierung feststellen. (Abb.32, S.72, Gruppe5) 71 Prozent TUNEL pos. B-Zellen Fas-induzierte Apoptose von vorstimulierten B-Zellen der Milz 100% 90% 80% 70% 60% 50% 40% 30% 20% 10% 0% Versuchsgruppe pos. Kontrolle neg. Kontrolle Gruppe 0: keine Stimulation Gruppe 1: nur Anti-CD40 Ak Gruppe 2: Anti-CD40 Ak und Anti-Fas Ak Gruppe 3: Anti-CD40 Ak, Anti-CD21/35-Ak und Anti-Fas Ak Gruppe 4: Anti-CD40 Ak, IL-4 (300U) und Anti-Fas Ak Gruppe 5: Anti-CD40 Ak, IL-4 (1200U) und Anti-Fas Ak Gruppe 6: Anti-CD40+Anti-CD8 Ak, Anti-CD21/35 Ak und Anti-Fas Ak Gruppe 7: Anti-CD40+Anti-CD8 Ak, IL-4 (300U) und Anti-Fas Ak Gruppe 8: Anti-CD40 Ak+T-Zellen Anti-CD21/35 Ak und Anti-Fas Ak Gruppe 9: Anti-CD40 Ak+T-Zellen, IL-4 (300U) und Anti-Fas Ak Abbildung 32: Einfluß der CD40-Vorstimulation und früher Komplementfaktoren auf die Fas (CD95)-induzierte Apoptose von aufgereinigten Splenozyten Prozent TUNEL pos. Zellen im Durchflußfluoreszenzzytometer mit Standardabweichung (n=3) pos. Kontrolle: 20h in PBS Mediumsentzug, (WEHI 231) neg. Kontrolle : 20h in PBS Mediumsentzug, TUNEL-Boehringer-Kit ohne spezifisch koppelndes Enzym verwendet (WEHI 231) 72 4 Diskussion In der vorliegenden Arbeit sollte die Bedeutung früher Komplementkomponenten für die Apoptose von B-Zellen im Rahmen der peripheren Toleranzentwicklung im Keimzentrum untersucht werden. Ausgangspunkt war die Erkenntnis, daß die Autoimmunerkrankung Systemischer Lupus Erythematodes, bei der autoreaktive B-Lymphozyten Antikörper gegen körpereigene Antigene produzieren, mit Defizienz der frühen Komplementfaktoren assoziiert ist. Wie es bei Komplementmangel zur Entstehung der Autoantikörper kommt, ist bis heute nicht abschließend geklärt, wenngleich verschiedene Erklärungsansätze postuliert worden sind. Eine dieser Erklärungen basiert auf der gestörten Elimination apoptotischer Zellen und Immunkomplexen bei Komplementmangel35,125,131. Eine andere Theorie geht von der Erkenntnis aus, daß die Entwicklung und Ausreifung der B-Zellen, die die für die Entwicklung des SLE pathogenetisch wichtigen Antikörper produzieren, über verschiedene Komplementkomponenten und -rezeptoren reguliert wird46,58,63. Dieser Theorie zufolge würde ein Komplementmangel die Krankheit über eine gestörte periphere Toleranzentwicklung der B-Zellen initiieren47,58,121,122,132. Ein wichtiger Mechanismus zur Toleranzinduktion von B-Zellen ist neben der Anergie78 die Apoptose133, der „induzierte Selbstmord“ von Zellen. Ein defekter Apoptosemechanismus hat eine mangelhafte Toleranzentwicklung zur Folge76,88,124,134. Im Rahmen dieser Arbeit wurde untersucht, ob die frühen Komplementkomponenten, die mit der Entstehung eins SLE assoziiert sind, einen Einfluß auf die Apoptose von BLymphozyten haben. Dazu wurden verschieden Experimente durchgeführt, die zeigen sollten, ob der Komplementmangel von C4-/-Mäusen, welche spontan Zeichen der Autoimmunerkrankung SLE entwickeln, einen gestörten Apoptosemechanismus zur Folge hat, und ob die Fas-induzierte Apoptose von B-Zellinien und isolierten B-Zellen der Milz durch Stimulation des Komplementrezeptors beeinflußbar ist. 73 4.1 Antigeninduzierte Apoptose: Versuche in vivo Versuche am lebenden Organismus zeichnen sich dadurch aus, daß Zusammenhänge in einem komplexen System untersucht werden. Es ist nicht leicht, ein relativ kurzes Ereignis wie die Apoptose von B-Zellen im Keimzentrum auf Einflußgrößen hin zu untersuchen, da apoptotische Zellen innerhalb des Keimzentrums nur selten nachzuweisen sind92. Sie werden in der Regel von Makrophagen schnell phagozytiert. Eine Möglichkeit, die Rate apoptotischer Zellen in den Keimzentren der Milz zu erhöhen, und damit sie für eine Untersuchung faßbar zu machen, ist die Antigeninduzierte Apoptose. Die Injektion einer großen Dosis löslichen Antigens in die etablierte Immunantwort eines Versuchstieres hinein läßt viele, während der Immunantwort gebildete antigenspezifische B-Zellen absterben92,93,94. Aufgrund der großen Zahl an apoptotischen Zellen wird dieser Versuchsaufbau auch als „Suicide-Versuch“ bezeichnet. 4.1.1 Die Humorale Immunantwort gegen Np 4.1.1.1 Die Humorale Immunantwort von Wildtypmäusen gegen Np Um die Antigeninduzierte Apoptose untersuchen zu können, wurde zunächst eine Immunantwort gegen ein Antigen, Np, induziert. Da Np ein Hapten ist, also isoliert keine Immunantwort auslöst, wurde es an ein Trägerprotein, CGG, gebunden injiziert. Dabei konnte bestätigt werden, daß die Injektion von 50µg Np-CGG eine Np-spezifische Immunantwort auslöst7,12,135,136. Am Tag 8 nach Injektion des Antigens fanden sich im Serum Np-spezifische Antikörper (Abb.10c, S.49) und PNA pos. Keimzentren in der weißen Pulpa der Milz. (Abb.7, S.45, Gruppe B) Die Np-spezifische Immunantwort von C57BL/6 Mäusen, der Stamm, der in dieser Arbeit sowohl als Wildtypkontrolle, als auch als genetisch veränderte Variante (C4-/-) verwendet wurde, besteht zum größten Teil aus Antikörpern der Klassen IgM, IgG1 und zum Teil auch IgG2b7,135. Antikörper dieser Klassen konnten auch in den Versuchen, die dieser Arbeit zugrunde liegen gefunden werden. Die Antikörpertiter stiegen erwartungsgemäß einige Tage nach der Immunisierung der Mäuse an und erreichten nach ein bis zwei Wochen (je nach Subklasse) ein Plateau, das sich über mehrere Wochen hielt. (Abb.10a, S.49 und 11a, S.51, Gruppe B) Aufgrund der nur halbquantitativen Meßmethoden (Vergleich der Proben mittels ELISA mit einem Standardserum, dessen exakter Gehalt an 74 Antikörpern nicht bekannt ist) konnte in dieser Arbeit kein Vergleich zwischen der Höhe der Serumtiter der verschiedenen Subklassen gezogen werden. Die Immunantwort der Antikörper der Klasse M (Anstieg der Serumtiter nach einigen Tagen bis zum Erreiche eines Plateau-Wertes nach etwa einer Woche) (Abb.10a, S.49, Gruppe B) warf zunächst Fragen auf. Anstatt wie beschrieben12 ca. 8-10 Tage nach der Injektion des Antigens, zum Zeitpunkt des Klassenwechsels der Immunantwort, wieder abzufallen blieb der IgM-Spiegel von Wildtyp- und C4-/-Mäusen auf erhöhtem Niveau. Dies läßt sich jedoch durch den Umstand erklären, daß das Antigen in einem Adjuvans, Alum, präzipitiert injiziert wurde. Dieses wirkt als Entzündungsreiz und Depot im Bauchraum, von dem aus Np über längere Zeit in den Kreislauf penetrieren, und somit die IgM-Bildung in Gang halten könnte. Der zeitliche Verlauf des IgG1-Spiegels verhielt sich dem des IgM-Spiegels ähnlich. Er stieg einige Tage nach Injektion des Antigens an, um dann, wie in dieser Subklasse zu erwarten, über mehrere Wochen konstant zu bleiben7,136. (Abb.11a, S.51, Gruppe B) In der IgG2b-Subklasse stiegen Konzentrationen Np-spezifischen Antikörper bis zum Tag 16 deutlich an. Eine Ursache für das frühe Absinken des IgG2b-Titers ab Tag 16 der Immunantwort (Abb.12a, S.52, Gruppe B) konnte nicht gefunden werden. Die Bedeutung dieser Immunglobulinsubklasse für die Immunantwort gegen Np wird allerdings kontrovers beurteilt7,135. In der Literatur ist keine Bildung von Immunglobulinen der Klasse G3 (IgG3) in der Immunantwort gegen Np beschrieben7,135. Dennoch wurden in dieser Arbeit Npspezifische IgG3-Antikörper im Serum der Mäuse bestimmt. Dabei ist zu beachten, daß für die Bestimmung dieser Antikörpersubklasse nur noch Seren weniger Mäuse (n=2) zur Verfügung standen, (Abb.13a, S.54, Gruppe B) und dementsprechend der Verlauf der unbeeinflußten IgG3-Immunantwort der Wildtypmäuse gegen Np nicht sicher aus den Daten zu bestimmen war. Es scheint aber, obwohl in der Literatur nicht erwähnt135, einen Anstieg der IgG3-Antikörper nach zwei Wochen zu geben, der sehr schnell wieder abfällt. Aufgrund der geringen Relevanz der Ergebnisse dieses Teilversuches für die Fragestellung wurde auf die Verwendung weiterer Tiere zur Wiederholung verzichtet. Es wurden keine Np-spezifischen IgG2a-Antikörper im Serum der Mäuse gemessen. Seit kurzem ist bekannt, daß verschiedene Mausstämme, darunter auch die hier verwendeten C57BL/6-Mäuse, nicht über die Subklasse IgG2a verfügen, sondern über eine andere, IgG2c130. Die hier verwendeten Antikörper sind gegen IgG2a gerichtet, und erkennen 75 folglich die ev. gebildeten IgG2c-Immunglobuline nicht. Da diese Subklasse in der Immunantwort gegen proteingebundene Haptene nicht bedeutend ist7,135,136, ist sie doch vor allem in der Antwort gegen virale Antigene von Bedeutung7,28,137, wurde auf die Suche nach einem IgG2c-Antikörper verzichtet. 4.1.1.2 Der Einfluß von C4 auf die humorale Immunantwort gegen Np Die humorale Immunantwort der C4-/-Mäuse war in den IgG-Subklassen gegenüber den Wildtypmäusen signifikant verringert, Antikörper der IgM-Subklasse wurde dagegen in ähnlichem Maße produziert. (Abb.10c, S.49 und 11c, S.51, Gruppen B und F) Dabei variierte die Immunantwort der einzelnen C4-/-Mäuse stark untereinander. Diese reduzierte humorale Immunantwort in C4-defizienten Tieren ist, wie schon in der Einleitung beschrieben, bekannt. Verschiedene Arbeiten beschreiben eine deutliche Reduktion derjenigen Antikörperklassen, die nach dem Klassenwechsel einer B-Zelle gebildet werden, wie IgG2a, IgG2b und IgG310,39,53,113,138, sowie die Reduktion der Zahl und Größe von Keimzentren in Milzen von C4-/-Mäusen10,39. Unterschiedlich wird dagegen die IgM- und IgG1-Bildung während der Immunantwort gegen T-Zell-abhängige Antigene von C4-/-Mäusen beurteilt. So ist die antigenspezifische IgM-Produktion während der Immunantwort gegen einen Bakteriophagen bei C4-/-Mäusen signifikant geringer als bei der Wildtypvergleichsgruppe39, während der Immunantwort gegen das Hapten Np, wie auch in dieser Arbeit jedoch gleich41. Dieser Unterschied in der Bedeutung von C4 für die IgM-Produktion könnte durch die verschiedenen Versuchsmodelle begründet sein. Die oligoklonale Immunantwort gegen ein Hapten (wie das hier verwendete Np) unterscheidet sich deutlich von der polyklonalen Antwort gegen einen Virus mit vielen verschiedenen antigenen Epitopen7. Zudem ist bekannt, daß die Defizienz des Komplementrezeptors 2 (CD21) bei größeren Antigendosen54,139 oder starker Affinität der B-Zellen zu dem Antigen10,139 eine geringere Rolle spielt. Die in der jeweiligen Arbeit verwendete Dosis wäre somit ein weiterer Faktor, der die Immunantwort beeinflussen könnte. Zusammenfassend läßt sich sagen, daß in dieser Arbeit die Bedeutung von C4 für die Bildung von IgG-Antikörpern während der humorale Immunantwort gegen eine Proteinantigen bestätigt werden konnte. 76 4.1.1.3 Apoptose im Rahmen der normalen Immunantwort gegen Np Im Laufe einer normal ablaufenden Immunantwort sind apoptotische Zellen innerhalb des Keimzentrums nur selten nachzuweisen92. Sie werden in der Regel von Makrophagen schnell phagozytiert. Auch in dem in dieser Arbeit gewählten Versuchsaufbau konnte dies bestätigt werden: unbehandelte Wildtypmäuse und Wildtypmäuse, die eine normale Immunantwort gegen Np etabliert hatten, zeigten nur eine geringe Anzahl apoptotischer Zellen in der Milz. (Abb.8, S.46, Gruppen B und D) Diese könnten B-Zellen des Keimzentrums sein, die bei der physiologischen Selektion durch mangelnde Kostimulation absterben8. Auch in C4-/-Mäusen konnten apoptotische Zellen nachgewiesen werden, woraus folgt, daß ohne den Komplementfaktor 4 Apoptose im Keimzentrum möglich ist. (Abb.8, S.46, Gruppe F) Interessanterweise war die Anzahl der apoptotischen Zellen in unbehandelten C4-/-Mäusen oder C4-/-Mäusen, die eine weitgehend intakte Immunantwort gegen Np etabliert hatten, im Vergleich Wildtypmäusen nicht signifikant erhöht, (Abb.8, S.46, Gruppen B und F) ein möglicher Hinweis auf einen intakten Abräummechanismus bei Komplementdefizienz. Solange apoptotische Zellen nicht gehäuft in der Milz C4-/-Mäuse anfallen, könnte deren Clearence dort ungestört sein. Fallen apoptotische Körperchen dagegen gehäuft an, so scheint in anderen Organen die Abräumfunktion apoptotischer Zellen Komplement zu benötigen125,140. So wurden apoptotische Zellen, die in den Peritonealraum C4-/-Mäuse injiziert wurden, dort langsamer beseitigt als im Peritonealraum der Wt-Vergleichsgruppe32. Geht man davon aus, daß die Clearence apoptotische Zellen auch in der Milz Komplement benötigt, so könnte die nicht erhöhte Anzahl apoptotischer Zellen in C4-/-Mäusen gegenüber Wildtypmäusen auch durch das verminderte Anfallen apoptotischer Zellen zu erklären sein. Es würden somit weniger Zellen apoptotisch, diese wären aber, da sie aber schlechter phagozytiert würden, besser nachweisbar. Falls diese Hypothese korrekt ist, sollten in den Experimenten dieser Arbeit weitere Anzeichen für eine mangelhaft ablaufende Apoptose bei C4-defizienten Mäusen gefunden werden. 4.1.2 Hochdosis-Toleranz Eine sehr hohe Dosis an Antigen löst in der Regel keine Immunantwort aus141. Dieses Phänomen wurde früher als „High-zone-tolerance“ (Hochdosis-Toleranz) bezeichnet und konnte auch in dieser Arbeit gezeigt werden: die alleinige Injektion von 4mg des Haptens 77 Np gekoppelt an ein Trägerprotein löste, im Gegensatz zu der wesentlich kleineren Dosis von 50µg sowohl bei Wildtyp- als auch bei C4-/-Mäusen keine Np-spezifische Immunantwort aus. (Abb.10a und b, S.49, und 11a und b, S.51, Gruppen C und G) In den Milzen der Mäuse, die nur diese hohe Dosis des Antigens (4mg Np-BSA i.p.) injiziert bekommen hatten, zeigten sich 8h nach der Injektion zahlreiche apoptotische Zellen wahllos über rote und weiße Pulpa verteilt. (Abb.7, S.45, Gruppen C und G) Da die Mäuse vorher nicht mit dem Antigen in Berührung gekommen waren, ist es unwahrscheinlich, daß all diese sterbenden Zellen Np-spezifische Lymphozyten sind. Es scheint sich somit um ein unspezifisches Phänomen zu handeln. Um es aber genau erklären zu können, müßten weitere Versuche durchgeführt und der apoptotische Zelltyp näher bestimmt werden. Bei den C4-/-Mäusen fanden sich vergleichsweise mehr apoptotische Zellen pro Gesichtsfeld als bei der Wildtypvergleichsgruppe. (Abb.8, S.46, Gruppen C und G) Dies könnte wiederum auf einen Abräumdefekt apoptotischer Zellen bei Komplementmangel hinweisen. Werden die Mäuse, die nur eine hohe Dosis Np-BSA (4mg) i.p. injiziert bekommen hatten, 6 Monate später (am Tag 180) mit einer kleinen Dosis Np-BSA (100µg i.p.) ohne weiteren Adjuvantien behandelt, so bilden sie nur wenige IgM-Antikörper und keine IgGAntikörper. (Abb.14a und b, S.57 und 15a und b, S.58, Gruppen C und G) Dies ist das typische Bild einer ohne Adjuvantien induzierten primären Immunantwort gegen Np. Im Gegensatz dazu würden bei einer sekundären Immunantwort hohe Spiegel Np-spezifischer Antikörper der IgG-Subklassen nachweisbar sein. (Kapitel 4.1.4.1) Daraus kann geschlossen werden, daß die Injektion von 4mg Np-BSA nicht nur keine direkte Antikörperproduktion auslöst, sondern auch keine Bildung von B-Gedächtniszellen induziert. 4.1.3 Die Antigeninduzierte Apoptose Eine der Vorraussetzungen für die Antigeninduzierte Apoptose ist die Erkenntnis, daß sich die Immunantwort gegen ein bestimmtes Antigen durch eine hohe Dosis der löslichen Form desselben unterbinden, oder, wenn bereits etabliert, unterbrechen läßt. Dabei spielt es offenbar keine Rolle, ob die hohe Dosis des Antigens vor142 oder nach der Etablierung einer Immunantwort injiziert wird143-146. Später konnte gezeigt werden, daß sich bei der Injektion einer hohen Dosis des Antigens in eine etablierte Immunantwort hinein 78 (apoptoseinduzierende Injektion, AI, (Abb.33)) viele apoptotischen Zellen lokalisiert in Clustern in den Keimzentren finden92-94. Abbildung 33: Schematischer Versuchsaufbau zur Untersuchung der Antigeninduzierten Apoptose Im Gegensatz zu der im vorangehenden Abschnitt diskutierten, wahrscheinlich unspezifischen Apoptose nach alleiniger Injektion einer hohe Dosis des Antigens, werden in diesem Fall spezifisch B-Zellen des Keimzentrums apoptotisch92-94. Eine extrem hohe Konzentration an löslichem Antigen in einem Keimzentrum löst in einer für dieses Antigen spezifischen B-Zelle Apoptose aus (Antigeninduzierte Apoptose)92-94. Dies könnte entweder durch den Entzug kostimulatorischer Signale der Follikulären Dendritischen Zellen (FDC), durch eine Abtötung mittels zytotoxischer T-Zellen oder durch Überschreitung eines Schwellenwertes der B-Zell-Stimulation geschehen, und wird kontrovers diskutiert. So vermutet M. Karvelas eine potentielle Rolle von T-Zellen in der Induktion dieser Form der Apoptose147. G. Nossal argumentiert dagegen mit ähnlichen Ergebnissen für einen direkten Effekt auf die B-Zellen, und gegen die Mitwirkung von TZellen146. Sicher scheint jedoch zu sein, daß diese Form der Apoptose unabhängig von dem Fas/Fas-L System induziert wird92-94, und auch nicht durch den Verlust der Stimulierung via CD40/CD40L begründet ist92. S. Han konnte zeigen, daß die wiederholte oder verlängerte Exposition der Keimzentren mit hohen Dosen des löslichen Antigens den strukturellen Aufbau der Keimzentren vollkommen auflöste92. Eine wahrscheinliche Erklärung hierfür wäre die Besetzung der BZellrezeptoren mit löslichem Antigen, so daß die B-Lymphozyten nicht mehr in der Lage sind das auf den Follikulären Dendritischen Zellen in Form von Antigen-AntikörperKomplement-Komplexen gebunden Antigen zu erkennen. Dadurch könnte den B-Zellen ein zum Überleben notwendiger Faktor verloren gehen, so daß sie absterben und von Makrophagen aufgenommen würden148. Diese verschiedenen Ergebnisse zeigen, daß der pathophysiologische Mechanismus der Antigeninduzierten Apoptose und die Einflüsse auf diese noch immer nicht geklärt sind. 79 Um die Abhängigkeit der Antigeninduzierte Apoptose von Komplement C4 zu untersuchen, wurde auch in dieser Arbeit in die etablierte Immunantwort gegen Np hinein eine hohe Dosis Np injiziert (Apoptoseinduzierende Injektion). (Abb.6, S.43 und Tab.8, S.44) Dann wurde die Apoptose der B-Zellen in Wildtyp- und C4-/-Mäusen zum einen direkt mittels Immunhistochemie, zum anderen indirekt über den Serumspiegel der Npspezifischen Antikörper bestimmt. Der Einfluß von C4 auf die Antigeninduzierte Apoptose wird im Kapitel 4.1.3.2 diskutiert. 4.1.3.1 Die Antigeninduzierte Apoptose bei Wildtypmäusen Bei Wildtypmäusen fiel der Spiegel Np-spezifischer Antikörper nach der Injektion von zusätzlichen 4mg Np am Tag 9 nach Etablierung einer Np-spezifischen Immunantwort innerhalb von Stunden ab. (Abb.10a, S.49 und 11a, S.51, Gruppe A) Zu diesem Zeitpunkt ließen sich immunhistochemisch eine Vielzahl apoptotischer Zellen in den Keimzentren der Milz nachweisen. (Abb.7, S.45, Gruppe A) Eine Woche nach der zweiten, hohen Dosis des Antigens beginnt der Antikörpertiter dann wieder anzusteigen, erreicht jedoch das Niveau einer ungestörten Immunantwort nicht mehr. (Abb.10a, S.49 und 11a, S.51, Gruppe A) Daraus läßt sich schließen, das zwar einige, aber nicht alle Antikörperproduzieren Zellen absterben, oder aber noch an Alum gebundenes Antigen vorhanden ist, welches erneut eine Antikörperproduktion induziert. Das Versuchstier ist in jedem Fall nicht vollkommen tolerant gegen das verwendete Antigen. Der steile Abfall der Antikörper direkt nach der Injektion der hohen Dosis an Antigen ist wahrscheinlich auf die Bindung der Antikörper an das zirkulierende Antigen zurückzuführen. Die Antikörper würden so als Teil der Immunkomplexe aus dem Kreislauf entfernt werden und mittels ELISA nicht mehr meßbar sein. Damit konnte in dieser Arbeit erstmals eine Antikörperproduktion nach dem Abbruch der Immunantwort gegen Np durch eine apoptoseinduzierende Injektion (AI) nachgewiesen werden. Zuvor hatten jedoch schon andere Arbeiten Hinweise auf einen inkompletten Abbruch der Immunreaktion gegeben. So beschreibt B.Pulendran, daß die Injektion von einer hohen Dosis löslichem Np-HSA in eine etablierte Immunantwort hinein zwar die Anzahl der Antikörperproduzierenden Zellen des Keimzentrums sowie die Zahl der Keimzentren stark reduziert, die Zahl der Antikörperproduzierenden Zellen in der weißen Pulpa, aber erhöht148. Diese Zellen der 80 sog. extrafollikulären Foci produzieren vor allem Antikörper mit niedriger Affinität für das Antigen12. In den Foci finden sich auch nur wenige apoptotische Zellen93. K.Shokat beschreibt zusätzlich eine „zweite Welle“ absterbender Zellen etwa 12h nach Injektion des löslichen Antigens, bei der sich auch apoptotische Zellen in der T-Zell-Zone der weißen Pulpa finden94. Doch auch er geht nicht davon aus daß diese apoptotischen Zellen die Antikörperproduzierenden Zellen der extrafollikulären Foci sind, sondern eher ausgereifte B-Zellen, die das Keimzentrum schon verlassen haben. Somit könnten die Antikörper, die im Rahmen der vorliegenden Arbeit einige Wochen nach der Injektion der hohen Dosis des Antigens im Serum gemessen wurden, von Zellen der extrafollikulären Foci produziert worden sein. Durch die Injektion des Antigens zusammen mit Alum58, welches eine Depotfunktion2 hat, könnte die Antikörperproduktion in den extrafollikulären Foci in Gang gehalten werden, da dort wahrscheinlich noch keine Selektion mittels Apoptose stattfindet. Die so entstehenden Antikörper wären damit größtenteils IgM-Antikörper niedriger Affinität, da die Affinitätsreifung und der Klassenwechsel ja erst im Keimzentrum stattfinden15,148. Entstehen durch das Antigendepot im Bauchraum nach einigen Tagen neue Keimzentren in der Milz, so wäre keinerlei Toleranz induziert worden, die Antigeninduzierte Apoptose wäre demnach in diesem Modell kein Mechanismus der peripheren Toleranzinduktion. Eine andere Theorie als Erklärung für die Tatsache weshalb die Mäuse im Rahmen der Antigeninduzierten Apoptose nicht vollkommen tolerant geworden waren, geht davon aus, daß sich die B-Zellen zwar zum Teil im Keimzentrum ausreifen, dort aber nicht ihre Effektorfunktion ausüben, d.h. Antikörper produzieren8. Da die Apoptose auf das Keimzentrum beschränkt bleibt, (Abb.7, S.45, Gruppe A) ist es möglich, daß durch die hohe Dosis an löslichem Antigen nur „der Nachschub“ antigenproduzierender Zellen vernichtet wird. Die Zellen, die bereits aus dem Keimzentrum ausgewandert sind, könnten dann für die später nachweisbare Antigenproduktion verantwortlich sein. Dies würde auch die Persistenz von Antikörpern der Klasse IgG erklären. Falls diese Theorie zuträfe, wäre dies für die Toleranzentwicklung von B-Zellen von besonderer Bedeutung. Wenn ein Großteil der B-Zellen, die sich zu dem Zeitpunkt der Injektion von löslichem Antigen im Keimzentrum in der Proliferations- oder Selektionsphase befinden, als Folge dieser Injektion absterben94, dann ist es sehr wahrscheinlich, daß dies ein physiologischer Prozeß zur Toleranzerhaltung während der somatischen Hypermutation ist. Eine B-Zelle, die ihren Rezeptor während der 81 Hypermutation im Rahmen einer Immunantwort so verändert, daß er jetzt (in großen Mengen löslich verfügbares) Selbstantigen wie Serumproteine erkennt, würde apoptotisch werden und absterben8,92,94. 4.1.3.2 Der Einfluß von C4 auf die Antigeninduzierte Apoptose In dieser Arbeit sollte der Einfluß von C4 auf die Antigeninduzierte Apoptose untersucht werden. Dabei konnten sowohl in Wildtypmäusen als auch in C4-/-Mäusen nach der Injektion von 4mg Np in eine etablierte Immunantwort hinein viele apoptotische Zellen in Keimzentren der Milz nachgewiesen werden. (Abb.7, S.45, Gruppen A und E) Die Antigeninduzierte Apoptose im Keimzentrum ist somit ohne C4 möglich. Die direkte quantitative Analyse der apoptotischen Zellen im Keimzentrum konnte keinen signifikanten Unterschied zwischen Wildtyp- und C4-/-Mäusen zeigen. Bei den C4-/Mäusen ist zeigte sich jedoch ein Trend zu mehr apoptotische Zellen in den Keimzentren. (Abb.8, S.46, Gruppen A und E) Dieses Ergebnis zeigt, daß durch den Mangel der Komplementkomponente C4 die Apoptose von antigenspezifischen B-Zellen im Keimzentrum offenbar nicht beeinträchtigt ist. Eventuell sind bei Komplementmangel sogar mehr apoptotische Zellen im Keimzentrum zu finden, entweder, weil mehr B-Zellen absterben, oder weil die apoptotischen Zellen durch einen Phagozytosedefekt schlechter abgeräumt werden können. Der obengenannte Trend (mehr apoptotische Zellen bei C4-/-Mäusen) könnte allerdings auch durch ein Artfakt der Methodik verursacht worden sein. So könnte die Auszählung TUNEL pos. Zellen im immunhistochemisch gefärbten Schnitt fehlerbehaftet sein, da jeweils nur eine Hälfte der Milz mit Hilfe dieser Methode analysiert wurde, und aus der jeweils anderen Hälfte eine Zellsuspension zur Analyse im Durchflußfluoreszenzzytometer gewonnen wurde. Doch auch diese zweite Methode stößt bei der quantitativen Auswertung sehr kleiner Teilmengen von Zellen an ihre Grenzen. Durch die relativ geringe Anzahl an apoptotischen Zellen verglichen mit der Gesamtzahl der B-Zellen der Milz erwies sich die Analyse im Durchflußfluoreszenzzytometer als ungeeignet, so daß kein Unterschied zwischen den verschiedenen Versuchsgruppen festgestellt werden konnte. (Abb.9, S.47) Um methodische Fehler auszuschließen wurde der Einfluß von C4 auf die Antigeninduzierte Apoptose mit Hilfe eines weiteren Analyseverfahrens untersucht. Um eine quantitative Aussage über die Antigeninduzierte Apoptose im Keimzentrum zu treffen, lassen sich auch indirekte Methoden wie die Analyse der Antikörperspiegel im 82 Serum mittels ELISA verwenden: je kleiner die Antikörperantwort nach der Injektion einer zweiten, hohen Dosis des Antigens ist, desto mehr spezifische B-Lymphozyten sollten abgestorben sein. Bei der Analyse der Serumtiter der Np-spezifischen Antikörper in C4-/-Mäusen ließ sich folgendes zeigen. Nach der Injektion von 50µg Np-CGG entwickelt sich auch bei C4-/Mäusen eine, wenn auch in den IgG-Subklassen im Vergleich zu Wildtypmäusen signifikant schwächere Np-spezifische Immunantwort. (Kapitel 4.1.1.2) Wie bei den Wildtyp-Kontrollmäusen fällt nach Injektion einer hohen Dosis des Antigens (4mg Np) am Tag 8 der Immunantwort der Antikörperspiegel zunächst steil ab, um nach einer Woche erneut anzusteigen. Der Antikörpertiter erreicht im weiteren Verlauf der Immunantwort nicht mehr das Niveau einer ungestörten Immunantwort. (Abb.10b, S.49, und 11b, S.51, Gruppe E) Im quantitativen Vergleich mit Wildtypmäusen fällt der Wiederanstieg des Npspezifischen IgG-Titers im Serum von C4-/-Mäusen nach dem antigeninduziertem Abfall am Tag 8 signifikant schwächer aus. (Abb.11d, S.51, und 12d, S.52) Wäre die Apoptose durch den Komplementmangel beeinträchtigt, so müßten mehr Zellen überleben und damit der Antikörperspiegel höher sein als bei Wildtypmäusen. Der geringere Wiederanstieg der IgG-Antikörper nach Apoptoseinduktion in C4-defizienten Tieren könnte somit erklärbar sein durch eine effektivere Apoptoseinduktion. Eine weitere Erklärung wäre allerdings auch eine vergleichbare Anzahl absterbender Zellen bei Wildtyp- und C4-/-Mäusen in Kombination mit einer geringeren Neuproduktion von Antikörpern aufgrund des C4Mangels. Der IgM-Spiegel im Serum C4defizeinter Mäuse nahm dagegen nach dem antigeninduzierten Abfall signifikant stärker zu als bei Wildtypmäusen. (Abb.10d, S.49) Der Großteil der IgM-Antikörper und nur ein Teil der IgG-Antikörper wird jedoch in den extrafollikulären Foci, den Orten der ersten Antikörperproduktion produziert, und nicht im Keimzentrum von Zellen die die Affinitätsreifung durchlaufen haben14,15,82. Solche Foci finden sich typischerweise in der T-Zell-Zone der Milz, ein Bereich in dem ein dieser Arbeit übereinstimmend mit der Literatur148 keine apoptotischen Zellen gefunden wurden. (Abb.8, S.46, Gruppen A und E) Die dort produzierten Antikörper sind daher möglicherweise von geringerer Bedeutung für die Beurteilung der Effektivität der Apoptose. Ein erhöhter IgM-Spiegel erlaubt somit keinen Rückschluß auf die Effektivität der Apoptose von B-Zellen im Keimzentrum. 83 In dieser Arbeit konnte somit gezeigt werden, daß Apoptose im Keimzentrum ohne C4 möglich ist, und die Antigeninduzierte Apoptose im Keimzentrum durch C4-Defizienz auch quantitativ nicht beeinträchtigt wird. Es konnten Hinweise auf eine möglicherweise höhere Apoptoserate bei C4-/-Mäusen im Vergleich zu Wildtypmäusen gefunden werden. 4.1.4 Beeinflussung des immunologischen Gedächtnisses durch die Antigeninduzierte Apoptose Neben der Affinitätsreifung ist die Reifung von B-Zellen zu B-Gedächtniszellen eine wichtige Funktion des Keimzentrums. Diese Zellen ermöglichen im Rahmen einer zweiten Immunisierung mit dem gleichen Antigen eine schnellere Produktion von Antikörpern höherer Affinität. Da die B-Gedächtniszellen den Klassenwechsel bereits während der ersten Immunantwort vollzogen haben, wird die zweite Immunantwort von Immunglobulinen der Klasse G (IgG) dominiert149,150. Sollten durch Injektion einer hohen Dosis des Antigens in eine etablierte Immunantwort hinein ein Großteil der im Keimzentrum befindlichen B-Zellen absterben, so wäre die Bildung dieser Gedächtniszellen gestört, und der Ablauf einer zweiten Immunantwort gegen das Antigen verändert. Im Umkehrschluß ist die Untersuchung der BGedächtniszellfunktion in einer sekundären Immunantwort im Suicide-Modell eine Möglichkeit, die Effektivität der Apoptose im Keimzentrum unter verschiedenen Einflußfaktoren, z.B. Komplementmangel, zu untersuchen. (Tab.9, S.55) Vorher unbehandelte Wildtypmäuse bilden nach der Injektion von 100µg Np-BSA i.p. ohne weitere Adjuvantien nur wenige Np-spezifische IgM-Antikörper und keine IgGAntikörper. (Abb.14a, S.57 und 15a, S.58, Gruppe D) Die Dosis ist, wenn sie ohne Alum i.p. injiziert wird, offenbar zu klein um eine volle primäre Immunantwort gegen Np hervorzurufen. Eine Bildung von Antikörpern der Klasse IgG nach der Injektion von 100µg Np-BSA ohne weiteren Adjuvantien ist somit sehr wahrscheinlich auf BGedächtniszellen zurückzuführen, und kann als Kennzeichen einer sekundären Immunantwort gewertet werden. 84 4.1.4.1 Der Einfluß der Antigeninduzierten Apoptose auf das immunologische Gedächtnis von Wildtypmäusen In dieser Arbeit konnte bestätigt werden, daß die sekundäre Immunantwort von Wildtypmäusen gegen Np von Antikörpern der Subklassen IgG1 und IgG2b dominiert wird136. (Abb.15a, S.58, und 16a, S.59, Gruppe B) Diese Antikörper werden in erster Linie von B-Gedächtniszellen produziert136. Vor allen in den ersten Tagen der Sekundärantwort kommt es zusätzlich zur Produktion von Antikörpern der Klasse M. (Abb.14a, S.57, Gruppe B) Dies geschieht wahrscheinlich durch neue Np-spezifische B-Lymphozyten, die zum ersten Mal mit dem Antigen in Kontakt kommen, und nicht durch B-Gedächtniszellen nach einem zweiten Antigenkontakt. Daher kann der Serumspiegel von IgM-Antikörpern der zweiten Immunantwort für die Untersuchung der Gedächtniszellfunktion vernachlässigt werden. In der Tat zeigte sich zwischen der normalen sekundären Immunantwort in der IgM-Antikörperklasse von Wildtypmäusen und der sekundären Immunantwort von Mäusen, deren erste Immunantwort durch die Injektion einer hohen Dosis des Antigens gestört wurde (Apoptoseinduzierende Injektion), kein signifikanter Unterschied. (Abb.14a, S.57, Gruppen A und B) Dagegen beeinflußt die Injektion einer hohen Dosis löslichen Antigens (Apoptoseinduzierende Injektion) während der ersten Immunantwort gegen Np die Produktion von IgG-Antikörpern während einer zweiten Immunreaktion 6 Monate später entscheidend. Im Vergleich zur physiologisch ablaufenden sekundären Immunantwort werden signifikant weniger IgG1- und IgG2b-Antikörper gebildet. (Abb.15a, S.58, und 16a, S.59, Gruppen A und B) In dieser Arbeit konnte somit erstmals gezeigt werden, daß durch die Antigeninduzierte Apoptose die Funktion der B-Gedächtniszellen während einer sekundären Immunantwort empfindlich gestört, aber nicht vollkommen aufgehoben wird. Schon früher gab es in verschiedenen Veröffentlichungen, die den Einfluß des „SuicideVersuches“ auf Bildung von sog. Vorläufern antikörperbildender Zellen (Frühform von BGedächtnis-Zellen151) untersuchten147,152, Hinweise auf eine solche Störung. Dort konnte gezeigt werden, daß nach Injektion einer hohen Dosis löslichen Antigens vor oder nach der Induktion einer Immunantwort gegen die präzipitierte Form des Antigens signifikant weniger solcher Vorläuferzellen gebildet werden152. Transferiert man diese Zellen in Mäuse, die keine eigenen Immunzellen haben, so werden dort weniger B-Gedächtniszellen gebildet147. Ob eine sekundäre Immunantwort noch nach Monaten gestört ist, wurde in diesen Arbeiten allerdings nicht untersucht. Aus diesen und den in dieser Arbeit gezeigten 85 Ergebnissen kann man schließen daß die Bildung der B-Gedächtniszellen durch den „Suicide-Versuch“ empfindlich gestört ist. Die Ergebnisse der Untersuchung der Gedächtniszellfunktion stützen außerdem die Vermutung, daß in diesem Modell durch die Antigeninduzierte Apoptose nur die im Keimzentrum befindlichen, noch nicht ausgereiften B-Zellen absterben. Da in einem Keimzentrum in den ersten Tagen vor allem antikörperproduzierende Zellen (Plasmazellen) gebildet werden, und üblicherweise erst später (nach ca. 14 Tagen) BGedächtniszellen das Keimzentrum verlassen21, sind am Tag 9 nach Beginn der primären Immunantwort, zum Zeitpunkt der Injektion des löslichen Antigens, offenbar noch nicht viele Gedächtniszellen gebildet. Durch das Absterben der im Keimzentrum befindlichen BZellen sistiert die Np-spezifische Antikörperproduktion zwar nicht vollständig, die Gedächtniszellfunktion dagegen ist stark eingeschränkt. 4.1.4.2 Der Einfluß von C4 auf das Immunologische Gedächtnis Die ungestörte sekundäre Immunantwort von C4-/-Mäusen ist der von Wildtypmäusen sehr ähnlich: beide werden von den Immunglobulinklassen IgG1, IgG2b und zum Teil auch IgM dominiert. Dabei werden vor allem die Antikörper der beiden IgG-Subklassen von Memoryzellen produziert. Obwohl in der Literatur bei C4-Defizienz eine Reduktion der sekundären Immunantwort gegen virale Antigene beschrieben wird50,153, konnte in dieser Arbeit gezeigt werden, daß sich im Verlauf der sekundären Immunantwort gegen ein Proteinantigen in der Höhe des Serumtiters der IgG1-Antikörper bei C4-/-Mäusen kein Unterschied zu Wildtypmäusen findet. (Abb.15c, S.58, Gruppen B und F) Die sekundäre Immunantwort gegen ein Proteinantigen in der IgG2b-Subklasse fiel dagegen bei C4-/-Tieren signifikant schwächer aus als die der Wildtypvergleichsgruppe. (Abb.16c, S.59, Gruppen B und F) Diese Ergebnisse scheinen paradox, erklären sich jedoch durch die unterschiedliche Bedeutung der Subklassen in der Immunantwort gegen verschiedene Antigene. Im Rahmen einer Immunantwort gegen ein Proteinantigen ist die IgG1-Produktion ist von Bedeutung136, gegen ein virales Antigen eher andere IgG-Subklassen. C4 scheint somit für die Entwicklung einer sekundären Immunantwort gegen Np nicht absolut notwendig zu sein. Fehlt dagegen der Komplementrezeptor (CD21/35), wie bei Cr-/-Mäusen, so entwickeln die Tiere eine deutlich reduzierte sekundäre Immunantwort50,54. 86 Antikörper der Klasse M (IgM) werden zwar auch im Rahmen einer sekundären Immunantwort gebildet, erlauben aber keinen Rückschluß auf die Funktion des immunologischen Gedächtnisses, da B-Gedächtniszellen vor allem Immunglobuline der Klasse G (IgG) bilden, und Immunglobuline der Klasse M (IgM) im Rahmen einer sekundären Immunantwort wahrscheinlich durch neue Np-spezifische B-Lymphozyten produziert wird. Eine Verringerung dieser Antikörperspiegel durch Komplementmangel konnte nicht gezeigt werden, da zwei der drei C4-/-Mäuse vor Beginn der zweiten Immunisierung, also 6 Monate nach dem letzten Kontakt mit dem Antigen, noch stark erhöhte Anti-Np IgM-Titer im Serum hatten. Die folgende zweite Immunisierung mit dem Antigen zum Auslösen der sekundären Immunantwort steigerte diesen noch deutlich, so daß dieser dann deutlich über dem der entsprechenden Wildtypgruppe lag. (Abb.14b und c, S.57, Gruppe F) Die durchschnittliche Überlebenszeit von antikörperproduzierenden Plasmazellen liegt bei 3-6 Wochen23, und eine Immunantwort wird nach Elimination des Antigens schnell herunterreguliert15,76. 6 Monate nach einer Antigengabe sollten somit nur noch wenige Antikörper im Serum der Mäuse nachweisbar sein. Es ist bekannt, daß es langlebige Plasmazellen gibt, die noch Jahre nach dem Antigenkontakt Antikörper sezernieren6. Weshalb diese jedoch nur in dieser Subgruppe einen vergleichsweise sehr hohen Antikörperspiegel hervorrufen, konnte nicht geklärt werden. Eine Erklärung wäre die Persistenz des Antigens aufgrund eines Abräumdefektes35,58 in diesen Mäusen, wobei nicht erklärt wäre, warum nach so langer Zeit nur IgM-Antikörper, die den Beginn einer Immunantwort dominieren, gebildet werden. 4.1.4.3 Der Einfluß von C4 auf das Immunologische Gedächtnis im „SuicideVersuch“ Vergleicht man die B-Gedächtniszellfunktion von C4-/-Mäusen im „Suicide-Versuch“, d.h. nach Unterbrechung der primären Immunantwort durch eine hohe Dosis lösliches Antigen, mit der einer Wildtypvergleichsgruppe, so konnte gezeigt werden, daß bei C4-/Mäusen diese gleichermaßen (IgG1) oder sogar signifikant stärker (IgG2b) beeinträchtigt ist als die gleich behandelter Wildtypmäuse. (Abb.15b und c, S.58, und 16d, c und d, S.59, Gruppen A und E) Die Apoptose in Keimzentren einer primären Immunantwort beim Mangel an C4 scheint also durchaus effizient zu sein. Ein zweiter Hinweis auf die effektive Apoptose bei C4-/-Mäusen ist die Tatsache, daß bei den Mäusen, bei denen bereits die Primärantwort durch den „Suicide-Versuch“ unterbrochen wurde, im Gegensatz zu den C4-/-Mäusen, die eine Primärantwort 87 entwickeln konnten, 6 Monate später kein erhöhter IgM-Spiegel gefunden wurde. (Abb.14b, S.57, Gruppe E) Zusammenfassend läßt sich sagen, daß weder im direkten Nachweis der Apoptose durch Immunhistochemische Färbungen und Analysen im Durchflußfluoreszenzzytometer, noch mit Hilfe verschiedener indirekter Methoden wie der Messung der produzierten Antikörper und der B-Gedächtniszellfunktion in vivo ein Hinweis auf einen gestörten Apoptosemechanismus bei C4-Defizienz gefunden werden konnte. Zudem konnte gezeigt werden, daß die sekundäre Immunantwort gegen ein Proteinantigen bei Mangel der frühe Komplementkomponente C4 nicht signifikant beeinträchtigt ist. Dennoch scheint C4 eine Rolle in der Toleranzinduktion von B-Zellen zu spielen. In C4defizienten Versuchstieren ließ sich im Rahmen der Antigeninduzierten Apoptose ein Trend zu mehr apoptotischen Zellen im Vergleich zu Wildtyptieren erkennen. 88 4.2 Fas (CD95)-induzierte Apoptose: Versuche in vitro Bei der Toleranzentwicklung spielt neben der Antigeninduzierte Apoptose auch die über den Fas-Rezeptor (CD95) induzierte Apoptose eine wichtige Rolle47,84,124,154,155. Diese Form der Apoptose kann insbesondere durch Fas-Ligand (CD95L), einen Liganden des Fas- Rezeptors (CD95) der auf T-Lymphozyten oder Follikulären Dendritischen Zellen des Keimzentrums exprimiert wird, ausgelöst werden9,86. Die physiologische Bedeutung dieses Rezeptors zeigt sich in Mäusen, die keinen funktionsfähigen Fas-Rezeptor (sog. lpr-Mäuse) exprimieren können, oder die dessen Liganden (sog. gld-Mäuse) nicht bilden können. Sie entwickeln autoreaktive B-Zellen und Zeichen der Autoimmunerkrankung SLE47,89,124. Das Fas/Fas-Ligand Systems scheint somit eine wichtige Rolle in der Aufrechterhaltung der peripheren Toleranz zu spielen. Es gibt Hinweise auf eine Bedeutung dieses Systems speziell in der Aufrechterhaltung der Homöostase der Keimzentrumsreaktion. So konnte gezeigt werden, daß in lpr-Mäusen während der späten Phase der Keimzentrumsreaktion einer Immunantwort autoreaktive BZellen entstehen156, und daß die Auflösung der während dieser Immunantwort gebildeten Keimzentren bei Fas-defizienten Tieren nach Ende der Immunantwort beeinträchtigt ist151. Ob nun die Ursache der Autoimmunität bei Fas-defizienten Tieren in einer gestörten Keimzentrumsreaktion liegt, ist allerdings umstritten76,86. So konnte von anderen Arbeitsgruppen bei Fas-defizienten Mäusen keine Einschränkung der Elimination von BZellen des Keimzentrums mit niedrigaffinen157 oder autoreaktiven154 Rezeptoren beobachtete werden. Eine mögliche Erklärung dieser widersprüchlichen Ergebnisse wäre, daß die Toleranzinduktion im Keimzentrum durch das Fehlen von Fas zwar beeinträchtigt, aber nicht vollkommen aufgehoben wird6. Unabhängig von der Bedeutung des Fas/Fas-Ligand Systems in der Keimzentrumsreaktion ist doch unumstritten, daß die Fas-induzierte Apoptose in der peripheren Toleranzentwicklung eine wichtige Rolle spielt. Aus diesem Grund wurde in dieser Arbeit mittels zweier muriner B-Zellinien und aus der Milz von Wildtypmäusen isolierten B-Lymphozyten der Einfluß früher Komplementkomponenten auf die Fas (CD95)-induzierte Apoptose untersucht. Nach einem Versuchsaufbau von L.Foote158, der die „Rettung“ von B-Zellen vor Fas-induzierter Apoptose mit IL-4 gelang, wurde untersucht, ob auch die Stimulation des Komplementrezeptors (CD21/35) die Zellen vor der Fas-induzierten Apoptose schützen 89 kann. Dies schien möglich zu sein, weil offenbar isolierte B-Zellen aus den Tonsillen, die ohne weiter Stimulation rasch absterben, durch die Stimulation des CR2 (CD21) am Leben erhalten werden können65, und weil Zellen der WEHI 231-Zellinie durch Kreuzvernetzung von CD21 mit dem Antigenrezeptor vor Antigenrezeptor induzierter Apoptose geschützt werden können159. 4.2.1 Der Einfluß von Komplement auf die Fas (CD95)-induzierte Apoptose von Zellen der WEHI 231- und 279-Zellinien In vitro Versuche mit Zellinien haben gegenüber in vivo Versuchen verschiedene Vorteile: die Anzahl der Einflußgrößen ist überschaubar, die Versuche sind aufgrund der großen Menge an verfügbaren Zellen beliebig oft wiederholbar und die Anzahl von Tierversuchen kann reduziert werden. Ein großer Nachteil ist dagegen möglicherweise die eingeschränkte Relevanz der in diesem Modell erbrachten Ergebnisse in Bezug auf den wirklichen Ablauf in vivo. Um beurteilen zu können, in wieweit dieses Modell die zu untersuchende Wirklichkeit abbildet, muß man die Eigenschaften der verwendeten Zellen mit denen der in vivo korrespondierenden Zellen vergleichen, und die Frage stellen, in wieweit die Apoptose in Tumorzellinien, zu denen die WEHI-Zellen gehören, schon per se gestört sein könnte. 4.2.1.1 Phänotypische Eigenschaften der WEHI 231- und 279-Zellen Zunächst wurde versucht, den in der Literatur berichteten Phänotyp der Zellen zu bestätigen. Laut der Produktbeschreibung des CAMR (Centre for applied Microbiology and Research, UK) sind WEHI 231-Zellen eines B-Zell-Lymphoms der Maus mit lymphoblastischer Morphologie, die membranständiges IgM tragen aber kein Immunglobulin sezernieren. Trotz dieser Charakterisierung als B-Lymphozyten der Maus wird nur wenig CD45R (B220, ein wichtiger B-Zell-Marker) auf den Zellen gefunden160. Vielfach wird jedoch bestätigt, daß diese Zellinie membranständiges IgM, ein Reifezeichen von B-Zellen trägt159-161. Über weitere Marker, die einen Hinweis auf den Reifegrad der Zellen geben können, wie membranständiges IgD und den Komplementrezeptor 2 (CD21) existieren unterschiedliche Angaben 159,160,162-164. (Abb.34, S.91) Einen Hinweis auf das Entwicklungsstadium von B-Zellen erbringt ihre Reaktion auf die kurzzeitige Stimulation des B-Zell-Rezeptors53: reife B-Zellen proliferieren daraufhin, 90 unreife sterben ab6,163. WEHI231-Zellen scheinen durch Antigenrezeptorstimulation apoptotisch zu werden159,161,162,165,166, und somit Zellen eines unreifen Stadiums zu sein. Auch über die WEHI 279-Zellinie existieren unterschiedliche Angaben. Ebenfalls als ein morphologisch den Lymphoblasten ähnliches B-Zell-Lymphom vertrieben, scheint es IgM oder IL-6167,168 sezernierende Subtypen zu geben. Wiederum besteht Einigkeit über die Tatsache, daß diese Zellen membranständigem IgM exprimieren169,170, aber keine Immunglobuline anderer Klassen170. Diese unterschiedlichen Angaben über die Eigenschaften der WEHI-Zellinien sind möglicherweise auf das Auftreten unterschiedlicher Subtypen in den verschiedenen Laboren zurückzuführen160,165. Deshalb wurde in dieser Arbeit versucht, die von uns verwendeten Zellinien näher zu charakterisieren, und so ihre Bedeutung als Modell der peripheren Toleranzentwicklung näher einzugrenzen. Abbildung 34: Schematische Übersicht über die Entwicklungsstufen der verwendeten Zellen Es konnte bestätigt werden, daß beide hier verwendeten Zellinien ein Immunglobulin der Klasse M exprimieren. (Abb.17, S.61) Da der zum Nachweis des IgM verwendete Antikörper die schwere Kette µ des Rezeptors erkennt, kann die Differenzierung zwischen unreifen B-Lymphozyten, die ein vollständiges membranständiges IgM exprimieren, und Prä- oder Pro-B-Zellen des Knochenmarkes, die nur die schwere Kette des Rezeptors auf ihrer Oberfläche tragen, so nicht getroffen werden. Da die Zellen der WEHI 231-Zellinie zu über 90% CD19 trugen, (Abb.17, S.61) ein Oberflächenmolekül welches bei murinen BLymphozyten erst von unreifen B-Zellen vollständig exprimiert wird, konnte ausgeschlossen werden, daß die hier verwendeten WEHI 231-Zellen Pro- oder Prä-BZellen sind. 91 Die Unterscheidung zwischen reifen und unreifen B-Zellen der Maus, die physiologischerweise beide in der Peripherie anzutreffen sind, kann mit Hilfe weiterer Rezeptoren getroffen werden. Reife B-Zellen exprimieren zusätzlich membranständiges IgD sowie einen vollständigen Korezeptorkomplex mit dem Komplementrezeptor 2 (CD21). Die Zellen der WEHI 231-Zellinie exprimierten membranständiges IgD nur zu ca. 50%, und den Komplementrezeptor 2/1 (CD21/35) nur zu ca. 40%. (Abb.17, S.61) Dies läßt die Vermutung zu, daß der von uns benutze WEHI 231-Klon aus Zellen einer Zwischenstufe, späten unreifen B-Zellen (transitional71), besteht. (Abb.34, S.91) Transitionalzellen exprimieren viel IgM, wenig IgD und teilweise auch den Komplementrezeptor54. Diese Zellen eignen sich also nur teilweise zur Simulation der peripheren Toleranzentwicklung von reifen B-Zellen im Keimzentrum. Zwar regeln auch reife B-Zellen im Keimzentrum ihre IgD-Expression herunter171, doch in Hinblick auf die ebenfalls schwache CD21/35-Expression und verschiedene Literatur- hinweise161,162,165,166,172 scheint die Annahme, WEHI 231-Zellen entsprächen eher unreifen B-Zellen, richtig. Die Zellen der zweiten Zellinie, WEHI 279, exprimierten den Komplementrezeptor zu ca. 50%, CD19 jedoch nur zu 40% und IgD fast gar nicht (10%). (Abb.17, S.61) Sie scheinen daher Zellen eines noch unreiferen Stadiums zu sein. (Abb.34, S.91) 4.2.1.2 Fas-Expression und Einflüsse auf die Fas-induzierte Apoptose von Zellen der WEHI 231- und 279-Zellinien Reife B-Zellen können, falls sie den Fas (CD95)-Rezeptor tragen, den apoptotischen Prozeß nach Stimulation des Rezeptors beginnen. Obwohl naive B-Zellen wenig CD95 exprimieren, wird dieses in Interaktion mit spezifischen T-Zellen über das CD40/CD40LSystem hochgeregelt173. Dies geschieht in besonderem Maße im Keimzentrum, wo die durch Zellteilung und somatische Hypermutation entstandenen Zentrozyten besonders empfindlich für Apoptoseinduktion sind86. Die in dieser Arbeit verwendeten Zellinien tragen beide CD95 schon ohne Stimulation mit CD40 zu ca.70%. (Abb.17, S.61) Dennoch waren nur die Zellen der unreiferen WEHI 279Zellinie für Fas-induzierte Apoptose sensibel, (Abb.22, S.64) ein Befund, der sich durch die Literatur bestätigen läßt170,174. Auch die Resistenz der anderen Zellinie findet sich in der Literatur wieder: sie wird teils mit der Expression eines inhibitorischen Proteins, cFlipL, im intrazellulären Signalweg des Rezeptors161, teils mit mangelnder Expression des 92 Fas-Rezeptors175 (CD95) erklärt. Da letzteres für die in dieser Arbeit gezeigten Ergebnisse (Fas-Resistenz trotz Fas-Expression) nicht als Erklärung zutreffen kann, scheint die Existenz eines inhibitorischen Proteins76 die Erklärung für die Resistenz von WEHI 231 zu sein. Dieses Protein, c-FlipL, ist auch in vivo in B-Zellen des Keimzentrums aktiv6. Auch andere Veröffentlichungen konnten in verschiedenen murinen Zellinien (u.a. auch WEHI-Zellen) zeigen, daß die Fas-Expression per se nicht mit Fas-Sensibilität gleichzusetzen ist76,176. Auch scheint die Stimulation des CD40-Rezeptors von WEHI 279 zwar die Expression von Fas, doch nicht deren Sensitivität auf Fas-induzierte Apoptose zu erhöhen161, so daß in dieser Arbeit auf einen Stimulationsversuch mit CD40 an WEHIZellen verzichtet wurde. Im weiteren wurde untersucht, ob sich die Fas-induzierte Apoptose der WEHI 279-Zellen durch Zugabe von Anti-CD21/35 oder IL-4 beeinflussen ließ. Dabei konnte gezeigt werden, daß nach Stimulation des CD95 (Fas)-Rezeptors über 10h ca. 60% der Zellen apoptotisch wurden. Weder die vorherige Stimulation des Komplementrezeptors (CD21/35) noch die Inkubation mit dem Zytokin IL-4 konnte dieses Ergebnis signifikant verändern. (Abb.23, S.66) WEHI 279-Zellen lassen sich somit durch die Stimulation von CD21/35 nicht vor Fasinduzierter Apoptose schützen. Für dieses Ergebnis gibt es zwei Erklärungen. Entweder hat CD21/35 keinen Einfluß auf die Fas-induzierte Apoptose von B-Zellen im Keimzentrum, oder das Modell (Zellen der WEHI-Zellinie) ist nicht geeignet diese Frage zu beantworten. Eine andere Arbeit konnte unter Verwendung der WEHI 231-Zellinie zeigen, daß die Kreuzvernetzung des Komplementrezeptors mit dem B-Zell-Rezeptor die Zellen vor BZell-Rezeptor induzierter Apoptose schützt159. Ob dieser Ergebnisse allerdings für die Apoptose im Rahmen der peripheren Toleranzinduktion relevant sind, ist zu bezweifeln, weil die Stimulation des Antigenrezeptors des dort verwendeten Zellklons zur Apoptose führt, was als ein Merkmal unreifer B-Zellen angesehen wird6. Möglicherweise wird durch die Kreuzvernetzung des B-Zell-Rezeptors mit dem Komplementrezeptor in der genannten Arbeit ersterer einfach blockiert, so daß eine Kreuzvernetzung der B-Zell-Rezeptoren untereinander nicht mehr stattfinden kann. In anderen Arbeiten konnte gezeigt werden, daß aufgereinigte Splenozyten, also reife BZellen, durch IL-4 vor dem Fas-Tod geschützt werden86,158, und daß IL-4 auch in vivo FasResistenz und damit Autoimmunität induzieren kann86,177. In den im Rahmen dieser Arbeit durchgeführten Versuchen hatte IL-4 dagegen keinen Einfluß auf die Fas-induzierte 93 Apoptose von WEHI 279-Zellen. Dies könnte ebenfalls daraufhindeuten, daß die hier verwendeten Zellen B-Zellen eines unreifen Stadiums entsprechen, und sie nur begrenzt zur Simulation der peripheren Toleranzentwicklung im Keimzentrum einsetzbar sind. Somit scheint die Frage, ob der Komplementrezeptor auf B-Zellen im Keimzentrum deren Apoptose beeinflußt, in diesem Modell (WEHI 231 und 279) nicht beantwortbar zu sein. 4.2.2 Der Einfluß von Komplement auf die Fas (CD95)-induzierte Apoptose von BLymphozyten der Milz Unter der Verwendung der WEHI 231- und 279-Zellinien konnte kein Einfluß der Stimulation von CD21/35 auf die Fas-induzierte Apoptose von B-Zellen gesehen werden. Um zu entscheiden, ob CD21/35 keinen Einfluß auf die Fas-induzierte Apoptose von BZellen im Keimzentrum hat, oder das Modell (Zellen der WEHI-Zellinie) nicht geeignet ist diese Frage zu beantworten, wurden die oben beschriebenen Versuche zusätzlich mit aus der Milz aufgereinigten B-Zellen durchgeführt. Diese werden als reife B-Lymphozyten beschrieben, sollten zunächst aber ebenfalls näher charakterisiert werden. 4.2.2.1 Charakterisierung der aufgereinigten Splenozyten Die Reinheit der durch die Aufreinigung mittels Dichtegradient und Oberflächenstruktur gewonnenen B-Zellen wurde anhand der B-Zell-Marker CD19 und B220 (CD45R) auf ca. 85% bestimmt. (Abb.26, S.68) Wurde im Durchflußfluoreszenzzytometer nur die der Größe und Granularität von Lymphozyten entsprechenden Zellen (FS/SS) gemessen, waren mehr als 90% der untersuchten Zellen B-Zellen. (Abb.24, S.67) Auch die Tatsache, daß B220 etwas stärker exprimiert wird als CD19, wird als charakteristisch für reife BZellen der Maus angesehen. (Abb.24, S.67) Es konnte gezeigt werden, daß ca. 90% der gewonnenen Zellen weitere Oberflächenmarker reifer naiver B-Zellen wie IgM, IgD und den Komplementrezeptor 2/1 (CD21/35) exprimieren. (Abb.26, S.68) Da die Milzen von unbehandelten Wildtypmäusen verwendet wurden, und sich bei unbehandelten Mäusen in der Regel nur wenige Keimzentren in der weißen Pulpa befinden, ist es sehr wahrscheinlich, daß die durch die Aufreinigung gewonnenen Zellen zum größten Teil reife ruhende B-Zellen (sog. naive B-Zellen) waren. (Abb.34, S.91) Die in den später beschriebenen Versuchen verwendeten und analysierten Zellen waren somit zu 90% reife B-Zellen der Milz. Die restlichen 10% Zellen der gewonnenen Zellen schienen vor allem T-Lymphozyten zu sein (sie trugen entsprechende Oberflächenmarker, CD3 und CD90.2 (Thy-1)). (Abb.26, 94 S.68) Zusätzlich fanden sich einige Granulozyten und Makrophagen, die jedoch für die Versuche von geringer Bedeutung waren. 4.2.2.2 Die Fas-induzierte Apoptose von B-Zellen der Milz Nur ca. 60% der verwendeten B-Zellen exprimierten den Fas-Rezeptor (CD95), können also auf dessen Stimulation reagieren. (Abb.26, S.68) Da bekannt ist, daß naive Lymphozyten nach ihrem Eintritt in das Keimzentrum durch Interaktion der CD40/CD40L-Rezeptoren zur Proliferation und zur weiteren Expression des Fas-Rezeptors (CD95) angeregt werden173, wurden in einem weiteren Versuchsansatz die Zellen über 48h mit Anti-CD40 Antikörper vorstimuliert. Eine solche Vorbehandlung sollte auch die FasSensibilität von reifen B-Zellen der Milz erhöhen25,84,178,179. Als Zeichen der Aktivierung durch CD40 konnte in dieser Arbeit eine veränderte Größe und optische Dichte der Zellen gesehen werden. (Abb.27, S.68) Obwohl die FasExpression durch diese Vorbehandlung nicht hochreguliert wurde, wurden die verwendeten B-Zellen dennoch erst durch die Stimulation des CD40-Rezepors für die Fasinduzierte Apoptose sensibel. (Abb.30, S.70 und Abb.32, S.72) Dies zeigt nochmals, daß die Fas-Expression per se nicht mit Fas-Sensibilität gleichzusetzen ist76. Schon frisch aus der Milz isolierte B-Zellen zeigten zu 30-40% Zeichen der Apoptose, was vermuten läßt, daß sie bereits bei dem Prozeß der Aufreinigung geschädigt wurden. Diese Zellen wurden nicht entfernt, sie waren somit bei jeder Messung als „Hintergrund“ vorhanden. Wurden die Zellen einige Tage in Kultur gehalten um sie mit verschiedenen Antikörpern oder Zytokinen zu stimulieren, so schien die Stimulation des CD40-Rezeptors auch für das Überleben der B-Lymphozyten essentiell zu sein. Nach drei Tagen in Kultur ohne Zugabe von Anti-CD40 Antikörper waren ca. 90% der Zellen apoptotisch. Dieses Ergebnis findet sich auch in der Literatur wieder. So konnte gezeigt werden, daß ruhende B-Zellen in Follikeln3 und aktivierte B-Zellen im Keimzentrum kostimulatorische Signale zum Überleben benötigen76. Auch in vitro ist die Stimulation des CD40-Rezeptors für das Überleben isolierte B-Lymphozyten erforderlich18,65, doch konnte gezeigt werden, daß isolierte B-Zellen der Tonsillen auch unter Zugabe von CD23, einem Liganden des Komplementrezeptors CD21 (oder einigen Antikörpern gegen diesen Rezeptor) überleben65. 95 4.2.2.3 Der Einfluß von IL-4 auf die Fas-induzierte Apoptose von B-Zellen der Milz Obwohl das in diesem Versuchsaufbau verwendete Modell (aufgereinigte Milzzellen) dem zu untersuchenden Mechanismus (Fas-induzierte Apoptose im Keimzentrum) wesentlich näher zu kommen schien, gelang es trotzdem nicht, mit IL-4 in den mit Anti-CD40 Antikörper vorbehandelten B-Zellen Resistenz gegen Fas-induzierte Apoptose zu erzeugen. Nur bei sehr hoher Dosierung des IL-4, der vierfache Menge der Dosis, die in anderen Arbeiten mit Erfolg verwendet wurde, zeigte sich ein Trend zu weniger apoptotischen Zellen. (Abb.32, S.72, Gruppen 4 und 5) Ein Grund für den mangelnden Erfolg, die IL-4 abhängige Apoptoseresistenz158 zu reproduzieren, könnten unterschiedliche Versuchsaufbauten sein. (Abb.31, S.71) Obwohl verschiedene Arten der Aufreinigung gewählt wurden, konnten in beiden Arbeiten die Zellen im Durchflußfluoreszenzzytometer als B-Zellen der Milz charakterisiert werden. Für die Dauer der CD40- oder IL-4-Stimulation wurden in dieser Arbeit die gleichen Zeiten gewählt. Ein Unterschied im Versuchsaufbau ließ sich jedoch bei der Vorstimulation der Zellen finden. Die Arbeitsgruppe um L. Foote stimulierte die Zellen mit einem CD40-CD8αFusions-Protein, welches mit Anti-CD8 quervernetzt wurde 84,158,180 , in dieser Arbeit wurden die B-Zellen dagegen mit Anti-CD40 Antikörper aktiviert. In der Literatur finden sich noch weitere Möglichkeiten B-Zellen über den CD40-Rezeptor zu aktivieren, wie z.B. mittels CD40L tragender L-Zellen181 oder Ovarialzellen des chinesischen Hamsters (CHO) 182 . Die Effektivität der in der in dieser Arbeit verwendeten Aktivierungsmethode konnte zwar gezeigt werden183, (Abb.27, S.68) dennoch besteht die Möglichkeit, daß nur über das Fusionsprotein aktivierte Zellen mit IL-4 vor Fas-induzierter Apoptose zu schützen sind. Dies würde die Bedeutung von IL-4 im Schutz von B-Zellen des Keimzentrums insgesamt in Frage stellen. Um eine veränderte Vorstimulation als Ursache der unterschiedlichen Ergebnisse auszuschließen, wurde der Versuch noch einmal unter veränderten Bedingungen wiederholt. Gleichzeitig mit den Anti-CD40 Antikörpern wurden Anti-CD8 Antikörper oder T-Zellen der Milz (die auch CD40L exprimieren) zum Medium zugegeben. Doch auch in diesem Versuchsaufbau schützte IL-4 nicht vor Fas-induzierter Apoptose. (Abb.32, S.72, Gruppe 7 und 9) Es ist somit möglich, daß die Stimulation mit IL-4 alleine nicht ausreicht, um isolierte B-Zellen der Milz vor Fas-induzierter Apoptose zu retten. Das von L.Foote verwendeten CD40-CD8α-Fusions-Protein könnte weitere 96 Signale liefern, die bei der Aktivierung durch Anti-CD40 Antikörper zusammen mit AntiCD8 Antikörper fehlen. Ein weiterer Unterschied zwischen den beiden Versuchsaufbauten ist die Art Apoptoseinduktion. Die Stimulation des Fas-Rezeptors mit Anti-Fas (CD95) Antikörper induziert offenbar ein wesentlich stärkeres Signal als das, welches durch die Stimulation des Rezeptors mit Fas-Ligand (löslich oder auf Th-1-Effektorzellen) induziert wird180. Somit könnte das in dieser Arbeit durch Anti-Fas Antikörper induzierte Signal zu stark sein, um signifikant durch IL-4 gehemmt zu werden. Diese Vermutung wird durch das Ergebnis, daß der IL-4 abhängige Schutz vor Fas-induzierter Apoptose lediglich bei unphysiologisch hohe Dosen zu erkennen war, (Abb.72, S.32, Gruppe5) untermauert. 4.2.2.4 Der Einfluß von Komplement auf die Fas-induzierte Apoptose von BLymphozyten der Milz In dieser Arbeit sollte der Einfluß von CD21/35 (CR2/1) auf die Fas-induzierte Apoptoserate von B-Lymphozyten untersucht werden. Dazu wurden aufgereinigte BZellen der Milz nach 48-stündiger Vorstimulation mit Anti-CD40 Antikörper über 10h mit Anti-CD21/35-bio sowie Avidin zur Kreuzvernetzung der Komplementrezeptoren inkubiert. (Abb.31, S.71) Danach wurden mittels Anti-Fas Antikörper Apoptose induziert. Es konnte so gezeigt werden, daß die Kreuzvernetzung von CD21/35 (CR2/1) keinen Einfluß auf die Fas-induzierte Apoptoserate von aufgereinigten Splenozyten hat. (Abb.32, S.72, Gruppen 3, 6 und 8) Die Fas (CD95)-induzierte Apoptose könnte somit komplementunabhängig sein. Es existieren Ergebnisse, die den schützenden Effekt der Kreuzvernetzung der Komplementrezeptoren (CD21/35) mit dem Antigenrezeptor zeigen159, doch sind diese in einem Modell unreifer oder transitionaler B-Zellen (der murinen Zellinie WEHI 231) gewonnen. Somit tragen sie damit nur begrenzt zur Diskussion um die Mechanismen der Toleranzentwicklung im Keimzentrum bei. Diese transitionalen B-Zellen exprimieren schon wie reife Zellen den Komplementrezeptor, können aber noch ähnlich wie unreife BZellen auf die Stimulation des Antigenrezeptors mit Apoptose reagieren71. (Abb.34, S.91) Dagegen konnte an reifen, aus humanen Tonsillen isolierten B-Zellen gezeigt werden, daß die Stimulation von CD21/35 mittels eines Liganden (CD23) oder eines Antikörpers vor Apoptose durch Mangel an kostimulatorischen Signalen schützt65. Die Fas-induzierte Apoptose wurde in diesem Rahmen nicht untersucht. 97 Die kurzzeitige Kreuzvernetzung des Antigenrezeptors von reifen B-Zellen in vitro schützt diese vor Fas-induzierter Apoptose84,86,184. Dieser Faktor scheint auch in vivo für das Überleben der Zentrozyten/Zentroblasten (B-Zellen im Keimzentrum) bedeutsam zu sein. Die B-Zellen des Keimzentrums müssen das von FDCs präsentierte Antigen erkennen und prozessieren können, um kostimulatorische Signale zu erhalten. Dennoch ist die Stimulation des Antigenrezeptors ist alleine nicht ausreichend um das Überleben der Zellen zu gewährleisten. So werden mit CD40L vorstimulierte humane, follikuläre BZellen aus Tonsillen, durch Kreuzvernetzung des Antigenrezeptor mit dem Korezeptorkomplex (CD21, CD19, CD81) besser vor Fas-induzierter Apoptose geschützt als durch Kreuzvernetzung des Antigenrezeptors alleine139. Dieser Effekt tritt offenbar vor allem bei niedriger Affinität und kleiner Dosis des Antigens auf139. Dieses Ergebnis könnte vermuten lassen, daß die Rolle des Komplementrezeptors in der Beeinflussung der Fas-induzierten Apoptose eher in seiner Bedeutung als Teil des Korezeptorkomplexes liegt, und damit in der Verstärkung des Signals des B-ZellRezeptors. Zieht man die in dieser Arbeit erbrachten Ergebnisse hinzu, läßt sich die Hypothese aufstellen, daß die Kreuzvernetzung des CR2/1 (CD21/35) ohne Einbeziehung des Antigenrezeptors keinen Einfluß auf die Fas-induzierte Apoptose von reifen, aktivierten B-Zellen hat. Zusammenfassend läßt sich sagen, daß in dieser Arbeit kein Hinweis auf einen Einfluß des Komplementrezeptors CD21/35 auf die Fas-induzierte Apoptose von reifen BLymphozyten gefunden werden konnte. Dennoch ist eine solche Beteiligung aufgrund einiger Besonderheiten des gewählten Versuchaufbaus (Kapitel 4.2.2.3) nicht vollkommen auszuschließen. 98 4.3 Bedeutung der Ergebnisse für die periphere Toleranzinduktion der B-Lymphozyten und für die Entwicklung der Autoimmunerkrankung Systemischer Lupus Erythematodes (SLE) Der systemische Lupus Erythematodes (SLE) ist eine Autoimmunerkrankung, bei der es zur Bildung von hochaffinen Autoantikörpern gegen Selbstantigene kommt. Diese Antikörper werden von autoreaktiven B-Lymphozyten, die den Prozeß der Somatischen Hypermutation im Keimzentrum abgeschlossen haben, produziert47,121-123. Physiologischerweise unterliegt die Entwicklung der B-Zellen einer strengen Regulation, um die Entstehung von solchen autoreaktiven Zellen zu vermeiden. Auch im Keimzentrum stellen verschiedene Mechanismen der Erhaltung der Selbsttoleranz sicher. Wird dieser Prozeß der peripheren Toleranzinduktion gestört, könnten während der Somatischen Hypermutation entstandene autoreaktive B-Zellen überleben und ein Reaktion gegen körpereigene Antigene auslösen. Ein bedeutender Mechanismus zur Erhaltung der Selbsttoleranz im Keimzentrum ist der programmierte Zelltod, der auch als Apoptose bezeichnet wird. Es liegt daher nahe, daß eine Störung der Apoptose der B-Lymphozyten im Keimzentrum zu Autoimmunität führen könnte. Seit langem ist bekannt, daß ein Mangel an frühen Komplementkomponenten wie C1q, C2 oder C4 die Entstehung des SLE begünstigt37,106-112, und daß diese Komplementkomponenten physiologischerweise einen regulierenden Einfluß auf die BZell-Immunität über den Komplementrezeptor CD21 entfalten42-44. Es wird postuliert, daß der Komplementmangel eine Störung der Toleranzinduktion induziert46,58,71. In dieser Arbeit wurde daher die Hypothese untersucht, ob der Mangel an frühen Komplementkomponenten über einen veränderten Apoptosemechanismus die periphere Toleranzentwicklung der B-Zellen stört, und damit die Entstehung eines SLE begünstigt. Verschiedenen Faktoren können bei einer reifen, aktivierten B-Zelle im Keimzentrum Apoptose induzieren, und somit verhindern, daß eine im Rahmen der Somatischen Hypermutation entstandene autoreaktive B-Zelle proliferiert. So kann ein B-Lymphozyt im Keimzentrum mangels kostimulatorischer Signale, durch die Stimulation des Fas (CD95)Rezeptors oder bei einer extrem hohen Antigendosis apoptotisch werden. Die Apoptose aus Mangel stimulatorischer Signale dient der Selektion von höheraffinen BZellen und der Elimination niedrigaffiner B-Zellen im Rahmen der Immunantwort. 99 Sichergestellt wird dies durch ein inhibitorisches Protein welches als c-FLIP bezeichnet wird. Dieses c-FLIP Protein ist intrazellulär mit einem vorgeformten CD95-Komplex gekoppelt. Erfolgt im Keimzentrum keine weitere Stimulation, so dissoziiert dieses Protein von dem Fas-Komplex, und die Apoptose wird eingeleitet6. Kostimulatorische Signale von FDC oder T-Lymphozyten stabilisieren diesen Komplex, so daß die B-Zelle im Keimzentrum überleben kann. Es konnte gezeigt werden, daß die Stimulation des CD40Rezeptors auf B-Zellen durch CD40L, der auf T-Lymphozyten exprimiert wird, aktivierend und lebenserhaltend auf die B-Zellen wirkt. Da die Apoptose aus Mangel stimulatorischer Signale mehr der Elimination niedrigaffiner B-Zellen im Rahmen der Immunantwort gegen Fremdantigen dient, und eher weniger der Erhaltung der Selbsttoleranz, wurde dieser Mechanismus in dieser Arbeit nicht näher untersucht. Allerdings wurde die Stimulation des CD40-Rezeptors zur Aktivierung aufgereinigter BLymphozyten der Milz in einigen in vitro Experimenten verwendet. Die Fas (CD95)-induzierte Apoptose durch Fas-Ligand tragende Zellen stellt einen ubiquitären Mechanismus zur Regulation von Wachstum und Proliferation dar. Im Keimzentrum scheint die durch T-Zellen über den Fas-Rezeptor induzierte Apoptose eine wichtige Rolle bei der Abtötung autoreaktive B-Zellen zu spielen. Die Stimulation durch IL-4 sowie die kurze Stimulation des Antigenrezeptors schützen die B-Zellen vor Fasinduzierter Apoptose, wirken dem Abtöten potentiell autoreaktiver Zellen also entgegen86,177. Im Rahmen dieser Arbeit wurde daher untersucht, ob auch die Stimulation des Komplementrezeptors CR2 (CD21) vor Fas-induzierte Apoptose schützen kann. Dies wurde sowohl an isolierten Maus B-Lymphozyten als auch an WEHI Zellinien analysiert. Die Stimulation von CD21 scheint aber keinen Einfluß auf die Fas-induzierte Apoptose zu haben und somit konnte keine Bedeutung des Komplementrezeptors in diesem Rahmen gezeigt werden. Die Antigeninduzierte Apoptose stellt wohl den wichtigsten Mechanismus zur Regulation autoreaktiver B-Zellen im Keimzentrum dar. Während im Knochenmark jedes Antigen, welches von unreifen B-Zellen erkannt wird, eine negative Regulation ausübt, gelingt dies an reifen B-Zellen innerhalb des Keimzentrums (Zentrozyten) nur bei sehr hohen Antigenkonzentrationen. Da man annimmt, daß Fremdantigene nur selten solch hohe Antigenkonzentrationen in der Milz erreichen, könnte die Antigenkonzentration eine wichtige Basis zur Unterscheidung zwischen Fremd und Selbst und somit zur 100 Toleranzerhaltung sein92-94. Die Antigeninduzierte Apoptose könnte durch den Entzug kostimulatorischer Signale der Follikulären Dendritischen Zellen (FDC), durch zytotoxische T-Zellen oder durch Überschreitung eines Schwellenwertes der B-ZellStimulation vermittelt werden. In dieser Arbeit wurde daher untersucht, ob die antigeninduzierte Apoptose vom Komplementsystem beeinflußt wird. Dabei konnte unter Verwendung von C4-/-Mäusen erstmals in vivo gezeigt werden, daß die Antigeninduzierte Apoptose von B-Zellen während der Keimzentrumsreaktion durch C4-Defizienz nicht beeinträchtigt wird. Es scheinen bei Komplementdefizienz im Vergleich zu Wildtypmäusen sogar mehr antigenspezifische B-Zellen abzusterben. Darüber hinaus war auch die Antikörperproduktion unmittelbar nach der Antigeninduzierten Apoptose vergleichbar, und erreicht die Ausgangswerte unabhängig von Komplement C4. Weiterhin konnte gezeigt werden, daß die Antigeninduzierte Apoptose insbesondere in der B-Gedächtniszellfunktion eine reduzierte Immunglobulinproduktion bewirkt. Auch hier konnte keine Abhängigkeit von Komplement C4 gezeigt werden. In Betrachtung der hier gewonnen Ergebnisse scheint es wahrscheinlich, daß der Zusammenhang zwischen Komplementdefizienz und dem Entstehen der Autoimmunerkrankung SLE nicht in der Störung der Apoptose von autoreaktiven B-Zellen liegt. Statt dessen wird heute der sogenannte „Waste-disposal-defect“ als alternative Erklärung für die Assoziation von SLE und Komplementmangel herangezogen. Apoptotische Körperchen als Quelle für Lupus typische Autoantigene werden weniger gut phagozytiert werden können, wenn C1q103,125 oder C432 fehlt35. Diese nicht phagozytierten apoptotischen Zellen können immunogen wirken99,127,185, und eine Autoimmunreaktion gegen darin enthaltene Antigene auslösen. Die Rolle des Komplementdefektes im Zusammenhang mit Autoimmunität wird heute daher weniger in der Beeinflussung der Apoptose an sich, als vielmehr in dem gestörten Abräumen von apoptotischem Material gesehen. 101 5 Zusammenfassung Der Systemische Lupus Erythematodes (SLE) ist eine Autoimmunerkrankung, bei der reife B-Lymphozyten Antikörper gegen Selbstantigene produzieren. Ausgehend von der Erkenntnis, daß diese Erkrankung mit der Defizienz früher Komplementkomponenten (C1, C4 und C2) assoziiert ist, und daß die Apoptose ein wichtiger Mechanismus zum Schutz vor solchen Autoimmunerkrankungen ist, wurde in dieser Arbeit der Einfluß von Komplement auf die Apoptose von B-Zellen im Rahmen der peripheren Toleranzinduktion untersucht. Dazu wurden Versuche in zwei verschiedenen Modellen durchgeführt. Zum einen wurde die Antigeninduzierte Apoptose bei C4-Defizienz in vivo, zum anderen der Einfluß des Komplementrezeptors (CR2/1, CD21/35) auf die Fas (Apo-1, CD95)induzierte Apoptose in vitro untersucht. Es konnte gezeigt werden, daß die Antigeninduzierte Apoptose von B-Zellen im Keimzentrum ohne C4 möglich ist, und daß sich in der Anzahl der apoptotischen Zellen im Keimzentrum bei C4-/-Mäusen kein signifikanter Unterschied im Vergleich zu Wildtypkontrollmäusen findet. Auch wenn die Antiköperproduktion in C4-/-Mäusen geringer ist als in Wildtypmäusen, bleibt diese jedoch sowohl in C4-defizienten Tieren als auch in deren Wildtyppendant im wesentlichen unbeeinflußt von der Antigeninduzierten Apoptose. Die B-Gedächtniszellfunktion unterscheidet sich bei Wildtyp- und C4-/-Mäusen in den für diese Immunantwort wichtigen Immunglobulinsubklassen nicht, wird allerdings in beiden Mausstämmen durch die Antigeninduzierte Apoptose empfindlich gestört. Auch dieses Phänomen scheint unabhängig von Komplement C4 zu sein, da hier insbesondere in der für diese Immunantwort typischen Antikörpersubklasse IgG1 vergleichbare Immunglobulinkonzentrationen gemessen wurden. Auch im Rahmen der in vitro Experimente konnte in dieser Arbeit kein Hinweis auf einen Einfluß des Komplementrezeptors CD21 auf die Fas-induzierte Apoptose von aufgereinigten B-Zellen der Milz gefunden werden. Weiterhin konnte die Stimulation von CD21/35 bei WEHI 279-Zellen diese nicht vor Fas-induzierter Apoptose schützen In der vorliegenden Arbeit konnte somit gezeigt werden, daß das Komplementsystem die Apoptose von reifen B-Lymphozyten im Keimzentrum nicht beeinflußt, und daß die Assoziation des Mangels früher Komplementkomponenten mit dem SLE folglich in einer anderen Funktion des Komplementsystems zu suchen ist. 102 Literatur 1. Goodnow, C.C. Pathways for self-tolerance and the treatment of autoimmune diseases. Lancet 357, 2115-2121 (2001). 2. Janeway, C.A., Travers, P. Immunologie. Spektrum, Akademischer Verlag 2.Aufl. Kapitel 5 (1997). 3. Cyster, J.G., Hartley, S.B., Goodnow, C.C. Competition for follicular niches excludes self-reactive cells from the recirculating B-cell repertoire. Nature 371, 389-395 (1994). 4. Kelsoe, G. Studies of the humoral immune response. Immunol. Res. 22, 199-210 (2000). 5. Ekland, E.H., Forster, R., Lipp, M., Cyster, J.G. Requirements for follicular exclusion and competitive elimination of autoantigen-binding B cells. J. Immunol. 172, 4700-4708 (2004). 6. Defrance, T., Casamayor-Palleja, M., Krammer, P.H. The life and death of a B cell. Adv. Cancer Res. 86, 195-225 (2002). 7. Toellner, K. M., Luther, S.A., Sze, D.M., Choy, R.K., Taylor, D.R., Mc Lennan, I.C., cha-Orbea, H. T helper 1 (Th1) and Th2 characteristics start to develop during T cell priming and are associated with an immediate ability to induce immunoglobulin class switching. J. Exp. Med. 20, 1193-1204 (1998). 8. Pulendran, B., van Driel, R., Nossal, G.J. Immunological tolerance in germinal centres. Immunol. Today 18, 27-32 (1997). 9. Hollmann, C., Gerdes, J. Follicular dendritic cells and T cells: nurses and executioners in the germinal centre reaction. J. Pathol. 189, 147-149 (1999). 10. Carroll, M.C. The role of complement and complement receptors in induction and regulation of immunity. Annu. Rev. Immunol. 16, 545-568 (1998). 11. Banchereau, J., Bazan, F., Blanchard, D., Briere, F., Galizzi, J.P., van Kooten, C., Liu, Y.J., Rousset, F., Saeland, S. The CD40 antigen and its ligand. Annu. Rev. Immunol. 12, 881-922 (1994). 12. Jacob, J., Kassir, R., Kelsoe, G. In situ studies of the primary immune response to (4-hydroxy-3-nitrophenyl)acetyl. I. The architecture and dynamics of responding cell populations. J. Exp. Med. 173, 1165-1175 (1991). 13. Kelsoe, G. The germinal center reaction. Immunol. Today 16, 324-326 (1995). 14. Jacob, J., Kelsoe, G. In situ studies of the primary immune response to (4-hydroxy3-nitrophenyl)acetyl. II. A common clonal origin for periarteriolar lymphoid sheath-associated foci and germinal centers. J. Exp. Med. 176, 679-687 (1992). 103 15. Liu, Y.J., Zhang, J., Lane, P.J., Chan, E.Y., MacLennan, I.C. Sites of specific B cell activation in primary and secondary responses to T cell-dependent and T cellindependent antigens. Eur. J. Immunol. 21, 2951-2962 (1991). 16. Jacob, J., Przylepa, J., Miller, C., Kelsoe, G. In situ studies of the primary immune response to (4-hydroxy-3-nitrophenyl)acetyl. III. The kinetics of V region mutation and selection in germinal center B cells. J. Exp. Med. 178, 1293-1307 (1993). 17. Kelsoe, G. Life and death in germinal centers (redux). Immunity. 4, 107-111 (1996). 18. Liu, Y.J., Josuah, D.E., Williams, G.T., Smith, C.A., Gordon, J., Mc Lennan I.C., Mechanism of antigen-driven selection in germinal centres. Nature 342, 929-931 (1989). 19. Han, S., Hathcock, K., Zheng, B., Kepler, T.B., Hodes, R., Kelsoe, G. Cellular interaction in germinal centers. Roles of CD40 ligand and B7-2 in established germinal centers. J. Immunol. 155, 556-567 (1995). 20. Liu, Y.J., Arpin, C. Germinal center development. Immunol. Rev. 156, 111-126 (1997). 21. Tarlinton, D.M., Smith, K.G. Dissecting affinity maturation: a model explaining selection of antibody-forming cells and memory B cells in the germinal centre. Immunol. Today 21, 436-441 (2000). 22. Benner, R., Hijmans, W., Haaijman, J.J. The bone marrow: the major source of serum immunoglobulins, but still a neglected site of antibody formation. Clin. Exp. Immunol. 46, 1-8 (1981). 23. Tew, J.G., DiLosa, R.M., Burton, G.F., Kosco, M.H., Kupp, L.I., Masuda, A., Szakal, A.K. Germinal centers and antibody production in bone marrow. Immunol. Rev. 126, 99-112 (1992). 24. Ridderstad, A., Tarlinton, D.M. Kinetics of establishing the memory B cell population as revealed by CD38 expression. J. Immunol. 160, 4688-4695 (1998). 25. Lagresle, C., Mondiere, P., Bella, C., Krammer, P.H., Defrance, T. Concurrent engagement of CD40 and the antigen receptor protects naive and memory human B cells from APO-1/Fas-mediated apoptosis. J. Exp. Med. 183, 1377-1388 (1996). 26. Blier, P.R., Bothwell, A. A limited number of B cell lineages generates the heterogeneity of a secondary immune response. J. Immunol. 139, 3996-4006 (1987). 27. Hennig, C. Charakterisierung heterophiler anti-immunglobuliner Antikörper. Med.Diss. Lübeck (2000). 28. Snapper, C.M., Paul, W.E. Interferon-gamma and B cell stimulatory factor-1 reciprocally regulate Ig isotype production. Science 236, 944-947 (1987). 104 29. Mayer, M.M. Highlights of complement research during the past twenty-five years. Immunochemistry. 7, 485-496 (1970). 30. Mayer, M.M. Complement. Historical perspectives and some current issues. Complement 1, 2-26 (1984). 31. Frank, M.M., Fries, L.F. The role of complement in inflammation and phagocytosis. Immunol. Today 12, 322-326 (1991). 32. Taylor, P.R., Carugati, A., Fadok, V.A., Cook, H.T., Carroll, M.C., Botto, M., Walport, M.J. A hierarchical role for classical pathway complement proteins in the clearance of apoptotic cells in vivo. J. Exp. Med. 192, 359-366 (2000). 33. Mevorach, D., Mascarenhas, J.O., Gershov, D., Elkon, K.B. Complementdependent clearance of apoptotic cells by human macrophages. J. Exp. Med. 188, 2313-2320 (1998). 34. Schifferli, J.A., Steiger, G., Schapira, M. The role of C1, C1-inactivator and C4 in modulating immune precipitation. Clin. Exp. Immunol. 60, 605-612 (1985). 35. Traustadottir, K.H., Sigfusson, A., Steinsson, K., Erlendsson, K. C4A deficiency and elevated level of immune complexes: the mechanism behind increased susceptibility to systemic lupus erythematosus. J. Rheumatol. 29, 2359-2366 (2002). 36. Pepys, M.B. Role of complement in induction of the allergic response. Nat. New Biol. 237, 157-159 (1972). 37. Pickering, M.C., Botto, M., Taylor, P.R., Lachmann, P.J., Walport, M.J. Systemic lupus erythematosus, complement deficiency, and apoptosis. Adv. Immunol. 76, 227-324 (2000). 38. Heyman, B. Regulation of antibody responses via antibodies, complement, and Fc receptors. Annu. Rev. Immunol. 18, 709-737 (2000). 39. Fischer, M.B., Ma, M., Goerg, S., Zhou, X., Xia, J., Finco, O., Han, S., Kelsoe, G., Howard, R.G., Kremmer, E., Rosen, F.S., Carroll, M.C. Regulation of the B cell response to T-dependent antigens by classical pathway complement. J. Immunol. 157, 549-556 (1996). 40. Cutler, A.J., Botto, M., van Essen D., Rivi, R., Davies, K.A., Walport, M.J. T celldependent immune response in C1q-deficient mice: defective interferon gamma production by antigen-specific T cells. J. Exp. Med. 187, 1789-1797 (1998). 41. Zachrau, B. Modifizierte Antigenlokalisation bei Komplement C4-Mangel im Mausmodell und ihre Einordnung in die Pathogenese des Systemischen Lupus erythematodes. Med.Diss. Lübeck (2004). 42. Bianco, C., Patrick, R., Nussenzweig, V. A population of lymphocytes bearing a membrane receptor for antigen-antibody-complement complexes. I. Separation and characterization. J. Exp. Med. 132, 702-720 (1970). 105 43. Chen, Z., Koralov, S.B., Kelsoe, G. Regulation of humoral immune responses by CD21/CD35. Immunol. Rev. 176, 194-204 (2000). 44. Ahearn, J.M., Fearon, D.T. Structure and function of the complement receptors, CR1 (CD35) and CR2 (CD21). Adv. Immunol. 46, 183-219 (1989). 45. Boackle, S.A., Holers, V.M. Role of complement in the development of autoimmunity. Curr. Dir. Autoimmun. 6,154-168 (2003). 46. Walport, M.J. Complement and systemic lupus erythematosus. Arthritis Res. 4, 279-293 (2002). 47. Navratil, J.S., Ahearn, J.M. Apoptosis and autoimmunity: complement deficiency and systemic lupus erythematosus revisited. Curr. Rheumatol. Rep. 2, 32-38 (2000). 48. Boackle, S.A. Role of complement receptor 2 in the pathogenesis of systemic lupus erythematosus. Adv. Exp. Med. Biol. 560, 141-147 (2005). 49. Diamant, E., Melamed, D. Class switch recombination in B lymphopoiesis: a potential pathway for B cell autoimmunity. Autoimmun. Rev. 3, 464-469 (2004). 50. Molina, H., Holers, V.M., Li, B., Fung, Y., Mariathasan, S., Goellner, J., StraussSchoenberger, J., Karr, R.W., Chaplin, D.D. Markedly impaired humoral immune response in mice deficient in complement receptors 1 and 2. Proc. Natl. Acad. Sci. U. S. A 93, 3357-3361 (1996). 51. Ahearn, J.M., Fischer, M.B., Croix, D., Goerg, S., Ma, M., Rothstein, T.L., Carroll, M.C. Disruption of the Cr2 locus results in a reduction in B-1a cells and in an impaired B cell response to T-dependent antigen. Immunity. 4, 251-262 (1996). 52. Rickert, R.C., Rajewsky, K., Roes, J. Impairment of T-cell-dependent B-cell responses and B-1 cell development in CD19-deficient mice. Nature 376, 352-355 (1995). 53. Tedder, T.F., Inaoki, M., Sato, S. The CD19-CD21 complex regulates signal transduction thresholds governing humoral immunity and autoimmunity. Immunity. 6, 107-118 (1997). 54. Haas, K.M., Tedder, T.F. Role of the CD19 and CD21/35 receptor complex in innate immunity, host defense and autoimmunity. Adv. Exp. Med. Biol. 560, 125139 (2005). 55. Hebell, T., Ahearn, J.M., Fearon, D.T. Suppression of the immune response by a soluble complement receptor of B lymphocytes. Science 254, 102-105 (1991). 56. Ahearn, J.M., Fischer, M.B., Croix, D., Goerg, S., Ma, M., Rothstein, T.L., Carroll, M.C. Disruption of the Cr2 locus results in a reduction in B-1a cells and in an impaired B cell response to T-dependent antigen. Immunity. 4, 251-262 (1996). 106 57. Birrell, L., Kulik, L., Morgan, B.P., Holers, V.M., Marchbank, K.J. B cells from mice prematurely expressing human complement receptor type 2 are unresponsive to T-dependent antigens. J. Immunol. 174, 6974-6982 (2005). 58. Gommerman, J.L., Carroll, M.C. Negative selection of B lymphocytes: a novel role for innate immunity. Immunol. Rev. 173, 120-130 (2000). 59. Tedder, T.F., Poe, J.C., Fujimoto, M., Haas, K.M., Sato, S. The CD19-CD21 signal transduction complex of B lymphocytes regulates the balance between health and autoimmune disease: systemic sclerosis as a model system. Curr. Dir. Autoimmun. 8, 55-90 (2005). 60. Carter, R.H., Fearon, D.T. CD19: lowering the threshold for antigen receptor stimulation of B lymphocytes. Science 256, 105-107 (1992). 61. Carter, R.H., Spycher, M.O., Ng, Y.C., Hoffman, R., Fearon, D.T. Synergistic interaction between complement receptor type 2 and membrane IgM on B lymphocytes. J. Immunol. 141, 457-463 (1988). 62. Dempsey, P.W., Allison, M.E., Akkaraju, S., Goodnow, C.C., Fearon, D.T. C3d of complement as a molecular adjuvant: bridging innate and acquired immunity. Science 19/271, 348-350 (1996). 63. Holers, V.M., Boackle, S.A. Complement receptor 2 and autoimmunity. Curr. Dir. Autoimmun. 7, 33-48 (2004). 64. Kozono, Y., Abe, R., Kozono, H., Kelly, R.G., Azuma, T., Holers, V.M. Crosslinking CD21/CD35 or CD19 increases both B7-1 and B7-2 expression on murine splenic B cells. J. Immunol. 160, 1565-1572 (1998). 65. Bonnefoy, J.Y., Henchoz, S., Hardie, D., Holder, M.J., Gordon, J. A subset of antiCD21 antibodies promote the rescue of germinal center B cells from apoptosis. Eur. J. Immunol. 23, 969-972 (1993). 66. Fischer, M.B., Goerg, S., Shen, L., Prodeus, A.P., Goodnow, C.C., Kelsoe, G., Carroll, M.C. Dependence of germinal center B cells on expression of CD21/CD35 for survival. Science 280, 582-585 (1998). 67. Qin, D., Wu, J., Carroll, M.C., Burton, G.F., Szakal, A.K., Tew, J.G. Evidence for an important interaction between a complement-derived CD21 ligand on follicular dendritic cells and CD21 on B cells in the initiation of IgG responses. J. Immunol. 161, 4549-4554 (1998). 68. Fearon, D.T., Carter, R.H. The CD19/CR2/TAPA-1 complex of B lymphocytes: linking natural to acquired immunity. Annu. Rev. Immunol. 13, 127-149 (1995). 69. Fang, Y., Xu, C., Fu, Y.X., Holers, V.M., Molina, H. Expression of complement receptors 1 and 2 on follicular dendritic cells is necessary for the generation of a strong antigen-specific IgG response. J. Immunol. 160, 5273-5279 (1998). 107 70. Prodeus, A.P., Goerg, S., Shen, L.M., Pozdnyakova, O.O., Chu, L., Alicot, E.M., Goodnow, C.C., Carroll, M.C. A critical role for complement in maintenance of self-tolerance. Immunity. 9, 721-731 (1998). 71. Carroll, M.C. The complement system in B cell regulation. Mol. Immunol. 41, 141146 (2004). 72. Yazdanbakhsh, K. Complement Receptor 1 therapeutics for prevention of immune hemolysis. Immunohematol. 21(3), 109-118 (2005). 73. Nagro, C., Kolla, R., Rickert R.C. A critical Role for Complement C3d and the BCell Coreceptor (CD19/CD21) Complex in the Initiation of Inflammatory Arthritis. J. Immunol. 175, 5379-5389 (2005). 74. Chen, Z., Koralov, S.B., Kelsoe, G. Complement C4 inhibits systemic autoimmunity through a mechanism independent of complement receptors CR1 and CR2. J. Exp. Med. 192, 1339-1352 (2000). 75. Goodnow, C.C., Adelstein, S., Basten, A. The need for central and peripheral tolerance in the B cell repertoire. Science 248, 1373-1379 (1990). 76. Rathmell, J.C. Apoptosis and B cell tolerance. Curr. Dir. Autoimmun. 6, 38-60 (2003). 77. Hartley, S.B., Cooke, M.P., Fulcher, D.A., Harris, A.W., Cory, S., Basten, A., Goodnow, C.C. Elimination of self-reactive B lymphocytes proceeds in two stages: arrested development and cell death. Cell 72, 325-335 (1993). 78. Seo, S.J., Mandik-Nayak, L., Erikson, J. B cell anergy and systemic lupus erythematosus. Curr. Dir. Autoimmun. 6, 1-20 (2003). 79. Tiegs, S.L., Russell, D.M., Nemazee, D. Receptor editing in self-reactive bone marrow B cells. J. Exp. Med. 177, 1009-1020 (1993). 80. Goodnow, C.C., Crosbie, J., Jorgensen, H., Brink, R.A., Basten, A. Induction of self-tolerance in mature peripheral B lymphocytes. Nature 342, 385-391 (1989). 81. Paul, E., Lutz, J., Erikson, J., Carroll, M.C. Germinal center checkpoints in B cell tolerance in 3H9 transgenic mice. Int. Immunol. 16, 377-384 (2004). 82. Guzman-Rojas, L., Sims-Mourtada, J.C., Rangel, R., Martinez-Valdez, H. Life and death within germinal centres: a double-edged sword. Immunology 107, 167-175 (2002). 83. Fields, M.L., Seo, S.J., Nish, S.A., Tsai, J.H., Caton, A.J., Ericson, J. The regulation and activation potential of autoreactive B cells. Immunol. Res. 27, 219234 (2003). 84. Rothstein, T.L., Wang, J.K., Panka, D.J., Foote, L.C., Wang, Z., Stanger, B., Ju, S.T., Marshak-Rothstein, A. Protection against Fas-dependent Th1-mediated apoptosis by antigen receptor engagement in B cells. Nature 374, 163-165 (1995). 108 85. Rathmell, J.C., Cooke, M.P., Ho, W.Y., Grein, J., Townsend, S.E., Davis, M.M., Goodnow, C.C. CD95 (Fas)-dependent elimination of self-reactive B cells upon interaction with CD4+ T cells. Nature 376, 181-184 (1995). 86. Mizuno, T., Zhong, X., Rothstein, T.L. Fas-induced apoptosis in B cells. Apoptosis. 8, 451-460 (2003). 87. Fishelson, Z., Attali, G., Mevorach, D. Complement and apoptosis. Mol. Immunol. 38, 207-219 (2001). 88. Melamed, D., Miri, E., Leider, N., Nemazee, D. Unexpected autoantibody production in membrane Ig-mu-deficient/lpr mice. J. Immunol. 165, 4353-4358 (2000). 89. Roark, J.H., Kuntz, C.L., Nguyen, K.A., Caton, A.J., Erikson, J. Breakdown of B cell tolerance in a mouse model of systemic lupus erythematosus. J. Exp. Med. 181, 1157-1167 (1995). 90. Strasser, A., Bouillet, P. The control of apoptosis in lymphocyte selection. Immunol. Rev. 193, 82-92 (2003). 91. Twomey, C., McCarthy, J. Pathways of apoptosis and importance in development. J. Cell. Mol. Med. 9, 345-359 (2005). 92. Han, S., Zheng, B., Dal Porto, J., Kelsoe, G. In situ studies of the primary immune response to (4-hydroxy-3-nitrophenyl)acetyl. IV. Affinity-dependent, antigendriven B cell apoptosis in germinal centers as a mechanism for maintaining selftolerance. J. Exp. Med. 182, 1635-1644 (1995). 93. Pulendran, B., Kannourakis, G., Nouri, S., Smith, K.G., Nossal, G.J. Soluble antigen can cause enhanced apoptosis of germinal-centre B cells. Nature 375, 331334 (1995). 94. Shokat, K.M., Goodnow, C.C. Antigen-induced B-cell death and elimination during germinal-centre immune responses. Nature 375, 334-338 (1995). 95. Darzynkiewicz, Z., Juan, G., Li, X., Gorczyca, W., Mrakami, T., Traganos, F. Cytometry in cell necrobiology: analysis of apoptosis and accidental cell death (necrosis). Cytometry 27, 1-20 (1997). 96. Garland, J.M., Halestrap, A. Energy metabolism during apoptosis. Bcl-2 promotes survival in hematopoietic cells induced to apoptose by growth factor withdrawal by stabilizing a form of metabolic arrest. J. Biol. Chem. 272, 4680-4688 (1997). 97. Navratil, J.S., Ahearn, J.M. Apoptosis, clearance mechanisms, and the development of systemic lupus erythematosus. Curr. Rheumatol. Rep. 3, 191-198 (2001). 98. Roos, A., Xu, W., Castellno, G., Nauta, A.J., Garred, P., Daha, M.R., van Kooten, C. Mini-review: A pivotal role for innate immunity in the clearance of apoptotic cells. Eur. J. Immunol. 34, 921-929 (2004). 109 99. Skoberne, M., Beignon, A.S., Larsson, M., Bhardwaj, N. Apoptotic cells at the crossroads of tolerance and immunity. Curr. Top. Microbiol. Immunol. 289, 259292 (2005). 100. Tang, S., Lui, S.L., Lai, K.N. Pathogenesis of lupus nephritis: an update. Nephrology. (Carlton. ) 10, 174-179 (2005). 101. Tan, E. M., Cohen, A.S., Fries, J.F., Masi, A.T., Mc Shane, D.J., Rothfield, N.F., Talal, N., Winchester, R.J. The 1982 revised criteria for the classification of systemic lupus erythematosus. Arthritis Rheum. 25, 1271-1277 (1982). 102. Illei, G.G., Tackey, E., Lapteva, L., Lipsky, P.E. Biomarkers in systemic lupus erythematosus: II. Markers of disease activity. Arthritis Rheum. 50, 2048-2065 (2004). 103. Trendelenburg, M., Schifferli, J.A. [Apoptosis and C1q: possible explanations for the pathogenesis of systemic lupus erythematosus]. Z. Rheumatol. 59, 172-175 (2000). 104. Foster, M.H., Cizman, B., Madaio, M.P. Nephritogenic autoantibodies in systemic lupus erythematosus: immunochemical properties, mechanisms of immune deposition, and genetic origins. Lab Invest 69, 494-507 (1993). 105. Wang, C., Khalil, M., Ravetch, J., Diamond, B. The naive B cell repertoire predisposes to antigen-induced systemic lupus erythematosus. J. Immunol. 170, 4826-4832 (2003). 106. Agnello, V. Lupus diseases associated with hereditary and acquired deficiencies of complement. Springer Semin. Immunopathol. 9, 161-178 (1986). 107. Atkinson, J.P. Complement deficiency: predisposing factor to autoimmune syndromes. Clin. Exp. Rheumatol. 7, S95-101 (1989). 108. Rupert, K.L., Moulds, J.M., Yang, Y., Arnett, F.C., Warren, R.W., Reveille, J.D., Myones, B.L., Blangchang, C.A., Yu, C.Y. The molecular basis of complete complement C4A and C4B deficiencies in a systemic lupus erythematosus patient with homozygous C4A and C4B mutant genes. J. Immunol. 169, 1570-1578 (2002). 109. Stone, N.M., Williams, A., Wilkinson, J.D., Bird, G. Systemic lupus erythematosus with C1q deficiency. Br. J. Dermatol. 142, 521-524 (2000). 110. Colten, H.R., Rosen, F.S. Complement deficiencies. Annu. Rev. Immunol. 10, 809834 (1992). 111. Bowness, P., Davies, K.A., Norswothy, P.J., Meyer, P.A., Walport, M.J. Hereditary C1q deficiency and systemic lupus erythematosus. QJM. 87, 455-464 (1994). 112. Sontheimer, R., Racila, E., Racila, D. C1q: its functions within the innate and adaptive immune responses and ist role in lupus autoimmunity. J. Invest. Dermatol. 125(1), 12-23 (2005). 110 113. Manderson, A.P., Botto, M., Walport, M.J. The role of complement in the development of systemic lupus erythematosus. Annu. Rev. Immunol. 22, 431-456 (2004). 114. Yang, Y., Chung, E.K., Zhu, B., Lhotta, K., Hebert, L.A., Birmingham, D.J., Rovin, B.H., Yu, C.Y. The intricate role of complement component C4 in human systemic lupus erythematosus. Curr. Dir. Autoimmun. 7, 98-132 (2004). 115. Koide, M., Shirahama, S., Tokura, Y., Takigawa M., Hayakawa, M., Furukawa, F. Lupus erythematosus associated with C1 inhibitor deficiency. J. Dermatol. 29, 503507 (2002). 116. Ohi, H., Yasugi, T. Occurrence of C3 nephritic factor and C4 nephritic factor in membranoproliferative glomerulonephritis (MPGN). Clin. Exp. Immunol. 95, 316321 (1994). 117. Paul, E., Pozdnyakova, O.O., Mitchell, E., Carroll, M. C. Anti-DNA autoreactivity in C4-deficient mice. Eur. J. Immunol. 32, 2672-2679 (2002). 118. Einav, S., Pozdnyakova, O.O., Ma, M., Carroll, M. C. Complement C4 is protective for lupus disease independent of C3. J. Immunol. 168, 1036-1041 (2002). 119. Bottger, E.C., Hoffmann, T., Hadding, U., Bitter-Suermann, D. Guinea pigs with inherited deficiencies of complement components C2 or C4 have characteristics of immune complex disease. J. Clin. Invest 78, 689-695 (1986). 120. Bao, L., Osawe, I., Puri, T., Lambris, J.D., Haas, M., Quigg, I.L. C5a promotes development of experimental lupus nephritis wich cab be blocked with a apecific receptor antagonist. Eur. J. Immunol. 35, 2496-2506 (2005). 121. Lipsky, P.E. Systemic lupus erythematosus: an autoimmune disease of B cell hyperactivity. Nat. Immunol. 2, 764-766 (2001). 122. Ring, G.H., Lakkis, F.G. Breakdown of self-tolerance and the pathogenesis of autoimmunity. Semin. Nephrol. 19, 25-33 (1999). 123. Levine, J.S., Koh, J.S. The role of apoptosis in autoimmunity: immunogen, antigen, and accelerant. Semin. Nephrol. 19, 34-47 (1999). 124. Singer, G.G., Carrera, A.C., Marshak-Rothstein, A., Martinez, C., Abbas, A.K. Apoptosis, Fas and systemic autoimmunity: the MRL-lpr/lpr model. Curr. Opin. Immunol. 6, 913-920 (1994). 125. Botto, M., Dell'Agnola, C., Bygrave, A.E., Thompson, E.M., Cook, H.T., Petry, F., Loos, M., Pandolfi, P.P., Walport, M.J. Homozygous C1q deficiency causes glomerulonephritis associated with multiple apoptotic bodies. Nat. Genet. 19, 56-59 (1998). 126. Munoz, L., Herrmann, M., Gaipl, U. An impaired clearebce of dying cells can lead to the development of chronic autoimmunity. Z. Rheumatol. 64, 370-376 (2005). 111 127. Mevorach, D., Zhou, J.L., Song, X., Elkon, K.B. Systemic exposure to irradiated apoptotic cells induces autoantibody production. J. Exp. Med. 188, 387-392 (1998). 128. Cook, H.T. Complement deficiencies, lupus and apoptosis. Adv. Nephrol. Necker Hosp. 31, 29-41 (2001). 129. Baumann, I., Kolowos, W., Voll, R.E., Manger, B., Kalden, J.R., Herrmann, M. Impaired uptake of apoptotic cells into tingible body macrophages in germinal centers of patients with SLE. Arthritis Rheum. 46, 191-201 (2002). 130. Martin, R.M., Brady, J.L., Lew, A.M. The need for IgG2c specific antiserum when isotyping antibodies from C57BL/6 and NOD mice. J. Immunol. Methods 212, 187192 (1998). 131. Navratil, J.S., Ahearn, J.M. Apoptosis, clearance mechanisms, and the development of systemic lupus erythematosus. Curr. Rheumatol. Rep. 3, 191-198 (2001). 132. Grammer, A.C., Lipsky, P.E. B cell abnormalities in systemic lupus erythematosus. Arthritis Res. Ther. 5, 22-27 (2003). 133. Salmon, M., Gordon, C. The role of apoptosis in systemic lupus erythematosus. Rheumatology. (Oxford) 38, 1177-1183 (1999). 134. Lopez-Hoyos, M., Marquina, R., Tamayo, E., Gonzales-Rojas, J., Izui, S., Merino, R., Merino, J. Defects in the regulation of B cell apoptosis are required for the production of citrullinated peptide autoantibodies in mice. Arthritis Rheum. 48, 2353-2361 (2003). 135. Jack, R.S., Imanishi-Kari, T., Rajewsky, K. Idiotypic analysis of the response of C57BL/6 mice to the (4-hydroxy-3-nitrophenyl)acetyl group. Eur. J. Immunol. 7, 559-565 (1977). 136. Toellner, K.M., Gulbranson-Judge, A., Taylor, D.R., Sze, D.M., MacLennan, I. C. Immunoglobulin switch transcript production in vivo related to the site and time of antigen-specific B cell activation. J. Exp. Med. 183, 2303-2312 (1996). 137. Coutelier, J.P., van der Logt, J.T., Heessen, F.W., Vink, A., van Snick, J. Virally induced modulation of murine IgG antibody subclasses. J. Exp. Med. 168, 23732378 (1988). 138. Zachrau, B., Finke, D., Kropf, K., Gosink, H.J., Kirchner, H., Goerg, S. Antigen localization within the splenic marginal zone restores humoral immune response and IgG class switch in complement C4-deficient mice. Int. Immunol. 16, 16851690 (2004). 139. Mongini, P.K., Jackson, A.E., Tolani, S., Fattah, R.J., Inman, J.K. Role of complement-binding CD21/CD19/CD81 in enhancing human B cell protection from Fas-mediated apoptosis. J. Immunol. 171, 5244-5254 (2003). 140. Munoz, L., Herrmann, M., Gaipl, U. An impaired clearebce of dying cells can lead to the development of chronic autoimmunity. Z. Rheumatol. 64(6), 370-376 (2005). 112 141. Burstein, H.J., Abbas, A.K. In vivo role of interleukin 4 in T cell tolerance induced by aqueous protein antigen. J. Exp. Med. 177, 457-463 (1993). 142. Dresser, D.W. Specific inhibition of antibody production. IV. Standardization of the antigen-elimination test; immunological paralysis of mice previously immunized. Immunology 9, 261-273 (1965). 143. Pulendran, B., Karvelas, M., Nossal, G.J. A form of immunologic tolerance through impairment of germinal center development. Proc. Natl. Acad. Sci. U. S. A 91, 2639-2643 (1994). 144. Claman, H.N., Bronsky, E. A. Production of tolerance in immunized mice and the effects of immunosuppression. J. Allergy 38, 208-214 (1966). 145. Muramatsu, S., Hosono, M. Quantitative and qualitative analyses of the antibody response of adult mice tolerized with deaggregated bovine gamma-globulin. I. At the serum antibody level. Jpn. J. Microbiol. 18, 357-366 (1974). 146. Nossal, G.J., Karvelas, M. Soluble antigen abrogates the appearance of anti-protein IgG1-forming cell precursors during primary immunization. Proc. Natl. Acad. Sci. U. S. A 87, 1615-1619 (1990). 147. Karvelas, M., Nossal, G.J. Memory cell generation ablated by soluble protein antigen by means of effects on T- and B-lymphocyte compartments. Proc. Natl. Acad. Sci. U. S. A 89, 3150-3154 (1992). 148. Pulendran, B., Smith, K.G., Nossal, G.J. Soluble antigen can impede affinity maturation and the germinal center reaction but enhance extrafollicular immunoglobulin production. J. Immunol. 155, 1141-1150 (1995). 149. Lane, P. Development of B-cell memory and effector function. Curr. Opin. Immunol. 8, 331-335 (1996). 150. Linton, P.J., Lo, D., Lai, L., Thorbecke, G.J., Klinman, N.R. Among naive precursor cell subpopulations only progenitors of memory B cells originate germinal centers. Eur. J. Immunol. 22, 1293-1297 (1992). 151. Takahashi, Y., Ohta, H., Takemori, T. Fas is required for clonal selection in germinal centers and the subsequent establishment of the memory B cell repertoire. Immunity. 14, 181-192 (2001). 152. Nossal, G.J., Karvelas, M., Pulendran, B. Soluble antigen profoundly reduces memory B-cell numbers even when given after challenge immunization. Proc. Natl. Acad. Sci. U. S. A 90, 3088-3092 (1993). 153. Da Costa, X., Brockmann, M.A., Alicot, E., Ma, M., Fischer, M.B., Zhou, X., Knipe, D.M., Carroll, M.C. Humoral response to herpes simplex virus is complement-dependent. Proc. Natl. Acad. Sci. U. S. A. 96, 12708-12712 (1999). 154. Rathmell, J.C., Goodnow, C.C. Effects of the lpr mutation on elimination and inactivation of self-reactive B cells. J. Immunol. 153, 2831-2842 (1994). 113 155. Ju, S. T., Panka, D.J., Cui, H., Ettinger, R., el-Khatib, M., Sherr, D.H., Stanger, B.Z., Marshak-Rothstein, A. Fas(CD95)/FasL interactions required for programmed cell death after T-cell activation. Nature 373, 444-448 (1995). 156. Hoch, S., Boyd, M., Malone, B., Gonye, B., Schwaber, J. Fas-mediated apoptosis eliminates B cells that acquire self-reactivity during the germinal center response to NP. Cell Immunol. 203, 103-110 (2000). 157. Smith, K.G., Nossal, G.J., Tarlinton, D.M. FAS is highly expressed in the germinal center but is not required for regulation of the B-cell response to antigen. Proc. Natl. Acad. Sci. U. S. A 92, 11628-11632 (1995). 158. Foote, L.C., Howard, R.G., Marshak-Rothstein, A., Rothstein, T.L. IL-4 induces Fas resistance in B cells. J. Immunol. 157, 2749-2753 (1996). 159. Kozono, Y., Duke, R.C., Schleicher, M.S., Holers, V.M. Co-ligation of mouse complement receptors 1 and 2 with surface IgM rescues splenic B cells and WEHI231 cells from anti-surface IgM-induced apoptosis. Eur. J. Immunol. 25, 1013-1017 (1995). 160. Haggerty, H.G., Wechsler, R.J., Lentz, V.M., Monroe, J.G. Endogenous expression of delta on the surface of WEHI-231. Characterization of its expression and signaling properties. J. Immunol. 151, 4681-4693 (1993). 161. Carey, G.B., Donjerkovic, D., Mueller, C.M., Liu, S., Hinshaw, J.A., Tonetti, L., Davidson, W., Scott, D.W. B-cell receptor and Fas-mediated signals for life and death. Immunol. Rev. 176, 105-115 (2000). 162. Bras, A., Ruiz-Vela, A., de Buitrago, G., Martinez, A. Caspase activation by BCR cross-linking in immature B cells: differential effects on growth arrest and apoptosis. FASEB J. 13, 931-944 (1999). 163. Jakway, J.P., Usinger, W.R., Gold, M.R., Mishell, R.I., DeFranco, A.L. Growth regulation of the B lymphoma cell line WEHI-231 by anti-immunoglobulin, lipopolysaccharide, and other bacterial products. J. Immunol. 137, 2225-2231 (1986). 164. Boyd, A.W., Goding, J.W., Schrader, J.W. The regulation of growth and differentiation of a murine B cell lymphoma. I. Lipopolysaccharide-induced differentiation. J. Immunol. 126, 2461-2465 (1981). 165. Gottschalk, A.R., Quintans, J. Apoptosis in B lymphocytes: the WEHI-231 perspective. Immunol. Cell Biol. 73, 8-16 (1995). 166. Hata, K., Yoshimoto, T., Mizuguchi, J. CD40 ligand rescues inhibitor of differentiation 3-mediated G1 arrest induced by anti-IgM in WEHI-231 B lymphoma cells. J. Immunol. 173, 2453-2461 (2004). 167. Hobbs, M.V., McEvilly, R.J., Koch, R.J., Cardenas, G.J., Noonan, D.J. Interleukin6 production by murine B cells and B cell lines. Cell Immunol. 132, 442-450 (1991). 114 168. Sidman, C.L., Marshall, J.D. B cell maturation factor: effects on various cell populations. J. Immunol. 132, 845-850 (1984). 169. Lanier, L.L., Warner, N.L., Ledbetter, J.A., Herzenberg, L.A. Quantitative immunofluorescent analysis of surface phenotypes of murine B cell lymphomas and plasmacytomas with monoclonal antibodies. J. Immunol. 127, 1691-1697 (1981). 170. Ben Jilani, K.E., Akarid, K., Arnoult, D., Petit, F., Baert, E., Gaillard, J.P., Ameisen, J.C., Estaquier, J. Gamma-interferon induces apoptosis of the B lymphoma WEHI-279 cell line through a CD95/CD95L-independent mechanism. Eur. Cytokine Netw. 12, 587-596 (2001). 171. Han, S., Zheng, B., Takahashi, Y., Kelsoe, G. Distinctive characteristics of germinal center B cells. Semin. Immunol. 9, 255-260 (1997). 172. Guilbault, B., Kay, R.J. RasGRP1 sensitizes an immature B cell line to antigen receptor-induced apoptosis. J. Biol. Chem. 279, 19523-19530 (2004). 173. Rathmell, J.C., Goodnow, C.C. The in vivo balance between B cell clonal expansion and elimination is regulated by CD95 both on B cells and in their microenvironment. Immunol. Cell Biol. 76, 387-394 (1998). 174. Wang, J., Lobito, A.A., Shen, F., Hornung, F., Winoto, A., Lenardo, M.J. Inhibition of Fas-mediated apoptosis by the B cell antigen receptor through c-FLIP. Eur. J. Immunol. 30, 155-163 (2000). 175. Tian, M.T., Chou, C.H., DeFranco, A.L. Apoptosis induced by the antigen receptor and Fas in a variant of the immature B cell line WEHI-231 and in splenic immature B cells. Int. Immunol. 13, 581-592 (2001). 176. Mueller, C.M., Scott, D.W. Distinct molecular mechanisms of Fas resistance in murine B lymphoma cells. J. Immunol. 165, 1854-1862 (2000). 177. Foote, L.C., Evans, J.W., Cifuni, J.M., Siracusa, M.C., Monteforte, G.M., McCole, J.L., D'Orazio, C.C., Hastings, W.D., Rothstein, T.L. Interleukin-4 produces a breakdown of tolerance in vivo with autoantibody formation and tissue damage. Autoimmunity 37, 569-577 (2004). 178. Wang, J., Taniuchi, I., Maekawa, J., Howard, M., Cooper, M.D., Watanabe, T. Expression and function of Fas antigen on activated murine B cells. Eur. J. Immunol. 26, 92-96 (1996). 179. Foote, L.C., Marshak-Rothstein, A., Rothstein, T.L. Tolerant B lymphocytes acquire resistance to Fas-mediated apoptosis after treatment with interleukin 4 but not after treatment with specific antigen unless a surface immunoglobulin threshold is exceeded. J. Exp. Med. 187, 847-853 (1998). 180. Rothstein, T.L., Zhong, X., Schram, B.R., Negm, R.S., Donohoe, T.J., Cabral, D.S., Foote, L.C., Schneider, T.J. Receptor-specific regulation of B-cell susceptibility to Fas-mediated apoptosis and a novel Fas apoptosis inhibitory molecule. Immunol. Rev. 176, 116-133 (2000). 115 181. Do, R.K., Hatada, E., Lee, H., Tourigny, M.R., Hilbert, D., Chen-Kiang, S. Attenuation of apoptosis underlies B lymphocyte stimulator enhancement of humoral immune response. J. Exp. Med. 192, 953-964 (2000). 182. Inaba, M., Inaba, K., Fukuba, J., Mori, S., Haruna, H., Doi, H., Adachi, Y., Iwai, H., Hosaka, N., Hisha, H. Activation of thymic B cells by signals of CD40 molecules plus interleukin-10. Eur. J. Immunol. 25, 1244-1248 (1995). 183. Arens, R., Nolte, M.A., Tesselaar, K., Heemskerk, B., Reedquist, K.A., van Lier, R.A., van Oers, M.H. Signaling through CD70 regulates B cell activation and IgG production. J. Immunol. 173, 3901-3908 (2004). 184. Foote, L. C., Schneider T.J., Fischer, G.M., Wang, J.K., Rasmussen, B., Campbell, K.A., Lynch, D.H., Ju, S.T., Marshak-Rothstein, A., Rothstein, T.L. Intracellular signaling for inducible antigen receptor-mediated Fas resistance in B cells. J. Immunol. 157, 1878-1885 (1996). 185. Munoz, L., Herrmann, M., Gaipl, U. An impaired clearebce of dying cells can lead to the development of chronic autoimmunity. Z. Rheumatol. 64, 370-376 (2005). 116 Danksagung Ich danke allen, die zur Entstehung dieser Arbeit beigetragen haben. Besonders danken möchte ich meinem Doktorvater PD Dr. med. S. Görg für die Überlassung des Themas, die Ideen, den Rückhalt und die Geduld, Herrn Prof. Dr. med. H. Kirchner für die engagierte Förderung und die Möglichkeit, in seinem Institut arbeiten zu können, Frau Dr. rer. nat. D. Finke für die vielen Stunden im Tierstall, für die netten Sonntagnachmittage im Labor und vor allem für die immer zu erreichende Hilfe bei kleinen und großen Problemen, mit der sie viele Versuche erst möglich machte, Frau K. Klempt-Gießing für die geduldige Einführung in verschiedene Methoden und für die immer wieder neue Etablierung der Standards der ELISA Messungen, Herrn PD Dr. med. P. Schlenke für die Einführung und Unterstützung in der Methodik der Durchflußfluoreszenzzytometrie, Herrn Prof. Dr. med. H. C. Dominick, Frau Dr. rer. nat. D. Finke, Frau N. Marquardt und meinen Eltern für die Korrekturvorschläge, allen „Bewohnern“ des Biologenzimmers für die lange Aufnahme, und allen in den ZKLaboren des Institutes für Immunologie arbeitenden Menschen, durch die es für mich (fast) immer eine Freude war, dort zu arbeiten, meinem Vater für die Motivation diese Arbeit zu beginnen und Freude daran zu finden, und meiner Mutter für das Durchhaltevermögen, mit dem ich diese Arbeit zu Ende bringen konnte. 117 Kongreßbeiträge und Veröffentlichungen Faust, K., Finke, D., Klempt-Giessing, K., Randers, K., Zachrau, B., Schlenke, P., Kirchner, H., Goerg, S. “Antigen induced B-cell apoptosis is independent of complement C4” Clinical and Experimental Immunology 2007, in press Faust, K., Finke, D., Klempt-Giessing, K., Zachrau, B., Kirchner, H., Goerg, S. „Antigen-induced apoptosis -an essential mechanism for maintaining self-tolerance?” Poster, 16th European Congress of Immunology (1st Joint meeting of European Societies of Immunology), Paris 2006 Finke, D., Kropf, K., Hennig, H., Hoerster, R., Lueddecke, K., Zawatzky, R., Goerg, S. “Role of Interferon alpha for the Development of Systemic Lupus Erythematosus in Complement C4 deficient Mice” Poster, 34. Jahrestagung der Deutschen Gesellschaft für Immunologie, Berlin 2003 Lüddecke, K., Finke, D., Kropf, K., Zachrau, B., Schlenke, P., Kirchner, H., Goerg, S. „Antigen-driven B-cell apoptosis in germinal centres does not abrogate antibody production completely” Poster, 34. Jahrestagung der Deutschen Gesellschaft für Immunologie, Berlin 2003 Finke, D., Kropf, K., Lüddecke, K., Zachrau, B., Schlenke, P., Kirchner, H., Goerg, S. “The expression of follicular dendritic cell (FDC) specific markers is influenced by complement C4” Poster, 33. Jahrestagung der Deutschen Gesellschaft für Immunologie, Marburg 2002 118 Lebenslauf Name: Kirstin Faust, geb. Lüddecke Geburtsdatum: 27. Januar 1979 Geburtsort: Ludwigshafen am Rhein 1985 - 1989 Grundschule im Mandelgraben, Mutterstadt 1989 - 1998 Geschwister-Scholl-Gymnasium, Ludwigshafen a. R. 26.Jun.1998 Abitur 1998 - 2005 Studium der Humanmedizin, Universität zu Lübeck Sep.2000 Ärztliche Vorprüfung Aug. 2001 Erster Abschnitt der Ärztlichen Prüfung Mrz. 2004 Zweiter Abschnitt der Ärztlichen Prüfung 2004 - 2005 Praktisches Jahr: Kinder- und Thoraxchirurgie, Universitätsklinikum Montpellier, Frankreich Pädiatrie, Universitätsklinikum Schleswig-Holstein, Campus Lübeck Innere Medizin, Sana - Kliniken Lübeck Aug. 2005 Heirat mit dem Schiffahrtskaufmann Dierk Oliver Faust Okt. 2005 Dritter Abschnitt der Ärztlichen Prüfung 2000 - 2005 Doktorandin des Institutes für Immunologie und Transfusionsmedizin der Universität Lübeck (Experimenteller Teil der Doktorarbeit 2000 - 2004) 119