Molekulares Docking von Substraten und Enzymen
Werbung

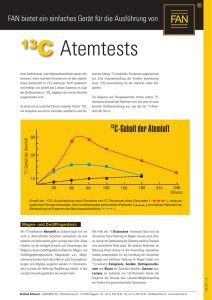
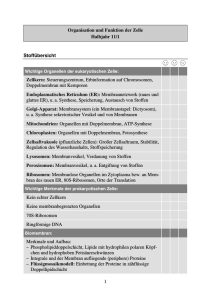
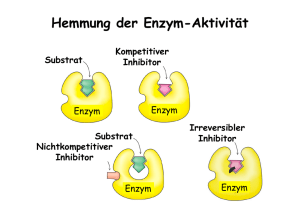
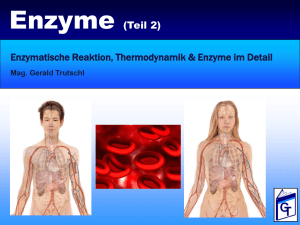
762_824_BIOsp_0709.qxd 30.10.2009 10:01 Uhr Seite 765 765 Proteindesign Molekulares Docking von Substraten und Enzymen BENJAMIN JUHL, JÜRGEN PLEISS INSTITUT FÜR TECHNISCHE BIOCHEMIE, UNIVERSITÄT STUTTGART In der industriellen („weißen“) Biotechnologie werden Enzyme zur Katalyse chemischer Reaktionen eingesetzt. An der Universität Stuttgart wurde die Methode des „molekularen Docking“ weiterentwickelt, um verbesserte Biokatalysatoren zu entwickeln. In industrial („white“) biotechnology, enzymes are applied as catalysts of chemical reactions. At the University of Stuttgart the method of molecular docking was extended to develop improved biocatalysts. ó Molekulares Docking wurde ursprünglich zur Modellierung der Bindung von Inhibitoren an medizinisch relevante Zielproteine entwickelt. Für die Untersuchung der Bindung von Substraten an Enzyme und der enzymatischen Umsetzung dieser Substrate musste die Methode in drei wichtigen Punkten modifiziert und erweitert werden. Erstens behandeln konventionelle DockingProgramme Enzyme als starr, während sie in Wirklichkeit flexibel sind und es vor und während der Substratbindung zu Konformationsänderungen im Enzym, insbesondere in der Bindetasche, kommen kann. Außerdem liegen die verfügbaren Enzymstrukturen, die für molekulares Docking benötigt werden, nicht immer in einer Konformation vor, die optimal für eine Substratbindung ist, da die Bedingungen, unter denen die Enzymstruktur aufgeklärt wurde, große Unterschiede zu den Bedingungen, unter denen Enzymkatalyse stattfindet, aufweisen. Die Berücksichtigung der Enzymflexibilität verbessert deshalb nicht BIOspektrum | 07.09 | 15. Jahrgang nur die Genauigkeit der Docking-Methode, sondern ermöglicht es auch, Enzymstrukturen zum Docking zu verwenden, die als starre Modelle ungeeignet wären [1, 2]. Zweitens ist das Docking von Substraten in ihrem Grundzustand nicht aussagekräftig, da die für die Katalyse wesentlichen Interaktionen einen Zustand betreffen, der zwischen der Struktur des Substrats und der des Produkts liegt. Im Unterschied zu Inhibitoren, die in ihrem Grundzustand an das Enzym binden, muss ein Substrat in seinem Übergangszustand gedockt werden. Und drittens ist die korrekte Positionierung eines Substrats in der Bindungstasche Voraussetzung für dessen effiziente Umsetzung durch das Enzym. Zur Überprüfung der spezifischen Interaktionen zwischen Enzym und Substrat wurde für Lipasen und Esterasen ein einfacher geometrischer Filter entwickelt (Abb. 1), der es ermöglicht, gedockte Substrate in produktive und nicht-produktive Substratpositionen einzuteilen [1, 2]. ˚ Abb. 1: Bindung von Ethylacetat (türkis; Wasserstoffe hellgrau) an Lipase B aus Candida antarctica: geometrischer Filter, um produktive Substratplatzierungen zu identifizieren. Das Substrat muss für eine effiziente Hydrolyse vier charakteristische Wasserstoffbrücken (a–d, orange) mit dem Enzym (grün; Wasserstoffe hellgrau) ausbilden. Diese drei Erweiterungen des molekularen Dockings wurden in ein mehrstufiges Verfahren integriert (Abb. 2). Dabei wird das Substrat zunächst in einem tetrahedralen Übergangszustand konstruiert und mit dem Programm FlexX [3] in das Enzym gedockt, wobei eine kovalente Bindung zu dem katalytisch aktiven Serin ausgebildet wird. Mit der bestbewerteten Substratposition wird dann jeweils ein Enzym-Substrat-Komplex gebildet. Dieser wird anschließend parametrisiert und mit dem Programm Amber [4] durch Energieminimierung geometrisch optimiert, um Überlappungen zwischen Substrat- und Enzymatomen zu beseitigen. Das Substrat wird dann aus dem optimierten Komplex entfernt und 762_824_BIOsp_0709.qxd 766 30.10.2009 10:01 Uhr Seite 766 MET H ODE N & AN WE N DU NGEN ˚ Abb. 2: Dreistufiges Dockingverfahren: In einem ersten Schritt wird ein Substrat in eine Enzymstruktur gedockt. Der so entstandene Enzym-Substrat-Komplex (hellgrün) wird energieminimiert, um einen optimierten Komplex (dunkelgrün) zu erhalten. Aus diesem optimierten Komplex wird eine optimierte Enzymstruktur (dunkelblau) extrahiert und für ein zweites Docking des gleichen Substrats (hellbraun) verwendet. Die resultierenden endgültigen Substratplatzierungen werden mittels eines geometrischen Filters klassifiziert und nach dem Docking-Score geordnet. Triethylcitrat Candida antarctica Lipase B Candida rugosa Lipase Alcaligenes sp. Esterase ˚ Abb. 3: Vergleich der relativen Aktivität von Candida antarctica-Lipase B, Candida rugosa-Lipase und Alcaligenes sp.-Esterase. Die relativen Aktivitäten sind auf die Aktivität für Methyllaurat (blau) normiert. Die Esterase aus Alcaligenes sp. zeigt für Diethylmalat (rot) und Triethylcitrat die höchste relative Aktivität. ˚ Abb. 4: Darstellung von Lipase B aus Candida antarctica (PDB-ID: 1TCA; grün) mit den über das Screening einer in silico-Mutantenbibliothek identifizierten Aminosäuren (orange), die die Bindung sperriger Substrate verhindern. Außerdem ist ein gedocktes sperriges Substrat (2-Ethylhexansäureethylester, türkis) gezeigt. in einem zweiten Dockingschritt nochmals in die nun für die Substratbindung optimierte Enzymstruktur kovalent gedockt. Die auf diese Weise generierten Substratpositionen in der optimierten Enzymstruktur werden mittels eines geometrischen Filters (Abb. 1) in produktive und nicht-produktive Lösungen eingeteilt und anhand ihres Docking-Scores bewertet. Eine mithilfe dieses neuen Verfahrens durchgeführte Docking-Studie verschiedener Substrate in mehrere Lipasen und Esterasen zeigte eine Trefferquote von 80 Prozent bei der Vorhersage von Substratspezifität und Stereoselektivität [1]. Die Methode wurde in einer Zusammenarbeit mit unserem Industriepartner Evonik Industries AG zur Entwicklung von Biokatalysatoren zur Synthese von Tensiden und anderen kosmetischen Inhaltsstoffen aus nachwachsenden Rohstoffen eingesetzt. Zur Entwicklung neuer Biokatalysatoren wurden zwei Strategien verfolgt. Zum einen wurden Enzymstrukturen von Lipasen und Esterasen, in denen das aktive Zentrum annotiert war, aus der „Lipase Engineering Database“ [5] entnommen und mittels molekularem Docking auf Substratbindung untersucht. Mit den in der Datenbank hinterlegten Informationen über die katalytischen Aminosäuren war es möglich, mehrere sperrige Substrate automatisch in die Enzymstrukturen zu docken und so ein in silico-Screening durchzuführen. Mit dieser Strategie konnte die Esterase aus Alcaligenes sp. identifiziert werden, für die eine Aktivität gegen sperrige Substrate vorhergesagt wurde. Eine experimentelle Überprüfung bestätigte diese Vorhersage und zeigte, dass diese Esterase eine hohe relative Aktivität für das sperrige Substrat Diethylmalat besitzt und für das ebenfalls sperrige Substrat Triethylcitrat zumindest eine Basisaktivität zeigt (Abb. 3). Im Gegensatz dazu BIOspektrum | 07.09 | 15. Jahrgang 762_824_BIOsp_0709.qxd 30.10.2009 10:01 Uhr besitzt die in der Biokatalyse häufig eingesetzte Lipase B aus Candida antarctica eine relativ niedrige Aktivität gegenüber dem sperrigen Diethylmalat und setzt Triethylcitrat nicht um. Da Lipase B aus C. antarctica bei hohen Temperaturen stabil ist und für viele Substrate eine hohe Selektivität besitzt, sollte das Enzym durch ProteinEngineering so verändert werden, dass es auch sperrige Substrate umsetzt. Daher wurden durch Docking diejenigen Aminosäuren in der Substratbindetasche identifiziert, die die Bindung von sperrigen Substraten verhindern (Abb. 4). Der Austausch dieser Aminosäuren sollte die katalytische Aktivität gegenüber sperrigen Substraten wesentlich erhöhen. Daher wurde durch Aminosäureaustausch an fünf Positionen eine in silico-Bibliothek mit insgesamt 2.400 Strukturmodellen angelegt, die alle möglichen Aminosäurekombinationen enthielt. Durch Docking mehrerer sperriger Substrate in diese Strukturmodelle wurden Aminosäureaustausche gefunden, die das Docking von sperrigen Substraten besser unterstützten als der Wildtyp. Einzelmutanten, die auf diese Weise identifiziert wurden, zeigten für sperrige Substrate im Experiment Aktivitätssteigerungen von bis zu 300 Prozent gegenüber dem Wildtyp. Fazit Mit dieser Erweiterung der Methode des molekularen Docking ist es möglich, Substratspezifität und Selektivität von Enzymen zuverlässig vorherzusagen und damit die Entwicklung neuer Biokatalysatoren zu unterstützen, indem einerseits durch Screening von Strukturdatenbanken mittels molekularem Docking neue Enzyme für industriell relevante Substrate identifiziert werden können, andererseits molekulares Docking aber auch dazu eingesetzt werden kann, um Aminosäurepositionen in bereits bekannten Enzymen zu identifizieren, bei denen ein Aminosäureaustausch zu einer Aktivitätssteigerung führt. ó BIOspektrum | 07.09 | 15. Jahrgang Seite 767 Literatur [1] Juhl PB, Trodler P, Tyagi S et al. (2009) Modelling substrate specificity and enantioselectivity for lipases and esterases by substrate-imprinted docking. BMC Struct Biol 9:39 [2] Tyagi S, Pleiss J (2006) Biochemical profiling in silico – predicting substrate specificities of large enzyme families. J Biotechnol 124:108–116 [3] Kramer B, Rarey M, Lengauer T (1999) Evaluation of the FLEXX incremental construction algorithm for protein-ligand docking. Proteins 37:228–241 [4] Case DA, Cheatham 3rd TE, Darden T et al. (2005) The Amber biomolecular simulation programs. J Comput Chem 26:1668–1688 [5] Fischer M, Pleiss J (2003) The Lipase Engineering Database: a navigation and analysis tool for protein families. Nucleic Acids Res 31:319–321 1 2 Korrespondenzadresse: Prof. Dr. Jürgen Pleiss1 Benjamin Juhl2 Institute of Technical Biochemistry Universität Stuttgart Allmandring 31 D-70569 Stuttgart Tel.: 0711-685-63191 Fax: 0711-685-63196 [email protected] www.itb.uni-stuttgart.de