7.7 Stammbaumanalyse
Werbung

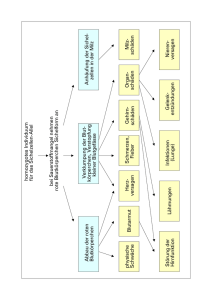
282 7 Formalgenetik mosomen mit dem w-Allel führt also zu weiß- bzw. rotäugigen Tieren. Damit war eindeutig belegt, dass Gene auf den Chromosomen liegen. Da auch X0-Tiere Männchen sind, zeigt diese Kreuzung außerdem, dass das Y-Chromosom bei der Geschlechtsbestimmung von Drosophila keine entscheidende Rolle spielt (S. 303). 7.7 Stammbaumanalyse 7 Die Charakteristika einer Reihe definierter Erbgänge beim Menschen (autosomal dominant, autosomal rezessiv und X-Chromosom gebunden) lassen sich anhand von Stammbäumen nachvollziehen. Für das Verständnis der genetischen Hintergründe von Merkmalen sind kontrollierte Kreuzungen und die Analyse einer größeren Zahl von Nachkommen bzw. Generationen nötig. Dies ist beim Menschen naturgemäß nicht möglich und auch bei größeren Säugetieren technisch schwierig. Einen Ausweg stellen in diesen Fällen Stammbaumanalysen dar, die gerade in der Humangenetik von großer Bedeutung sind, denn in vielen Fällen werden erbliche Krankheiten als Merkmale beobachtet. Dabei werden die lebenden Familienmitglieder untersucht und befragt, um krankheitsbezogene Informationen auch über verstorbene Familienmitglieder zu erhalten. Ist der Stammbaum erstellt, analysiert man das Verhalten eines Merkmals über mehrere Generationen hinweg und zieht dann Schlüsse über Dominanz und Rezessivität von Genen und ihre Lokalisation auf Autosomen oder Sexchromosomen. Ist die Art des Erbgangs bestimmt, kann die Häufigkeit abgeschätzt werden, mit der das Merkmal an die Nachkommen vererbt wird. Der amerikanische Humangenetiker Victor McKusick hat sich die Aufgabe gestellt, die genetisch bedingten Merkmale des Menschen in einer Liste zu erfassen. Diese Liste ist mittlerweile als McKusick-Katalog (http://www.ncbi.nlm.nih.gov/omim/) bekannt und enthielt im Mai 2009 insgesamt fast 20 000 Einträge zu Genen und phänotypischen Merkmalen. 7.7.1 Autosomal dominanter Erbgang Autosomal dominant vererbte Merkmale sind beim Menschen recht häufig. Auch einige Krankheiten wie das Retinoblastom (Tumor der Retina), die Neurofibromatose und die familiäre Hypercholesterolämie, die hier als Beispiel dienen soll, zeigen diesen Erbgang. Die familiäre Hypercholesterolämie ist die Folge einer Genmutation auf dem kurzen Arm von Chromosom 19. Das Gen codiert für ein Rezeptorprotein, das für Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Geschlechtsgebundene Vererbung: Erbgang von heterosomal codierten Merkmalen, hemizygotes Allel beim heterogameten Geschlecht. Reziproke Kreuzung liefert andere Zahlenverhältnisse. 283 Abb. 7.15 Autosomal dominanter Erbgang. Stammbaum einer Familie mit Hypercholesterolämie. Es sind vier Generationen (I bis IV) erfasst, wobei die Urgroßeltern bereits verstorben sind. Das Individuum III-1 war homozygot (AA) für das dominante Allel und ist jung verstorben. Die anderen Merkmalsträger sind heterozygot (Aa). die Aufnahme von sogenannten Low Density Lipoproteins (LDL) in die Zellen sorgt. Fällt das Rezeptorprotein aus, ergeben sich anormal hohe Blutwerte für LDL. Die Hauptsymptome bestehen in der Ausbildung von knotenartigen verschiebbaren Fetteinlagerungen in der Haut (Xanthome), und die Patienten leiden in relativ frühem Alter an Erkrankungen der Herzkranzgefäße. Familiäre Hypercholesterolämie tritt bei einem von 500 Individuen auf. Der Stammbaum einer betroffenen Familie zeigt die Charakteristika autosomal dominanter Erbgänge (Abb. 7.15). Frauen wie auch Männer zeigen das Merkmal zu gleichen Anteilen. Liegt vollständige Penetranz vor, tritt das Merkmal in allen Generationen auf und wird von Frauen und Männern gleichermaßen an die Nachkommen weitergegeben. Personen, die das Merkmal nicht zeigen, übertragen es auch nicht. Somit ist ein autosomal dominanter Erbgang relativ leicht zu entdecken. Bei einer autosomal dominant vererbten Krankheit besteht für die Nachkommen ein relativ hohes Risiko ebenfalls zu erkranken. Es hat Heiraten zwischen Individuen mit Hypercholesterolämie gegeben, und entsprechend der Mendel-Regeln waren dann 25 % der Nachkommen nicht betroffen (aa), 50 % waren heterozygot (Aa) für das Merkmal und 25 % waren homozygot (AA) für das Merkmal. Bei der familiären Hypercholesterolämie entwickeln homozygote Merkmalsträger die Krankheitssymptome bereits in der Kindheit, und die Patienten versterben, bevor sie das Erwachsenenalter erreichen. Bei der Heirat zwischen einem heterozygoten Merkmalsträger und einem nicht betroffenen Individuum sind 50 % heterozygote (Aa) Merkmalsträger und 50 % gesunde Individuen (aa) zu erwarten. Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 7.7 Stammbaumanalyse 7 7 Formalgenetik 7.7.2 Autosomal rezessiver Erbgang Beispiele für den autosomal rezessiven Erbgang finden wir beim Menschen in der Adenosindeaminasedefizienz (ADA), einer Erkrankung, die ein nicht funktionsfähiges Immunsystem nach sich zieht, der zystischen Fibrose (Mukoviszidose), eine Funktionsstörung der schleim- und schweißproduzierenden Drüsen, und der Sichelzellenanämie (Anämie = Blutarmut), beruhend auf einer zu gerinBiochemie, Zellbiologie). gen Zahl an Erythrocyten ( Bei erwachsenen Menschen ist das Blutpigment Hämoglobin A (Allel HbA oder kurz A) ein Tetramer aus zwei a-Globinen und zwei b-Globinen. Die Sichelzellenanämie wird durch eine Punktmutation in den Genen für die b-Globine verursacht. Es resultiert ein verändertes Pigment, das als Hämoglobin S (Allel HbS oder kurz S) bezeichnet wird. Rote Blutkörperchen mit HbS nehmen bei niedrigem Sauerstoffpartialdruck eine charakteristische Sichelzellform an, die zum Namen der Erkrankung geführt hat. Homozygote Träger (SS) für das S-Allel leiden an chronischer Blutarmut und erhöhtem Infarktrisiko, da die verformten Blutkörperchen dazu neigen, Blutgefäße zu blockieren. Die Krankheit tritt gehäuft bei Afrikanern und Afroamerikanern auf. Man geht davon aus, dass HbS die Viskosität des Cytoplasmas verändert. Dadurch wird die Infektion mit dem Malariaparasiten Plasmodium falciparum verhindert. In malariagefährdeten Gebieten haben also die heterozygoten Träger des HbS-Allels einen Vorteil. Die heterozygoten Träger (AS) sind unauffällig und benötigen in der Regel keine medizinische Betreuung. Im Stammbaum einer von Sichelzellenanämie betroffe- Abb. 7.16 Autosomal rezessiver Erbgang. Stammbaum einer Familie mit einem seltenen autosomal rezessiv vererbten Merkmal. In dieser Familie ist Verwandtenehe (=) in der fünften Generation dafür verantwortlich, dass das Individuum VI-4 homozygot für ein rezessives Allel ist. Das Allel ist höchstwahrscheinlich durch Spontanmutation in einem der beiden Eltern (I-1, I-2) in der ersten erfassten Generation entstanden. Auch wenn ein Merkmal selten ist, kommt es natürlich vor, dass auch bei Heirat mit einem nicht verwandten Überträger (V-4) homozygote Individuen entstehen (VI-6 und VI-9). Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 7 284 285 nen Familie wird offenbar, dass die Eltern der Merkmalsträger nicht betroffen sind. Es ist typisch für rezessive Allele, dass sie unvorhersehbar auftreten. Sie können über mehrere Generationen durch nicht betroffene sogenannte Überträger (Konduktoren) weitergegeben werden (Abb. 7.16). Erst bei der Heirat zwischen zwei Überträgern wird das Merkmal im Phänotyp ihrer Kinder sichtbar. Dabei sind nach den Mendel-Regeln 25 % Betroffene (SS), 50 % Überträger (AS) und 25 % gesunde Individuen (AA) zu erwarten. Wie beim autosomal dominanten Erbgang sind auch beim autosomal rezessiven Erbgang beide Geschlechter gleichermaßen betroffen, und das Allel wird von beiden Geschlechtern weiter vererbt. Treten seltene autosomal rezessiv vererbte Merkmale im Phänotyp auf, spielt oft Verwandtenehe (Konsanguinität) eine Rolle. Das Allel ist wahrscheinlich in einem gemeinsamen Vorfahren entstanden. 7.7.3 X-Chromosom-gebundene Vererbung Sowohl Y-Chromosom-gebundene Merkmale als auch dominante an das X-Chromosom gebundene Merkmale sind sehr selten, so dass auf eine Darstellung hier verzichtet wird. Wichtig sind dagegen rezessive Merkmale, die vom X-Chromosom kontrolliert werden. Dazu gehören die Rot-Grün-Blindheit, das Lesh-NyhanSyndrom (Störung im Purinstoffwechsel), zwei Formen der Hämophilie (Bluterkrankheit) und die Duchenne-Muskeldystrophie (DMD). Die sogenannte Hämophilie A ist bei Angehörigen europäischer Königshäuser häufig und wahrscheinlich auf eine Spontanmutation bei einem der Eltern von Königin Viktoria zurückzuführen. DMD ist eine Erkrankung mit voller Penetranz, die Jungen mit einer Häufigkeit von 1 zu 3 500 bis 4000 betrifft. Die Krankheit ist durch fortschreitenden Verfall der Muskulatur gekennzeichnet und beginnt sich zu zeigen, wenn die Jungen ein Alter von etwa sechs Jahren erreicht haben. Wenige Erkrankte werden älter als 20 Jahre. Wenn – wie im Fall der DMD – das Allel nicht häufig ist, sind weitaus mehr männliche als weibliche Individuen betroffen. Im Stammbaum (Abb. 7.17) ist keine erkrankte Frau zu finden, aber fünf betroffene männliche Individuen. Diese sind hemizygot für das Krankheitsallel. Es gibt in keinem Fall eine Übertragung des Krankheitsallels vom Vater auf die Söhne. Im Fall der DMD sind die männlichen Individuen steril. Bei weniger schwer wiegenden X-chromosomal vererbten Krankheiten wie der Rot-Grün-Blindheit haben die betroffenen Männer bei einer Heirat mit einer Nicht-Überträgerin nur gesunde Söhne. Alle Töchter erkrankter Männer sind jedoch Überträgerinnen. Bei der Heirat zwischen einer Überträgerin und einem gesunden Mann haben die Söhne der Überträgerinnen eine 50 %ige Chance, das Krankheitsallel zu bekommen. Die Töchter aus einer Heirat zwischen einer Überträgerin und einem gesunden Mann sind nicht betroffen, aber 50 % von ihnen sind wieder Überträgerinnen. Da Überträgerinnen erst erkannt werden, wenn unter ihren Nachkommen wieder betroffene männliche Individuen auftreten, kann über den Status von Frauen in manchen Linien des Stammbaums keine Aussage gemacht werden. Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 7.7 Stammbaumanalyse 7 7 Formalgenetik 7 Abb. 7.17 X-chromosomal-gebundener Erbgang. Stammbaum einer Familie mit Duchenne-Muskeldystrophie, eine X-chromosomal rezessiv vererbte Krankheit. Die Überträgerinnen (Konduktorinnen) (I-1, II-3, II-9, III-7 und IV-14) geben das Krankheitsallel an die Hälfte ihrer Söhne weiter. autosomal dominante Erbgänge: Beispiele: Retinoblastom, Neurofibromatose, familiäre Hypercholesterolämie. autosomal rezessive Erbgänge: Beispiele: Adenosindeaminasedefizienz, Zystische Fibrose (Mukoviszidose), Sichelzellenanämie. Konduktor: Nicht erkrankter Überträger eines krank machenden rezessiven Allels. heterosomal rezessive Erbgänge: Beispiele: Rot-Grün-Blindheit, Lesh-NyhanSyndrom (Störung im Purinstoffwechsel), Hämophilie, Duchenne-Muskeldystrophie. 7.8 Formalgenetik bei haploiden Organismen Organismen, die in ihrem vegetativen Lebenszyklus nur einen haploiden Chromosomensatz besitzen, eignen sich recht gut für genetische Experimente, da jedes Allel im Phänotyp ausgeprägt ist. Da jedes Allel im Phänotyp ausgeprägt ist, kann man bei haploiden Organismen naturgemäß nicht von Homo- oder Heterozygotie sprechen. Insbesondere haploide Ascomyceten wurden gerne für Kreuzungsexperimente herangezogen Mikrobiologie). Ihr Vorteil liegt darin, dass die aus der Meiose hervorgehen( den Zellen, die Ascosporen, als eine Reihe von haploiden Zellen in einem sack- Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 286