Infektionen durch Staphylococcus aureus
Werbung

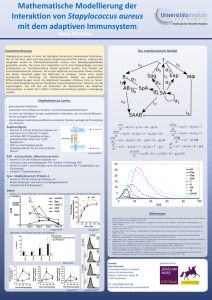
Infektiologie © 2008 65 Schattauer GmbH Infektionen durch Staphylococcus aureus − verändert sich das Krankheitsspektrum? Fabian Lander, Reinhard Berner Zentrum für Kinder- und Jugendmedizin des Universitätsklinikums Freiburg (Ärztlicher Direktor: Prof. Dr. med. Andrea Superti-Furga) Schlüsselwörter Keywords Staphylococcus aureus, Infektionskrankheiten, Antibiotika-Therapie Staphylococcus aureus, infectious diseases, antibiotic treatment Zusammenfassung Summary Das grampositive Bakterium Staphylococcus aureus ist auch im Kindes- und Jugendalter ein wichtiger Infektionserreger. Die häufigsten Erkrankungen sind eitrige Hautund Weichteilinfektionen. Weitere dem Erreger zugeordnete, invasive Krankheitsbilder sind Pneumonien, Endokarditiden, Osteomyelitiden sowie Toxin-vermittelte Syndrome. Während manche Infektionen wie beispielsweise die Osteomyelitis an Häufigkeit abzunehmen scheinen, mehren sich Berichte über neuartige Krankheitsentitäten assoziiert mit hoch virulenten, im ambulanten Bereich erworbenen S. aureus-Stämmen. Ein aktuelles Beispiel hierfür ist die nekrotisierende, hämorrhagische Pneumonie, die bei immunkompetenten Patienten auftritt und aus unverstandenen Gründen bevorzugt Kinder und Jugendliche betrifft. Auch das bisher fast ausschließlich mit einer fulminanten Meningokokken-Infektion assoziierte Waterhouse-FriderichsenSyndrom kann durch S. aureus verursacht werden. In der Behandlung von S. aureus-Infektionen werden vorzugsweise Betalaktam-Antibiotika wie penicillinasefeste Penicilline, Aminopenicilline in Kombination mit Betalaktamase-Inhibitoren oder staphylokokkenwirksame Cephalosporine verwendet. Daneben kommen je nach Krankheitsbild und Resistenzlage eine Anzahl weiterer Antibiotika unterschiedlicher Stoffklassen zur Anwendung. A ls Verursacher eitriger Infektionen beim Menschen ist Staphylococcus aureus (S. aureus) ein „alter Bekannter“. Die Erstbeschreibung erfolgte vor mehr als 125 Jahren durch den schottischen Arzt Sir Alexander Ogston (1844–1929) (15). Er beschrieb in Haufen zusammenliegende „Micrococcen“ als Erreger vonAbszessen, die er aufgrund ihrer kugeligen Form und traubenförmigen Anordnung im mikroskopischen Präparat sowie der goldenen Koloniefärbung auf Blutagar „Staphylococcus aureus“ nannte. Im Gegensatz zu dem in der Antike und im Mittelalter vorherrschenden, durch Galen ge- S. aureus is an important pathogen in childhood and adolescene. Most frequently it causes pyogenic skin and soft tissue infections. Other diseases associated with this microorganism include pneumonia, endocarditis, osteomyelitis as well as toxin mediated syndromes. While the incidence of some infections, osteomyelitis for instance, appears to decrease, reports on novel disease entities associated with highly virulent S. aureus strains are on the rise. One example is the necrotizing, hemorrhagic pneumonia occuring in immunocompetent patients and especially affecting children and adolescents. Another one is the Waterhouse-Friderichsen syndrome formerly associated almost exclusively with severe meningococci infection that can be caused by S. aureus as well. The treatment relies mainly on betalactame-antibiotics such as penicilinase-resistant penicillins, aminopenicillins in combination with betalactamase inhibitors or cephalosporins active against S. aureus. Depending on clinical picture and resistance situation a number of other antibiotics from different substance classes may be used. Infections caused by Staphylococcus aureus – new diseases on the rise? Kinder- und Jugendmedizin 2008; 8: 65–71 prägten Konzept des „pus bonum et laudabile“, wonach Eiter ein wichtiger Bestandteil der normalen Wundheilung war, konnte Ogston demonstrieren, dass sich durch die im Eiter enthaltenen Bakterien abszedierende Infektionen übertragen ließen. Bis heute haben Staphylokokken nichts von ihrer klinischen Relevanzeingebüsst.DerErregerverursachtvorallem eitrige Infektionen, die meist lokal begrenzt bleiben, aber das Potenzial einer hämatogenenAusbreitungbesitzen.Danebengibtes eine Reihe schwerer invasiver sowie toxischer Krankheitsbilder, die durch S. aureus verursacht werden. In letzter Zeit sind zwei neue Aspekte in den Mittelpunkt getreten. Einerseits wird eine sich dramatisch verschlechternde Resistenzlage beobachtet: In zunehmender Häufigkeit werden auch bei im ambulanten Bereich aufgetretenen Infektionen Methicillinresistente S. aureus (MRSA)-Stämme isoliert (7). Vor allem aus den USA gibt es alarmierende Daten, die eine zunehmende Prävalenz von MRSA in pädiatrischen Kollektiven dokumentieren (4, 20). Auch in Deutschland wird eine Zunahme an MRSA-Isolaten berichtet (19). Bei Kindern scheint sich dieser Trend bislang noch nicht umzusetzen (9). Es muss allerdings befürchtet werden, dass diese Entwicklung in den kommenden Jahren vor der Pädiatrie nicht halt machen wird. Andererseits scheint sich das Spektrum gerade der schwerwiegenden Staphylokokken-Infektionen zu verändern. Es mehren sich besorgniserregende Berichte über neuartige invasive Erkrankungen, ausgelöst durch hoch virulente S. aureus-Stämme. Ein Beispiel ist die nekrotisierende, hämorrhagische Pneumonie, die aus unverstandenen Gründen vor allem bei ansonsten immunkompetenten Kindern und Jugendlichen auftritt (10, 13). Auch Krankheitsbilder wie das WaterhouseFriderichsen-Syndrom oder die nekrotisierende Fasziitis, die bisher nicht oder nur sehr selten mit S. aureus in Verbindung gebracht wurden, können durch diese neuartigen Stämme verursacht werden (1). In Deutschland sind diese Erkrankungen bisher glücklicherweise Raritäten; Einzelfallberichte nehmen jedoch zu. Daneben scheinen in Deutschland in den letzten beiden Jahrzehnten invasive S. aureus-Infektionen bei Kindern mit klassischen Kranheitsbildern insgesamt deutlich seltener geworden zu sein. Insbesondere eine früher pathognomonische S. aureus-Erkrankung, die akute hämatogene Osteomyelitis des Kindesalters, verliert zahlenmäßig an Bedeutung. Downloaded from www.kinder-und-jugendmedizin-online.de on 2017-08-22 | IP: 88.99.70.242 Eingegangen: 5. Oktober 2007; angenommen: 9.For Oktober 2007 personal or educational use only. No other uses without permission. All rights reserved. Kinder- und Jugendmedizin 2/2008 66 Lander, Berner Tab. 1 Empfohlene Dosierungen ausgewählter Staphylokokken-wirksamer Antibiotika und Chemotherapeutika Medikament Applikation Dosen pro Tag Dosierung pro kg KG und Tag maximale Tagesdosis i. v. 4–6 100 000–200 000 24 Mio. E. i. v., p. o. 3–4 100 (–200) mg 8g Penicilline Penicillin G penicillinasefeste Penicilline Flucloxacillin enzymgeschützte Penicilline (Kombination mit Betalaktamase-Inhibitoren) Ampicillin/Sulbactam i. v. 3–4 Amoxicillin/Clavulansäure p. o. 2–3 Piperacillin/Tazobactam i. v. 3–4 150 mg 50 mg 12 g 3,75 g 250–300 mg 18 g Carbapeneme und Monobactame Imipenem i. v. 4 40–60 mg 4g Meropenem i. v. 3 60 mg 6g (bei Meningitis) i. v. 3 120 mg parenterale Cephalosporine Cefazolin i. v. 3 50–100 (–150) mg Cefamandol i. v. 3–4 75–100 mg Cefotiam i. v. 3 60–100 (–150) mg 6g Cefuroxim i. v. 3 75–150 mg 6g Cefalexin p. o. 4 50–100 mg 4g Cefadroxil p. o. 2 50–100 mg 4g Cefaclor p. o. 3 40–60 (–100) mg 4g Loracarbef p. o. 2 15–30 mg 0,8 g Cefuroxim p. o. 2–3 20–30 mg 1g p. o., i. v. 3 20 (–40) mg 2,4 g Vancomycin i. v. 3 20–40 mg Teicoplanin i. v. 1 initial 20 mg, dann 10 mg 2 8 mg TMP/40 mg SMZ 150 (–300) mg 6g 12 g Oralcephalosporine Lincosamide Clindamycin Glykopeptide 0,8 Folsäureantagonisten Trimethroprim/Sulfamethoxazol i. v., p. o. (TMP/SMZ) Antibiotika unterschiedlicher Stoffklassen Fosfomycin i. v. 3 Rifampicin i. v., p. o. 1–2 10–20 mg Linezolid (Kinder >12 Jahre) i. v., p. o. 2 20 mg Linezolid (Kinder <12 Jahre) i. v., p. o. 3 30 mg Im Folgenden sollen wesentliche durch S. aureus verursachte Krankheitsbilder dargestellt sowie die antimikrobielle Behandlung kurz skizziert werden. In Tabelle 1 werden die für die Pädiatrie empfohlenen Dosierungen der gebräuchlichsten Antibiotika und Chemotherapeutika erläutert. Kinder- und Jugendmedizin 2/2008 20 g 0,6 g Oberflächliche Hautinfektionen Eitrige Infektionen der Haut sind die häufigsten von S. aureus verursachten Erkrankungen. Die klinische Präsentation ist vielfältig und reicht von einer Follikulitis über Furunkel- und Karbunkelbildung bis hin zur Entstehung größerer konfluierender Abszesse (6, 16) (Abb. 1, 2). Die Tendenz einer lokalen Ausbreitung der Erkrankung ist im Gegensatz zu Infektionen mit Streptokokken eher gering. Komplikationen entstehen meist durch Einbruch des Erregers in den Blutstrom und durch die Folgen der Bakteriämie, die zu einer hämatogenen Absiedelung des Erregers im Körper führen können. Eintrittspforte für eitrige Hautinfektionen sind kutane (Mikro-)Verletzungen wie Kratzer, Stiche oder Mazerationen sowie präformierte anatomische Strukturen wie beispielsweise die Haarfollikel. Prädisponierende Faktoren sind mangelnde Hygiene, Diabetes mellitus, eine atopische Diathese und Abwehrschwäche (siehe Beitrag von Bernuth H, Ehl S). Therapeutisch ist die Sanierung des Eiterherdes von entscheidender Bedeutung. Nur bei gering ausgeprägten pustulösen Infektionen ist eine lokale antiseptische Behandlung ausreichend. Abszesse müssen adäquat drainiert werden („Ubi pus ibi evacua“). Inwiefern eine alleinige chirurgische Therapie bei sonst unbeeinträchtigten, gesunden Patienten ausreichend sein kann, wird in der Literatur kontrovers dikutiert (14, 17). Bei ausgedehnteren Befunden ist im Regelfall eine zumindest orale, staphylokokkenwirksame Behandlung erforderlich. Hier bieten sich orale Cephalosporine der ersten Generation (z. B. Cefadroxil) mit einer hohen oralen Bioverfügbarkeit und guten Staphylokokken-Wirksamkeit an. Auch Clindamycin stellt eine Behandlungsoption dar, allerdings muss mit einer Resistenzrate von 10% und mehr gerechnet werden, sodass die Clindamycin-Empfindlichkeit des Isolats im Labor bestätigt sein muss. Aufgrund hoher Resistenzraten sind Makrolide heute nicht mehr als primäre Therapeutika zu empfehlen. Ein kleinerer Prozentsatz von S. aureus-Isolaten ist auch heute noch Penicillin-empfindlich; bei entsprechendem Nachweis bietet sich eine „einfache“ Penicillin-Therapie aufgrund der außerordentlich guten Wirksamkeit an. Auf eine lokale Antibiotikatherapie, z. B. mit Mupirocin, sollte verzichtet werden, da dies für die Sanierung von MRSA-Trägerschaft reserviert bleiben sollte. Eine vor allem Säuglinge und Kleinkinder betreffende Form der oberflächlichen Sta- Downloaded from www.kinder-und-jugendmedizin-online.de on 2017-08-22 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. 67 Infektionen durch Staphylococcus aureus phylokokkeninfektionen stellt die Impetigo contagiosa dar (Abb. 3, 4). Während die häufigere kleinblasige Impetigo durch ß-hämolysierende Streptokokken der GruppeA (Streptococcus pyogenes) hervorgerufen wird, verursacht S. aureus eine großblasige Form der Erkrankung, die bullöse Impetigo contagiosa. Pathogenetisch spielt dabei, insbesondere was die Blasenbildung angeht, die Bildung von Exfoliativtoxinen eine Rolle. S. aureus zerstört die epidermale Barriere durch die Produktion von Ceramidasen, Destruktion von Desmogleinen, Zerstörung von Keratinozyten und Abbau bzw. Inhibition antimikrobieller Peptide. Der Erreger vermag so das Stratum corneum zu penetrieren und somit in und durch die Epidermis hindurch zu gelangen. Klinisch zeigen die Patienten zunächst ein makulopapulöses Exanthem, auf dessen Boden sich bis zu 1–2 cm große, gelegentlich auch größere, rasch rupturierende Blasen bilden. Die Vesikel sind zunächst klar und trüben sekundär ein. Von wenigen Ausnahmefällen mit sehr begrenzten Hautläsionen abgesehen, sollte immer eine orale antimikrobielle Therapie erfolgen, schon allein, weil eine Mischinfektion mit Streptokokken meist nicht sicher ausgeschlossen werden kann. Zusätzlich kommen topische Antiseptika zur Anwendung. Auf lokale Antibiotika sollte verzichtet werden. Abb. 1 Furunkel der Bauchhaut Tiefere Hautund Weichteilinfektionen Während die meisten Hautinfektionen durch S. aureus oberflächlich verlaufen und lokal begrenzt bleiben, kommt es in seltenen Fällen zur regionären Ausbreitung. Bei der Phlegmone, im englischen Sprachgebrauch als „Cellulitis“ bezeichnet, handelt es sich um eineWeichteilinfektion im Bereich der tieferen Dermis und des subkutanen Fettgewebes. Klinisch imponiert die Erkrankung durch eine diffuse, ödematöse, druckschmerzhafte Schwellung und eine − in Abgrenzung zum vorwiegend durch Streptococcus pyogenes verursachten Erysipel − unscharf begrenzte Rötung. Die Infektion wird meist von Fieber undAbgeschlagenheit begleitet. Die Behandlung muss initial parenteral erfolgen, um hohe Wirkspiegel zu sichern und eine weitereAusbreitung zu unterbinden. Zur an- Abb. 2 Abszess im Bereich der Oberlippe tibiotischen Therapie können penicillinasefeste Penicilline wie Flucloxacillin, Betalaktamasegeschützte Aminopenicilline wie Amoxicillin plus Clavulansäure oder staphylokokkenwirksame Cephalosporine wie Cefazolin, Cefotiam oder Cefuroxim eingesetzt werden. Die schwerste Form der Weichteilinfektion durch S. aureus stellt die (tropische) Pyomyositis dar (8, 18). In tropischen Ländern ist diese Erkrankung häufig und betrifft vor allem gesunde Kinder und junge Erwachsene. In gemäßigten Breiten ist die Erkrankung we- Downloaded from www.kinder-und-jugendmedizin-online.de on 2017-08-22 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. Kinder- und Jugendmedizin 2/2008 68 Lander, Berner Abb. 3 Impetigo contagiosa Abb. 4 sentlich seltener mit jedoch zunehmender Häufigkeit und kommt vor allem bei immunkompromittierten erwachsenen Patienten, insbesondere bei HIV-Infizierten vor. Die Infektion des Muskels erfolgt hämatogen. Häufig geht eine Vorschädigung des Muskelgewebes durch ein Trauma oder starke körperliche Belastung voraus. Prinzipiell kann jeder Skelettmuskel betroffen werden, meist jedoch ist eine einzelne Muskelgruppe der unteren Extremität infiziert. Dabei kommt es zunächst zu Fieber und einer schmerzhaften Verhärtung im Bereich des Muskels. Eine begleitende Hautrötung kann bei tiefem Sitz der Infektion fehlen. Ab der zweiten Krankheitswoche kommt es zur Abszessbildung begleitet von hohem Fieber. Diagnostisch wegweiKinder- und Jugendmedizin 2/2008 Impetigo contagiosa auf dem Boden einer Neurodermitis send sind erhöhte Infektparameter mit beschleunigter Blutsenkung, Leukozytose und hohem CRP sowie bildgebende Verfahren. Sichern lässt sich die Diagnose durch eine Nadelaspiration von Eiter. Die Behandlung besteht aus chirurgischem Débridment und parenteraler antimikrobieller Therapie. Untere Atemwegsinfektionen Primäre Pneumonien durch S. aureus treten vor allem im frühen Säuglingsalter auf, sind jedoch in den letzten Jahren extrem selten geworden. Klinisch zeichnen sich diese Lungenentzündungen durch einen raschen Verlauf aus. Eine meist nur kurze fieberhafte Prodromalphase wird gefolgt von einer sich schnell verschlechternden respiratorischen Symptomatik mit Stöhnen,Tachydyspnoe und eventuell Zyanose. Initiale Röntgenaufnahmen können durchaus noch unauffällig sein. Im späteren Stadium zeigen sich charakteristische häufig einseitige pulmonale Infiltrate, die sehr oft von Pleuraergüssen begleitet sind. In ungefähr einem Drittel der Fälle sind die Blutkulturen positiv. Häufige Komplikationen sind die Bildung von Pneumatozelen oder das Auftreten eines Pneumothorax. Aufgrund der Gefahr eines foudroyanten Verlaufs müssen Kinder mit Verdacht auf Staphylokokken-Pneumonie stationär betreut und parenteral antimikrobiell behandelt werden. Bei jungen Säuglingen wird Downloaded from www.kinder-und-jugendmedizin-online.de on 2017-08-22 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. 69 Infektionen durch Staphylococcus aureus dem in der Primärbehandlung der Pneumonie mit staphylokokkenwirksamen Antibiotika Rechnung getragen. Eine gefürchtete, häufig letale Komplikation einer Influenzavirus-Infektion ist die nekrotisierende Pneumonie durch S. aureus bereits in den ersten Krankheitstagen. Neben diesem schon lange bekannten Krankheitsbild sind in den letzten Jahren Berichte erschienen, die eine neue Form der Lungenentzündung durch S. aureus beschreiben, die so genannte diffuse, nekrotisierende, hämorrhagische Pneumonie (10, 13). Sie tritt aus ungeklärten Gründen bei älteren sonst gesunden, immunkompetenten Kindern und Jugendlichen ohne spezielle Risikofaktoren für eine S. aureus-Infektion auf.Verursacht wird die Erkrankung durch ambulant erworbene MRSA-Stämme, die das Exotoxin Panton-Valentine-Leukozidin (PVL) exprimieren. Die Erkrankung beginnt oft mit einem wenige Tage anhaltenden grippeähnlichen Prodromalstadium. Danach kommt es zu einer akuten Verschlechterung mit hohem Fieber, Hämoptysis und Leukopenie. Rasch kommt es zum respiratorischenVersagen und zur Kreislaufinsuffizienz. Histopathologisch verursacht die Infektion ausgedehnte Ulzerationen der trachealen und bronchialen Schleimhaut sowie hämorrhagische Nekrosen der interalveolären Septen. Die Therapie besteht aus einem aggressiven antimikrobiellen und intensivmedizinischen Management. Dennoch ist die Letalität auch bei optimaler Therapie mit bis zu 56% sehr hoch. Ungünstige prognostische Faktoren sind dasAuftreten von pulmonalen Blutungen, einer Eythrodermie und einer Leukopenie (11). Aufgrund der besseren Gewebegängigkeit sollte hier dem Linezolid vor Vancomycin der Vorzug gegeben werden. Bei nachgewiesener Empfindlichkeit kann auch Clindamycin und/oder Rifampicin eingesetzt werden. Bakteriämie und Sepsis Alle Formen von Infektionen durch S. aureus können durch eine hämatogene Streuung zur Bakteriämie und schließlich zur Absiedelung in prinzipiell allen Körperregionen führen.Typische Komplikationen der S. aureus-Bakteri- ämie sind Endokarditis, Organ- oder Weichteilabszesse, eine septische Arthritis oder Osteomyelitis. Diese scheinen bei Kindern jedoch seltener aufzutreten als bei Erwachsenen (5). S. aureus ist einer der häufigsten Erreger einer grampositiven Sepsis, dennoch entwickelt glücklicherweise nur eine Minderheit der Patienten mit S. aureus-Bakteriämie eine Sepsis. In den letzten Jahren mehren sich jedoch die Berichte über schwere durch S. aureus verursachte Septitiden mit Kreislaufinsuffizienz und Multiorganversagen, die sich klinisch nur wenig vom Bild einer gramnegativen Sepsis unterscheiden (12). Auch das bisher fast ausschließlich mit einer fulminanten Meningokokken-Infektion assoziierteVollbild eines Waterhouse-Friderichsen-Syndroms kann durch S. aureus ausgelöst werden (1). Dieses Krankheitsbild ist klinisch gekennzeichnet durch eine Gerinnungsstörung mit Petechien, flächigen Hautblutungen sowie disseminierter intravasaler Gerinnung. Daneben treten Multiorganversagen, metabolische Azidose und eine schwere Kreislaufinsuffizienz auf. Hämatologisch zeigt sich eine ausgeprägte Leuko- und Neutropenie. In der Autopsie findet sich die pathognomonische bilaterale Nebennierenblutung. Die Letalität der schweren S. aureus-Sepsis ist trotz aggressiver intensivmedizinischer Maßnahmen und effektiver antibiotischerTherapie sehr hoch. Die antibiotische Therapie sollte nach Empfehlungen der Paul-Ehrlich-Gesellschaft aus Linezolid oder einem Glykopeptid in Kombination mit Rifampicin oder Fosfomycin (oder Cotrimoxazol) erfolgen, wobei der Einsatz von Rifampicin, Fosfomycin oder Cotrimoxazol bei Nachweis von MRSA stets erst nach Vorliegen des Antibiogramms erfolgen sollte. Endokarditis Im Unterschied zu anderen EndokarditisErregern, die einen subakuten Verlauf verursachen, zeigt sich S. aureus virulenter und führt typischerweise zu einem raschen Erkrankungsbeginn mit hohem Fieber und einem schnelleren Verlauf, der unter Umständen binnen weniger Tage zu einer Destruktion der Herzklappe mit konsekutiver Herzinsuffizienz führen kann. Die Erkrankung betrifft überwiegend das linke Herz und dort vorwiegend die Mitralklappe. Nur im Fall von Endokarditiden, die mit intravenösem Drogenmissbrauch assoziiert sind, ist häufiger das rechte Herz betroffen. Charakteristisch für die durch S. aureus verursachte akute Endokarditis sind hohes Fieber und ein schweres, rasch progredientes Krankheitsbild. Diagnostisch wegweisend, aber nicht immer auftretend, ist ein neues oder verändertes Herzgeräusch. Weitere, allerdings selten anzutreffende, klinische Zeichen sind Osler-Knötchen oder andere periphere durch septische Embolien bedingte Hautläsionen. Komplikationen sind die Herzinsuffizienz infolge Klappenzerstörung, Myokarditis, Perikarditis, Myokardabszesse und embolische Herzinfarkte. Klappenringabszesse können Überleitungsstörungen nach sich ziehen. Extrakardiale Manifestationen sind häufig und entstehen durch septische Embolien oder durch Absiedelung im Rahmen der Bakteriämie. Gesichert wird die Erkrankung durch den Nachweis des Erregers in Blutkulturen sowie die Darstellung von valvulären Vegetationen in der Echokardiografie, die im Zweifelsfall auch transösophageal durchgeführt werden muss. Prädisponierende Faktoren sind vor allem Herzfehler: Dabei gehen zyanotische Herzvitien, Zustand nach Implantation einer Herzklappe, eines Konduits oder Anlage eines Shunts mit einem besonders hohen Risiko einher. Eine überstandene mikrobielle Endokarditis in der Vorgeschichte stellt ebenfalls ein hohes Risiko dar. Daneben prädisponieren alle Faktoren, die eine S. aureus-Bakteriämie begünstigen, wie intravenöse Katheter oder vorhergehende S. aureus-Infektionen. Die Therapie erfolgt durch eine langfristige, mindestens sechs Wochen andauernde intravenöse Antibiotika-Behandlung. Hier wird üblicherweise ein penicillinasefestes Penicillin (z. B. Flucloxacillin) oder ein staphylokokkenwirksames Cephalosporin eingesetzt und mit einem Aminoglykosid kombiniert. Je nachAusmaß der Klappenschädigung und der Vegetationen kann ein kardiochirurgischer Eingriff notwendig werden. Bei der Endokarditis durch S. aureus müssen auch nach Beginn der antibiotischen Therapie so lange Blutkulturen entnommen werden, bis der Beweis der „Sterilisierung“ des Blutstroms erbracht ist. Downloaded from www.kinder-und-jugendmedizin-online.de on 2017-08-22 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. Kinder- und Jugendmedizin 2/2008 70 Lander, Berner Osteomyelitis Die akute,hämatogene Osteomyelitis ist eine seltene Erkrankung vorwiegend des Kindesalters. Angaben zur Inzidenz sind lokal unterschiedlich und schwanken zwischen 2,9 und 20 Fällen pro 100 000 und Jahr. Insgesamt lässt sich eine deutlich rückläufige Tendenz der Erkrankungshäufigkeit in den letzten Jahren ausmachen (2). Jungen sind etwa doppelt so häufig betroffen wie Mädchen. S. aureus ist der häufigste Erreger; jenseits des Säuglingsalters verursacht er 70–95% der akuten Ostoemyelitiden. Die akute Osteomyelitis ist definiert mit einem Krankheitsverlauf von weniger als zwei Wochen. Sie manifestiert sich vor allem an der unteren Extremität und dort vorwiegend in den Metaphysen der langen Röhrenknochen. Die Symptomatik ist zum einen geprägt von unterschiedlich stark ausgebildeten Allgemeinsymptomen, wie Fieber, Abgeschlagenheit bis hin zu einem sepsisähnlichen Krankheitsbild. Zum anderen zeigen sich lokale Entzündungszeichen mit Druckdolenz, schmerzhafter Bewegungseinschränkung, Schwellung und Rötung. Unbehandelt schreitet die Infektion mit Bildung eines subperiostalen Abszesses und Übergreifen auf dieWeichteile fort. Bei jungen Säuglingen verläuft die Symptomatik subtiler mit dem Bild der Pseudoparalyse. Fieber kann fehlen. Häufig sind die Gelenke mitbetroffen, da die Erkrankung in diesem Alter noch über die Epiphysenfugen hinweg greifen kann. Diagnostisch zeigt sich neben dem klinischen Bild eine Erhöhung der Infektparameter mit Leukozytose, Linksverschiebung, CRP-Erhöhung und insbesondere erhöhter Blutsenkung. Der für die Therapieplanung unbedingt anzustrebende Erregernachweis erfolgt aus Blutkulturen. Dies gelingt in 30–50% der Fälle, weshalb eine wiederholte Abnahme zur Erhöhung der Sensitivität obligat ist. Bei Vorliegen einesGelenkergussessolltedieserausdiagnostischen und therapeutischen Gründen punktiert werden. Auch bei subperiostalen oder intraossären Abszessen sollte durch Punktion der Erregernachweis angestrebt werden. Die primäre Therapie besteht in einer rasch eingeleiteten intravenösen hoch dosiertenAntibiotikabehandlung. Dabei ist wichtig, dass die Gewebegängigkeit der eingesetzten Antibiotika berücksichtigt wird, um ausreichende Wirkspiegel im Knochen zu erreichen. Für die paKinder- und Jugendmedizin 2/2008 renterale Therapie werden wiederum penicillinasefeste Penicilline wie Flucloxacillin oder staphylokokkenwirksame Cephalosporine eingesetzt.Antibiotika wie Fosfomycin bieten sich aufgrundihrermikrobiologischenundpharmakokinetischen Eigenschaften für den Einsatz bei Knocheninfektion an. Valide Daten aus kontrollierten klinischen Studien fehlen jedoch. Ebenfalls aus pharmakokinetischen Gründen ist Clindamycin ein günstiges MedikamentzurBehandlungvonKnochen-undGelenkinfektionen, allerdings muss aus den oben genannten Gründen zum Teil hoher Resistenzraten die Empfindlichkeit des Isolats im Labor nachgewiesen sein. Für die orale Therapie bieten sich Clindamycin oder Oralcephalosporine mit hoher Bioverfügbarkeit wie Cefadroxil an. Die Frage des Zeitpunkts der Umstellung einer primär parenteralen auf eine orale antibiotische Therapiewirdkontroversbeurteiltundmussim Einzelfall entschieden werden. Voraussetzung sind in jedem Fall das gute klinische Ansprechen und ein komplikationsloser Verlauf. Hier kann möglicherweise bereits nach ein bis zwei Wochen auf eine oraleTherapie umgesetzt werden. Chirurgische Eingriffe sind indiziert, wenn initial bereits zusätzliche Komplikationen wie Abszesse, Knochennekrosen oder Fistelnvorliegen.DiePrognosefüreinevollständige Heilung ist gut, insbesondere bei frühzeitiger Diagnosestellung und adäquater Therapie. Hauptsächliche Spätkomplikationen sind Wachstumsstörungen nach Befall der Wachstumsfuge im jungen Säuglingsalter. Toxin-vermittelte Erkrankungen S. aureus kann eine Reihe von Exotoxinen produzieren, die eigenständige Krankheitsbilder verursachen können. Das selteneToxic Shock Syndrome (TSS) wird durch das von bestimmten S. aureus-Stämmen produzierte Toxic-Shock-Syndrome-Toxin-1 (TSST-1) ausgelöst (3). Häufig ist die Quelle derToxinBildung eher eine Kolonisation als eine Infektion. In der Mehrzahl der Fälle ist das Krankheitsbild mit der Verwendung von Tampons während der Menstruation assoziiert. Das Toxic-Shock-Syndrome-Toxin agiert als so genanntes Superantigen und kann durch unspezifische Bindung an Klasse-II-MHC-MoleküleT-Zellen direkt aktivie- ren. Die Folge ist eine massive Stimulation von T-Zellen und Makrophagen, die zur Freisetzung großer Mengen an proinflammatorischen Zytokinen und letztlich zu einer fulminanten systemischen Inflammationsreaktion (SIRS) führt. Klinisch spiegelt sich diese Entzündungskaskade in einem hoch akuten Krankheitsbeginn mit Fieber, unspezifischen Allgemeinsymptomen und starker Verschlechterung des Allgemeinzustandes wieder. Häufig zeigt sich ein diffuses makuläres Exanthem mit nachfolgender groblamellärer Schuppung. Bereits in der Frühphase kann sich durch ein ausgeprägtes Kapillarleck ein Volumenmangelschock entwickeln. Im weiteren Verlauf entwickelt sich definitionsgemäß ein Multiorganversagen. Die Behandlung erfordert neben intensivmedizinischem Management eine staphylokokkenwirksame antibiotische Therapie. Hier wird aus theoretischen Überlegungen der Einsatz von Clindamycin in Kombination mit einem Betalaktam-Antibiotikum empfohlen. Da Clindamycin die Proteinbiosynthese hemmt, erhofft man sich eine unterdrückende Wirkung auf die Toxinprodukion des Erregers. Des Weiteren werden häufig intravenöse Immunglobuline eingesetzt, in der Vorstellung, damit die Superantigene zu neutralisieren. Eine weitere Toxin-vermittelte Staphylokokken-Erkrankung ist das Staphylococcal Scalded Skin Syndrome (SSSS). Die generalisiserte Form im Säuglingsalter wird auch Dermatitis exfoliativa neonatorum oder Morbus Ritter von Rittershain genannt (Abb. 5). Betroffen sind vor allem junge Säuglinge; Erkrankungen jenseits des Kleinkindesalters sind eine Rarität. Durch zwei Exfoliativtoxine (A und B), die eine intraepidermale Spaltbildung hervorrufen, kommt es zunächst zu einem generalisierten makulösen Exanthem und im weiteren Verlauf innerhalb von 1–3 Tagen zur Bildung von schlaffen Blasen, die sehr leicht aufreißen. Bereits durch leichtes Bestreichen lassen sich Hautfetzen ablösen (positives Nikolski-Zeichen). Klinisch ähnelt das Bild einer Verbrühung. Allgemeinsymptome können vorhanden sein; oft sind die Kinder aber bei Ausbleiben sekundärer Komplikationen erstaunlich unbeeinträchtigt. Die Heilung ohne Narbenbildung erfolgt binnen zwei Wochen. Die Bildung von Enterotoxinen durch einen großen Anteil der Staphylokokken-Stämme Downloaded from www.kinder-und-jugendmedizin-online.de on 2017-08-22 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. 71 Infektionen durch Staphylococcus aureus Abb. 5 Staphylococcal Scalded Skin Syndrome bei einem jungen Säugling kann zu einer Lebensmittelintoxikation führen. Die am häufigsten vorkommenden Enterotoxine A und B sind sehr hitzeresistent, sodass auch das Abkochen verseuchter Nahrung nicht vor einer Intoxikation schützt. Die Inkubationszeit ist mit ein bis zwei Stunden sehr kurz. Meist setzt die Symptomatik sehr heftig mit rezidivierendem Erbrechen, krampfartigen Bauchschmerzen und profusen, wässrigen Durchfällen ein. Der Verlauf ist in der Regel kurz und selbstlimitierend und eine erregerbezogene Therapie nur in Ausnahmefällen notwendig. Literatur 1. Adem PV, Montgomery CP, Husain AN et al. Staphylococcus aureus sepsis and the WaterhouseFriderichsen syndrome in children. N Engl J Med 2005; 353 (12): 1245–1251. 2. Blyth MJ, Kincaid R, Craigen MA, Bennet GC. The changing epidemiology of acute and subacu- te haematogenous osteomyelitis in children. J Bone Joint Surg Br 2001; 83 (1): 99–102. 3. Chuang YY, Huang YC, Lin TY. Toxic shock syndrome in children: epidemiology, pathogenesis, and management. Paediatr Drugs 2005; 7 (1): 11–25. 4. Collins D, Anderson A, Sexton DJ, Kaye KS. Agerelated variability in the prevalence of community-acquired Methicillin-resistant Staphylococcus aureus Infections, 2000–2005. ICAAC 2006. 5. Denniston S, Riordan FA. Staphylococcus aureus bacteraemia in children and neonates: a 10 year retrospective review. J Infect 2006; 53 (6): 387–393. 6. Deutsche Gesellschaft für Pädiatrische Infektiologie. Handbuch. Infektionen bei Kindern und Jugendlichen. München: Futuramed 2003. 7. Eady EA, Cove JH. Staphylococcal resistance revisited: community-acquired methicillin resistant Staphylococcus aureus − an emerging problem for the management of skin and soft tissue infections. Curr Opin Infect Dis 2003; 16 (2): 103–124. 8. Fan HC, Lo WT, Chu ML, Wang CC. Clinical characteristics of Staphylococcal pyomyositis. J Microbiol Immunol Infect 2002; 35 (2): 121–124. 9. Fluegge K, Adams B, Luetke Volksbeck U et al. Low prevalence of Methicillin-resistant Staphylococcus aureus (MRSA) in a southwestern region of Germany. Eur J Pediat. 2006; 165 (10): 688–90. 10. Gillet Y, Issartel B, Vanhems P et al. Association between Staphylococcus aureus strains carrying gene for Panton-Valentine leukocidin and highly lethal necrotising pneumonia in young immunocompetent patients. Lancet 2002; 359 (9308): 753–759. 11. Gillet Y, Vanhems P, Lina G et al. Factors predicting mortality in necrotizing communityacquired pneumonia caused by Staphylococcus aureus containing Panton-Valentine leukocidin. Clin Infect Dis 2007; 45 (3): 315–321. 12. Gonzalez BE, Martinez-Aguilar G, Hulten KG et al. Severe Staphylococcal sepsis in adolescents in the era of community-acquired Methicillin-resistant Staphylococcus aureus. Pediatrics 2005; 115 (3): 642–648. 13. Labandeira-Rey M, Couzon F, Boisset S et al. Staphylococcus aureus Panton-Valentine leukocidin causes necrotizing pneumonia. Science 2007; 315 (5815): 1130–1133. 14. Lee MC, Rios AM, Aten MF et al. Management and outcome of children with skin and soft tissue abscesses caused by community-acquired methicillin-resistant Staphylococcus aureus. Pediatr Infect Dis J 2004; 23 (2): 123–127. 15. Ogston A. Micrococcus Poisoning. J Anat Physiol 1882; 17: 24–58. 16. Reinhardt D. (Hrsg). Therapie der Krankheiten im Kindes- und Jugendalter. Berlin, Heidelberg, New York: Springer Verlag 2003. 17. Ruhe JJ, Smith N, Bradsher RW, Menon A. Community-onset Methicillin-resistant Staphylococcus aureus skin and soft-tissue infections: impact of antimicrobial therapy on outcome. Clin Infect Dis 2007; 44 (6): 777–784. 18. Skoutelis A, Andonopoulos A, Panagiotopoulos E, Bassaris H. Non-tropical pyomyositis in adults: report of four cases and literature review. Eur J Clin Microbiol Infect Dis 1993; 12 (10): 769–772. 19. Tiemersma EW, Bronzwaer SL, Lyytikainen O et al. European Antimicrobial Resistance Surveillance System Participants. Methicillin-resistant Staphylococcus aureus in Europe, 1999–2002. Emerg Infect Dis 2004; 10 (9): 1627–1634. 20. Zaoutis TE, Toltzis P, Chu J et al. Clinical and molecular epidemiology of community-acquired methicillin-resistant Staphylococcus aureus infections among children with risk factors for health care-associated infection: 2001–2003. Pediatr Infect Dis J 2006; 25 (4): 343–348. Korrespondenzadresse: Fabian Lander Zentrum für Kinder- und Jugendmedizin Pädiatrische Infektiologie und Immunologie Universitätsklinikum Freiburg Mathildenstraße 1 79106 Freiburg Tel.: 07 61/2 70–4480 Fax.: 07 61/2 70–4598 E-Mail: [email protected] Downloaded from www.kinder-und-jugendmedizin-online.de on 2017-08-22 | IP: 88.99.70.242 For personal or educational use only. No other uses without permission. All rights reserved. Kinder- und Jugendmedizin 2/2008