Integrins
Werbung

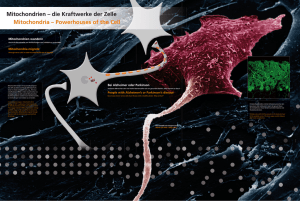
Forschungsabteilung Research Department Molekulare Medizin Aktivierbare Zellanker Molecular Medicine A Switchblade like Signaling Machine for Cells P r o f . D r. R e i n h a r d F ä s s l e r A Prof. Dr. Reinhard Fässler [email protected] www.biochem.mpg.de/faessler lle Zellen des Körpers besitzen Integrine. Diese Proteine durchqueren die Zellmembran und verbinden das Zellinnere mit der Umgebung: das äußere Ende des Integrins vermittelt die Anheftung der Zelle an die extrazelluläre Matrix (Proteingeflecht außerhalb der Zellen). Das andere Ende des Integrins verbindet das Zellskelett mit der Zellmembran. Integrine können sich wie ein Taschenmesser auf- und wieder zusammenklappen. In ihrer aufgeklappten Form sind Integrine aktiv und nehmen die unterschiedlichsten Aufgaben wahr. Aktive Integrine übertragen Signale, die zahlreiche Zellprozesse beeinflussen. Unter anderem sind sie essentiell für die Zellteilung, für das Überleben der Zelle und für die Blutgerinnung. Darüber hinaus entscheiden Integrine zusammen mit dem Zellskelett über die Zellform und bestimmen so, wo in einer Zelle oben und unten sowie vorne und hinten ist. Ihre Vielseitigkeit macht Integrine zu einem sehr interessanten Forschungsobjekt, dem sich Reinhard Fässler und sein Team in der Forschungsabteilung „Molekulare Medizin“ widmen. Anker und Antrieb in einem Die Zellform ist für die Fortbewegung wichtig: Wenn Zellen wandern – beispielsweise bei Haarfollikel in der Schwanzhaut der Maus: Das Bild zeigt Zellkerne der Oberhaut (blau) und drei Haarfollikel mit den zugehörigen Talgdrüsen, an deren korrekter Entwicklung Integrine (rot) und Integrin-assoziierte Proteine (grün) entscheidend beteiligt sind (links). Hair follicles in the mouse tail skin. The image shows the cell nuclei (blue) of the epidermis and three hair follicles with their associated sebaceous glands. Integrins (red) and a focal adhesion protein (green) are important for their development (left). Harnleiterzelle aus einer sich entwickelnden Niere der Maus. Die Integrine sind blau gefärbt und die Aktinfilamente grün. Diese Verbindung der Integrine mit dem Aktingerüst ist für Zellbewegungen und daher für die Ausbildung der Nieren entscheidend (rechts). Ureteric bud cell isolated from a developing mouse kidney. The blue staining shows the integrin adhesion sites that are used to bind extracellular matrix proteins. Integrins are linked to the actin filaments (green) of the cytoskeleton, which is essential for cell migration and the formation of a kidney (right). I ntegrins are found in all mammalian cells. They cross the cell membrane and mediate attachment of cells to the extracellular matrix (a gigantic protein complex outside of the cells) via their large extracellular domains. The cytoplasmic domain of integrins connects to the actin cytoskeleton. The extracellular domain of integrins can switch between inactive (bent) and active (straight) conformations. In their active conformation, integrins bind extracellular matrix proteins and transmit signals which influence numerous cellular processes including cell division, cell survival and cell polarity by modulating the dynamics and the stability of the cytoskeleton. Reinhard Fässler and his team in the research department “Molecular Medicine” are investigating the functions of integrins and integrin-associated proteins at the level of the molecule, the cell and the organism. Anchor and Signal Transducer All in One Migrating cells – for instance in immune reactions, wound healing or cancer metastasis – adopt a polarized shape with activated integrins in the front of the cell, which adhere the cell’s leading edge to the extracellular matrix and control the pushing forces of the actin filaments of the Sich entwickelndes Herz­ kreislaufsystem eines elf Tage alten Mausembryos. Integrine koordinieren die Gefäßbildung. Endothelzellen sind grün dargestellt, die glatten Gefäßmuskelzellen rot. Immunreaktionen, Wundheilung oder Krebs­ metastasierung – wirken aktivierte Integrine im Frontbereich der Zelle als Kleber, welche die Zelle an die extrazelluläre Matrix fixieren. Im Heck der Zelle dagegen werden die Integrine inaktiviert, damit die Zellmembran sich von der extrazellulären Matrix lösen kann. Anschließend ziehen Kontraktionen des Zellskeletts den hinteren Teil der Zelle nach vorne. Integrine können auch prüfen, ob die Zelle sich auf dem rechten Weg befindet: Fehlen die Signale des korrekten Bindungspartners, dann senden sie ein Todes­ signal, welches das Absterben der Zelle einleitet. Defekte Integrine führen fast immer zu Krankheiten, was diese Proteine auch medizinisch sehr interessant macht. Die Wissenschaftler konnten beispielsweise nachweisen, dass bei einer schweren Erbkrankheit Immunzellen nicht mehr aus den Blutgefäßen ins Gewebe einwandern können, weil ein bestimmtes Protein fehlt, das für die Integrin-Aktivierung notwendig ist. Fässler und seine Mitarbeiter untersuchen die Funktion von Integrinen sowohl in einzelnen Zellen als auch in Mäusen, indem sie die entsprechenden Gene ausschalten. Dadurch kann entweder kein Integrin gebildet werden oder die Funktion der Integrine ist gestört. Dabei stellt die Vielzahl der Gewebe und Prozesse, die durch Integrine beeinflusst werden, sie immer wieder vor neue Herausforderungen. Denn schon jetzt ist klar: Integrine arbeiten individuell – schaltet man sie aus, führt das je nach Gewebetyp zu unterschiedlichen Symptomen. Developing cardiovascular system of an 11-day-old mouse embryo. Integrins coordinate vascular development. Endothelial cells are shown in green, vascular smooth muscle cells in red. protruding plasma membrane. In the rear of the cell integrins become inactivated, so that the cell membrane detaches from the extracellular matrix and the cell body can contract and be propelled forward. Integrins also continuously check whether migrating cells are on track. If the correct signals of the extracellular matrix highway are missing, they convey a death signal and eliminate the straying cells. Defective integrins almost always lead to diseases, which makes them very important from a medical point of view. For instance, Fässler and his team were able to show that in a severe hereditary disease, called Leukocyte Adhesion Deficiency (LAD) type III, immune cells lack an essential protein required to activate integrins, which prevents the patient’s leukocytes to extravasate from the circulation into the tissue. Fässler and his colleagues use a broad repertoire of cutting-edge techniques to investigate the function of integrins in genetically modified mice and cells. They use the embryonic stem cellbased transgenic technology to either inactivate or to modify integrin genes, so that either no or a functionally disturbed integrin or integrinassociated protein is generated. The large number of tissues and processes that are influenced by integrins pose multiple new challenges, and it is clear that the outcome of integrin signaling critically depends on the cell context because the ablation of integrin signals leads to different defects depending on the tissue type. Prof. Dr. Reinhard Fässler 1981 Medical Doctor, University of Innsbruck, Austria 1981 – 1988 Resident at various hospitals in Austria and at the Institute for General and Experimental Pathology, University of Innsbruck, Austria 1988 – 1992 Postdoctoral fellow at the Whitehead Institute for Biomedical Research, Cambridge, USA 1993 – 1998 Group Leader at the MPI of Biochemistry 1998 – 2001 Professor and Chairman of the Department of Experimental Pathology, University of Lund, Sweden Since 2001 Director of the Department Molecular Medicine at the MPI of Biochemistry, Martinsried, Germany Reinhard Fässler has been honored for his research with the Hermann und Lilly Schilling Professorship (1995) and with the Göran Gustafsson Prize (2001), among other awards. He is honorary professor at the Ludwig-MaximiliansUniversität in Munich, University of Copenhagen and University of Hong Kong. In 2000 he was elected member of EMBO and in 2008 he became a corresponding member of the Austrian Academy of Sciences. Selected Publications Lange A., Wickström S.A., Jacobson M., Zent R., Sainio K. and Fässler R. (2009). “Integrin-linked kinase is an adaptor with essential functions during mouse development.” Nature, 461: 1002-1006. Moser M., Bauer M., Schmid S., Ruppert R., Schmidt S., Sixt M., Wang H.-V., Sperandio M., and Fässler, R. (2009). “Kindlin-3 is required for β2 integrin-mediated leukocyte adhesion to endothelial cells.” Nature Medicine, 15: 300-305. Moser M., Legate K.R., Zent R., and Fässler R. (2009). “The tail of integrins, talin and kindlins.” Science, 324: 895-899. Research Group Leader Dr. Markus Moser (interest in integrin signalling) 30 | 31