Untitled - Die Onleihe
Werbung

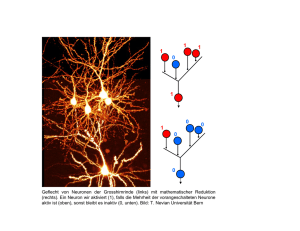
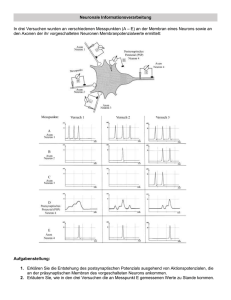
Elektrisch aktiv 15 Für fast 100 Jahre war die im Text erwähnte Golgi-Methode die einzige Möglichkeit, einzelne Neurone vollständig anzufärben. Nach Behandlung des Gewebes mit verschiedenen Salzlösungen bildet sich auf einzelnen Neuronen ein tiefdunkler, unlöslicher Silberniederschlag, der fast alle neuronalen Details im Mikroskop sichtbar werden lässt (Abb. 1B). Warum nur einzelne und nicht alle Neurone angefärbt werden, ist unklar. Mitte der 1970er Jahre gelang es erstmals, einzelne Neurone zu färben, indem die winzige Spitze einer flüssigkeitsgefüllten Glaskapillare ins Innere eines Neurons gestochen wurde. Durch Anlegen einer elektrischen Spannung wird der in der Flüssigkeit gelöste, elektrisch geladene Farbstoff in das Neuron transportiert und verteilt sich dort. Als Farbstoffe werden beispielsweise Fluoreszenzfarbstoffe verwendet, etwa Lucifer Yellow («Teufelsgelb»), die einzelne Neurone direkt, ohne weitere Behandlung unter dem Fluoreszenz-Mikroskop sichtbar werden lassen (Abb. 1C). Mit feinen Glaskapillaren können auch andere Stoffe in einzelne Neurone injiziert werden, etwa bestimmte Enzyme, die wiederum eine Farbreaktion bewirken. Revolutioniert wurde die Färbung von Neuronen durch die 2008 mit dem Nobelpreis gewürdigte Entdeckung des grün fluoreszierenden Proteins (GFP). Nach Einfügung des GFP-Gens in die DNA eines Neurons beginnt dieses, das Protein zu synthetisieren, und wird so permanent angefärbt. Da es möglich ist, Gene spezifisch nur zu bestimmten Zeiten und in bestimmten Zelltypen zu aktivieren, haben Forscher eine recht gute Kontrolle darüber, welche Neurone gefärbt werden. Mittlerweile gibt es eine große Zahl von Farbvarianten des GFPs, so dass sich gleichzeitig viele Neurone mit unterschiedlichen Farben markieren lassen (Abb. 1D). Bevor wir beschreiben, wie Neurone mithilfe ihrer Fortsätze Informationen aufnehmen, verarbeiten und über Synapsen an andere Neuronen weiterleiten, sollten wir an dieser Stelle nicht vergessen, darauf hinzuweisen, dass das Gehirn keineswegs nur aus Neuronen besteht. Als zweite wichtige und zahlenmäßig viel größere Zellklasse findet man im Gehirn die Gliazellen. Ursprünglich ging man davon aus, dass Gliazellen im Wesentlichen Hilfsfunktionen im Gehirn haben und für die Ernährung und den Schutz von Neuronen zuständig sind. Inzwischen wissen wir, dass Gliazellen viele weitere Aufgaben wahrnehmen und zum Beispiel eine 16 Mark Hübener und Rüdiger Klein aktive Rolle bei der Signalverarbeitung und der Regulation des Blutflusses im Gehirn spielen. Gliazellen werden uns noch an einigen weiteren Stellen dieses Kapitels begegnen. Um nun aber wieder zu den Neuronen zurückzukommen: Was ist das Besondere an diesen Zellen, und was macht sie so geeignet für die Verarbeitung von Informationen? Neurone sind elektrisch aktiv Basis für ihre Fähigkeit zur Informationsverarbeitung ist die elektrische Erregbarkeit von Neuronen, eine Eigenschaft, die sie unter allen Zellen des Körpers nur mit Muskelzellen teilen. Um die neuronale Erregungsentstehung und -weiterleitung näher zu verstehen, müssen wir uns kurz mit einigen Grundlagen der Physiologie vertraut machen. Wie bei allen Zellen besteht zwischen der Innen- und der Außenseite der neuronalen Zellmembran eine elektrische Spannung: Das Zellinnere ist gegenüber der Außenseite negativ geladen, die Größe dieses sogenannten Ruhepotenzials beträgt etwa –70 mV, also etwa ein Zwanzigstel einer Taschenlampenbatterie. Das Ruhepotenzial beruht auf der ungleichen Verteilung bestimmter Ionen zwischen Zellinnerem und -äußerem sowie der selektiven Durchlässigkeit der Zellmembran für unterschiedliche Ionen. Im Ruhezustand ist die Membran sehr gut für positiv geladene Kaliumionen durchlässig, nicht jedoch für die ebenfalls positiv geladenen Natriumionen. Da die Konzentration von Kaliumionen im Inneren des Neurons hoch, außen aber niedrig ist, werden diese Ionen entsprechend ihrem Konzentrationsgefälle die Zelle verlassen. Da jedes Kaliumion eine positive Ladung mit nach außen nimmt, lädt sich das Innere der Zelle negativ auf. Wie kommt es, dass die Zellmembran für bestimmte Ionen durchlässig ist, für andere aber nicht? Verantwortlich dafür sind in die Membran eingelagerte komplexe Proteine, sogenannte Ionenkanäle, die einige Ionen passieren lassen, andere jedoch nicht. Was ist nun darunter zu verstehen, wenn ein Neuron elektrisch erregt wird? Es kommt zu einer nur etwa eine tausendstel Sekunde dauernden Änderung der elektrischen Spannung, die kurzzeitig auf +30 mV ansteigt, um dann sofort wieder auf den Ruhewert von –70 mV abzufallen. Diese plötzliche Spannungsänderung in Neuronen wird als Aktionspotenzial bezeichnet und beruht auf der Fähigkeit vieler Ionenkanäle, ihre Durchlässigkeit zu ändern. Für das Aktionspotenzial sind in erster Linie Elektrisch aktiv 17 die sogenannten schnellen Natriumkanäle verantwortlich. Diese werden vermehrt geöffnet, sobald das Ruhepotenzial zu etwas positiveren Werten verschoben wird. Dadurch strömen Natriumionen in die Zelle, treiben das Potenzial zu positiveren Werten, weitere Natriumkanäle werden geöffnet, bis sich schließlich beim Überschreiten der sogenannten Feuerschwelle dieser Prozess explosionsartig beschleunigt und das Potenzial nach oben schießt. Beendet wird das Aktionspotenzial dadurch, dass sich der schnelle Natriumkanal sehr rasch wieder schließt und dass anschließend ein weiterer spannungsgesteuerter Kanal kurzzeitig geöffnet wird. Durch diesen strömen positiv geladene Kaliumionen aus dem Neuron heraus, wodurch das Potenzial wieder auf den Ruhewert von –70 mV abfällt. Ein guter Teil der Kunst der Neurophysiologie besteht übrigens darin, diese kleinen und kurzen Spannungsschwankungen einzelner Neurone zuverlässig zu messen (siehe Box 2). 2 – Messung von Aktionspotenzialen Der direkte Weg, das Feuern von Neuronen, also Aktionspotenziale, zu messen, besteht darin, eine fein ausgezogene, mit Salzlösung gefüllte Glaskapillare durch die Zellmembran zu stoßen und Änderungen der Spannung zwischen dem Inneren und Äußeren des Neurons mit empfindlichen elektronischen Verstärkern aufzuzeichnen. Bei der von den beiden Nobelpreisträgern Erwin Neher und Bert Sakmann entwickelten Patch-Clamp-Technik wird eine Kapillare mit etwas größerer Öffnung (etwa ein tausendstel Millimeter) zunächst auf die Zellmembran aufgesetzt und durch Anlegen eines leichten Unterdrucks festgesaugt. Wird der Sog verstärkt, bricht schließlich die Membran auf, was den direkten elektrischen Zugang zum Inneren des Neurons ermöglicht. Beide intrazellulären Ableitmethoden erfordern viel Feingefühl. Bei Patch-Clamp-Ableitungen etwa wird der genau dosierte Unterdruck dadurch erzeugt, dass der Experimentator einen mit der Glaskapillare verbundenen Schlauch im Mund hält und daran saugt. Technisch etwas einfacher sind extrazelluläre Ableitungen: Hier wird die feine Spitze einer Metallelektrode (oft aus Wolfram gefertigt) in die Nähe eines Neurons gebracht. Feuert das Neuron ein Aktionspotenzial, führt das auch außerhalb der Zelle zu einer Spannungsschwankung. Diese ist allerdings sehr klein, so dass deutlich mehr Aufwand betrieben werden muss, um die Signale elektronisch zu verstärken und gegen Störungen, etwa von elektrischen Geräten, abzuschirmen. 18 Mark Hübener und Rüdiger Klein In jüngster Zeit benutzen Neurophysiologen zunehmend optische Methoden, um neuronale Aktivität darzustellen. Spezielle Fluoreszenzfarbstoffe leuchten intensiver, wenn die Konzentration bestimmter Ionen ansteigt. Bringt man zum Beispiel einen calciumsensitiven Farbstoff in ein Neuron, so lässt jedes Aktionspotenzial das Neuron kurz aufleuchten, da neben Natrium immer auch etwas Calcium in die Zelle einströmt. Mit empfindlichen Mikroskopen lassen sich diese Lichtblitze erfassen. Entscheidend für die Informationsverarbeitung im Gehirn ist, dass Aktionspotenziale sehr schnell über das Axon eines Neurons weitergeleitet werden. Ein Aktionspotenzial an einer Stelle des Axons führt zu einem leichten Anstieg des Potenzials an einer benachbarten Stelle, an der damit wiederum ein Aktionspotenzial ausgelöst wird usw. So «hüpft» das Aktionspotenzial entlang des Axons, wobei sich mithilfe einiger «Tricks» Leitungsgeschwindigkeiten von bis zu 120 m/s erreichen lassen. Das ist zwar im Vergleich zur Leitung von elektrischem Strom im Kupferkabel zweieinhalb Millionen mal langsamer, aber doch so schnell, dass ein Aktionspotenzial nur wenige tausendstel Sekunden benötigt, um von einem Neuron im Rückenmark bis zum Muskel im Bein zu gelangen. Synaptische Übertragung Wie aber kann das Aktionspotenzial auf nachfolgende Neurone (oder Muskelzellen) übertragen werden? Dies geschieht an den bereits erwähnten Synapsen, also den Kontaktstellen zwischen Neuronen. Synapsen spielen eine herausragende Rolle bei vielen Gehirnfunktionen; sie sind nicht nur an der Informationsverarbeitung beteiligt, sie sind auch die Stellen im neuronalen Netzwerk, an denen die Stärke der Kopplung zwischen Neuronen sehr effizient verändert werden kann. Dies ist, wie wir weiter unten zeigen werden, entscheidend für die Gehirnentwicklung und auch Grundlage für eine der wichtigsten Leistungen unseres Gehirns, Lernen und Gedächtnis (vgl. Kap. 3). Da Synapsen außerdem bevorzugte Wirkorte sehr vieler Substanzen zur Behandlung von Erkrankungen des Nervensystems sind, werden wir uns etwas genauer mit diesen Kontaktstellen oder «protoplasmatischen Küssen», wie Ramón y Cajal sie nannte, befassen. Elektrisch aktiv 19 Die meisten Synapsen im Gehirn sind chemische Synapsen, an denen biochemische Stoffe, sogenannte Neurotransmitter, Informationen von einer Nervenzelle zur anderen weitergeben. In die Synapse einlaufende Aktionspotenziale bewirken die Ausschüttung der Neurotransmitter aus ihren Speicherorten, den synaptischen Vesikeln – kleinen, membranumhüllten Bläschen innerhalb des axonalen Boutons. Durch die Fusion der Vesikel mit der Membran des Boutons gelangen die Transmittermoleküle in den synaptischen Spalt, durch den sie sich bis zum nachgeschalteten postsynaptischen Neuron ausbreiten und dort an ihre spezifischen Rezeptoren (Antennen) binden. Dieser Vorgang spielt sich in Tausendstelsekunden ab. Neurotransmitter passen zu ihren Rezeptoren wie ein Schlüssel ins Schlüsselloch, und ihre Bindung bewirkt, dass der Rezeptor seine Form und infolgedessen seine Funktion verändert. Generell unterscheidet man zwei verschiedene Rezeptortypen. «Ionotrope» Rezeptoren sind Ionenkanäle, die sich bei Bindung des Transmitters in Sekundenbruchteilen öffnen, bestimmte Ionen durchlassen und dadurch das Ruhepotenzial des nachgeschalteten Neurons etwas verändern. «Metabotrope» Rezeptoren haben keine Poren, sondern aktivieren eine Signalkaskade von sekundären Botenstoffen innerhalb der postsynaptischen Zelle. «Metabotrop» ist von Metabolismus abgeleitet, da diese Mechanismen bestimmten Stoffwechselvorgängen in der Zelle ähneln. Die Übertragungsstärke von Synapsen kann sich ändern, je nachdem, wie viel Neurotransmitter vom präsynaptischen Neuron ausgeschüttet wird, wie viele Rezeptoren sich in der postsynaptischen Membran befinden oder wie effizient die Signale verarbeitet werden. Bei den Neurotransmittern unterscheidet man entsprechend ihrer Wirkung auf das nachgeschaltete Neuron erregende, hemmende und modulierende Transmitter. Der wichtigste erregende Neurotransmitter im zentralen Nervensystem von Wirbeltieren ist L-Glutamat, auch L-Glutaminsäure oder einfach Glutamat genannt. Glutamat zählt zu den Aminosäuren und ist daher ein wichtiger Baustein der Proteine. Im Zentralnervensystem wird Glutamat an Synapsen freigesetzt und bindet an spezifische Glutamatrezeptoren, deren Dichte an der postsynaptischen Membran dieser sogenannten «glutamatergen» Synapsen besonders hoch ist. Glutamat findet sich in fast allen proteinhaltigen Lebensmitteln und wird in Salzform auch als Geschmacksverstärker in Lebensmitteln eingesetzt. Eine glutamatreiche Ernährung hat allerdings keinen nennenswerten Einfluss auf die Glutamatkonzentration im Gehirn. Sollte es dennoch