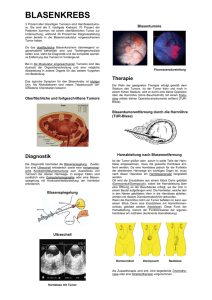
Odontogene Tumoren und ihre histopathologische Aufarbeitung in
Werbung

DIPLOMARBEIT Odontogene Tumoren und ihre histopathologische Aufarbeitung in der Mund-, Kiefer- und Gesichtschirurgie im Zeitraum von 2004 bis 2012 eingereicht von Alwin Sokolowski geb. 06.07.1989 zur Erlangung des akademischen Grades Doktor der Zahnheilkunde (Dr. med. dent.) ausgeführt an der klinischen Abteilung für Mund-, Kiefer- und Gesichtschirurgie der Universitätsklinik für Zahn-, Mund- und Kieferheilkunde Graz unter der Anleitung von Univ.-Prof. DDr. Günter Schultes Univ.-Ass. DDr. Lucia Gerzanic Graz, Juni 2014 Alwin Sokolowski Eidesstattliche Erklärung Ich erkläre ehrenwörtlich, dass ich die vorliegende Arbeit selbstständig und ohne fremde Hilfe verfasst habe, andere als die angegebenen Quellen nicht verwendet habe und die den benutzten Quellen wörtlich oder inhaltlich entnommenen Stellen als solche kenntlich gemacht habe. Graz, am 26.06.2014 Sokolowski Alwin 1 Danksagung Mein Dank gebührt vor allem Univ.-Ass. DDr. Lucia Gerzanic, sowie Univ.-Prof. DDr. Günter Schultes für ihre Betreuung und Unterstützung beim Erstellen dieser Arbeit. Weiters gilt mein Dank Prof. Dr. Alfred Beham für die Übergabe der Daten für die statistische Analyse und seine fachkundige Beratung. Mag. Martyna McLaren und DDr. Armin Andreas Sokolowski möchte ich für die Hilfestellung und Ratschläge zur statistischen Auswertung und Korrektur der Arbeit danken. Mein ganz besonderer Dank geht an meine Eltern, die mir dieses Studium ermöglicht und mich immerzu unterstützt haben. Zudem gebührt mein Dank meiner gesamten Familie und meinen zahlreichen Freunden, die mich auf meinem Weg durchs Studium begleitet haben. 2 Zusammenfassung Die retrospektive Analyse dieser Arbeit bestand aus der Aufarbeitung statistischer Daten aus den Jahren 2004-2012 der klinischen Abteilung für Mund-, Kiefer- und Gesichtschirurgie und der Universitätsklinik für Zahn-, Mund- und Kieferheilkunde Graz, mit dem Ziel, die Anzahl der diagnostizierten Tumorarten, das Geschlecht und das Alter der Betroffenen, die Lokalisationen und Rezidivraten der untersuchten Tumore und die Art der gewählten Therapie zu erfassen. Im untersuchten Zeitraum wurden 185 PatientInnen mit der histopathologisch gestellten Diagnose eines odontogenen Tumors dokumentiert. Das mittlere Patientenalter lag bei ca. 37 Jahren, wobei bei Männern im Verhältnis von 1:1,3 etwas seltener ein odontogener Tumor diagnostiziert wurde. 98.4% der odontogenen Tumoren konnten als benigne eingestuft werden. Die größte Gruppe nahm mit 65,4% der keratozystische odontogene Tumor ein, an zweiter Stelle, mit 14,6%, lag das Odontom, gefolgt vom Ameloblastom mit 10,8%. Die restlichen benignen Tumoren nahmen etwa 7,6% ein. Im Vergleich zu internationalen Studien war der adenomatoide odontogene Tumor in unserer Analyse eher selten vertreten. Die malignen Läsionen nahmen mit nur 3 Fällen eine sehr kleine Gruppe ein. Das entspricht 1,6% aller untersuchten odontogenen Tumoren. Unsere retrospektive Analyse bestätigt die in der Literatur beschriebene Dominanz des keratozystischen odontogenen Tumors in der Epidemiologie der odontogenen Tumoren. Die Verteilung der odontogenen Tumoren zeigt in unserer Untersuchung Parallelen zu anderen aktuellen Analysen aus europäischen Ländern auf. Im Vergleich zu Studienergebnissen aus Afrika oder Asien konnten zum Teil deutliche Unterschiede festgestellt werden. 3 Abstract This paper describes the results of the retrospective analysis of data from the years 2004-2012 evaluated at the Maxillofacial Surgery of the Medical University of Graz and the Dental Department of Graz. The analysis was performed using descriptive statistics, to detect the number of diagnosed tumour types, further the sex and age of persons concerned, the location of the tumour, number of relapses, and nature of the chosen therapy. The study included 185 patients with histopathologically identified diagnosis of odontogenic tumours. The mean patient age was 37 years, with a male to female ratio of 1:1.3. 98.4% of the odontogenic tumours were classified as benign. The most often diagnosed odontogenic tumour was the keratocystic odontogenic tumour representing 65.4%, followed by odontoma with 14.6%, and ameloblastoma with 10.8%. The remaining benign tumours took only about 7.6%. In comparison to international studies, the adenomatoid odontogenic tumour was rarely represented in our analysis. The malignant lesions took only 3 cases corresponding to 1.6% of all diagnosed odontogenic tumours, making it a very small group. Our retrospective analysis confirmed the dominance of the keratocystic odontogenic tumour in the epidemiology of odontogenic tumours, as described in the literature. Our study shows similarities to current analyses from European countries. On the other hand differences to study results from Africa or Asia could be found. 4 Abkürzungsverzeichnis A Ca Ameloblastisches Karzinom AME Ameloblastom AOT Adenomatoider odontogener Tumor CCO Klarzelliges odontogenes Karzinom CCOT Kalzifizierender zystischer odontogener Tumor CEOT Kalzifizierender odontogener Tumor CTB Zementoblastom DGCT Odontogener ghost-cell Tumor KZOT / KCOT Keratozystischer odontogener Tumor OD Odontom OF Odontogenes Fibrom OM Odontogenes Myxom PIO Primär intraossäres Karzinom 5 Inhaltsverzeichnis 1 Einleitung ........................................................................................................ 7 1.1 Allgemeine Onkologie des Kiefers ............................................................ 8 1.2 Zahnentwicklung ....................................................................................... 9 1.3 Nomenklatur der odontogenen Tumoren................................................. 12 1.4 Allgemeine Diagnostik und Symptomatik odontogener Tumoren ............ 13 1.4.1 Klinische/Radiologische Diagnostik ................................................... 13 1.4.2 Immunhistochemischer Nachweis ..................................................... 13 1.5 Gutartige Läsionen .................................................................................. 14 1.5.1 Odontogene epitheliale Tumoren mit fibrösen Stroma ohne odontogenes Ektomesenchym.................................................. 14 1.5.2 Odontogene epitheliale Tumoren mit odontogenem Ektomesenchym, mit oder ohne Hartsubstanzbildung ................................... 21 1.5.3 Odontogene ektomesenchymale Tumoren mit oder ohne inkorporiertes odontogenes Epithel ....................................................... 25 1.6 Bösartige Läsionen.................................................................................. 27 1.6.1 Odontogene Karzinome ..................................................................... 27 1.6.2 Odontogene Sarkome ........................................................................ 30 1.7 Differentialdiagnosen odontogener Tumoren .......................................... 31 1.7.1 Zystische Läsionen ............................................................................ 31 1.7.2 Zentrales Riesenzellgranulom ........................................................... 36 2 Zielsetzung .................................................................................................... 38 3 Material und Methode.................................................................................... 40 4 3.1 Patientendaten ........................................................................................ 40 3.2 Datenerhebung ....................................................................................... 40 Ergebnisse .................................................................................................... 44 4.1.1 Alters- und Geschlechtsverteilung ..................................................... 50 4.1.2 Größenverteilung ............................................................................... 52 4.1.3 Rezidivraten ....................................................................................... 53 5 Diskussion ..................................................................................................... 55 6 Literaturverzeichnis ....................................................................................... 62 7 Abbildungsverzeichnis................................................................................... 69 8 Tabellenverzeichnis ...................................................................................... 70 6 1 EINLEITUNG Das Wort Tumor, lateinisch für Schwellung, Wucherung, ist im engeren Sinne eine Neubildung von Körpergeweben, die durch eine Fehlregulation des Zellwachstums verursacht werden kann (Jundt, 2006). Unter dem Begriff odontogene Tumoren versteht man eine Gruppe an Neoplasmen und tumorartigen Fehlbildungen, die aus Zellen des odontogenen Apparates und dessen Resten entstehen können, das heißt aus odontogenen Geweben und deren Vorläuferzellen. Sie kommen ausschließlich im Kiefer oder in der Gingiva vor (Schwenzer, et al., 2009). Im Laufe der Zeit hat sich die Nomenklatur der odontogenen Tumoren, aufgrund genauerer Kenntnisse und der Erforschung einer breiteren Palette an Tumoren, mehrmals geändert (Jundt, 2006). Odontogene Tumoren, die sich aus Resten des Zahnkeimes oder dem Zahnapparat ableiten, sind selten, noch seltener als Knochentumoren. Angesichts dieser Seltenheit odontogener Läsionen sind auch heute noch nur spärliche Daten über genaue Häufung, Alters- und Geschlechtsverteilung oder Symptomatik vorhanden. Ebenso ist nicht eindeutig geklärt, ob beobachtete kulturelle Unterschiede für die Verteilung relevant sind (Barnes, 2005). Differentialdiagnostisch können odontogene Tumoren zu einem benignen oder einem malignen Befund führen, sie sind jedoch vorab von entzündlichen Prozessen und Zysten abzugrenzen. Aufgrund des Ausmaßes des Tumors und unter Einbeziehung des höchstmöglichen Wohlbefindens des Patienten, muss zwischen einer therapeutischen oder einer palliativen Therapie unterschieden werden. Als therapeutische Intervention wird heute in den meisten Fällen eine Totalexzision im Rahmen einer Exzisionsbiopsie, empfohlen (Jundt, 2006). Je nach Größe und Lokalisation muss eine Defektdeckung im Sinne einer für den Patienten optimalen Ausheilung angestrebt werden. Somit kann bei großen Defekten eine gestielte Knochentransplantation erforderlich werden. Nach der operativen Entfernung muss in den meisten Fällen eine langfristige Rezidivkontrolle stattfinden, um einen neuerlichen Ausbruch der Erkrankung zu minimieren (Schwenzer, et al., 2009). Die richtige Diagnose und Therapie von odontogenen Tumoren stellt eine wichtige 7 Rolle im Klinikalltag eines Zahnarztes oder Kieferchirurgen dar. Das Erkennen der möglichen Symptomatik und das richtige Handeln sind bei Verdacht auf ein solches Geschehen essentiell. Diese Arbeit widmet sich der Aufarbeitung des heutigen Wissensstandes über die richtige Diagnosefindung, Therapie und Nachsorge odontogener Tumoren, sowie der Analyse odontogener Tumoren über ihre Jahres-, Geschlechter- und Altersverteilung in Graz, in Bezug auf die histopathologische Art des odontogenen Tumors, und dem Vergleich zu anderen in der Literatur angegebenen Verteilungen. 1.1 Allgemeine Onkologie des Kiefers Die meisten Tumoren und tumor-ähnlichen Läsionen im Kieferbereich weisen Großteiles klinisch eine sehr ähnliche Symptomatik auf. Zu den häufigsten Krankheitszeichen gehören Sensibilitätsausfälle und mehr oder Schmerzen. weniger Durch harte diese Schwellungen, recht unspezifische Symptomatik, für die auch viele andere mögliche Ursachen in Frage kämen, wird daher als erster diagnostischer Schritt eine radiologische Untersuchung durchgeführt. Bei Verdacht auf einen Tumor sollte auch eine dreidimensionale Abklärung mit Hilfe einer Computer-Tomographie des Kiefers durchgeführt werden (Jundt, 2006). Als wichtigster, charakteristischer Röntgenbefund zeigt sich eine Osteolyse im Unterkiefer, beziehungsweise eine meist homogene, milchglasartige Verschattung im Oberkiefer (Jundt, 2006). Die Osteolyse kann mehr oder weniger scharf begrenzt sein, ein sklerotischer Randsaum gibt meist einen Hinweis auf den benignen Charakter einer Läsion. In der Osteolysezone können sich bei einer Reihe von Läsionen, vor allem den zement- und knochenbildenden Läsionen, mehr oder weniger röntgenopake, vereinzelte oder konfluierende Verdichtungen finden. Durch mögliche Abgrenzbarkeit, knöcherne sind die Überlagerungen diagnostischen und eine Möglichkeiten nicht eindeutige der Radiologie eingeschränkt. Deshalb sollte bei insuffizienter Aussagekraft des Röntgenbildes in 8 jedem Fall eine dreidimensionale Volumentomographie, einer Aufnahme, im Computertomographie Sinne oder einer einer Digitalen Kernspin- tomographie, durchgeführt werden (Freyschmidt, 2010). Als nächsten Schritt der Diagnostik ergibt sich die zwingende Notwendigkeit, die Diagnose eines Kiefertumors durch eine Biopsie zu untermauern. Kleinere Läsionen können anhand einer Exzisionsbiopsie zur histopathologischen Untersuchung geführt werden, bei größeren Läsionen sollte eine offene Biopsie durchgeführt werden, um genügend Material gewinnen zu können. Das so gewonnene Gewebe sollte, wenn eine sofortige Weiterbearbeitung möglich ist, unfixiert in unter 30 Minuten, am besten gekühlt, zur Schnellschnittdiagnostik gebracht werden, um einen optimalen Erhaltungszustand für die histologische Untersuchung zu gewährleisten. Sollte eine sofortige Weiterverarbeitung nicht möglich sein, wird empfohlen das Biopsat in gepuffertem, 4%igen Formalin zu fixieren, und so schnell wie möglich dem Pathologen vorzubringen (Jundt, 2006). Da die histologische Interpretation selbst einer perfekt erhaltenen Biopsie teils zu erheblichen Problemen führen kann - benigne und maligne Tumoren können ein sehr ähnliches histologisches Bild aufweisen - sollte die histologische Untersuchung im besten Fall von einem auf diesem Spezialgebiet erfahrenen Pathologen erfolgen. 1.2 Zahnentwicklung Um die Pathogenese odontogener Tumoren verstehen zu können, ist eine genaue Kenntnis der Zahnentwicklung sowie der beteiligten Gewebe unabdingbar. Wie bei den meisten mehr-zahnigen Säugetieren entstehen die Zähne auch beim Menschen in einer sehr frühen Entwicklungsstufe des Fötus. Die Milchzahnkeime entwickeln sich bereits vom Beginn der 4. bis zur 17. Woche nach der Befruchtung. Das ektodermale Epithel der primären Mundbucht proliferiert bereits in der 4. bis 6. Entwicklungswoche und bildet somit eine örtlich begrenzte U-förmige Verdickung im Bereich der Unter- und Oberkieferbögen. Durch das weitere proliferative Wachstum dieses odontogenen Epithelbandes, der so genannten Zahnplatte, wird die Bildung der Zahnleiste vorangetrieben (Reitemeier, et al., 2006). 9 In dieser Periode wird aus dem anfänglichen epithelialen Zellhaufen zunächst eine Zahnknospe, die mit der Zeit zur Zahnkappe, und schließlich zur Zahnglocke reift. Zugleich mit der Entwicklung des vom epithelialen Anteil ausgehenden Schmelzorganes, entstehen aus dem Zahnmesenchym die Zahnpapille und das eigentliche Zahnsäckchen. Diese drei Strukturen bilden gemeinsam den Zahnkeim. Während sich die Zahnknospen über das Kappenstadium zur Zahnglocke entwickeln, verlängert sich die Zahnleiste, wird zur lateralen Zahnleiste und verbindet Zahnkeim und die generelle Zahnleiste miteinander. Die Zuwachszahnkeime der drei bleibenden Molaren entstehen am blinden Ende der sich nach distal durch proliferatives Wachstum verlängernden Zahnleiste der Milchmolaren. Die Ersatzzahnkeime entstehen lingual bzw. palatinal der Milchzahnkeime, wo die generelle Zahnleiste von Keim zu Keim der 1. Dentition zieht. Diese Leiste verlängert sich nach apikal und bildet schließlich die Ersatzzahnleiste. Als Resultat einer Kette sich beeinflussender Wechselwirkungen zwischen Zellen des Ektoderms und des Ektomesenchyms, zeigen sich die Initiation der Zahnkeimentwicklung, die Morphogenese der formspezifischen Zahnglocke durch das Schmelzorgan, die terminale Differenzierung von Odontoblasten und Ameloblasten, und der Beginn der Hartsubstanzbildung. Unter normalen Umständen induzieren die von der kranialen Neuralleiste abstammenden Zellen des Ektomesenchyms die Bildung des odontogenen Epithels der Zahnleiste, sowie die epitheliale Zahnsprossung, und steuern die Entwicklung und Morphogenese des Schmelzorgans und der Hertwig‘schen Epithelscheide, welche die spätere Form der Zahnwurzel bedingt. Nach Abschluss ihrer Differenzierung beginnen die Odontoblasten mit der Synthese der Dentinmatrix, die gegen die Basallamina des inneren Schmelzepithels ausgeschüttet wird, zum Prädentin ausreift und von der Peripherie her zu mineralisieren beginnt. Zeitgleich mit dem Einsetzen der Dentinbildung und der Bildung einer ersten dünnen Prädentinschicht erfolgt die Differenzierung der Präameloblasten zu Ameloblasten, durch die anschließend die Synthese der Schmelzmatrix erfolgt. Dentin und Schmelz werden schichtweise gebildet und aus dem Verlauf der 10 zwischen den Schichten entstehenden Wachstumslinien lassen sich die aufeinanderfolgenden Phasen der Zahnhartsubstanzbildung ablesen (Schroeder, 1999). Die Bildung der Zahnwurzel wird von der Hertwig‘schen Epithelscheide geleitet. Wenn das Schmelzorgan die definitive Größe erreicht hat, und damit die zervikale Schlinge im Bereich der späteren Schmelzzementgrenze liegt, führt ununterbrochenes proliferatives Wachstum zur Verlängerung dieser Schlinge. Daraus entstehen die inneren und äußeren Schmelzepithelschichten, die zur späteren Form der Zahnwurzel führen. Durch Proliferation wächst das Schmelzorgan in diesem Bereich weiter in die Tiefe und präformiert die Anlage der späteren Zahnwurzel, indem die Ränder teilweise auf einander zuwachsen und einen, zwei oder drei Wurzelkanäle freilassen (Schroeder, 1999). Wenn die Hertwig‘sche Epithelscheide zu verfallen beginnt, differenzieren sich die Follikel-Zellen zu Zementoblasten, sondern feine Kollagen-Fibrillen rechtwinklig zur Wurzeloberfläche ab und bewegen sie sich vom Zahn weg. Unterwegs lagern sie weiteres Kollagen ab, um die Faserbündel zu verlängern und zu verdicken (Steiniger, 2010). Mit dem Beginn der Mineralisation dieses azellulären Zements, entfernen sich die Zementoblasten vom Wurzelzement und die zurückbleibenden Fasern verbinden sich mit den periodontalen Bändern. Beim zellulären Wurzelzement unterscheidet man Gemischtfaserzement. Der Eigenfaserzement ist Eigenfaserzement und ein reines Zemento- blastenprodukt und erscheint erst, wenn die Zahnbildung fast abgeschlossen ist. Er entsteht rund Zementoblasten um werden die in Faserbündel dem von der ihnen periodontalen produzierten Bänder. Die Wurzelzement eingeschlossen (Schroeder, 1999). Die Morphogenese des Zahnkeims, sowie die Differenzierung der sekretorischen Ameloblasten und Odontoblasten, werden durch wechselseitige epitheliomesenchymale Interaktionen gesteuert. Wachstumsfaktoren wie der fibroblast-growth-factor, die bonemorphogenetic proteins, Activine oder das Sonic-Hedgehog-Protein regulieren die Expression von Genen und die Differenzierungsvorgänge in der Zahnpapille. Sie können bei Mutationen neben anderen Auslösefaktoren zur Bildung benigner oder maligner Prozesse führen (Reitemeier, et al., 2006). 11 1.3 Nomenklatur der odontogenen Tumoren Im Laufe der Zeit wurde die Nomenklatur der odontogenen Tumoren, aufgrund besserer Kenntnisse der Histopathologie und Tumorpathologie, eines besseren Verständnisses der induktiven Interaktionen odontogener Gewebe, sowie der Erforschung einer breiteren Palette an Tumoren, mehrmals adaptiert und verbessert. Im 18. und frühen 19. Jahrhundert entstanden die ersten Einzelbeschreibungen und Publikationen über odontogene Tumoren, dennoch dauerte es noch bis 1868, als zum ersten Mal eine Klassifikation aufgestellt wurde, die auf den ersten Stadien der Entwicklung des wachsenden Zahnes beruhte. Bis 1946 wurden jedoch die meisten odontogenen Tumoren als Ameloblastome oder als Odontome bezeichnet (Broca, 1968). Die 1971 erstmals publizierte Klassifikation der WHO beruht auf der Arbeit von Pindborg und Clausen (1958). Diese erste Klassifikation der WHO unterschied zwischen Tumoren und Läsionen des odontogenen Apparats, Neoplasien und anderen Läsionen des Knochens, sowie epithelialen Zysten. Je nach ihrem biologischen Verlauf wurden bereits benigne und maligne Läsionen unterschieden. 1992 erschien die zweite Auflage der WHO, die diese Einteilung im Wesentlichen beibehielt, in der jedoch bereits zahlreiche Umgruppierungen notwendig geworden waren (Kramer, et al., 1993). Die heute gängige Klassifikation der Kopf-Hals-Tumoren wurde 2005 von der WHO veröffentlicht. Im Gegensatz zu vorangegangenen Tumorklassifikationen, die sich hauptsächlich mit den Tumoren eines einzelnen Organs befassten, wird nun eine Zusammenfassung der Pathologie und Genetik der Tumoren zusammengehöriger Organsysteme bzw. Regionen präsentiert (Barnes, 2005). Die neu erforschten histopathologischen Aspekte auf Basis genetischer Befunde führten unter anderem dazu, dass die früher als Keratozyste bezeichnete Läsion, aufgrund molekulargenetischer Befunde, heute als Tumor („keratozystischer odontogenener Tumor“) angesehen wird (Freyschmidt, 2010). Aufgrund der Tatsache, dass sich viele dieser Läsionen radiologisch und makroskopisch mit einem gleichförmigen Erscheinungsbild präsentieren, ist zur Diagnosestellung in jedem Fall eine Biopsie notwendig, auch wenn in manchen Fällen Klinik und Lokalisation die Differentialdiagnose bereits erheblich einengen können. 12 1.4 Allgemeine Diagnostik und Symptomatik odontogener Tumoren 1.4.1 Klinische/Radiologische Diagnostik Wie jede neoplastische Erkrankung bedürfen auch odontogene Tumoren einer genauen Untersuchung, um eine exakte Diagnose stellen zu können. Dabei sind eine detaillierte Anamnese, eine genaue Inspektion und die Palpation die wichtigsten non-invasiven Maßnahmen des Arztes/der Ärztin und können bereits erste wichtige Hinweise auf die Art der Erkrankung geben. Odontogene Tumoren können von wenig bis gar keine Symptome, bis hin zu einer beachtlichen Minderung der Lebensqualität oder gar zum Tod führen. Die präoperative Verdachtsdiagnose stützt sich neben der Anamnese, auf den klinischen Befund, der meist unspezifische Krankheitszeichen, wie Schmerzen, Sensibilitätsstörungen, Devitalität von Zähnen, Schwellung, Zahndurchbruchs- und Zahnstellungsanomalien, erhöhte Zahnmobilität, Kieferauftreibungen, oder eventuell sogar pathologische Frakturen aufweisen kann. Als radiologische Unterscheidungsmerkmale sind verschiedene Radioopazitäten, wie Aufhellungen, aber auch Verschattungen im Sinne von Verkalkungen erkennbar. Resorptionen von anatomischen Nachbarstrukturen sind einerseits typisch für maligne Tumoren mit destruktiven Tendenzen, konnten aber auch bei anderen odontogenen Läsionen beschrieben werden (Gundlach, 2000). Zur weiteren Abklärung bei nicht eindeutigen Befunden bzw. bei großen Aufhellungen mit Verdacht auf Nervenbeteiligung, sollte auf jeden Fall auch eine erweiterte radiologische Abklärung, im Sinne eines Röntgens in zweiter Ebene, oder einer dreidimensionalen Abklärung mithilfe einer Computertomographie oder Magnetresonanztomographie, erfolgen. 1.4.2 Immunhistochemischer Nachweis Immunhistochemische Marker können dem Pathologen dabei helfen, eine eindeutige Diagnose zu stellen. Mittels einer Stanzapparatur können aus einer repräsentativen Region der eingeschickten Tumorblöcke Biopsien entnommen und in einen leeren 13 Paraffinblock transferiert werden. Unter der Verwendung eines Avidin-BiotinProtokolls zur Markierung und Detektion der Antikörper, kann ein immunhistochemischer Nachweis einer erhöhten Expression der Effektorproteine in odontogenen Tumoren auf Gewebemikroarrays durchgeführt werden. Somit lässt sich zum Beispiel eine aberrante Aktivierung des Sonic-HedgehogSignalweges bei Patienten mit keratozystischen odontogenen Tumoren nachweisen. Bei Patienten mit Gorlin-Goltz-Syndrom sind genetische Mutationen für diese Aktivierung verantwortlich, doch auch bei nicht-syndromalen keratozystischen odontogenen Tumoren lässt sich eine Dysregulation des SonicHedgehog-Signalweges nachweisen (Freier, et al., 2009) . 1.5 Gutartige Läsionen 1.5.1 Odontogene epitheliale Tumoren mit fibrösen Stroma ohne odontogenes Ektomesenchym Epitheliale odontogene Tumoren leiten sich vom odontogenen Epithel ab: Der Zahnleiste, dem Schmelzorgan und der Hertwig‘schen Epithelscheide. Aufgrund der fehlenden odontogen-mesenchymalen Beteiligung beinhalten diese Läsionen keine Zahnhartsubstanz und keine myxoiden Gewebe. 1.5.1.1 Ameloblastom 1890 wurde das Ameloblastom erstmals von Malassez als eigenständiger odontogener Tumor erkannt (Baden, 1965). Der Name des Ameloblastoms leitet sich vom Altenglischen amel „Schmelz“ und Altgriechischen blastä „Keim“ ab. Vor 1929 war das Ameloblastom unter dem fälschlicherweise auch heute noch oft benutzen Terminus „Adamantinom“ bekannt (Churchill, 1932). Der Name „Adamantinom“ rührt von der falschen Annahme her, dass es sich dabei um eine schmelzbildende Neubildung handelt, was jedoch für die Diagnose des Ameloblastoms nicht der Fall ist. Das Ameloblastom ist mit 18% einer der häufigsten odontogenen Tumoren. Beide Geschlechter sind etwa gleich häufig davon betroffen und zeigen den Altersgipfel zwischen dem 4. und 6. Lebensjahrzehnt (DÖSAK-Register). Mehr als drei Viertel aller Fälle treten im Unterkiefer auf, davon die Hälfte in der Prämolaren- bzw. 14 Molarenregion (Jundt, 2006). Die Ätiologie ist immer noch unklar. Man vermutet jedoch ihre Entstehung aus den Resten der Zahnleiste, dem Schmelzorgan oder der Hertwig‘schen Epithelscheide. Häufig treten Ameloblastome zusammen mit odontogenen Zysten, wie der kalzifizierenden odontogenen Zyste und der follikulären Zyste, sowie dem früher als „Keratozyste“ bekannten keratozystischem odontogenen Tumor, auf. Das Ameloblastom zeigt eine häufige Rezidivneigung, ist jedoch in den meisten Fällen gutartig und bildet nur in Ausnahmefällen Metastasen aus. Aufgrund des unterschiedlichen klinischen Verlaufs und der Invasivität werden Ameloblastome in vier Subtypen unterteilt: Solides konventionelles/multizystisches Ameloblastom Peripheres Ameloblastom Desmoplastisches Ameloblastom Unizystische Ameloblastom Mit über 80% ist der solide konventionelle oder multizystische der am häufigsten vertretene Typ (Jundt, 2006). Als klinische Zeichen treten für gewöhnlich Schwellungen, Schmerzen und Entzündungen auf. Weiters kann es durch die Schwellung zu Spannungen, oberflächlichen Erosionen, Bissverletzungen, Lockerung von Zähnen und im Oberkiefer zur Einschränkung der Nasenatmung bzw. Nasenbluten kommen. Makroskopisch zeigt sich eine grau-weiße, meist solide Struktur, welche zystenartige Räume unterschiedlicher Größe aufweisen kann. Aufgrund des charakteristischen semimalignen, lokal aggressiv invasiven Wachstums ist eine eindeutige radiologische beziehungsweise histologische Abgrenzung nicht möglich. Als radiologische Veränderung lässt sich eine Aufhellung im Sinne einer Osteolysezone erkennen, die mehr oder weniger scharf begrenzt sein kann und häufig eine seifenblasenartige Struktur aufweist. Resorptionen an Zähnen und Zahnwurzeln sind nicht eindeutig beweisend für das Ameloblastom, können jedoch als Zusatzbefund auftreten. In der Histologie der soliden konventionellen Ameloblastome unterscheidet man zwischen zwei Ausprägungen: Dem follikulären Typ, bei dem sich die 15 Epithelverbände zu einzelnen Inseln organisieren, und dem plexiformen Typ mit netzförmigen Verbänden. Diese Unterscheidung scheint jedoch keine prognostische Bedeutung zu haben. Meistens liegen diese Epithelverbände im lockeren Bindegewebe und werden durch reichliche Blutgefäße versorgt. Stellenweise kann das Epithel eine Plattenepithelmetaplasie oder auch basaloide Zellen enthalten. Durch Lyse des umgebenden Gewebes können sich zystenartige Hohlräume entwickeln. Für die Prognose ist die primäre chirurgische Therapie entscheidend. Es wird eine großzügige Resektion weit im Gesunden angestrebt, um das Risiko einer Rezidivbildung zu minimieren. Das periphere Ameloblastom tritt in etwa 2 – 10% der Fälle auf, zeigt einen Altersgipfel im 5. bis 7. Lebensjahrzehnt und neigt in 16-19% zur Rezidivbildung (Gardner, 2005). Die Lokalisation ist bei bezahntem Kiefer vorwiegend im Unterkiefer, bei zahnlosen Patienten in der alveolären Gingiva und befindet sich extraossär im submukösen Bindegewebe (Philipsen, 2001). Im Gegensatz zum soliden konventionellen Typ schließt eine invasive Osteodestruktion die Diagnose eines peripheren Ameloblastoms meist aus, aggressive Entartungen können jedoch in Einzelfällen auftreten. Das desmoplastische Ameloblastom zeigt histologisch eine Desmoplasie mit verstärkter Kollagenfaserbildung, erhöhter Zellularität und metaplastischer Knochenbildung und ist am Häufigsten im Frontzahnbereich anzutreffen. Das radiologische Bild zeigt gröbere Verdichtungen und das biologische Verhalten ist mit dem des konventionellen Ameloblastoms zu vergleichen (Jundt, 2006). Das seltene unizystische Ameloblastom zeigt ein vermehrtes Auftreten bei jüngeren Patienten mit einem Durchschnittsalter von 16 Jahren (Gardner, 2005). Makroskopisch präsentiert sich eine unilokuläre Osteolysezone, die meist mit einem retinierten Molaren assoziiert ist. Histologisch lassen sich zwei Subtypen unterscheiden: Eine luminale, auf das Zystenepithel beschränkte Form, und eine murale Form, bei der die Zystenwand infiltriert wird. Prognostisch führt nach Enukleation die murale Form durch ihr infiltrierendes Wachstum häufiger zu einer Rezidivbildung. Deshalb kann eine radikalere Resektion notwendig werden. Spätrezidive können noch Jahre nach Erstdiagnose auftreten, sodass enge Verlaufskontrollen notwendig sind. 16 1.5.1.2 Odontogener Plattenepitheltumor Der odontogene Plattenepitheltumor ist ein seltener benigner odontogener Tumor. Er wurde erstmals1975, bereits nach der ersten WHO-Klassifikation, von Pullon beschrieben (Pullon, et al., 1975). Er tritt bei beiden Geschlechtern gleich häufig auf, und sein Wachstum ist infiltrativ, aber nicht aggressiv. Er tritt bevorzugt paradental auf, was klinisch zu einer erhöhter Zahnmobilität führen kann. Radiologisch sind unspezifische, scharf begrenzte Osteolyszonen im Unterkiefer und Oberkiefer sichtbar, histologisch sind Plattenepithelinseln in lockerem Bindegewebe ohne Atypien oder Pleomorphie erkennbar. Als Therapie wird eine sorgfältige Kürettage, bzw. eine lokale Exzision im Gesunden empfohlen. Aufgrund vereinzelt beobachteter Rezidive sind regelmäßige Nachkontrollen unbedingt anzuraten. Aggressive Formen können gelegentlich mit dem Plattenepithelkarzinom, einem akanthomatösen Ameloblastom oder einem kalzifizierenden odontogenen Tumor verwechselt werden. (Gundlach, 2000) 1.5.1.3 Verkalkender epithelialer odontogener Tumor ( Pindborg-Tumor, CEOT) Der kalzifizierende epitheliale odontogene Tumor wurde 1955 von Pindborg aus der Gruppe der Ameloblastome herausgenommen und als eigenständiger odontogener Tumor definiert, da histologisch keine den Ameloblasten ähnliche Zellen nachzuweisen waren. Die Bezeichnung Pindborg-Tumor wird als Synonym für diese Tumorart verwendet. Er enthält deutlich mehr Verkalkungen als der Plattenepitheltumor und zeigt neben einem Plattenepithelverband stets allmählich kalzifizierende amyloidähnliche Ansammlungen. Radiologisch zeigen sich, im Unterschied zum Ameloblastom, immer Verkalkungsherde unterschiedlichen Ausmaßes. Rezidive wurden in etwa 15% der Fälle beobachtet, die Geschlechts- und Altersverteilung entspricht der des Amelobastoms. (Basu, et al., 1984) 17 1.5.1.4 Adenomatoider odontogener Tumor Der früher fälschlicherweise als Sonderform des Ameloblastoms beschriebene adenomatoide odontogene Tumor (Abb. 1) zeigt seinen Altersgipfel vor allem bei jüngeren Patienten, im Kindesalter. Ein Auftreten im Oberkiefer ist häufiger zu beobachten als im Unterkiefer, radiologisch kann das Bild eine follikuläre Zyste vortäuschen. Histologisch zeigen sich verkalkende dentinähnliche Hartgewebsablagerungen, sowie ringförmige Epithelstrukturen, die an quergeschnittene Drüsengänge erinnern. Das führte zu der alten Namensgebung „Adenoameloblastom“, und später zu der aktuellen Bezeichnung. Nach einer einfachen Ausschälung als Therapie der Wahl werden keine Rezidive beobachtet. (Gundlach, 2000) Abb. 1: Adenomatoider odontogener Tumor am linken Ramus mand. (LKH Graz) 1.5.1.5 Odontogener keratozystischer Tumor (vormals: odontogene Keratozyste/Primordialzyste) Der keratozystische odontogene Tumor (Abb. 2, Abb. 3) nimmt seit der ersten Beschreibung von Philipsen im Jahr 1956 eine Sonderstellung unter den odontogenen Tumoren ein. Aufgrund der wissenschaftlichen Evidenz, dass es sich dabei tatsächlich um eine zystische Neoplasie handelt, wurde der keratozystische odontogene Tumor vom vormals gängigen Namen „Keratozyste“ umgetauft. Es handelt sich dabei um eine entwicklungsbedingte zystische Neoplasie, welche aufgrund der Pathogenese und des klinischen Bildes eine Sonderrolle einnimmt 18 und einer speziellen therapeutischen und prognostischen Prozedur unterzogen werden muss. Charakteristisch für den keratozystischen odontogenen Tumor sind vor allem ein aggressives Wachstumsverhalten und eine hohe Rezidivrate, was besondere Anforderungen an die Therapie und Nachbetreuung stellt. Pathogenetisch entsteht der keratozystische odontogene Tumor aus primär versprengten Epithelien der Zahnleiste mit entsprechendem Differenzierungspotenzial. Er macht etwa 11% aller zystischen Prozesse der Mandilbula und Maxilla aus (Barnes, 2005). Dieser Tumor kann sporadisch auftreten, signifikant ist jedoch eine starke Häufung bei PatientInnen mit dem autosomal-dominant vererbten Gorlin-Goltz-Syndrom (Nävoid-Basalzell-Karzinom-Syndrom) (Woolgar, et al., 1987). Als anatomische Prädilektionsstelle des keratozystische odontogene Tumors wird in der Literatur in etwa 75% der Unterkiefer beschrieben, dabei vor allem der aufsteigende Unterkieferast, sowie der posteriore Unterkieferkorpus (Freier, et al., 2009; Böhme, et al., 1993).Im Oberkiefer sind hauptsächlich die Regionen der Molaren betroffen. Die Altersverteilung kann sehr unterschiedlich sein und wurde in der Literatur vor allem zwischen der 2. und 4. Lebensdekade beschrieben, wobei Männer etwas häufiger betroffen sind als Frauen. Histologisch zeigt sich eine dünne fibröse Kapsel, die charakteristisch durch ein verhorntes mehrschichtiges Plattenepithel ausgekleidet ist, das selten mehr als fünf Schichten und Para- oder Orthokeratose aufweist (Pindborg, et al., 1971). Die basale Zellschichte zeigt hochzylindrische Zellen in palisadenförmiger Anordnung mit gelegentlichen Zallatypien und Zelldysplasien (Shear, et al., 1976). Bei der Eröffnung des Zystenbalges entleert sich ein „vanillepuddingartiger“ Inhalt. Das Wachstum schreitet meist langsam voran und nur selten kommt es zu eindeutigen klinischen Beschwerden. Meist tritt aufgrund der intraspongiösen Ausbreitung als erstes Symptom ein Kippen bzw. eine Lockerung der Zähne auf, es kann aber auch zu Verlagerungen und Verdrängungen von noch nicht durchgebrochenen Zähnen kommen. Diese können trotz dessen meist vital bleiben und in der Regel keine eindeutigen Beschwerden beim Patienten hervorrufen. Bei Hinzutreten einer Entzündung kommt es zu klassischen Beschwerden, wie Schmerzen und Schwellungen (Schmid, et al., 2012). 19 Die Diagnose des keratozystischen odontogenen Tumors beruht meist auf einem radiologischen Zufallsbefund. Radiologisch manifestiert sich dieser Tumor als umschriebene, mehrkammerige, durch einen kortikalisierten Randsaum scharf begrenzte Läsion mit girlandenförmiger Umrisslinie, die durch lokale Osteolysen bedingt ist (Schwenzer, et al., 2009)(Abb. 3). Abb. 3: Keratozystischer odontogener Tumor im Bereich der linken Kieferhöhle (LKH Graz) Abb. 2: Keratozystischer odontogener Tumor am linken Ramus mandibulae (LKH Graz) Vor allem gegenüber dem Ameloblastom ist der keratozystische odontogene Tumor radiologisch nicht sicher abzugrenzen, da bei beiden eine multilokuläre Expansion und Mehrkammerigkeit auftreten können. Somit kann eine gesicherte Diagnose nur durch eine histologische Abklärung erfolgen. Therapeutisch ist eine vollständige Entfernung des keratozystischen odontogenen Tumors, inklusive der für das bloße Auge nicht sichtbaren Satelliten- und Tochterzellen, empfohlen. Eine histologische Abklärung des so gewonnenen Materials ist immer angezeigt. Bei relativ großen keratozystischen odontogenen Tumoren, beziehungsweise bei Rezidiven, kann außer der Resektion der eigentlichen Neoplasie, auch die Resektion des randständigen Knochens bzw. Kieferanteile notwendig werden, und somit zu konsekutiver plastischer Rekonstruktion führen. Rezidive entstehen meist aus übriggebliebenen Epithelinseln und Mikrozysten in der Bindegewebskapsel, aber auch durch Reimplantation und Invasion in die umgebenden Weichteile. Um im Rahmen der chirurgischen Entfernung der neoplastischen Anteile sämtliche Tochterzellen zu eliminieren, wurde in der 20 Literatur die Behandlung des Zystenlumens mittels Carnoy’scher Lösung, die Eisen-III-Chlorid, Essigsäure, Chloroform, und Ethylalkohol beinhaltet, empfohlen (Schwenzer, et al., 2009). Sie wird nach der Entfernung des Zystenbalges mittels Wattetupfer mehrmals in die Resektionshöhle eingebracht. Das geronnene Blut, sowie das nekrotische Material werden anschließend mit einer scharfen Kürette entfernt und die Höhle mit Kochsalzlösung gespült. Selbstverständlich ist dieses Prozedere bei Exposition freier Wurzeloberflächen oder des nervus alveolaris inferior kontraindiziert. Zur Minderung der Rezidivrate kann nach Entfernung des Zystenbalges auch ein Anfrischen der knöchernen Zystenwand mit einer Fräse durchgeführt werden, um mögliche Satellitenzysten zu erfassen (Jakse, 2004). Eine alleinige Zystostomie ist aufgrund der hohen Rezidivrate unbedingt abzulehnen. Die Rezidivrate wird in der Literatur je nach Behandlungsmethode mit einer breiten Streuung zwischen 2% und 63% beschrieben (Schroll, 1997). So zeigt sich bei radikaler Zystektomie die geringste, bei Zystostomien die höchste Rezidivneigung. Deshalb sollten postoperativ auf alle Fälle genaue Nachuntersuchungen in geringen Zeitabständen erfolgen, um ein möglichst frühes Einschreiten im Sinne einer einfachen Nachresektion zu gewährleisten. Bei multiplen Kieferzysten bereits in jungen Lebensjahren sollte unbedingt eine diagnostische Abklärung hinsichtlich eines Gorlin Goltz Syndroms stattfinden, und innerhalb der Familie eventuelle weitere Krankheitsträger ausgeforscht werden. 1.5.2 Odontogene epitheliale Tumoren mit odontogenem Ektomesenchym, mit oder ohne Hartsubstanzbildung 1.5.2.1 Ameloblastisches Fibrom und ameloblastisches Fibrodentinom Die bisher beschriebenen odontogenen Neoplasien zeigen aufgrund des epithelialen Ursprungs, keine mesektodermalen Reaktionen auf das neoplastische Gewebe. Die folgenden Tumortypen sind hingegen maßgeblich durch die Aktivität der Zellen des odontogenen Mesoektoderms gekennzeichnet, das dem Neutralleistenmaterial entstammt. Das ameloblastische Fibrom wurde vor mehr als 40 Jahren fälschlicherweise zu den Ameloblastomen gezählt, da histologisch ein mesenchymales Bindegewebe 21 sichtbar ist, in das Stränge odontogenen Epithels eingestreut sind. Den Altersgipfel bilden vor allem jugendliche Patienten. Mädchen und Buben sind gleichermaßen betroffen und als Prädilektionsstelle wird in der Literatur der dorsale Unterkiefer genannt. (Gundlach, 2000). Radiologisch sind Radioluzenzen ohne Verkalkungsherde sichtbar und, im Gegensatz zum Ameloblastom, wird ein nicht aggressives Wachstum beschrieben. Rezidive treten selten auf, trotzdem sollte nach einer sorgfältigen operativen Entfernung ein engmaschiges Recall zur Früherkennung erfolgen. Die maligne Form des ameloblastischen Fibroms, das ameloblastische Sarkom tritt extrem selten auf. 1.5.2.2 Ameloblastisches Fibro-Odontom und Odonto-Ameloblastom Diese sehr seltene Art von odontogenen Tumoren hat seinen Altersgipfel im Kindes- beziehungsweise frühen Jugendalter und betrifft beide Geschlechter etwa im gleichen Ausmaß. Es tritt häufiger im Unterkiefer auf und wird vor allem in distalen Abschnitten angetroffen. Radiologisch stellt sich das ameloblastische Fibro-Odontom meist als eine schmelzdichte Verschattung über einem retinierten Zahn dar, die von einem osteolytischen Hof umgeben ist. Histologisch zeigen sich schmale Züge odontogenen Epithels in Unterscheidungsmerkmal einem vom zellreichen Ameloblastom proliferierenden zeigen sich Stroma. Als pulpa-ähnliche Mesenchymalabschnitte, sowie eine Bildung von Zahnhartsubstanzen im Stroma, die durch ihre Anordnung an Zähne erinnern können. Auch hier ist die Enukleation das Mittel der Wahl zur Therapie. Rezidive sind relativ selten (Jundt, 2006). Aufgrund der mehrfach beschriebenen aggressiven Wachstumstendenzen, ist vom ameloblastischen Fibro-Odontom das Odonto-Ameloblastom abzugrenzen. Auch hier findet man einen Altersgipfel bei etwa 15 Jahren und die Häufigkeit der Lokalisationen entspricht ebenso dem ameloblastischen Fibro-Odontom. Radiologisch ist meist kein retinierter Zahn angrenzend, jedoch zeigt sich ebenso eine schmelzdichte Verschattung mit osteolytischem Randsaum. Als therapeutischer Ansatz gilt wie beim Ameloblastom die komplette chirurgische Entfernung (Jundt, 2006). 22 1.5.2.3 Kalzifizierender zystischer odontogener Tumor/ verkalkende odontogene Zyste und dentinogener Schattenzell-haltiger Tumor In der neuersten WHO-Klassifikation wird die vormals als Zyste bezeichnete Läsion nunmehr als zystischer Tumor bezeichnet. Sie gehört zu den sogenannten gemischt odontogenen Tumoren, die zu Neoplasien von epithelialen sowie mesenchymalen odontogenen Anteilen, gezählt werden (Gundlach, 2000). Es ist kein eindeutiger Altersgipfel festzustellen, sodass ein Auftreten in jedwedem Alter stattfinden kann. Auch eine eindeutige geschlechterspezifische Häufung ist nicht feststellbar. Als Prädilektionsstellen des kalzifizierenden zystischen odontogenen Tumors sind meist der Frontzahnbereich, sowie der vordere Seitenzahnbereich beschrieben. Zu 80% liegen diese Läsionen intraossär, und zu 20% gingival (Jundt, 2006). Die Symptome sind meist unspezifisch und stellen sich meist nur als eine schmerzlose Schwellung mit leichter Größenprogredienz dar. Radiologisch imponiert dieser Tumor vor allem als unilokuläre, unregelmäßig begrenzte kleine Osteolysezone mit einstrahlenden, irregulär verteilten Verkalkungsherden. In bis zu einem Drittel der Fälle tritt dieser Tumor zusammen mit einem retinierten Zahn auf (Buchner A, 1990). Das histologische Bild zeigt einen Zystenbalg mit einer Basalschicht und darüber liegenden sternförmigen Zellen, die an das Schmelzorgan eines sich bildenden Zahnes erinnern. In dieser Epithelschicht zeigen sich die für die Namensgebung dieses Tumors spezifischen Schattenzellen oder ghost-cells. Die Zellkerne dieser Zellen verdämmern, die Zellgrenzen sind jedoch meist gut erhalten und zeigen eine Verkalkungstendenz. Gelegentlich können sich kleine Ablagerungen von Dentin-ähnlichem Material an der Unterfläche der Basalzellschicht entwickeln (Jundt, 2006). Der maligne Typ dieses odontogenen Tumors tritt äußerst selten auf und wird als schattenzellhaltiges odontogenes Karzinom bezeichnet. Als Therapie ist auch in diesem Fall die chirurgische Enukleation angezeigt. Rezidive werden nur selten beschrieben. Aufgrund einer häufigen Kombination mit anderen odontogenen Tumoren, wie den Odontomen, aber auch Ameloblastomen, richtet sich die Therapie immer nach der aggressivsten Komponente. Im 23 Allgemeinen sollte der schattenzellhaltige Tumor aufgrund seines infiltrativen Wachstums weit im Gesunden reseziert werden (Ledesma-Montes, et al., 2008). 1.5.2.4 Odontom Das Odontom kann in zwei verschiedene Typen unterteilt werden. Man unterscheidet zwischen dem komplexen Odontom und dem Verbund-Odontom. Beide Typen zeigen Altersgipfel in der zweiten Lebensdekade, jedoch keine spezifischen Häufungen nach Geschlecht. Die häufigste Lokalisation ist beim Verbund-Odontom der Frontzahnbereich, vor allem im Oberkiefer. Das komplexe Odontom tritt bevorzugt im Seitenzahnbereich des Unterkiefers auf (Jundt, 2006). Auch bei diesen odontogenen Tumoren ist oft ein Auftreten an retinierten Zähnen feststellbar. Die Symptome sind auch hier unspezifisch und zeigen als erstes Zeichen meist eine schmerzlose Schwellung. Radiologisch lassen sich beim komplexen Typ ungeordnete knochen- und schmelzdichte Verschattungen feststellen, beim Verbund-Odontom kann man sogar kleine zahnartige Gebilde erkennen (Abb. 4). Diese Eigenheiten spiegeln sich auch im histologischen Bild wieder: Zu erkennen sind meist ungeordnete Hartzahnsubstanzen von Schmelz, Dentin und Zement. Es können aber auch Reste von Odontoblasten- und Ameloblastensäumen nachgewiesen werden. Abb. 4: Röntgenbilder mehrerer Odontome (LKH Graz) 24 1.5.3 Odontogene ektomesenchymale Tumoren mit oder ohne inkorporiertes odontogenes Epithel 1.5.3.1 Odontogenes Fibrom Dieser odontogene Tumor wird zu den bindegewebigen Neoplasien gezählt, die ihren Ursprung im Mesoektoderm nehmen (Gundlach, 2000). Das odontogene Fibrom, nicht zu verwechseln mit dem ameloblastischen Fibrom, kann in zwei Typen unterteilt werden: Der zentrale Typ ist überwiegend bei Frauen zu finden, der periphere bei Männern (Slabbert H, 1991). Bei der Altersverteilung zeigt sich ein überwiegend gleichbleibender Verlauf und es sind keine eindeutigen Spitzen feststellbar. Diese Läsionen treten bevorzugt in der Prämolarenregion des Unterkiefers auf. Radiologisch zeigen sich gut begrenzte, rundliche Radioluzenzen, die meist in Kontakt zu Zahnwurzeln stehen. Diese Nähe kann zu Wurzelresorptionen, aber auch zu Verlagerungen und Kippungen von Zähnen führen. Größere Fibrome können multilokulär auftreten und zeigen einen partiell sklerotischen Randsaum (Jundt, 2006). Histologisch lässt sich das odontogene Fibrom in einen epithelreichen und einen epithelarmen Typ einteilen. Makroskopisch präsentiert es sich weiß, solide und zeigt nur eine sehr geringe Infiltrationstendenz. Aus diesem Grund ist das therapeutische Mittel der Wahl die Enukleation der oft gut begrenzten Läsion. Rezidive wurden nur selten beobachtet. 1.5.3.2 Myxom (odontogenes Myxom, Myxofibrom) Das odontogene Myxom gilt nach dem Ameloblastom, als zweithäufigster aggressiver odontogener Tumor und tritt praktisch nur im Kieferwinkelbereich auf (Gundlach, 2000). Es hat seinen Altersgipfel in der 2. bis 4. Lebensdekade und zeigt sich nur selten im Kindesalter. Frauen sind dabei etwas häufiger betroffen. In zwei Drittel der Fälle tritt dieser odontogene Tumor im Unterkiefer, vor allem in der Molarregion auf (Jundt, 2006). Radiologisch stellt sich das Myxom anhand von multilokulären, seifenblasenartigen Osteolysen dar, die oft eine Trabekulierung aufweisen können. Meist zeigt sich eine scharfe Begrenzung und Verdrängung von Zähnen, wobei auch eine Nähe zu retinierten Zähnen bestehen kann. 25 Das histologische Bild variiert stark. Es präsentieren sich myxomatöse Strukturen, die durch ihre faserarme Struktur der Zahnpulpa ähneln. Das Tumorgewebe ist zellarm und besitzt eine stark aufgelockerte, helle Zwischensubstanz, die stellenweise Kollagenfasern aufweist. Die Zellen sind meist spindelig oder sternförmig und zeigen meist monomorphe, ovale Keime (Jundt, 2006). In bis zu 25% der operierten Fälle zeigen sich Rezidive (Kaffe, et al., 1997). Aufgrund des infiltrativen Wachstums sind eine sorgfältige Ausschälung des Tumors, sowie regelmäßige Nachkontrollen essentiell, um einen dauerhaften Therapieerfolg zu gewährleisten. 1.5.3.3 Zementoblastom Seit der neuen WHO-Klassifikation wird von vormals vier Zementomen heute nur noch das Zementoblastom als das „wahre Zementom“ angeführt. Dieser odontogene Tumor wird als ein äußerst gutartiger Tumor beschrieben, er tritt etwas häufiger bei Männern auf und zeigt seinen Altersgipfel in der 2. Lebensdekade, wobei Fälle im Alter vom 1. bis 6. Lebensjahrzehnt beschrieben wurden (Brannon, et al., 2002). In etwa 80% der Fälle tritt das Zementoblastom im Unterkiefer auf, vor allem an den Wurzeln des zweiten Prämolaren oder des ersten Molaren (Gundlach, 2000). Radiologisch zeigt sich eine meist kugelige, radioopake oder scharf begrenzte Osteolyse an der Wurzelspitze, die mit zunehmendem Alter der Läsion mit einem homogenen knochendichten Material ausgefüllt wird. Der Parodontalspalt ist dabei obliteriert. Es kann teilweise auch eine Resorption von Zahnwurzeln beobachtet werden (Jundt, 2006). Histologisch besteht die Läsion aus großen Mengen beinahe zellfreier Hartsubstanz, die in ein zelldichtes Stroma eingebettet ist. Durch die verschiedenen Anbauschübe können Kittlinien entstehen, die auch an die eines Morbus Paget erinnern können. In der Literatur gibt es verschiedene Auffassungen über die Rezidivrate, wobei nach neuersten Untersuchungen von einer Rezidivneigung in etwa 20% der Fälle ausgegangen werden muss. Somit sollten Zementoblastome zusammen mit den betroffenen Zähnen entfernt und der angrenzende Knochen großzügig ausgefräst werden (Brannon, et al., 2002). 26 1.6 Bösartige Läsionen 1.6.1 Odontogene Karzinome 1.6.1.1 Metastasierendes Ameloblastom (früher: malignes Ameloblastom) Radiologisch und histologisch unterscheidet sich der vormals als malignes Ameloblastom bekannte Tumor nicht wesentlich von einem konventionellen Ameloblastom. Die Diagnose wird beeinflusst durch den klinischen Verlauf und die Feststellung von Metastasen (Klöppel, et al., 2009). Ein wesentlicher Hinweis sind Metastasen in Lymphknoten oder Knochengeweben, wobei immer ein zusätzliches Tumorgeschehen ausgeschlossen werden muss. Betroffen sind alle Altersgruppen und beide Geschlechter, jedoch kann der Zeitraum zwischen Diagnosestellung und Metastasierung sehr groß sein. Metastasen treten am häufigsten in der Lunge auf, seltenerer in Lymphknoten, Pleura, Skelett, Nieren und Milz. Die Therapie besteht immer in einer weiten Resektion im Gesunden (Schwenzer, et al., 2009). 1.6.1.2 Ameloblastisches Karzinom Das ameloblastische Karzinom ist ein sehr seltener odontogener Tumor und tritt in allen Altersgruppen auf. Es ist in annähernd 80% der Fälle im Unterkiefer lokalisiert. Radiologisch zeigt sich im Gegensatz zu benignen Ameloblastomen ein etwas aggressiveres, knochendestruktives Bild und es können gelegentlich Kalzifikationen auftreten, die dystropischen Verkalkungen entsprechen (Jundt, 2006). Ameloblastische Karzinome, die sich auf dem Boden eines Ameloblastoms entwickeln, werden als sekundäre oder dedifferenzierte ameloblastische Karzinome bezeichnet. Sie treten nur sehr selten, vor allem bei älteren Patienten mit lang bestehenden Ameloblastomen, auf (Jundt, 2006). Histologisch zeigen sich oft atypische Kerne, eine erhöhte Mitoseaktivität, eine verschobene Kern-Plasma Relation, sowie gelegentlich nekrotische Areale. Die Prognose ist trotz einer Therapie mittels Resektion im Gesunden eher ungünstig. Immer wieder können selbst Jahre nach der chirurgischen Entfernung Rezidive, beziehungsweise Metastasen auftreten. Todesfälle werden noch 10 Jahre nach durchgeführter Therapie beobachtet (Jundt, 2006). Eine 27 Verbesserung des Outcomes durch eine adjuvante Radiatio bzw. Chemotherapie wird untersucht, es können aber noch keine eindeutigen Empfehlungen dafür ausgesprochen werden (Dhir, et al., 2003). 1.6.1.3 Primäres intraossäres Karzinom Das primäre intraossäre Karzinom ist ein extrem seltener Tumor und scheint von den Überresten des odontogenen Epithels abzustammen, kann sich aber auch auf dem Boden eines odontogenen keratozystischen Tumors oder einer odontogenen Zyste entwickeln (Schwenzer, et al., 2009). Männer sind etwa doppelt so häufig betroffen wie Frauen und das Durchschnittsalter beträgt 55 Jahre. Prädestinierte Lokalisationen sind vor allem die Areale der distalen Mandibula (Jundt, 2006). Radiologisch lassen Kortikalisdestruktionen sich erkennen. irregulär begrenzte Histologisch zeigt Osteolysen sich ein Bild und eines Plattenepithelkarzinoms sowohl in seiner verhornenden als auch in seiner nichtverhornenden Form. Als therapeutische Option zeigt sich auch hier die radikale Resektion als Mittel der Wahl. Die Notwendigkeit einer Entfernung der Lymphknoten und einer adjuvanten Radiatio wird in der Literatur diskutiert. In den meisten Fällen, in denen eine Lymphknotenausräumung mittels Neck-Dissection durchgeführt wurde, wurden keine Metastasen festgestellt. Treten Metastasen auf, wird, die Prognose sehr ungünstig (Nölken, et al., 2006). Die alleinige chirurgische Therapie führt in den meisten Fällen zu sehr guten Ergebnissen, wobei der Einsatz der Radiotherapie in den meisten Berichten keine wesentlichen Verbesserungen der Prognose zeigt (Nölken, et al., 2006). 1.6.1.4 Klarzelliges odontogenes Karzinom Dieses erst seit der neuen WHO-Klassifikation unter den odontogenen Tumoren aufgeführte Karzinom, tritt bei Patienten zwischen 14 und 89 Jahren auf, wobei Frauen etwa dreieinhalbmal so häufig betroffen sind wie Männer. Insgesamt ist dieser Tumor jedoch sehr selten und es wurden bisher erst etwa 50 Fälle publiziert (Jundt, 2006). Als prädestinierte Lokalisation sind vor allem zahntragende Abschnitte des Unterkiefers zu nennen. Radiologisch können sich irreguläre, meist unscharf begrenzte Osteolysezonen 28 darstellen, die auch Wurzelresorptionen verursachen und in Einzelfällen Verdichtungen aufweisen können. Histologisch lassen sich Gruppen von Zellen mit mittelgroßen Kernen, die von einem gut abgegrenzten, vakuolisierten hellen Zytoplasma umgeben sind, erkennen, die in ein mäßig zelldichtes Bindegewebe eingebettet sind (Schwenzer, et al., 2009). Die meisten beschriebenen klarzelligen odontogenen Tumoren weisen eine relativ aggressive Wachstumsneigung mit häufiger Lymphknotenmetastasierung und Rezidivbildung auf. Aus diesem Grund sollte eine Resektion sicher im Gesunden durchgeführt werden. Zu diesem Zweck eignet sich die radikale Chirurgie mittels Neck-Dissection (Jundt, 2006). Von diesem odontogenen Tumor abzugrenzen sind die sich häufig ähnlich darstellenden Metastasen eines Nierenzellkarzinoms oder eines Mukoepidermoidkarzinoms. 1.6.1.5 Schattenzell-haltiges odontogenes Karzinom Das schattenzell-haltige odontogene Karzinom ist ein sehr seltener Tumor, der das erste Mal im Jahr 1971 dokumentiert wurde und 2005 in die neue WHOKlassifikation aufgenommen wurde. Er zeigt sich vor allem bei asiatischen Männern in der 3. Lebensdekade und ist überwiegend im Oberkiefer lokalisiert (Zhi-Jun, et al., 2007). Radiologisch finden sich schlecht umschriebene, osteolytische Radioluzenzen, die radioopake Strukturen beinhalten können. Auch Zahnverlagerungen, Wurzelresorptionen und impaktierte Zähne können auftreten (Jundt, 2006). Das schattenzell-haltige odontogene Karzinom kann auf Basis des verkalkenden odontogenen Tumors entstehen und präsentiert somit auch im histologischen Bild Ähnlichkeiten. Es zeigen sich eine erhöhte Mizosezahl und eine hohe Proliferationsaktivität, sowie eine Ansammlung atypischer, kleiner, basaloider Zellen mit dunklen Kernen, aber auch größerer Zellen mit vesikulären Kernen und den für den Tumor namensgebenden Schattenzellen. Aufgrund des infiltrierenden und zum Teil aggressiven Wachstums sollte therapeutisch eine Resektion im Gesunden angestrebt werden (Zhi-Jun, et al., 2007). 29 1.6.2 Odontogene Sarkome 1.6.2.1 Ameloblastisches Fibrosarkom Das ameloblastische Fibrosarkom ist ein sehr seltener maligner odontogener Tumor und besteht aus einem gutartigen epithelialen und einem bösartigen mesenchymalen Anteil. Es wird als der maligne Gegenpart zum gutartigen ameloblastischem Fibrom angesehen. Zwei Drittel dieser Tumoren entstehen de novo, der Rest entsteht auf Basis rezidivierender ameloblastischer Fibrome oder ameloblastischer Fibro-Odontome (Slootweg, 2013). Die meisten bis jetzt dokumentierten Fälle wurden bei Patienten unter 40 Jahren diagnostiziert und in zwei Dritteln der Fälle waren Männer betroffen. Der posteriore Unterkiefer war die am häufigsten befallene Region. Etwa 40% der therapierten Tumoren entwickelten ein neuerliches Rezidiv, Metastasen waren jedoch sehr selten (Jundt, 2006). Radiologisch sind ausgedehnte Osteolysen mit meist scharfer Begrenzung zu sehen. Histologisch zeigen sich Inseln odontogenen Epithels mit Palisadierung der randständigen Zellen. Das umgebene zelldichte Stroma zeigt eine mäßige bis starke Polymorphie der Zellen und Zellkerne (Kobayashi, et al., 2005). Auch hier ist die radikale chirurgische Entfernung des Tumors die angestrebte Therapie. Aufgrund der Seltenheit von Metastasen, sollte aber von einer NeckDissection abgesehen werden (Jundt, 2006). 1.6.2.2 Ameloblastisches Fibro-Odontosarkom Das ameloblastische Fibro-Odontosarkom wurde bis jetzt erst in etwa 20 Fällen eindeutig diagnostiziert. Die Histologie entspricht dem des ameloblastischen Fibrosarkoms, das jedoch Anteile von dysplastischem Dentin und Schmelz zeigt. Aufgrund der Seltenheit dieses Tumors sind keine eindeutigen Aussagen bezüglich Aggressivität, Therapie und Prognose zu stellen. 30 1.7 Differentialdiagnosen odontogener Tumoren Aufgrund der Ähnlichkeit der Symptomatik und der radiologischen Darstellung wird in diesem Kapitel zum besseren Verständnis und Abgrenzbarkeit auf die wichtigsten Differentialdiagnosen zu odontogenen Tumoren eingegangen. 1.7.1 Zystische Läsionen Die wichtigste Differentialdiagnose zu odontogenen Tumoren sind unterschiedliche Kiefer- und Weichteilzysten. Bei der Klassifikation durch die WHO (Kramer, et al., 1993) wird, ebenso wie bei den odontogenen Tumoren, die mögliche Genese und die Herkunft des Epithels berücksichtigt. Man unterscheidet zwischen nicht-epithelialen Kieferzysten, die als nicht-neoplastische Knochenläsionen definiert werden, und epithelialen Zysten, die wiederum in entwicklungsbedingte, odontogene Zysten und entzündungsbedingte radikuläre Zysten unterteilt werden (Tab. 1). Epitheliale Zysten Entwicklungsbedingte Zysten Entzündungsbedingte Zysten Odontogene Zysten: Radikuläre Zysten: Follikuläre Zysten Residuale radikuläte Zysten Gingivale Apikale und laterale radikuläre Zysten Perlen) Parodontale Zysten Eruptionszyste Entzündliche kollaterale Zysten Laterale parodontale Zysten Gingivale Zysten des Erwachsenen Glanduläre odontogene Zysten Kalzifizierende odontogene Zysten Nicht odontogene Zysten Nasolabiale / Nasoalveoläre Zysten Zysten des Ductus palatinus Zyste bei Kindern (Epstein Nicht-epitheliale Zysten Solitäre Knochenzyste Aneurysmatische Knochenzyste Staphnezyste Tab. 1: Eintelung der Zysten im Mund- Kiefer-und Zahnbereich (Jundt, 2006) 31 Eine Mehrzahl der radikulären Zysten findet sich mit etwa 58% im Oberkiefer (Böhme, et al., 1993). Odontogene Zysten hingegen sind mit 64% eher im Unterkiefer anzutreffen. Dies lässt sich durch den Umstand erklären, dass es vorwiegend im Unterkiefer zu Zahnretentionen, und somit zu Ausweitungen des Zahnsäckchens mit der Komplikation einer Zyste kommt. Die richtige Unterscheidung zwischen odontogenen Tumoren und Zysten stellt eine wichtige Aufgabe dar, um die Therapie sowie die Rezidivkontrollen richtig anpassen zu können. 1.7.1.1 Follikuläre Zyste Follikuläre Zysten sind in der allgemeinen Zahnarzt-Praxis relativ selten zu sehen. Sie finden sich vor allem bei retinierten oberen Eckzähnen, unteren Weisheitszähnen, sowie Prämolaren. Bevorzugt treten follikuläre Zysten bei Männern zwischen dem 20 und 40 Lebensjahr auf (Weiss, et al., 2011). Sie können auch mit genetischen Defekten assoziiert sein. Beispielsweise finden sich diese Zysten vermehrt bei Patienten mit angeborenen Dentinhyperplasien, Dysostosis deidocranialis und dem Klippel-Feil-Syndrom. Typisch ist eine Entstehung im Bereich der Zahnkronen von noch nicht durchgebrochenen Zähnen. Radiologisch zeigt sich ein gut begrenzter, rundlicher, osteolytischer Bereich an einem retinierten Zahn. Der Zystenbalg inseriert an der Schmelz-Zement-Grenze (Fehler! Verweisquelle konnte nicht gefunden werden.). Der Hohlraum wird von einem zweischichtigen Epithel begrenzt, selten findet man verhornendes Plattenepithel oder Flimmerepithel. Eine wichtige Komplikation, die ausgeschlossen werden muss, ist eine Ausartung zu einem Ameloblastom, das meist einem plexiformen Typus entspricht. Auch eine mögliche Entartung des auskleidenden Plattenepithels zu einem Karzinom wurde beschrieben (Jundt, 2006). Als Therapie kommen eine zahnerhaltende Zystektomie oder eine nicht zahnerhaltende Extirpation der Zyste samt retiniertem Zahn in Frage. In beiden Fällen muss eine histologische Begutachtung stattfinden, um ein malignes Geschehen ausschließen zu können. 32 Abb. 5: Follikuläre Zyste (Weiss, et al., 2011) 1.7.1.2 Eruptionszyste (Dentitionszyste) Als Eruptionszyste bezeichnet man eine Zyste, die sich während der Dentition (meist von Milchzähnen) kappenartig oberhalb der Zahnkrone bildet (Weiss, et al., 2011). Diese Zyste ist eine Sonderform der follikulären Zyste und weist somit von ihrer Genese her große Ähnlichkeiten mit jener auf. Der Hohlraum wird von einem mehrschichtigen Plattenepithel ausgekleidet. In der Regel sind diese Zysten gutartige Gebilde und schmerzlos, können jedoch den Grundstein für eine Dentitio difficilis bilden. Meist kommt es zu einer spontanen Ruptur ohne Therapieindikation. Kommt es zu hingegen einer schmerzhaften Entzündung, ist die gängigste Therapie eine Gingivektomie mit Entfernung des Zystenbalgs. 1.7.1.3 Laterale parodontale Zyste Die laterale parodontale Zyste entsteht aus verschiedenen Teilen odontogener Epithelresten zwischen den Wurzeln von vitalen Zähnen. Bei dieser Zyste handelt es sich mit einem Anteil von 0,4% an allen odontogenen Zysten um eine seltene Pathologie (Jones, et al., 2006;). Der Häufigkeitsgipfel zeigt sich zwischen dem 4. bis 7. Lebensjahrzehnt. Meistens sind sie im Gebiet der unteren Prämolaren und Eckzähne lokalisiert, gefolgt vom Oberkiefer anterior der ersten Prämolaren, (Siponen, et al., 2011). Ausschlaggebend für die Bildung der lateralen 33 parodontalen Zyste können reduziertes Schmelzepithel, Reste der Zahnleiste oder Malassezsche Zellreste sein (Wangerin, 2009). Im Röntgen ist eine unspezifische, gut abgegrenzte, runde bis ovale, unilokuläre Radioluzenz, mit sklerotischen Rändern in interradikulärer Lage, gelegentlich mit einem sklerosierendem Rand zu sehen (Abb. 6). Histologisch ist die Zyste von einem dünnen, nicht keratinisierten, squamösen oder kuboiden Epithel ausgekleidet. Eine Divergenz bzw. Lyse der Wurzeln kann auftreten. Abb. 6: Laterale Parodontale Zyste (Weiss, et al., 2011) 1.7.1.4 Glanduläre odontogene Zyste Diese Zyste entsteht oberhalb des Knochens in den zahntragenden Arealen des Kiefers und ist sehr selten (Wangerin, 2009). Charakteristisch sind eine epitheliale Auskleidung mit kuboiden oder säulenförmigen Zellen und ein langsames Wachstum. Histologisch zeigt sich das Epithel teilweise squamös und die oberflächlichen Schichten können teils zilienartige, aber auch Muzin produzierende Zellen beinhalten. Der Anteil dieser Zysten an allen odontogenen Zysten liegt bei 0,2 %, das mittlere Alter der Patienten beträgt 46 Jahre und das zahlenmäßige Verhältnis von Männern zu Frauen ist 1,3:1, der Unterkiefer ist mit 70 % deutlich häufiger betroffen als der Oberkiefer (Kaplan, et al., 2008). Die glanduläre odontogene Zyste zeigt ein expansives, lokal aggressives Wachstumsmuster, sowie Wurzelresorptionen, Osteolyse der Kortikalis und Extension in die Weichgewebe (Siponen, et al., 2011). Glanduläre odontogene Zysten können eine beträchtliche Größe annehmen, was meist zu einem erhöhten Rezidivrisiko führt (Weiss, et al., 2011) (Abb. 7). Klinisch können sich Gesichtsasymmetrien oder –schwellungen zeigen, radiologisch uni- oder multilokuläre Aufhellungen mit scharf begrenzten Rändern. 34 Angrenzende Zähne können Wurzelresorptionen oder Dislokationen aufweisen. Abb. 7: Glanduläre odontogene Zyste (Weiss, et al., 2011) 1.7.1.5 Gingivale Zyste Bei der Gingivalen Zyste handelt es sich um eine Läsion, die aus der Gingiva oder der alveolären Mukosa, und nicht aus dem Alveolarknochen stammt (Kelsey, et al., 2009). Sie tritt überwiegend in der unteren Eckzahn- und Prämolarenregion, sowie im Oberkiefer auf, meist im Bereich der Schneide- und Eckzähne. Der Häufigkeitsgipfel liegt zwischen dem 5. und 6. Lebensjahrzehnt, Frauen sind leicht häufiger betroffen als Männer (Kelsey, et al., 2009). Radiologisch zeigt sich meist eine kleine scharf begrenzte Radioluzenz. Klinisch präsentiert sich eine unilaterale kleine Schwellung an der fazialen Seite der Gingiva, die mit Flüssigkeit gefüllt sein kann (Abb. 8). Die Größen variieren zwischen 5mm bis 10mm. Differentialdiagnostisch kommen Läsionen mit gingivaler Schwellung in Frage. Ein peripheres Fibrom, ossifizierendes Fibrom, Riesenzellgranulom bzw. eine Mukozele sind abzuklären. Als Therapie wird meist eine einfache Exzisionsbiopsie durchgeführt. 35 Abb. 8: Gingivale Zyste (Weiss, et al., 2011) 1.7.1.6 Pseudozyste Als Pseudozyste bezeichnet man einen Hohlraum des Knochens, bei dem die Epithelauskleidung fehlt. Man kann zwischen drei Typen differenzieren: der solitären, der aneurysmatischen, sowie der latenten Pseudozyste. Aufgrund der klinischen und radiologischen Symptomatik sind Pseudozysten nicht eindeutig den Zysten zuzuordnen und gehören den nicht-neoplastischen Knochenläsionen an. Eine Beschwerdesymptomatik ist nur sehr selten festzustellen, die radiologische Darstellung kann jedoch einer echten Zyste oder einem odontogenen Tumor ähneln, eine weitere Abklärung ist meist angeraten. Empfehlenswert ist eine radiologische Verlaufsbeobachtung nach zwei Monaten, einem halben und einem Jahr und die Überprüfung der Befundänderungen. Tritt keine Veränderung ein, so ist eine Therapie nicht erforderlich. Eine operative Revision sollte nur in Einzelfällen aus differenzialdiagnostischen Erwägungen erfolgen (Jundt, 2006). 1.7.1.7 Keratozystische odontogene Zyste Die kalzifizierende odontogene Zyste wird in der neuen WHO-Klassifikation zu den odontogenen Tumoren gezählt, und wird somit erst im nächsten Kapitel behandelt. 1.7.2 Zentrales Riesenzellgranulom Das zentrale Riesenzellgranulom ist eine Läsion der Kieferknochen, die sporadisch oder im Zusammenhang mit anderen Erkrankungen, vor allem einem Hyperparathyreoidismus, vorkommen kann. Erstmals beschrieben wurde die Läsion als eine lokal reparative Reaktion des Knochens auf ein vorangegangenes 36 Trauma bzw. eine Blutung (Jaffe, 1953). In der neuesten WHO-Klassifikation wird das zentrale Riesenzellgranulom als zentrale Riesenzellläsion bezeichnet, deren histologisches Bild von Ansammlungen mehrkerniger Riesenzellen in einem Spindelzellenstroma geprägt wird. Da der vermutete Zusammenhang zwischen Traumatisierung und Entstehung der Läsion nicht für alle zentralen Riesenzellgranulome nachvollzogen werden kann, gilt die Ätiologie als ungeklärt. Das zentrale Riesenzellgranulom zeigt seinen Häufigkeitsgipfel bei zumeist jungen PatientInnen bis zur 3. Lebensdekade und betrifft Frauen häufiger als Männer. Es ist überwiegend in den zahntragenden Kieferanteilen lokalisiert, wobei die Läsion häufiger in der Mandibula als in der Maxilla zu finden ist. Klinisch kann meist eine schmerzlose Schwellung beobachtet werden. Das Wachstum ist meist expansiv osteolytisch und in etwa 12% der Fälle treten Rezidive auf (Driemel, et al., 2005). Radiologisch tritt das zentrale Riesenzellgranulom als Knochenaufhellung mit einoder mehrkammeriger Architektur auf. Als Therapieformen werden klassischerweise eine Kürettage bzw. eine en-blocResektion, seltener eine Applikation von Calcitonin, ortikosteroiden oder Interferon angewendet (Feyerling, et al., 2005). 37 2 ZIELSETZUNG In der vorliegenden Arbeit sollten zunächst die allgemeine Onkologie des Kiefers, danach die Zahnentwicklung, anschließend die Klassifikation odontogener Tumoren, ihre Ätiologie und ihr Entstehungsmechanismus, sowie die Diagnose, mögliche Differentialdiagnosen und Therapieansätze beziehungsweise entsprechende Behandlungskonzepte beschrieben werden. Im Rahmen einer retrospektiven Analyse sollten Daten des pathologischen Institutes der Universitätsklinik Graz über odontogene Tumoren aus den Jahren 2004 bis 2012 gesammelt, und mit in nationaler und internationaler Literatur beschriebenen, aktuellen Studien verglichen werden. Weiters sollen die Ergebnisse der retrospektiven Analyse, als Ausgangspunkt der Hypothesengenerierung für nachfolgende Studien dienen. Als Grundlage für die Erhebung der Patientendaten dienten die histopathologischen Auswertungen des Pathologischen Institutes, sowie die Aufzeichnungen in den Operationsbüchern der klinischen Abteilung für Mund-, Kiefer- und Gesichtschirurgie der Medizinischen Universität Graz. Zusätzlich wurden diese Daten mit den histopathologischen Auswertungen der Universitätsklinik für Zahn- Mund und Kieferheilkunde Graz verglichen. Einzug in die Studie fanden Patienten, die einem operativen Eingriff mit Verdacht auf einen odontogenen Tumor unterzogen wurden, bzw. nach einem Exzisionspräparat die Diagnose “Odontogener Tumor“ erhalten haben. Da es sich um eine retrospektive Auswertung von Patientendaten handelt, ziehen eingeschlossene Patienten keinen direkten Nutzen aus der Studie. Gleichzeitig ist für sie auch kein Risiko zu erwarten, besonders da alle Patientendaten, um ein Bekanntwerden sensibler personenbezogener Daten weitgehend zu verhindern, k-anonymisiert wurden und Zugriffsbeschränkungen unterlagen. Die Auswertung der Patientendaten soll einen Überblick über die Alters- und Geschlechtsverteilung der betreffenden Diagnosen in der Zeit zwischen 01.01.2004 und 31.12.2012 liefern, sowie etwaige Veränderungen in Bezug auf Tumorgenese, Schweregrad und Häufungen innerhalb des untersuchten 38 Zeitraums darlegen. Weiters sollen die Häufigkeit und Art einer notwendig gewordenen operativen Knochen- oder Weichgewebsrekonstruktion untersucht werden. Ferner soll festgestellt werden, wie oft Rezidivraten bzw. Häufungen nach der chirurgischen Resektion bestimmter Tumoren auftraten. Die Ergebnisse dieser Arbeit sollen durch Daten anderer nationaler und internationaler Studien ergänzt werden, um einen Vergleich zu anderen Kliniken herzustellen. Anschließend soll auch über die Verbesserung der Diagnostik und der Behandlungskonzepte diskutiert werden. 39 3 MATERIAL UND METHODE 3.1 Patientendaten Für die vorliegende Arbeit wurden Patientendaten der klinischen Abteilung für Mund-, Kiefer- und Gesichtschirurgie, sowie des Instituts für Pathologie der Medizinischen Universität Graz einer retrospektiven Analyse unterzogen. Diese wurde von der Grazer Ethikkommission überprüft und genehmigt. Als Grundlage für die Erhebung der Patientendaten dienten die Aufzeichnung in den Operationsbüchern der Mund-, Kiefer- und Gesichtschirurgie, sowie die histologischen Auswertungen des Pathologischen Institutes. Berücksichtigt wurden Patienten mit einer odontogenen Tumorerkrankung und einem Eingriffsdatum zwischen dem 01.01.2004 und 31.12.2012, bei dem eine histologisch gesicherte Diagnose durchgeführt wurde. Einzug in die statistischen Auswertungen fanden somit Patienten der klinischen Abteilung für Mund-, Kieferund Gesichtschirurgie Graz, sowie des Departments für zahnärztliche Chirurgie Graz. Im Weiteren wurden die Häufigkeiten der durchgeführten therapeutischen Interventionen zwischen diesen beiden Instituten verglichen. Keine Beachtung fanden Eingriffe, die außerhalb des vorgegebenen Zeitrahmens stattfanden, bzw. histologische Präparate, die von außerhalb des Grazer LKH zur histologischen Untersuchung an das Pathologische Institut gesandt wurden. Erkrankte dieselbe Person innerhalb des Untersuchungszeitraumes, an derselben Diagnose im Sinne eines Rezidives, wurden diese Personen gesondert statistisch ausgewertet und es wurden Rezidivneigungen bezüglich Geschlecht- und Altersverteilung, sowie des zu Grunde liegenden odontogenen Tumors untersucht. 3.2 Datenerhebung In Zusammenarbeit mit dem Institut für Medizinische Informatik, Statistik und Dokumentation wurden von den relevanten Patientenfällen folgende persönlichen Daten erfasst: 40 Name Geschlecht Geburtsdatum (soweit angegeben) Alter zum Zeitpunkt des Eingriffs (in Jahren) Diagnose Lokalisation des Tumors Als nächster Schritt wurden die Patientendaten anonymisiert, indem jedem Patienten eine Laufnummer anstelle des Namens zugewiesen wurde. Weiters wurde das Datum des Eingriffs, sowie der histologischen Auswertung dokumentiert. Bei Patienten, die mehr als einen Eingriff zur Therapie der Neoplasie hatten, wurde das Datum der definitiven, abschließenden Therapie dokumentiert. Anschließend wurde die angegebene Lokalisation des Tumors anhand der statistischen Auswertung übernommen und mithilfe der vorhandenen Röntgenbilder sowie der Operationsberichte verifiziert. Zur Unterteilung der odontogenen Tumoren wurde die aktuell international anerkannte Nomenklatur der WHO verwendet. Zur Analyse der Größe der odontogenen Tumoren wurden in absteigender Priorität die Operationsberichte, präoperative bzw. postoperative Röntgenbilder sowie die Auswertung des Präparates am pathologischen Institut verwendet. Der Vergrößerungsfaktor von ca. 1,3 bei Panoramaaufnahmen wurde bei der Analyse der Röntgenbilder berücksichtigt (Schwenzer, et al., 2009). Zur Vereinfachung der statistischen Vergleichbarkeit mit anderen Auswertung und Studien, wurde wegen einer besseren ausschließlich der größte Durchmesser des odontogenen Tumors, und nicht etwa die dreidimensionale Abmessung verwendet. Die in die Studie einfließenden odontogenen Tumoren wurden einerseits nach Dignität und histologischer Diagnose, andererseits nach der Lokalisation in: Anterior (Bereich zwischen den distalen Flächen der Eckzähne), Prämolarenbereich (Bereich zwischen den mesialen Flächen der ersten Prämolaren und den distalen Flächen der zweiten Prämolaren), Molarenbereich (Bereich zwischen den mesialen Flächen der ersten Molaren und dem distalen Flächen der Weisheitszähne) und 41 Ramus- bzw. Tuberbereich eingeteilt. Die betroffene Seite wurde in Relation zur Medianen erfasst. Läsionen, deren Ausdehnung zwei oder mehrere Bereiche umfasste, wurden jener Region zugeordnet, die der Mitte der Läsion am nächsten war. Weiters wurde zwischen Oberkiefer und Unterkieferlokalisation unterteilt, um eine Mandibula-Maxilla-ratio zu errechnen, und die erhobenen Größen in Gruppen zu unterteilen. Die durchgeführten Therapien wurden in Tumorresektion radikale Entfernung mit großzügigem Ausschaben der Knochenflächen operative Versorgungen mit plastischer Deckung eingeteilt. Bei plastischer Deckung wurde dokumentiert, welche Lappentechnik bzw. welche Gewebetransplantation durchgeführt wurde. Zu den möglichen plastischen Deckungen gehören die Beckenkammplastik, sowie eine Transplantation mit Anteilen der Scapula und des musculus latissimus dorsi. Die oben angeführten Parameter, die einer Auswertung unterzogen werden sollten, wurden im Tabellenkalkulationsprogramm Microsoft Excel® (Version Microsoft Office Professional Plus 2010, Microsoft Corporation, Redmond, WA) zur Verarbeitung erfasst und entsprechend codiert (Tab. 2). Die statistische Auswertung erfolgte wiederum mittels Microsoft Excel®, sowie mit PASW (Predictive Analytics Software) Statistics 18 von SPSS (Statistical Package for Social Sciences) für Windows. Zunächst wurde eine deskriptive Auswertung der Häufigkeiten der festgestellten Tumoren erstellt, unterteilt in jene Diagnosen, die an der klinischen Abteilung für Mund-, Kiefer- und Gesichtschirurgie und am Department für zahnärztliche Chirurgie Graz gestellt wurden. Als nächster Schritt wurde eine Unterteilung nach Alter und Geschlecht durchgeführt, sowie eine Einteilung nach der betroffenen Lokalisation getroffen. 42 Lokalisation Unterkiefer Lokalisation Oberkiefer Lokalisation Rechts Lokalisation Links Lokalisation Anterior/Frontzahnbereich Lokalisation Prämolarenbereich Lokalisation Molarenbereich Lokalisation Tuber/Ramusbereich Größe <1cm Größe 1-2cm Größe 2-3cm Größe 3-4cm Größe 4-5cm Größe 5-6cm Größe 6-7cm Größe 7-8cm Größe 8-9cm Lokalisation mehrere Diagnose Ameloblastom Diagnose keratozystischer odontogener Tumor (KZOT) Diagnose Odontom Diagnose Myxofibrom Diagnose Fibrom Diagnose Fibrosarkom Diagnose Adenomatoider odontogener Tumor DiagnoseAmeloblastisches Karzinom Diagnose Zementoblastom Plastische Deckung Plastische Deckung Scapula Plastische Deckung Beckenkamm Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Ja/nein Tab. 2: Codierungsschema der durchgeführten Analyse 43 4 ERGEBNISSE Einzug in die Studie nahmen insgesamt 185 PatientInnen. Davon waren 105 männlich und 80 weiblich (Abb. 9). männlich weiblich Abb. 9: Geschlechtsverteilung des untersuchten Patientenkollektivs Der jüngste Patient war mit 5 Jahren vertreten, der älteste mit 87. Die Anzahl an TumorpatientInnen schwankte in den Jahren 2004-2012 um einem Mittelwert von etwa 20 Fällen pro Jahr, wobei das Jahr 2009 mit 11 Fällen im Vergleich deutlich weniger Diagnosestellungen aufweist. Das Jahr mit den meisten Diagnosestellungen war mit 29 Fällen das Jahr 2012 (Abb. 10). 35 30 Ameloblastom 25 Adenomatoider OT Zementom 20 Fibrom KZOT 15 Myxom Odontom 10 Sarkom AmeloCa 5 0 2004 2005 2006 2007 2008 2009 2010 2011 2012 Abb. 10: Jahresverteilung der odontogenen Tumoren des untersuchten Patientenkollektivs 44 Die folgende Grafik zeigt die Anzahl der odontogenen Tumoren nach histologischer Klassifizierung und nach Auftreten pro Jahr (Abb. 11). 25 20 15 10 5 0 2004 2006 2008 2010 2012 KCOT Ameloblastom AOT Odontom Myxofibrom Fibrom Amelo Ca Zementoblastom Sarkom Abb. 11: Verteilung nach jährlichem Auftreten im Vergleich zum Tumortyp des untersuchten Patientenkollektivs Im Verhältnis zwischen benignen und malignen Tumoren nahmen die bösartigen Tumoren nur 1,6% aller odontogenen Tumoren ein (Abb. 12). Den Vergleich zwischen den verschiedenen Tumortypen, zeigt Abb. 13. Der keratozystische odontogene Tumor, das Ameloblastom und das Odontom nahmen zusammen etwa 90.8% aller odontogenen Tumoren ein. Insgesamt lässt sich feststellen, dass der am häufigsten aufgetretene Tumor der keratozystische odontogene Tumor war und mit etwa 65% aller diagnostizierten Tumoren eine vorrangige Stellung einnahm (Tab. 3). Er war über alle Altersklassen hinweg in etwa gleichbleibend häufig nachweisbar. 45 Ameloblastoma Adenomatoider OT Zementom Fibrom Benign KZOT Malign Myxom Odontom Sarkom Amelo Ca Abb. 12: Häufigkeitsverteilungen nach Dignität des untersuchten Patientenkollektivs. Abb. 13: Häufigkeitsverteilungen nach Tumortyp des untersuchten Patientenkollektivs Histological Type N % Benign tumours 182 98.4% Odontogenic epithelium with mature fibrous stroma and without odontogenix ectomesenchyme Ameloblastoma Calcifying epithelial odontogenic tumour (CEOT) Adenomatoid odontogenic tumour (AOT) 143 20 0 2 77.3% 10.8% 0% 1.1% 121 65.4% 27 27 0 14.6% 14.6% 0% 0 0% Mesenchyme and/or odontogenic ectomesenchyme, with or without odontogenic epithelium Odontogenic fibroma (OF) Odontogenic myxoma/myxofibroma (OM) Cementoblastoma (CB) 12 6 4 1 6.5% 3.2% 2.2% 0.5% Malignant tumours Odontogenic carcinomas Ameloblastic carcinoma Odontogenic sarcomas 3 2 2 1 1.6% 1.1% 1.1% 0.5% 185 100% Keratocystic odontogenic tumour (KCOT) Odontogenic epithelium with odontogenic ectomesenchyme, with or without hard tissue formation Odontoma Calcifying cystic odontogenic tumour (CCOT) Dentinogenic ghost cell tumour (DGCT) Total Tab. 3: Einteilung der Häufigkeit odontogener Tumoren nach histologischer Diagnose an der klinischen Abteilung für Mund- Kiefer- und Gesichtschirurgie Graz und dem Department für Zahnärztliche Chirurgie Graz gemeinsam In den Jahren 2004-2012 wurden an der klinischen Abteilung für Mund-, Kieferund Gesichtschirurgie in Graz insgesamt 71 Fälle (Tab. 4), am Department für zahnärztliche Chirurgie 114 Fälle (Tab. 5) diagnostiziert und operiert. Die klinische Abteilung für Mund- Kiefer- und Gesichtschirurgie hatte in etwa das gleiche Verteilungsmuster an odontogenen Tumoren, wie das Department für 46 zahnärztliche Chirurgie. Der Hauptunterschied bezog sich jedoch auf die malignen Tumoren, die ausschließlich auf der Kieferchirurgie operiert wurden (3 Fälle). Im Gegensatz dazu wies das Department für zahnärztliche Chirurgie eine höhere Zahl an Odontomen (24 Fälle) auf. Histological Type N % Benign tumours 68 95.8% Odontogenic epithelium with mature fibrous stroma and without odontogenix ectomesenchyme Ameloblastoma Calcifying epithelial odontogenic tumour (CEOT) Adenomatoid odontogenic tumour (AOT) 61 13 1 85.9% 18.3% 0% 1.4% 47 66.2% 3 3 - 4.2% 4.2% 0% - 0% Mesenchyme and/or odontogenic ectomesenchyme, with or without odontogenic epithelium Odontogenic fibroma (OF) Odontogenic myxoma/myxofibroma (OM) Cementoblastoma (CB) 4 1 3 - 5.6% 1.4% 4.2% 0% Malignant tumours Odontogenic carcinomas Ameloblastic carcinoma Odontogenic sarcomas 3 3 2 1 4.2% 4.2% 2.8% 1.4% Total 71 100% Keratocystic odontogenic tumour (KCOT) Odontogenic epithelium with odontogenic ectomesenchyme, with or without hard tissue formation Odontoma Calcifying cystic odontogenic tumour (CCOT) Dentinogenic ghost cell tumour (DGCT) Tab. 4: Einteilung der Häufigkeit odontogener Tumoren nach histologischer Diagnose an der klinischen Abteilung für Mund- Kiefer- und Gesichtschirurgie Graz (2004-2012) Histological Type N % Benign tumours 114 100% Odontogenic epithelium with mature fibrous stroma and without odontogenix ectomesenchyme Ameloblastoma Calcifying epithelial odontogenic tumour (CEOT) Adenomatoid odontogenic tumour (AOT) 82 7 1 71.9% 6.1% 0% 0.9% 74 65.9% 24 24 - 21% 21% 0% - 0% Mesenchyme and/or odontogenic ectomesenchyme, with or without odontogenic epithelium Odontogenic fibroma (OF) Odontogenic myxoma/myxofibroma (OM) Cementoblastoma (CB) 8 5 2 1 7% 4.4% 1.8% 0.9% Malignant tumours Odontogenic carcinomas Ameloblastic carcinoma Odontogenic sarcomas - 0% 0% 0% 0% 114 100% Keratocystic odontogenic tumour (KCOT) Odontogenic epithelium with odontogenic ectomesenchyme, with or without hard tissue formation Odontoma Calcifying cystic odontogenic tumour (CCOT) Dentinogenic ghost cell tumour (DGCT) Total Tab. 5: Einteilung der Häufigkeit odontogener Tumoren nach histologischer Diagnose an dem Department für Zahnärztliche Chirurgie Graz (2004-2012) 47 In unserer Analyse zeigte sich im Verhältnis 1:1,3 eine leichte Dominanz der Erkrankungen bei Männern. Nur etwa 2% der PatientInnen waren zum Zeitpunkt der Diagnosestellung unter 10 Jahre und etwa 8% über 70 Jahre alt. Der Altersgipfel aller odontogenen Tumoren lag vor allem bei PatientInnen in der zweiten Lebensdekade. Bei Kindern und Jugendlichen war vor allem das Odontom ein sehr häufig aufgetretener odontogener Tumor, der mit zunehmendem Alter jedoch eine recht schnell fallende Inzidenz aufweist. Maligne odontogene Tumoren wurden alle im Alter über 60 diagnostiziert. (Abb. 14, Tab. 6) 70% 0-9 60% 10-19 50% 20-29 40% 30-39 30% 40-49 50-59 20% 60-69 10% 70-79 0% Benign Malignant 80-89 Total Abb. 14: Altersverteilung des untersuchten Patientenkollektivs Benign KCOT OD AME OM CCOT OF CTB AOT CEOT DGCT Sex ratio (M:F) 1:8 1:0.5 1:0.8 1:2.3 1:1.5 1:5 0:1 0:2 - Malignant A Ca PIO CCO Sarcoma 1:2 1:1 0:1 Total 1:0.8 Histological type Age (years-old) 0-9 2% 11% 5% - 10-19 22% 17% 55% 10% 40% 17% - 20-29 19% 21% 22% 10% 17% - 30-39 15% 16% 4% 25% 20% 17% 50% - 40-49 15% 19% 4% 5% 20% 17% - 50-59 10% 7% 4% 20% 20% 33% 100% - 60-69 8% 10% 10% 50% - 70-79 6% 7% 5% - 80-89 3% 2% 10% - Mean(SD) 36 (20.3) 39 (19.7) 18 (10.4) 45 (22.8) 33 (19.8) 36 (18.4) 53 47 (18.4) - Range 5-87 10-87 5-51 8-82 11-57 10-56 53 34-60 - - - - - - - 66% 50% 100% - 33% 50% - 69 (15.3) 74 (19.1) 61 60-87 60-87 61 2% 22% 19% 15% 15% 10% 9% 5% 3% 37 (20.9) 5-87 Tab. 6: Geschlechts- und Altersverteilung der Grazer Studie mit 185 odontogenen Tumoren im Vergleich zur Histologie 48 Die Lokalisation mit den meisten aufgetretenen odontogenen Tumoren war eindeutig die Molarenregion der Mandibula. Dies liegt daran, dass die meisten keratozystischen odontogenen Tumoren in der Molarenregion diagnostiziert wurden. Begutachtet man die restlichen Tumoren, zeigt sich eine in etwa gleichbleibende Verteilung im Unterkiefer, und eine Prädestination für den anterioren Bereich, mit fallender Inzidenz nach posterior im Oberkiefer. Das Ameloblastom zeigt ein häufigeres Auftreten im Prämolarenbereich des Unterkiefers, das Odontom hingegen zeigt ein Auftreten vor allem im anterioren Bereich im Oberkiefer und Molarenbereich im Unterkiefer. Es lässt sich erkennen, dass alle untersuchten odontogenen Tumoren im Verhältnis Oberkiefer zu Unterkiefer eine Prädestination mit 1:3,4 für den Unterkiefer haben. Allein das odontogene Fibrom und der adenomatoide odontogene Tumor weisen eine 1:1 Verteilung auf, aufgrund der geringen Patientenanzahl kann hier jedoch keine eindeutige Aussage getroffen werden. Der keratozystische odontogene Tumor zeigte sogar eine 1:5 Verteilung. Die linke Seite war mit 1:1,2 etwas häufiger betroffen als die rechte. Die malignen odontogenen Tumoren befanden sich ausschließlich im Unterkiefer (Tab.7). Maxilla Histological Mandible type Ant Pre Molar Tuber Total Benign KCOT OD AME OM CCOT OF CTB AOT CEOT DGCT 15 6 6 1 1 - 11 3 4 1 1 - 14 9 3 2 - 1 1 - - - - - 42 20 13 4 1 3 1 - Malignant A Ca PIO CCO Sarcoma - - - - Total 15 11 14 1 Anterior N Mx:Md Ri:Le Total A ratio ratio - 140 101 14 16 4 3 1 1 - 25 19 1 3 1 1 - 1:3.3 1:5 1:1.1 1:4 1:4 1:1 0:1 1:1 - 1:1.2 1:1 1:1.6 1:1.7 1:0.4 1:0.7 0:1 0:2 - Premolar Molar Ramus 20 10 4 3 2 - 18 5 3 5 1 - 70 51 6 3 2 2 1 1 - 23 18 2 - - - - 1 1 - - 3 2 1 2 1 1 0:3 0:2 0:1 2:1 1:1 1:0 42 20 18 71 23 143 27 1:3.4 1:1.2 Tab. 7: Lokalisationsverteilung der odontogenen Tumoren des untersuchten Patientenkollektivs 49 Die folgenden Diagramme zeigen die Lokalisationsverteilung nach Tumortyp: Total 80 KZOT 60 50 60 40 30 40 20 20 10 0 0 Maxilla Mandibula Maxilla Ameloblastom 6 Mandibula Odontom 7 6 5 5 4 4 3 3 2 2 1 1 0 0 Maxilla Maxilla Mandibula 160 140 120 100 80 60 40 20 0 Mandibula Abb. 15: Lokalisationsverteilung nach Tumortyp des untersuchten Patientenkollektivs Maxilla Mandible Benign Malign 4.1.1 Alters- und Geschlechtsverteilung Die Altersverteilung in der von uns durchgeführten retrospektiven Analyse zeigte beim adenomatoiden odontogenen Tumor annähernd gleichbleibende Werte bei den Altersgruppen. Das Ameloblastom zeigte bei den 30-39 Jährigen, bei den 50-59 Jährigen, sowie bei den 80-89 Jährigen höhere Werte. Das ameloblastische Karzinom kam besonders häufig bei den 80-89 Jährigen vor, das Zementoblastom 50 bei den 50-59 Jährigen. Bei den letzteren zeigte sich auch beim Fibroblastom ein leichter Anstieg. Der keratozystische odontogene Tumor zeigte neben relativ hohen Werten über alle Altersklassen hinweg, besonders drei ausgeprägte Gipfel, jedoch mit einer abfallenden Inzidenz bei 20-29 Jährigen, den 40-49 Jährigen, sowie den 60-69 Jährigen. Das Myxom kam bei den 10-19jährigen leicht vermehrt vor. Einen deutlichen Gipfel zeigte das Odontom bei den 10-19 Jährigen, den 5059 Jährigen, sowie einen Gipfel bei den 80-89 Jährigen. 30 25 Ameloblastom Adenomatoider OT 20 15 Zementom Fibrom KZOT 10 5 Myxom Odontom Sarkom 0 Ameloblast Ca Abb. 16: Altersverteilung nach Tumortyp Insgesamt waren über alle Tumoren hinweg drei sichtbare Gipfel auszumachen. Einen in der dritten, einen in der sechsten und einen in der neunten Lebensdekade Das folgende Diagramm (Abb. 17) zeigt eine Alterspyramide, aufgeteilt nach Geschlecht und Alter, verglichen mit der Diagnose. Es zeigt sich eine deutliche Häufung von keratozystischen odontogenen Tumoren bei Männern, mit einem starken Anstieg im Alter von 19 bis 40 und einer sinkenden Häufigkeit im Alter von über 40 Jahren. Im Alter von 80 Jahren aufwärts kam in unserer Untersuchung bei Männern kein Fall eines kerotozystischem odontogenen Tumors vor. Der adenomatoide odontogene Tumor wurde in unserer retrospektiven Analyse nur beim weiblichen Geschlecht gefunden, bei den 30-39 Jährigen sowie den 60-69 Jährigen. Das odontogene Fibrom zeigt ebenfalls eine Häufung beim 51 weiblichen Geschlecht, besonders im Alter von 20-60 Jahren. Im Alter von 0-20 kam er hingegen nur einmal vor, bei einem Mann. Im Alter von 60 Jahren aufwärts wurde kein Fall von odontogenen Fibromen erfasst. Das ameloblastische Karzinom trat bei Männern nur im späten Erwachsenenalter vor, bei Frauen nur im hohen Alter. Das Sarkom kam insgesamt nur bei Frauen im späten Erwachsenenalter vor. Das Odontom trat bei Frauen nur zwischen dem 10 und 29 Lebensjahr auf. Bei Männern trat das Odontom besonders im ersten Lebensdrittel auf, hingegen nicht mehr im letzten. Bemerkenswert ist hierbei auch die relativ hohe Anzahl an Odontom-Fällen bei männlichen Kindern unter 10 Jahren. Dieser Tumor kommt insgesamt vermehrt bei Kindern und Jugendlichen vor. Abb. 17: Alterspyramide unterteilt nach Tumortyp und Geschlecht 4.1.2 Größenverteilung 55% aller odontogenen Tumoren waren zwischen 1 und 2 cm im größten Durchmesser groß. Auffallend ist dabei, dass beide von uns erfassten ameloblastischen Karzinome eine Größe von über 9 cm aufwiesen (Abb. 18). Das Odontom weist eine Tendenz zu eher kleineren Läsionen bis 4 cm auf, der keratozystische odontogene Tumor zeigt sich hingegen in allen Größenbereichen vertreten. 52 70 60 Ameloblastom Adenomatoider OT 50 Zementom 40 Fibrom KZOT 30 Myxom Odontom 20 Sarkom 10 AmeloCa 0 <=1 1-2 2-3 3-4 4-5 5-6 6-7 7-8 8-9 9-10 Abb. 18: Größenverteilung nach Tumortyp beim untersuchten Patientenkollektiv 4.1.3 Rezidivraten In dem untersuchten Zeitraum wurden insgesamt 32 Rezidivfälle beschrieben. Den größten Anteil nahm dabei mit 28 Fällen der keratozystische odontogene Tumor ein. Dahinter, an zweiter Stelle, lag das benigne Ameloblastom mit drei Fällen, den dritten Platz belegte mit einem Fall das ameloblastische Karzinom. Prozentuell gesehen, fanden somit Rezidive beim Ameloblastom in 15%, beim ameloblastischen Karzinom in 50% und beim keratozystischen odontogenen Tumor in 23% der Fälle statt (Abb. 19). Dabei muss aber berücksichtigt werden, dass im untersuchten Zeitraum insgesamt nur 2 ameloblastische Karzinome beobachtet worden sind. Somit sind diese Ergebnisse nicht auf alle diese Karzinome übertragbar. 153 32 Rezidive 60% 50% 40% 30% 20% 10% 0% 50% 23% 15% KZOT Ameloblastom Ameloblast. Ca Abb. 19: Anteil an Rezidiven und Prozentsatz an Rezidiven nach Tumortyp beim untersuchten Patientenkollektiv 53 Als therapeutische Maßnahme wurde in allen Fällen eine operative Zystektomie mit Entfernung des gesamten Zystengewebes durchgeführt. In 8 Fällen musste eine Beckenkammtransplantation zur primären Gewebsdeckung durchgeführt werden. Dieser Eingriff war dabei mit 5 Fällen beim Ameloblastom, und jeweils einem Fall beim ameloblastischen Karzinom, keratozystischen odontogenen Tumor, sowie einem Myxofibrom nötig. Die Ausdehnung der Defekte belief sich dabei auf 4 bis 10 cm im größten Durchmesser. In drei Fällen wurde eine Transplantation mit Anteilen der Scapula sowie des musculus latissimus dorsi durchgeführt. Dieser Eingriff war dabei mit jeweils einem Fall beim ameloblastischen Karzinom, keratozystischen odontogenen Tumor, sowie einem Ameloblastom nötig. Hier bemaßen die Defekte zwischen 6,5 und 9 cm im größten Durchmesser. Diese großen operativen Eingriffe fanden ausschließlich an der klinischen Abteilung für Mund-, Kiefer- und Gesichtschirurgie statt. Beckenkammtransplantation Scapulatransplantation Ameloblastom 5 1 1 1 Ameloblast. Ca KZOT 1 Ameloblastom 1 Ameloblast. Ca 1 KZOT Myxofibrom Abb. 20: Art der Defektdeckung beim untersuchten Patientenkollektiv 54 5 DISKUSSION Für die Suche nach entsprechender Literatur wurde eine Recherche mithilfe der Onlinedatenbanken PubMed, Medline, LILACS, Cochrane-Reviews und GoogleScholar durchgeführt. Als Suchbegriffe wurden hauptsächlich die einzelnen Klassifikationen von odontogenen Tumoren, vor allem in Verbindung mit dem Querverweis zu epidemiologischen Studien, verwendet. Weiters wurden auch Fallberichte, aktuelle sowie ältere Lehrbücher und andere am pathologischen Institut Graz durchgeführten Studien zur Informationsgewinnung verwendet. Als Vergleichsstudie und als Richtlinie zur Klassifizierung und Kodierung der durchgeführten retrospektiven Analyse wird vor allem die Studie von J.P.S Servato aus den Jahr 2012 verwendet (Servato, 2012). Diese Arbeit beschreibt aufgrund von Datenerhebungen an Pathologieinstituten in Brasilien die Epidemiologie und die klinische Präsentation odontogener Tumoren innerhalb von 31 Jahren, und vergleicht deren Ergebnisse mit internationalen Statistiken. Um eine möglichst gute Vergleichbarkeit zu gewährleisten, wurden die dort angewandte WHONomenklatur und das statistische Verfahrensschema beibehalten. Die Ergebnisse aus verschiedenen Ländern variieren teils sehr stark, somit wurden im nächsten Schritt diese Ergebnisse, mit denen der vorliegenden Studie verglichen. Es wurde auf entsprechende Abweichungen und Gemeinsamkeiten eingegangen. Mittels retrospektiver Analyse konnten die gesetzten Ziele erfüllt werden, sowie die Anzahl und Typologie der untersuchten Tumorarten festgestellt werden. Die daraus resultierenden Ergebnisse wurden mit internationaler Literatur verglichen und es konnten Ähnlichkeiten, aber auch einige konträre Aussagen eruiert werden. Im Vergleich zu vielen anderen publizierten Studien wurden bei unserer Untersuchung auch das Auftreten von Rezidiven und die Größenverteilung der einzelnen odontogenen Tumoren miterfasst. Diese Daten könnten in weiterer Folge für neuerliche Hypothesengenerierung und Gegenüberstellungen verwendet werden. 55 In der Grazer Studie war mit einem Anteil von 65,4% der keratozystische odontogene Tumor der häufigste Vertreter unter den odontogenen Tumoren. Verglichen mit anderen Studien ist das ein besonders hoher Anteil. Das häufigste Auftreten des keratozystischen odontogenen Tumors war in China 2009 (Luo, et al., 2009), sowie in Mexiko 2010 (Gaitán-Cepeda, et al., 2010) mit jeweils etwa 38%. Auffallend ist dabei auch, dass der keratozystische odontogene Tumor erst bei den untersuchten Studien ab dem Jahr 2007 auf den ersten drei Plätzen vermerkt ist. Dies ist auf die Tatsache zurückzuführen, dass der keratozystische odontogene Tumor in den früheren WHO-Klassifikationen vor 2005 nicht als odontogener Tumor definiert war, sondern als zystische Läsion. Für das Odontom zeigten sich hingegen in der vorliegenden Analyse mehr Ähnlichkeiten zu anderen Studien. So sind die Odontome in Graz mit 14,6% an zweiter Stelle, ebenso wie in Studien aus der Türkei 1990, 2006 (Günhan, et al., 1990; Olgac, et al., 2006) und Brasilien 2005 (Fernandes, et al., 2005). Das Ameloblastom zeigt sich mit 10,8% in Graz an dritter Stelle. Im Gegensatz dazu nimmt es in den meisten anderen Ländern die erste, beziehungsweise zweite Stelle ein. Am ehesten sind hierbei die Studien aus Mexiko 2010 (GaitánCepeda, et al., 2010), Italien 2006 (Pippi, 2006) und USA 2006 (Buchner, et al., 2006) vergleichbar, die eine ähnliche prozentuelle Verteilung aufweisen. Die Altersverteilung zeigt sich im internationalen Vergleich ähnlich unseren Ergebnissen. In der Grazer Studie wurde jedoch mit 37 Jahren das höchste Durchschnittsalter festgestellt, in Chile 2002 mit 25 Jahren das niedrigste (Ochsenius, et al., 2002). 56 WHO classification 1971 1992 1992 1992 2005 Country, year Period (years) N % Most common histological types Malignant tumours 2nd 3rd AOT/AF/CT/OD (6.9% each) AME (11.0%) PCD (8.0%) CB (14.0%) OD (4.0%) OD (18.0% CB (12.5%) AME (17.8%) OF (13.7%) OM (11.8%) AOT (6.2%) OM (7.4%) AF (6.7%) OM (21.1%) AOT (16.1%) AME (23.7%) OM (17.7%) OM (8.4%) AOT (8.3%) AME (30.7%) AOT (8.6%) OM (10.3%) CB (5.2%) AME (20.4%) OM (8.8%) OM (4.3%) AOT (4.3%) AME (25.3%) AF (16.0%) OM (7.0%) OD (2.6%) AOT (7.5%) OM (6.5%) OD (24.9%) OM (9.1%) OM (11.9%) AF (3.1%) AME (12.4%) OF (3.4%) OD (21.0%) OM (16.0%) AME (15.0%) OF (13.2%) AOT (9.3%) OM (4.9%) AOT (12.4%) OM (6.0%) AOT (9.0%) OD (7.8%) OD (26.7%) OM/AOT (9.1%) NA NA NA 1.5% 1.6% 5.2% NA 2.3% 1.1% 6.1% NA NA 0.6% 1.4% 1.3% 0.9% 3.4% 0.6% 1.3% 0.5% 1.1% NA 2.7% 1.2% 3% 1.8% Prevalent type NA type NA NA NA O Ca O Ca NA PIO SCCa PIO SCCa A Ca NA NA O Ca/AF As A Ca PIO SCCa COC Ca A Ca A Ca/COC Ca O Ca A Ca A As NA COC Ca A Ca PIO SCCa NA AME (22.2%) OM (14.9%) NA OD (4.7%) OD (22.7%) OD (6.1%) OD (19.5%) OD (13.4%) AME (18.3%) AME (20.0%) AME (10.8%) 3.0% 0.4% 5.9% NA 3.7% NA 2.1% 1.6% Nigeria, 1975 USA, 1978 Hong Kong, 1985 Turkey, 1990 Canada, 1994 Nigeria, 1995 Zimbabwe, 1996 Nigeria, 1997 Mexico, 1997 China, 1998 Brazil, 2001 Tanzania, 2002 Chile, 2002 Jamaica, 2003 Estonia, 2004 Tanzania, 2005 Nigeria, 2005 Brazil, 2005 Nigeria, 2005 USA, 2006 Turkey, 2006 Italy, 2006 Sri Lanka, 2007 India, 2008 India, 2010 Iran, 2010 11 42 20 31 27 21 10 15 37 43 30 16 26 16 25 5 24 51 20 21 33 16 7 36 39 31 29 706 82 409 445 289 148 128 349 759 127 213 362 70 75 116 319 340 318 1133 527 53 226 250 489 165 15.0% 1.3% 0.1% NA 1.1% 19.1% 8.6% 30.0% 2.2% NA 2.4% 12.2% 1.3% 23.9% 0.7% NA 9.6% 1.8% 32.0% 1.2% 1.2% NA NA NA 4.1% 1.9% 1st AME (65.0%) OD (67.0%) AME (72.0%) AME (36.5%) OD (45.8%) AME (58.5%) AME (79.1%) AME (76.6%) OD (34.6%) AME (58.6%) OD (50.4%) AME (73.7%) OD (44.7%) AME (67.0%) OD (34.6%) AME (80.1%) AME (63.0%) AME (45.3%) AME (73.3%) OD (72.9%) AME (25.0%) OD (52.8%) AME (69.8%) AME (61.5%) AME (67.7%) AME (40.6%) Mexico, 2010 24 342 2.7% ODO (45.0%) China, 2007 Brazil, 2008 China, 2009 Libya, 2009 Egypt, 2010 Mexico, 2010 Brazil, 2012 Graz, 2013 53 16 22 17 16 3 31 9 1642 238 1309 148 82 136 240 185 NA 4.8% 3.9% 36.5% NA 5.0% 2.1% NA KCOT(35.8%) AME (40.3%) KCOT (30.0%) AME (23.7%) KCOT (38.7%) AME (36.5%) KCOT (35.1%) AME (22.3%) KCOT(19.5% AME (41.5%) )ODO (30.8%) KCOT (38.9%) KCOT/OD (31.2% each) KCOT (65.4%) ODO (14.6%) Proportion Sex ratio (F:M) (F:M) Mean age (range) 1:1.1 1:1.03 1:1.3 1:0.9 NA 1.2:1 1.1:1 1.1:1 1:1.2 1.3:1 1:1.7 1:1.05 1:1.1 1:1.2 1:1.7 1:1.9 1:1.0 1:1.2 1.3:1 1.1:1 1:1.1 1:1.6 1:1.1 1:1.2 1.1:1 1:1.2 30y (5–60) 31y (2–81) 33.3y (NA) 27.8y (2–86) NA 27.7y (2–82) NA 31y (8–75) NA (3–79) 29.3y (3–77) 26.6y (4–82) NA (27–71) 25.2y (1–82) NA 32.5y (NA) NA 29.9y (4–85) 25.5y (1–82) 35.2y (1–78) 33.3y (1–80) NA (3–85) 30.2y (6–78) 31.4y (1–84) 29.8y (2.5–75) 32.6y (5–75) 26y (6–81) NA 1.6:1 NA A Ca PIO SCCa PIO SCCa NA PIO SCCa NA A Ca A Ca 1.4:1 1:1.3 1.4:1 1.3:1 1.2:1 1.6:1 1:1.1 1:1.3 32.1y (3–84) 30.7y (4–99) 34.5y (1–83) 32.4y 5–75) 29.6y (4–80) NA 29y (3–87) 37.1 (5-87) Tab. 8: Odontogene Tumoren nach WHO Klassifikation, Auftreten und Demographie (Servato, 2012) im Vergleich mit Grazer retrospektiver Studie (2013) 57 Die Verteilung zwischen Männern und Frauen war in den meisten Studien in etwa gleichbleibend. Auch der Anteil an malignen Tumoren ist in den meisten Studien relativ gering. (Martínez, et al., 2014). Graz befindet sich hierbei mit 1,6% an malignen Tumoren im unteren Bereich im internationalen Vergleich. Abb. 21: Prozentsatz an malignen Tumoren in unterschiedlichen Studien (Martínez, et al., 2014) Allgemein lässt sich jedoch sagen, dass die Ergebnisse aus Graz im internationalen Vergleich keine typische Verteilung aufzeigen. Dies kann möglicherweise auf die Tatsache zurückgeführt werden, dass die meisten Studien über odontogene Tumoren aus afrikanischen, südamerikanischen, südostasiatischen und südwestasiatischen Ländern stammen und sich somit ethnische oder kulturelle Unterschiede in der Häufigkeitsverteilung zeigen. Es gibt nur wenige Studien über odontogene Tumoren aus europäischen Ländern, weshalb eine gute Vergleichbarkeit erschwert ist. 58 In dem von uns untersuchten Zeitraum von 2004-2012 wurden insgesamt 32 Rezidivfälle erkannt. Dies entspricht 17,3% aller von uns erfassten odontogenen Tumoren. Den größten Anteil nahm dabei mit 28 Fällen der keratozystische odontogene Tumor ein. Dessen hohe Rezidivneigung ist bekannt und wurde auch in der Literatur so beschrieben (Jundt, 2006). Interessant ist dabei das häufigere Auftreten des keratozystischen odontogenen Tumors im Zuge des NävoidBasalzell-Karzinom-Syndrom, dem sogenannten Gorlin-Goltz-Syndrom. Bei Patienten mit einem bekannten Gorlin-Goltz-Syndrom werden die tumorösen Läsionen in der Regel in einem jüngeren Alter diagnostiziert (Bornstein, et al., 2005). Weiters scheinen bei Patienten mit diesem Syndrom, keratozystische odontogene Tumoren vor allem zwischen dem zehnten und zwanzigsten Lebensjahr vorzukommen (Woolgar, et al., 1987). In unserem Patientenkollektiv war die gesicherte Diagnose eines Gorlin-GoltzSyndroms nicht in allen Fällen eruierbar, weshalb aussagekräftige Ergebnisse hinsichtlich dieser Thematik nicht möglich waren. Auch das in der Literatur beschriebene gleichzeitige Auftreten von multiplen tumorösen Läsionen beim Basalzellnävus-Syndrom konnte wegen einer zu geringen Patientenzahl in unserer Studie nicht bestätigt, beziehungsweise widerlegt werden (Woolgar, et al., 1987). Erkrankte dieselbe Person innerhalb des Untersuchungszeitraumes zur gleichen Zeit an zwei lokal getrennten tumorösen Läsionen, wurde dieser Umstand in der statistischen Auswertung als zwei voneinander getrennte Diagnosefälle gehandelt. Dies war bei 4 PatientInnen der Fall, wobei es sich jedes Mal um keratozystische odontogene Tumoren handelte. Die Prädilektionsstelle des keratozystischen odontogenen Tumors am Unterkiefer und im speziellen am aufsteigenden Ast, beziehungsweise posterioren Unterkieferkorpus (Freier, et al., 2009), konnte in unserer Analyse nicht bestätigt werden. In unserer Studie war die am häufigsten aufgetretene Stelle die Unterkiefer-Molarenregion. Im Oberkiefer konnte die Molarenregion als Prädilektionstelle hingegen bestätigt werden (Böhme, et al., 1993). Ebenso spiegelt unsere Analyse die Ergebnisse anderer Studien wieder, die eine Altersverteilung mit einem Altersgipfel in der 3. und 5. Lebensdekade und das häufigere Auftreten beim männlichen Geschlecht beschreiben (Böhme, et al., 1993; Jundt, 2006). 59 Die in der Literatur beschriebene Altersverteilung beim Ameloblastom stimmte mit unserer Arbeit Großteils überein. Es zeichnete sich ein Altersgipfel im vierten und sechsten Lebensjahrzehnt ab, jedoch trat das Ameloblastom bei unserer Analyse mit einem Verhältnis von 1:2,3 häufiger beim weiblichen Geschlecht auf. Das Odontom zeigte in der Altersverteilung keine Überraschungen. 55% aller Odontome traten in der zweiten Lebensdekade auf und 77% vor dem 40. Lebensjahr (Jundt, 2006). Ein interessanter Umstand ist die Tatsache, dass die Anzahl an operierten odontogenen Tumoren am Department für Zahnärztliche Chirurgie mit 114 Fällen größer ist, als auf der klinischen Abteilung für Mund- Kiefer- und Gesichtschirurgie mit 68 Fällen. Dies kann durch den Umstand erklärt werden, dass die Anzahl an ambulant durchgeführten Eingriffen, vor allem an Läsionen mit geringerer Größe und Aggressivität, am Department für Zahnärztliche Chirurgie deutlich größer ist und an der klinischen Abteilung für Mund- Kiefer- und Gesichtschirurgie vermehrt zugewiesene, schwierigere Operationsfälle stattfinden. Aus diesem Grund wurden ausschließlich alle malignen odontogenen Tumoren sowie vermehrt größere Läsionen an der klinischen Abteilung für Mund- Kiefer- und Gesichtschirurgie operiert. Das therapeutische Vorgehen fand in unserer Analyse bei allen als odontogener Tumor diagnostizierten Fällen mittels einer Totalexzision der Läsion statt. In der Literatur wurden als andere Therapieoptionen die Behandlung mittels Carnoyscher Lösung und Kryotherapie beschrieben. Diese Behandlungsmethoden wurden in Einzelfällen als ausreichend erachtet, können jedoch ohne eine effiziente Entfernung des odontogenen Tumors im Gesunden zur Rezidivbildung führen (Schmid, et al., 2012). Auch eine Behandlung mittels Chemotherapie beziehungsweise Strahlentherapie wird in Einzelfällen und vor allem bei malignen, metastasierenden Tumoren durchgeführt (Schwenzer, et al., 2009). Solche Therapieformen wurden in unserem Patientenkollektiv nicht verwendet. Die dieser Arbeit zugrundeliegenden Patientendaten wurden den Aufzeichnungen der klinischen Abteilung für Mund-, Kiefer- und Gesichtschirurgie, der Universitätsklinik für Zahn- Mund- und Kieferheilkunde Graz, sowie den statistischen Auswertungen aus dem MEDOCs-System entnommen. Aufgrund verschiedener Faktoren muss bei der Erfassung und statistischer Aufarbeitung 60 von Patientendaten immer mit Ungenauigkeiten und auch Fehlern gerechnet werden. Die Aufzeichnungen in den OP-Berichten enthalten nicht immer die gleichen Informationen. Oft wird auch auf eine genaue Größenbeschreibung der Läsion, sowie des gesetzten Defekts verzichtet. Die Aufzeichnungen werden auch von verschiedenen Operateuren mit unterschiedlicher Sorgfalt ausgefüllt. Nicht immer wurde bei den beschriebenen Tumoren auch eine genaue Röntgendiagnostik durchgeführt. Auch Fehler durch die unterschiedlichen Größenangaben aus Röntgenbildern, Operationsberichten und Auswertungen des Instituts für Pathologie können aufgetreten sein. Außerdem musste bei der Vermessung anhand des Röntgenbildes der Vergrößerungsfaktor von 30% beachtet werden. Es besteht auch die Möglichkeit, dass durch einen falschen Diagnoseverdacht eine fälschlicherweise als Zyste bezeichnete Läsion totalexzidiert wurde und wegen des Verzichts auf eine histologische Überprüfung ein odontogener Tumor übersehen worden ist. Dem Goldstandard entsprechend sollte jedoch jede zystische Läsion unbedingt dem Pathologen zur entsprechenden Analyse geschickt werden. Aufgrund einiger nicht lückenlos dokumentierter Diagnosen und Tumorerkrankungen erwies sich die Datenerhebung in einigen Fällen als schwierig. So musste der größte Durchmesser bei fehlenden Größenangaben in den Operationsberichten aus radiologischen Bildern oder den Befunden des Instituts für Pathologie erhoben werden. Bei einigen untersuchten odontogenen Tumoren war in unserer Studie die Patientenanzahl so gering, dass keine allgemein gültigen Aussagen über diese Tumorart getroffen werden konnten. Dies trifft vor allem auf das Zementoblastom mit nur einem untersuchten Fall und den adenomatoiden odontogenen Tumor mit zwei Fällen zu. Somit können die in der Literatur beschriebenen Tendenzen leider weder bestätigt noch widerlegt werden. Zur Generierung von aussagekräftigeren Ergebnissen müsste auf jeden Fall ein noch längerer Zeitraum, mit einem dementsprechend größeren Patientenpool bearbeitet werden. Dann könnten spezifische Tendenzen und Eigenheiten bestimmter Tumoren noch besser beschrieben und analysiert werden. 61 6 LITERATURVERZEICHNIS (1) [Journal] / Verf. DÖSAK-Register. (2) [Buchabschnitt] / Verf. Schroll K., Watzek, G. // Zahnärztliche Chirurgie: Ausgewählte Kapitel aus Mund-, Kiefer- und Gesichtschirurgie. - [s.l.] : Maudrich, 1997. - Bd. 3. (3) [Buchabschnitt] / Verf. Schwenzer N. und Ehrenfeld M. // Zahnärztliche Chirurgie, Zahn-Mund-Kiefer-Heilkunde. - Stuttgart : Thieme, 2009. - Bd. 4. Auflage. (4) Activation of sonic hedgehog signaling in keratocystic odontogenic tumors [Buch] / Verf. Freier K. [et al.]. - [s.l.] : Springer Medizin Verlag, 2009. - Bd. HNO. (5) Ameloblastic carcinoma of the maxilla [Buchabschnitt] / Verf. Dhir K. und Sciubba J Tufano R // Oral Oncology. - [s.l.] : Elsevier, 2003. (6) Ameloblastomas [Buchabschnitt] / Verf. Gardner D.G. // Pathology and Genetics of Head and Neck Tumours / Buchverf. Cancer The International Agency for Research on. - 2005. (7) Beiträge zur Klassifizierung der Tumoren des Mundes und seiner Nebenorgane [Journal] / Verf. Churchill H.R.. - Med. Fakultär Universität Rostock : [s.n.], 1932. (8) Benign odontogenic tumours: Clinical, epidemiological and therapeutic aspects of a sixteen years sample. [Buchabschnitt] / Verf. Pippi R.. - [s.l.] : Minerva Stomatol., 2006. (9) Calcifying epithelial odontogenic tumor: a case showing features of malignacy [Buchabschnitt] / Verf. Basu M.K. und Matthews JB Sear AJ, Browne RM // Oral Pathology. - 1984. 62 (10) Calcifying epithelial odontogenic tumors [Buchabschnitt] / Verf. Pindborg JJ Vedtofte P, Reibel J, Praetorius F. // Acta Pathol Microbiol Scand. - 1955. (11) Cementoblastoma: An innocuous neoplasm? A clinicopathologic study of 44 cases and review of the literature with special emphasis on recurrence [Buchabschnitt] / Verf. Brannon R.B. und Fowler CB Carpenter WM, Corio RL. // Oral and Maxillofacial Pathology. - New Orleans : [s.n.], 2002. (12) Central (intraosseous) calcifying odontogenic cyst. [Buchabschnitt] / Verf. Buchner A Merrell PW, Carpenter WM, Leider AS // Int J Oral Maxillofac Surg.. - Israel : [s.n.], 1990. (13) Clinical and radiological features of odontogenic myxoma of the jaws. [Buchabschnitt] / Verf. Kaffe I. und Naor H Buchner A // Dentomaxillofac Radiol.. - 1997. (14) Cysts, bone lesions, odontogenic tumors. [Buchabschnitt] / Verf. Wangerin K. // Oral and implant surgery. - [s.l.] : Chicago: Quintessence, 2009. (15) Das zentrale Riesenzellgranulom des Kiefers: Therapie und Prognose. [Artikel] / Verf. Feyerling D. und A. Beham // Diplomarbeit. Graz Medical University : [s.n.], 2005. (16) Dental Pathology [Buch] / Verf. Slootweg P.J.. - Berlin Heidelberg : Springer-Verlag , 2013. (17) Die odontogene Keratozyste - odontogene Zyste oder benigner Tumor? [Buchabschnitt] / Verf. Bornstein M. und Andreas Filippi Hans Jörg Altermatt, J Thomas Lambrecht, Daniel Buser // Schweiz Monatsschr Zahnmed, Vol 115. - Basel : [s.n.], 2005. (18) Einführung in die Zahnmedizin [Buch] / Verf. Reitemeier, et al.. - [s.l.] : Georg Thieme Verlag, 2006. 63 (19) Entwicklungsbedingte odontogene Zysten [Buchabschnitt] / Verf. Weiss P. und A. Filippi J. Lambrecht // Orale Medizin Quintessence. 2011. (20) Giant-cell reparative granuloma, traumatic bone cyst, and fibrous (fibro-oseous) dysplasia of the jawbones. [Buchabschnitt] / Verf. Jaffe HL // Oral Surg Oral Med Oral Pathol.. - 1953. (21) Gingival cyst of the adult: regenerative therapy of associated root exposure. A case report and literature review. [Buchabschnitt] / Verf. Kelsey W.P. und Kalmar JR Tatakis DN. // Periodontol. - 2009. (22) Glandular odontogenic cyst: a challenge in diagnosis and treatment. [Buchabschnitt] / Verf. Kaplan I. und Anavi Y Hirshberg A. // Oral Dis. 2008. (23) Histological Typing of odontogenic Tumours, Jaw Cysts, and Allied Lesions [Buchabschnitt] / Verf. Pindborg J.J. und Kramer // International Histological Classification of Tumours No. 5. - Geneva : World Health Organisation, 1971. (24) International collaborative study on ghost cell odontogenic tumours: calcifying cystic odontogenic tumour, dentinogenic ghost cell tumour and ghost cell odontogenic carcinoma. [Buchabschnitt] / Verf. Ledesma-Montes C. und Gorlin RJ Shaer M, Prae Torius F, MosquedaTaylor A, Altini M, Unni K, Paes de Almeida O, Carlos-Bregni R, Romero de León E, Phillips V,Delgado-Azañero W, Meneses-García A. // J Oral Pathol Med.. - Mexico : [s.n.], 2008. (25) Kieferzysten - Differentialdiagnosen und Therapie [Buchabschnitt] / Verf. Jakse N.. - Graz : Onlineinformationen der Universitätsklinik für Zahn-, Mund- und Kieferheilkunde, 2004. (26) Knochentumoren mit Kiefertumoren: Klinik - Radiologie - Pathologie [Buchabschnitt] / Verf. Freyschmidt / Buchverf. J. Freyschmidt H. Ostertag, G. Jundt. - [s.l.] : Springer, 2010. 64 (27) Malignant odontogenic tumors: a multicentric Latin American study of 25 cases. [Buchabschnitt] / Verf. Martínez M. und Mosqueda-Taylor A Carlos R, Delgado-Azañero W, de Almeida OP // Oral Diseases. - Brazil : Wiley&Sons, 2014. (28) Malignant transformation of ameloblastic fibroma to ameloblastic fibrosarcoma: case report and review of the literature [Buchabschnitt] / Verf. Kobayashi K. und Ryuichi Murakami Tohru Fuji, Akiyoshi Hirano // Journal of Cranio-Maxillofacial Surgery. - Japan : Elsevier, 2005. (29) Mikroskopische Anatomie der Zähne und des Parodonts [Buchabschnitt] / Verf. Steiniger / Buchverf. Steiniger. - 2010. (30) Multifocal lateral periodontal cysts: a report of 4 cases and review of the literature [Buchabschnitt] / Verf. Siponen M. und Neville BW Damm DD, Allen CM. // Oral Pathol Oral Radiol Endod. - 2011. (31) Odontogene Tumoren [Buchabschnitt] / Verf. Gundlach K.K.H. // Mund Kiefer GesichtsChir (2000) 4 [Suppl 1]. - Rostock : Srpinger Verlag, 2000. (32) Odontogene [Buchabschnitt] / und Verf. nicht-odontogene Jundt G. // Läsionen der Kiefer Mund-Kiefer-Gesichtschirurgie / Buchverf. Horch H.H.. - [s.l.] : Elsevier Urban & Fischer, 2006. - 4. Auflage. (33) Odontogenic Ghost Cell Carcinoma in the Maxilla: A Case Report and Literature Review [Buchabschnitt] / Verf. Zhi-Jun S. und Yi-Fang Zhao Lu Zhang, Zu-Bing Li, Xin-Ming Chen, Wen-Feng Zhang // Journal of Oral and Maxillofacial Surgery. - [s.l.] : Elsevier, 2007. (34) Odontogenic tumors in Chile: a study of 362 cases [Buchabschnitt] / Verf. Ochsenius G. und Ortega A Godoy L, Peñafiel C, Escobar E. // J Oral Pathol Med. - 2002. (35) Odontogenic tumors: a study of 1309 cases in a Chinese population [Buchabschnitt] / Verf. Luo H.Y. und TJ Li // Oral Oncol. - 2009. 65 (36) Odontogenic tumors: a study of 340 cases in a Brazilian population. [Buchabschnitt] / Verf. Fernandes A.M. und Duarte EC Pimenta FJ, Souza LN, Santos VR, Mesquita RA, et al. // J Oral Pathol Med. - 2005. (37) Odontogenic tumours in Istanbul:527 cases [Buchabschnitt] / Verf. Olgac V., Koseoglu BG. und Aksakalli N. // Br J Oral Maxillofac Surg. 2006. (38) Odontogenic tumours. A series of 409 cases [Buchabschnitt] / Verf. Günhan O. [et al.] // Aust Dent J. - 1990. (39) Odontogenic tumours: 240 cases diagnosed over 31 years at a Brazilian university and a review of international literature [Buchabschnitt] / Verf. Servato J.P.S. // Int. J. Oral Maxillofac. Surg.. Brazil : Elsevier, 2012. (40) Odontogenic tumours: analysis of 706 cases [Buchabschnitt] / Verf. Regezi JA Kerr DA, Courtney RM. // J Oral Surg. - 1978. (41) Orale Chirurgie [Buchabschnitt] / Verf. Sailer H Pajarola G.. - Stuttgart : Thieme, 1996.. (42) Orale Strukturbiologie [Buchabschnitt] / Verf. Schroeder / Buchverf. Schroeder. - [s.l.] : Thieme Georg Verlag; Auflage: 4., 1999. (43) Pathologie, Kopf-Hals-region, Weichgewebstumoren, Haut [Buchabschnitt] / Verf. Klöppel G. und Kreipe H Remmele W. - [s.l.] : Springer, 2009. - Bd. I. (44) Peripheral ameloblastoma: biological profile based on 160 cases from the literature. [Artikel] / Verf. Philipsen HP // Oral Oncol.. - 2001. (45) Peripheral odontogenic fibroma: a clinicopathologic study [Buchabschnitt] / Verf. Slabbert H Altini M. // Oral Surg Oral Med Oral Pathol.. - Johannesburg : [s.n.], 1991. (46) Primäres intraossäres Plattenepithelkarzinom auf der Basis einer odontogenen Zyste - Eine Falldarstellung [Buchabschnitt] / Verf. Nölken R und F.W. Neukam. - Köln : Deutscher Ärzte-Verlag, 2006. 66 (47) Range and demographics of odontogenic cysts diagnosed in a UK population over a 30-year period. [Buchabschnitt] / Verf. Jones A.V. und Craig GT Franklin CD. // J Oral Pathol Med. - 2006;. (48) Recherches sur un nouveau groupe de tumeurs designees sous le nom d'odontomes. [Buchabschnitt] / Verf. Broca P. P / Buchverf. Broca P. P. - [s.l.] : Gaz Heb MedChir8, 1968. (49) Reclassification of odontogenic keratocyst as tumour. Impact on the odontogenic tumours prevalence [Buchabschnitt] / Verf. Gaitán-Cepeda L.A. und Quezada-Rivera D Tenório-Tocha F, Leyva-Huerta ER. // Oral Dis. - 2010. (50) Relative frequency of central odontogenic tumors: a study of 1,088 cases from Northern California and comparison to studies from other parts of the world. [Buchabschnitt] / Verf. Buchner A. und Merrell PW Carpenter WM. // J Oral Maxillofac Surg. - 2006. (51) Retrospektive histologische Klassifikation von Kieferzysten [Buchabschnitt] / Verf. Böhme K. und Morgenroth K // Deutsche Zahnärztliche Zeitschrift. - 1993. (52) Spätrezidive beim keratozystischen odontogenen Tumor(KZOT) [Buchabschnitt] / Verf. Schmid I., Grätz K.W. und Locher M.C. // Schweiz Monatsschr Zahnmed Vol 122. - Zürich : [s.n.], 2012. (53) Squamous odontogenic tumor. Report of six cases of a previously undescribed lesion. [Buchabschnitt] / Verf. Pullon .PA. und Shafer WG Elzay RP, Kerr DA, Corio RL. // Oral Surg Oral Med Oral Pathol.. - 1975. (54) Taschenatlas der Zahnärztlichen Radiologie [Buchabschnitt] / Verf. Pasler / Buchverf. F. Pasler. - [s.l.] : Thieme, 2003. (55) Terminology of the Ameloblastoma: History and current Usage [Journal] / Verf. Baden E.. - J Oral Surg. : [s.n.], 1965. 67 (56) The odontogenic keratocyst and its occurrence in the nevoid basal cell carcinoma syndrome. [Buchabschnitt] / Verf. Woolgar J.A. und Rippin JW Browne RM. // Oral Surg Oral Med Oral Pathol.. - 1987. (57) The possible inductive role of ektomesenchyme in the pathogenesis of some odontogenic lesions [Buchabschnitt] / Verf. Shear M. und M Altini. - South Africa : J Dent Assoc, 1976. (58) The World Health Organization histological typing of odontogenic tumours. Introducing the second edition. [Buchabschnitt] / Verf. Kramer I.R., Pindborg J.J. und Shear M.. - London : Eur J Cancer B Oral Oncol., 1993. (59) World Health Organization classification of Tumours: Pathology and Genetics of Head and Neck Tumours [Buchabschnitt] / Verf. Barnes / Buchverf. Barnes L Eveson J, Reichart P, Sidransky D (eds). - Lyon : IARC Press, 2005. (60) Zentrales Riesenzellgranulom des Unterkiefers - Begriffsbestimmung und Differentialdiagnose [Buchabschnitt] / Verf. Driemel O. und R. Staudenmaier K. Hertel, H. Pistner, H. Kosmehl // HNO. - München : Springer Medizin verlag, 2005. 68 7 ABBILDUNGSVERZEICHNIS Abb. 1: Adenomatoider odontogener Tumor am linken Ramus mand. (LKH Graz) ............................................................................................................................. 18 Abb. 2: Keratozystischer odontogener Tumor am linken Ramus mandibulae (LKH Graz) .................................................................................................................... 20 Abb. 3: Keratozystischer odontogener Tumor im Bereich der linken Kieferhöhle (LKH Graz) ........................................................................................................... 20 Abb. 4: Röntgenbilder mehrerer Odontome (LKH Graz) ...................................... 24 Abb. 5: Follikuläre Zyste (Weiss, et al., 2011) ...................................................... 33 Abb. 6: Laterale Parodontale Zyste (Weiss, et al., 2011) ..................................... 34 Abb. 7: Glanduläre odontogene Zyste (Weiss, et al., 2011) ................................. 35 Abb. 8: Gingivale Zyste (Weiss, et al., 2011)........................................................ 36 Abb. 9: Geschlechtsverteilung des untersuchten Patientenkollektivs ................... 44 Abb. 10: Jahresverteilung der odontogenen Tumoren des untersuchten Patientenkollektivs................................................................................................ 44 Abb. 11: Verteilung nach jährlichem Auftreten im Vergleich zum Tumortyp des untersuchten Patientenkollektivs .......................................................................... 45 Abb. 12: Häufigkeitsverteilungen nach Dignität des untersuchten Patientenkollektivs................................................................................................ 46 Abb. 13: Häufigkeitsverteilungen nach Tumortyp des untersuchten Patientenkollektivs................................................................................................ 46 Abb. 14: Altersverteilung des untersuchten Patientenkollektivs ........................... 48 Abb. 15: Lokalisationsverteilung nach Tumortyp des untersuchten Patientenkollektivs................................................................................................ 50 Abb. 16: Altersverteilung nach Tumortyp ............................................................. 51 Abb. 17: Alterspyramide unterteilt nach Tumortyp und Geschlecht ...................... 52 Abb. 18: Größenverteilung nach Tumortyp beim untersuchten Patientenkollektiv 53 Abb. 19: Anteil an Rezidiven und Prozentsatz an Rezidiven nach Tumortyp beim untersuchten Patientenkollektiv ............................................................................ 53 Abb. 20: Art der Defektdeckung beim untersuchten Patientenkollektiv ................ 54 Abb. 21: Prozentsatz an malignen Tumoren in unterschiedlichen Studien (Martínez, et al., 2014) ......................................................................................... 58 69 8 TABELLENVERZEICHNIS Tab. 1: Eintelung der Zysten im Mund- Kiefer-und Zahnbereich (Jundt, 2006) .... 31 Tab. 2: Codierungsschema der durchgeführten Analyse ..................................... 43 Tab. 3: Einteilung der Häufigkeit odontogener Tumoren nach histologischer Diagnose an der klinischen Abteilung für Mund- Kiefer- und Gesichtschirurgie Graz und dem Department für Zahnärztliche Chirurgie Graz gemeinsam ............ 46 Tab. 4: Einteilung der Häufigkeit odontogener Tumoren nach histologischer Diagnose an der klinischen Abteilung für Mund- Kiefer- und Gesichtschirurgie Graz (2004-2012) ................................................................................................. 47 Tab. 5: Einteilung der Häufigkeit odontogener Tumoren nach histologischer Diagnose an dem Department für Zahnärztliche Chirurgie Graz (2004-2012) ..... 47 Tab. 6: Geschlechts- und Altersverteilung der Grazer Studie mit 185 odontogenen Tumoren im Vergleich zur Histologie .................................................................... 48 Tab. 7: Lokalisationsverteilung der odontogenen Tumoren des untersuchten Patientenkollektivs................................................................................................ 49 Tab. 8: Odontogene Tumoren nach WHO Klassifikation, Auftreten und Demographie (Servato, 2012) im Vergleich mit Grazer retrospektiver Studie (2013) ............................................................................................................................. 57 70