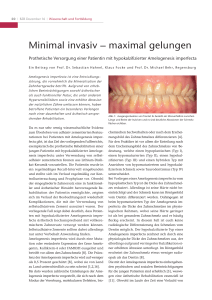
Wie korreliert der Phänotyp mit dem Genotyp?
Werbung

Roswitha Heinrich-Weltzien, Stefanie Baum, Sabine Bertzbach, Jan Kühnisch, Julia Hentschel ZAHNERHALTUNG Genetische Grundlagen der Amelo­ genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? Indizes Amelogenesis imperfecta, Zahnschmelz, Schmelzbildung, Phänotyp, Genotyp, Gene, Mutationen Zusammenfassung Die Bildung des menschlichen Zahnschmelzes ist ein komplexer Prozess, der auf molekularer Ebene reguliert wird. Er schließt tausende Gene und ihre Produkte ein. Bei der Amelogenesis imperfecta (AI) handelt es sich um eine erblich bedingte qualitative und quantitative Störung der Schmelzbildung mit heterogener genetischer Genese. Die Diagnose erfolgt anhand des klinischen Erscheinungsbildes. Phänotypisch imponieren ein hypoplastischer, hypomaturierter und hypokalzifizierter Schmelz sowie klinische Mischformen. Mutationen in den Genen Enamelin (ENAM), Amelogenin (AMELX), Kallikrein 4 (KLK4), Enamelysin (Matrix Metalloproteinase 20, MMP20), Distal-less Homeobox 3 (DLX3), WD Repeat-containing Protein 72 (WDR72) und Family with sequence similarity, member H (FAM83H) verursachen eine isolierte AI mit unterschiedlichen Phänotypen. Dennoch lässt sich bei einer Reihe von Patienten mit klinisch manifester AI keine Mutation in den o. g. Genen nachweisen. Es ist daher zu erwarten, dass weitere AI verursachende Gene durch molekulargenetische Untersuchungen identifiziert werden. Definition und Epidemiologie Stefanie Baum Dr. med. dent. Poliklinik für Präventive Zahnheilkunde und Kinderzahnheilkunde Universitätsklinikum Jena Bachstraße 4 07743 Jena E-Mail: [email protected] Sabine Bertzbach Zahnärztin Zahnarztpraxis, Bremen Jan Kühnisch Priv.-Doz. Dr. med. dent. Poliklinik für Zahnerhaltung und Parodontologie Klinikum der Ludwig-Maximilians-Universität München Bei der Amelogenesis imperfecta (AI) handelt es sich um eine klinisch und ätiologisch heterogene Gruppe von genetisch bedingten Erkrankungen, die durch qualitative und quantitative Störungen der Schmelz­ entwicklung charakterisiert sind, während die Dentin­ struktur unverändert ist13. Die AI kann entweder isoliert oder in Kombination mit weiteren Krankheitszeichen bei zahlreichen syndromalen Erkrankungen auftreten, wobei die nicht syndromalen Formen am häufigsten vorkommen3,4. Sie wird autosomal-dominant, auto­ somal-rezessiv oder X-gebunden vererbt, kann aber auch sporadisch in einer Familie in Erscheinung tre­ ten. Daten zum Vorkommen der AI sind sehr begrenzt. Bei 3- bis 19-Jährigen in Nordschweden lag eine Präva­ Quintessenz 2015;66(4):373–386 Roswitha Heinrich-Weltzien Prof. Dr. med. dent. Julia Hentschel Dr. rer. nat. CF-Zentrum – Klink für Kinder- und Jugendmedizin Universitätsklinikum Jena und Institut für Humangenetik Universitätsklinikum Leipzig 373 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? lenz von 1,4:1.000 vor2. Die ermittelte Häufigkeit betrug in einer großen israelischen Studiengruppe 1:8.0009 und in einer US-amerikanischen Population 1:14.00034. Somit variieren die Angaben beträchtlich zwischen den untersuchten Regionen. Für Deutschland sind im Schrifttum keine epidemiologischen Daten verfügbar. Klinisches Erscheinungsbild und Diagnostik Das klinische Erscheinungsbild der AI ist sehr vielfältig, da sie durch unterschiedliche Störungen der Schmelz­ bildung verursacht wird (Tab. 1). Als dominierende klinische Manifestation tritt bei 60 bis 73 % der Betrof­ fenen eine Schmelzhypoplasie auf8, wobei der korrekt mineralisierte Zahnschmelz aufgrund des insuffizienten appositionellen Wachstums in Verbindung mit einer fehlenden Kristallitverlängerung pathologisch dünn oder hypoplastisch ist16 (Abb. 1a bis d). Die schwerste Form der hypoplastischen AI stellt die Schmelzagene­ sis dar, bei welcher klinisch und röntgenologisch kein Schmelz erkennbar ist. In Abhängigkeit von der Schmelz­ ­dicke gestaltet sich der Approximalkontakt; fehlende Kontakte sind für kleine Zähne typisch. Die Zahnfarbe ist gelblich bis bräunlich. Die Störung einer adäquaten Entfernung der orga­ nischen Matrix und Reifung der Schmelzkristallite in der Schmelzentwicklung führt zu einem pathologisch Tab. 1 Klinische und genetische Charakteristika der phänotypischen vier AI-Hauptgruppen nach Wright35. AD = autosomaldominant, AR = autosomal-rezessiv AI-Typen Klinisches Erscheinungsbild Schmelzdicke Röntgenologisches Erscheinungsbild Genetik Typ I: Hypoplasie des Schmelzes • Größe der Kronen variiert in Abhängigkeit von der Schmelzdicke • Fehlender Approximalkontakt bei kleinen Zähnen • Zahnoberfläche ist rau • Zahnfarbe variiert von normal bis opak weiß oder gelblich-bräunlich • Variiert in Dicke von normal bis dünn oder fehlend • Es imponieren Furchen, Rillen, Grübchen • Schmelz hat normale bis leicht reduzierte Opazität AD, AR oder X-chromosomal Typ II: Hypomaturation des Schmelzes • Zahnoberfläche ist weich und rau • Zahnfarbe variiert von cremig opak bis gelb/braun • Häufige dentale Hypersensitivität • Häufig offener Biss • Normale Dicke • Röntgenopazität • Schmelz abradiert/ entspricht der von attritiert sehr leicht Dentin oder ist nur geringfügig stärker • Nicht durchgebrochene Zähne zeigen normale Morphologie AD, AR oder X-chromosomal Typ III: Hypokalzifikation des Schmelzes • Zahnoberfläche ist weich und rau • Zahnfarbe variiert von weiß bis gelb/braun • Häufige dentale Hypersensitivität • Häufig offener Biss • Häufig starke Zahnsteinablagerung • Normale Dicke • Röntgenopazität • Schmelz abradiert/ entspricht der von attritiert sehr leicht Dentin oder ist nur geringfügig schwächer • Nicht durchgebrochene Zähne zeigen normale Morphologie AD, AR Typ IV: Hypomaturation/ Hypoplasie/ Taurodontismus • Größe der Kronen variiert in Abhängigkeit von der Schmelzdicke • Fehlender Approximalkontakt bei kleinen Zähnen • Zahnfarbe variiert von weiß bis gelb/braun • Reduzierte Dicke • Hypomineralisier­ te Areale und Grübchen AD 374 • Normale Röntgenopazi­ tät bzw. geringfügig stärker als die von Dentin • Große Pulpenkammern Quintessenz 2015;66(4):373–386 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? a b c d Abb. 1a bis d Die hypoplastische AI (AI-Typ I) tritt phänotypisch äußerst variabel auf. Klinisch kann eine sehr raue (a) bis weniger raue Zahnoberfläche (b) imponieren, wobei röntgenologisch in Abhängigkeit von der Stärke der Schmelzhypoplasie fehlender Schmelz erkennbar ist (c und d). Die Patienten fühlen sich aufgrund des Aussehens ihrer Zähne ästhetisch stark beeinträchtigt weichen Schmelz oder zur Hypomaturationsform der AI16. Die Zahnkronen sind von normaler Größe und weisen Approximalkontakte auf. Der Schmelz ist weich, rau und abradiert leicht; die Röntgendichte ent­ spricht der von Dentin. Die Patienten klagen häufig über eine Hypersensitivität und weisen nicht selten einen offenen Biss auf (Abb. 2a und b). Eine Störung der Mineralisation geht mit der hypo­ kalzifizierten AI-Form einher16. Die Schmelzschicht ist normal dick, rau sowie weich und zeigt schnelle Ab­ nutzungserscheinungen nach dem Zahndurchbruch. Neben dem offenen Biss imponieren bei Patienten mit dieser AI-Form auch ausgeprägte Zahnsteinablage­ rungen (Abb. 3a und b). Quintessenz 2015;66(4):373–386 Da der Schmelz bei der hypomaturierten und der hypokalzifizierten AI-Form nicht den Mineralisations­ grad von gesundem Schmelz erreicht, bezeichnet man beide Formen auch als hypomineralisierte AI. Etwa 20 bis 40 % der AI-Fälle werden der Hypomaturation und etwa 7 % der Hypokalzifikation zugeordnet8. Als AI-Typ IV wird das Vorliegen einer Kombination von Hypomaturation und Hypoplasie in Verbindung mit einem Taurodontismus bezeichnet (Tab. 1). Während der dominierende Erbgang für den jewei­ ligen klinischen Phänotyp der Tabelle 1 entnommen werden kann, fasst Tabelle 2 die Charakteristika für den autosomal-dominanten, den autosomal-rezessiven und den X-gebundenen Erbgang der AI zusammen. 375 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? a b Abb. 2a und b Charakteristisch für die Hypomaturationsform der AI (AI-Typ II) ist ein Schmelz von normaler Dicke und Härte, aber weißlicher Farbe (a). Differenzialdiagnostisch muss diese AI-Form von einer mittleren Dentalfluorose abgegrenzt werden (b), insbesondere wenn nahezu alle Zähne betroffen sind. In der Regel erlaubt eine sorgfältige Anamnese die Erstellung der Differenzialdiagnose a b Abb. 3a und b Die hypokalzifizierte Form der AI (AI-Typ III) zeichnet sich durch eine normal dicke, aber weiche und raue Oberfläche aus (a). Die Röntgenopazität des Schmelzes entspricht der von Dentin (b) Tab. 2 Charakteristika der unterschiedlichen Erbgänge bei Vorliegen einer AI Erbgang Charakteristika Autosomal- dominant • Mögliche Übertragung von männlichen auf männliche Individuen • Es liegt eine 50%ige Chance vor, dass ein Kind eines betroffenen Elternteils auch betroffen ist • Betroffene männliche und weibliche Patienten zeigen ein ähnliches klinisches Erscheinungsbild Autosomal-rezessiv • Nicht betroffene Eltern können betroffene Kinder haben • Durchschnittlich ist eines von vier Kindern betroffen, wenn die Eltern Träger des Gendefektes sind • Häufiger vorkommend, wenn Eltern blutsverwandt sind X-chromosomal • Keine Übertragung von männlichen auf männliche Individuen • Alle Töchter eines betroffenen Mannes sind Trägerinnen des Gendefektes • Die Hälfte der Söhne einer mütterlichen Trägerin des Gendefektes sind betroffen • Betroffene männliche Individuen weisen schwerere Manifestationen als weibliche Individuen auf • Mädchen/Frauen können aufgrund einer Lyonisation (zufällige Inaktivierung eines der beiden X-Chromosomen) keine bis schwere Manifestationen aufweisen. Trägt die Frau auf einem der beiden X-Chromosomen eine AI verursachende Mutation, kann es zur Ausprägung einer AI kommen. Der Schweregrad hängt von dem aktiven Anteil des X-Chromosoms ab, welches die Mutation trägt 376 Quintessenz 2015;66(4):373–386 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? Weitere Leitsymptome einer AI sind Hypersensibili­ tät oder Schmerzen auf thermische und chemische Reize sowie rasche Attrition der Zähne mit Verlust der vertikalen Dimension (Bisshöhe). Pathologische Gingi­ vabefunde wie Gingivitis oder Gingivahyperplasie werden häufig begleitend beobachtet11,17. Die Folgen sind funktionelle und ästhetische Einschränkungen – viele Patienten berichten von einem gestörten Sozial­ verhalten und psychischen Problemen25. Daher ist ein vertrauensvolles Zahnarzt-Patienten-Verhältnis für die im frühen Kindesalter beginnende und erst im jungen Erwachsenenalter mit der definitiven Versorgung en­ dende zahnärztliche Betreuung erforderlich, welche bei vielen Patienten von einer kieferorthopädischen Behandlung flankiert werden muss32. Die AI kann auch zusammen mit anderen dentofa­ ­ zialen Störungen wie einer verzögerten Eruption, Zahn­unterzahl, Dentikeln, pathologischen Kronen- und Wurzelresorptionen sowie dem bereits erwähnten Tauro­ dontismus auftreten10,14. Des Weiteren besteht eine a b erhöhte Tendenz zu impaktierten bleibenden Zähnen und follikulären Zysten. Ein frontal offener Biss tritt, abhängig vom AI-Typ, mit einer Prävalenz von 30 bis 60 % auf13,28. Die Diagnose und die Klassifikation der AI basieren traditionell auf dem klinischen Erscheinungsbild oder dem Phänotyp. Die am weitesten verbreitete Klassifi­ kation der AI teilt die Erkrankung auf der Grundlage der dominierenden Schmelzbildungsstörung in die ge­ nannten vier AI-Haupttypen (Tab. 1) ein, die aufgrund des vielfältigen Phänotyps in weitere 14 unterschiedli­ che Subtypen unterteilt werden33. Differenzialdiagnostik Differenzialdiagnostisch muss die AI von den exogen und endogen bedingten Strukturstörungen abgegrenzt werden21,22. Charakteristikum einer exogen bedingten Strukturstörung ist ihr solitäres Auftreten (Abb. 4a bis d). Betroffen sind vor allem die bleibenden Frontzähne c d Abb. 4a bis d Exogen bedingte Strukturstörungen imponieren als Schmelzbildungsstörungen von Einzelzähnen – in der Regel sind die Frontzähne und Prämolaren betroffen. a: Hypoplasie und Opazität an der Labialfläche von Zahn 21 nach Frontzahntrauma im Alter von 3 Jahren. b: Hypoplasie an der Labialfläche von Zahn 41 nach Frontzahntrauma im Alter von 2 Jahren. c und d: Ausgeprägte Hypoplasien an den Zähnen 35 und 45 nach apikalen Parodontitiden an den Zähnen 75 und 85 Quintessenz 2015;66(4):373–386 377 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? a b Abb. 5a und b Endogen bedingte Strukturstörungen imponieren als Schmelzbildungsstörungen von Zahngruppen, die in der gleichen Zeit mineralisieren. a: Schmutzig gräulich-bräunliche Verfärbung der Zähne infolge einer Tetracyclin-Medikation. b: Hypoplasien an den oberen und unteren Schneidezähnen nach häufiger Antibiotikagabe im Kleinkindalter und Prämolaren. Zu den Ursachen gehören apikale Parodontitiden als Folge unbehandelter Milchzahnkaries oder von Milchzahntraumata im Fall der Frontzähne21. Sie werden auch Turner-Zähne genannt. Als Kennzeichen der endogen (oder systemisch) be­ dingten Strukturstörungen gelten das symmetrische Auftreten und die anamnestisch mögliche zeitliche Zu­ ordnung zu einem Ameloblasten schädigenden In­ sult21,22. Am bekanntesten sind medikamentös beding­ te Störungen durchTetracyclin, Minocyclin, Ciprofloxacin und Fluoride30. Je nach Entwicklungsphase werden verschiedene Zahngruppen oder Zahnanteile betroffen, die sich der Dauer des jeweiligen Insultes zeitlich zuord­ nen lassen (Abb. 5a und b). Systemerkrankungen (Dia­ betes, Zöliakie) oder strahlenbedingte Schäden können sich ebenfalls an den Zähnen als Entwicklungsstörun­ 378 gen manifestieren. Die häufigste Differenzialdiagnose zu einer AI stellt die Dentalfluorose dar, insbesondere wenn alle Zähne betroffen sind. Im Fall einer Fluoridauf­ nahme von mehr als 0,05 bis 0,07 mg/kg Körpergewicht ist das Risiko einer Dentalfluorose gegeben15. Hier reicht das Spektrum von weißlichen, unregelmäßig be­ grenzten Flecken bei den milden Formen bis hin zu aus­ gedehnten schmutzig grauen oder bräunlichen Verfär­ bungen mit lochartigen Hypoplasien bei den schweren Formen (Abb. 6a und b). Letztere finden sich nur bei Patienten, die während der gesamten Zahnentwicklung (über das 8. Lebensjahr hinaus) in Gebieten mit hohem Fluoridgehalt im Trinkwasser gelebt haben. Genetisch bedingte Strukturstörungen zeichnen sich durch ihr Vorkommen an allen Zähnen im Milchwie auch im bleibenden Gebiss aus (Abb. 7a und b). Quintessenz 2015;66(4):373–386 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? a b Abb. 6a und b Differenzialdiagnostische Abgrenzung unterschiedlicher Schwergrade der Dentalfluorose von der AI. a: Mittlere Dentalfluorose mit Schmelzeinbruch an den Zähnen 11 und 21. b: Seitenzahngebiet eines Patienten mit einer schweren Dentalfluorose. Die Zähne sind stark braun verfärbt und weisen zahlreiche lochfraßartige Schmelzdefekte auf. Beide Patienten lebten während der gesamten Gebissentwicklungsphase in endemischen Fluorosegebieten a b Abb. 7a und b Genetisch bedingte Strukturstörungen imponieren als Schmelzbildungsstörungen an allen Zähnen beider Dentitionen. a: Hypoplastische AI mit rauer, gefurcht und erodiert erscheinender Oberfläche. b: Dentinogenesis imperfecta Quintessenz 2015;66(4):373–386 379 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? Neben den unterschiedlichen Formen der AI ist noch die Dentinogenesis imperfecta klinisch bedeutsam. Vier einfache Fragen können bei der differenzialdia­ gnostischen Abgrenzung zu den endogen bedingten Strukturstörungen hilfreich sein11: 1. Hat noch jemand in der Familie eine vergleichbare Erkrankung der Zähne? 2. Sind alle Zähne in gleicher Weise betroffen? 3. Besteht ein chronologischer Zusammenhang zur Zahnbildung? 4. Liegen Grundleiden, metabolische Erkrankungen oder frühere Medikamenteneinnahmen vor, die ei­ nen Einfluss auf die Schmelzbildung haben? Genetische Grundlagen der Amelogenesis imperfecta Obwohl seit den 1990er Jahren zahlreiche ursächlich für eine AI verantwortliche Gendefekte identifiziert wurden, sind die molekularen Grundlagen vieler AI-Formen nach wie vor nicht bekannt. Für den Kliniker besteht die Möglichkeit, sich in der Online-Datenbank „Online Medelian Inheritance of Man“ (OMIM) über die geneti­ sche Heterogenität der AI zu informieren24. Gegenwärtig sind 12 Gene bekannt, die eine iso­ lierte Form der AI verursachen können31,36,38. Tabelle 3 führt sie nach ihrem Erbgang, dem OMIM-Erkran­ Tab. 3 Identifiziert Kandidatengene, die eine nicht syndromale AI verursachen und in der genetischen Datenbank OMIM24 gelistet sind36 OMIM PhänotypErkrankungsnummer Kandidatengene/ (Chromosomale Lokalisation) Beschreibung des Schmelz-Phänotyps Autosomal-dominante Vererbung 104500 ENAM (4q21) Lokalisierte oder generalisierte hypoplastische AI, Taurodontismus ist möglich 104510 DLX3 (17q21.3-q22) Hypoplastischer und hypomaturierter Schmelz 130900 FAM83H (8q24.3) Lokalisierter oder generalisierter hypokalzifizierter Schmelz Autosomal-rezessive Vererbung 204650 ENAM (4q21) Generalisierte hypoplastische AI 204700 KLK4 (19q13.4) Normale hypomineralisierte Schmelzdicke von orange-brauner Färbung 612529 MMP20 (11q22.3-q23) Normale hypomineralisierte Schmelzdicke von orange-brauner Färbung 613211 WDR72 (15.q21.3) Hypomaturationsform der AI mit cremig opakem Schmelz beim Zahndurch­ bruch, Verfärbung und Verlust der Zahnhartsubstanz posteruptiv 614253 FAM20A (17q24.2) Generalisierte hypoplastische AI mit Störung der Zahneruption und Gingiva­ hypertrophie 614832 C4orf26 (4q21.1) Hypomaturationsform der AI 615887 SLC24A4 (14q32) Hypomaturationsform der AI AMELX (Xq22-q28) Schmelzhypoplasie oder Schmelzhypomaturation X-gebundene Vererbung 301201 380 Quintessenz 2015;66(4):373–386 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? kungscode und den jeweils betroffenen Genen bzw. der chromosomalen Lokalisation auf. Der Erbgang ist je nach dem betroffenen Gen variabel. Mutationen im ENAM (Enamelin)-Gen (4q21) weisen in Abhängigkeit von der Mutationsart einen autosomal-dominanten (OMIM-Nr. 104500) oder autosomal-rezessiven Erb­ gang (OMIM-Nr. 204650) auf. Veränderungen in den Genen DLX3 (Distal-less Homeobox 3; 17q21.3-q22; OMIM-Nr. 104510) und FAM83H (Family with sequen­ ce similarity, member H; 8q24.3; OMIM-Nr. 130900) bedingen eine autosomal-dominante AI-Form. Auto­ somal-rezessive AI-Formen werden durch Veränderun­ gen in den Genen KLK4 (Kallikrein 4; 19q13.4; OMIMNr. 204700), MMP20 (Matrix Metalloproteinase 20 Enamelysin; 11q22.3-q23; OMIM-Nr. 204700) und WDR72 (WD Repeat-containing Protein 72; 15.q21.3; OMIM-Nr. 613211) verursacht. Nach jüngsten Berich­ ten sind Mutationen der Gene C4orf26 (4q21.1; OMIMNr. 614832) und SLC24A4 (Solute carrier family 24 member 24/NCKX4; 14q32; OMIM-Nr. 615887) mit einer Hypomaturationsform der AI vergesellschaftet26,27,36. Die X-gebundene AI-Form ist ursächlich durch eine Mutation im AMELX-Gen (Amelogenin; Xq22-q28; OMIM-Nr. 301201) bedingt18,31. In einer aktuellen Übersicht zu den molekularen Grundlagen von genetischen Schmelzdefekten beim Menschen, die auf der Basis der OMIM-Datenbank im Jahr 2014 erstellt wurde, finden sich 93 phänotypisch gelistete Schmelzbildungsstörungen36. Von ihnen sind 12 Schmelzfehlbildungen isolierte nicht syndromale AI-Formen. Sowohl bei der isolierten als auch bei der syndromassoziierten AI imponieren die Schmelzhypo­ plasien als der häufigste Phänotyp und die Hypomine­ ralisationsdefekte als die seltensten Formen einer AI36. Kritisch wird von der Arbeitsgruppe um Wright ange­ merkt, dass die unterschiedlichen Beschreibungen des klinischen Phänotyps verwirrend sind. So finden sich Termini wie dysplastischer, hypomineralisierter und hypokalzifizierter Schmelz neben dem Begriff der Hy­ pomaturation. Weiterhin stellen die Autoren fest, dass selbst nach Sichtung der Originalarbeiten keine Grup­ pierung der verschiedenen Phänotypen möglich war. Von insgesamt 93 phänotypisch beschriebenen Schmelz­ Quintessenz 2015;66(4):373–386 bildungsstörungen sind für 72 Schmelzdefekte die molekulare Ätiologie oder die assoziierten Genloci in der OMIM-Datenbank gelistet. Das heißt, dass die mo­ lekulare Basis für 23 % aller hereditären Schmelzde­ fekte bislang nicht bekannt ist oder nicht aufgeführt wurde36. Eine wichtige Schlussfolgerung aus dieser OMIMÜbersicht besteht darin, dass die Phänotyp-Charakte­ risierung der Schmelzdefekte noch immer zu lücken­ haft ist und zukünftige Studien notwendig sind, die den Phänotyp von Schmelzfehlbildungen detaillierter erfassen. Vor dem Hintergrund der selbst für den er­ fahrenen Kliniker schwierigen Differenzierung der ein­ zelnen AI-Formen sowie der alleinigen genetischen Ursache der Erkrankung wurde die Klassifikation an­ hand des Genotyps favorisiert1. Demgegenüber wird jedoch auch deutlich herausgestellt, dass detailliertere Phänotyp-Beschreibungen bereits klare Hinweise bezüg­ lich der Rolle einzelner Gene, der von ihnen exprimier­ ten Proteine und möglicher Störungen in den unterschied­ lichen Phasen der Schmelzbildung liefern können36. Insofern sollte eine zukünftige Klassifikation von here­ ditären Schmelzdefekten eine Phänotyp-Ordnung, den Vererbungsmodus, den molekularen Defekt, Protein­ funktionen und ihre Rolle in der Schmelzbildung oder pathologische Mechanismen beinhalten. Ein solches Klassifikationssystem würde einen soliden Ordnungs­ ansatz liefern, der eine logische und informative Grup­ pierung der diversen genetischen Schmelzbildungs­ störungen erlaubt36. Phänotyp-Genotyp-Vergleiche Die jüngste und bislang größte multinationale Studie zur Phänotyp-Genotyp-Beziehung von der Arbeits­ gruppe um Wright38 schloss 71 Familien ein. Davon waren 224 Individuen von einer AI betroffen. In der Untersuchung erfolgten die Genotypisierung der sie­ ben Gene ENAM, AMELX, KLK4, MMP20, DLX3, WDR72 und FAM83H sowie die klinische und rönt­ genographische Phänotyp-Beschreibung und eine Stammbaumerstellung. Im Ergebnis der Studie konnte die molekulare Diagnose für 132 Individuen mit einer 381 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? AI (59 %) und 26 Familien (37 %) erstellt werden. Insge­ samt wurden in der Klientel 19 unterschiedliche Muta­ tionen der sechs Gene identifiziert. Am häufigsten lie­ ßen sich Mutationen im FAM83H-Gen nachweisen, gefolgt von AMLEX- und ENAM-Mutationen. Seltener konnten Mutationen in den Genen KLK4, MMP20 und WDR72 nachgewiesen werden. Im Vergleich zu einer früheren multinationalen Familienstudie aus dem Jahr 2006, in der lediglich für 25 % der AI-Fälle eine moleku­ lare Ätiologie festgestellt wurde20, resultiert der mole­ kulardiagnostische Zugewinn in der o. g. Studie von 2011 vorrangig aus der Identifikation der AI verursa­ chenden Kandidatengene FAM83H und WDR7212,19. Während Mutationen des WDR72-Gens mit der Hypomaturationsform der AI (OMIM-Nr. 613211, vgl. Tab. 3) assoziiert sind, zeichnet sich der Phänotyp der zahlreichen allelen Mutationen im FAM83H-Gen ent­ weder durch eine generalisierte Hypokalzifikation der gesamten Dentition oder durch lokalisierte, vorrangig in der zervikalen Region gelegene hypokalzifierte Defekte aus37 (OMIM-Nr. 130900, vgl. Tab. 3). Wesent­ liches Fazit der Studie war, dass es weitere AI ver­ ursachende Gene gibt, die zukünftig zu identifizieren sind. Eigene Untersuchungen zu Phänotyp-Genotyp-Ver­ gleichen bestätigen die Schlussfolgerungen von Baum5 sowie Wright et al.38. In der Studie wurden 44 Mitglieder von 17 Familien auf Schmelzdysplasien un­ tersucht. Für 32 Personen erfolgte eine molekular­ genetische Diagnostik, wobei 24 Patienten von einer AI betroffen waren, während 8 Personen als nicht be­ troffen charakterisiert wurden. Die Betroffenen zeigten das heterogene klinische Bild mit den bekannten AI-Phänotypen einer Hypoplasie, Hypomaturation und Hypokalzifikation sowie von unterschiedlichen Misch­ formen. Diese Phänotypen bildeten auch die Grund­ lage zur Klassifikation der AI (vgl. Tab. 1) und korrelie­ ren mit Störungen in den verschiedenen Stadien der Amelogenese. Patienten, bei denen neben der AItypischen Schmelzanomalie weitere morphologische Veränderungen oder syndromale Erkrankungen vor­ lagen, wurden nicht in die Untersuchung einge­ schlossen. 382 Zur Bestimmung des Genotyps diente den Patienten entnommenes venöses Vollblut. Die Untersuchungen wurden in einer Stufendiagnostik durchgeführt. Zuerst erfolgte die Komplettsequenzierung des ENAM-Gens, da in der Literatur ENAM-Mutationen als häufige Ursa­ che für eine isolierte AI beschrieben werden18. Im Fall eines unauffälligen Befundes des ENAM-Gens wurden die übrigen sechs Gene AMELX, KLK4, MMP20, DLX3, WDR72 und FAM83H analysiert. Ein weiteres Studien­ ziel war die Bestimmung der unterschiedlichen Häufig­ keit betroffener Gene. Mit der genetischen Untersuchung wurden in drei von sieben Genen pathogene Mutationen detektiert. In zwei Familien trat jeweils eine ENAM-Mutation bei Pati­ enten im homozygoten und heterozygoten Zustand auf. Die Merkmalsausprägungen einer generalisierten hypoplastischen AI waren bei unseren homozygoten Mutationsträgern wie in der Literatur beschrieben nach­ weisbar (Abb. 8a bis d). Die Hälfte der Patienten wies einen frontal offenen Biss auf. Demgegenüber wurde bei dem heterozygoten Patienten mit einer ENAMMutation eine lokalisierte hypoplastische, also mildere AI vorgefunden (Abb. 9a bis c). Klinisch sind für diese AI-Form die hypoplastischen Grübchen auf den Labial­ flächen der Frontzähne sowie die grübchen- und furchen­ artigen Defekte an den Molaren charakteristisch13,29. Die unterschiedlichen Phänotypen bestätigen somit die variable Expressivität einer ENAM-Mutation13. Ei­ ne weitere Familie war von einer DLX3-Mutation be­ troffen. Beide Mutationen wurden bereits mehrfach als krankheitsverursachend beschrieben6,7,13,29. In einer konsanguinen türkischstämmigen Familie konnte bei drei Geschwistern im WDR72-Gen eine Mutation nachgewiesen werden (Abb. 10a bis c). Die Patienten zeigten das klinische Erscheinungsbild einer AI vom Hypomaturationstyp in allen Phasen der Gebiss­ entwicklung. Diese Veränderung wurde bislang noch nicht im Zusammenhang mit einer AI beschrieben, sie ist jedoch zweifelsfrei als pathogen einzuschätzen. Im Ergebnis des Phänotyp-Genotyp-Vergleiches unserer AI-Patienten war das ENAM-Gen am häufigsten von einer Mutation betroffen, was mit den molekular­ genetischen Untersuchungen anderer Arbeitsgruppen Quintessenz 2015;66(4):373–386 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? a b c d Abb. 8a bis d Generalisierte hypoplastische AI im bleibenden Gebiss bei homozygoten Patientinnen mit einer ENAM- Mutation. Die Eltern der Patientinnen sind gesund, so dass ein autosomal-rezessiver Erbgang vorlag. a und b: Der sehr dünne Zahnschmelz der Patientin 1 ist eher glatt, röntgenologisch lässt sich kein Schmelz erkennen, und es bestehen keine Approximalkontakte. Aufgrund des frontal offenen Bisses und eines rechtsseitigen Kreuzbisses wurde eine kieferorthopädische Behandlung eingeleitet. c und d: Die Patientin 2 wurde prothetisch nur bis zu den Prämolaren mit Keramikkronen versorgt. Die unversorgten Molaren sind stark hypoplastisch a b c Abb. 9a bis c Lokalisierte hypoplastische AI im bleibenden Gebiss einer heterozygoten Patientin mit einer ENAM-Mutation. Hypoplastische Grübchen liegen an der Hälfte der Labialflächen der Schneidezähne (a) und der Molaren (b) vor. Die Eckzähne (c) sind im inzisalen Drittel stark hypoplastisch Quintessenz 2015;66(4):373–386 383 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? a b c Abb. 10a bis c Gebisssituation dreier türkischstämmiger Geschwister von blutsverwandten Eltern mit generalisierter, ausgeprägt hypoplastisch-hypomaturierter AI, bernsteinfarbener dünner bzw. fehlender Schmelzschicht und pathologischer Kronenanatomie. Patient 1 (a) weist ein permanentes Gebiss auf, Patient 2 (b) befindet sich in der mittleren Wechselgebissphase, und Patient 3 (c) ist in der frühen Wechselgebissphase. 1. Reihe: Frontalansichten. Frontal offener Biss bei Patient 1 sowie frontal und seitlich offener Biss bei Patient 2. 2. Reihe: Oberkieferaufsichten. 3. Reihe: Unterkieferaufsichten. 4. Reihe: In den Panoramaschichtaufnahmen der drei Geschwister wird die fehlende Schmelzschicht an allen Zähnen deutlich 384 Quintessenz 2015;66(4):373–386 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? korrespondiert6,13,18,29. Dennoch zeichneten die identi­ fizierten Mutationen für weniger als die Hälfte der AI-Fälle in unserer Studienpopulation ursächlich ver­ antwortlich. Aufgrund der hohen genetischen Hetero­ genität und des oftmals sporadischen Auftretens der Erkrankung ist daher zukünftig mit der Identifizierung von neuen Krankheitsgenen zu rechnen. Neueste Se­ quenziertechnologien („next-generation sequencing“, NGS) machen es möglich, dass alle proteincodieren­ den Sequenzen, das sogenannte Exom, gleichzeitig sequenziert werden können23. Der Begriff NGS um­ fasst verschiedene neue Sequenziermethoden. Da alle einen höheren Durchsatz als die Standardmethode der „Sanger-Sequenzierung“ aufweisen, sprechen die Autoren von einer neuen Ära des Sequenzierens, die zukünftig auch für die molekulare Diagnostik große Bedeutung erlangen wird. Fazit Die molekulargenetische Untersuchung stellt eine wich­ tige diagnostische Ergänzung zur sicheren Identifizierung von AI-Patienten dar. Das diagnostische Vorgehen wird durch den vorherrschenden Phänotyp bestimmt, der Rückschlüsse auf das am wahrscheinlichsten betroffene Gen zulässt. Die zweifelsfrei pathogene neue Mutation im WDR72-Gen von Patienten unseres Unter­suchungsgutes sowie die im Schrifttum vorliegenden Phänotyp-GenotypVergleiche unterstützen die These, dass bislang iden­ tifizierte Mutationen nur etwa die Hälfte der AI-Fälle bedingen. Die Existenz weiterer AI-Kandidatengene ist daher sehr wahrscheinlich. Durch einen standardisierten diagnostischen Ablauf bei AI-Patienten könnten zu­künf­ tig Versorgungsansprüche gegenüber der gesetzlichen Krankenversicherung geltend gemacht werden. Literatur 1. Aldred MJ, Savarirayan R, Crawford PJ. Amelogenesis imperfecta: a classification and catalogue for the 21st century. Oral Dis 2003;9:19-23. 2. Bäckman B, Holm AK. Amelogenesis imperfecta: prevalence and incidence in a northern Swedish county. Community Dent Oral Epidemiol 1986;14:43-47. 3. Bailleul-Forestier I, Berdal I, Vinckier F, de Ravel T, Fryns JP, Verloes A. The genetic basis of inherited anomalies of the teeth. Part 2: syndromes with significant dental involvement. Eur J Med Genet 2008;51: 383-408. 4. Bailleul-Forestier I, Molla M, Verloes A, Berdal A. The genetic basis of inherited anomalies of the teeth. Part 1: clinical and molecular aspects of non-syndromic dental disorders. Eur J Med Genet 2008;51: 273-291. 5. Baum S. Genetische Grundlagen der Amelogenesis imperfecta –Mutations­ frequenzen und Genotyp-PhänotypKorrelationen. Jena: Med. Diss., 2014. 6. Chan HC, Estrella NM, Milkovich RN, Kim JW, Simmer JP, Hu JC. Target gene analyses of 39 amelogenesis imperfecta kindreds. Eur J Oral Sci 2011;119(Suppl 1): 311-323. 7. Chan HC, Mai L, Oikonomopoulou A et al. Altered enamelin phosphorylation site causes amelogenesis imperfecta. J Dent Res 2010;89:695-699. Quintessenz 2015;66(4):373–386 8. Chaudhary M, Dixit S, Singh A, Kunte S. Amelogenesis imperfecta: Report of a case and review of literature. J Oral Maxillofac Pathol 2009;13:70-77. 9. Chosack A, Eidelman E, Wisotski I, Cohen T. Amelogenesis imperfecta among Israeli Jews and the description of a new type of local hypoplastic autosomal recessive amelogenesis imperfecta. Oral Surg Oral Med Oral Pathol 1979;47:148-156. 10. Collins MA, Mauriello SM, Tyndall DA, Wright JT. Dental anomalies associated with amelogenesis imperfecta: a radiographic assessment. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 1999;88:358-364. 11. Crawford PJ, Aldred M, Bloch-Zupan A. Amelogenesis imperfecta. Orphanet J Rare Dis 2007;2:17-28. 12. El-Sayed W, Parry DA, Shore RC et al. Mutations in the beta propeller WDR72 cause autosomal-recessive hypomaturation amelogenesis imperfecta. Am J Hum Genet 2009;85:699-705. 13. Hart TC, Hart PS, Gorry MC et al. Novel ENAM mutation responsible for autosomal recessive amelogenesis imperfecta and localized enamel defects. J Med Genet 2003;40:900-906. 14. Hegde S. Multiple unerupted teeth with amelogenesis imperfecta in siblings. N Am J Med Sci 2012;4:235-237. 15. Hellwig E, Schiffner U, Schulte A. Fluori­die­rungsmaßnahmen zur Karies­prophylaxe. S2k-Leitlinie der Deutschen Gesellschaft für Zahn-, Mund- und Kieferheilkunde. Stand: 23.01.2013. Internet: www.dgzmk.de/ uploads/tx_szdgzmkdocuments/ LLFluoridierungLangUpdate2013.pdf. Abruf: 03.03.2015. 16. Hu JC, Chun YH, Al Hazzazzi T, Simmer J. Enamel formation and amelogenesis imperfecta. Cells Tissues Organs 2007;186:78-85. 17. Jaouad IC, El Alloussi M, El Alaoui SC, Zahra Laarabi FZ, Lyahyai J, Sefiani A. Further evidence for causal FAM20A mutations and first case of amelogenesis imperfecta and gingival hyperplasia syndrome in Morocco: a case report. BMC Oral Health 2015;15:14. 18. Kang HY, Seymen F, Lee SK et al. Candidate gene strategy reveals ENAM mutations. J Dent Res 2009;88:266-269. 19. Kim JW, Lee SK, Lee ZH et al. FAM83H mutations in families with autosomal-dominant hypocalcified amelogenesis imperfecta. Am J Hum Genet 2008;82:489-494. 20. Kim JW, Simmer JP, Lin BP, Seymen F, Bartlett JD, Hu JC. Mutational analysis of candidate genes in 24 amelogenesis imperfecta families. Eur J Oral Sci 2006;114(Suppl 1):3-12, discussion 39-41. 21. Kühnisch K, Mach D, Bücher K, van Waes H, Hickel R, Heinrich-Weltzien R. Struktur­ störungen des Zahnschmelzes und des Dentins. Teil 1: Grundlagen, Terminologie, Diagnostik und Klassifikation. Quintessenz 2011;62:7-17. 385 ZAHNERHALTUNG Genetische Grundlagen der Amelo­genesis imperfecta – Wie korreliert der Phänotyp mit dem Genotyp? 22. Kühnisch K, Mach D, Bücher K, van Waes H, Hickel R, Heinrich-Weltzien R. Struktur­ störungen des Zahnschmelzes und des Dentins. Teil 2: Klinisches Erscheinungsbild. Quintessenz 2011;62:171-186. 23. Neveling K, Hoischen A. Exom-Sequenzierung zur Identifizierung von Krankheitsgenen. Med Gen 2012;24:4-11. 24. Online Mendelian Inheritance in Man (OMIM). Internet: www.ncbi.nlm.nih.gov/omim. 25. O’Sullivan J, Bitu CC, Daly SB et al. WholeExome sequencing identifies FAM20A mutations as a cause of amelogenesis imperfecta and gingival hyperplasia syndrome. Am J Hum Genet 2011;88: 616-620. 26. Parry DA, Brookes SJ, Logan CV et al. Mutations in C4orf26, encoding a peptide with in vitro hydroxyapatite crystal nucleation and growth activity, cause amelogenesis imperfecta. Am J Hum Genet 2012;91:565-571. 27. Parry DA, Poulter JA, Logan CV et al. Identification of mutations in SLC24A4, 386 encoding a potassiumdependent sodium/ calcium exchanger, as a cause of amelo­ genesis imperfecta. Am J Hum Genet 2013; 92:307-312. 28. Ravassipour DB, Powell CM, Phillips CL et al. Variation in dental and skeletal open bite malocclusion in humans with amelogenesis imperfecta. Arch Oral Biol 2005;50:611-623. 29. Seymen F, Lee KE, Koruyucu M et al. ENAM mutations with incomplete penetrance. J Dent Res 2014;93:988-992. 30. Tredwin CJ, Scully C, Bagan-Sebastian JV. Drug-induced disorders of teeth. J Dent Res 2005;84:596-602. 31. Urzua B, Ortega-Pinto A, Morales-Bozo I, Rojas-Alcayaga G, Cifuentes V. Defining a new candidate gene for amelogenesis imperfecta: from molecular genetics to biochemistry. Biochem Genet 2011;49: 104-121. 32. Wirsching E. Therapiekonzepte zur Behandlung der Amelogenesis imperfecta vom Kindes- bis zum Erwachsenenalter. Quintessenz 2014;65:1327-1338. 33. Witkop CJ Jr. Amelogenesis imperfecta, dentinogenesis imperfecta and dentin dysplasia revisited: problems in classification. J Oral Pathol 1988;17:547-553. 34. Witkop CJ, Sauk JJ. Heritable defects of enamel. In: Stewart R, Prescott G (eds). Oral facial genetics. St. Louis: CV Mosby, 1976:151-226. 35. Wright J. The diagnosis and treatment of dentinogenesis imperfecta and amelo­ genesis imperfecta. Hellenic Dent J 1993;2: 17-24. 36. Wright JT, Carrion IA, Morris C. The molecular basis of hereditary enamel defects in humans. J Dent Res 2015;94: 52-61. 37. Wright JT, Frazier-Bowers S, Simmons D et al. Phenotypic variation in FAM83H-associated amelogenesis imperfecta. J Dent Res 2009; 88:356-360. 38. Wright JT, Torain M, Long K et al. Amelo­ genesis imperfecta: genotype-phenotype studies in 71 families. Cells Tissues Organs 2011;194:279-283. Quintessenz 2015;66(4):373–386