2 Endokrinologie
Werbung

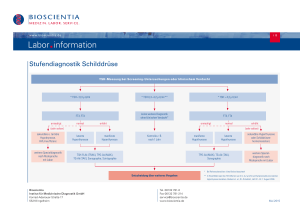
18 2 Endokrinologie 2.1 Schilddrüsendiagnostik Leitlinie zur Schilddrüsendiagnostik (Version 2)1, 2 III. In-vitro-Diagnostik Markus Dietlein, Jochen Dressler, Frank Grünwald, Klaus Joseph, Bernhard Leisner, Ernst Moser, Christoph Reiners, Johann Rendl, Harald Schicha, Peter Schneider, Otmar Schober 1. Indikationen: a. Bestandteil jeder Schilddrüsenfunktionsdiagnostik b. TSH-Screening bei Neugeborenen 2. Standardmethoden: immunometrische Methoden der zweiten, dritten oder vierten Generation (IRMA, ILMA) 3. Qualitätskriterien: a. funktionelle Assaysensitivität (TSH-Konzentration bei VK ≤ 20 %): < 0,1 mU/l b. Messung von WHO- oder Medical Research Council (MRC) Standards mit ±5 % des erwarteten Wertes c. sichere Trennung von euthyreoten und hyperthyreoten Patientenkollektiven (Überlappung < 1 %) d. kein High-Dose-Hook-Effekt bis zu einer TSH-Konzentration von 300 mU/l e. Parallelität von Verdünnungskurven von Patientenseren zur Standardkurve (±10 %) f. Kreuzreaktion mit anderen Glykoproteinen (LH, FSH, hCG) < 0,01 % 4. Beurteilung: a. Referenzbereich: meist 0,4−4,0 mU/l b. bei Hypothyreose: > 4,0 mU/l c. bei Hyperthyreose supprimiert: < 0,1 mU/l d. bei klinischer Euthyreose und normalem TSH zusätzliche Bestimmung der Schilddrüsenhormone nicht nötig! I. Zielsetzung Diagnostik von Schilddrüsenkrankheiten mit Labormethoden und bildgebenden Verfahren II. Definition Schilddrüsenkrankheiten sind durch pathologische Veränderungen entweder der Morphologie (Struma, benigne oder maligne) und/oder des Funktionszustandes des Organs (Hypothyreose oder Hyperthyreose) definiert. Die genaue Klassifikation der Schilddrüsenerkrankungen der Sektion Schilddrüse der Deutschen Gesellschaft für Endokrinologie befindet sich in den Tabellen 2-1 und 2-2. 1 Die vorliegende Leitlinie wurde abgestimmt zwischen der Deutschen Gesellschaft für Nuklearmedizin (Vorstand, Arbeitsausschuss Klinisches Qualitätsmanagement, Arbeitsgemeinschaft Therapie, Arbeitsgemeinschaft Schilddrüse), der Deutschen Gesellschaft für Endokrinologie (Sektion Schilddrüse) und der Deutschen Gesellschaft für Chirurgie (Chirurgische Arbeitsgemeinschaft Endokrinologie). 2 Aus: Nuklearmedizin 2003; 42: 109–15. A.Basales TSH B. TRH-Test 1. Indikationen: nur noch in Problemfällen a. Non-Thyroidal Illness (NTI) und gleichzeitig Verdacht auf Schilddrüsenkrankheit b. Vorliegen einer hypophysären oder hypothalamischen Erkrankung 2.1 Schilddrüsendiagnostik 19 Tab. 2-1 Einteilung der Schilddrüsenfunktionsstörungen (nach Sektion Schilddrüse 1985) Hypothyreose Hyperthyreose 1. Neugeborenen-Hypothyreose 1. bei Immunthyreopathie 1.1 1.1 bei Morbus Basedow angeboren (irreversibel) 1.1.1 bei Schilddrüsenaplasie 1.1.2 bei Schilddrüsendysplasie 1.1.2.1 entop 1.2bei anderen Immunkrankheiten (z. B. Hashimoto-Thyreoditis) 2. bei anderen Entzündungen 1.1.3 bei Iodfehlverwertung 3. bei funktioneller Autonomie 1.1.4 bei peripherer Hormonresistenz 3.1 disseminiert 1.1.5 bei TSH-Mangel 3.2 unifokal (sog. autonomes Adenom) 1.2intrauterin erworben, z. B. durch Iodmangel, Iodexzess, immunogen 3.3 multifokal 4. bei Neoplasien 4.1 Adenome 4.2 Karzinome 1.1.2.2 ektop 2. postnatal erworben 2.1 primär (mit und ohne Struma) 2.1.1 entzündlich 2.1.2 postoperativ 2.1.3 nach Strahlenbehandlung 2.1.4 durch strumigene Substanzen 2.1.5 bei extremem Iodmangel 2.1.6 anderer Art 2.2sekundär (hypophysär bzw. hypothalamisch) 3. periphere Hormonresistenz 2. Standardmethoden: a. 200 µg TRH i. v. oder 1 mg als Spray nasal, bei Kindern Dosis körpergewichtsbezogen reduzieren b. Zeitpunkt der zweiten Blutentnahme abhängig von der Applikationsart und der Fragestellung: 30 min nach i. v. Applikation, 45 min nach nasaler Applikation bei vermuteter primärer Schilddrüsenerkrankung. Bei vermuteter hypophysärer oder hypothalamischer Erkrankung werden Blutentnahmen über 2–3 h in Intervallen von 30–60 min empfohlen. 5.durch TSH oder TSH-ähnliche Aktivitäten 5.1 hypophysär 5.2 paraneoplastisch 6. bei Iodexzess 7.durch exogene Hormonzufuhr (Thyreotoxicosis factitia) 3. Beurteilung: Stimulationswert 2,5−25 mU/l, Voraussetzung ist die Bestimmung des basalen TSH nach obigen Qualitätskriterien! C.Schilddrüsenhormone 1. Indikationen: a. erniedrigtes (< 0,4 mU/l) oder supprimiertes (< 0,1 mU/l) basales TSH zum Ausschluss oder Nachweis einer manifesten Hyperthyreose: Bestimmung von f T4 und f T3 (bzw. TT3) b. erhöhtes (> 4,0 mU/l) basales TSH: alleinige Bestimmung von f T4 ausreichend 20 2 Endokrinologie Tab. 2-2 Einteilung der Schilddrüsenkrankheiten (nach Sektion Schilddrüse 1985 und WHO 1988) Struma Schilddrüsenentzündungen A. Befunddeskription 1. akute Thyreoiditis a. entop (im Halsbereich) 1.1 eitrig 1.2 nicht eitrig (z. B. radiogen) a.α. diffus a.β. einknotig a.γ. mehrknotig b. 2.akut-subakute Thyreoiditis de Quervain dystop 3. chronische Thyreoiditis b.α. intrathorakal 3.1 Immunthyreopathie b.β. Zungengrundstruma 3.1.1 Struma lymphomatosa Hashimoto B. Pathogenese 1. bei Iodmangel 2. durch strumigene Substanzen 3. mit Autonomie 4.bei Zystenbildung, durch Blutung, nach Trauma 5. bei Immunthyreopathien 6. bei anderen Entzündungen 7. bei Schilddrüsentumoren 3.1.2 atrophische Thyreoditis 3.2 invasiv-sklerosierend (Riedel-Struma) 3.3spezifische Entzündungen (z. B. Tbc, Sarkoidose) 4.andere (sog. silent oder postpartale Thyreoditis) Schilddrüsentumoren I. epitheliale Tumoren A. benigne 1. follikuläres Adenom 2. andere bei Akromegalie B. maligne 10. bei Iodfehlverwertung 1. follikuläres Karzinom 11. bei Hormonresistenz 2. papilläres Karzinom 3. medulläres Karzinom 4. undifferenzierte Karzinome 5. andere II. nicht epitheliale Tumoren A. benigne B. maligne III. maligne Lymphome IV. andere VI. unklassifizierbare Tumoren 8.bei neoplastischer Produktion von TSH oder TSH-ähnlichen Aktivitäten 9. 12.bei Befall der Schilddrüse durch extrathyreoidale bzw. systemische Erkrankungen 13. andere VII. „tumor-like lesions“ 2.1 Schilddrüsendiagnostik 2. Standardmethoden: a. 2-Schritt-Verfahren b. 1-Schritt-Verfahren c. Indexmethode 3. Qualitätskriterien: 2-Schritt-Verfahren und moderne 1-Schritt-Verfahren sind weniger störanfällig und deshalb Analog-Tracer-Methoden vorzuziehen. 4. Beurteilung: a. Bei Kindern liegen höhere, bei Älteren (> 60 Jahre) niedrigere Hormonspiegel vor, deshalb sind altersentsprechende Referenzbereiche erforderlich! b. Fehlbestimmung freier Schilddrüsenhormone in folgenden Situationen möglich • bestimmte Medikamente (z. B. Heparin, Barbiturate, Acetylsalicylsäure usw.). • schwerkranke Patienten mit NTI-Syndrom • Schilddrüsenhormonantikörper • angeborene Anomalien der Schilddrüsenhormonbindungsproteine (bei Index-Methoden!) D Schilddrüsenautoantikörper 1. Antikörper gegen den TSH-Rezeptor (TSHR-AK) a. Indikationen: • Abgrenzung immunogene/nicht immunogene Hyperthyreose • bei Hyperthyreose und gleichzeitiger endokriner Orbitopathie entbehrlich • bei Schwangeren mit bestehendem oder zurückliegendem Morbus Basedow b. Standardmethoden: Radioligandenassay mit solubilisierten Thyreozytenmembranen vom Schwein; besser Assaysysteme der zweiten Generation (ILMA), bei denen als Antigen der rekombinante menschliche TSH-Rezeptor eingesetzt wird c. Beurteilung: • in etwa 80 % bei Patienten mit unbehandeltem Morbus Basedow TSH-R-AK nachweisbar, bei den Assays der zweiten Generation in mehr als 90 % der Patienten • selten bei Patienten mit Thyreoiditis Hashimoto oder atrophischer Thyreoiditis 21 • keine Aussage über die funktionelle Aktivität von TSH-R-AK • kein gesicherter Stellenwert in der Ver- laufsbeurteilung des Morbus Basedow hohe Titer sprechen jedoch für hohe Rezidivgefahr 2. Antikörper gegen Schilddrüsenperoxidase (TPO-AK) a. Indikationen: Verdacht auf chronisch lymphozytäre Thyreoiditis • bei echoarmer Binnenstruktur im Sonogramm, insbesondere vor Einleitung einer Therapie mit Iodid • bei latenter oder manifester Hypothyreose • Abgrenzung einer immunogenen von einer nicht immunogenen Hyperthyreose b. Standardmethoden: RIA, IRMA, ILMA, ELISA mit gereinigter humaner oder rekombinanter Schilddrüsenperoxidase als Antigen c. Qualitätskriterien: • Quantifizierung in internationalen Einheiten (IU/l) • Referenzpräparation: MRC 66/387 • Referenzbereich sollte in jedem Labor überprüft und neu erstellt werden. • Hämagglutinationstests sollten wegen ihrer geringen Sensitivität nicht mehr verwendet werden. d.Beurteilung: • bei Hashimoto-Thyreoiditis oder atrophischer Thyreoiditis in etwa 90 % der Fälle erhöht • Inzidenz bei Morbus Basedow geringer • mäßig erhöhte Titer auch bei nicht immunogenen Schilddrüsenerkrankungen • leicht erhöhte Titer gelegentlich bei älteren Menschen ohne Schilddrüsenerkrankungen 3. Antikörper gegen Thyreoglobulin (Tg-AK) a. Indikationen: • Verdacht auf chronisch lymphozytäre Thyreoiditis, wenn TPO-AK negativ sind • in Zusammenhang mit der Bestimmung von Thyreoglobulin • sehr 22 2 Endokrinologie b. Standardmethoden: RIA, IRMA, ILMA, ELISA c. Qualitätskriterien: siehe TPO-AK d. Beurteilung: • bei etwa 60−70 % der Patienten mit Hashimoto-Thyreoiditis oder atrophischer Thyreoiditis nachweisbar • bei etwa 20−40 % der Patienten mit Morbus Basedow nachweisbar E.Thyreoglobulin (Tg) 1. Indikationen: a. Verlaufskontrolle des differenzierten Schilddrüsenkarzinoms b. konnatale Hypothyreose c. Hyperthyreosis factitia 2. Standardmethoden: IRMA, ICMA 3. Qualitätskriterien: funktionelle Assaysensitivität: ≤ 1 ng/ml bei Interassay-CV ≤ 20 % 4. Beurteilung: a. zur Abschätzung einer möglichen Interferenz von Tg-AK • initial Tg-AK bestimmen; wenn Tg-AK erhöht, spätere Verlaufskontrollen • Bei jeder Tg-Bestimmung ist ein Wiederfindungstest obligatorisch! b. High-Dose-Hook-Effekt bei Wiederfindung ≤ 80 % beachten! F. Calcitonin/Pentagastrin-Test 1. Indikationen: medulläres Schilddrüsenkarzinom: Verdacht, Nachsorge und Verlaufskontrolle 2. Standardmethoden: Two-Site-Immunoassays: ICMA, ELISA 3. Qualitätskriterien: funktionelle Assaysensitivität sollte bei 1 pg/ml liegen 4. Beurteilung: a. Erhöhung bzw. grenzwertig hohes basales Calcitonin bei Patienten mit medullärem Schilddrüsenkarzinom b. erhöhte Calcitonin-Spiegel auch bei anderen Tumoren wie Karzinoiden, kleinzelligen Bronchialkarzinomen, selten auch bei Mamma- und Magenkarzinomen c. eindeutiger Anstieg im Pentagastrintest beweisend für ein manifestes medulläres Schilddrüsenkarzinom d. grenzwertiger oder fehlender Anstieg bei den anderen Tumoren G.Iodbestimmung im Urin 1. klinische Indikationen: bei klinischem Verdacht Ausschluss bzw. Nachweis einer Iodkontamination bei a. Patienten mit klinisch schwer verlaufender Hyperthyreose bzw. thyreotoxischer Krise b. Patienten mit therapieresistenter Hyperthyreose unter üblich dosierter thyreostatischer Therapie c. Patienten mit malignen Schilddrüsenerkrankungen vor Diagnostik oder Therapie mit radioaktivem Iod d. Kindern mit kongenitaler Hypothyreose 2. Standardmethoden: a. automatisierte Methoden: • Technikon-Autoanalyzer • HPLC b. nicht automatisierte Methoden: • Cer-Arsenit-Methode nach Wawschinek • Ammoniumpersulfat-Methode nach Pino c. semiquantitative Methoden: • Urojod®-Test • Fast-B-Methode nach Dunn 3. Qualitätskriterien: a. Herstellung von Standardpräparationen: Kaliumiodat (KIO3) oder Kaliumiodid (KI) b. Interassay-CV der quantitativen Methoden für Konzentrationen ≤ 50 µg/l unter 25 %, bei Konzentrationen > 50 µg/l unter 15 % c. Wiederfindungsrate für Iod sollte generell zwischen 90 und 110 % liegen d. interne Kontrollprobe obligat, z. B. gepoolter Urin mit Konzentration im Bereich 50−100 µg/l 4. Beurteilung: a. in Iodmangelgebieten Konzentrationen < 100 µg Iod/l bzw. < 100 µg Iod/g Kreatinin typisch