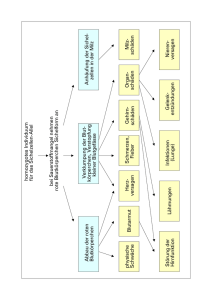
Genetische Parameter vor medikamentöser Therapie
Werbung

Nr. 192 - 04/2012 Genetische Parameter vor medikamentöser Therapie - Mutationen im Thiopurin-S-Methyltransferase (TPMT) -Gen - HLA B5701 und Abacavir - IL-28B und HCV-Therapie Mutationen im Thiopurin-S-Methyltransferase (TPMT) -Gen Die TPMT-Aktivität ist für die Verträglichkeit bzw. mögliche Toxizität von Thiopurinen entscheidend. Mutationen im TPMT-Gen können die Aktivität des Enzyms vermindern und so zu vermehrten Nebenwirkungen bei erhöhter Myelotoxizität führen. Besondere Vorsicht ist angezeigt bei gleichzeitiger Einnahme von Aminosalicylsäure (inkl. Mesalazin-Sulfasalazin), die das TPMT Enzym hemmen. TPMT Genotypen Das TPMT-Gen ist auf Chromosom 6 (6p22.3) lokalisiert. Folgende gut charakterisierte Mutationen im TPMTGen, die zusammen für ca. 90 - 95% der TPMT-Aktivitätsreduktion verantwortlich sind, werden durch die Analyse erfasst: Die Mutation der Base an Position 238 (Veränderung von G nach C), führt zu einem Austausch der Aminosäure Alanin nach Prolin (Allel TPMT*2). Dies vermindert die Enzymaktivität um den Faktor 100. Die Mutation der Base an Position 460 (Veränderung von G nach A), führt zu einem Austausch der Aminosäure Alanin nach Threonin (Allel TPMT*3B). Dies vermindert die Enzymaktivität um den Faktor 9. Die Mutation der Base an Position 719 (Veränderung von A nach G), führt zu einem Austausch der Aminosäure Tyrosin nach Cystein (Allel TPMT*3C). Dies vermindert die Enzymaktivität um den Faktor 1,4. Welche Bedeutung haben die TPMT Genotypen? Klasse Häufigkeit Genotyp (Beispiele) Interpretation Keine TPMT Defizienz ca. 89% 1/1 Uneingeschränkte Aktivität Mutation auf einem Allel ca. 11% 1 /2 od. 1/3B od. 1/3C Verminderte Aktivität Mutationen auf beiden Allelen in Compound Position ca. 0,3% 3A/3A od. 3A/3C od. 3A/2A stark verminderte Aktivität TPMT und Thiopurine Indikation der genetischen Analyse vor Einsatz von Thiopurinen (Azathioprin, 6-Mercaptopurin und 6-Thioguanin) in der Therapie autoimmuner Erkrankungen und chronisch-entzündlicher Darmerkrankungen sowie der Transplantationsmedizin. Bei Feststellung einer Myelosuppression in regelmäßigen Kontrollen des Blutbildes ist eine Reduktion bzw. das Absetzen der ThiopurinMedikation angeraten. Bei Vorliegen einer homozygoten TPMT-Defizienz sollte die Indikation von dosisreduziertem Azathioprin sehr streng gestellt werden. Abrechnung TPMT-Genanalyse EBM GOÄ Ziffer Punkte Ziffer 11322 2.825 3926, 3922, 3920 € (1,15-fach) 227,91 Nr. 192 - 04/2012 HLA B5701 und Abacavir Seit 1999 ist das Nukleosidanalogon Abacavir zur HIV-Therapie zugelassen und häufiger Bestandteil der Behandlung. Bei ca. 5% der Patienten ergibt sich durch die Gabe von Abacavir eine sogenannte Hypersensitivitätsreaktion (HSR). Diese tritt meist innerhalb der ersten sechs Wochen der Therapie auf und hat meistens einen schwerwiegenden Verlauf. Beim Auftreten einer HSR muss Abacavir abgesetzt werden und darf vom Patienten nicht wieder eingenommen werden. Studien belegen*, dass der überwiegende Teil von Patienten mit einer HSR auf Abacavir Träger eines HLA*B5701Allels ist. Patienten ohne HRS sind nur selten Träger dieses Allels. Abrechnung HLA B5701 EBM Abrechnung IL-28B EBM GOÄ Ziffer Punkte Ziffer 11320 780 3922, 3920 IL-28B und HCV-Therapie Assoziationsstudien haben Zusammenhänge zwischen dem Ansprechen der Therapie und einer Allelvariante des Interleukin IL-28B gezeigt. Ein single nucleotide polymorphismus (SNP) auf Chromosom 19 (rs12979860) führt zu zwei verschiedenen Allelen, bei denen entweder Cytosin (C) oder Thymidin (T) vorliegt. Patienten mit einer chronischen HCV-Infektion vom Genotyp 1, die homozygot für das C-Allel sind (C/C-Genotyp), haben 6 Monate nach Therapieende eine signifikant höhere Ansprechrate auf die Interferon-Kombinationstherapie („sustained viral response“, SVR bis zu 80%) als die, die den T/TGenotyp (SVR nur bis zu 30%) aufweisen. GOÄ € (1,15-fach) Ziffer Punkte Ziffer 93,84 11322 2.825 3924, 3922, 3920 € (1,15-fach) 113,95 Praktische Hinweise g Material 5 mL EDTA Blut Bitte beachten Sie, dass bei der Versendung des Materials eine rechtswirksame Einwilligungserklärung für die genetischen Untersuchungen vorliegt. Aufkleber sowie Einwilligungs- und Aufklärungsbögen können Sie als Einsender des LADR-Laborverbunds kostenfrei bei Intermed Service bestellen. freecall 0800 0850-113 freefax 0800 0850-114 Art.-Nr. Einwilligungs- und Aufklärungsbogen für: Art.-Nr. Einwilligungs- und Aufklärungsbogen für: 110336 Diagnostische genetische Untersuchungen* Prädiktive genetische Untersuchungen* 110342 Vorgeburtliche Risikoabklärung* 110464 Aufkleber für Anforderungsschein 110341 *Formulare ohne Durchschreibemöglichkeit können Sie sich unter www.ladr.de herunterladen. *Die Umfangreichste ist die PREDICT-1-Studie (S. Mallal et al., New Engl. J. Med. 2008, 358:568-579). Haben Sie Fragen zu diesem Thema? Ihr LADR-Labor berät Sie gern. Baden-Baden Berlin Braunschweig Bremen Bremerhaven Büdelsdorf Geesthacht Hannover Köln Kyritz Leer Münster Plön Recklinghausen – Dortmund Rostock Wittstock LADR-Labor Dr. Röck, Dr. Löbel Dr. Caspari Herr John Prof. Dr. Klouche, Dr. Kunz, Dr. Sandkamp Dr. Ambrosch, Dr. Prenzel Dr. Wrigge Dr. Kramer & Kollegen Dr. Dr. Wolff, Dr. Sloot Dr. Boogen Dr. Haßfeld Dr. Schott Dr. Dr. Belkien Dr. Krenz-Weinreich, Dr. Schulze Dr. Bachg, Dr. Haselhorst, Dr. Neef, Prof. Dr. Gödde Dr. Jung, Prof. Dr. Schaefer Prof. Dr. Mauff Telefon 07221 030 0531 0421 0471 04331 04152 0511 0221 033971 0491 0251 04522 02361 0381 03394 2117-0 301187-0 31076-100 4307-300 4805-539 70820-20 803-0 90136-11 935556-0 895-0 454590 48267-0 504-0 3000-0 659310 47711-0 Laborärztliche Arbeitsgemeinschaft für Diagnostik und Rationalisierung e. V. Lauenburger Straße 67 • 21502 Geesthacht • Telefon 04152 848-190 • Telefax 04152 848-490 E-Mail: [email protected] • Internet: www.ladr.de • freecall 0800 0850-111