ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
Werbung

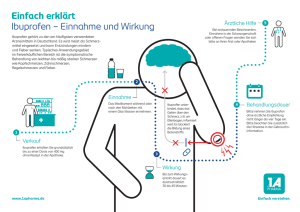
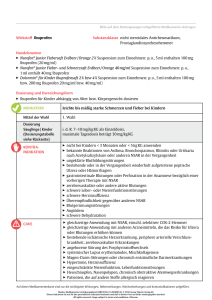
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 31 1. BEZEICHNUNG DES ARZNEIMITTELS Thomaprodol 400 mg - Weichkapseln 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede Weichkapsel enthält 400 mg Ibuprofen. Sonstiger Bestandteil mit bekannter Wirkung: 1 Kapsel enthält 95,94 mg Sorbitol Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1. 3. DARREICHUNGSFORM Weichkapsel Hellgelbe, ovale, transparente Weichgelatinekapseln mit einer Länge von 16-18 mm und dem schwarz aufgedruckten Schriftzug „B400“ 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete Zur kurzzeitigen symptomatischen Behandlung von – leichten bis mäßig starken Schmerzen wie Kopf-, Zahn- und Menstruationsschmerzen – Fieber und Schmerzen bei einer Erkältung Thomaprodol wird bei Erwachsenen und Jugendlichen ab 12 Jahren mit einem Gewicht über 40 kg angewendet. 4.2 Dosierung und Art der Anwendung Dosierung Erwachsene und Jugendliche ab 12 Jahren mit einem Gewicht über 40 kg: 400 mg Ibuprofen als Initialdosis. Falls erforderlich können weitere 400-mg-Dosen Ibuprofen eingenommen werden. Das Dosierungsintervall sollte entsprechend der Symptomatik und der empfohlenen maximalen Tagesdosis gewählt werden und nicht unter 6 Stunden liegen. Innerhalb von 24 Stunden sollte eine Gesamtdosis von 1.200 mg Ibuprofen nicht überschritten werden. Nur zur kurzfristigen Anwendung geeignet. Nebenwirkungen können minimiert werden, wenn die zur Symptomkontrolle erforderliche niedrigste wirksame Dosis über den kürzest möglichen Zeitraum angewendet wird (siehe Abschnitt 4.4). Der Patient sollte einen Arzt aufsuchen, wenn die Behandlung mit Thomaprodol bei Erwachsenen bei Fieber länger als 3 Tage und bei Schmerzen länger als 4 Tage erforderlich ist oder wenn sich die Symptome verschlimmern. Patienten mit empfindlichem Magen wird empfohlen, Thomaprodol während der Mahlzeiten einzunehmen. 32 Wird Thomaprodol kurz nach dem Essen eingenommen, setzt die Wirkung möglicherweise verzögert ein. In diesem Fall ist nicht mehr Thomaprodol einzunehmen, als in Abschnitt 4.2 (Dosierung) empfohlen wird. Thomaprodol ist erst nach Ablauf des entsprechenden Dosierungsintervalls erneut einzunehmen. Besondere Patientengruppen Ältere Personen Eine besondere Dosisanpassung ist nicht erforderlich. Aufgrund des möglichen Nebenwirkungsprofils (siehe Abschnitt 4.4) wird empfohlen, ältere Patienten besonders sorgfältig zu beobachten. Niereninsuffizienz Bei Patienten mit leichter bis mittlerer Nierenfunktionsstörung ist keine Dosisanpassung erforderlich (Patienten mit schwerer Niereninsuffizienz siehe Abschnitt 4.3). Leberinsuffizienz (siehe Abschnitt 5.2) Bei Patienten mit leichter bis mittlerer Leberfunktionsstörung ist keine Dosisanpassung erforderlich (Patienten mit schwerer Leberinsuffizienz siehe Abschnitt 4.3). Kinder und Jugendliche Thomaprodol darf aufgrund des hohen Wirkstoffgehalts bei Jugendlichen mit einem Körpergewicht unter 40 kg und bei Kindern unter 12 Jahren nicht angewendet werden (siehe Abschnitt 4.3). Wenn dieses Arzneimittel bei Jugendlichen länger als 3 Tage angewendet werden soll, oder wenn sich die Symptome verschlimmern, sollte ein Arzt konsultiert werden. Art der Anwendung Zum Einnehmen. Die Kapseln nicht kauen. 4.3 Gegenanzeigen Thomaprodol darf nicht angewendet werden bei: – – – – – – – – – – – 4.4 33 einer Überempfindlichkeit gegen Ibuprofen oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile Überempfindlichkeitsreaktionen (z. B. Bronchospasmen, Asthma, Rhinitis, Angioödeme oder Urtikaria) in Verbindung mit der Einnahme von Acetylsalicylsäure oder anderen nichtsteroidalen Antirheumatika (NSAR) in der Vergangenheit ungeklärten Blutbildungsstörungen bestehenden oder in der Vergangenheit wiederholt aufgetretenen Magengeschwüren/Blutungen (zwei oder mehr eindeutige Episoden einer diagnostizierten Ulzeration oder Blutung) gastrointestinalen Blutungen oder Perforationen in Verbindung mit einer NSAR-Therapie in der Vorgeschichte zerebrovaskulären oder anderen aktiven Blutungen schwerer Herzinsuffizienz (NYHA-Klasse IV) (siehe auch Abschnitt 4.4) schwerer Leberinsuffizienz oder schwerer Niereninsuffizienz (siehe auch Abschnitt 4.4) einer Schwangerschaft im letzten Trimenon (siehe Abschnitt 4.6) Jugendlichen mit einem Körpergewicht unter 40 kg und Kindern unter 12 Jahren Patienten mit schwerer Dehydratation (verursacht durch Erbrechen, Durchfall oder unzureichende Flüssigkeitsaufnahme) Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Nebenwirkungen können durch die Anwendung der niedrigsten wirksamen Dosis über die kürzeste Dauer, die zur Kontrolle der Symptome erforderlich ist (siehe unten unter gastrointestinale und kardiovaskuläre Risiken), reduziert werden. Besondere Vorsicht ist geboten bei Patienten mit folgenden Erkrankungen, die durch die Einnahme von Thomaprodol verschlimmert werden könnten: systemischer Lupus erythematodes und Mischkollagenose (mixed connective tissue disease): erhöhtes Risiko einer aseptischen Meningitis (siehe Abschnitt 4.8) angeborene Störung des Porphyrinstoffwechsels (z. B. akute intermittierende Porphyrie) gastrointestinale Erkrankungen und chronisch-entzündliche Darmerkrankungen (Colitis ulcerosa, Morbus Crohn) (siehe Abschnitt 4.8) Hypertonie und/oder Herzfunktionsstörungen, da sich die Nierenfunktion verschlechtern kann (siehe Abschnitte 4.3 und 4.8) Nierenfunktionsstörung (siehe Abschnitte 4.3 und 4.8) Leberfunktionsstörung (siehe Abschnitte 4.3 und 4.8) direkt im Anschluss an einen schweren operativen Eingriff bei Patienten mit allergischen Reaktionen gegen andere Stoffe, da bei ihnen das Risiko einer Überempfindlichkeitsreaktion bei Anwendung von Thomaprodol erhöht ist bei Patienten mit Heuschnupfen, Nasenpolypen oder chronisch obstruktiven Atemwegserkrankungen, da bei ihnen ein erhöhtes Risiko auf allergische Reaktionen besteht; diese können in Form eines Asthmaanfalls (sogenanntes Analgetika-Asthma), eines QuinckeÖdems oder einer Urtikaria auftreten. Gastrointestinale Wirkungen Die Anwendung von Thomaprodol zusammen mit NSAR, einschließlich selektiver Zyklooxygenase-2-Inhibitoren, erhöht das Risiko von Nebenwirkungen (siehe Abschnitt 4.5) und sollte vermieden werden. Ältere Personen Bei älteren Personen treten häufiger Nebenwirkungen unter NSAR auf, insbesondere in Form von gastrointestinalen (GI) Blutungen und Perforationen, die tödlich sein können (siehe Abschnitt 4.2). Gastrointestinale Blutung, Ulzeration oder Perforation In Verbindung mit allen NSAR wurden gastrointestinale Blutungen, Ulzerationen oder Perforationen berichtet, die mit oder ohne Warnsymptome oder frühere gastrointestinale Ereignisse in der Vorgeschichte zu allen Zeitpunkten der Behandlung aufgetreten sind und die tödlich sein können. Tritt bei mit Ibuprofen behandelten Patienten eine gastrointestinale Blutung oder Ulzeration auf, wird empfohlen, die Behandlung abzubrechen. Das Risiko einer gastrointestinalen Blutung, Ulzeration oder Perforation erhöht sich mit steigender NSAR-Dosis und ist bei Patienten mit Geschwüren in der Vorgeschichte, insbesondere in Verbindung mit Komplikationen wie Blutungen oder Perforationen (siehe Abschnitt 4.3), und bei älteren Patienten erhöht. Diese Patienten sollten die Behandlung mit der niedrigsten verfügbaren Dosis beginnen. Für diese Patienten und bei Patienten, die gleichzeitig eine geringe Dosis Acetylsalicylsäure oder ein anderes Arzneimittel benötigen, das möglicherweise das gastrointestinale Risiko (siehe unten und Abschnitt 4.5) erhöht, sollte eine Kombinationstherapie mit schützenden Arzneimitteln (z. B. Misoprostol oder Protonenpumpeninhibitoren) in Betracht gezogen werden. Patienten mit gastrointestinaler Toxizität in der Vorgeschichte, insbesondere älteren Personen, wird vor allem in der Anfangsphase der Behandlung empfohlen, alle ungewöhnlichen abdominalen Symptome (insbesondere gastrointestinale Blutungen) zu berichten. Vorsicht ist geboten bei Patienten, die gleichzeitig mit Arzneimitteln behandelt werden, die das Risiko einer Ulzeration oder Blutung erhöhen können, z. B. orale Kortikosteroide, Antikoagulanzien wie 34 Warfarin, selektive Serotonin-Wiederaufnahmehemmer oder Thrombozytenaggregationshemmer wie Acetylsalicylsäure (siehe Abschnitt 4.5). NSAR sollten Patienten mit gastrointestinalen Erkrankungen (Colitis ulcerosa, Morbus Crohn) mit Vorsicht verabreicht werden, da die Erkrankung verschlimmert werden könnte (siehe Abschnitt 4.8). Hautreaktionen In Verbindung mit der Anwendung von NSAR wurde sehr selten von schweren Hautreaktionen, einige mit Todesfolge, berichtet, darunter exfoliative Dermatitis, Stevens-Johnson-Syndrom und toxische epidermale Nekrolyse (siehe Abschnitt 4.8). Das höchste Risiko dieser Reaktionen scheint im Frühstadium der Therapie zu bestehen, da die Reaktionen in den meisten Fällen innerhalb des ersten Monats der Behandlung auftraten. Der Patient sollte bei den ersten Anzeichen eines Hautausschlags, von Schleimhautläsionen oder bei allen anderen Anzeichen einer Überempfindlichkeit die Einnahme von Thomaprodol abbrechen. In Ausnahmefällen können Varizellen die Ursache schwerwiegender infektiöser Komplikationen der Haut oder des Weichgewebes sein. Bisher kann nicht ausgeschlossen werden, dass NSAR zur Verschlimmerung dieser Infektionen beitragen. Deshalb wird von der Anwendung von Thomaprodol bei einer Varizellen-Infektion abgeraten. Kardiovaskuläre und zerebrovaskuläre Effekte Da in Verbindung mit einer NSAR-Therapie von Wassereinlagerungen, Hypertonie und Ödemen berichtet wurde, ist vor Beginn einer Behandlung von Patienten mit Hypertonie und/oder Herzinsuffizienz in der Vorgeschichte Vorsicht geboten (Absprache mit dem Arzt oder Apotheker). Klinische Studien weisen darauf hin, dass die Anwendung von Ibuprofen, insbesondere in hohen Dosen (2.400 mg / Tag) möglicherweise mit einem geringfügig erhöhten Risiko arterieller thrombotischer Ereignisse (z. B. Myokardinfarkt oder Schlaganfall) assoziiert ist. Insgesamt weisen epidemiologische Studien nicht darauf hin, dass Ibuprofen in niedrigen Dosen (z. B. ≤ 1.200 mg / Tag) mit einem erhöhten Risiko arterieller thrombotischer Ereignisse assoziiert ist. Bei Patienten mit unkontrollierter Hypertonie, Herzinsuffizienz (NYHA II-III), bestehender ischämischer Herzkrankheit, peripherer arterieller Verschlusskrankheit und/oder zerebrovaskulärer Erkrankung sollte Ibuprofen nur nach sorgfältiger Abwägung angewendet und hohe Dosen (2.400 mg/Tag) vermieden werden. Eine sorgfältige Abwägung sollte auch vor Beginn einer Langzeitbehandlung von Patienten mit Risikofaktoren für kardiovaskuläre Ereignisse (z. B. Hypertonie, Hyperlipidämie, Diabetes mellitus, Rauchen) stattfinden, insbesondere wenn hohe Dosen von Ibuprofen (2.400 mg/Tag) erforderlich sind. Weitere Anmerkungen Schwere akute Überempfindlichkeitsreaktionen (z. B. anaphylaktischer Schock) werden sehr selten beobachtet. Bei den ersten Anzeichen einer Überempfindlichkeitsreaktion nach Einnahme/Verabreichung von Thomaprodol Kapseln muss die Therapie abgebrochen werden. Das medizinische Fachpersonal muss symptombezogen die medizinisch erforderlichen Maßnahmen einleiten. Ibuprofen, der Wirkstoff von Thomaprodol Kapseln, kann die Thrombozytenfunktion (Thrombozytenaggregation) vorübergehend hemmen. Deshalb sollten Patienten mit Gerinnungsstörung sorgfältig beobachtet werden. Bei einer Langzeitbehandlung mit Ibuprofen müssen die Leber- und Nierenwerte sowie das Blutbild regelmäßig überprüft werden. Die längere Anwendung jeglicher Art von Analgetika gegen Kopfschmerzen kann diese verschlimmern. Ist dies der Fall oder wird dies vermutet, sollte medizinischer Rat eingeholt und die 35 Behandlung abgebrochen werden. Die Diagnose von Kopfschmerzen durch übermäßigen Medikamentengebrauch kann bei Patienten vermutet werden, die an häufigen oder täglichen Kopfschmerzen leiden, obwohl (oder gerade weil) sie regelmäßig Arzneimittel gegen Kopfschmerzen einnehmen. Allgemein kann die gewohnheitsmäßige Einnahme von Analgetika, insbesondere in Kombination mit mehreren schmerzstillenden Wirkstoffen, zu einer permanenten Schädigung der Nieren mit dem Risiko einer Niereninsuffizienz (Analgetikanephropathie) führen. Dieses Risiko kann sich bei einem mit körperlicher Belastung einhergehenden Salzverlust und bei Dehydratation erhöhen und sollte daher vermieden werden. Bei Anwendung von NSAR kann der gleichzeitige Konsum von Alkohol Nebenwirkungen, insbesondere solche, die den Gastrointestinaltrakt oder das zentrale Nervensystem betreffen, verstärken. NSAR können die Symptome einer Infektion und von Fieber maskieren. Kinder und Jugendliche Bei dehydrierten Jugendlichen besteht das Risiko einer Nierenfunktionsstörung. Thomaprodol enthält Sorbitol. Patienten mit seltener hereditärer Fructose-Intoleranz sollten dieses Medikament nicht einnehmen. 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Bei gleichzeitiger Anwendung von Ibuprofen mit: Mögliche Wirkungen: Anderen NSAR, einschließlich Salicylaten: Die gleichzeitige Gabe mehrerer NSAR kann das Risiko gastrointestinaler Ulcera und Blutungen aufgrund eines synergistischen Effekts erhöhen. Die gleichzeitige Anwendung von Ibuprofen mit anderen NSAR sollte deshalb vermieden werden (siehe Abschnitt 4.4). Digoxin: Die gleichzeitige Anwendung von Thomaprodol mit Digoxinpräparaten kann den Serumspiegel von Digoxin erhöhen. Eine Überprüfung des Serum-DigoxinSpiegels ist bei korrekter Anwendung (maximal über eine Dauer von 4 Tagen) normalerweise nicht erforderlich. Kortikosteroiden: Kortikosteroide können das Risiko von Nebenwirkungen, insbesondere des Gastrointestinaltrakts (gastrointestinale Ulzerationen oder Blutungen) erhöhen (siehe Abschnitt 4.4). Thrombozytenaggregationshemmern: Erhöhtes Risiko gastrointestinaler Blutungen (siehe Abschnitt 4.4). Acetylsalicylsäure: Die gleichzeitige Verabreichung von Ibuprofen und Acetylsalicylsäure wird im Allgemeinen aufgrund des Potenzials für vermehrte Nebenwirkungen nicht 36 empfohlen. Experimentelle Daten weisen darauf hin, dass Ibuprofen die Wirkung niedrig dosierter Acetylsalicylsäure auf die Thrombozytenaggregation kompetitiv hemmen kann, wenn beide gleichzeitig verabreicht werden. Obwohl Unsicherheiten in Bezug auf die Extrapolation dieser Daten auf die klinische Situation bestehen, kann die Möglichkeit, dass eine regelmäßige Langzeitanwendung von Ibuprofen die kardioprotektive Wirkung niedrig dosierter Acetylsalicylsäure reduzieren kann, nicht ausgeschlossen werden. Bei gelegentlicher Anwendung von Ibuprofen ist eine klinisch relevante Wechselwirkung nicht wahrscheinlich (siehe Abschnitt 5.1). Antikoagulanzien: NSAR können die Wirkung von Antikoagulanzien wie Warfarin verstärken (siehe Abschnitt 4.4). Phenytoin: Die gleichzeitige Anwendung von Thomaprodol mit Phenytoinpräparaten kann den Serumspiegel von Phenytoin erhöhen. Eine Überprüfung des Serum-PhenytoinSpiegels ist bei korrekter Anwendung (maximal über eine Dauer von 4 Tagen) normalerweise nicht erforderlich. Selektiven SerotoninWiederaufnahmehemmern (SSRI): Erhöhtes Risiko gastrointestinaler Blutungen (siehe Abschnitt 4.4). Lithium: Die gleichzeitige Anwendung von Thomaprodol mit Lithiumpräparaten kann den Serumspiegel von Lithium erhöhen. Eine Überprüfung des Serum-LithiumSpiegels ist bei korrekter Anwendung (maximal über eine Dauer von 4 Tagen) nicht erforderlich. Probenecid und Sulfinpyrazon: Arzneimittel, die Probenecid oder Sulfinpyrazon enthalten, können die Ausscheidung von Ibuprofen verzögern. Diuretika, ACE-Inhibitoren, Betarezeptorenblockern und Angiotensin-IIAntagonisten: NSAR können die Wirkung von Diuretika und anderen Antihypertensiva mindern. Bei einigen Patienten mit eingeschränkter Nierenfunktion (z. B. dehydratisierte Patienten oder ältere Patienten mit eingeschränkter Nierenfunktion) kann die gleichzeitige Verabreichung von ACEInhibitoren, Betarezeptorenblockern oder Angiotensin-II-Antagonisten und Wirkstoffen, die die Zyklooxygenase hemmen, zu einer weiteren Verschlechterung der Nierenfunktion führen, einschließlich einer möglichen 37 akuten Niereninsuffizienz, die normalerweise reversibel ist. Deshalb sollte diese Kombination, insbesondere bei älteren Patienten, mit Vorsicht angewendet werden. Auf einen angemessenen Wasserhaushalt der Patienten ist zu achten; die Nierenfunktion sollte nach Beginn einer Begleittherapie sowie anschließend in regelmäßigen Abständen beobachtet werden. Kaliumsparenden Diuretika: Die gleichzeitige Gabe von Thomaprodol und kaliumsparenden Diuretika kann zu einer Hyperkalämie führen. Methotrexat: Die Gabe von Thomaprodol innerhalb von 24 Stunden vor oder nach Verabreichung von Methotrexat kann zu einer erhöhten Methotrexatkonzentration führen und dessen toxische Wirkung verstärken. Ciclosporin: Das Risiko einer Nierenschädigung aufgrund von Ciclosporin steigt bei gleichzeitiger Gabe bestimmter nichtsteroidaler Antirheumatika. Diese Wirkung kann auch bei einer Kombination von Ciclosporin und Ibuprofen nicht ausgeschlossen werden. Tacrolimus: Das Risiko einer Nephrotoxizität ist erhöht, wenn beide Arzneimittel gleichzeitig verabreicht werden. Zidovudin: Es gibt Hinweise auf ein erhöhtes Risiko von Hämarthrosen und Hämatomen bei HIV-positiven Patienten mit Hämophilie, die gleichzeitig mit Zidovudin und Ibuprofen behandelt werden. Sulfonylharnstoffen: Klinische Untersuchungen zeigten Wechselwirkungen zwischen nichtsteroidalen Antirheumatika und Antidiabetika (Sulfonylharnstoffen). Wenngleich bis heute nicht von Wechselwirkungen zwischen Ibuprofen und Sulfonylharnstoffen berichtet wurde, wird bei gleichzeitiger Einnahme als Vorsichtsmaßnahme eine Überprüfung des Blutzuckerspiegels empfohlen. Chinolon-Antibiotika: Daten aus tierexperimentellen Studien weisen darauf hin, dass NSAR das Risiko von Konvulsionen in Zusammenhang mit Chinolon-Antibiotika erhöhen können. Bei Patienten, die NSAR und Chinolone einnehmen, ist möglicherweise das Risiko, Konvulsionen zu entwickeln, erhöht. 38 CYP2C9-Hemmern: Die gleichzeitige Anwendung von Ibuprofen mit CYP2C9-Hemmern kann die Exposition gegenüber Ibuprofen (CYP2C9Substrat) erhöhen. In einer Studie mit Voriconazol und Fluconazol (CYP2C9Hemmer) wurde eine erhöhte S(+) – Ibuprofen Exposition um ungefähr 80 bis 100 % nachgewiesen. Bei gleichzeitiger Gabe von potenten CYP2C9-Hemmern sollte eine Reduzierung der Ibuprofendosis in Erwägung gezogen werden, insbesondere, wenn hochdosiertes Ibuprofen mit Voriconazol oder Fluconazol verabreicht wird. Mifepriston Nach der Anwendung von Mifepriston sollte für 8 – 12 Tage auf die Einnahme von NSAR verzichtet werden, da NSAR die Wirkung von Mifepriston abschwächen können. 4.6 Fertilität, Schwangerschaft und Stillzeit Schwangerschaft Die Hemmung der Prostaglandinsynthese kann schädliche Auswirkungen auf die Schwangerschaft und/oder die embryonale/fötale Entwicklung haben. Daten aus epidemiologischen Studien deuten auf ein erhöhtes Risiko für Fehlgeburten sowie kardiale Missbildungen und Gastroschisis nach der Anwendung eines Prostaglandinsynthese-Hemmers in der Frühschwangerschaft hin. Das absolute Risiko für eine kardiovaskuläre Missbildung erhöhte sich von weniger als 1 % auf annähernd 1,5 %. Es wird angenommen, dass das Risiko mit der Dosis und der Dauer der Therapie steigt. Bei Tieren wurde nachgewiesen, dass die Gabe von Prostaglandinsynthese-Hemmern zu einem erhöhten prä- und postimplantären Verlust und zu einer erhöhten embryofötalen Letalität führt. Zudem wurde bei Tieren, denen während der Phase der Organogenese ein Prostaglandinsynthese-Hemmer verabreicht wurde, von einer erhöhten Inzidenz verschiedener Missbildungen, einschließlich kardiovaskulärer Missbildungen, berichtet. Ibuprofen darf während des ersten und zweiten Trimenons nicht angewendet werden, es sei denn, dies ist eindeutig erforderlich. Wird Ibuprofen bei Frauen angewendet, die vorhaben, schwanger zu werden, oder die sich im ersten oder zweiten Trimenon befinden, sollte die Dosis so gering und die Dauer der Behandlung so kurz wie möglich gehalten werden. Während des dritten Trimenons können alle Prostaglandinsynthesehemmer folgende Auswirkungen haben: auf den Fötus: – kardiopulmonale Toxizität (mit vorzeitigem Verschluss des Ductus arteriosus Botalli und pulmonalem Bluthochdruck); – renale Dysfunktion, die bis zu Nierenversagen mit Oligohydramnion fortschreiten kann; auf Mutter und Neugeborenes am Ende der Schwangerschaft: – mögliche Verlängerung der Blutungszeit, eine aggregationshemmende Wirkung, die schon bei sehr geringen Dosen auftreten kann; – Hemmung der Uteruskontraktionen und in weiterer Folge verzögerte oder verlängerte Wehen. Im letzten Trimenon ist Ibuprofen daher kontraindiziert. 39 Stillzeit Ibuprofen und seine Metaboliten können in geringen Konzentrationen in die Muttermilch übergehen. Bis heute sind keine schädigenden Auswirkungen auf Säuglinge bekannt. Deshalb ist bei einer kurzzeitigen Behandlung mit der empfohlenen Dosis bei Schmerzen und Fieber eine Unterbrechung des Stillens in der Regel nicht erforderlich. Fertilität Es gibt gewisse Hinweise darauf, dass Arzneimittel, die die Zyklooxygenase/Prostaglandinsynthese hemmen, die weibliche Fertilität beeinträchtigen können, da sie die Ovulation beeinflussen. Dieser Effekt ist nach Absetzen der Behandlung reversibel. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Da bei der Anwendung von Thomaprodol in höheren Dosen zentralnervöse Nebenwirkungen wie Müdigkeit oder Schwindel möglich sind, können Reaktionsfähigkeit sowie Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen in Einzelfällen beeinträchtigt sein. Dies wird durch den Konsum von Alkohol verstärkt. 4.8 Nebenwirkungen Die Liste der folgenden Nebenwirkungen enthält alle Nebenwirkungen, die bei der Behandlung mit Ibuprofen bekannt wurden, einschließlich der Nebenwirkungen, die bei einer hochdosierten Langzeitbehandlung von Patienten mit Rheuma beobachtet wurden. Die angegebenen Häufigkeiten, die über sehr selten berichtete Nebenwirkungen hinausgehen, beziehen sich auf die kurzzeitige Anwendung einer Tagesdosis von bis zu maximal 1.200 mg Ibuprofen in oralen Darreichungsformen und maximal 1.800 mg als Zäpfchen. Bei den folgenden Nebenwirkungen muss beachtet werden, dass diese überwiegend dosisabhängig sind und interindividuell unterschiedlich. Die am häufigsten beobachteten Nebenwirkungen betreffen den Gastrointestinaltrakt. Ulcus pepticum, Perforationen oder gastrointestinale Blutungen, in manchen Fällen mit Todesfolge, können insbesondere bei älteren Patienten auftreten (siehe Abschnitt 4.4). Übelkeit, Erbrechen, Diarrhoe, Flatulenz, Konstipation, Dyspepsie, abdominale Schmerzen, Meläna, Hämatemesis, Stomatitis ulcerosa, Exazerbation der Colitis ulcerosa und von Morbus Crohn (siehe Abschnitt 4.4) wurden nach Anwendung berichtet. In selteneren Fällen wurde eine Gastritis beobachtet. Insbesondere das Risiko einer gastrointestinalen Blutung ist von der Dosis und der Dauer der Behandlung abhängig. In Zusammenhang mit einer Behandlung mit NSAR wurde von Ödemen, Hypertonie und Herzinsuffizienz berichtet. Klinische Studien weisen darauf hin, dass die Anwendung von Ibuprofen, insbesondere in hohen Dosen (2.400 mg / Tag), möglicherweise mit einem geringfügig erhöhten Risiko arterieller thrombotischer Ereignisse (z. B. Myokardinfarkt oder Schlaganfall) assoziiert ist (siehe Abschnitt 4.4). Die Patienten sollten darauf hingewiesen werden, dass sie die Einnahme von Thomaprodol sofort abbrechen und einen Arzt aufsuchen, sobald schwerwiegende Nebenwirkungen auftreten. Sehr häufig (≥ 1/10) Häufig (≥ 1/100 bis < 1/10) Gelegentlich (≥ 1/1.000 bis < 1/100) Selten (≥ 1/10.000 bis < 1/1.000) Sehr selten (< 1/10.000) Unbekannt (Häufigkeit auf Grundlage der verfügbaren 310 Daten nicht abschätzbar) Infektionen und parasitäre Erkrankungen Sehr selten Beschrieben wurde die Exazerbation von infektionsbezogenen Entzündungen (z. B. Entwicklung einer nekrotisierenden Fasziitis) in zeitlichem Zusammenhang mit der Anwendung eines nichtsteroidalen Antirheumatikums. Dies steht möglicherweise in Zusammenhang mit dem Wirkmechanismus nichtsteroidaler Antirheumatika. Bei der Anwendung von Ibuprofen wurden Symptome einer aseptischen Meningitis wie Nackensteifigkeit, Kopfschmerzen, Übelkeit, Erbrechen, Fieber oder Bewusstseinstrübung beobachtet. Patienten mit Autoimmunerkrankungen (Mischkollagenosen) scheinen prädisponiert zu sein. Erkrankungen des Blutes und des Lymphsystems Sehr selten Blutbildungsstörungen (Anämie, Leukopenie, Thrombozytopenie, Panzytopenie, Agranulozytose). Zu den ersten Anzeichen zählen Fieber, Halsschmerzen, oberflächliche Wunden im Mundraum, grippeähnliche Beschwerden, schwere Abgeschlagenheit, Nasenbluten und Hautblutungen. Bei einer Langzeitbehandlung sollte das Blutbild regelmäßig untersucht werden. Erkrankungen des Immunsystems Gelegentlich Überempfindlichkeitsreaktionen einhergehend mit Hautausschlägen und Juckreiz sowie Asthmaanfällen (möglicherweise mit Blutdruckabfall) Sehr selten Schwerwiegende allgemeine Überempfindlichkeitsreaktionen. Sie können sich äußern als Gesichtsödem, Schwellungen der Zunge, Schwellungen der inneren Kehlkopfmuskulatur mit Konstriktion der Atemwege, Atemnot, Herzrasen, Blutdruckabfall bis hin zu einem lebensbedrohlichen Schock. Tritt eines dieser Symptome auf, was bereits bei der ersten Anwendung vorkommen kann, ist sofortige ärztliche Hilfe erforderlich. Psychiatrische Erkrankungen Sehr selten Psychotische Reaktionen, Depression Erkrankungen des Nervensystems Gelegentlich Störungen des zentralen Nervensystems wie Kopfschmerzen, Schwindel, Schlaflosigkeit, Erregung, Reizbarkeit oder Müdigkeit 311 Augenerkrankungen Gelegentlich Sehstörungen Erkrankungen des Ohrs und des Labyrinths Selten Tinnitus Herzerkrankungen Sehr selten Palpitationen, Herzinsuffizienz, Myokardinfarkt Gefäßerkrankungen Sehr selten Arterielle Hypertonie, Vaskulitis Erkrankungen des Gastrointestinaltrakts Häufig Gastrointestinale Beschwerden wie Pyrosis, abdominale Schmerzen, Übelkeit, Dyspepsie, Erbrechen, Flatulenz, Diarrhoe, Konstipation und leichter gastrointestinaler Blutverlust, die in Ausnahmefällen eine Anämie verursachen können. Gelegentlich Gastrointestinale Ulzera, möglicherweise einhergehend mit Blutungen und Perforationen; Stomatitis ulcerosa, Exazerbation einer Colitis und Morbus Crohn (siehe Abschnitt 4.4), Gastritis Leber- und Gallenerkrankungen Sehr selten Ösophagitis, Pankreatitis, Bildung intestinaler diaphragmaartiger Strikturen. Der Patient muss das Arzneimittel absetzen und umgehend einen Arzt aufsuchen, sobald starke Schmerzen im oberen Abdomen, Melaena oder Hämatemesis auftreten. Sehr selten Leberfunktionsstörungen, Leberschäden, insbesondere bei Langzeitbehandlung, Leberinsuffizienz, akute Hepatitis Erkrankungen der Gelegentlich Diverse Hautausschläge Haut und des Unterhautzellgewebes Sehr selten Bullöse Hautreaktionen, einschließlich Stevens-Johnson-Syndrom und toxischer epidermaler Nekrolyse (Lyell’s Syndrom), Alopezie. In Ausnahmefällen können während einer Infektion mit Varizellen schwere Hautinfektionen und Komplikationen mit dem Weichgewebe auftreten (siehe auch „Infektionen und parasitäre Erkrankungen“). Erkrankungen der Niere und Harnwege 312 Selten Schädigung des Nierengewebes (papilläre Nekrose) und eine erhöhte Harnsäurekonzentration im Blut können in seltenen Fällen auftreten. Sehr selten Bildung von Ödemen, insbesondere bei Patienten mit arterieller Hypertonie oder Niereninsuffizienz, nephrotisches Syndrom und interstitielle Nephritis, die mit einer akuten Niereninsuffizienz einhergehen können. Die Nierenfunktion sollte deshalb regelmäßig untersucht werden. Gegebenenfalls sollten Patienten entsprechend darauf hingewiesen werden, dass sie die Einnahme von Thomaprodol sofort abbrechen und einen Arzt aufsuchen, sobald eine der folgenden Nebenwirkungen auftritt: starke gastrointestinale Beschwerden, Pyrosis oder abdominale Schmerzen Hämatemesis Meläna oder Blut im Harn Hautreaktionen wie juckende Ausschläge Atembeschwerden und/oder Ödeme des Gesichts oder des Larynx Müdigkeit, einhergehend mit Appetitverlust Halsschmerzen, einhergehend mit Aphthenbildung, Müdigkeit und Fieber schwere Epistaxis und Hautblutungen ungewöhnliche Müdigkeit, einhergehend mit reduzierter Harnausscheidung Ödeme der Füße und Beine Schmerzen im Brustkorb Sehstörungen Meldung des Verdachts auf Nebenwirkungen Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem anzuzeigen: Bundesamt für Sicherheit im Gesundheitswesen Traisengasse 5 1200 WIEN ÖSTERREICH Fax: + 43 (0) 50 555 36207 Website: http://www.basg.gv.at/ 4.9 Überdosierung Symptome einer Überdosierung Zu den Symptomen einer Überdosierung zählen Symptome des zentralen Nervensystems wie Kopfschmerzen, Schwindel, Benommenheit und Bewusstlosigkeit (ebenso myoklonische Anfälle bei Kindern), abdominale Schmerzen, Übelkeit, Erbrechen, gastrointestinale Blutungen sowie Funktionsstörungen der Leber und der Nieren; Hypotonie, Atemnot und Zyanose. Therapeutische Maßnahmen bei Überdosierung Es gibt kein spezifisches Gegenmittel. Wird der Patient innerhalb 1 Stunde nach Einnahme einer möglicherweise toxischen Dosis vorstellig, kann eine orale Verabreichung von Aktivkohle in Betracht gezogen werden. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1 Pharmakodynamische Eigenschaften 313 Pharmakotherapeutische Gruppe: ATC-Code: Antiphlogistika und Antirheumatika, nichtsteroidale Arzneimittel, Propionsäure-Derivate M01AE01 Ibuprofen ist ein nichtsteroidales Antirheumatikum (NSAR), das sich in den üblichen tierexperimentellen Entzündungsmodellen über die Prostaglandinsynthesehemmung als wirksam erwies. Beim Menschen reduziert Ibuprofen entzündlich bedingte Schmerzen, Schwellungen und Fieber. Des Weiteren hemmt Ibuprofen reversibel die ADP- und die kollageninduzierte Thrombozytenaggregation. Experimentelle Daten weisen darauf hin, dass Ibuprofen die Wirkung niedrig dosierter Acetylsalicylsäure auf die Thrombozytenaggregation kompetitiv hemmen kann, wenn beide gleichzeitig verabreicht werden. Einige pharmakodynamische Studien zeigten, dass es bei Einnahme von Einzeldosen von 400 mg Ibuprofen innerhalb von 8 Stunden vor oder innerhalb von 30 Minuten nach der Verabreichung von Acetylsalicylsäure-Dosen mit schneller Freisetzung (81 mg) zu einer verminderten Wirkung der Acetylsalicylsäure auf die Bildung von Thromboxan oder die Thrombozytenaggregation kam. Obwohl Unsicherheiten in Bezug auf die Extrapolation dieser Daten auf die klinische Situation bestehen, kann die Möglichkeit, dass eine regelmäßige Langzeitanwendung von Ibuprofen die kardioprotektive Wirkung niedrig dosierter Acetylsalicylsäure reduzieren kann, nicht ausgeschlossen werden. Bei gelegentlicher Anwendung von Ibuprofen ist eine klinisch relevante Wechselwirkung nicht wahrscheinlich (siehe Abschnitt 4.5). 5.2 Pharmakokinetische Eigenschaften Nach oraler Gabe wird Ibuprofen im Magen teilweise und anschließend im Dünndarm vollständig resorbiert. Im Anschluss an die hepatische Metabolisierung (Hydroxylierung, Carboxylierung) werden die pharmakologisch inaktiven Metaboliten zum Großteil über die Nieren (90 %), aber auch über die Galle eliminiert. Die Eliminationshalbwertszeit liegt bei gesunden Menschen und bei Patienten mit Leber- und Nierenerkrankungen bei 1,8-3,5 Stunden, die Plasmaproteinbindung beträgt etwa 99 %. Die Peak-Plasma-Konzentration wird nach oraler Gabe in einer normal freisetzenden Darreichungsform (Tablette) nach 1-2 Stunden erreicht. Nach oraler Gabe von Thomaprodol Weichkapseln wird Ibuprofen – im Vergleich zu Standardtabletten – jedoch schneller im Gastrointestinaltrakt resorbiert. In einer pharmakokinetischen Studie betrug die Zeit bis zum Erreichen der Peak-Plasma-Konzentration (mediane Tmax) im Nüchternzustand für Ibuprofensäure Tabletten 75 Minuten gegenüber 45 Minuten für Thomaprodol Weichkapseln. 5.3 Präklinische Daten zur Sicherheit Die subchronische und chronische Toxizität von Ibuprofen zeigte sich in tierexperimentellen Studien vor allem in Form von Läsionen und Ulzerationen im Gastrointestinaltrakt. In-vitro- und In-vivoStudien ergaben keine klinisch relevanten Hinweise auf ein mutagenes Potenzial von Ibuprofen. In Studien an Ratten und Mäusen wurden keine Hinweise auf eine kanzerogene Wirkung von Ibuprofen gefunden. Ibuprofen führte zu einer Hemmung der Ovulation beim Kaninchen sowie zu Störungen der Implantation bei verschiedenen Tierspezies (Kaninchen, Ratte, Maus). Experimentelle Studien zeigten, dass Ibuprofen die Plazenta passiert. Nach Gabe von maternotoxischen Dosen kam es bei der Nachkommenschaft von Ratten zu einer erhöhten Inzidenz von Missbildungen (ventrikuläre Septumdefekte). 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Inhalt der Kapseln: 314 Macrogol 600 Kaliumhydroxid Destilliertes Wasser Kapselhülle: Gelatine Sorbitol flüssig Destilliertes Wasser Druckfarbe Bestandteile von Opacode WB Black NS-78-17821: Eisenoxid schwarz (E172) Propylenglykol (E1520) Hypromellose 6 cP 6.2 Inkompatibilitäten Nicht zutreffend. 6.3 Dauer der Haltbarkeit 3 Jahre 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich. 6.5 Art und Inhalt des Behältnisses Triplex-Blisterpackung (PVC/PE/PVDC) und Aluminiumfolie Packungsgrößen: 6 Kapseln 12 Kapseln 20 Kapseln Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen. 7. INHABER DER ZULASSUNG sanofi-aventis GmbH Leonard-Bernstein-Straße 10 1220 Wien Österreich 8. ZULASSUNGSNUMMER Z. Nr.: 1-30974 315 9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG Datum der Erteilung der Zulassung: 5. Jänner 2012 Datum der letzten Verlängerung der Zulassung: 07. Oktober 2016 10. STAND DER INFORMATION Juni 2017 VERSCHREIBUNGSPFLICHT/APOTHEKENPFLICHT Rezeptfrei, apothekenpflichtig 316