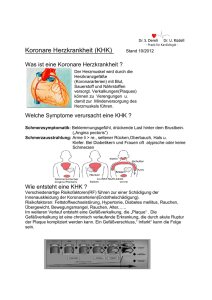
Stellenwert der nicht-invasiven Diagnostik der koronaren
Werbung

Ruhr Universität Bochum Prof. Dr. med. D. Uhlenbrock Dienstort: Medizinisches Versorgungszentrum (MVZ), St. Josefs Hospital Dortmund Radiologie, Strahlentherapie und Nuklearmedizin Stellenwert der nicht-invasiven Diagnostik der koronaren Herzkrankheit am Beispiel der Adenosin-Stress-MRT-Untersuchung Inaugural-Dissertation zur Erlangung des Doktorgrades der Medizin einer Hohen Medizinischen Fakultät der Ruhr-Universität Bochum vorgelegt von Tobias Enno Kostka aus Dortmund 2014 Dekan: Prof. Dr. med. Klaus Überla Referent: Prof. Dr. med. Detlev Uhlenbrock Korreferent: Prof. Dr. med. Wolfgang Burchert Tag der Mündlichen Prüfung: 13.11.2014 Abstract Tobias Enno Kostka Stellenwert der nicht-invasiven Diagnostik der koronaren Herzkrankheit am Beispiel der Adenosin-Stress-MRT-Untersuchung Problem: Aufgrund der hohen Prävalenz stellt die differenzierte Diagnostik der koronaren Herzkrankheit eine Herausforderung für die medizinische Bildgebung dar. Den Ausschluss einer stenosierenden Herzerkrankung gewährleistet nur die Koronarangiographie. Dank technischer Fortschritte können heute auch nicht-invasive Verfahren eine hohe Sensitivität und Spezifität vorweisen. Diese Arbeit hat sich zum Ziel gesetzt, die Wertigkeit der Adenosin-Stress-MRT-Untersuchung anhand des Goldstandards Koronarangiographie in einem ambulanten Setting zu überprüfen und die Möglichkeiten der verschiedenen bildgebenden Verfahren zu diskutieren. Methode: Dieser Arbeit liegt die retrospektive Analyse der Daten von 54 Patientinnen/Patienten zugrunde, bei denen in zeitlicher Nähe (<180 Tage) bei verdächtigter oder bekannter koronarer Herzkrankheit sowohl Stress-MRT als auch Koronarangiographie durchgeführt wurden. Mit Hilfe des 17-Segment-Modells der American Heart Association wurde die kardiale Stress-MRT territorienbasiert auf ihre Sensitivität, Spezifität sowie positiven und negativen prädiktiven Wert überprüft. Ergebnis: Beruhend auf einer visuellen Auswertung konnte nach Analyse von 160 Versorgungsbezirken die Wertigkeit der Stress-MRT mit einer Sensitivität von 91,1% und einer Spezifität von 84,6% beziffert werden. Der positive prädiktive Wert lag bei 76,1%, der negative prädiktive Wert bei 94,6%. Diskussion: Die Adenosin-Stress-MRT-Untersuchung kann in Ihrer Wertigkeit das große Potential nicht-invasiver Bildgebungen veranschaulichen. Angesichts des hohen negativen prädiktiven Wertes wird bei unauffälliger Perfusionsstudie mit hoher Wahrscheinlichkeit der Ausschluss einer stenosierenden KHK erbracht, während eine aufgezeigte Durchblutungsminderung die Relevanz einer Stenose gut widerzuspiegeln vermag. Gerade bei einer niedrigen bis mittleren Vortestwahrscheinlichkeit für das Vorliegen einer KHK könnten nicht-invasive Bildgebungen als patientenschonendes diagnostisches Verfahren in Zukunft einen hohen Stellenwert besitzen. Meinen lieben Eltern INHALTSVERZEICHNIS I EINLEITUNG......................................................................................................................... 7 1.1 BEDEUTUNG DER KORONAREN HERZKRANKHEIT ............................................................ 7 1.2 PATHOPHYSIOLOGIE DER KHK ............................................................................................ 8 1.3 STUFENDIAGNOSTIK DER KHK ............................................................................................ 9 1.4 INVASIVE VERFAHREN .......................................................................................................... 11 1.4.1 KORONARANGIOGRAPHIE ............................................................................................................. 11 1.4.2 FRAKTIONELLE FLUSSRESERVE .................................................................................................... 11 1.4.3 INTRAVASKULÄRER ULTRASCHALL............................................................................................... 12 1.5 NICHT-INVASIVE VERFAHREN ............................................................................................. 12 1.5.1 SPECT ................................................................................................................................................ 12 1.5.2 PET ..................................................................................................................................................... 13 1.5.3 BELASTUNGS-ELEKTROKARDIOGRAPHIE ................................................................................... 13 1.5.4 STRESS-ECHOKARDIOGRAPHIE ..................................................................................................... 14 1.5.5 COMPUTERTOMOGRAPHIE UND KORONARER CALCIUM-SCORE............................................ 14 1.5.6 MAGNETRESONANZTOMOGRAPHIE ............................................................................................. 15 II ZIELSETZUNG .................................................................................................................... 16 III MATERIAL UND METHODEN ..................................................................................... 17 3.1 PATIENTEN ............................................................................................................................. 17 3.2 KARDIO-MRT ........................................................................................................................ 18 3.2.1 PHYSIKALISCHE GRUNDLAGEN DER MAGNETRESONANZTOMOGRAPHIE .......................... 18 3.2.2 BESONDERHEITEN DER KARDIO-MRT ....................................................................................... 21 3.2.3 UNTERSUCHUNGSABLAUF / PROTOKOLL ................................................................................... 23 3.2.4 AUSWERTUNG ................................................................................................................................... 24 3.3 KORONARANGIOGRAPHIE ................................................................................................... 27 3.3.1 VORBEREITUNG, DURCHFÜHRUNG .............................................................................................. 27 3.3.2 QUALITATIVE BEURTEILUNG VON STENOSEN .......................................................................... 28 3.4 VERGLEICH BEIDER UNTERSUCHUNGSVERFAHREN ........................................................ 28 3.5 STATISTISCHE METHODEN ................................................................................................... 31 IV ERGEBNISSE ....................................................................................................................... 32 4.1 KLINISCHE CHARAKTERISIERUNG DER PATIENTEN ........................................................ 32 4.2 ERGEBNISSE DER KORONARANGIOGRAPHISCHEN UNTERSUCHUNGEN ...................... 32 4.3 ERGEBNISSE UND WERTIGKEIT DER ADENOSIN-STRESS-MRT..................................... 33 1 4.3.1 AUSWERTUNG DER LAD-VERSORGUNGSBEZIRKE ................................................................... 34 4.3.2 AUSWERTUNG DER LCX VERSORGUNGSBEZIRKE .................................................................... 36 4.3.3 AUSWERTUNG DER RCA-VERSORGUNGSBEZIRKE ................................................................... 39 4.3.4 DIAGNOSTISCHE WERTIGKEIT DER ADENOSIN-STRESS-MRT: GESAMTWERTE ................ 41 4.3.5 ZUSATZAUSWERTUNG: KORONARSTENOSEN ≥70% ALS HÄMODYNAMISCH RELEVANT EINGESTUFT ................................................................................................................. 41 4.4 LATE-ENHANCEMENT .......................................................................................................... 42 V DISKUSSION ......................................................................................................................... 43 5.1 EINORDNUNG DER ERGEBNISSE ......................................................................................... 43 5.2 EINSCHRÄNKUNGEN IM HINBLICK AUF DIE VERGLEICHBARKEIT ................................ 45 5.3 VOR- UND NACHTEILE DER STRESS-MRT-UNTERSUCHUNG UND WEITERER NICHT-INVASIVER TECHNIKEN ........................................................................................... 48 5.4 BESONDERHEITEN EINER AMBULANTEN STUDIE ............................................................ 53 5.5 AUSBLICK ................................................................................................................................ 55 VI ZUSAMMENFASSUNG ..................................................................................................... 58 VII LITERATURVERZEICHNIS .......................................................................................... 60 ANHANG .......................................................................................................................................................... 75 2 VERZEICHNIS DER ABKÜRZUNGEN AHA American Heart Association BMI body mass index BMS bare-metal stent CRP C-reaktives Protein CT Computertomographie DES drug-eluting stent DFP Dosis-Flächen-Produkt DNA deoxyribonucleic acid EKG Elektrokardiogramm FFR fraktionelle Flussreserve FID free induction decay GFR glomeruläre Filtrationsrate KHK koronare Herzkrankheit KI Konfidenzintervall LAD left anterior descending LCX left circumflex coronary artery MACCE major adverse cardiac and cerebrovascular events MACE major adverse cardiac events MRT Magnetresonanztomographie pAVK periphere arterielle Verschlusskrankheit PET positron emission tomography 3 PTCA percutaneous transluminal coronary angioplasty TE time of echo TR time of repetition RCA right coronary artery SPECT single photon emission computer tomography 4 VERZEICHNIS DER ABBILDUNGEN ABBILDUNG 1: ANREGUNG ......................................................................................................................... 19 ABBILDUNG 2: SEGMENTEINTEILUNG DES HERZENS ........................................................................... 25 ABBILDUNG 3: ZUORDNUNG DER SEGMENTE ZU DEN VERSORGUNGSBEZIRKEN DER KORONARARTERIEN LAD, RCA UND LCX .................................................................................... 29 ABBILDUNG 4: ERGEBNISSE: ÜBERSICHT ÜBER DIE GESAMTZAHL DER AUSGEWERTETEN VERSORGUNGSBEZIRKE UND DEN VERANTWORTLICHEN KORONARGEFÄßEN ..................... 34 ABBILDUNG 5: ERGEBNISSE: LAD GESAMT (53 PATIENTEN) .............................................................. 35 ABBILDUNG 6: ERGEBNISSE: LAD OHNE VORHERIGE INTERVENTION (43 PATIENTEN) .............. 35 ABBILDUNG 7: ERGEBNISSE: LAD BEI Z.N. STENT-IMPLANTATION (10 PATIENTEN) .................... 36 ABBILDUNG 8: ERGEBNISSE: LCX GESAMT (53 PATIENTEN) .............................................................. 37 ABBILDUNG 9: ERGEBNISSE: LCX OHNE VORHERIGE INTERVENTION (48 PATIENTEN) .............. 38 ABBILDUNG 10: ERGEBNISSE: LCX BEI Z.N. STENT-IMPLANTATION (5 PATIENTEN) .................... 38 ABBILDUNG 11: ERGEBNISSE: RCA GESAMT (54 PATIENTEN) ............................................................ 39 ABBILDUNG 12: ERGEBNISSE: RCA OHNE VORHERIGE INTERVENTION (47 PATIENTEN) ............ 40 ABBILDUNG 13: ERGEBNISSE: RCA BEI Z.N. STENT-IMPLANTATION (7 PATIENTEN) .................... 40 ABBILDUNG 14: GESAMTWERTE FÜR SENSITIVITÄT, SPEZIFITÄT, POSITIVEN PRÄDIKTIVEN WERT UND NEGATIVEN PRÄDIKTIVEN WERT (160 AUSGEWERTETE VERSORGUNGSBEZIRKE) .................................................................................................................... 41 ABBILDUNG 15: DIAGNOSTISCHE WERTIGKEIT IM VERGLEICH, BASIEREND AUF HAUPTAUSWERTUNG UND NEBENAUSWERTUNG ......................................................................... 42 ABBILDUNG A 1: PERFUSIONSSTUDIE (1/4)............................................................................................. 75 ABBILDUNG A 2: PERFUSIONSSTUDIE (2/4)............................................................................................ . 75 ABBILDUNG A 3: PERFUSIONSSTUDIE (3/4)............................................................................................. 75 ABBILDUNG A 4: PERFUSIONSSTUDIE (4/4) ............................................................................................. 75 ABBILDUNG A 5: PERFUSIONSSTUDIE II (1/4)......................................................................................... 76 ABBILDUNG A 6: PERFUSIONSSTUDIE II (2/4)......................................................................................... 76 ABBILDUNG A 7: PERFUSIONSSTUDIE II (3/4)......................................................................................... 76 ABBILDUNG A 8: PERFUSIONSSTUDIE II (4/4) ......................................................................................... 76 ABBILDUNG A 9: RUHE, ENDDIASTOLISCH (1/2).................................................................................... 76 ABBILDUNG A 10: RUHE, ENDSYSTOLISCH (2/2) .................................................................................... 76 5 VERZEICHNIS DER TABELLEN TABELLE 1 - PATIENTENCHARAKTERISIERUNG ...................................................................................... 17 TABELLE 2 - KLINISCHE PATIENTENCHARAKTERISIERUNG ................................................................ 32 TABELLE 3 - ERGEBNISSE KORONARANGIOGRAPHIE ........................................................................... 33 6 I 1.1 Einleitung Bedeutung der koronaren Herzkrankheit Die koronare Herzerkrankung (KHK) ist trotz vieler Maßnahmen zur Primär- und Sekundärprävention die häufigste Todesursache in den westlichen Industrienationen (Lloyd-Jones et al., 2010). Für 352689 der insgesamt 858768 Todesfälle in der Bundesrepublik Deutschland im Jahre 2010 werden Krankheiten des HerzKreislaufsystems verantwortlich gemacht (Statistisches Bundesamt, 2010). 20% aller Todesfälle sind auf die KHK zurückzuführen. Die Lebenszeitprävalenz der KHK in Deutschland beträgt für Männer 12,3%, für Frauen 6,4% (Gößwald et al., 2013) und nimmt mit steigendem Lebensalter und niedrigerem sozioökonomischen Status zu. Angesichts der demographischen Entwicklung und einer Zunahme der kardiovaskulären Risikofaktoren wie arterielle Hypertonie, Dyslipoproteinämie, Diabetes mellitus, Adipositas, Bewegungsmangel wird die Zahl der Betroffenen in Zukunft weiter ansteigen. Die KHK ist die Folge einer oftmals über Jahrzehnte hinweg verlaufenden Verengung der epikardialen Koronararterien durch Atherosklerose. Das resultierende Missverhältnis zwischen Sauerstoffangebot und Sauerstoffbedarf des Herzens lässt die Erkrankung als myokardiale Ischämie manifest werden (Schächinger und Zeiher, 2004). Dies kann als eine stumme Ischämie im Sinne einer asymptomatischen KHK geschehen, aber auch symptomatisch in Form ischämisch bedingter pectanginöser Beschwerden, Herzrhythmusstörungen, Myokardinfarkten und Herzmuskelschädigungen mit der Folge einer möglichen Herzinsuffizienz und der Komplikation des plötzlichen Herztodes. Hauptrisikofaktoren für die Entwicklung einer KHK sind eine Erhöhung des LDLCholesterins, eine Erniedrigung des HDL-Cholesterins, arterielle Hypertonie, Diabetes mellitus, Nikotinabusus und atherosklerotische Folgeerscheinungen wie KHK, Myokardinfarkte oder Schlaganfälle bei erstgradigen Familienmitgliedern vor Erreichen des 55. Lebensjahres bei Männern bzw. des 65. Lebensjahres bei Frauen. Weitere Risikofaktoren sind körperliche Inaktivität und Adipositas mit Betonung der abdominellen Fettspeicher, Lipidstoffwechsel- und Glucosetoleranzstörungen. Biomarker wie Homocystein, Entzündungsmarker Fibrinogen sollten ebenso (high-sensitivity-CRP). Auch Berücksichtigung genetische finden wie Disposition und psychosoziale Faktoren sind mit einem erhöhten Risiko für eine KHK assoziiert (Perk et al., 2012). 7 1.2 Pathophysiologie der KHK Die Atherosklerose stellt das gemeinsame Korrelat verschiedener ischämischer Erkrankungen dar und ist als verantwortlich für einen großen Teil der Morbidität und Mortalität anzusehen. Wie die unterschiedlichen beeinflussbaren und unbeeinflussbaren Risikofaktoren zur Bildung der atherosklerotischen Plaques in den Gefäßen beitragen, ist jedoch weitestgehend unbekannt. Entgegen früherer Betrachtungen wird die Atherosklerose heute als multifaktorielles Geschehen betrachtet, das einen chronischentzündlichen Verlauf aufweist und an dem verschiedene Zelltypen wie T-Lymphozyten, Monozyten, Makrophagen, Thrombozyten, Endothelzellen und glatte Gefäßmuskelzellen beteiligt sind. Im Zuge einer Ungleichheit zwischen pro- und antiinflammatorischen Mechanismen kommt es zur Entstehung atherosklerotischer Plaques (Libby et al., 2010). In Bezug auf die Koronargefäße ist sowohl die mikro- wie auch die makrovaskuläre Herzkrankheit von Interesse. Die Kaskade der Veränderungen beginnt mit einer Funktionsstörung des Endothels, die eine Veränderung seiner Eigenschaften beinhaltet. Dyslipidämie, vasokonstriktorische Mediatoren und proinflammatorische Zytokine bewirken eine erhöhte Permeabilität für Lipoproteine, eine Hyperkoagulabilität sowie eine Induktion von Adhäsionsmolekülen. Eine vermehrte Einwanderung von Entzündungszellen wie T-Lymphozyten, Monozyten und Makrophagen in die Gefäßwand ist die Folge und führt zur Akkumulierung von Lipiden als sogenannte "fatty streaks". Die involvierten Zelltypen sezernieren vasoaktive Substanzen, Zytokine und Wachstumsfaktoren, welche die Bildung von atheromatösen Plaques fördern. Im Verlauf der Erkrankung kommt es neben einer verstärkten Entzündungsreaktion zu einer Migration glatter Muskulaturzellen aus der Media in die Intima. Diese proliferieren und fördern so eine Fibrosierung und Verdickung der Gefäßwand. Eine Reihe weiterer zellulärer Reaktionen fördern den Entzündungsprozess (Baer und Rosenkranz, 2008). Apoptotische Prozesse von Makrophagen und glatten Muskelzellen können schließlich zur Ausbildung eines nekrotischen, lipidhaltigen Kerns führen. Der fortwährende Entzündungsprozess bedingt durch weitere apoptotische Vorgänge eine Beeinträchtigung des Kollagens und der fibrösen Membran, was eine Instabilität der entstandenen Plaque zur Folge haben kann (Faxon et al., 2004). Es sind die Extremformen einer nach intraluminal wachsenden, stenosierenden Läsion und einer abluminal wachsenden, nicht primär stenosierenden Läsion zu unterscheiden. Erstere ist eher fibrotisch dominiert und führt zu Angina pectoris und Perfusionsdefekten, letztere ist im höheren Maße vulnerabel und kann zum akuten Gefäßverschluss führen. 8 Das Risiko einer Plaqueruptur hängt folglich mehr von der Zusammensetzung der Plaque als vom Schweregrad der durch ihn verursachten Stenose ab. Hauptdeterminanten der Stabilität der Plaque sind die Zusammensetzung des atheromatösen Kerns, die Dicke der fibrösen Membran und der Entzündungsgrad (Falk et al., 1995). Eine Plaqueruptur als akutes Ereignis führt durch das Zusammenspiel von Kollagen, Von-Willebrand-Faktor und des sogenannten "tissue factors" zu einer rapiden Bildung thrombotischer Auflagerungen, was sich klinisch als akutes Koronarsyndrom widerspiegeln kann. Mögliche Folgen sind in Abhängigkeit von Versorgungsgebiet und Grad der Stenosierung schwerwiegende Myokardinfarkte mit konsekutiver mikrovaskulärer Obstruktion und plötzlicher Herztod. 1.3 Stufendiagnostik der KHK Die Art und Reihenfolge des diagnostischen Vorgehens hängt von den individuellen Beschwerden, der Versorgungsebene und der Vortestwahrscheinlichkeit für das Vorliegen einer KHK ab. Zunächst sollte klinisch festgestellt werden, ob die vorliegenden Beschwerden einer KHK geschuldet sein könnten und welche Differentialdiagnosen in Betracht zu ziehen sind. Eine Basisdiagnostik umfasst neben einer körperlichen Untersuchung von Herzund Gefäßsystem mit Ermittlung von Größe und Gewicht eine Blutdruckmessung, zudem die Ableitung eines Ruhe-EKGs mit 12 Ableitungen. Laborchemisch sollten neben einem kleinen Blutbild zur Erhebung des Risikostatus Nüchternfette mit Gesamtcholesterin und LDL- und HDL-Fraktionen sowie die Nüchternglucose bestimmt werden. Je nach Art der Schmerzen als nicht-anginöse Brustschmerzen, atypische oder typische Angina kann verbunden mit Geschlecht, Alter und vorliegenden kardialen Risikofaktoren eine Vortest-Wahrscheinlichkeit für das Vorliegen einer KHK ermittelt werden. So werden drei Gruppen von Patienten unterschieden. Bei einer niedrigen Vortestwahrscheinlichkeit von <10% ist eine weitergehende Diagnostik nicht erforderlich, bei einer hohen Wahrscheinlichkeit von >90% sollte eine invasive Diagnostik mittels Koronarangiographie eingeleitet werden. Bei der dritten Gruppe mit einer mittleren Wahrscheinlichkeit zwischen 10% und 90% ist das richtige Vorgehen zu diskutieren. Ist die mittlere Vortestwahrscheinlichkeit auf die Faktoren Alter, Geschlecht und klinische Symptomatik zurückzuführen, sollte ein EKG unter Belastung durchgeführt werden. Sind die betroffenen Patienten nicht so belastungsfähig, dass ein relevanter 9 Befund erzielt werden könnte oder ist die durchgeführte ergometrische Untersuchung nicht aussagekräftig, ist ein bildgebendes Verfahren unter pharmakologischer Belastung indiziert. Empfohlen wird diese Möglichkeit auch generell bei Patienten mit mittlerer Vortestwahrscheinlichkeit. Für eine bestmögliche Bildqualität sollte die Wahl des Verfahrens an den jeweiligen Patienten angepasst werden. Die Verfügbarkeit der Untersuchung ebenso wie die Erfahrungswerte des Zentrums mit der erwählten Technik gilt es zu berücksichtigen (Nationale Versorgungsleitlinie Chronische KHK, 2012). Die eingeleitete Diagnostik unter Berücksichtigung der verschiedenen zur Verfügung stehenden bildgebenden Verfahren sollte unterschiedlichen Ansprüchen gerecht werden. Ziel ist es, eine KHK entweder auszuschließen oder zu diagnostizieren, die funktionelle Signifikanz einer etwaigen Stenose zu überprüfen, die Zellintegrität des versorgten Myokardareals der stenosierten Arterie zu evaluieren und die globale und regionale ventrikuläre Funktion zu ermitteln (Pakkal et al., 2011). Geben die bildgebenden Verfahren unter pharmakologischer Belastung wie StressEchokardiographie, Myokardszintigraphie oder Stress-Magnetresonanztomographie bzw. Myokard-Perfusions-Magnetresonanztomographie einen Hinweis auf einen möglicherweise einer KHK geschuldeten Perfusionsdefekt oder zeigen dysfunktionales Myokard auf, ist eine invasive Diagnostik anzuraten (Gibbons et al., 2003). Zuvor sollte die Vitalität des betroffenen Areals untersucht werden, um die therapeutischen Erfolgsaussichten einer anstehenden invasiven Koronarangiographie besser einschätzen zu können. Die Angiographie mittels CT findet in den allgemeinen Leitlinien zur chronischen KHK noch keine Berücksichtigung. Empfohlen wird das Verfahren, wenn eine mittlere Vortestwahrscheinlichkeit und typische Symptome einer KHK bestehen, insbesondere im Falle eines nicht aussagekräftigen Belastungs-EKGs (Taylor et al., 2010). Der mittels CT erhobene koronare Calcium-Score besitzt einen wissenschaftlich bewiesenen Stellenwert (Budoff et al., 2007), ist jedoch ebenfalls nicht in den Nationalen Versorgungsleitlinien enthalten. 10 1.4 Invasive Verfahren 1.4.1 Koronarangiographie Die invasive Koronarangiographie stellt sowohl zum Ausschluss als auch zur Diagnosestellung einer KHK ein maßgebendes Verfahren dar (Barkhausen et al., 2004). Die Untersuchung vermag Lokalisation, Schweregrad, Länge und Morphologie der Stenosierung (Atherom, Thrombus, Dissektion, Spasmus, Muskelbrücke) in den epikardialen Arterien aufzuzeigen (Hamm et al., 2008). Gefäßläsionen bzw. Stenosierungen können während der selben Untersuchung therapiert werden. So kann eine perkutane transluminale Koronarangioplastie (PTCA) durchgeführt und ein Stent implantiert werden. Hierbei kann es sich um nicht beschichtete bare-metal stents (BMS) oder drug-eluting stents (DES) handeln, wobei letztere wirkungsvoller in der Prävention von Restenosierungen sind (Laarman et al., 2006). Im Jahr 2008 wurden in der Bundesrepublik Deutschland insgesamt 845.172 diagnostische Herzkatheteruntersuchungen durchgeführt. In 303.832 Fällen erfolgte eine Koronarintervention, was einem Anteil von 35,95% entspricht (van Buuren, 2010). Als invasive Untersuchungsform weist die Koronarangiographie seltene, aber typische Komplikationen auf. Hierzu gehören schwerwiegende Komplikationen (Tod, Myokardinfarkt, Schlaganfall, sog. MACCE = major adverse cardiac and cerebrovascular events) und weitere schwere, aber nicht unmittelbar lebensbedrohliche Komplikationen wie koronarer Gefäßverschluss, Perforation, Linksherzdekompensation, Lungenembolie, transfusionsbedürftige Einblutungen und anaphylaktischer Schock. Hinzu kommen passagere Nebenwirkungen supraventrikuläre wie Tachykardien, vagotone Reaktionen, Kammerflimmern, Bradykardie, Asystolie, Kammerflattern und Kontrastmittelunverträglichkeiten. Komplikationen an der Punktionsstelle treten in ca. 0,5% der Eingriffe auf. Die Häufigkeit von MACCE wird in nicht selektionierten Registern mit 0,3-0,63% angegeben (Hamm et al., 2008). 1.4.2 Fraktionelle Flussreserve Angesichts der limitierten Aussagekraft der Koronarangiographie bezüglich der physiologischen Relevanz etwaiger Stenosen (White et al., 1984) wurde mit der Bestimmung der fraktionellen Flussreserve (FFR) ein Verfahren entwickelt, das diesbezüglich Informationen bieten kann. Die FFR ist definiert als der maximal erreichbare Blutfluss in einem Myokardareal im Falle einer vorgeschalteten 11 Koronarstenose geteilt durch den theoretischen normalen Blutflusswert im selben Bezirk (Pijls et al., 1996). Der maximale Blutfluss wird mit Hilfe einer pharmakologisch durch die Gabe von Adenosin erzeugten Hyperämie ermittelt. Folglich beziffert die FFR das Ausmaß der Blutflussbegrenzung durch die Stenose. Mittels Drucksensoren wird der mittlere arteriellen Druck distal der Stenose und in der Aorta gemessen und daraus die FFR berechnet. Diese ist unabhängig von Blutdruck, Puls und myokardialer Kontraktilität (Kim and Koo, 2012). Empfohlen wird das Verfahren bei fehlendem nichtinvasiven Ischämienachweis und kann zielführend in der Frage sein, ob eine Intervention sinnvoll ist (Wijns et al., 2010). 1.4.3 Intravaskulärer Ultraschall Der intravaskuläre Ultraschall (IVUS) ermöglicht die Darstellung des Wandaufbaus und der Dimensionen eines Revaskularisierungsmethode Gefäßes und vereinfachen. kann Mit damit Hilfe von die Wahl der miniaturisierten Ultraschalltransducern, die auf den Koronarkathetern plaziert werden, kann eine örtliche Auflösung von 150-300 µm erzielt werden (Rieber, 2012). Aufgrund der niedrigen Sensitivität und Spezifität findet die Methode im klinischen Alltag nur selten Einsatz. Große Schwierigkeiten bestehen in der Identifizierung fibröser Plaques, während calcifizierte Plaques akkurat erkannt werden (Rieber et al., 2006). Eine Rolle kann der IVUS periprozedural spielen, indem die Expansion und Apposition des implantierten Stents kontrolliert werden und die Restenose- und Revaskularisierungsrate hierdurch verringert werden (Parise et al., 2011). 1.5 Nicht-invasive Verfahren Nicht-invasive Verfahren können im Hinblick auf die KHK einerseits die Koronararterien direkt darstellen (CT-Angiographie, MR-Angiographie) und andererseits die funktionelle Signifikanz von Koronarstenosen untersuchen (SPECT, PET, StressMRT, Echokardiographie). Bezüglich der globalen kardialen Funktion bieten diese im Vergleich zu den invasiven Verfahren einen größeren Informationsgewinn. 1.5.1 SPECT Die Szintigraphie myokardialer Perfusion wurde in den 1970er Jahren entwickelt und brachte durch technische Weiterentwicklungen heute etablierte Techniken wie die Single photon emission computer tomography (SPECT) hervor. Die nuklearmedizinische Bildgebungstechnik setzt zur Darstellung der Aktivitätsverteilung des Herzens die 12 intravenöse Injektion kleiner Mengen eines radioaktiven Tracers wie chlorid oder 99m 201 Ti-Thallium(I)- Technetium-MIBI voraus, üblicherweise verbunden mit einer myokardialen Belastungssituation unter pharmakologischem oder ergometrischem Stress. Die Verteilung des Radiopharmakons wird anschließend mittels SPECT unter Belastung und in Ruhe aufgezeichnet. Die Intensität der Anreicherung im Myokard erlaubt Aussagen über die Perfusion, die gesonderte Betrachtung von Ruhe- und Belastungsphasen als Vitalitätsdiagnostik eine Unterscheidung von belastungsgetriggerter Ischämie und Myokardnarbe. Die Aufnahmen werden mit Hilfe einer um den Patienten rotierenden Gammakamera gewonnen, die Schnittbilder können beliebig orientiert werden. Vorteile der präferierten 99mTechnetium-Pharmaka gegenüber Thallium(I)-chlorid sind die geringere Strahlenexposition (7mSv gegenüber 17 mSv) und die geringere physikalische Halbwertszeit (6 Stunden gegenüber 73 Stunden). Die Auswertung erfolgt visuell und quantitativ. 1.5.2 PET Als weiteres nuklearmedizinisches Verfahren macht die Positron emission tomography (PET) eine Untersuchung des myokardialen Stoffwechsels und der Perfusion des Herzens möglich. Mit Hilfe der PET können regionale Perfusionsänderungen absolut gemessen werden, während die SPECT auf der Wahrnehmung von relativen Perfusionsunterschieden beruht. Grundlage für die Bildgebung ist ebenfalls die Gabe eines Tracers. So kommen unter anderem 13N-Ammoniak, 15O-Wasser und 82Rubidium bei der Messung des regionalen myokardialen Blutflusses in Ruhe und unter körperlicher oder pharmakologischer Belastung zum Einsatz. Zur Beurteilung des myokardialen Stoffwechsels wird 18Fluor-Deoxyglucose (FDG) eingesetzt. Anhand dessen kann vitales Myokardgewebe erkannt und eine Vorhersage über eine funktionelle Erholung getroffen werden. Ein bedeutender Unterschied zur SPECT besteht in der emittierten Strahlung des verwendeten Radiopharmakons. Das vom Tracer ausgesandte Positron zerfällt in 2 Photonen, die von der Messung erfasst werden können. Mit Hilfe von GammastrahlenRingdetektoren wird eine dreidimensionale Datenakquisition ermöglicht. Die primäre Auswertung erfolgt visuell. 1.5.3 Belastungs-Elektrokardiographie Das EKG unter Belastung ist eine weitere Methode zur Identifizierung von potentiellen Patienten mit KHK. Indiziert ist es unter anderem bei einem unauffälligen oder unspezifische Veränderungen aufzeigenden Ruhe-EKG zur weiteren Abklärung sowie 13 bei asymptomatischen Patienten mit einem ausgeprägten kardiovaskulären Risikoprofil. Es bietet die Möglichkeit, myokardiale Ischämien zu identifizieren, die erst nach Überschreiten einer bestimmten Ischämieschwelle auftreten. Die ubiquitär in Hausarztpraxen und Krankenhäusern verfügbare Untersuchung ist kostengünstig und relativ einfach durchzuführen. Bei hoher Variabilität konnte im Rahmen einer MetaAnalyse eine Sensitivität von 68% und Spezifität von 77% aufgezeigt werden (Gianrossi et al., 1989). Bei Patienten mit niedriger bis mittlerer Vortestwahrscheinlichkeit für das Vorliegen einer KHK wird der Untersuchung eine besonders geringe diagnostische Wertigkeit bescheinigt (Maffei et al., 2010). 1.5.4 Stress-Echokardiographie Die Stress-Echokardiographie ist ein vielerorts verfügbares und kostengünstiges Verfahren, mit dem das Herz auf Wandbewegungsstörungen untersucht wird. Dies kann unter körperlicher oder pharmakologischer Belastung mit Gabe von Dobutamin geschehen. Tritt unter Belastung eine Wandbewegungsstörung neu auf oder verschlimmert sich, kann dem eine ischämische Ursache zugrunde liegen. Mit Hilfe der M-Mode-Darstellung kann die linksventrikuläre Funktion erfasst werden. Eine normale Stress-Echokardiographie ist mit einer exzellenten Prognose assoziiert. Die Jahreswahrscheinlichkeit für schwerwiegende kardiale Ereignisse liegt bei einer Patientengruppe mit mittlerer bis hoher Vortestwahrscheinlichkeit für eine KHK bei 0,8% (Chung et al., 2004). Die für den Patienten wenig belastende Untersuchung besitzt weiterhin einen Vorteil im Fehlen ionisierender Strahlung. 1.5.5 Die Computertomographie und koronarer Calcium-Score CT-Angiographie stellt ein Verfahren zur direkten Visualisierung der Koronararterien dar. Technische Fortschritte auf Seiten der zur Verfügung stehenden Geräte haben in den letzten Jahren ebenso zu einer Verbesserung der räumlichen Auflösung geführt wie eine bessere Softwareaufbereitung. Gleichzeitig konnte die Belastung durch ionisierende Strahlen deutlich reduziert werden. Die Methode kann eine hohe Sensitivität zur Erkennung einer vorliegenden KHK und einen hohen negativen prädiktiven Wert vorweisen (Budoff et al. 2008), allerdings ist die Spezifität durch Probleme bei schwer kalzifizierten Koronararterien, kleinen Gefäßen oder der Anwesenheit von Stents eingeschränkt. Auch bietet die CT-Angiographie keine Aussage über die tatsächliche funktionelle Relevanz einer Stenose (van Werkhoven et al., 2010). Eine virtuelle FFR-Messung basierend auf CT-Daten bietet in Studien gute Ergebnisse 14 (Koo et al., 2011). CT-Perfusionsbildgebungen finden immer weitere Verbreitung und werden in Studien hinsichtlich ihres diagnostischen Wertes überprüft (Feuchtner et al., 2012). Etabliert ist hingegen das Verfahren zur Quantifizierung von Calciumablagerungen in den Koronararterien. Verbunden mit einer geringen Strahlendosis kann der sogenannte Agatston-Score erhoben werden, der einen unabhängigen Risikofaktor für das Vorliegen einer KHK darstellt. Die Präsenz von koronaren Calciumablagerungen ist sensitiv aber nicht spezifisch bei der Diagnosestellung der Erkrankung und hat prognostischen Wert. Werden keine Ablagerungen festgestellt, beträgt die Wahrscheinlichkeit eines kardialen Ereignisses in den nächsten 50 Monaten <1,01% (Sarwar et al., 2009). 1.5.6 Magnetresonanztomographie Die Magnetresonanztomographie kann im Hinblick auf die KHK auf verschiedene Weise wertvolle Informationen liefern. Die Adenosin-Stress-MRT wird in der vorliegenden Studie thematisiert. Mit Hilfe dieser Perfusionsbildgebung kann der first-pass eines Kontrastmittels betrachtet werden und unter pharmakologischer Belastung zum Beispiel Hinweise auf eine reversible Ischämie liefern. Die late-enhancement-Aufnahmen können hingegen unter anderem das Ausmaß eines Infarktareals abbilden. Die MR-Koronarangiographie bietet die Möglichkeit, eine anatomische Bildgebung mit einer MRT-Untersuchung der kardialen Funktion, Struktur und Perfusion zu verbinden (Foo et al., 2005). Als alleinige Untersuchung zur Diagnosestellung einer KHK weist die MR-Koronarangiographie in einer Meta-Analyse eine Sensitivität von 72% (69%-75% [95% KI]) bei einer Spezifität von 87% (86%-88% [95% KI]) auf (Schuijf et al., 2006). Der klinische Nutzen ist wegen der relativ langen Untersuchungszeit und Schwierigkeiten aufgrund von Bewegungsartefakten derzeit begrenzt (Bluemke et al., 2008). Die Möglichkeit zur Darstellung der koronararteriellen Gefäßwand und ihrer Morphologie hat das Potential, eine bedeutsame Rolle bei der Beurteilung und Risikobewertung von koronaren Plaques zu spielen. Als Goldstandard wird die kardiale MRT bei der Evaluierung der globalen myokardialen Vitalität und der regionalen Funktionsanalyse des linken Ventrikels angesehen. Weitere Indikationen sind die Evaluation kongenitaler Herzfehler und erworbener Erkrankungen der großen Gefäße, der Nachweis von Raumforderungen des Herzens sowie die Diagnostik von Perikarderkrankungen und Kardiomyopathien. 15 II Zielsetzung Diese Arbeit hat sich zum Ziel gesetzt, den Stellenwert der nicht-invasiven Diagnostik der KHK am Beispiel der Adenosin-Stress-MRT in einem ambulanten Rahmen zu untersuchen. Die diagnostische Wertigkeit der MRT-Untersuchung bei der Unterscheidung zwischen einer hämodynamisch relevanten und einer nicht relevanten Koronarstenose soll anhand des invasiven Goldstandards Koronarangiographie überprüft und im Hinblick auf die heute zur Verfügung stehenden nicht-invasiven Techniken diskutiert werden. Es wird postuliert, dass die Adenosin-Stress-MRT-Untersuchung nicht signifikant schlechter in der Unterscheidung zwischen relevanten und nicht relevanten Koronarstenosen ist, als die Koronarangiographie. Eine Besonderheit der vorliegenden Arbeit stellen das ambulante Umfeld und das der klinischen Realität entstammende Entscheidungsprozesse in der unverfälschte Stufendiagnostik Berücksichtigung finden. 16 Patientengut dar. der sollen KHK Ambulante ebenfalls III Material und Methoden 3.1 Patienten Der vorliegenden Arbeit liegt eine retrospektive Analyse der anonymisierten Daten von 54 Patientinnen/Patienten (im Folgenden als „Patienten“ bezeichnet) zugrunde. Die Einschlusskriterien setzten voraus, dass sich jene innerhalb eines Zeitfensters von 180 Tagen sowohl einer ambulanten Kardio-MRT als auch einer Koronarangiographie unterzogen hatten. Im Durchschnitt vergingen zwischen den beiden Untersuchungen 39,9 ±41 Tage. Sämtliche Untersuchungen erfolgten aus klinischer Indikation bei vermuteter oder bereits diagnostizierter KHK. Das durchschnittliche Patientenalter lag bei 62,4 ±8,6 Jahren, es wurden 19 Frauen und 35 Männer in die statistische Auswertung einbezogen. Bei 20 Patienten wurde in der Vorgeschichte eine Koronarangiographie mit Implantation eines oder mehrerer Stents durchgeführt. Patienten mit Zustand nach Bypass-Operation wurden von der Studie ausgeschlossen. Tabelle 1: Patientencharakterisierung Gesamtzahl 54 Alter in Jahren 62,4 ±8,6 Frauen 19 Männer 35 Frauen in % 35,2 Männer in % 64,8 Z.n. Stentimplantation 20 Patienten mit LCA-Stent 12 Patienten mit LCX-Stent 4 Patienten mit RCA-Stent 8 Ø Zeitintervall zwischen Kardio-MRT und Koronarangiographie 17 39,9 ±41 3.2 Kardio-MRT Im folgenden Abschnitt sollen zunächst die Grundlagen der Akquirierung von Bildern mittels Magnetresonanztomographie beschrieben werden, um im Anschluss Besonderheiten der MRT des Herzens zu behandeln. Dabei soll auch auf die Bedeutung pharmakologischer Belastung und der Kontrastmittelgabe eingegangen werden. 3.2.1 Physikalische Grundlagen der Magnetresonanztomographie Das Prinzip der Magnetresonanztomographie macht sich den hohen Wasseranteil des menschlichen Körpers zunutze. Der Atomkern des Wasserstoffs bringt zwei für die Technik der Untersuchung relevante Eigenschaften mit. Das Proton besitzt ein magnetisches Moment, folglich wirkt es wie ein kleiner Magnet. Zudem dreht es sich um die eigene Achse, was man als (Kern)spin bezeichnet. Ein äußeres Magnetfeld B0 kann die Lage der Protonen verändern. Die Spins liegen zum Teil antiparallel, bevorzugt aber parallel ausgerichtet vor, was energetisch günstiger ist. Aus der Summe der Magnetvektoren der Protonen resultiert die Längsmagnetisierung. Sie liegt im Grundzustand in z-Richtung vor und wird als Mz bezeichnet. Wird eine äußere Magnetkraft auf die Spins gelenkt, so folgt eine Präzessionsbewegung der Protonen um die z-Achse des Feldes. Diese geschieht mit einer ihr eigenen Frequenz, die Larmor-Frequenz genannt wird. Jene hängt proportional von der Stärke des Magnetfeldes B0 ab (Weishaupt et al., 2009). Die Messung eines Signals durch die Empfangsantennen des MR-Systems setzt eine Drehung der Längsmagnetisierung Mz in die Querrichtung voraus. Dies geschieht im Rahmen der sogenannten Anregung, die energetisch durch einen Hochfrequenzpuls bewirkt und mit einer der Larmor-Frequenz entsprechenden Frequenz von einer Antennenspule ausgesendet wird. Bei richtiger Leistung und Dauer des eingebrachten elektromagnetischen Impulses hat dies zur Folge, dass die Magnetisierung um 90° aus der z-Richtung in die xy-Ebene kippt und mit der Larmor-Frequenz rotiert (Uhlenbrock und Forsting, 2007). Dieser Zustand der Anregung im Sinne einer Transversalmagnetisierung induziert ein Signal, das proportional zur Stärke des entstandenen Mxy ist. Das Signal wird auch als FID („free induction decay“) bezeichnet und kann mit Hilfe von sensiblen Verstärkern und Computern zum MR-Bild verarbeitet werden. 18 Abbildung 1: Anregung (modifiziert nach van Geuns et al., 1999). Die Längsmagnetisierung in Mz-Richtung wird durch einen Hochfrequenzpuls um genau 90° in die Mxy-Ebene umgeklappt. Diesen Zustand bezeichnet man als Transversalmagnetisierung. Nach der Anregung kreisen die Spins in der xy-Ebene. Zwei verschiedene Mechanismen spielen bei der anschließenden Relaxation eine Rolle. Diese beinhaltet, dass das MRSignal abnimmt und der stabile Grundzustand vor der Anregung wieder erreicht wird. Man nennt die betreffenden Vorgänge Längs- und Querrelaxation. Die Längsrelaxation wird aus dem Grund so bezeichnet, weil die Protonen aus dem Zustand der Anregung zurück in die Längsmagnetisierung Mz relaxieren. Die Dauer, die die Protonen zur Rückkehr aus dem angeregten Zustand in diesen Grundzustand benötigen, bezeichnet die T1-Zeit. Sie hängt sowohl von der Kraft des äußeren Magnetfeldes B0 als auch von der inneren Bewegung der Moleküle ab. Die T2-Zeit hingegen bemisst die Geschwindigkeit der Dephasierung der Präzession der Protonen. Unmittelbar nach der Anregung ist die Präzessionsbewegung der Spins weitestgehend synchron. Diese sogenannte Phasenkohärenz wird jedoch im Verlauf durch Magnetfeldveränderungen benachbarter Protonen und Moleküle gestört. Ebenso tragen zeitlich konstante Inhomogenitäten des äußeren Magnetfeldes zur Dephasierung bei. Ein reales inhomogenes Magnetfeld zerfällt mit seiner Zeitkonstanten T2* rascher als ein ideales homogenes. Vor allem an Gewebegrenzen kommt dieser Inhomogenitätsfaktor zustande. In der Folge nehmen Mxy und damit auch das MR-Signal 19 immer weiter ab, bis es schließlich verschwindet. Der beschriebene Vorgang wird Querrelaxation genannt. Um Inhomogenitäten auszugleichen, wird mittels eines 180° Rephasierungspulses, ebenfalls ein HF-Puls, ein weiteres Signal erzeugt. Dieses wird Spinecho genannt. Beide Vorgänge, die auch als T1-Relaxation bezeichnete Längsrelaxation wie auch die Querrelaxation, T2-Relaxation genannt, laufen gleichzeitig und unabhängig voneinander ab. Die Prozesse unterliegen gewebsinternen Einflüssen und können zur Charakterisierung eingesetzt werden (Weishaupt et al., 2009). Die Bildkontraste im MR-Bild werden durch Protonendichte, T1- und T2-Zeit bestimmt. Diese drei Parameter können im betrachteten Gewebe sehr unterschiedlich ausgeprägt sein und sind von diagnostischem Nutzen. Das MR-Bild beruht auf einer Vielzahl von Rohdatensätzen, von denen jede einzelne Datenzeile eine erneute Anregung der untersuchten Schicht voraussetzt. Als Repetitionszeit TR wird die Dauer zwischen zwei Anregungen bezeichnet. Unterschiedliche TR bestimmen über die Zeit die Anzahl der Spins, die in den Grundzustand in z-Richtung zurückgelangen und führen zu verändertem Kontrast im T1-Bild. So zeigt sich bei einem kurzen TR von beispielsweise 600 ms eine starke T1-Gewichtung, folglich erscheint ein Gewebe mit einer kurzen T1Zeit hell, da hier ansässige Spins relativ schnell relaxieren und mehr Signal beisteuern. Eine lange TR-Zeit von mehr als 1500 ms hingegen verhilft auch Gewebe mit langem T1 in den Zustand der Längsmagnetisierung zu kommen, so dass alle Gewebe vergleichbar viel Signal abgeben und der Kontrast geringer ist. In diesem Falle hängt der Kontrast von der Protonendichte PD des Gewebes ab (Uhlenbrock und Forsting, 2007). In Bezug auf T2-gewichtete Aufnahmen ist die Echozeit TE ausschlaggebend, also die Zeit, die zwischen Anregung und Messung des MR-Signals vergeht. Eine kurze Echozeit von weniger als 30 ms Dauer bedeutet, dass die T2-Relaxation erst wenig fortgeschritten ist und sich Gewebe wenig kontrastiert darstellt. Eine mit mehr als 60 ms länger bemessene Echozeit lässt Gewebe mit relativ kurzem T2 dunkel erscheinen, da jene bereits große Anteile ihrer Signalintensität verloren haben. Protonengewichtete Bilder vereinen Eigenschaften T1- und T2-basierter Bilder und weisen eine lange TR und eine kurze TE auf. Wenn die TE im Bereich von 40 ms Dauer liegt, entstehen sogenannte intermediär gewichtete Bilder. Beide Möglichkeiten spielen bei der Beurteilung von Gewebe eine bedeutsame Rolle (Uhlenbrock und Forsting, 2007). 20 Die Wahl der Schicht ist auch bei der Untersuchung des kardiovaskulären Systems für die Beurteilung entscheidend. Das durch den zuvor beschriebenen Zustand der Anregung erzeugte MR-Signal impliziert in einem homogenen Magnetfeld, dass alle Protonen die identische Larmorfrequenz besitzen und mit einem entsprechenden Anregungspuls der gesamte Körper angeregt werden würde. Die Schnittbildgebung setzt allerdings voraus, dass nur die Protonen einer bestimmten Schicht angeregt und ihr Summensignal aufgezeichnet wird (Dymarkowski and Bosmans, 2005). Aus diesem Grund wird das Feld in einer gewählten Richtung durch eine weitere Magnetspule inhomogen gemacht. Jene verstärkt das magnetische Feld auf einer Seite und schwächt es auf der anderen Seite, so dass ein Gradient geschaffen wird. Folglich ergibt sich entlang dieses Gradienten eine fließende Veränderung der Larmorfrequenz der Protonen, wodurch jede Schicht eine individuelle Frequenz besitzt, die mit dem passenden HF-Puls angeregt werden kann. Die Schichtdicke ist abhängig von der Gradientenstärke. Nach Anregung einer bestimmten Schicht werden weitere Magnetspulen zur Ortskodierung der Bildinformation hinzugeschaltet. Die insgesamt drei Gradientenspulen schlüsseln das Signal in der Folge weiter auf und ergeben eine Kodierung des Signals in drei Raumebenen. Eine Kontraindikation zur MRT-Untersuchung stellt das Tragen eines Schrittmachers oder ICD-Systems dar. Ausgesandte Hochfrequenzpulse können zu Störungen der Funktion führen. Mittlerweile wurden MRT-kompatible Schrittmacher entwickelt, auch werden die unterschiedlichen implantierten Systeme hinsichtlich ihrer MRT-Sensibilität in weiteren Studien überprüft (Jung et al., 2012). Weitere Ausschlussgründe können künstliche Herzklappen, Gefäßclips, Metallsplitter aus ferromagnetischem Material oder Implantate wie Insulinpumpen und Cochleaimplantate sein. Darüber hinaus stellen das erste Trimenon und Klaustrophobie relative Kontraindikationen dar. 3.2.2 Besonderheiten der Kardio-MRT Kernspintomographische Aufnahmen des Herzens erfolgen im Normalfall in Anpassung an das EKG des Patienten. Durch diese Triggerung soll gewährleistet werden, dass die meist in mehreren Herzzyklen notwendige Datenakquisition stets im gleichen Zeitraum eines Zyklus erfolgt und Artefakte infolge der Herzbewegung deutlich reduziert werden. Auch die Minimierung von Atemartefakten spielt bei der Datengewinnung eine Rolle. Bei kooperativen Patienten ist die Atemanhaltetechnik erfolgversprechend, alternativ kann auch eine Triggerung an die Atembewegung vorgenommen werden. 21 Die Wahl der Bildparameter bei der Kardio-MRT hängt von der Fragestellung ab (Dymarkowski and Bosmans, 2005). Beispielsweise profitiert die Beurteilung der linksventrikulären Wanddicke und des Perikards von T1-basierten Aufnahmen. Auch bei der Frage nach Infarktarealen oder Myokardfibrose erfordert die Darstellung von Gewebe nach intravenöser Kontrastmittelgabe eine T1-Wichtung. Die Echozeit TE wird an die Herzfrequenz angepasst und kurz gehalten (5 - 15 ms), die Repetitionszeit TR entspricht einem R-R-Intervall im EKG des untersuchten Patienten. T2-gewichtete Bilder spielen zum Beispiel bei der Frage nach einem myokardialen Ödem eine Rolle. Im Rahmen der KHK-Diagnostik kann die Kardio-MRT unter Zuhilfenahme einer Bolusinfusion eines intravenösen Kontrastmittels den sogenannten first-pass, die Kontrastmittelanflutung durch das Myokard, darstellen. Dies bringt einen Informationsgewinn über das Ausmaß und die physiologische Signifikanz etwaiger Koronarstenosen mit sich (Ishida et al., 2003). Technisch wird die Beurteilung der myokardialen Perfusion durch Serien EKG-getriggerter T1-gewichteter Bilder ermöglicht. Während der Patient die Luft anhält, werden die Herzaktionen während des first-pass des Kontrastmittelbolus aufgenommen (Knobelsdorff-Brenkenhoff and Schulz-Menger, 2012). Simultan erfolgt die Infusion eines Vasodilatators wie Dipyridamol oder Adenosin, die zur Erweiterung der nicht von einer KHK betroffenen Arterien führen. Infolge des sogenannten Steal-Phänomens kommt es zu einer Verminderung der Perfusion im Versorgungsbereich einer stenosierten Koronararterie. Im Rahmen der dieser Studie zugrundeliegenden Stress-MRT-Untersuchungen fand Adenosin Verwendung. Adenosin greift direkt an A2A-Rezeptoren an und sorgt dadurch für eine beinahe vollständige Ausschöpfung der Koronarreserve. Allerdings werden mit A1, A2B und A3 auch weitere Rezeptoren ungewollt stimuliert und hierdurch mögliche Nebenwirkungen wie ein atrioventrikulärer Block oder Bronchokonstriktion hervorgerufen (Shryock and Belardinelli, 1997). Die intravenöse Gabe dieses Medikaments zur Beurteilung der myokardialen Perfusion ist unter sorgfältiger Beachtung der Kontraindikationen sicher und wird auch von Patienten mit schwerer KHK gut vertragen (Karamitsos et al., 2008). Die kontrastmittelverstärkte MRT erfolgt unter der Gabe eines paramagnetischen Kontrastmittels wie Gadolinium. Paramagnetische Kontrastmittel entziehen angeregten Protonen rascher Energie und verstärken durch eine Verkürzung der T1-Zeit das gemessene Signal. Hierdurch ist zum Beispiel eine genauere Differenzierung von vitalem 22 Myokard gegenüber Narbengewebe möglich und das transmurale Ausmaß vitalen Myokards besser abgrenzbar, was eine Aussage über den Erfolg einer Revaskularisierungsmaßnahme erlaubt (Kim et al., 2000). Das beobachtete Lateenhancement, die myokardiale Spätanreicherung nach Gabe des extrazellulären Kontrastmittels, ist vermutlich durch verschiedene Faktoren bedingt. So dürfte der Verlust der Integrität von Zellmembranen ebenso eine Rolle spielen wie der vergrößerte Extrazellulärraum infolge eines interstitiellen Ödems beim akuten Myokardinfarkt oder Narben nach Infarzierung (Sandstede, 2003). Im Hinblick auf die Analyse der Herzfunktion mittels kardialer MRT können die ventrikulären Volumina bestimmt werden. Die enddiastolischen und endsystolischen Volumina werden anhand der Simpson-Methode bestimmt. Hierzu kommen Kurzachsenschnitte entlang der langen Herzachse zum Einsatz. Für die einzelnen Schichten werden in Enddiastole und Endsystole die Volumina durch die Multiplikation von Fläche und Schichtdicke gemessen und anschließend für den gesamten Ventrikel summiert. Nach Bestimmung des enddiastolischen (EDV) und endsystolischen Volumens (ESV) kann aus diesen Parametern das Schlagvolumen (SV), die Ejektionsfraktion (EF) und das Herzzeitvolumen (HZV) berechnet werden. Als Ergänzung sollte die Myokardmasse (MM) ermittelt werden (Ley und Kreitner, 2007). 3.2.3 Untersuchungsablauf / Protokoll Neben den bereits erwähnten allgemeinen Ausschlussgründen wurden weitere Kontraindikationen zur Durchführung einer Stress-MRT-Untersuchung unter pharmakologischer Belastung mit Adenosin beachtet, wie Hypotonie von <90mmHG systolisch, hochgradige Aortenklappenstenose, instabile Angina pectoris sowie Zustand nach Myokardinfarkt innerhalb der vergangenen 48 Stunden. Bei Neigung zu Bronchospasmen, oder bestehender pulmonaler Hypertonie wurde ebenfalls auf eine pharmakologische Belastung mit Adenosin verzichtet. Weiterhin waren schwere Arrhythmien und Leitungsstörungen wie AV Block II. oder III. Grades, Sick-SinusSyndrom und QT-Verlängerung ein Ausschlussgrund. Im Hinblick auf die Gabe des gadoliniumhaltigen Kontrastmittels war der Kreatinin-Wert zu bestimmen. Bei einer GFR von <30 ml / min / 1,73 m2 ist eine sorgfältige Abwägung von Risiko und Nutzen zu treffen. 23 Die Patienten wurden angewiesen, innerhalb von 24 Stunden vor der Untersuchung auf den Genuss von Kaffee, Tee, Energydrinks und Schokolade, und in den letzten 4 Stunden gänzlich auf Nahrungsaufnahme zu verzichten. Die Untersuchungen erfolgten an einem 1,5 Tesla Kernspintomographen der Firma Siemens mit der Bezeichnung Siemens Magnetom Avanto TIM 76x18. Als Kontrastmittel kam Gadovist® (Bayer Vital GmbH, Leverkusen) zum Einsatz, zur pharmakologischen Belastung wurde Adenoscan® (Sanofi Aventis Deutschland GmbH, Frankfurt am Main) verwendet. Es wurde eine prospektive EKG-Triggerung eingesetzt. Die Patienten lagen während der Untersuchung auf dem Rücken, unter stetiger Kontrolle ihrer Vitalparameter. Zur weiteren Patientenüberwachung dienten Sprechkontakt und Kameraüberwachung. Nach Anfertigung von Übersichtsaufnahmen zur exakten Lokalisierung der Lage und Achsen des Herzens wurden Sequenzen zur Beurteilung von Herzmorphologie und der Myokardfunktion in Ruhe durchlaufen. Diese schlossen Langachsenschnitte mit 4-Kammerblick, 2-Kammerblick und 3-Kammerblick und lückenlose Kurzachsenschnitte mit ein. Eine Ventrikelvolumetrie wurde anhand der Analyse kurzer Herzachsenschnitte durchführt. Zu Beginn der Perfusionsaufnahmen wurde Adenosin als kontinuierliche Infusion über 6 Minuten als koronarer Vasodilatator mit einer Rate von 140 µg / kg / min verabreicht. 3 Minuten nach Beginn der AdenosinInfusion wurde über einen weiteren Zugang das gadoliniumhaltige Kontrastmittel gegeben und in Atemanhaltetechnik die myokardiale Kontrastmittelanflutung unter Belastung unter Verwendung kurzer Herzachsenschnitte aufgezeichnet. Die Myokardkinetik unter Dobutamin-Stress kann im Rahmen weiterer Sequenzen ebenfalls untersucht werden. Spätanreicherung des Die Spätaufnahmen injizierten zur Kontrastmittels Beurteilung wurden der 15 myokardialen Minuten nach Kontrastmittelapplikation durchgeführt. 3.2.4 Auswertung Eine Kardio-MRT kann auf unterschiedliche Weise ausgewertet werden. Zum einen besteht die Möglichkeit einer Einteilung in Vorder-, Seiten-, Hinterwand und Septum zu folgen, zum anderen stellt das von der American Heart Association im Jahre 2002 vorgestellte 17-Segment-Modell eine anerkannte Nomenklatur dar. Diese wurde ursprünglich für die Echokardiographie entwickelt und unterteilt den linken Ventrikel des Herzens für die Beurteilung von Kontraktilität und myokardialer Perfusion in 17 Segmente. Anhand eines Längsachsenschnitts wird die Kammer in einen basalen, einen 24 mittventrikulären und einen apikalen Anteil unterteilt, so dass folglich drei Kurzachsenschnitte entstehen. Benannt werden die myokardialen Segmente ausgehend von diesen Schnittebenen anhand ihrer Lokalisation im linken Herzen (Cerqueira et al., 2002). 1 – basale Vorderwand 2 – basales anteriores Septum 3 – basales inferiores Septum 4 – basale Hinterwand 5 – basale inferiore Seitenwand 6 – basale anteriore Seitenwand 7 – mittventrikuläre Vorderwand 8 – mittventrikuläres anteriores Septum 9 – mittventrikuläres inferiores Septum 10 – mittventrikuläre Hinterwand 11 – mittventrikuläre inferiore Seitenwand 12 – mittventrikuläre anteriore Seitenwand 13 – apikale Vorderwand 14 – apikales Septum 15 – apikale Hinterwand 16 – apikale Seitenwand 17 – Apex Abbildung 2: Segmenteinteilung des Herzens (modifiziert nach Cerqueira M. et al., 2002) Im Rahmen der visuellen Analyse der Cinesequenzen oder der Schnittbilder als Film können Kontraktilität und Perfusion beurteilt werden. So lässt sich die Wandbewegung bei regelrechter Funktion als normokinetisch, im Falle einer verminderten Einwärtsbewegung als hypokinetisch, bei keinerlei Wandbewegung als akinetisch und in Folge einer beispielsweise paradoxen systolischen Bewegung des Myokards als dyskinetisch beschreiben. Bei der visuellen oder qualitativen Analyse von Perfusionsstudien wird das Signalverhalten zum Zeitpunkt der maximalen Kontrastierung des Myokards betrachtet. Dies geschieht bevorzugt durch simultane Darstellung der Ruheaufnahmen und der Belastungsaufnahmen als Cinesequenz. Das Augenmerk wird dabei auf langsamere und signalärmere Areale gelegt, Hypointensitäten werden als verdächtig für Perfusionsdefekte erachtet. Hierbei ist eine Unterscheidung von subendokardialen und transmuralen Perfusionsstörungen möglich (Sandstede et al., 2007). Hilfreich für die Bewertung einer etwaigen Perfusionsstörung ist der Vergleich von Ruhe- und Stressuntersuchung. Der pharmakologische Stress simuliert Belastungsbedingungen und deckt auf diese Weise eingeschränkte Perfusionsreserven auf. Diese äußern sich in einer sichtbaren 25 Verminderung der regionalen Myokardperfusion oder aber durch Wandbewegungsstörungen. Die Diagnose einer belastungsabhängigen Ischämie setzt eine normale Perfusion in Ruhe und eine relative Hypoperfusion im intrinsischen Vergleich voraus. In Ruhe und unter Stress vergleichbar ausgeprägte Perfusionsstörungen können als mikrovaskuläre Obstruktionen beim akuten Infarkt oder in Folge von transmuralen Infarktnarben gesehen werden (Grebe, 2004). Die zeitversetzt nach Kontrastmittelgabe angefertigten Spätaufnahmen erlauben durch den ausgeprägteren Kontrast eine bessere Unterscheidung von Infarktzone und vitalem Myokard (Vöhringer et al, 2007). Die Bestimmung des transmuralen Infarktausmaßes ist für die Einschätzung einer möglicherweise reversiblen Dysfunktion wichtig. Bedeutsam für die Differentialdiagnose sind vor allem Lokalisation und Verteilungsmuster der Bereiche späten Enhancements (Sandstede et al., 2003). So zeigt sich zum Beispiel ein ischämisches Late-enhancement stets durch Miteinbeziehung subendokardialer Regionen. Durch eine Minderperfusion bedingte Enhancements erscheinen flächig und lassen sich üblicherweise einer Koronararterie zuordnen, während nichtischämische Lateenhancements diesen Regeln nicht folgen müssen und diffus auftreten können. Die Aussagekraft der Spätaufnahmen ist zu dem Zeitpunkt am höchsten, wenn normale, vitale Myokardareale vollständig signalgemindert sind. Die semiquantitative Auswertung basiert auf der Messung von Signalintensitäten in Beziehung zur Zeit und versucht auf diese Weise die relativen Perfusionsunterschiede in verschiedenen Myokardarealen zu erfassen. Ein zusätzlicher Einsatz der semiquantitativen Auswertung neben der visuellen Analyse hat das Potential, die geringe Rate an falsch-negativen Kardio-MRT-Untersuchungen noch weiter zu verringern (Pilz et al., 2010). Die quantitative Auswertung erfordert die Einbeziehung umfangreicher mathematischer Modelle zur näherungsweisen Bestimmung des myokardialen Blutflusses und ist als diagnostische Methode Gegenstand von Studien. 26 3.3 Koronarangiographie 3.3.1 Vorbereitung, Durchführung Nach Prüfung der Indikationsstellung, eingehender Sichtung der Risikofaktoren, bestehender Begleiterkrankungen (beispielsweise Schilddrüsen- und Nierenerkrankungen, Diabetes, Blutungs- Medikamenten- oder und Thromboseneigungen) und Kontrastmittelunverträglichkeiten Allergien sollte bzw. etwaiger bei elektiver Koronarangiographie in angemessenem zeitlichen Abstand zur Untersuchung die Aufklärung über Nutzen, Risiken und Folgen der Untersuchung einschließlich etwaiger Interventionen und deren Alternativen erfolgen. In Herzkatheterlaboren wird heute zur Untersuchung bevorzugt eine biplane Anlage vorgehalten, die eine gleichzeitige Durchleuchtung in zwei Ebenen ermöglicht. Die Linksherzkatheteruntersuchung kann mit Hilfe eines Zugangs über die rechte / linke Arteria femoralis, die rechte / linke Arteria brachialis oder die rechte / linke Arteria radialis erfolgen. Die zunehmende Bedeutung der ambulanten Koronarangiographie hat – auch durch Fortschritte in der Verkleinerung des technischen Materials begünstigt – dazu geführt, dass die zwischenzeitlich deutlich seltener eingesetzten Zugangswege vom Arm einen neuen Stellenwert wiedergewonnen haben (Windecker et al., 2000). Die meistgewählte Gefäßpunktionsstelle ist aufgrund der relativ unkomplizierten Punktion allerdings weiterhin die A. femoralis. Verlassen wird dieser Zugang beispielsweise bei schwerer pAVK. Nach erfolgreicher Punktion wird der Katheter über einen weichen Führungsdraht bis in den Aortenbogen geführt. Anschließend wird das Ostium des linken, dann des rechten Herzkranzgefäßes sondiert und nach Einbringen eines niederosmolaren nicht-ionischen Röntgenkontrastmittels eine Darstellung der Koronarien erzielt. Für die Visualisierung einer Koronararterie genügen üblicherweise 510 ml Kontrastmittel. Im Idealfall wird jedes Segment der Koronarien in zwei senkrecht aufeinander stehenden Projektionen ohne Überlagerung und unverkürzt dargestellt. Die Aufnahme sollte mit 12,5 Bildern/Sekunde erfolgen und wird als Film gespeichert (Hamm et al., 2008). Je nach Fragestellung kann ein LV-Angiogramm, eine Aortographie oder die Beurteilung etwaiger Bypässe in den Untersuchungsgang aufgenommen werden. Die Strahlenbelastung einer diagnostischen oder interventionellen Koronarangiographie sollte ein DFP von 3500 µGy x m2 nicht überschreiten (Bundesamt für Strahlenschutz, 2010). 27 3.3.2 Qualitative Beurteilung von Stenosen Der Schweregrad einer Stenose wird in der Regel anhand einer visuellen Einschätzung durch den Untersucher festgelegt. Hierbei wird der Durchmesser des stenosierten Gefäßabschnitts mit nicht krankhaft veränderten Abschnitten verglichen und in Prozentwerten beziffert. Dieser subjektive Beurteilungsprozess ist in hohem Maße von der Erfahrung des Untersuchers und der optimalen technischen Ausführung der Untersuchung abhängig. So ergeben sich sowohl eine große Bandbreite angiographischer Bewertungen des Schweregrades von Koronarstenosen als auch Schwierigkeiten bei der Einschätzung ihrer hämodynamischen Relevanz. 3.4 Vergleich beider Untersuchungsverfahren Sämtliche in die Arbeit einbezogenen MRT-Untersuchungen erfolgten ambulant im Medizinischen Versorgungszentrum Prof. Dr. Uhlenbrock & Partner im St. Josefs Hospital in Dortmund und wurden von zwei erfahrenen Untersuchern befundet. Die Adenosin-Stress-MRTs aus den Jahren 2004 bis 2011 wurden in Bezug auf Hinweise auf ischämische Minderperfusion überprüft. Weiterhin wurde eruiert, ob sich die Patienten, bei denen sich aufgrund des pathologischen Untersuchungsbefundes der Verdacht auf eine Perfusionsstörung ergeben hat, ebenfalls einer KHK-Diagnostik mittels Herzkatheters unterzogen haben. Bei allen in die Auswertung eingeschlossenen Patienten wurde in zeitlicher Nähe (<180 Tage) zur kardialen Stress-MRT eine Koronarangiographie durchgeführt. Diese Untersuchungen fanden in verschiedenen Krankenhäusern statt. Um einen Vergleich zwischen den Ergebnissen der bei jedem Patienten durchgeführten Stress-MRT und Herzkatheteruntersuchung zu ziehen, wurden die vorliegenden MRTBefunde mit Hilfe des zuvor beschriebenen 17-Segment-Modells der AHA ausgedrückt. Die einzelnen myokardialen Segmente den jeweils für ihre Durchblutung verantwortlichen Koronararterien zuzuweisen, ist trotz der großen Variabilität der epikardialen Gefäßversorgung möglich (Gallik et al., 1995). So können die Segmente 1, 2, 7, 8, 13 und 14 der LAD zugeordnet werden, die Segmente 3, 4, 9, 10 und 15 einer dominanten RCA und die weiteren Segmente 5, 6, 11, 12 und 16 der LCX. Das Segment 17 kann von jeder der Koronararterien perfundiert werden (Cerqueira et al, 2002). In Kenntnis des individuellen Versorgungstyps, der im Rahmen der angiographischen Untersuchung festgelegt worden ist, konnte für jeden in die 28 vorliegende Studie eingehenden Patienten das vorgestellte Segmentmodell angepasst werden. Abbildung 3: Zuordnung der Segmente zu den Versorgungsbezirken der Koronararterien LAD, RCA und LCX (modifiziert nach Cerqueira M. et al., 2002) Im Hinblick auf die Auswertung der Koronarangiographie im Vergleich zur Schnittbilduntersuchung wurde die Definition einer signifikanten Koronarstenose bei einer Lumeneinengung des Gefäßes von >50% festgelegt. Basierend auf den Erkenntnissen von Gould (Gould and Lipscomb, 1974) legen die meisten Studien als unteren Schwellenwert für eine relevante Stenose 50% des Diameters zugrunde. Ab diesem Grad der Stenosierung sind regionale Perfusionsstörungen des Myokards zu erwarten, wobei die Existenz von Kollateralgefäßen berücksichtigt werden sollte (Herold, 2012). Im klinischen Alltag wird der Schwellenwert für eine kritische Stenosierung häufig erst bei >70% gesehen (Pakkal et al., 2011), dem soll mit einer gesonderten Auswertung Rechnung getragen werden. Die im Adenosin-Stress-MRT sichtbar minderperfundierten, Störungen in der Wandbewegung aufweisenden oder durch eine irreguläre Spätanreicherung gekennzeichneten Areale wurden neben den beim selben Patienten visuell erfassten Stenosegraden der Herzkranzgefäße aufgetragen. Anhand dieses Referenzstandards Koronarangiographie wurde die Wertigkeit der Adenosin-Stress-MRT-Untersuchung überprüft. Als richtig diagnostiziert konnte eine im betrachteten Versorgungsgebiet mittels MRT gesehene Minderperfusion, Wandbewegungsstörung oder ein positives Lateenhancement dann gewertet werden, wenn im Zuge der Herzkatheteruntersuchung eine 29 signifikante Stenose oder Re-Stenose im für die Durchblutung verantwortlichen Gefäß nachgewiesen wurde. Die drei Koronararterien LAD, LCX und RCA wurden im Zusammenhang mit den von ihnen jeweils versorgten Myokardsegmenten separat ausgewertet. Eine Untersuchung konnte folglich als richtig positiv gewertet werden, wenn in einem myokardialen Versorgungsbezirk der betrachteten Koronararterie eine Minderperfusion und/oder Wandbewegungsstörung gesehen wurde und im Rahmen der Herzkatheteruntersuchung des Patienten eine signifikante Stenosierung des Herzkranzgefäßes oder eines großen Teilastes vorlag. Als falsch positiv wurde eine im Rahmen der Stress-MRT gesehene kinetische Störung oder Minderperfusion gewertet, wenn diese kein Korrelat in der zugeordneten Koronarangiographie fand. Richtig negativ konnten die untersuchten Gefäßbezirke gewertet werden, in denen durch die Stress-MRT keine Hinweise auf Ischämien gesehen worden waren und die zugehörige Herzkatheteruntersuchung keine signifikante Stenosierung im betrachteten Gefäß aufzeigte. Als falsch negativ ging die Stress-MRT in dem Falle in die Auswertung ein, dass das überprüfte Segment in der Untersuchung keine pathologische Bewegungsstörung oder Minderperfusion aufwies, die Koronarangiographie jedoch eine signifikante Stenosierung oder Re-Stenosierung im Bereich des evaluierten Gefäßes darstellen konnte. Falls im betroffenen Gefäß der Zustand nach Implantation eines Stents gegeben war, wurden verschiedene Konstellationen berücksichtigt. In bestimmten Fällen wurde als weiterer Parameter ein während der MRT-Untersuchung beobachtetes Late-enhancement zugrunde gelegt. Ein gestentetes Gefäß ohne Re-Stenosierung ging als durchgängig in die Auswertung ein, während eine In-Stent-Stenose von >50% als signifikant aufgefasst wurde. Eine weitere Stenose neben einem bereits vorhandenen Stent im betrachteten Gefäß wurde eigenständig betrachtet, stets unter Überprüfung der hämodynamischen Relevanz in Abhängigkeit von Lokalisation, Gefäßdurchmesser und Versorgungstyp. Sofern im Rahmen des Stress-MRTs eine Minderperfusion und / oder kinetische Störung aufgezeigt wurde, der Stent im für das Myokardareal verantwortlichen Herzkranzgefäß jedoch durchgängig war, wurde ein etwaiges Late-enhancement in den Auswertungsprozess miteinbezogen. So zeigt dieses auf, ob die interventionell therapierte Stenosierung bereits ischämische Schädigungen des Myokards nach sich gezogen hat und folgerichtig eine etwaige Pathologie erklärt (Cury et al., 2006). 30 Im Rahmen der meisten MRT-Untersuchungen wurde die Ejektionsfraktion (EF), das linksventrikuläre enddiastolische und endsystolische Volumen, das Schlagvolumen, das Herzzeitvolumen sowie die myokardiale Masse bestimmt. Diese Werte wurden in diese Arbeit als Parameter zur Charakterisierung des Patientengutes einbezogen. 3.5 Statistische Methoden Die Beurteilung der diagnostischen Güte der kardialen MRT-Untersuchungen im Vergleich zum Referenzstandard Koronarangiographie wird mit Hilfe der berechneten Kennzahlen Sensitivität, Spezifität, positiver prädiktiver Wert (PPV) und negativer prädiktiver Wert (NPV) ausgedrückt. Die deskriptiven metrischen Daten sind in Text, Abbildungen und Tabellen als arithmetisches Mittel ±Standardfehler angegeben. In Abbildungen entspricht der Fehlerbalken dabei dem Standardfehler des Mittelwertes (engl.: standard error of the mean), welcher sich folgendermaßen berechnet: S.E.M. = 31 !! ! = ! ! IV Ergebnisse 4.1 Klinische Charakterisierung der Patienten Zur weiteren Charakterisierung des Patientenguts dienen die in 38 von 54 kardialen MRT-Untersuchungen im Rahmen der linksventrikulären Volumetrie ermittelten Werte. Tabelle 2: Klinische Patientencharakterisierung Während der kardialen MRT-Untersuchung erhobene Werte Durchgeführte Volumetrien 38 Ø Ejektionsfraktion (EF) in % 60,6 ±11,4 Ø Enddiastolisches Volumen (EDV) in ml 116,6 ±36,3 Ø Endsystolisches Volumen (ESV) in ml 48,2 ±27,7 Ø Schlagvolumen (SV) in ml 68,8 ±18,1 Ø Herzzeitvolumen (HZV) in l / min 4,71 ±1,24 Ø Myokardiale Masse in g 117,2 ±40,5 4.2 Ergebnisse der koronarangiographischen Untersuchungen Bei der Auswertung der Koronarangiographie als Goldstandard zur Feststellung einer koronaren Herzerkrankung wurde bei 28 Patienten eine Eingefäßerkrankung, bei 12 Patienten eine Zweigefäßerkrankung und bei 3 Patienten eine Dreigefäßerkrankung aufgezeigt. Bei 11 Patienten konnte eine KHK ausgeschlossen werden. Bei einem Patienten war das linke Koronarsystem nicht darstellbar. Die Zuordnung der ermittelten Stenosen zu den Koronararterien wie auch der durchschnittliche Stenosegrad der einzelnen Gefäße oder großer Teiläste lassen sich untenstehender Tabelle entnehmen. 32 Tabelle 3: Ergebnisse Koronarangiographie Balancierter Versorgungstyp 23 Linksversorgungstyp 5 Rechtsversorgungstyp 26 1 – Gefäß – KHK 11 2 – Gefäß – KHK 28 3 – Gefäß – KHK 3 keine KHK 11 Stenosen im Bereich der LCA 28 LCA - Stenosegrad in % 77,9 ±19,7 Stenosen im Bereich der LCX 12 LCX - Stenosegrad in % 80,8 ±21 Stenosen im Bereich der RCA 20 RCA - Stenosegrad in % 71,5 ±21,3 Ø Ø Ø 4.3 Ergebnisse und Wertigkeit der Adenosin-Stress-MRT Während der kardialen MRT-Untersuchungen kam es zu keinerlei Komplikationen. Keine der 54 Untersuchungen musste aufgrund ausgeprägten Blutdruckabfalls, neu aufgetretener Herzrhythmusstörungen, Klaustrophobie, Panikattacken oder weiterer klinisch relevanter Ereignisse abgebrochen werden. Bei einer der Untersuchungen wurde die Adenosin-Infusionszeit wegen einer hierdurch provozierten schweren Angina pectoris auf 60 sec verkürzt. Die Bildqualität war in allen Fällen für eine Analyse ausreichend. Bei einem Patienten konnte aufgrund von Atembewegungsartefakten keine Auswertung der Late-enhancement-Aufnahmen vorgenommen werden. Im Folgenden soll die Wertigkeit der kardialen Stress-Adenosin-MRT-Untersuchung anhand der Ergebnisse für die einzelnen Versorgungsbezirke der Koronararterien aufgezeigt werden. Ein Bezirk setzt sich aus den myokardialen Segmenten zusammen, für die die jeweils betrachtete Koronararterie die Durchblutung gewährleistet. Insgesamt wurden 160 Versorgungsareale ausgewertet. 22 wiesen einen Zustand nach 33 Stentimplantation im für die Perfusion zuständigen Herzkranzgefäß auf, folglich ist bei für 138 Areale verantwortlichen Koronararterien in der Vorgeschichte keine interventionelle Therapie erfolgt. Versorgungsbezirke ohne vorherige Intervention Z.n. Stentimplantation 160 Gesamtzahl ausgewerteter Bezirke 53 43 LAD Stent 54 47 22 10 LAD 53 48 138 7 5 LAD Gesamt LCX LCX Stent LCX Gesamt RCA RCA Stent RCA Gesamt Gesamt Abbildung 4: Ergebnisse: Übersicht über die Gesamtzahl der ausgewerteten Versorgungsbezirke und den verantwortlichen Koronargefäßen 4.3.1 Auswertung der LAD-Versorgungsbezirke Es wurden insgesamt die LAD-Versorgungsbezirke von 53 Patienten ausgewertet. Ein Patient wurde ausgeschlossen, weil das linke Koronarsystem im Rahmen der Herzkatheteruntersuchung nicht dargestellt werden konnte. Bei 24 Patienten wurde die KHK durch die Stress-MRT richtig diagnostiziert (richtig positiv), bei 3 Patienten konnte der pathologische Befund der Stress-MRT im Rahmen der Koronarangiographie nicht bestätigt werden (falsch positiv). Bei weiteren 23 Patienten wurde richtig erkannt, dass keine KHK im Bereich der LAD vorliegt (richtig negativ), bei 3 Patienten wurde die Stress-MRT als unauffällig befundet, während die Herzkatheteruntersuchung eine signifikante Stenose in diesem Bereich aufzeigen konnte (falsch negativ). Aus diesen Ergebnissen ergibt sich für die Sensitivität der Adenosin-Stress-MRT im Hinblick auf das myokardiale Versorgungsareal der LAD ein Wert von 88,9%, für die Spezifität ergibt sich ein Wert von 88,5%. Der positive prädiktive Wert beträgt 88,9%, der negative prädiktive Wert liegt bei 88,5%. 34 LAD: Gesamt 100% 88,9% 88,5% Sensitivität Spezifität 88,9% 88,5% 80% 60% 40% 20% 0% pos. präd. Wert neg. präd. Wert Abbildung 5: Ergebnisse: LAD Gesamt (53 Patienten) Betrachtet man die 43 Personen umfassende Untergruppe an Patienten, bei denen in der Vorgeschichte keine Stentimplantation in der LAD vorgenommen wurde, stellt sich die diagnostische Wertigkeit der Stress-MRT wie folgt dar. Korrekt als krank erkannt wurden 18 Patienten (richtig positiv), fälschlich als krank gewertet wurden 2 Personen (falsch positiv). Eine KHK des zugehörigen Gefäßes wurde in 21 Fällen korrekt ausgeschlossen (richtig negativ) und bei 2 Patienten falsch negativ gewertet. Daraus ergeben sich eine Sensitivität von 90% und eine Spezifität von 91,3%. Der positive prädiktive Wert beträgt 90%, der negative prädiktive Wert 91,3%. LAD ohne vorherige Intervention 100% 90,0% 91,3% Sensitivität Spezifität 90,0% 91,3% 80% 60% 40% 20% 0% pos. präd. Wert neg. präd. Wert Abbildung 6: Ergebnisse: LAD ohne vorherige Intervention (43 Patienten) Im Hinblick auf die Subgruppe von 10 Patienten, bei denen im Rahmen einer früheren Untersuchung ein Stent im Bereich der LAD implantiert wurde, lässt sich die Stress-MRT wie folgt bewerten. Bei 6 Patienten wurde die durch das Stress-MRT aufgezeigte Pathologie auch in der Koronarangiographie nachgewiesen (richtig positiv), 1 Patient 35 wurde fälschlich als krank bewertet (falsch positiv). Die LAD-versorgten Segmente wurden bei 2 Patienten als nicht perfusionsgemindert eingestuft, entsprechend wurde im Rahmen der Herzkatheteruntersuchung keine relevante Stenosierung gesehen (richtig negativ). Bei 1 Patienten war die Schnittbilddiagnostik als unauffällig beurteilt worden, obgleich in der Koronarangiographie eine signifikante Re-Stenosierung der LAD aufgezeigt werden konnte (falsch negativ). So ergibt sich für die Sensitivität bei der Betrachtung dieser Untergruppe ein Wert von 85,7%, für die Spezifität ein Wert von 66,7%. Der positive prädiktive Wert ist 85,7%, der negative prädiktive Wert ist 66,7%. LAD bei Z.n. Stent-Implantation 100% 85,7% 80% 85,7% 66,7% 66,7% 60% 40% 20% 0% Sensitivität Spezifität pos. präd. Wert neg. präd. Wert Abbildung 7: Ergebnisse: LAD bei Z.n. Stent-Implantation (10 Patienten) 4.3.2 Auswertung der LCX Versorgungsbezirke Es wurden bei insgesamt 53 Patienten die Versorgungsbezirke der LCX ausgewertet. Bei der Herzkatheteruntersuchung eines Patienten konnte das linke Koronarsystem nicht dargestellt werden. Bei 9 Patienten wurde die während der Stress-MRT aufgetretene Perfusionsstörung und / oder Wandbewegungsstörung durch eine mittels Herzkatheters nachgewiesene signifikante Stenosierung der LCX oder eines großen Teilasts bestätigt (richtig positiv). Bei 7 Patienten wurde aufgrund der MRT-Untersuchung der Verdacht auf eine durch Stenosierung verursachte Perfusionsstörung geäußert, die nicht durch den koronarangiographisch erhobenen Befund begründet werden konnte (falsch positiv). 36 LCX: Gesamt 100,0% 100% 100,0% 84,1% 80% 56,3% 60% 40% 20% 0% Sensitivität Spezifität pos. präd. Wert neg. präd. Wert Abbildung 8: Ergebnisse: LCX Gesamt (53 Patienten) Bei 37 Patienten deckten sich Stress-MRT und Herzkatheteruntersuchung in der Aussage, dass keine KHK vorliegt (richtig negativ). Bei keiner Untersuchung eines myokardialen Versorgungsareals der LCX war der Fall gegeben, dass eine Stenose vorhanden war, aber das Stress-MRT diesbezüglich keinen Hinweis gegeben hat (falsch negativ). Folglich ergeben sich für die Sensitivität und Spezifität Werte von 100% bzw. 84,1%. Der positive prädiktive Wert liegt bei 56,3%, während der negative prädiktive Wert 100% beträgt. Bei der 48 Patienten umfassenden Subgruppe derer, die vor der Studie keine Intervention im Bereich der LCX erfahren hatten, ergaben sich folgende Ergebnisse. Bei 7 Patienten stimmten Stress-MRT und Koronarangiographie in ihrem Befund überein (richtig positiv), bei 5 Patienten wurde der pathologische Befund der MRT als falsch positiv gewertet, weil im Zuge der Herzkatheteruntersuchung keine signifikante Stenosierung der verantwortlichen Arterie gefunden wurde. Eine KHK wurde bei 36 Patienten mittels der Stress-MRT korrekt ausgeschlossen (richtig negativ), bei keinem Patienten war die Untersuchung falsch negativ zu werten. Es ergeben sich hinsichtlich der diagnostischen Wertigkeit ein Wert von 100% für die Sensitivität, sowie ein Wert von 87,8% für die Spezifität. Der positive prädiktive Wert liegt bei 58,3%, der negative prädiktive Wert bei 100%. 37 LCX ohne vorherige Intervention 100,0% 100% 90% 80% 70% 60% 50% 40% 30% 20% 10% 0% 100,0% 87,8% 58,3% Sensitivität Spezifität pos. präd. Wert neg. präd. Wert Abbildung 9: Ergebnisse: LCX ohne vorherige Intervention (48 Patienten) Die Gruppe Patienten, bei denen der Zustand nach Stentimplantation im Ramus circumflexus der linken Koronararterie gegeben war, umfasste 5 Patienten. Bei 2 Patienten war der Befund der Stress-MRT als richtig positiv zu werten, bei 2 Patienten bestätigte sich dieser nicht, das betrachtete Gefäß erwies sich als durchgängig (falsch positiv). Bei einem Patienten wurde die Durchblutungssituation anhand der Stress-MRT richtig eingeschätzt (richtig positiv). Der Fall einer falsch negativen Stress-MRT ergab sich nicht. Die Sensitivität bei Betrachtung dieser Untergruppe liegt somit bei 100%, die Spezifität bei 33,3%. Der positive prädiktive Wert beträgt 50%, der negative prädiktive Wert 100%. LCX bei Z.n. Stent-Implantation 100,0% 100,0% 100% 80% 60% 50,0% 33,3% 40% 20% 0% Sensitivität Spezifität pos. präd. Wert neg. präd. Wert Abbildung 10: Ergebnisse: LCX bei Z.n. Stent-Implantation (5 Patienten) 38 4.3.3 Auswertung der RCA-Versorgungsbezirke Bei der Auswertung der von der rechten Koronararterie versorgten myokardialen Segmente wurden die Stress-MRTs von 54 Patienten anhand ihrer koronarangiographischen Befunde überprüft. In 18 Fällen wurde der Befund bestätigt (richtig positiv), in 6 Fällen fand die im Rahmen der MRT-Untersuchung aufgefallene Pathologie in der Herzkatheteruntersuchung kein morphologisches Korrelat (falsch positiv). Bei 28 Patienten wurde eine KHK mit Hilfe der Stress-MRT korrekt ausgeschlossen (richtig negativ), bei 2 Patienten zeigte die Koronarangiographie eine signifikante Stenose bei unauffälliger Stress-MRT im zugeordneten Versorgungsbezirk. Daraus ergibt sich hinsichtlich der diagnostischen Wertigkeit ein Wert von 90% für die Sensitivität, für die Spezifität von 82,4%. Der positive prädiktive Wert liegt bei 75%, der negative prädiktive Wert bei 93,3%. RCA: Gesamt 100% 90% 80% 70% 60% 50% 40% 30% 20% 10% 0% 90,0% Sensitivität 93,3% 82,4% Spezifität 75,0% pos. präd. Wert neg. präd. Wert Abbildung 11: Ergebnisse: RCA Gesamt (54 Patienten) In der Subgruppe der 47 Patienten, die vor den in den Vergleich eingehenden Untersuchungen keinerlei interventioneller Therapie unterzogen wurden, ergibt sich aufgrund der Auswertung eine Sensitivität von 92,9% und eine Spezifität von 84,8%. Der positive prädiktiver Wert liegt bei 72,2%, der negative prädiktive Wert beläuft sich auf 96,6%. Bei 13 Patienten wurde eine myokardiale Perfusionsstörung korrekt durch die Stress-MRT nachgewiesen (richtig positiv), bei 5 Patienten konnte der geäußerte Verdacht auf eine Pathologie im Zuge der Herzkatheteruntersuchung nicht bestätigt werden (falsch positiv). Korrekt ausgeschlossen wurde eine KHK im Bereich der rechten Koronararterie bei 28 Patienten (richtig negativ). Falsch negativ war der Befund im Falle eines Patienten. Hier konnte die Koronarangiographie eine relevante Stenose im betrachteten Gefäß aufzeigen. 39 RCA ohne vorherige Intervention 100% 92,9% 96,6% 84,8% 72,2% 80% 60% 40% 20% 0% Sensitivität Spezifität pos. präd. Wert neg. präd. Wert Abbildung 12: Ergebnisse: RCA ohne vorherige Intervention (47 Patienten) Bei Betrachtung der Gruppe von 7 Patienten, bei denen in der Vorgeschichte ein Stent im Bereich der rechten Koronararterie implantiert worden ist, ergibt sich in Bezug auf die diagnostische Wertigkeit eine Sensitivität von 100%. Die Spezifität lässt sich mit einem Wert von 50% beziffern. Der positive prädiktive Wert beträgt 83,3%, der negative prädiktive Wert 100%. Bei 5 Patienten wurde mittels Stress-MRTs eine KHK richtig diagnostiziert (richtig positiv), bei 1 Patienten ergab sich in der koronarangiographischen Untersuchung keine signifikante Stenosierung (falsch positiv). Bei einem Patienten wurde der unauffällige Stress-MRT Befund durch die Katheteruntersuchung bestätigt (richtig negativ). Als falsch negativ wurde kein Befund von Untersuchungen in dieser Subgruppe gewertet. RCA bei Z.n. Stent-Implantation 100,0% 100% 100,0% 83,3% 80% 60% 50,0% 40% 20% 0% Sensitivität Spezifität pos. präd. Wert neg. präd. Wert Abbildung 13: Ergebnisse: RCA bei Z.n. Stent-Implantation (7 Patienten) 40 4.3.4 Diagnostische Wertigkeit der Adenosin-Stress-MRT: Gesamtwerte Nach Auswertung von insgesamt 160 Versorgungsbezirken ergeben sich folgende Gesamtwerte. Die Sensitivität liegt bei Betrachtung aller untersuchten Areale in Zusammenschau mit den zugehörigen Koronararterien bei 91,1%, die Spezifität beträgt 84,6%. Der positive prädiktive Wert liegt bei 76,1%, der negative prädiktive Wert bei 94,6%. Diagnostische Wertigkeit der Stress-MRT: Gesamtwerte 100% 91,1% 90% 94,6% 84,6% 76,1% 80% 70% 60% 50% 40% 30% 20% 10% 0% Sensitivität Spezifität pos. präd. Wert neg. präd. Wert Abbildung 14: Gesamtwerte für Sensitivität, Spezifität, positiven prädiktiven Wert und negativen prädiktiven Wert (160 ausgewertete Versorgungsbezirke) 4.3.5 Zusatzauswertung: Koronarstenosen ≥70% als hämodynamisch relevant eingestuft Die diagnostische Wertigkeit der Adenosin-Stress-MRT im Hinblick auf die in diese Studie eingehenden 160 Versorgungsbezirke wurde zusätzlich unter einem anderen Schwellenwert ausgewertet, ab dem eine Koronarstenose als signifikant eingestuft werden kann. Unter der Hypothese, dass erst ab einer Lumenverengung von ≥70% eine Stenose als hämodynamisch relevant gewertet wird, ergibt sich folgende diagnostische Wertigkeit. Die Sensitivität wird mit 90,7% beziffert, während die Spezifität 76,1% beträgt. Der positive prädiktive Wert ist 58,2%, der negative prädiktive Wert 95,7%. Die Unterschiede zu den im Rahmen der Hauptauswertung ermittelten diagnostischen Kennzahlen soll das unten abgebildete Diagramm veranschaulichen. Im Rahmen dieser wurden koronare Stenosierungen ≥50% als hämodynamisch relevant und somit signifikant gewertet. 41 Diagnostische Wertigkeit im Vergleich 100% 91,1% 90,7% 90% 94,6% 95,7% 84,6% 76,1% 80% 76,1% 70% 58,2% 60% 50% 40% 30% 20% 10% 0% Sensitivität Spezifität pos. präd. Wert Signifikante Stenose: >50% neg. präd. Wert Signifikante Stenose: >70% Abbildung 15: Diagnostische Wertigkeit im Vergleich, basierend auf Hauptauswertung und Nebenauswertung 4.4 Die Late-Enhancement Aufnahme später Gadolinium basierter Aufnahmen in das MRT- Untersuchungsprotokoll konnte bei der Auswertung der 53 Patienten keinen Patienten hinsichtlich einer im Rahmen der Perfusionsaufnahmen nicht aufgefallenen koronaren Herzkrankheit demaskieren. Zu große Atembewegungsartefakte verhinderten bei einem Patienten die Auswertung der Late-Gadolinium-Aufnahmen. Bei 21 Patienten zeigten sich in Form von Kontrastmittelspätanreicherung Hinweise auf einen stattgehabten Myokardinfarkt. Bei 17 Patienten war diese auf einen Infarkt zurückzuführen. Durch die Untersuchung ergab sich ein Informationsgewinn bezüglich der Ausdehnung innerhalb der Myokardwand. Bei 2 Patienten zeigte sich ein LateEnhancement in Kombination mit einer Perfusionsstörung und wurde im Hinblick auf eine unauffällige Koronarangiographie als falsch positiv eingeschätzt. Ein Patient zeigte in seiner MRT-Untersuchung ein grobfleckiges Enhancement als Ausdruck von Ablationsnarben, bei einem weiteren Patienten war die Spätanreicherung in ihrer Charakteristik am ehesten postentzündlich zu werten. 42 V Diskussion 5.1 Einordnung der Ergebnisse In der vorliegenden Arbeit wurde die Wertigkeit einer nicht-invasiven Untersuchungsmethode zur Erkennung und Evaluierung einer KHK mit dem Vergleich von Stress-MRT und dem Goldstandard Koronarangiographie untersucht. Anhand einer visuellen Auswertung ergaben sich in dieser Studie eine Sensitivität von 91,1% und eine Spezifität von 84,6%. Eine 17 Studien zur Wertigkeit der kardialen MRT zur Diagnosestellung einer KHK umfassende Meta-Analyse beziffert im Durchschnitt eine Sensitivität von 84% und eine Spezifität von 83% (Jaarsma et al., 2012). Als nichtinvasive Alternativen bei der Beurteilung myokardialer Perfusion unter vergleichbaren Bewertungsgrundlagen erreichte die SPECT unter pharmakologischem Stress in MetaAnalysen eine Sensitivität von 90% und eine Spezifität von 75-80% (Underwood et al., 2004), während die PET eine Sensitivität von 81% und Spezifität von 87% erzielen konnte (Nandalur et al., 2008). Somit sind die drei Methoden hinsichtlich einer zuverlässigen Diagnostik von Ischämien zweifellos vergleichbar. Ishida et al. untersuchten die Wertigkeit von Stressuntersuchungen mittels SPECT und kardialer MRT und zeigten auf, dass letztere Untersuchungsform enger mit den Befunden der Koronarangiographie korreliert (Ishida et al., 2003). Die Werte für Sensitivität und Spezifität zeigten auch in einer Studie von Sakuma eine Überlegenheit der kardialen MRT (Sakuma et al., 2004). Die MR-IMPACT II-Studie spricht bei der Analyse von 533 Patienten mit einer KHK-Prävalenz von 49% der Stress-MRT eine höhere Sensitivität, aber eine geringere Spezifität im Vergleich zur SPECT zu (Schwitter et al., 2012). Verglichen mit der PET, ist die Stress-MRT in der Identifikation von Perfusionsstörungen als gleichwertig, hinsichtlich des Informationsgewinns über das genaue Ausmaß als überlegen anzusehen (Schwitter et al., 2001). Eine Meta-Analyse aus dem Jahr 2007 bezieht sich auf den Vergleich von Stress-Echokardiographie und StressMRT, jeweils gemessen an der Koronarangiographie. Dabei kam eine Sensitivität von 83% und Spezifität von 86% für die Stress-Echokardiographie unter Gabe von Dipyridamol oder Dobutamin zustande, während für die Perfusionsaufnahmen im Rahmen der Stress-MRT Werte von 91% für die Sensitivität und von 81% für die Spezifität aufgezeigt werden konnten. Die selektive Auswertung der Echokardiographie unter pharmakologischer Belastung nur mit Dobutamin ergab eine höhere Sensitivität von 85% bei unveränderter Spezifität. Die bessere Sensitivität der Stress-MRT im Vergleich zur Stress-Echokardiographie kann dadurch erklärt werden, dass im Rahmen 43 der ischämischen Kaskade zunächst die Perfusion reduziert ist und darauf folgend je nach Schweregrad Wandbewegungsstörungen auftreten (Nesto and Kowalchuk, 1987). Der 64- oder mehrzeiligen computertomographischen Angiographie als Alternative zur invasiven Bildgebung konnte in einer Meta-Analyse von 17 Studien eine Sensitivität von 94,9% und Spezifität von 89,5% im Vergleich zur Koronarangiographie zugeschrieben werden (Paech and Weston, 2011). Unter Beachtung der zuvor dargestellten Ergebnisse anderer Studien kann insgesamt der Schluss gezogen werden, dass die Ergebnisse dieser Studie im Vergleich zu weiteren nicht-invasiven Bildgebungen konkurrenzfähig sind. Allerdings sind in diesem Zusammenhang die Restriktionen der vorliegenden Arbeit anzuführen. Die vorliegende Studie wurde retrospektiv als Vergleich der Befunde von kardialer StressMRT und Koronarangiographie bei 54 Patienten durchgeführt. Der Studie lagen ausschließlich Stress-MRT-Untersuchungen zugrunde, aufgrund derer der Verdacht auf eine Perfusionsstörung geäußert wurde und die Patienten einer Koronarangiographie zugeführt worden sind. Folglich wurde keine Erkenntnis darüber gewonnen, ob die Patienten, deren Stress-MRT als unauffällig befundet worden war und keine Koronarangiographie erhielten, auch tatsächlich gesund waren. Angesichts des ambulanten Rahmens, in dem die in der vorliegenden Studie betrachteten Untersuchungen durchgeführt wurden, war kein follow-up der Patienten mit einer normalen Adenosin-Stress-MRT durchführbar. Falsch negative MRT-Befunde sind im vergleichbaren Zeitraum nicht bekannt geworden. Dieser Umstand muss allerdings unter Berücksichtigung weiterer Studien angezweifelt werden. Die wenigen Veröffentlichungen, die den prognostischen Wert unauffälliger StressAdenosin-MRT-Untersuchungen thematisieren, verfolgen einen Zeitraum von 12 Monaten nach der Untersuchung hinsichtlich des Auftretens schwerwiegender kardiovaskulärer Ereignisse (MACE). Hierzu zählen kardiovaskuläre Sterblichkeit, Myokardinfarkt, Indikation zur Revaskularisierung sowie Hospitalisierung aufgrund eines kardiovaskulären Ereignisses. Bei einem follow-up von 218 Patienten zeigte sich kein Herztod oder Myokardinfarkt bei einem negativen prädiktiven Wert von 99,1% (Pilz et al., 2008). Zu einem ähnlichen Ergebnis kamen Lerakis et al. bei einem durchschnittlich 277 Tage langen follow-up von 89 Patienten, die sich initial mit Brustschmerzen in der Notaufnahme vorgestellt hatten und eine Ischämie elektrokardiographisch und labormedizinisch ausgeschlossen worden war. Die anschließend durchgeführte Stress- 44 MRT hatte einen negativen prädiktiven Wert von 100% (Lerakis et al., 2009). Die sehr gute prognostische Aussagekraft einer unauffälligen MRT wird von einer weiteren Studie bestätigt (Ingkanisorn et al., 2006). Diese Ergebnisse weisen eindeutig daraufhin hin, dass im Rahmen der KHK-Diagnostik ein großes Potential besteht, die hohe Zahl an Herzkatheteruntersuchungen ohne unmittelbare therapeutische Konsequenz zu vermindern. 5.2 Einschränkungen im Hinblick auf die Vergleichbarkeit Die in dieser Studie angestellte Überprüfung der diagnostischen Wertigkeit der StressMRT anhand der Koronarangiographie gestaltet sich durch verschiedene Umstände schwierig. Durch Einbringen des Kontrastmittels in die Herzkranzgefäße kann visuell der Durchmesser einer Stenose bestimmt werden. Die Vergleichbarkeit mit anderen Untersuchungen ist jedoch dadurch eingeschränkt, dass der hämodynamische Einfluss einer epikardialen Gefäßstenose auf die Perfusion nicht immer ihrem angiographisch bestimmten Grade entspricht (Topol and Nissen, 1995). Hinzu kommt, dass die visuelle Beurteilung in hohem Maße abhängig vom Untersucher ist. Stenosen über 60% werden häufig unterschätzt, Stenosen unter 60% des Gefäßdurchmessers werden sowohl unterals auch überschätzt (White et al., 1984). In der vorliegenden Studie wurde eine Stenosierung des Gefäßdiameters über 50% als signifikant angenommen, in einer Nebenauswertung wurde ein Wert von 70% als Schwelle zugrunde gelegt. Hierbei fällt auf, dass in der Nebenauswertung bei unveränderter Sensitivität und negativem prädiktiven Wert die Kennzahlen für Spezifität und positivem prädiktiven Wert schlechter sind. Die Spezifität ist 76,1% im Vergleich zu 84,6%, während der negative prädiktive Wert 58,2% im Vergleich zu 76,1% beträgt. Maßgeblich ist hierbei der höhere Anteil falsch positiver Befunde. So ist festzustellen, dass die überwiegende Zahl an untersuchten Myokardarealen, deren versorgendes Koronargefäß eine mittelgradige Stenosierung von 50-69% aufwies, unter pharmakologischer Belastung eine Perfusionsminderung zeigte. Wurden erst Stenosen von >70% als relevant eingeordnet, fanden diese in der Stress-MRT sichtbaren Perfusionsdefekte definitionsgemäß kein funktionell relevantes Korrelat in der Herzkatheteruntersuchung und mussten als falsch positiv gewertet werden. Auch andere pathophysiologische Bedingungen können eine im MRT sichtbare und typisch für KHK erscheinende Minderperfusion imitieren und zu falsch positiven Ergebnissen führen, da in diesem Falle in der korrespondierenden Koronarangiographie 45 keine Zeichen einer KHK erkennbar sind. So kann eine Verminderung des myokardialen Blutflusses beispielsweise einer linksventrikulären Hypertrophie bei Hypertonus oder einer Beteiligung der Endstromgebiete bei Diabetes mellitus geschuldet sein (Kelle et al., 2006). Patienten mit sogenanntem Syndrom X leiden unter dem Auftreten von Angina pectoris trotz eines unauffälligen Status ihrer Koronararterien. Bei diesen Patienten konnte mit Hilfe der kardialen MRT eine Verminderung der subendokardialen Perfusionsreserve aufgezeigt werden und eine ischämische Ursache der Beschwerden diskutiert werden (Panting et al., 2002). Entscheidend war hierbei dank der besseren transmuralen Auflösung der kardialen MRT im Vergleich zu anderen Techniken die gesonderte Betrachtung subepikardialer und subendokardialer Ischämien. Auch das zur Feststellung von Infarktarealen probate myokardiale Late-enhancement des gadoliniumhaltigen Kontrastmittels kann im Rahmen anderer Erkrankungen auftreten, beispielsweise bei dilatativer Kardiomyopathie, hypertrophischer Kardiomyopathie und entzündlichen oder infiltrativen myokardialen Erkrankungen (Vöhringer et al., 2007). Somit bereiten vor allem Erkrankungen, die ein ähnliches Erscheinungsbild wie eine KHK in der Stress-MRT-Bildgebung aufweisen, wie auch die subjektive Einschätzung von Stenosen im Rahmen der Koronarangiographie, Schwierigkeiten beim Vergleich der beiden Untersuchungsverfahren im Hinblick auf die KHK. Dies kann zur Folge haben, dass aufgrund falsch positiver Befunde die Leistung der Perfusionsuntersuchung unterbewertet wird. Falsch positiv wurden in dieser Studie 16 myokardiale Versorgungsbezirke beurteilt. In 12 Fällen wurde bei den betroffenen Patienten keine KHK festgestellt, in einem Fall hatte der Patient eine 1-Gefäß-Erkrankung, in 3 Fällen eine 2-Gefäß-Erkrankung. Die Konstellation, dass die Perfusionsuntersuchung unter Stress als unauffällig gewertet wurde, die Koronarangiographie jedoch eine signifikante Stenose aufzeigte, ist gleichbedeutend mit einem falsch negativen Ergebnis. Bei den Erklärungsansätzen für diese Situation ist neben der fraglichen hämodynamischen Relevanz der festgestellten Stenosierung des Koronargefäßes in besonderem Maße eine etwaige Kollateralenbildung von Interesse. Bei Patienten mit chronischer KHK können weite Teile des Stromgebietes eines verengten Herzkranzgefäßes durch Kollateralgefäße versorgt werden und damit die durch die Stenose verminderte Durchblutung bis zu einem gewissen Grad kompensieren. Die Anflutung eines Kontrastmittels in der Perfusionsuntersuchung kann im Vergleich zum normalen Myokard verspätet sein (Jerosch-Herold et al., 2004). Die Perfusion ist 46 jedoch im Falle einer ausgeprägten Kollateralenbildung in einem geringeren Maße vermindert als es der Stenosegrad der versorgenden Koronararterie vermuten ließe und kann dadurch zu falsch negativen Ergebnissen führen (Muehling et al., 2007). Probleme bereitet bei den gegenwärtig zur Verfügung stehenden Untersuchungen besonders die Erkennung der kleinen Kollateralgefäße, so dass sowohl ihr Vorhandensein als auch ihre hämodynamische Bedeutung durchweg unterschätzt werden (Tayebjee et al., 2004). Der Anteil falsch positiver Befunde bei der Adenosin-Stress-MRT-Untersuchung ist im Hinblick auf weitere Entwicklungen der Untersuchungsmethode ein bedeutsamer Ansatzpunkt. Im Entscheidungsprozess innerhalb der KHK-Diagnostik ist es dahingehend von Relevanz, dass bei einem Verdacht auf Minderperfusion in einem oder mehreren Myokardarealen in der überwiegenden Zahl der Fälle zur weiteren Abklärung und möglichen Therapie eine Koronarangiographie die logische Folge ist. Erst diese führt in dieser Konstellation zum Ausschluss der KHK, weist aber aufgrund ihrer Invasivität bestimmte Risiken auf. Von größerer Bedeutung für den einzelnen Patienten ist zweifellos der seltene Fall einer falsch negativen Untersuchung. Angesichts des hohen negativen prädiktiven Wertes der Stress-MRT wird nach einer fälschlich unauffälligen Untersuchung eine invasive Abklärung mit hoher Wahrscheinlichkeit zunächst zurückgestellt und erst bei Beschwerdepersistenz und damit verbundenem zeitlichen Verzug durchgeführt. In der vorliegenden Studie wurden 5 Versorgungsbezirke falsch negativ bewertet. In 4 Fällen zeigte die Stress-MRT jedoch Perfusionsstörungen in einem anderen Versorgungsbezirk auf, so dass ohnehin eine invasive Abklärung angeraten wurde. Neben dieser Problematik sind auch Unzulänglichkeiten des beim Vergleich der beiden Untersuchungsverfahren zum Einsatz kommenden 17-Segment-Modells zu benennen. So findet dieses von der American Heart Association empfohlene Modell im klinischen Alltag weite Verbreitung, berücksichtigt allerdings nicht die patientenspezifischen Unterschiede in der Anatomie der Koronararterien. Abgesehen vom Segment 17 (Apex) wird jedes myokardiale Segment einer bestimmten Koronararterie zugeschrieben. Eine nuklearmedizinische Perfusionsstudie mittels SPECT zu diesem Thema gelangt allerdings zu der Erkenntnis, dass lediglich 9 der 16 Segmente weitestgehend konstant von einem bestimmten Koronargefäß versorgt werden und die übrigen Segmente hinsichtlich ihrer Versorgung einer großen Variabilität unterliegen (Pereztol-Valdés et al., 2005). Eine auf kontrastmittelbasierter Bildgebung mittels Kardio-MRT aufbauende Studie schreibt der 47 LAD sogar nur 4 Segmente spezifisch zu, während der LCX und RCA kein Segment generell zuzurechnen ist. Gerade im Bereich apikaler und mitt-anterolateraler Segmente sei das Versorgungsgebiet der LAD deutlich größer einzuschätzen als im von der AHA propagierten 17-Segment-Modell vorgesehen (Ortiz-Pérez et al., 2008). Besonders in den Randgebieten der im 17-Segment-Modell der AHA aufgezeigten Versorgungsbezirke scheint eine deutliche Variabilität hinsichtlich des perfundierenden Koronargefäßes zu bestehen. Wünschenswert ist folglich ein Bewertungsmodell, das den individuellen Versorgungstyp berücksichtigt. Einen Ansatz stellt die patientenspezifische Kartierung der epikardialen Koronargefäße mit Hilfe eines in die Untersuchung integrierten Scans des gesamten Herzens dar, welcher nach Umsetzung in ein Voronoi-Diagramm ein dem Verlauf der Herzkranzgefäße angepasstes 17-Segment-Modell liefern soll (Termeer et al., 2010). Bei der vorliegenden Studie konnte der im Rahmen der Koronarangiographie ermittelte Versorgungstyp des jeweils betrachteten Patienten in die Auswertung einbezogen werden. 5.3 Vor- und Nachteile der Stress-MRT-Untersuchung und weiterer nicht-invasiver Techniken Im Vergleich zu anderen nicht-invasiven Untersuchungen liegen Vorzüge der StressMRT in der sehr guten diagnostischen Wertigkeit der Perfusionsdarstellung. Perfusionsdefekte mit einem großen transmuralen Ausmaß in Folge höhergradiger, proximal lokalisierter Stenosierungen werden praktisch ausnahmslos erkannt. Dank der deutlich höheren räumlichen Auflösung der kardialen MRT im Vergleich zu den nuklearmedizinischen Techniken (Wagner et al., 2003) gelingt auch die Unterscheidung zwischen subendokardialen und transmuralen Infarkten. Schwierigkeiten können allerdings bei mittelgradigen Stenosierungen auftreten, welche lediglich kleine subendokardiale Defekte bzw. diskrete Helligkeitsunterschiede zur Folge haben. In diesem Falle kann die Durchmusterung von Einzelbildern mit unterschiedlicher Fensterung sinnvoll sein (Merkle und Bernhardt, 2009). Als weiteres Verfahren bietet die CT-Angiographie in der Erkennung und Einschätzung der Schwere einer KHK eine sehr gute Genauigkeit (Miller et al., 2008). Eine höhergradige Kalzifikation der Koronararterien kann jedoch zur Überschätzung etwaiger Stenosierungen führen und stellt einen limitierenden Faktor für die Untersuchungsmethode dar (Taylor et al., 2010). Dank des höchsten negativen prädiktiven Wertes aller nicht-invasiven Techniken (99%) vermag die CT-Angiographie 48 eine obstruktive KHK mit hoher Wahrscheinlichkeit auszuschließen (Budoff et al., 2008). Allerdings bietet diese nicht-invasive anatomische Bildgebung keine Informationen über die funktionelle Signifikanz der koronaren Atherosklerose in Form von regionalen myokardialen Ischämien, so dass eine Kombination mit einer Perfusionsbildgebung anzustreben ist. Aufgrund der hohen räumlichen Auflösung und dem Fehlen ionisierender Strahlung könnte sich die kardiale MRT im Vergleich zu nuklearmedizinischen Techniken als geeigneter Partner der CT für eine kombinierte nicht-invasive anatomische und funktionelle Bildgebung empfehlen (van Werkhoven et al., 2010). Aufgrund ihrer relativ geringen Sensitivität von 72% eignet sich hingegen die MRAngiographie gegenwärtig nur als Ergänzung einer kardialen MRT-Untersuchung (Schuijf et al., 2006). Im Vergleich bietet die Angiographie mittels CT eine bessere Verfügbarkeit, höhere räumliche Auflösung und kürzere Untersuchungszeiten, während die MRAngiographie über den Vorteil der fehlenden Strahlenbelastung und eines nichtjodhaltigen Kontrastmittels verfügt (Bluemke et al., 2008). Bei Vorhofflimmern oder anderen Arrhythmien sind beide Verfahren derzeit nicht zu empfehlen, überdies kann auch ein hoher BMI zu einer schlechteren Bildqualität führen. Gegenwärtig wird der Stellenwert der CT-Angiographie in Kombination mit einer CTPerfusionsuntersuchung untersucht und kann im Vergleich zur SPECT konkurrenzfähige Ergebnisse vorweisen. Beispielsweise bei der Abklärung unklarer Brustschmerzen in der Notaufnahme wäre eine einzige Untersuchung mit vergleichsweise kurzer Untersuchungszeit wünschenswert. Die Bildgebung mittels CT könnte dies mit der komplementären Darstellung von Herzkranzgefäßen und myokardialer Perfusion ermöglichen (Feuchtner et al., 2012). Eine 30 Patienten umfassende Studie widmete sich der Untersuchung des diagnostischen Wertes der myokardialen Perfusionsbildgebung mittels eines 128-Zeilen-Dual-Source-CT in Ruhe und unter pharmakologischer Belastung (Adenosin). Dabei konnte eine gute diagnostische Genauigkeit im Vergleich zum Referenzstandard kardialer MRT und invasiver Koronarangiographie festgestellt werden, bei einer angegebenen Strahlungsbelastung von lediglich 2,5 mSv (Feuchtner et al. 2011). Schwierigkeiten bei der Identifizierung von relativen Perfusionsunterschieden bei Mehrgefäßerkrankungen oder Hauptstammstenosen trüben das Bild von der Genauigkeit der nicht-invasiven Bildgebung. So kann vor allem eine balancierte Ischämie Probleme 49 bei der Erkennung von Perfusionsstörungen bereiten, da sich die visuelle Auswertung auf relative Helligkeitsunterschiede stützt. Eine ausgedehnte myokardiale Ischämie kann somit der Wahrnehmung entgehen, da die Techniken präferiert das Areal mit der größten Ausprägung einer Ischämie identifizieren (Melikian et al., 2010). Bei ansonsten vergleichbaren Ergebnissen schneidet die Stress-MRT in der Diagnostik von Mehrgefäßerkrankungen im Vergleich zur SPECT besser ab (Schwitter et al., 2008). Eine Studie untersuchte die Erkennung von Perfusionsstörungen mittels SPECT bei Hauptstammstenosen und kam zu dem Ergebnis, dass 13-15% der Patienten aufgrund einer vermutlich balancierten Ischämie eine normale Perfusion zugeschrieben worden ist (Berman et al., 2007). Ein Vergleich der beiden zur Verfügung stehenden nuklearmedizinischen Techniken zeigt in vielen Punkten eine Überlegenheit der PET gegenüber der SPECT. So weist die PET eine höhere diagnostische Genauigkeit bei Stenosen >50% auf (87% gegenüber 71%), zudem sind weniger Attenuationsartefakte zu beklagen, was sich positiv auf die Bildqualität auswirkt (Bateman et al., 2006). Dadurch, dass die PET eine Darstellung des myokardialen Blutflusses in absoluten Werten aufzeigen kann, nimmt die Methode eine Sonderstellung ein. Gerade im Hinblick auf eine Evaluierung der Mikrozirkulation ist dies von Bedeutung (Camici and Rimoldi, 2009). Trotz der anerkannten Vorteile gegenüber der SPECT wird die PET seltener durchgeführt, was auf eine geringere Verbreitung der Geräte und höhere Kosten zurückzuführen ist (Nandalur et al., 2008). Die myokardiale Viabilität kann mittels 18 Fluor-Deoxyglucose-PET in einigen Fällen besser beurteilt werden als mittels kardialer MRT, während letztere vergleichsweise mehr kleine Infarktareale identifizieren kann (Wu et al., 2006). Die bei der SPECT relativ häufig auftretenden Attenuationsartefakte zeigen sich in der MRT nicht (Wagner et al., 2003), jedoch ist auch bei der diagnostischen Beurteilung von MRT-Aufnahmen das mögliche Auftreten von Artefakten zu berücksichtigen. Diese führen zu einer schlechteren Bildqualität und entstehen unter anderem durch Bewegung, an Grenzflächen von Geweben mit unterschiedlichen magnetischen Eigenschaften oder durch chemische Verschiebung der Protonen. Von besonderer Bedeutung sind die sogenannten Suszeptibilitätsartefakte. Diese erscheinen als sehr dunkle, subendokardiale Streifen und können in der Perfusionsbildgebung wie eine Ischämie imponieren. Technische Maßnahmen können Artefakte bis zu einem gewissen Grad kompensieren, in Bezug auf Bewegungsartefakte ist jedoch die Compliance des untersuchten Patienten in der Umsetzung der Atemanhaltetechnik ein entscheidender Faktor. Vor allem die 50 Einhaltung der Atemkommandos kann neben der relativ langen Untersuchungszeit bei unruhigen Patienten zu Problemen führen. Der Einsatz gadoliniumhaltigen Kontrastmittels bei den Spätaufnahmen der kardialen MRT bringt einen großen Informationsgewinn bezüglich der Erfolgsaussichten einer perkutanen Koronarintervention mit sich. Bei Patienten mit abgelaufenem Myokardinfarkt kann die kontrastmittelbasierte MRT die Größe und das transmurale Ausmaß des Infarktes bemessen und im akuten Stadium nach Revaskularisierung frühzeitig das reperfundierte Myokardareal identifizieren. Dies ist mit einem hohen prognostischen Wert für klinischen Verlauf und Ergebnis verbunden (Merten et al., 2008). Trotz der erfolgreichen Rekanalisation einer für einen Infarkt verantwortlichen Arterie kann die Durchblutung des betroffenen Myokards bei bis zu 30% der Patienten nicht wieder hergestellt werden. Dafür wird eine mikrovaskuläre Obstruktion verantwortlich gemacht, die im Rahmen der Perfusionsbildgebung erkennbar ist (Nijveldt et al., 2008). Die Kombination von Adenosin-Stress-MRT und delayed-enhancement-Aufnahmen erlaubt eine prognostische Beurteilung einer möglichen KHK. Bei einer 908 Patienten umfassenden Studie, die sich aus klinischer Indikation einer Stress-MRT unterzogen haben, zeigten sich in einem follow-up über 2,6±1,2 Jahre insgesamt 101 kardiale Ereignisse (Tod, Myokardinfarkt oder späte Revaskularisation). Im Falle einer unauffälligen Untersuchung betrug die Jahreswahrscheinlichkeit für ein kardiales Ereignis 2,4% (Tod oder Myokardinfarkt <1%), eine pathologische Untersuchung war mit Werten von 5,6-7,0% assoziiert (Bingham and Hachamovitch, 2011). Vor der Gabe Nierenfunktion von der gadoliniumhaltigem Patienten überprüft Kontrastmittel werden. sollte Bei allerdings einer die schweren Nierenfunktionsstörung mit einer GFR <30 ml / min / 1,73 m2 besteht die Gefahr, dass aufgrund der langsamen Ausscheidung des Kontrastmittels die Gadoliniumchelate dissoziieren und toxisches Gadolinium frei wird. Verschiedene Studien weisen darauf hin, dass ein Zusammenhang zum Auftreten einer nephrogenen systemischen Fibrose (NSF) besteht. Aufgrund der unterschiedlichen chemischen Eigenschaften der Kontrastmittel erfolgte eine gewisse Risikoabstufung. So wird dem bei der vorliegenden Studie zum Einsatz gekommenen Gadovist® aufgrund der zyklischen Struktur nur ein geringes Risiko zur Entstehung einer NSF zugeschrieben (Thomson et al., 2012). Die Koronarangiographie nimmt aufgrund der unmittelbaren Therapiemöglichkeit einer 51 vorliegenden Gefäßläsion eine Sonderstellung ein, stellt aber auch weiterhin den Goldstandard zur Diagnose einer KHK dar (Cerci et al., 2012). Allerdings ist es schwierig, allein auf der Basis des koronarangiographischen Befundes eine klinische Entscheidung zu treffen, vor allem bei mittelgradigen Stenosen, die 50-70% des Gefäßdiameters verlegen (Fischer et al., 2002). Die FAME-Studie zeigt, dass eine Bestimmung der fraktionellen Flussreserve als Hinweis auf die tatsächliche funktionelle Signifikanz einer Gefäßverengung die Rate schwerwiegender kardialer Ereignisse (MACE) im Verlauf signifikant reduzieren kann. Von den 50-70% des Gefäßdiameters einnehmenden Stenosierungen wurden 35% als funktionell relevant eingeschätzt, bezüglich der 71-90% des Gefäßdiameters umfassenden Stenosierungen lag der Wert bei 80%. Die Koronarangiographie ist bei Patienten mit Mehrgefäßerkrankungen folglich eine inadäquate Methode zur Erfassung ihrer hämodynamischen Relevanz (Tonino et al., 2010). Aus diesem Grund ist es sinnvoll, die angiographischen Erkenntnisse in Relation zu anderen Befunden zu werten, die auf eine myokardiale Ischämie hinweisen. Auch weitere Autoren stellen hervor, dass eine invasive Behandlung von Stenosen ohne einen Hinweis auf durch sie verursachte Ischämien weder den klinischen Verlauf noch anginöse Beschwerden bessere. Die gängige Praxis, dass mittlere Stenosen bei Vorliegen einer hochgradigen Stenose an anderer Stelle ebenfalls behandelt werden, folge keiner Evidenz (Pijls et al., 2007). Die Ergebnisse der Studien weisen darauf hin, dass bei einer vorgeschalteten nicht-invasiven Diagnostik mit Augenmerk auf stress-induzierte Ischämien die Risiken durch eine invasive Untersuchung vermieden werden könnten. Der hohe negative prädiktive Wert dieser Techniken unterstützt ein solches Vorgehen. Generell erscheint ein primäres nicht-invasives Vorgehen vor allem bei Patienten mit einer geringen Vortestwahrscheinlichkeit für das Vorliegen einer KHK ratsam, gerade angesichts der hohen Zahl an diagnostischen Herzkatheteruntersuchungen ohne unmittelbare therapeutische Konsequenz (van Buuren, 2010). Ein bedeutender Nachteil der Koronarangiographie, der Computertomographie wie auch der nuklearmedizinischen Untersuchungstechniken SPECT und PET gegenüber der Magnetresonanztomographie ist der Einsatz ionisierender Strahlung. Die Strahlenbelastung, der ein Patient im Verlauf einer koronaren CT-Untersuchung durchschnittlich ausgesetzt wird, beträgt 7,4 mSv, während der Vergleichswert einer SPECT-Untersuchung 13,3 mSv beträgt (Min et al., 2012). Eine andere Studie spricht von einer durchschnittlichen effektiven Dosis von 22 mSv bei der CT-Angiographie (Smith-Bindman et al., 2009). Mit 13,8 mSv wird im Jahre 2007 die Strahlenbelastung bei der PET-CT-Untersuchung angegeben 52 (Sampson et al., 2007), aktuelle Veröffentlichungen beziffern die Belastung eines PET-CT mit 3,51-10,54 mSv deutlich niedriger (Dorbala et al., 2013). Die Bestimmung des koronaren Calcium-Scores bringt eine Strahlungseinwirkung von 1-3 mSv mit sich. Als diagnostische Untersuchung wird die invasive Koronarangiographie mit einer durchschnittlichen effektiven Dosis von 7 mSv angegeben, als perkutane koronare Intervention beträgt die Dosis 15 mSv (Gerber et al., 2009). Die hohe diagnostische Aussagekraft, gepaart mit einer immer höheren Verfügbarkeit von Computertomographen, führt zu einer steigenden durchschnittlichen Strahlungsbelastung der Gesamtbevölkerung (Mettler et al., 2008). Für den einzelnen Patienten bedeutet dies, dass sowohl indirekt, durch Entstehung von mit der DNA interagierenden Radikalen, wie auch direkt durch Induktion von Punktmutationen, chromosomalen Translokationen und Genfusionen eine karzinogene Veränderung durch die Röntgenstrahlung zustande kommen kann (Brenner and Hall, 2007). Aufgrund der nicht vorhandenen Belastung durch ionisierende Strahlung nimmt die Stress-MRT in der Schnittbilddiagnostik des Herzens eine Ausnahmestellung ein. Einen vergleichbar hohen Informationsgewinn über die kardiale Funktion ohne eine damit verbundene Strahlenbelastung kann neben der MRT lediglich die Echokardiographie vorweisen. 5.4 Besonderheiten einer ambulanten Studie Die Möglichkeiten der nicht-invasiven diagnostischen Möglichkeiten sind gerade für den ambulanten Rahmen von großem Interesse. Stationäre Patienten im Krankenhaus sind im Kollektiv kränker als Vortestwahrscheinlichkeit ambulante für das Patienten Vorliegen und einer haben KHK. eine Hier höhere steht die Koronarangiographie im Mittelpunkt der kardiologischen Diagnostik und ist bei diesem Patientenklientel auch häufiger indiziert. In Anbetracht der lediglich bei einem Anteil von 35,95% aller Untersuchungen durchgeführten Koronarintervention sollte die Indikation jedoch sorgfältig gestellt werden und weniger invasive Alternativen zukünftig mehr Berücksichtigung finden (van Buuren, 2010). Im ambulanten Bereich ist bei den in ihrer Gesamtheit gesünderen Patienten auch im Sinne einer Risiko-Nutzen-Abwägung zu entscheiden. Hierbei gilt es, vor allem bei dem Patientenklientel mit einer mittleren Vortestwahrscheinlichkeit zwischen 10% und 90% für das Vorliegen einer chronischen KHK, das große Spektrum der nicht-invasiven Möglichkeiten zu bedenken, auch im Hinblick auf die Limitationen der Belastungs-EKGUntersuchung (Maffei et al, 2010). Dieser ist trotz der Einschränkungen bei sorgfältiger 53 Auswertung ein bedeutender diagnostischer und prognostischer Wert zuzuschreiben (Kligfield and Lauer, 2006), so dass die auch im hausärztlichen Bereich vielerorts verfügbare Untersuchung weiterhin ihren Stellenwert besitzt, insbesondere als Basisuntersuchung an einem für den Patienten vertrauten Ort. In den aktuellen für Deutschland verfassten Leitlinien finden verschiedene Untersuchungsmöglichkeiten Versorgungsleitlinie noch Chronische keine KHK, Berücksichtigung 2012). Auch wird (Nationale hinsichtlich der Verfahrensweise lediglich bei einer niedrigen (<10%) oder einer hohen (>90%) Vortestwahrscheinlichkeit für das Vorliegen einer KHK eindeutig Stellung bezogen. Es erscheint sinnvoll, die Patientengruppe mit einer mittleren Vortestwahrscheinlichkeit weiter zu unterteilen, um das bevorzugte Verfahren für den jeweiligen Patienten herauszufinden. Die Gruppe der Patienten mit einer Vortestwahrscheinlichkeit von 1029% gilt es von denen mit einer von 30-60% zu unterscheiden, ferner wären die Patienten mit einem höheren Risiko von 61-90% abzugrenzen. Bei ersterer Patientengruppe könnte im Falle eines typischen oder atypischen pectanginösen Schmerzes zunächst ein CT-Scan zur Bestimmung des Calcium-Scores erfolgen und im Falle eines Scores von 0 auf die mit einer Angiographie verbundene weitere Strahlenbelastung verzichtet werden. Die Bestimmung ist aufgrund ihrer geringen Spezifität bei höhergradigen Stenosen nicht in die deutschen Leitlinien eingebunden. Von Bedeutung könnte diese Untersuchung auch für asymptomatische Patienten sein, die ein 10-20%iges Risiko für ein koronares Ereignis in den nächsten 10 Jahren aufweisen (Greenland et al., 2010). Diese Idee beruht darauf, dass ein - bisher verborgener erhöhter Calcium-Score zur früheren Einleitung einer beispielsweise cholesterinsenkenden Arzneimitteltherapie und damit einer Prognoseverbesserung führen könnte. Bei einer Vortestwahrscheinlichkeit von 30-60% besitzen funktionelle Bildgebungen einen hohen Stellenwert. So könnte die myokardiale Perfusion beispielsweise mittels SPECT oder Adenosin-Stress-MRT evaluiert werden. Unter Berücksichtigung der Kontraindikationen und Einschränkungen der Untersuchungen sollte auch der Patientenwunsch bedacht werden, ebenso die lokale Verfügbarkeit und Erfahrung mit der Untersuchungsmodalität (Skinner et al., 2010). Die nicht-invasiven funktionellen Untersuchungen könnten auch bei den Patienten, die eine hohe Wahrscheinlichkeit für das Vorliegen einer KHK besitzen, aber bisher eine invasive Diagnostik verweigern, die Bereitschaft zur Koronarangiographie steigern. Der Untergruppe von Patienten mit einer Vortestwahrscheinlichkeit von 61-90% für das 54 Vorliegen einer KHK wird in Großbritannien der NICE angina guideline folgend bei pectanginösen Beschwerden eine Koronarangiographie als Untersuchung erster Wahl angeboten. Voraussetzung dafür ist, dass eine Revaskularisation in Betracht gezogen wird, die Untersuchung dem jeweiligen Patienten zumutbar und der klinischen Gesamtsituation angemessen ist (Timmis et al., 2011). Sind diese Bedingungen nicht erfüllt, sollte der Patient einer nicht-invasiven Ischämiediagnostik zugeführt werden. 5.5 Ausblick Hinsichtlich der nicht-invasiven Diagnostik der KHK sind weiter bedeutsame Entwicklungen zu erwarten. So scheint sich auf Seiten der pharmakologischen Belastung der Wirkstoff Regadenoson (Lexiscan®) als Alternative zu Adenosin mit dessen bekannten Nebenwirkungen zunehmend zu etablieren. Es handelt sich hierbei um einen selektiven A2A-Rezeptor-Agonisten, der nur geringe Effekte auf systemischen Blutdruck, bronchiale Muskulatur und atrioventrikuläre Überleitung ausübt. Aufgrund der erst relativ kurze Zeit zurückliegenden Markteinführung von Regadenoson gibt es noch keine prognostischen Daten, Erfahrungswerte mehren sich jedoch aufgrund des zunehmenden klinischen Einsatzes (Palani and Ananthasubramaniam, 2012). Bisher zeigten sich vor allem Dyspnoe, Kopfschmerzen und Flush als häufigste Nebenwirkungen, seltener atrioventrikuläre Blockbilder. Empfehlenswert erscheint der Einsatz für Patienten mit obstruktiven Lungenerkrankungen oder moderaten reaktiven Atemwegserkrankungen, bei denen von einer Gabe von Adenosin abgeraten wird (Bengalorkar et al., 2012). Ein großer Fortschritt ist hinsichtlich der Darstellung atherosklerotischer Plaques zu erwarten. Der intravaskuläre Ultraschall ist in der Lage, bestimmte Arten von Plaques darzustellen (Rieber et al., 2006) und auch die PET kann mit Hilfe spezifischer Tracer die Entzündungsaktivität der Plaques visualisieren (Camici and Rimoldi, 2009). Im Gegensatz zur SPECT verspricht die PET somit nicht nur durch die Erfassung von Gefäßverengungen sondern auch durch die Charakterisierung atherosklerotischer Entzündungsaktivität mittels 18 Fluor-Deoxyglucose wertvolle Informationen zu liefern (Tawakol et al., 2006). Bei der Bildgebung mittels Hybrid-PET/MR werden bisher eigenständige Untersuchungsmethoden kombiniert, ihre klinische Relevanz ist allerdings noch zu überprüfen (Nensa et al., 2013). Derzeit vermag allerdings keine Technik zuverlässige Informationen über die genaue Wandbeschaffenheit von Koronargefäßen geben. Die bessere Einschätzung von Gefäßplaques könnte der Risikoabschätzung zugute kommen und eventuell zu einer früheren sekundärpräventiven konservativen oder 55 interventionellen Therapie führen. Von Interesse ist eine höherwertige Darstellung der Gefäßwand, weil es in der Frühphase der Plaqueentstehung zu einem atherosklerotischen Wachstum nach außen ohne eine relevante Einengung des Gefäßlumens kommt (Glagov et al., 1988). Dieses Phänomen des positiven Remodelings wird auch Glagov-Effekt genannt. Ein Drittel aller Myokardinfarkte kommt durch die Ruptur eines nicht stenosierenden Plaques zustande. Dabei hängt das Risiko einer Plaqueruptur mehr von Zusammensetzung und Verletzlichkeit der Plaque als vom Grad seiner stenosierenden Wirkung ab (Falk et al., 1995). Als instabile Plaques bezeichnet man diejenigen mit lipidreichem Kern und einer dünnen fibrösen Membran, die häufig keine relevante Stenose produzieren. Da die Koronarangiographie nur das Gefäßlumen darzustellen weiß, sind hier die nichtinvasiven bildgebenden Verfahren von Interesse. Eine herausragende Rolle könnten in der Hinsicht die MR- und CT-Angiographie einnehmen. Die MR-Angiographie bietet die Möglichkeit zur Darstellung der koronararteriellen Gefäßwand und deren Morphologie, ist jedoch durch den geringen Durchmesser der Gefäße, Herzbewegungs- und Atmungsartefakte und ein ungenügendes Signal-Rausch-Verhältnis eingeschränkt. Die dreidimensionale Darstellung des Herzens bzw. des Herzkranzgefäßbaums sollte grundsätzlich anhand der Evaluierung der Wanddicke auch subklinische Erkrankunge identifizieren können (Kim et al., 2002). Eine weitere Verbesserung könnte der Einsatz von Kontrastmitteln erzielen, die durch ihre T1 Relaxivität die Signalintensität steigern und durch eine reversible Albuminbindung länger als bisher verwandte Kontrastmittel im Gefäßsystem verbleiben (Kelle et al., 2007). Kernspintomographen mit einer Magnetfeldstärke von 3 Tesla finden immer größere klinische Verbreitung und bieten gegenüber 1,5 Tesla eine höhere räumliche Auflösung und ein günstigeres Signal-Rausch-Verhältnis und könnten folglich eine bessere Darstellung atherosklerotischer Plaques ermöglichen. Auch die Perfusionsbildgebung könnte hinsichtlich der diagnostischen Wertigkeit von einer höheren Feldstärke profitieren (Ebersberger et al., 2011). Abgesehen von den genannten Vorteilen bietet eine Verwendung von 3 Tesla auch Nachteile wie ausgeprägtere Suszeptibilitätsartefakte und wesentlich stärkere Inhomogenitäten im Magnetfeld. Bei stetig zunehmenden Erfahrungswerten und zahlreichen Optimierungsmöglichkeiten hinsichtlich der Untersuchungsprotokolle bietet diese neue Untersuchungstechnik vielversprechende Aussichten (Oshinski et al., 2010). 56 Die CT-Angiographie kann dank der sehr guten räumlichen Auflösung einen sehr guten diagnostischen Wert vorweisen (Paech and Weston, 2011) und bietet eine relativ kurze Untersuchungszeit, birgt jedoch als Nachteil eine bedeutsame Strahlungsbelastung für den Patienten und Artefaktanfälligkeit bei stark calcifizierten Koronararterien oder Stentimplantationen. Neuere technologische Entwicklungen könnten hier Abhilfe schaffen. Eine prospektive EKG-Triggerung in Verbindung mit einer high-pitch-spiral Bildaquisition vermag bei weiterhin sehr guten diagnostischen Ergebnissen die Strahlenbelastung um ein Vielfaches zu senken (Kröpil et al., 2012). Iterative Rekonstruktionen ermöglichen neben einer signifikanten Senkung der Strahlenbelastung eine bessere Beurteilung von implantierten Stents (Ebersberger U., 2012). Von Nachteil ist allerdings, dass bei den Untersuchungen mit deutlich reduzierter Strahlendosis Patienten mit Arrhythmien aufgrund der fehlenden Möglichkeit zur Änderung des Rekonstruktionsfensters nicht untersucht werden können (Sechtem et al., 2010). Auch Perfusionsstudien mittels CT finden immer mehr klinischen Einsatz und zeigen ebenso wie die virtuelle Messung der fraktionierten Flussreserve im Rahmen einer CTAngiographie vielversprechende Resulate (Koo et al., 2011). Im Hinblick auf die Koronarangiographie lässt sich sagen, dass diese aufgrund der Möglichkeit zur interventionellen Therapie weiterhin nicht ersetzbar sein wird, die Zahl der diagnostischen Herzkatheteruntersuchungen allerdings im Verhältnis zu den therapeutischen kleiner werden wird. Dies ist auf die immer größer werdende Bedeutung der nicht-invasiven Techniken bei der Diagnosestellung der KHK zurückzuführen. 57 VI Zusammenfassung Die koronare Herzkrankheit ist die häufigste Todesursache in den westlichen Industrienationen. Der Diagnostik dienen unterschiedliche invasive und nicht-invasive Verfahren. Die vorliegende Arbeit hat sich zum Ziel gesetzt, die Wertigkeit der nichtinvasiven Adenosin-Stress-MRT-Untersuchung anhand des invasiven Goldstandards Koronarangiographie zu überprüfen und den Stellenwert im Hinblick auf die zur Verfügung stehenden Untersuchungsmethoden zu diskutieren. Eine Besonderheit stellt das Patientengut dar, das einem ambulanten Bereich entstammte und die klinische Realität gut repräsentiert. Der Studie zugrunde lag die retrospektive Analyse der Untersuchungen von 54 Patientinnen/Patienten mit einem Durchschnittsalter von 62 Jahren, die sich aus klinischer Indikation sowohl einer ambulanten Kardio-MRT als auch einer Koronarangiographie unterzogen hatten. Um den Vergleich anstellen zu können, wurde das etablierte 17-Segment-Modell der AHA verwendet (Cerqueira et al. 2002). Beruhend auf einer visuellen Auswertung, konnte in dieser Studie der kardialen MRT in der Unterscheidung zwischen einer relevanten und nicht relevanten Koronarstenose nach Analyse von 160 Versorgungsbezirken eine Sensitivität von 91,1% und eine Spezifität von 84,6% zur Diagnosestellung einer KHK zugeschrieben werden. Diese Ergebnisse korrelieren mit den Ergebnissen weiterer Studien und sind vergleichbar mit den diagnostischen Kennzahlen von SPECT und PET. Zahlreiche Studien unterstreichen überdies den hohen negativen prädiktiven Wert nichtinvasiver Verfahren. Angesichts der hohen Zahl diagnostischer Herzkatheteruntersuchungen ohne unmittelbare therapeutische Konsequenz lässt sich der Schluss ziehen, dass eine vorgeschaltete nicht-invasive Diagnostik mit dem Ziel der Evaluierung stress-induzierter Ischämien einen hohen Anteil invasiver Untersuchungen verzichtbar machen könnte. Im Vergleich zu anderen nicht-invasiven Untersuchungstechniken stellt der fehlende Einsatz ionisierender Strahlen ein patientenschonendes Alleinstellungsmerkmal der Kardio-MRT dar. Die vorliegende Arbeit kann die Adenosin-Stress-Perfusionsbildgebung mittels Magnetresonanztomographie als im klinischen Alltag etablierte Technik zur Evaluierung einer möglichen KHK auch als vielversprechende Methode aus ambulanter Perspektive bestätigen. Gerade bei Patienten mit einer mittleren Vortestwahrscheinlichkeit von 3060% für das Vorliegen einer KHK besitzen funktionelle Bildgebungen einen hohen 58 Stellenwert und werden in Zukunft in der differenzierten Stufendiagnostik eine bedeutende Rolle spielen. 59 VII Literaturverzeichnis Barkhausen J., Hunold P., Waltering K.U. (2004). MRI in coronary artery disease. European Radiology 14, 2155-2162 Bateman T.M., Heller G.V., McGhie A.I., Friedman J.D., Case J.A., Bryngelson J.R., Hertenstein G.K., Moutray K.L., Reid K., Cullom S.J. (2006). Diagnostic accuracy of rest/stress ECG-gated Rb-82 myocardial perfusion PET: comparison with ECG-getaed Tc-99m sestamibi SPECT. Journal of Nuclear Cardiology 13 (1), 24-33 Bengalorkar G.M., Bhuvana K., Sarala N., Kumar T.N. (2012). Regadenoson. Journal of postgraduate medicine 58 (2), 140-6 Berman D.S., Kang X., Slomka P.J., Gerlach J, de Yang L., Hayes S.W., Friedman J.D., Thomson L.E., Germano G. (2007). Underestimation of extent of ischemia by gated SPECT myocardial perfusion imaging in patients with left main coronary artery disease. Journal of Nuclear Cardiology 14 (4), 521-8 Bingham S.E., Hachamovitch R. (2011). Incremental prognostic significance of combined cardiac magnetic resonance imaging, adenosin stress perfusion, delayed enhancement, and left ventricular function over preimaging information for the prediction of adverse events. Circulation 123 (14), 1509-18 Bluemke D.A., Achenbach S., Budoff M., Gerber T.C., Gersh B., Hillis L.D., Hundley W.G., Manning W.J., Printz B.F., Stuber M., Woodard P.K. (2008). Noninvasive coronary artery imaging: magnetic resonance angiography and multidetector computed tomography angiography: a scientific statement from the American Heart Association Committee on Cardiovascular Imaging and Intervention of the Council on Cardiovascular Radiology and Intervention, and the Councils on Clinical Cardiology and Cardiovascular Disease in the Young. Circulation 118 (5), 586-606 Brenner D.J., Hall E.J. (2007). Computed Tomography - An Increasing Source of Radiation Exposure. The New England Journal of Medicine 357, 2277-84 Budoff M.J., Dowe D., Jollis J.G., Gitter M., Sutherland J., Halamert E., Scherer M., Bellinger R., Martin A., Benton R., Delago A., Min J.K. (2008). Diagnostic performance of 64-multidetector row coronary computed tomographic angiography for evaluation of coronary artery stenosis in individuals without known coronary artery disease: results 60 from the prospektive multicenter ACCURACY trial. Journal of the American College of Cardiology 52 (21), 1724-32 Budoff M.J., Shaw L.J., Liu S.T., Weinstein S.R., Mosler T.P., Tseng P.H., Flores F.R., Callister T.Q., Raggi P., Berman D.S. (2007). Long-term prognosis associated with coronary calcification: observations from a registry of 25,253 patients. Journal of the American College of Cardiology 49 (18), 1860-70 Bundesamt für Strahlenschutz (2010): Bekanntmachung der aktualisierten diagnostischen Referenzwerte für diagnostische und interventionelle Röntgenuntersuchungen. Salzgitter, 22. Juni 2010 Bundesärztekammer, Kassenärztliche Bundesvereinigung, Arbeitsgeschmeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (2012). Nationale Versorgungsleitlinie Chronische KHK - Langfassung. Version 1.12 März 2012, basierend auf der Fassung von Juni 2006. AWMF-Register-Nr.: nvl-004 Camici P.G., Rimoldi O.E. (2009). The clinical value of myocardial blood flow measurement. Journal of Nuclear Medicine 50 (7), 1076-87 Cerci R.J., Arbab-Zadeh A., George R.T., Miller J.M., Vavere A.L., Mehra V., Yoneyama K., Texter J., Foster C., Guo W., Cox C., Brinker J., Di Carli M., Lima J.A. (2012). Aligning Coronary Anatomy and Myocardial Perfusion Territories: An Algorith for the CORE320 Multicenter Study. Circulation: Cardiovascular Imaging August 10, 2012; DOI: 10.1161/CIRCIMAGING.111.970608 Cerqueira M., Weissman N.J., Dilsizian V., Jacobs A.K., Kaul S., Laskey W.K., Pennell D.J., Rumberger J.A., Ryan T., Verani M.S. (2002). Standardized Myocardial Segmentation and Nomenclature for Tomographic Imaging of the Heart: A Statemant for Healthcare Professionals From the Cardiac Imaging Committee of the Council on Clinical Cardiology of the American Heart Association. Circulation 105, 539–542 Chung G., Krishnamani R., Senior R. (2004). Prognostic value of normal stress echocardioagram in patients with suspected coronary artery disease - a British general hospital experience. International Journal of Cardiology 94 (2-3), 181-6 Cury R.C., Cattani, C.A., Gabure L.A., Racy D.J., deGois J.M., Siebert U., Lima S.S., Brady T.J. (2006). Diagnostic Performance of Stress Perfusion and Delayed- 61 Enhancement MR Imaging in Patients with Coronary Artery Disease. Radiology 240 (1), 39-45 Dorbala S., Di Carli M.F., Delbeke D., Abbara S., DePuey E.G., Dilsizian V., Forrester J., Janowitz W., Kaufmann P.A., Mahmarian J., Moore S.C., Stabin M.G., Shreve P. (2013). SNNMI/ASNC/SCCT guideline for cardiac SPECT/CT and PET/CT 1.0. Journal of Nuclear Medicine 54 (8): 1485-507 Dymarkowski S. and Bosmans, H. (2005). Cardiac MRI Physics. in Bogaert, J., Dymarkowski S., Taylor A.M.; Clinical Cardiac MRI. Springer Verlag, Berlin Heidelberg Ebersberger, U., Makowski M.R., Platz U., Rieber J., Antoni H., Hoffmann E., Leber A.W. (2011). 3T Myocardial Perfusion Imaging with Multitransmit Technology Compared to Coronary Angiography and FFR. Circulation, 124: A17192 Ebersberger U., Tricarico F., Schoepf U.J., Blanke P., Spears J.R., Rowe G.W., Halligan W.T., Henzler T., Bamberg F., Leber A.W., Hoffmann E., Apfaltrer P. (2012). CT evaluation of coronary artery stents with iterative image reconstruction: improvements in image quality and potential for radiation dose reduction. European Radiology. DOI: 10.1007/s00330-012-2580-5 Baer F.M., Rosenkranz S. (2008). Koronare Herzkrankheit und akutes Koronarsyndrom. in Erdmann E. (Hrsg.); Klinische Kardiologie. 7. Auflage. Springer Verlag Heidelberg Falk E., Shah P.K., Fuster V. (1995). Coronary plaque disruption. Circulation 92 (3), 65771 Faxon D.P., Fuster V., Libby P., Beckman J.A., Hiatt W.R., Thompson R.W., Topper J.N., Annex B.H., Rundback J.H., Fabunmi R.P., Robertson R.M., Lodcalzo J., American Heart Association (2004). Atherosclerotic Vascular Disease Conference: Writing Group III: pathophysiology. Circulation 109 (21), 2617-25 Feuchtner G., Goetti R., Plass A., Wieser M., Scheffel H., Wyss C., Stolzmann P., Donati O., Schnabl J., Falk V., Alkadhi H., Leschka S., Cury R.C. (2011). Adenosine Stress HighPitch 128-Slice Dual-Source Myocardial Computed Tomography Perfusion for Imaging of Reversible Myocardial Ischemia. Circulation: Cardiovascular Imaging 4, 540-549 Feuchtner G.M., Plank F., Pena C., Battle J., Min J., Leipsic J., Labounty T., Janowitz W., Katzen B., Ziffer J., Cury R.C. (2012). Evaluation of myocardial CT perfusion in patients 62 presenting with acute chest pain to the emergency department: comparison with SPECTmyocardial perfusion imaging. Heart 10.1136/heartjnl-2012-302531 Fischer J.J., Samady H., McPherson J.A., Sarembock I.J., Powers E.R., Gimple L.W., Ragosta M. (2002). Comparison between visual assessment and quantitative angiography versus fractional flow reserve for native coronary narrowings of moderate severity. American Journal of Cardiology 90 (3), 210-5 Foo T.K., Ho V.B., Saranathan M., Cheng L.Q., Sakuma H., Kraitchman D.K., Wu K.C., Bluemke D.A. (2005). Feasibility of integrating high-spatial-resolution 3D breath-hold coronary MR angiography with myocardial perfusion and viability examinations. Radiology 235 (3), 1025-30 Hamm C.W., Albrecht A., Bonzel T.,Kelm M., Lange H., Schächinger V., Terres W., Voelker W. (2008). Leitlinie Diagnostische Herzkatheteruntersuchung. Clinical Research in Cardiology 97, 475-512 Gallik D.M., Obermueller S.D., Swarna, U.S., Guidry G.W., Mahmarian J.J., Verani M.S. (1995). Simultaneous Assessment of Myocardial Perfusion and Left Ventricular Function During Transient Coronary Occlusion. Journal of the American College of Cardiology 25, 1529-38 Gerber T.C., Carr J.J., Arai A.E., Dixon R.L., Ferrari V.A., Gomes A.S., Heller G.V., McCollough C.H., McNitt-Gray M.F., Mettler F.A., Mieres J.H., Morin R.L., Yester M.V. (2009). Ionizing Radiation in Cardiac Imaging: A Science Advisory From the American Heart Association Commitee on Cardiac Imaging of the Council on Clinical Cardiology and Commitee on Cardiovascular Imaging and Intervention of the Council on Cardiovascular Radiology and Intervention. Circulation 119, 1056-1065 Gibbons R.J., Abrams J., Chatterjee K., Daley J., Deedwania P.C., Douglas J.S., Fergusion T.B. jr., Fihn S.D., Fraker T.D. jr., Gardin J.M., O´Rourke R.A., Pasternak R.C., Williams S.V., ACC, AHA Task Force on parctice guidlines (Committee on the Management of Patients With Chronic Stable Angina). Journal of the American College of Cardiology 41 (1), 159-68 Gianrossi R., Detrano R., Mulvihill D., Lehmann K., Dubach P., Colombo A., McArthur D., Froelicher V. (1989). Exercise-induced ST depression in the diagnosis of coronary artery disease. A meta-analysis. Circulation 80 (1), 87-98 63 Glagov S., Zarins C., Giddens D.P., Ku D.N., (1988). Hemodynamics and atherosclerosis. Insights and perspectives gained from studies of human arteries. Archives of pathology and laboratory medicine 112 (10), 1018-31 Gould K.L., Lipscomb K. (1974); Effects of coronary stenoses on coronary flow reserve and resistance. The American Journal of Cardiology 34, 48-55 Grebe O. (2005). in Hombach V., Grebe O., Jakob, P. (Hrsg.). Kardiovaskuläre Magnetresonanztomographie – Grundlagen –Technik – klinische Anwendung. Schattauer Verlag, Stuttgart Greenland P., Bonow R.O., Brundage B.H., Budoff M.J., Grundy S.M., Lauer M.S., Post W.S., Raggi P., Redberg R.F., Rodgers G.P., Shaw L.J., Taylor A.J., Weintraub W.S. (2007). ACCF/AHA 2007 clinical expert consensus document on coronary artery calcium scoring by computed tomography in global cardiovascular risk assessment and in evaluation of patients with chest pain: a report of the American College of Cardiology Foundation Clinical Expert Consensus Task Force developed in collaboration with the Society of Atherosclerosis Imaging and Prevention and the Society of Cardiovascular Computed Tomography. Journal of the American College of Cardiology 49 (3), 378-402 Gößwald A., Schienkiewitz A., Nowossadeck E., Busch M.A. (2013). Prävalenz von Herzinfarkt und koronarer Herzkrankheit bei Erwachsenen im Alter von 40-79 Jahren in Deutschland. Ergebnisse der Studie zur Gesundheit Erwachsener in Deutschland (DEGS1). Bundesgesundheitsblatt 56, 650-655 Herold G. (2012). Koronare Herzerkrankung; Innere Medizin 2012. Köln Ingkanisorn P., Kwong R.Y., Bohme N.S., Geller N.L., Rhoads, K.L., Dyke C.K., Paterson D.I., Mushabbar A.S., Aletras A.H., Arai A.W. (2006). Prognosis of Negative Adenosine Stress Magnetic Resonance in Patients Presenting in an Emergeny Department With Chest Pain. Journal oft he American College of Cardiology 47 (7), 1427-32 Ishida N., Sakuma H., Motoyasu M., Okinika T., Isaka N, Takeda K. (2003). Noninfarcted myocardium: correlation between dynamic first-pass contrast-enhanced myocardial MR imaging and quantitative coronary angiography. Radiology 229 (1), 20916 64 Jaarsma C., Leiner T., Bekkers S.C., Crijns H.J., Wildberger J.E., Nagel E., Nelemans P.J., Schalla S. (2012). Diagnostic Performance of Noninvasive Myocardial Perfusion Imaging Using Single-Photon Emission Computed Tomography, Cardiac Magnetic Resonance, and Positron Emission Tomography Imaging for the Detection of Obstructive Coronary Artery Disease - A Meta-Analysis. Journal of the American College of Cardiology 59 (19), 1719-28 Jerosch-Herold M., Seethamraju R.T., Swingen C.M., Wilke N.M., Stillman A.E. (2004). Analysis of Myocardial Perfusion MRI. Journal of Magnetic Resonance Imaging 19, 758770 Jung W., Zvereva V., Hajredini B., Jäckle S. (2012). Safe magnetic resonance imaging scanning of the pacemaker patient: current technologies and future directions. Europace 14, 631-637 Karamitsos T.D., Arnold J.R., Pegg T.J., Cheng A.S., van Gaal W.J., Francis J.M., Banning A.P., Neubauer S., Selvanayagam J.B. (2009). Tolerance and safety of adenosine stress perfusion cardiovascular magnetic resonance imaging in patients with severe coronary artery disease. The International Journal of Cardiovascular Imaging 25 (3), 27783 Kelle S., Nagel E., Fleck E. (2006). Kardio-MRT - Ersatz für die diagnostische Koronarangiographie? Der Internist 47, 18-27 Kelle S., Thouet T., Tangcharoen T., Nassenstein K., Chiribiri A., Paetsch I., Schnackenburg B., Barkhausen J., Fleck E., Nagel E. (2007). Whole-heart coronary magnetic resonance angiography with MS-325 (Gadofosveset). Medical Science Monitor 13 (11), CR 469-474 Kim J.E., Koo B.K. (2012). Fractional flow reserve: the past, present and future. Korean Circulation Journal 42 (7), 441-6 Kim R.J., Wu E., Rafael A., Chen E.L., Parker M.A., Simonetti O., Klocke F.J., Bonow R.O., Judd R.M. (2000). The use of contrast-enhanced magnetic resonance imaging to identify reversible myokardial dysfunction. The New England Journal of Medicine 343 (20), 1445-53 65 Kim W.Y., Stuber M., Börnert P., Kissinger K.V., Manning W.J., Botnar R.M. (2002). Three-dimensional black-blood cardiac magnetic resonance coronary vessel wall imaging detects positive arterial remodeling in patients with nonsignificant coronary artery disease. Circulation 106 (2), 296-9 Kligfield P., Lauer M.S. (2006). Exercise electrocardiogram testing: beyond the ST segment. Circulation 114 (19), 2070-82 Knobelsdorff-Brenkenhoff F., Schulz-Menger J. (2012). Cardiovascular Magnetic Resonance Imaging in Ischemic Heart Disease. Journal of Magnetic Resonance Imaging 36, 20-38 Koo B.K., Erglis A., Doh J.H., Daniels D.V., Jegere S., Kim H.S., Dunning A., DeFrance T., Lansky A., Leipsic J., Min J.K. (2011). Diagnosis of ischemia-causing coronary stenoses by noninvasive fractional flow reserve computed from coronary computed tomographic angiograms. Results from the prosepctive multicenter DISCOVER-FLOW study. Journal of the American College of Cardiology 58 (19), 1989-97 Kröpil P., Rojas C.A., Ghoshhajra B., Lanzmann R.S., Miese F.R., Scherer A., Kalra M., Abbara S. (2012). Prospectively ECG-triggered high-pitch spiral acquisition for cardiac CT angiography in routine clinical practice: initial results. Journal of Thoracic Imaging 27 (3), 194-201 Laarman G.J., Suttorp M.J., Dirksen M.T., van Heerebeek L., Kiemeneij F., Slagboom T., van der Wieken L.R:, Tijssen J.G., Rensing B.J., Patterson M. (2006). Paclitaxel-eluting versus uncoated stents in primary percutaneous coronary intervention. New England Journal of Medicine 355 (11), 1105-13 Lerakis S., McLean D.S., Anadiotis A.V., Janik M., Oshinski J.N., Alexopoulos N., Zaragoza-Macias E., Veledar E., Stillman A.E. (2009). Prognostic value of adenosinestress cardiovascular magnetic resonance in patients with low-risk chest pain. Journal of Cardiovascular Magnetic Resonance 11: 37 Ley S. und Kreitner, K.F. (2007). in Thelen, M., Erbel R., Kreitner K.F., Barkhausen J.. Bildgebende Kardiodiagnostik. Georg Thieme Verlag, Stuttgart Libby P., Okamoto Y., Rocha V.Z., Folco E. (2010). Inflammation in atherosclerosis: transition from theory to practice. Circulation Journal 74 (2), 213-20 66 Lloyd-Jones D., Adams R.J., Brown T.M., Carnethon M., Dai S., De Simone G., Ferguson T.B., Ford E., Furie K., Gillespie C., Go A., Greenlund K., Haase N., Hailpern S., Ho P.M., Howard V., Kissela B., Kittner S., Lackland D., Lisabeth L., Marelli A., McDermott M.M., Meigs J., Mozaffarian D., Mussolino M., Nichol G., Roger V.K., Rosamand W., Sacco R., Sorlie P., Stafford R., Thom T., Wasserthiel-Smoller S., Wong N.D., Wylie-Rosett J.; AHA Statistics Commitess and Stroke Statistics Subcommittee (2010). Executive summary: heart disease and stroke statistics - 2010 update: a report from the American Heart Assocation. Circulation 121 (7), 948-54 Maffei E., Seitun S., Martini C., Palumbo A., Tarantini G., Berti E., Grille R., Tedeschi C., Messalli G., Guaricci A., Weustink A.C., Mollet N.R., Cademartiri F. (2010). CT coronary angiography and exercise ECG in a population with chest pain and low-tointermediate pre-test likelihood of coronary artery disease. Heart 96 (24), 1973-9 Melikian N., De Bondt, P., Tonino P., De Winter O., Wyffels E., Bartunek J., Hyndrickx G.R., Fearon W.F., Pijls N.H.J., Wijns W., De Bruyne B. (2010). Fractional Flow Reserve and Myocardial Perfusion Imaging in Patients With Aniographic Coronary Artery Disease. JACC: Cardiovascular Interventions 3 (3), 307-14 Merkle N. und Bernhardt P. (2009) in Hombach (Hrsg.). Kardiovaskuläre Magnetresonanztomographie - Atlas und DVD. Schattauer Verlag, Stuttgart Merten C., Stehen H., Kulke C., Giannitsis E., Katus H.A. (2008). Contrast-enhanced magnetic resonance imaging reveals early decrease of transmural extent of reperfused acute myocardial infarction. Clinical Research in Cardiology 97 (12), 913-6 Mettler F.A. Jr., Thomadsen B.R., Bhargavan M., Gilley D.B., Gray J.E., Lipoti J.A., McCrohan J., Yoshizumi T.T., Mahesh M. (2008). Medical radiation exposure in the U.S. in 2006: preliminary results. Health Physics 95 (5), 502-7 Miller J.M., Rochitte C.E., Dewey M., Arbab-Zadeh A., Niinuma H., Gottlieb I., Paul N., Clouse M.E., Shapiro E.P., Hoe J., Lardo A.C., Bush D.E., de Roos A., Cox C., Brinker J., Lima J.A. (2008). Diagnostic performance of coronary angiography by 64-row CT. New England Journal of Medicine 359 (22), 2324-36 Min J.K., Koduru S., Dunning A.M. Cole J.H., Hines J.L., Greenwell D., Biga C., Fanning G., Labounty T.M., Gomez M., Horowitz J.M., Hadimitzsky M., Hausleiter J., Callister T.Q., Rosanski A.R., Shaw L.J., Berman D.S., Lin F.Y (2012). Coronary CT 67 angiography versus myocardial perfusion imaging for near-term quality of life, cost and radiation exposure: A prospective multicenter randomized pilot trial. Journal of Cardiovascular Computed Tomography 6 (4), 274-83 Muehling O.M., Huber A., Cyran C., Schoenberg S.O., Reiser M., Steinbeck G., Nabauer M., Jerosch-Herold M. (2007). The delay of contrast arrival in magnetic resonance firstpass perfusion imaging: a novel non-invasive parameter detecting collateral-dependent myocardium. Heart 93, 842-847 Nandalur K.R., Dwamena B.A., Choudhri A.F., Nandalur S.R., Reddy P., Carlos R.C. (2008). Diagnostic performance of positron emission tomography in the detection of coronary artery disease: a meta-analysis. Academic Radiology 15 (4), 444-51 Nensa F., Poeppel T.D., Beiderwellen K., Schelhorn J., Mahabadi A.A., Erbel R., Heusch P., Nassenstein J., Bockisch A., Forsting M., Schlosser T. (2013). Hybrid PET/MR imaging of the heart: feasibility and inital results. Radiology 268 (2), 366-73 Nesto R.W., Kowalchuk G.J. (1987). The ischemic cascade: temporal sequence of hemodynamic, electrocardiographic and symptomatic expressions of ischemia. The American Journal of Cardiology 59 (7), 23C-30C Nijveldt R., Beek A.M., Hirsch A., Hofmann MB, Umans V.A., Algra P.R., van Rossum A.C. (2008). `No-reflow´ after acute myocardial infarction: direct visualisation of microvascular obstruction by gadolinium-enhanced CMR. Netherlands Heart Journal 16 (5), 179-81 Ortiz-Pérez, J.T., Rodiguez J., Meyers S.N., Lee D.C., Davidson C., Wu E. (2008). Correspondance Between the 17-Segment Model and Coronary Arterial Anatomy Using Contrast-Enhanced Cardiac Magnetic Resonance Imaging. JACC Cardiovascular Imaging 1 (3), 282-93 Oshinski J.N., Delfino J.G., Sharma P., Gharib A.M., Pettigrew R.I. (2010). Cardiovascular magnetic resonance at 3,0T: current state of the art. Journal of Cardiovascular Magnetic Resonance 12: 55 Paech D.C., Weston A.R. (2011). A Systematic review of the clinical effectiveness of 64slice or higher computed tomography angiography as an alternative to invasive coronary 68 angiography in the investigation of suspected coronary artery disease. BMC Cardiovascular Disorders 11: 32 Pakkal M., Raj V., McCann G.P. (2011). Non-invasive imaging in coronary artery disease including anatomical and functional evaluation of ischaemia and viability assessment. The British Journal of Radiology 84, S280-S295 Palani G., Ananthasubramaniam K. (2012). Regadenoson: Review of its Established Role in Myocardial Perfusion Imaging and Emerging Applications. Cardiology in review. 2012 May 25. DOI: 10.1097/CRD.0b013e3182613db6 Panting J.R., Gatehouse P.D., Yang G.Z., Grothues F., Firmin D.N., Collins P., Pennell D.J. (2002). Abnormal subendocardial perfusion in cardiac syndrome X detected by cardiovascular magnetic resonance imaging. New England Journal of Medicine 346 (25), 1948-53 Parise H., Maehara A., Stone G.W., Leon M.B., Mintz G.S. (2011). Meta-analysis of randomized studies comparing intravascular ultrasound versus angiographic guidance of percutanous coronary intervention in pre-drug-eluting stent era. American Journal of Cardiology 107 (3), 374-82 Pereztol-Valdés O., Candell-Riera J., Santana-Boado C., Angel J., Aguiadé-Bruix S., Castell-Conesa J., Garcia E.V., Soler-Soler J. (2005). Correspondence between left ventricular 17 myocardial segments and coronary arteries. European Heart Journal 26, 2637-2643 Perk J., De Backer G., Gohlke H., Graham I., Reiner Z., Verschuren M., Albus C, Benlian P., Boysen G., Cifkova R., Deaton C., Ebrahim S., Fisher M., Germano G., Hobbs R., Hoes A., Karadeniz S., Mezzani A., Prescott E., Ryden L., Scherer M., Syvänne M., Scholto op Reimer W.J., Vrints C., Wood D., Zamorano J.L., Zannad F. (2012). European Guidelines on cardiovascular disease prevention in clinical practive. The Fifth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practica. European Heart Journal 33 (13), 1635-701 Pijls N.H., De Bruyne B., Peels K., Van der Voort P.H., Bonnier H.J., Bartunek J., Koolen J.J. (1996). Measurement of fractional flow reserve to assess the functional severity of coronary-artery stenoses. New England Journal of Medicine 334 (26), 1703-8 69 Pijls N.H., wan Schaardenburgh P., Manoharan G., Boersma E., Bech J.W., van´t Veer M., Bär F., Hoorntje J., Koolen J., Wijns W., de Bruyne B. (2007). Percutaneous coronary intervention of functionally nonsignificant stenosis: 5-year follow-up of the DEFER Study. Journal of the American College of Cardiology 49 (21), 2105-11 Pilz G., Eierle S., Heer T., Klos M., Eman A., Scheck R., Wild M., Bernhardt P., Hoefling B. (2010). Negative Predictive Value of Normal Adenosine Stress Cardiac MRI in the Assessment of Coronary Artery Disease and Correlation With Semiquantitative Perfusion Analysis. Journal of Magnetic Resonance Imaging 32, 615-621 Pilz G., Jeske A., Klos M., Ali E., Hoefling B., Scheck R., Bernhardt P. (2008). Prognostic value of normal adenosine-stress cardiac magnetic resonance imaging. The American Journal of Cardiology 101 (10): 1408-12 Rieber J. (2012). Intravascular imaging and its integration intro coronary angiography. Deutsche medizinische Wochenschrift 137 (14), 726-31 Rieber J., Meissner O., Babaryka G., Reim S., Oswald M., Koenig A., Schiele T.M., Shapiro M., Theisen K., Reiser M.F., Klauss V., Hoffmann U. (2006). Diagnostic accuracy of optical coherence tomography and intravascular ultrasound for the detection and characterization of atherosclerotic plaque composition in ex-vivo coronary specimens: a comparison with histology. Coronary Artery Disease 17 (5), 425-30 Sakuma H., Suzawa N., Ichikawa Y., Makino K., Hirano T., Kitagawa K., Takeda K. (2004). Diagnostic accuracy of stress first-pass contrast-enhanced myocardial perfusion MRT compared with stress myocardial perfusion scintigraphy. American Journal of Roentgenology 185 (1), 95-102 Sampson U.K., Dorbala S., Limaye A., Kwong R., Di Carli M.F. (2007). Diagnostic accuracy of rubidium-82 myocardial perfusion imaging with hybrid positron emission tomography/computed tomography in the detection of coronary artery disease. Journal of the American College of Cardiology 49 (19), 1052-8 Sandstede J. (2003). Assessment of myocardial viability by MR Imaging. European Radiology 13 (1), 52-61 70 Sandstede J., Voigtländer Th., Pabst Th., Mohrs O. in Freyschmidt, J. (2007). in Hahn D. (Hrsg.); Handbuch diagnostische Radiologie – Kardiovaskuläres System. Springer Verlag Berlin, Heidelberg Sarwar A., Shaw L.J., Shapiro M.D., Blankstein R., Hoffmann U., Cury R.C., Abbara S., Brady T.J., Budoff M.J., Blumenthal R.S., Nasir K. (2009). Diagnostic and prognostic value of absence of coronary artery calcification. JACC Cardiovascular Imaging 2 (6), 675-88 Schächinger V., Zeiher A. (2004). in Berdel W., Böhm M., Classen M., Diehl V., Kochsiek Schmiegel W. (Hrsg.). Innere Medizin. Urban & Fischer Verlag München Schuijf J.D., Bax J.J., Shaw L.J., de Roos A., Lamb H.J., van der Wall E.E., Wijns W. (2006). Meta-analysis of comparative diagnostic performance of magnetic resonance imaging and multislice computed tomography for noninvasive coronary angiography. American Heart Journal 151 (2), 404-11 Schulte B., Boldt A., Beyer D. (2005). MRT des Herzens und der Gefäße: Indikationen – Strategien – Abläufe – Ergebnisse. Springer Verlag Berlin, Heidelberg Schwitter J., Nanz D. , Kneifel S., Bertschinger K., Büchi M., Knüsel P.R., Marincek B., Lüscher T.F., von Schulthess G.K. (2001). Assessment of Myocardial Perfusion in Coronary Artery Disease by Magnetic Resonance - A Comparison With Positron Emission Tomography and Coronary Angiography. Circulation 103, 2230-2235 Schwitter J., Wacker C.M., van Rossum A.C., Lombardi M., Al-Saadi N., Ahlstrom H., Dill T., Larsson H.B.W., Flamm S.D., Marquardt M., Johansson L. (2008). MR-IMPACT: comparison of perfusion-cardiac magnetic resonance with single-photon emission computed tomography fort he detection of coronary artery disease in a multicentre, multivendor, randomized trial. European Heart Journal 29, 480-489 Schwitter J., Wacker C.M., Wilke N., Al-Saadi, N., Sauer E., Huettle K., Schönberg S.O., Luchner A., Strohm O., Ahlstrom H., Dill T., Hoebel N., Simor T. (2012). MR-IMPACT II: Magnetic Resonance Imaging for Myocardial Perfusion assessment in Coronary artery disease Trial: perfusion-cardiac magnetic resonance vs. single-photon emission computed tomography for the detection of coronary artery disease: a comparative multicentre, multivendor trial. European Heart Journal DOI: 10.1093/eurheartj/ehs022 71 Sechtem U., Geissler A., Athanasiadis A., Ong P., Mahrholdt H. (2010). Cardiac computed tomography and magnetic resonance imaging in patients with coronary artery disease. Der Internist 51 (5), 625-38 Shryock J.C., Belardinelli L. (1997). Adenosine and adenosine receptors in the cardiovascular system: biochemistry, physiology and pharmacology. American Journal of Cardiology 79 (12A), 2-10 Skinner J.S., Smeeth, L., Kendall J.M., Adams P.C., Timmis A. (2010). NICE guidance. Chest poain of recent onset: assessment and diagnosis of recent onset chest pain or discomfort of suspected cardiac origin. Heart 96 (12), 974-8 Smith-Bindman R., Lipson J., Marcus R., Kim K.P., Mahesh M., Gould R., Berrington de Gonzalez A., Miglioretti D.L. (2009). Radiation dose associated with common computed tomography examinations and the associated lifetime attributable risk of cancer. Archives of Internal Medicine 169 (22), 2078-86 Statistisches Bundesamt der Bundesrepublik Deutschland (2010). Todesursachen Anzahl der Gestorbenen nach Kapiteln der International Statistical Classification of Diseases and Related Health Problems (ICD-10). http://www.destatis.de Tawakol A., Migrino R.Q., Bashian G.G:, Bedri S., Vermylen D., Cury R.C., Yates D., LaMuraglia G.M., Furie K., Houser S., Gewirtz H., Muller J.E., Brady T.J., Fischman A.J. (2006). In vivo 18F-fluorodeoxyglucose positron emission tomography imaging provides a noninvasive measure of carotid plaque inflammation in patients. Journal of the American College of Cardiology 48 (9), 1818-24 Tayebjee M.H., Lip G.Y., MacFadyen R.J. (2004). Collateralization and the responce to obstruction of epicardial coronary arteries. QJM 97 (5), 259-72 Taylor A.J., Cerqueira M., Hodgson J.M., Mark D., Min J., O´Gara P., Rubin G.D. (2010). ACCF/SCCT/ACR/AHA/ASE/ASNC/NASCI/SCAI/SCMR 2010 Appropriate Use Criteria for Cardiac Computed Tomography. Journal of cardiovascular computed tomography 4 (6), 407, e1-33 Termeer M., Bescós J.O., Breeuwer M., Vilanova A., Gerritsen F. (2010). Patient-Specific Mappings between Myocardial and Coronary Anatomy. Scientific Visualization: Advanced Concepts 196-209 72 Thomsen H.S., Morcos S.K., Almen T., Bellin M.F., Bertolotto M., Bongartz G., Clement O., Leander P., Heinz-Peer G., Reimer P., Stacul F., van der Molen A., Webb J.A. (2012). Nephrogenic systemic fibrosis and gadolinium-based contras media: updated ESUR Contrast Medium Safety Comitee guidelines. European Radiology DOI 10.1007/s00330012-2597-9 Timmis A., Henderson R., Antoniou S., et al. (2011). Management of Stable Angina: NICE clinical guideline. http://www.nice.org.uk/nicemedia/live/13549/55657/ 55657.pdf Tonino P.A.L., Fearon W.F., De Bruyne B., Oldroyd K.G., Leesar M.A., Ver Lee P.N., Maccarthy P.A., Van´t Veer M., Pijls N.H. (2010). Angiographic versus functional severity of coronary artery stenoses in the FAME study fractional flow reserve versus angiography in multivessel evaluation. Journal of the American College of Cardiology 55 (25), 2816-21 Topol E.J., Nissen S.E. (1995). Our Preoccupation With Coronary Luminology - The Dissociation Between Clinical and Angiographic Finding in Ischemic Heart Disease. Circulation 92, 2333-2342 Uhlenbrock D., Forsting M. (2007). MRT und MRA des Kopfes. Georg Thieme Verlag, Stuttgart Underwood S.R., Anagnostopoulos C., Cerqueira M., Ell P.J., Flint E.J., Habinson M., Kelion A.D., Al-Mohammad A., Prvulovich E.M., Shaw L.J., Tweddel A.C.; British Cardiac Society; British Nuclear Cardiology Society; British Nuclear Medicine Society; Royal College of Physicians of London; Royal College of Radiologists (2004). Myocardial perfusion scintigraphy: the evidence. European Journal of Nuclear Medicine and Molecular Imaging 31 (2), 261-91 Van Buuren F. (2010). 25. Bericht über die Leistungszahlen der Herzkatheterlabore in der Bundesrepublik Deutschland. Kardiologe 4, 502-508 Van Geuns R., Wielopolski P.A., de Bruin H.G., Rensing B.J., van Ooijen Peter M.A., Hulshoff M., Oudkerk M., de Feyter P.J. (1999). Basic Principles of Magnetic Resonance Imaging. Progress in cardiovascular diseases 42 (2), 149-56 73 Van Werkhoven J.M., Heijenbrok M.W., Schuijf J.D., Jukema J.W., van der Wall E.E., Schreur J.H., Bax J.J. (2010). Combined non-invasive anatomical and functional assessment with MSCT and MRI for the detection of significant coronary artery disease in patients with an intermediate pre-test likelihood. Heart 96(6), 425-31 Vöhringer M., Mahrholdt H., Yilmaz A., Sechtem U. (2008). Significance of Late Gadolinium Enhancement in Cardiovascular Magnetic Resonance Imaging (CMR). Herz 32, 129-37 Wagner A., Mahrholdt H., Holly T.A., Elliott M.D., Regenfus M., Parker M., Klocke F.J., Bonow R.O., Kim R.J., Judd R.M. (2003). Contrast-enhanced MRI and routine single photon emission computed tomography (SPECT) perfusion imaging for detection of subendocardial myocardial infarcts: an imaging study. The Lancet 361 (9355), 374-9 Weishaupt D., Köchli V.D., Marincek (2009). Wie funktioniert MRI? 2009. Springer Verlag, Berlin White C.W., Wright C.B., Doty D.B., Hiratza L.F., Eastham C.L., Harrison D.G., Marcus M.L. (1984). Does visual interpretation oft he coronary arteriogram predict the physiologic importance of a coronary stenosis? New England Journal of Medicine 310 (13), 819-24 Wijns W., Kolh P., Danchin N., Di Mario C., Falk V., Folliguet T., Garg S., Huber K., James S., Knuuti J., Lopez-Sendon J., Marco J., Menicanti L., Ostojic M., Piepoli M.F., Pirlet C., Pomar J.L., Reifart N., Ribichini F.L., Schalij M.J., Sergeant P., Serruys P.W., Silber S., Sousa Uva M., Taggart D. (2010). Guidelines on mycoardial revascularization. European Heart Journal 31 (20), 2501-55 Windecker S., Maier W., Hess O.M. (2000). in Hess O.M., Simon R.W.R. (Hrsg.). Herzkatheter – Einsatz in Diagnostik und Therapie. Springer Verlag, Berlin Heidelberg Wu Y.W., Tadamura E., Kanao S., Yamamuro M., Marui A., Komeda M., Toma M., Kimura T., Togashi K. (2007). Myocardial viability by contrast-enhanced cardiovascular magnetic resonance in patients with coronary artery disease: comparison with gated single-photon emission tomography and FDG position emission tomography. International Journal of Cardiovascular Imaging 23 (6), 757-765 74 Anhang Unterhalb beispielhaft dargestellt ist eine Perfusionsstudie im Rahmen einer kardialen MRT. Unter Adenosin-Stress konnte eine signifikante Minderperfusion mitt-ventrikulär anteroseptal aufgezeigt werden (siehe Pfeile Abbildungen A 2, A 3, A 4). In der fünf Tage später durchgeführten Koronarangiographie konnte eine subtotale RIVA-Stenose nachgewiesen werden. Abbildung A 1: Perfusionsstudie (1/4) Abbildung A 2: Perfusionsstudie (2/4) Abbildung A 3: Perfusionsstudie (3/4) Abbildung A 4: Perfusionsstudie (4/4) 75 Unterhalb dargestellt ist eine weitere Perfusionsstudie. Es zeigt sich eine inferolaterale Perfusionsstörung bei myokardialer Narbe bei Z.n. Myokardinfarkt im Versorgungsgebiet der RCA (siehe Pfeile Abbildungen A 7, A 8). Deutlich erkennbar ist eine erhebliche Ausdünnung des Myokards in diesem Bereich. Die Aufnahmen in Ruhe (Abbildungen A 9, A 10) zeigen eine nahezu akinetische Hinterwand. Abbildung A 5: Perfusionsstudie II (1/4) Abbildung A 6: Perfusionsstudie II (2/4) Abbildung A 7: Perfusionsstudie II (3/4) Abbildung A 8: Perfusionsstudie II (4/4) Abbildung A 9: Ruhe, enddiastolisch (1/2) Abbildung A 10: Ruhe, endsystolisch (2/2) 76 Danksagungen An erster Stelle danke ich Herrn Prof. Detlev Uhlenbrock für die Überlassung dieses interessanten Themas, die umfassende Unterstützung und wohlwollende Betreuung dieser Arbeit. Ein großer Dank gilt auch seinen Mitarbeiterinnen im Medizinischen Versorgungszentrum im St. Josefs Hospital in Dortmund. Ich danke Herrn Priv.-Doz. Dr. J.-L. Maeso-Madronero aus Witten für die hervorragende Kooperation und freundliche Mithilfe. Ein großer Dank gilt Gabriele Bobrowski und Sabine Wortmann für die unermüdliche Unterstützung und Kreativität in organisatorischen Problemen. Mein besonderer Dank gebührt Birte Kallmeyer für ihre stets inspirierenden Gedanken, ihre große Geduld und liebevollen Rückhalt. Mein Dank gilt auch meinen Freunden, insbesondere Nicklars Achenbach und Nils Kunze, für die stetige Ermutigung und den großen Beistand in schwierigen Phasen. Zu tiefstem Dank verpflichtet bin ich auch meinen Eltern Iris und Günter Kostka sowie meinem Bruder Gereon Kostka für die liebevolle Fürsorge und die moralische wie auch tatkräftige Unterstützung während meines gesamten Lebens. Ihnen sei diese Arbeit gewidmet. Lebenslauf Persönliche Daten Name Tobias Enno Kostka Geburtsdatum 31.05.1983 Geburtsort Dortmund Schulische Ausbildung 1989 - 1993 Busenberg-Grundschule in Dortmund 1993 - 2002 Phoenix Gymnasium in Dortmund 17. Juni 2002 Abschluss der Schulausbildung (Abitur) Studium / Medizinische Ausbildung 2003 - 2004 Studiengang Medizin-Management, Universität Duisburg-Essen 2004 - 2010 Studiengang Humanmedizin, Georg-August-Universität Göttingen 2010 - 2011 Praktisches Jahr in der Klinik für Innere Medizin, Klinikum Links der Weser in Bremen, in der Klinik für Allgemeine und Viszeralchirurgie im Pius-Hospital in Oldenburg sowie in der Klinik für Kinderheilkunde im Klinikum Oldenburg 18. Oktober 2011 Abschluss des Studiums der Humanmedizin (Staatsexamen) 17. November 2011 Approbation als Arzt Beruflicher Werdegang 2002 - 2003 Zivildienst auf der interdiziplinären Intensivstation, St. Josefs Hospital in Dortmund seit 2012 Weiterbildung zum Facharzt Innere Medizin, Klinikum Bremen Mitte