K ºC Temperatur Temperaturmessung
Werbung

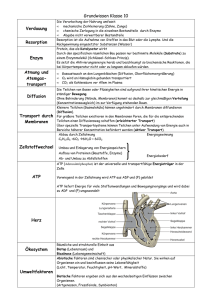
Temperatur der Temperaturbegriff ist eng mit der Bewegung von Teilchen gekoppelt Maß für die Teilchenbewegung, für die mittlere kinetische Energie der Teilchen auch in Festkörpern bewegen sich Teilchen (Schwingungen um die Ruhelage) m 2 3 v = kT 2 2 Kelvin- und Celsiusskala T - absolute Temperatur [T]=K ºC - 273 0 100 0 273 373 Kelvin k - Boltzmann-Konstante k= 1,38x10-23 J/K K T = t + 273 K gleiche Temperaturdifferenzen auf beiden Skalen Temperaturmessung die Größe von Körpern hängt von der Temperatur ab Ausdehnungsthermometer Festkörper und Flüssigkeiten dehnen sich bei Temperaturerhöhung aus lT ∆l l0 α - lineare Ausdehnungskoeffizient lT = l0 + ∆l lT = l0 (1 + α ∆t) [ α ] = K-1 Dichte von Festkörpern und Flüssigkeiten nimmt bei Temperaturerhöhung ab ρT = ρ0 (1 + γ ∆t) γ - Volumenausdehnungskoeffizient [ γ ] = K-1 γ ≈ 3α Ausnahme: Wasser in der Nähe des Gefrierpunktes ρmax bei 4ºC stehende Gewässer gefrieren von oben 1 Temperaturmessung auch elektrischen Parameter hängen von der Temperatur ab Widerstandsthermometer Thermoelement Temperatur-abhängige Kontaktspannung an Lötstellen zweier unterschiedlicher Metalle RT = R0 (1 + α ∆t) A α - Temperaturkoeffizient des Widerstandes bei T1 = T2 [ α ] = K-1 T1 U1 + U2 = 0 U1 α > 0 Metalle Kontaktstellen T2 U2 für Messungen: α < 0 Halbleiter Kontaktstelle 1: Eichung Kontaktstelle 2: Messfühler Heißleiter (Thermistoren) Vorteil: kleiner Messfühler kleine Wärmekapazität Temperatur winziger Objekte kann gemessen werden Zustandsgleichung idealer Gase Druck, Temperatur und Volumen eines Gases sind miteinander verknüpft Ideales Gas: punktförmige Moleküle (kein Eigenvolumen) keine Wechselwirkungskräfte untereinander Moleküle verhalten sich bei Stößen wie vollelastische Kugeln Zustandsgrößen: beschreiben den Zustand eines Gases Druck p Temperatur T Volumen V Zustandsgleichung pV = nRT n - Stoffmenge des Gases R - Gaskonstante R = 8,314 T – absolute Temperatur (Angabe in Kelvin!) J mol K für eine bestimmte Gasmenge in zwei verschiedenen Zuständen: p1V1 T1 = p2V2 T2 2 Zustandsänderungen bei bestimmten äußeren Bedingungen können einzelne Zustandsgrößen konstant bleiben pV = nRT isotherm T = const isobar p = const p V = const V~T Gesetz von Boyle-Mariotte Gesetz von Gay-Lussac isochor p~T Beispiel: Ausdehnung eines Gases bei Erwärmung Beispiel: Kompression eines Gases in einem Zylinder durch Kolbendruck p V Beispiel: Zunahme des Druckes bei Erwärmung eines Gases in einem geschlossenem Gefäß p1 p Isobare T2 V = const V1 Isochore p2 Isotherme V2 T1 V T T Gasgemische in einem Gasgemisch verhalten sich die einzelnen Komponenten unabhängig voneinander Beispiel: Luft pi = ni Sauerstoff, Stickstoff, Wasserdampf, Kohlendioxid, Edelgase RT Partialdruck, Druck einer Komponente V Gesetz von Dalton Der Druck eines Gasgemisches ist der Summe der Partialdrücke seiner Komponenten. p = p1 + p2 + p3 + ... = Σ pi pLuft = p N2 + p O2 + p CO2 +p + p Edelgase Rest 101,3 kPa = 79,1 kPa + 21,2 kPa + 0,03 kPa + 0,9 kPa + ... 3 Wärmemenge und Temperatur durch Zufuhr von Wärme kann ein Körper seine Temperatur erhöhen Wärme ist eine Energieform Wärmezufuhr: Erwärmung des Körpers Wärmekapazität Phasenumwandlung Verrichten von Arbeit ∆Q = m c ∆T C=mc Grundgleichung der Kalorik Wasser: J c = 4184 ∆Q - zugeführte Wärmemenge kg K ∆T - Temperaturänderung m - Masse des Körpers c - spezifische Wärmekapazität [c] = J kg K Phasenumwandlung durch Zufuhr oder Abgabe von Wärme kann ein Körper seinen Phasenzustand ändern Beispiele: Schmelzen von Eis Verdampfen von Wasser Eis → Wasser ∆Q t, ºC ∆t = const Q=rm Q - Wärmemenge für Phasenumwandlung m - Masse Wasser 0 Eis Eis-WasserGemisch r - spezifische Umwandlungswärme Zeit Temperatur bleibt während der Phasenumwandlung konstant Zahlenwerte für r Schmelzen (Eis → Wasser) 335x103 J/kg T = 273 K Sieden (Wasser → Wasserdampf) 2,26x106 T = 373 K J/kg 4 Erster Hauptsatz der Wärmelehre eine Form des Energieerhaltungssatzes unter Berücksichtigung der Wärme a) V, T, p Gas V = const ∆T ↑, ∆p ↑ Innere Energie U wird erhöht + ∆Q b) T = const, p = const ∆V ↑ ∆W = - p ∆V Volumenarbeit wird verrichtet Die Änderung der inneren Energie eines Systems ist gleich der Summe der zugeführten (bzw. abgegebenen) Wärmemenge und der am System verrichteten (bzw. vom System verrichteten) Arbeit. ∆U = ∆Q + ∆W Vorzeichenregel! Wärmeleitung Wärme wird dabei ohne makroskopischen Massentrasnport übertragen l T1 - T2 A T2 T1 PQ = ∆Q ∆t = λA l - Temperaturgradient T1 - T2 PQ - Wärmestrom l [ PQ ] = W λ - spez. Wärmeleitvermögen [ λ ] = J / (m K s) Wärme wird infolge von Stoßprozessen zwischen benachbarten Teilchen übertragen 5 Konvektion Wärmetransport erfolgt hierbei durch makroskopische Bewegungen der Stoffe Wärmetransport durch strömende Medien Flüssigkeiten, Gase Wärmeleitung hingegen wird vor allem bei Festkörpern beobachtet weniger dichte, erhitzte Flüssigkeit steigt auf freie Konvektion Gase bzw. Flüssigkeiten werden bewegt Pumpen Druckdifferenzen erzwungene Konvektion Beispiele: Blutzirkulation Luftzirkulation in Räumen (Heizgeräte) Luftzirkulation in der Atmosphäre (klimatische Einflüsse) Verdunstung dazu wird Energie in Form von Umwandlungswärme benötigt Wasserdampf H2O P=r ∆m ∆t r - spezifische Verdunstungswärme ∆m - verdunstete Wassermenge ∆t - Zeit, in der das Wasser verdunstet die für die Phasenumwandlung notwendige Wärmemenge wird dem Körper entzogen Schwitzen mit folgender Verdunstung ist der einzige wirksame Wärmetransportmechanismus des Menschen bei höheren Umgebungstemperaturen funktioniert nicht bei wasserdampfgesättigter Luft 6 Wärmestrahlung Energie wird hierbei in Form elektromagnetischer Wellen übertragen zwei thermisch voneinander isolierte Körper Wärmeabgabe bzw. -aufnahme durch elektromagnetische Strahlung sowohl durch Materie als auch durch Vakuum möglich (z. B. Wärmetransport von der Sonne zur Erde) T2 beide Körper emittieren und absorbieren elektromagnetische Strahlung Wärmeabgabe eines Körpers P = α σ A T4 T1 Stefan-BoltzmannGesetz Wärmeabgabe und -aufnahme P = α A σ (T4 - Tu4) A - strahlende Fläche 0<α<1 α - Emissionsgrad W ideal schwarze, σ = 5,67 x 10-8 m2 K4 stumpfe Oberfläche Stefan-Boltzmannideal weiße, Konstante Tu - Temp. der Umgebung A - strahlende bzw. absorbierende Fläche sind gleich groß glänzende Oberfläche Wärmestrahlung Energie wird hierbei in Form elektromagnetischer Wellen übertragen Spektralbereich der Wärmestrahlung I T3 > T2 > T1 Emission von Infrarotstrahlung bei normalen Temperaturen Emission von sichtbarem Licht bei deutlich höheren Temperaturen glühende Metalle, Glühfaden einer Lampe, Sonnenlicht λmax λ λmax T = const Anwendungen: Thermographie Infrarotkameras Wien‘sche Verschiebungsgesetz 7 Wärmebewegung in Flüssigkeiten und Gasen ändern die Teilchen ständig ihren Ort Alle Teilchen eines Stoffes befinden sich in ständiger Bewegung Flüssigkeiten, Gase: Wechsel in andere Volumenelemente Festkörper: Schwingungen am Ort m 2 3 v = kT 2 2 3 1 Brownsche Molekularbewegung thermische Bewegung kleiner Teilchen unter dem Mikroskop 4 Kugel mit dem Radius r um ein Teilchen t=0 2 r 1 nach der Zeit t erreicht das Teilchen die Peripherie der Kugel r2 = 6 D t 5 t 5 kT D = 6 πηr T [D]= m2/s t wird aus vielen Experimenten gemittelt D - Diffusionskonstante Diffusion Diffusionsphänomene resultieren aus der Wärmebewegung der Teilchen Zeit Diffusion - gerichteter Massetransport im Laufe der Zeit resultiert ein vollständiger Konzentrationsausgleich 8 Diffusionsgesetz es liefert die quantitative Beschreibung für die irreversiblen Diffusionsprozesse A c1 c2 c1 > c2 ∆c J Diffusionsstromstärke (Nettostrom durch A) ∆x J = Nettomenge der durch A transportierten Teilchen ∆n ∆t J = - DA Teilchenstrom von links nach rechts überwiegt = c1 - c2 Konzentrationsgradient ∆x Teilchen gelangen in das jeweils andere Kompartment infolge der thermischen Bewegung ∆c ∆c ∆x Diffusionsgesetz 1. Ficksche Gesetz D - Diffusionskonstante Biologische Membranen als Diffusionsbarriere Membranen trennen einzelne Kompartmente (Reaktionsräume) voneinander J = - DA c1 c2 ∆x ∆c ∆x entspricht der Membrandicke d d = 4 nm ... 5 nm d d = 40 Å ... 50 Å beidseits biologischer Membranen bestehen für viele gelöste Stoffe und Ionen deutliche Konzentrationsunterschiede diese Unterschiede bleiben über lange Zeiträume erhalten (Zu- bzw. Abstrom von Metaboliten, Stoffwechselvorgänge) → stationäre Diffusion D P= Angström 1 Å = 10-10 m Diffusionskonstante für den jeweiligen Stoff in der Membran D d J = P A ∆c P - Permeabilitätskoeffizient [ P ] = m s-1 9 Transport durch Membranen bestimmte Stoffe benötigen Energie für ihren Transport durch Membranen Passiver Transport entlang Aktiver Transport ∆c entgegen ∆x keine zusätzliche Energie erforderlich ∆c ∆x Energiequelle notwendig ATP-ase ATP + H2O → ADP + Pi normale Diffusion ATP-getriebene Transportmechanismen existieren für H+, Na+ (gekoppelt mit K+), Ca2+, erleichterte Diffusion spezielle Ionenkanäle spezielle Transportmoleküle Carrier spezielle Transporter eine Substanz wird passiv, eine zweite aktiv transportiert Osmose Membranen sind nur für bestimmte Substanzen permeabel durch eine Trennfläche können nicht alle Komponenten einer Lösung diffundieren kleine Moleküle sind permeabel, große Moleküle nicht semipermeable Membran im Extremfall diffundiert nur das Lösungsmittel, nicht die gelösten Substanzen Pfeffersche Zelle Wilhelm Pfeffer (1845-1920) Zellmembranen sind semipermeabel seit 1887 in Leipzig Pflanzenphysiologe 1877 „Osmotische Untersuchungen“ 10 Pfeffersche Zelle sie dient als Modell für Osmose in Pflanzenzellen Wasser strömt in das kleine Gefäß, Zuckerlösung wird verdünnt Einstellen eines Gleichgewichtes gleiche Wasserströme in beide Richtungen h Zuckerlösung aber: kein Konzentrationsausgleich Lösung im kleinen Gefäß steht unter einem höheren Druck π = ρgh H2O osmotische Druck semipermeable Membran eine verdünnte Lösung eines Nichtelektrolyten verhält sich wie ein ideales Gas durchlässig für H2O undurchlässig für Zuckermoleküle Osmotische Druck er hängt von der Anzahl der dissoziierten Teilchen in Lösung ab π = icRT Formel von van‘t Hoff c - Konzentration des gelösten Stoffes i - Anzahl der Teilchen (Ionen), in die ein Molekül beim Lösen zerfällt Isotone Lösung (Beispiel: Blutzellen) im osmotischen Gleichgewicht mit Zellen des menschlichen Blutes NaCl: 0,9% oder 0,154 mol/l Hypotone Lösung πLösung < πBlut i=1 Glucose, Zuckermoleküle i=2 NaCl, KCl i=3 K2SO4, CaCl2 i=4 FeCl3, K3Fe(CN)6 Hypertone Lösung πLösung > πBlut der osmotische Druck ist eine Funktion der Teilchenzahl 11 Beispiel: Pflanzenzelle der Protoplast einer Pflanzenzelle ist von einer zusätzlichen, starren Membran (Zellwand aus Zellulose) umgeben kein Platzen in hypotonen Lösungen Zelle ist mehr oder weniger prall gefüllt zusätzliche Druckkomponente in Form eines Stempeldruckes (entspricht der Schweredruckkomponente in der Pfefferschen Zelle) Turgor (Zellwanddruck) wichtig für Stabilität und Steifheit pflanzlicher Gewebe Pflanzen, die Wasser verlieren, werden schlaff und welk Beispiel: Pflanzenzelle Wasserentzug in hypertonen Lösungen Protoplast schrumpft, kleinere Vakuolen teilweise Ablösung von der Zellwand Plasmolyse dieser Vorgang ist in der Regel reversibel (Deplasmolysierung bei Überführung der Zellen in hypotone Lösungen) 12 Donnan-Gleichgewicht dieses Gleichgewicht tritt vor allem an Blut- und Endothelzellen auf elektrochemisches Verteilungsgleichgewicht an semipermeablen Membranen Protein (impermeabel) - + Proteinkompartment permeable Ionen mehr diffusible Kationen weniger diffusible Anionen - + + + + + - + - + - + + + - + + - + + - - + - + + - + - + - + für diffusible Ionen gilt - - Gleichgewichtsbedingungen - + + - + - + c+‘ • c-‘ = c+‘‘ • c-‘‘ und U = RT F ln c+‘‘ RT c- ‘ = ln c+ ‘ c-‘‘ F Ionenverteilung in Zellen aktive Mechanismen führen zu einer Ungleichverteilung von Ionen in den Zellen Ionen sind ungleich in den einzelnen Zellkompartmenten verteilt außen innen 5 mM 140 mM Na+ 145 mM 5-15 mM Cl- 110 mM 5-15 mM Anionen- 40 mM 140 mM K+ typische Säugerzelle Ursache für diese Verteilung: Na+/K+-ATPase Ionen sind stets so verteilt, dass die einzelnen Medien faktisch elektrisch neutral sind 13 Permeabilität der Ionen manche Ionen permeieren besser, andere schlechter durch biologische Membranen die Permeabilität biologischer Membranen ist unterschiedlich für die einzelnen Ionensorten Permeabilität wird bestimmt durch passive Permeabilität durch die Lipid-Doppelschicht spezielle Ionenkanäle Kaliumionen weisen die höchste Permeabilität durch nicht erregte („ruhende“) Membranen auf PK > PCl ≈ PNa 1 : 0,05 : 0,04 (für Riesenaxon des Tintenfisch) Diffusion von K+ ist wesentlich für die Ausbildung eines Ruhepotentials Ruhepotenzial einer Zelle solche Potenziale treten vor allem an Nerven- und Muskelzellen auf ungleiche Ionenverteilung hohe Permeabilität für anderen Ionen K+ K+ K+ + + + + - K+ K+ K+ K+ K+ K+ K+ RT zF ln [K+]a [K+]i K+ R - Gaskonstante K+ K+ K+ K+ K+ gegenüber U= K+ K+ Nernstsche Gleichung K+ K+ K+ T - absolute Temperatur F - Faraday-Konstante K+ K+ wenige K+ diffundieren nach außen es resultiert ein Membranpotenzial dieses Potenzial behindert den weiteren Ausstrom von K+ und begünstigt den Einstrom von K+ F = 96463 As / mol z - Wertigkeit des permeablen Ions Beispiel: [K+]a = 5 mM [K+]i = 140 mM T = 310 K U = - 89 mV Gleichgewicht der beiden K+-Ströme 14 Goldman-Gleichung die Nernst‘sche Gleichung ist als einfacher Sonderfall in der Goldman-Gleichung enthalten Nernstsche Gleichung: gute Näherung experimenteller Werte Goldman-Gleichung: berücksichtigt auch die Permeabilitäten von Na+, Cl- U = RT F ln PNa[Na]a + PK[K]a + PCl[Cl]i PNa[Na]i + PK[K]i + PCl[Cl]a Aktionspotenzial sie spielen eine wesentliche Rolle in der Elektrophysiologie Ruhepotenzial → Aktionspotenzial U, mV 30-50 mV Erregungsleitung in Nerven - und Muskelzellen Öffnung und Schließen Spannungskontrollierter Natriumkanäle t, ms 0 1 2 3 Na+-Permeabilität nimmt zu Öffnung und Schließen Spannungskontrollierter Kaliumkanäle K+-Permeabilität nimmt vorübergehend zu, schnellere Rückführung auf das Ruhepotenzial Na+/K+-ATPase Wiederherstellung der alten Ionenverteilung Alles-oder-Nichts-Prozess überschreitet die Änderung des Ruhepotenzials eine bestimmte Schwelle wird immer ein Aktionspotenzial ausgelöst 15