Kap.16 Magenkarzinom
Werbung

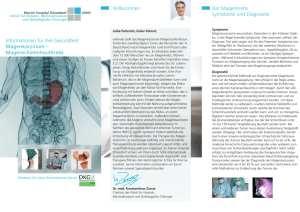
GASTROENTEROLOGIE MAGENKARZINOM 1. Screening/Surveillance • Risikoerkrankungen: Chronisch atrophische Gastritis mit intestinaler Metaplasie, M. Ménétrier, subtotale Gastrektomie, adenomatöse Polypen, hyperplastische Polypen > 2cm, FAP, HNPCC. • Familiäre Belastung: Hereditäres diffuses Magenkarzinom (HDGC). • Vorsorge: Adenomatöse Polypen, FAP, HNPCC, HDGC. Allgemeines Screening der Normalbevölkerung nicht etabliert. 2. Klinisches Bild Meist nur unspezifische Beschwerden: Völlegefühl, Schwäche, Leistungsabfall, Oberbauchbeschwerden, Foetor ex ore. Warnsymptome sind Blutung, Gewichtsverlust. Da eine frühzeitige Diagnosestellung von entscheidender Bedeutung für die Prognose ist, ist die Indikation zur ÖGD großzügig zu stellen. 3. Tumorklassifikation • Histologie: Adeno- (~70%), undifferenziertes (~20%), Siegelringzell- (~10%), adenosquamöses, Plattenepithel-, kleinzelliges und andere Karzinome. • Laurén-Klassifikation: Intestinaler Typ (häufiger distal) mit makroskopisch meist klaren Tumorgrenzen, diffuser Typ (häufiger proximal) mit oft erheblicher Diskrepanz zwischen makroskopischem und histologischem Tumorrand und diffus-infiltrativem Wachstum. • Magenfrühkarzinom: Karzinome, die auf die Mukosa und Submukosa beschränkt sind, unabhängig von Lymphknotenbefall (LK). Bei Tumoren bis Mukosa in 3% LK, bei Tumoren bis Submukosa in 20% LK. Magenfrühkarzinome können häufig lokal begrenzt therapiert werden. Allerdings muss darauf geachtet werden, dass sie multifokal auftreten können. Die Klassifikation erfolgt in drei Typen: Typ I: vorgewölbt;Typ IIa: leicht erhaben; Typ IIb: flach; Typ IIc: leicht eingesenkt; Typ III: ulceriert. Intravitalfärbung mit Kongorot oder Methylenblau erhöht die Treffsicherheit. • Tumorlokalisation: Korpus (40%), Kardia-subkardial-Fundus (30%), Angulusfalte-Antrum-Pylorus (20%), gesamter Magen (5-10%). Kardiakarzinome sind alle Karzinome des gastroösophagealen Übergangs von 5 cm oral bis 5 cm aboral der Schleimhautgrenze (s. Ösophaguskarzinome). • Tumorausbreitung: Zum Zeitpunkt der OP bereits in ~60% Infiltration der Serosa und in ~70% bereits Lymphknotenmetastasen. Ausbreitung per continuitatem (Leber, Pankreas, Milz, Colon, Netz), über Lymphgefässe (retropankreatische, mesenteriale, paraaortale Lymphknoten gelten als Fernmetastasen) und hämatogen (beim intestinalen Typ überwiegend Leberfiliae, bei diffusem Typ überwiegend Lungenmetastasen). In etwa 6% der Fälle Knochenmetastasen. 4. Diagnostik und Staging • Endoskopie: 6 bis 8 Biopsien aus dem Randbereich und dem Zentrum der Läsion. Die Linitis plastica, die sich submukös flächenhaft ausbreitet, entzieht sich häufig dem endoskopischen Nachweis. Diagnostisch wegweisend kann hier die Magen-Brei-Passage sein. • Endosonographie: Methode der Wahl zur Beurteilung der Eindringtiefe (TStadium) und des Lymphknotenstatus (N-Stadium). Unterscheidung zwischen Mukosa- / Submukosatyp des Frühkarzinoms nur in etwa 70% der Fälle. • Computertomographie: Schlechter als die Endosonographie zur Beurteilung des lokalen Lymphknotenstatus (N-Stadium). Mittels CT Abdomen und Thorax werden Fernmetastasen (M-Stadium) ausgeschlossen. 33 GASTROENTEROLOGIE • MAGENKARZINOM Skelettszintigraphie bei Patienten mit fortgeschrittenen Tumoren oder im Falle von Beschwerden. PET/PET-CT: Derzeit keine gesicherte Indikation beim Magenkarzinom. Diagnostische Laparoskopie: Zum Ausschluss einer Peritonealkarzinose bei lokal fortgeschrittenen Karzinomen, zur Bestimmung der Leberbeteiligung und zum Lymphknotenstaging. Magen-Brei-Passage in Doppelkontrasttechnik bei unklarem endoskopischem Befund, z.B. bei submukös wachsendem Karzinom (Linitis plastica). Tumormarker: CEA, CA 72-4 und CA 19-9 nicht zur Diagnosestellung, nur zur Verlaufsbeurteilung. • • • • TX T0 Tis T1 T2 T3 T4 N0 N1 N2 N3 M0 M1 0 IA IB II IIIA IIIB IV TNM-Klassifikation der Magenkarzinome Primärtumor kann nicht beurteilt werden kein Anhalt für Primärtumor Carzinoma in situ (intraepithelialer Tumor ohne Einbruch in Lamina propria mucosae Tumor infiltriert lamina propria mucosae (T1m) oder Submucosa (T1sm) Tumor infiltriert muscularis propria oder Subserosa oder Ausbreitung in Lig. gastrocolicum oder hepatogastricum, das grosse oder kleine Netz ohne Penetration des viszeralen Peritoneums Tumor penetriert Serosa (viszerales Peritoneum), infiltriert aber nicht Nachbarstrukturen Tumor infiltriert Nachbarorgane keine regionären Lymphknoten befallen 1-6 regionäre Lymphknoten befallen 7-15 regionäre Lymphknoten befallen >15 regionäre Lymphknoten befallen keine Fernmetastasen Fernmetastasen Tis T1 T1 T2 T1 T2 T3 T2 T3 T4 T3 T1-3 T4 jedes T UICC-Stadien der Magenkarzinome N0 N0 N1 N0 N2 N1 N0 N2 N1 N0 N2 N3 N1-3 jedes N 34 M0 M0 M0 M0 M0 M0 M0 M0 M0 M0 M0 M0 M0 M1 GASTROENTEROLOGIE MAGENKARZINOM 5. Stadienadaptierte Therapie • Frühkarzinome (T1m): Bei Frühkarzinomen vom Mukosatyp kann eine endoskopische Therapie erfolgen. Voraussetzungen sind: differenziertes Karzinom (G1/G2); leicht erhabener Typ (IIa) <2 cm Durchmesser; leicht erniedrigter Typ (IIc), nicht-ulzeriert, <1 cm Durchmesser; keine Lymphknotenmetastasen; keine tiefe submuköse Invasion. Die 5-JahresÜberlebensraten erreichen bei Einhaltung dieser Kriterien 86% und liegen in etwa gleich auf mit der chirurgischen Resektion. Zu beachten ist, dass synchrone Läsionen vorliegen können. Alternative: laparoskopische „wedge resection“. • Lokalisierten Stadien (T1sm-T3 N0-N1 M0, ggf. bis T4 N2 M0): Abhängig von Lokalisation, histologischem Typ und patientenbezogener Risikobeurteilung. Bei präoperativ unklaren Fällen wird eine explorative Laparoskopie vorgeschaltet. Distale Karzinome vom intestinalen Typ können in der Regel mit einer 4/5Resektion des Magens behandelt werden. Eine totale Gastrektomie ist in der Regel bei proximalen Karzinomen und solchen vom diffusen Typ erforderlich. Karzinome des gastroösophagealen Übergangs vom Typ II und Typ III werden mittels einer abdominalen transhiatalen erweiterten Gastrektomie und einer distalen Ösophagusresektion behandelt. Die mit der Gastrektomie assoziierte Mortalität beträgt ca. 3%. Eine chirurgische Resektion von Fernmetastasen beim Magenkarzinom ist nicht sinnvoll. • Neoadjuvante Chemotherapie: Bei lokal fortgeschrittenen und als primär inoperabel eingeschätzten Tumoren sollte eine neoadjuvante Therapie zur Tumorverkleinerung durchgeführt werden. Nach Abschluss der präoperativen Therapie wird dann die R0-Resektion angestrebt. Für die operablen, aber lokal fortgeschrittenen Tumorstadien T3 und T4 wird gegenwärtig im Rahmen von Studien der Nutzen einer neoadjuvanten Therapie überprüft. Die postoperative Morbidität und Mortalität wird durch die neoadjuvante Therapie nicht erhöht. In der neoadjuvanten Situation hat sich das gut verträgliche Protokoll PLF (Cisplation, 5-Fluorouracil, Calciumfolinat) bewährt. Nach zwei Zyklen wird zur Überprüfung des Ansprechens in der Regel ein Zwischenstaging durchgeführt. Die Rate R0-resezierbarer Karzinome kann durch diese neoadjuvante Chemotherapie bis auf 65% gesteigert werden. • Adjuvante Chemotherapie: Wert nicht gesichert, nur innerhalb von Studien. • Palliative Chemotherapie: Die palliative Chemotherapie ist der supportiven Behandlung hinsichtlich Überlebenszeit und Lebensqualität überlegen. Vor allem drei Protokolle, mit denen mediane Überlebenszeiten von 6 bis 11 Monaten und Remissionsraten bis über 50% erzielt werden, sind verbreitet: Das ELF-Schema zeichnet sich durch eine gute Verträglichkeit aus und wird vor allem bei älteren Patienten eingesetzt. Wichtigste Nebenwirkung ist die Alopezie. Wirksamer sind das ECF- und das PLF-Protokoll. Nachteil des ECF-Schemas ist die 21-tägige 5FU-Dauerinfusion. Als Standard in der palliativen Therapie gilt das PLF-Schema (Ansprechraten von 60 bis 70% und mediane Überlebenszeiten von 10 bis 11 Monate). Die Wirksamkeit neuerer Substanzen wie Paclitaxel, Docetaxel, Irinotecan und Oxaliplatin beim Magenkarzinom wird derzeit im Rahmen von Studien untersucht. Bei Patienten in schlechtem Allgemeinzustand kann auch eine Monotherapie mit 5-FU/Folinsäure oder Capecitabin durchgeführt werden. • Endoskopische und chirurgische Palliation bei lokalen Komplikationen wie Blutung und Stenosen. Bei diffusen Tumorblutungen Argonplasmakoagulation. Bei Magenausgangsstenosen können als Alternative zur offenen oder laparoskopischen Gastroenterostomie selbstexpandierende Metallstents appliziert werden. 35 GASTROENTEROLOGIE MAGENKARZINOM 6. Nachsorge Nach Gastrektomie vierteljährlich Vitamin-B12-Substitution. Nach kurativer Resektion in den ersten 24 Monaten alle 3 Monate (bei Magenfrühkarzinom alle 6 Monate), dann bis zum 5. postoperativen Jahr halbjährlich: Anamnese, körperliche Untersuchung, Blutbild, Harnstoff, Kreatinin, Albumin, γGT, AP, LDH, CEA, CA19-9, Oberbauchsonographie, Gastroskopie (halbjährlich bis 24 Monate, dann jährlich). Fehler! Es ist nicht möglich, durch die Bearbeitung von Feldfunktionen Objekte zu erstellen. Palliative Chemotherapieprotokolle beim Magenkarzinom Dosis Protokoll/ Applikationsmodus Therapietage Wiederholung Wichtige Nebenwirkungen (mg/m2) Substanz ELF (Wilke 1990) Knochenmarksdepression, Etoposid 120 i.v. (30-60 Min.) Übelkeit, Stomatitis, 1-3 Tag 22 Calciumfolinat 300 i.v. (10 Min.) Alopezie, Diarrhö, Hand5-FU 500 i.v. (10 Min.) Fuß-Syndrom, Angina pectoris ECF (Findlay 1994) Alopezie, Kardiotoxizität, Epirubicin 50 i.v. Bolus 1 KnochenTag 22 Cisplatin 60 i.v. (30 Min.) 1 marksdepression, GI5-FU 200 i.v. (24 h) 1-21 Beschwerden. Kumulative max. Dosis Epirubicin: 900-1000 mg/m2, ab 450 mg/m2 Monitoring. PLF (Wilke 1994) Knochenmarksdepression, 1, 8, 15, Calciumfolinat 500 i.v. (120 Min.) GI-Beschwerden, SehTag 50 22, 29, 36 5-FU 2000 i.v. (24 h) und Hörstörungen, Cisplatin 50 i.v. (60 Min.) 1, 15, 29 Elektrolytstörungen, Kardiotoxizität Nachsorge: 36 In den ersten 24 Monaten nach nach kurativer Resektion alle 3 Monate (bei Magenfrühkarzinom alle 6 Monate), dann bis zum 5. postoperativen Jahr halbjährlich: