Ubungen zur T4p Statistische Physik Blatt 5
Werbung

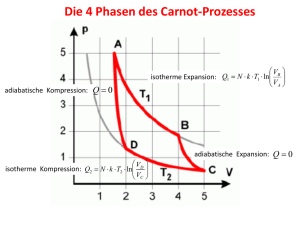
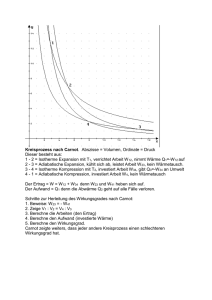
LMU München / Fakultät für Physik WS 2013/14 Übungen zur T4p Statistische Physik Blatt 5 11.11.2013 5.1 Lernkontrolle 1.) Gegeben sei ein TD System in thermischem Kontakt mit einem Wärmereservoir. Erlaubt der 2. HS der Thermodynamik Prozesse, in denen die Entropie des Systems abnimmt? 2.) Die Gleichung dS ≥ 0 des 2. HS wird oft als interpretiert als “Maximierung der Entropie im GGW”. Die ZV S ist aber nur im GGW definiert. Erläutern Sie eine widerspruchsfreie Interpretation beider Aussagen am Beispiel einer plötzliche Expansion des idealen Gases. 5.2 Kreisprozesse 1.) Carnot Prozess mit Photongas Betrachtet wird ein Carnot Prozess mit Photongas. Für das Photongas gelten die Zustandsgleichungen U = 3P V , P = σ3 T 4 , σ = (π 2 k 4 )/(15~3 c3 ). a) Leiten Sie mit Hilfe des ersten Hauptsatzes der Thermodynamik die Beziehung her: ∂T ∂V = −(P + δQ=0 ∂U ∂V )/ T ∂U ∂T . V b) Zeigen Sie, daß eine adiabatische Zustandsänderung des Photongases durch T V δ = const. beschrieben wird und bestimmen Sie den Exponenten δ. c) Berechnen Sie die in jedem der vier Schritte ausgetauschten Arbeits- und Wärmemengen und geben Sie den Wirkungsgrad der Maschine an. 2.) Mehrstufiger Kreisprozess Ein thermodynamisches System absorbiert Q1 = 200J von einem Reservoir bei T1 = 400K und zusätzlich Q2 = 300J von einem Reservoir bei T2 = 300K. Anschliessend gibt es eine Wärmemenge Q3 an eine Reservoir der Temperatur T3 ab und kehrt dann zum Anfangszustand zurück. In einem Umlauf leistet das System ausserdem eine Gesamtarbeit W = 100J. a) Wie ändert sich die Entropie des Systems nach Durchlaufen des Gesamtzykels? b) Bestimmen Sie T3 für den Fall, dass der Prozess reversibel ist. c) Der Zyklus sei nun zu einem mehrstufigen Carnot-Prozess erweitert, bei dem 3 isotherme mit 3 adiabatischen Schritten abwechseln. Skizzieren Sie diesen Prozess in einem T S-Diagramm. Welche Bedeutung hat die vom Graphen eingeschlossene Fläche? 3.) Stirling’scher Kreisprozess Betrachten Sie eine Wärmekraftmaschine, die mit einem idealen Gas nach dem folgenden 4-stufigen Zyklus arbeitet: 1-2 2-3 3-4 4-1 isotherme Expansion bei Temperatur T1 vom Volumen V1 auf das Volumen V2 . Isochore Abkühlung von T1 zu T2 . isotherme Kompression bei Temperatur T2 von V2 auf V1 . Isochore Erwärmung von T2 auf T1 . a) Zeichnen Sie das P V -Diagram für diesen Prozess. b) Berechnen Sie den Wirkungsgrad unter der Annahme, dass die im Schritt 2-3 vom System abgegebene Wärmeenergie im Schritt 4-1 vollständig an das System zurückgeführt wird.