Antikörper - theunderground.at
Werbung

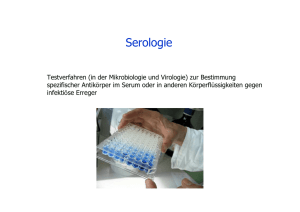
Immunologie Michael Roth Immunologie Antikörper Antikörper sind Glykoproteine mit gemeinsamer Grundstruktur bestehend aus einem Proteinund Kohlenhydratteil. Sie werden im Organismus als Reaktion auf bestimmte Stoffe, die so genannten Antigene (antibody generator) gebildet. Antigene sind körperfremde Moleküle (Proteine, Polysaccharide, Kohlenhydrate). Unter gewissen Umständen können auch körpereigene Stoffe als fremd erkannt werden. Dieser Fehler führt zu Autoimmunerkrankungen. Antikörper erkennen nicht das gesamte Antigen sondern nur die sogenannte antigene Determinante (Epitop). Die entsprechende Antigenbindungstelle am Antikörper heißt Paratop. Struktur von Antikörpern Jeder Antikörper besteht aus je zwei gleichen schweren und leichten Ketten (heavy chains HKetten, light chains L-Ketten). Diese sind durch kovalente Disulfidbrücken zu einer Ypsilonförmigen Struktur verknüpft. Die leichten Ketten bestehen aus jeweils einer variablen und einer konstanten Domäne. Bezeichnet werden diese als VL (variabel) und CL (konstant). Die schweren Ketten hingegen haben jeweils eine variable und 3 (IgG, IgA) bzw. 4 (IgM, IgE) konstante Domänen. Die variablen Domänen Antigenbindungsstelle. einer leichten und Seite 1 von 8 einer schweren Kette bilden die Immunologie Michael Roth Wirkungsweisen von Antikörpern Antikörper haben verschiedene Wirkmechanismen: Neutralisation der Antigene Durch die Bindung des Antigens an den Antikörper wird dieses blockiert und kann seine Wirkung nicht mehr entfalten oder wird durch den angelagerten Antikörper räumlich am Eindringen in Zellen oder Gewebe gehindert. Opsonierung ( „Lecker machen“) Durch Einhüllen mit dem Antikörper wird das Seite 2 von 8 Immunologie Michael Roth Antigen markiert. Die konstante Region des Antikörpers wird von Phagozyten (Fresszellen) erkannt und diese können das Bakterium aufnehmen und verdauen. Aktivierung von NK-Zellen (natürliche Killerzellen, Teil des angeborenen Immunsystems) die fremde Bestandteile abtöten. Dieser Prozess wird auch als „Antibody-dependent cell-mediated cytotoxicity“ (ADCC) bezeichnet. Agglutination (Komplexbildung) Weist ein Antikörper zwei Antigenbildungsstellen auf, kann es zu der Ausbildung einen Komplexes kommen. Antikörperklassen Die einzelnen Antikörper werden mit IgX bezeichnet, wobei Ig für Immunglobuline steht und X für G, M, A, D, E sowie Y oder W stehen kann. Jede Klasse hat andere Eigenschaften und Vorkommen im Organismus. Sie können Monomere, Dimere oder Pentamere sein. Immunglobulin A Macht etwa 15% der Ig im menschlichen Serum aus. Es dient zur Abwehr von Krankheitserregern, vor allem an den Schleimhäuten wie Augen, Nase, Darm oder Rachen. Immunglobulin D IgD macht unter 1% der Ig im menschlichen Serum aus. Seine Funktion ist bis heute nicht genau geklärt. Es liegt als Monomer vor und wird sehr rasch abgebaut. Immunglobulin E IgE macht unter 1% der Ig im menschlichen Serum aus. Es dient zur Abwehr von Parasiten und spielt eine wichtige Rolle bei Allergien. Seite 3 von 8 Immunologie Michael Roth Immunglobin M IgM wird vom Körper in der ersten Phase einer Infektion produziert und dient zur Aktivierung des Komplementsystems. Im Serum zeigt sein Vorkommen eine momentane Infektion an. Die Konzentration an IgM sinkt nach der akuten Phase der Infektion rasch wieder ab. Immunglobulin M, bestehend aus 5 Grundeinheiten 1 Grundeinheit 2 H-Kette 3 L-Kette 4 J-Kette 5 Intermolekulare Disulfidbrücken Immunglobin G IgG macht mit etwa 11-18% des gesamten Bluteiweißes den größten Teil der Ig im menschlichen Serum aus. Es dient zur Produktion von Antikörpern, die vor allem gegen Bakterien wirken. ELISA Enzyme-Linked Immuno Sorbent Assay ELISA ist ein immunologisches Testverfahren, das sowohl qualitativ als auch quantitativ angewendet werden kann. Seine Anwendungsgebiete reichen von medizinischen Untersuchungen (zB. HIV-Test) bis hin zur Lebensmittelanalytik (Bestimmung von unerlaubten Antibiotika/Masthilfsmittel). Dieses Verfahren beruht auf der Bildung des Immunkomplexes aus Antikörper und Antigen. Der ELISA kann indirekt, als Sandwich-ELISA oder auch kompetitiv/konkurrierend durchgeführt werden. Indirekter ELISA Schematische Durchführung eines indirekten ELISA Seite 4 von 8 Immunologie Michael Roth 1. In einem ersten Schritt wird ein Trägermaterial mit Antigen beschichtet, dies kann eine Membran oder eine Kaverne in einer Mikrotiterplatte sein. Bei standardisierten Untersuchungen sind die Titerplatten in einem Testkit bereits beschichtet und können direkt verwendet werden. 2. In einem Zweiten Schritt wird der Erstantikörper zugegeben. Dieser Erstantikörper ist der Antikörper der im Organismus bei Vorhandensein des entsprechenden Antigens gebildet wird. Es wird daher nicht direkt das Antigen untersucht, sondern der als Immunantwort gebildete Antikörper. Die Lösung wird durch Ausklopfen entfernt. Die freien Bindungsmöglichkeiten am Antigen werden mit Proteinen wie BSA (Bovine Serum Albumin) oder Casein vollständig besetzt. Dieser Schritt wird als Blocking bezeichnet. 3. Waschen 4. In einem dritten Schritt wird ein mit einem Enzym markierter Antikörper, der Zweitoder Sekundärantikörper zugesetzt. Er ist meistens ein tierischer Antikörper, für den der an das Antigen gebundene Antikörper selbst ein Antigen darstellt. 5. Der überschüssige nicht gebundene markierte Antikörper wird durch Waschen entfernt. 6. In einem vierten Schritt wird ein Substrat zugegeben. Das Enzym setzt das Substrat um. Das erhaltene Produkt muss entweder zu einer Färbung führen oder ein lumineszierendes oder fluoreszierendes Produkt bilden. Am einfachsten ist die Verwendung eines farbbildenen Reagens, einem Chromogen, und einer Seite 5 von 8 Immunologie Michael Roth anschließenden Auswertung mit einem Spektrometer, wobei die Extinktion der Antikörperkonzentration im Analyten direkt proportional ist. Nachteil dieser Methode ist die mangelnde Selektivität, da verschiedene Bestandteile des Analyten am Antigen gebunden werden können. Sandwich - ELISA Der Unterschied zum indirekten ELISA besteht darin, dass hier zuerst ein Antikörper an der Wand der Kavernen vorliegt, der verschiedene Antigene aus dem Analyten bindet. Dann wird ein auf das gesuchte Antigen spezifischer Antikörper zugesetzt. An diesen lagert sich dann der markierte Sekundärantikörper an. Waschschritte und Blocking sind gleich wie beim indirekten ELISA. Schema eines Sandwich-ELISA Kompetitiver ELISA Hier wird eine bestimmte Menge eines Antikörpers mit einer bestimmten Menge eines markierten Antigens und einer unbekannten Menge eines nicht markierten Antigens versetzt. Je mehr nicht markiertes Antigen vorhanden ist desto mehr des markierten Antigens wird verdrängt und desto geringer ist das Signal. Die Antigenkonzentration ist also indirekt proportional zum Messsignal. Western-Blot Seite 6 von 8 Immunologie Michael Roth Immun-Blot Der Western-Blot dient zur Übertragung der aufgetrennten Proteine auf eine Trägermembran. Eine Durchführung könnte folgendermaßen aussehen: 1. Durchführung einer SDS, einer IEF oder einer anderen geeigneten elektrophoretischen Trennung des Proteingemisches 2. Blotting: Diffusionsplotting Kapilarblotting Anlegen eines senkrecht zum Gel stehenden Stromes und Übertragung der Banden auf eine Trägermembran wie zB. Nitrocellusose, Nylon oder Polyvinyldifluorid. 3. Wenn eine SDS durchgeführt wurde wird das SDS ausgewaschen und die Proteine renaturieren und erhalten ihre Sekundär bzw. Tertiärstruktur teilweise wieder zurück. 4. Freie Bindungsstellen auf der Membran werden entweder durch chemische Polymere oder durch Proteine abgesättigt ( zB. BSA, fettarmes Milchpulver oder Gelatine ). 5. Die Membran wird mit einer verdünnten Antikörperlösung behandelt, der Antikörper muss selektiv auf den Analyten sein, sonst reagiert er mit weiteren Proteinen, die nicht dem Analyten entsprechen. 6. Durch Waschen werden nur schwachgebundene unspezifisch gebundene Antikörper ausgewaschen. 7. Ein markierter Sekundärantikörper wird zugegeben, er muss selektiv gegen den Primärantikörper sein. 8. Durch Waschen wird überschüssiger Sekundärantikörper entfernt. 9. Die Detektion erfolgt bei Enzym-markierten Sekundärantikörpern durch Umsetzen eines Substrates. Häufig wird dafür Peroxidase aus Meerrettich ( hourseradish peroxidase, HRP ) verwendet, die Luminol/-derivate oxidiert und dadurch Lumineszenz hervorruft. Werden Radioaktiv-markierte Sekundärantikörper verwendet werden die die entsprechenden Banden durch Autoradiographie von Röntgenplatten sichtbar gemacht ( Autoradiographie mit Röntgenplatten – Schwarzfärbung der Platte bei radioaktiver Strahlung ). Seite 7 von 8 Immunologie Michael Roth 10. Möchte man keine speziellen Banden sichtbar machen, sondern die gesamten Proteine, so kann man mit Tusche, Coomassie, Poncreu S oder kolloidalem Gold die Gesamtheit der Proteine sichtbar machen. Skizze eines Antigens, das mit einem mit HPR markierten Sekundärantikörpers detektiert wurde Seite 8 von 8