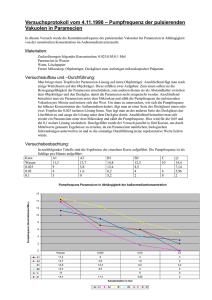
Paramecium
Werbung

Paramecium - Einzeller des Jahres 2007 Görtz H.-D. Universität Stuttgart, Biologisches Institut Das erste Mal gibt es 2007 einen Einzeller des Jahres. Die Deutsche Gesellschaft für Protozoologie will damit aufmerksam machen auf die große Organismengruppe der Einzeller, die Protisten. Zwar sind Einzeller klein, kaum einer kann mit bloßem Auge gesehen werden, jedoch sind sie für die Ökosysteme der Erde wichtig. Grüne Protisten der Meere produzieren mit ihrer Photosynthese mehr Sauerstoff als alle Landpflanzen. Viele Einzeller können Mensch und Tier als Parasiten gefährlich werden. Der Malaria-Erreger, Plasmodium, ist ein Einzeller, der jährlich mehr als 2 Millionen Opfer fordert. Bei den Einzellern gibt es eine große Vielfalt und die Arten sind in Aufbau, Stoffwechsel, Genom-Organisation und Lebensstrategien sehr unterschiedlich. Sie sind deshalb auch für die Forschung in der Zellbiologie, Genetik, Molekularbiologie, Ökologie, Evolutionsbiologie und selbst für die Medizin und pharmazeutische Industrie enorm interessant. Auf dieser Website sind die Wesensmerkmale von Paramecium und einzelne Aspekte aktueller Forschungsthemen mit Paramecien in kleinen Kapiteln dargestellt. Paramecium wurde als erster Einzeller des Jahres ausgewählt, weil es vielleicht der bekannteste Einzeller ist, der oft schon im Biologie-Unterricht vorgestellt wird. Paramecium hat auch praktische Bedeutung bei der Bewertung der Gewässergüte und ist überall auf der Welt ein intensiv untersuchtes Forschungsobjekt. Von Paramecium tetraurelia wurde das Genom sequenziert und wird jetzt untersucht. Man weiss nun, dass das Paramecium-Genom in der Evolution mehrfach verdoppelt worden ist. Die erzeugten Gen-Duplikate könnten für neue Funktionen "genutzt" worden sein. Paramecien, die Pantoffeltierchen, leben in Seen, Teichen und Flüssen. Sie gehören zu den Ciliaten, den Wimperlingen. In einer einzigen Zelle vereinen sie alle Lebensfunktionen. Sie können sich durch Teilung vermehren, sich sexuell fortpflanzen und sie altern. Große Paramecien kann man mit bloßem Auge sehen. Sechs hintereinander messen einen Millimeter. Es gibt viele Paramecium-Arten, zum Beispiel das große P. caudatum, das grüne P. bursaria und das im Brackwasser lebende P. calkinsi. Manche sind nur in bestimmten Regionen der Erde zu finden. Im Meer und im Boden wurden keine Paramecien gefunden. Bauplan von Paramecium aurelia, Länge der Zelle etwa 0,15 mm (aus Berger, Foissner & Kohmann 1997) Paramecien ernähren sich von Mikroorganismen und dienen ihrerseits großen Einzellern, Fischbrut und anderen kleinen Tieren als Nahrung. Sie sind wichtige Bioindikatoren bei der biologischen Gewässeranalyse. Die "farblosen" Arten zeigen starke Verschmutzungen an, wenn sie in größeren Mengen vorkommen, während das grüne Paramecium (P. bursaria) reines bis leicht verschmutztes Wasser anzeigt. Paramecium bursaria beherbergt pro Zelle ca. 300 kleine Grünalgen der Gattung Chlorella. Bei ausreichendem Licht geben die Algensymbionten soviel Maltose, einen Zucker, an die Wirtszelle ab, dass die Paramecien notfalls ihren gesamten Energiestoffwechsel damit decken können. Paramecien sind ideale Objekte für den Biologieunterricht und relativ einfach in Kultur zu halten (*). Zellbiologische Aspekte sind ebenso gut an ihnen darzustellen wie reizphysiologische, genetische, ökologische und evolutionsbiologische Phänomene. Paramecien enzystieren sich nicht, obwohl das vielfach behauptet wird. In einem Heuaufguss sind sie also nicht zu finden, es sei denn, es wird Wasser aus einem natürlichen Gewässer zugesetzt. Für speziell Interessierte wird jeweils eine Auswahl an Fachliteratur aufgeführt. Es sei darauf hingewiesen, dass auf den Jahrestagungen der Deutschen Gesellschaft für Protozoologie immer auch aktuelle Fragen zur Forschung an Paramecien vorgetragen und diskutiert werden. In folgenden Lehrbüchern und Monographien finden Sie zusammenfassende Darstellungen zur Biologie von Paramecium und anderen Ciliaten: Berger H., Foissner W. & Kohamnn F. (1997): Bestimmung und Ökologie der Mikrosaprobien nach DIN 38 410. G. Fischer, Stuttgart, Jena, Lübeck, Ulm. Foissner W., Berger H. & Kohmann F. (1994): Taxonomische und ökologische Revision der Ciliaten des Saprobiensystems. Band III: Hymensotomata, Prostomatida, Nassulida. Informationsberichte des Bayerischen Landesamtes für Wasserwirtschaft, Heft 1/94. Görtz H.-D. (ed.) (1988): Paramecium. Springer Verlag. Hausmann K. & Bradbury P.S. (1996): Ciliates - cells as organisms. G. Fischer, Stuttgart. Hausmann K., Hülsmann N. & Radek R. (2003): Protistology. E. Schweizerbart'sche Verlagsbuchhandlung, Stuttgart. Janisch R. (1987): Biomembranes in the life and regeneration of Paramecium. Purkyne Univ. Brno. Jurand A. & Selman G.G. (1969): The anatomy of Paramecium aurelia. Macmillan St. Martin's Press, New Yourk. Kalmus H. (1931): Paramecium - das Pantoffeltierchen. G. Fischer, Jena. Nanney D.L. (1980): Experimental Ciliatology. J. Wiley & Sons, New York. Plattner H. (2002): My favorite cell - Paramecium. Bio Essays 24: 649. van Wagtendongk W.J. (1974): Paramecium - a current survey. Elsevier Sci. Publ. Amsterdam. Wichterman R. (1986): The Biology of Paramecium, 2nd ed. Plenum Press, New York. (*) Bezug und Kulturanleitung von Paramecien 1) Aus der Natur: Paramecien leben auf der ganzen Erde in Teichen und anderen Süßgewässern und sogar im Brackwasser. Als Bakterien-Fresser leben sie bevorzugt benthisch, überwiegend im Eulitoral, also innerhalb weniger Dezimeter Tiefe am Gewässerrand. Das grüne Paramecium, P. bursaria, ist häufig in der freien Wassersäule anzutreffen. Die Zelldichten sind oft gering; deshalb sind in Wasserproben nicht selten nur ein bis zwei Zellen pro hundert Milliliter anzutreffen. 2) Aus dem Labor: Eventuell kann es sinnvoll sein, Paramecien schon als Reinkultur zu beziehen. Kulturansätze können gegen eine kleine Porto- und Bearbeitungsgebühr von Zoologischen Instituten verschiedener Universitäten bezogen werden, zum Beispiel von Prof. Dr. H.D. Görtz Biologisches Institut Universität Stuttgart Pfaffenwaldring 57 70569 Stuttgart [email protected] (unter Betreff bitte Paramecium angeben) Mailen Sie 3 bis 4 Wochen, bevor Sie die Paramecien benötigen. Nach Terminabsprache und Zusage schicken Sie bitte 3 € für Porto und Materialkosten in Briefmarken. Sie erhalten 25 ml einer P. caudatum- oder P. bursaria-Kultur. Kulturmedien: Stammlösung: 80 g Wiesenheu-/Weizenstroh-Gemisch, mit 1 L Wasser 10 Min aufkochen, über ein Handtuch filtrieren. Die Stammlösung kann eingefroren aufbewahrt werden. Gebrauchslösung: Stammlösung 1 : 25 mit Wasser verdünnen, auf 70 °C erhitzen oder autoklavieren, erkalten lassen. Eventuell sollte der pH-Wert kontrolliert werden (pH 6,5 - 7,5). Mit dieser Gebrauchslösung wird die Paramecien-Kultur verdoppelt. Die Kultur kann man länger stehen lassen, wenn einige aufgekochte Strohhalme in dem Medium belassen werden. Paramecium: die Zelle Görtz H.-D. Universität Stuttgart, Biologisches Institut Paramecium ist ein Einzeller. Paramecien sind auf der gesamten Zelloberfläche bewimpert. Die Zelle ist von der Zellmembran umgeben, die damit auch die Cilien (Wimpern) umgibt. Die Zellmembran ist Abgrenzung, aber auch Ort intensiver Kommunikation mit der Umgebung, das ist für Paramecium nicht anders als für andere Zellen. Viele zellbiologische Erkenntnisse wurden und werden an Paramecium gewonnen. Hier sei auf den Abschnitt 6 "Membrandynamik und Exocytose" verwiesen. Unter der Zellmembran liegen die Alveolen, flache Vesikel, wie sie sich in ähnlicher Form auch bei den anderen Alveolaten (dazu gehören neben den Ciliaten auch die Dinoflagellaten und die Apicomplexe) finden. Bei Paramecium sind die Alveolen von H. Plattner und seiner Arbeitsgruppe als Ca++-Speicher identifiziert worden. Die Cilienaxoneme, die parasomalen Säckchen und die Trichozystenspitzen reichen durch das Alveolen-Netz hindurch bis zur Zellmembran. Über den kontraktilen Vakuolen ist eine Lücke im Alveolen-System und auch im Bereich des Mundfeldes gibt es keine Alveolen. Blockdiagramm des Zellcortex von Paramecium. Unter der Zellmembran und den Alveolen spannen sich Netze verschiedener Cytoskelett-Elemente, in die Organellen wie Cilien mit ihren Basalkörpern, Trichozysten, Mitochondrien eingebettet sind. kf - kinetodesmale Fibrillen; ps parasomales Säckchen; tr - Trichozyste. (Aus Hausmann, Hülsmann & Radeck, Protistology, 2003) Unter den Alveolen liegt ein Mikrotubuli-Netzwerk, in das die Basalkörper (Kinetosomen) der Cilien fest eingebunden sind. Weitere Strukturen des Cytoskeletts konnten insbesondere durch Immunmarkierung unter den Alveolen lokalisiert werden. Die Außenschicht der Zelle mit den Cytoskelett-Netzwerken und den dort eingebundenen Zellorganellen wie Trichozysten und Mitochondrien wird auch als Kortex bzw. als Pellicula bezeichnet. Die erwähnten Trichozysten sind Verteidigungsorganellen, die auf mechanische oder chemische Reize hin exozytiert werden und sich strecken, also quasi abgeschossen werden. Diese Exozytose ist ein äußerst schneller Vorgang, bei dem sich die Proteine der Trichozysten gleichzeitig zu einem pfeilartigen Gebilde strecken. Exozytose und Streckvorgang werden durch Ca++--Ionen induziert. Näheres zur Struktur und zum Exozytosevorgang findet sich auf dieser Website unter Kapitel 6 "Membrandynamik und Exozytose" sowie im Buch "Protozoology" von Hausmann, Hülsmann & Radek (2003). Gequetschte Paramecium-Zelle im Phasenkontrast, fokussiert auf die Cortexebene über der kontraktilen Vakuole. Gut zu erkennen sind Cilien (C, am Rand) und Trichozysten (T, dunkel, flaschenförmig). Die kleinen, blasseren Strukturen sollten überwiegend Mitochondrien sein. Dominierendes Zellorganell ist der große Zellkern, der Makronukleus. Weitere Kerne sind die Mikronuklei - bei einigen Paramecien nur einer, bei anderen zwei und bei einzelnen Arten mehr als zwei. Über die Funktion des Makronukleus lesen Sie im Abschnitt 5 "Fortpflanzung, Sexualität und Vererbung". Weitere Zellorganellen sind die bei Paramecium tubulären Mitochondrien, Peroxisomen und verschiedene Vesikel, aber auch die kontraktilen Vakuolen, die das im Süßwasser kontinuierlich in die Zelle strömende Wasser wieder hinaus pumpen. Weitere Details zur Paramecium-Zelle, zu den Zellorganellen, zur Physiologie der Zelle und zur Vererbung finden Sie in der angegebenen Literatur. Literatur Görtz H.-D. (ed.) (1988): Paramecium. Springer Verlag. Hausmann K. & Bradbury P.C. (1996): Ciliates - cells as organisms. G. Fischer, Stuttgart. Hausmann K., Hülsmann N. & Radek R. (2003): Protistology E. Schweizerbart'sche Verlagsbuchhandlung, Stuttgart. Paramecium: die Gattung Fokin S.I. Biological Institute, St. Petersburg Stage University, St. Petersburg, Russia presently: Visiting Professor at the University of Pisa, Italy [email protected] Die phylogenetische Position von Paramecium wird wie folgt gesehen: Stamm Alveolata, Unterstamm Ciliophora (mit den Schwester-Unterstämmen Dinozoa und Apicomplexa) gehört Paramecium zur Klasse Oligohymenophorea de Puytorac et al., 1974, Ordnung Peniculia Fauré-Fremiet in Corliss, 1956 (siehe Adl et al. 2005). Mehr als 40 Arten der Gattung Paramecium wurden beschrieben, jedoch ist die Zahl der validen Arten geringer. Unlängst wurde vorgeschlagen - in Weiterführung der Vorschläge von Jankowski (1969) - die Gattung Paramecium auf der Basis morphometrischer, biologischer und molekularer Unterschiede (Abbildung) in vier Untergattungen zu unterteilen: Paramecium, Chloroparamecium, Helianter und Cypriostomum. Gattung Paramecium Müller, 1773 Untergattung Paramecium Müller, 1773. Typus-Art: Paramecium (Paramecium) caudatum Ehrenberg, 1833 (Abbildung). Weitere Arten: P. aurelia-Komplex (Abbildung) 15 Arten; P. multimicronucleatum Powers & Mitchel, 1910; P. jenningsi Diller & Earl, 1958; P. wichtermani Mohammed & Nashed, 1968; P. africanum Dragesco, 1970; P. jankowskii Dragesco, 1972; P. ugandae Dragesco, 1972; P. schewiakoffi Fokin et al., 2001. Untergattung Chloroparamecium Fokin et al., 2004. Typus-Art: Paramecium (Chloroparamecium) bursaria Focke, 1836 (Abbildung). Untergattung Helianter Jankowski, 1969. Typus-Art: Paramecium (Helianter) putrinum Claparéde & Lachman, 1858. Weitere Art: P. duboscqui Chatton and Brachon, 1933 (Abbildung) Untergattung Cypriostomum Fokin et al., 2004. Typus-Art: Paramecium (Cypriostomum) calkinsi Woodruff, 1921. Weitere Arten: P. polycaryum Woodruff & Spencer, 1923 (Abbildung); P. nephridiatum Gelei, 1925; P. woodruffi Wenrich, 1928; P. pseudotrichium Dragesco, 1970. Im Augenblick können mindestens 17 Morphospezies in der Gattung erkannt werden. Dabei können neue Arten mit größerer Wahrscheinlichkeit in abgelegenen und daher weniger untersuchten Gebieten (Südamerika, Afrika, tropisches Asien) gefunden werden. Aus den letzten Jahren können eine weitere Morphospezies und zwei eher kryptisch beschriebene europäische Paramecium-Arten - hauptsächlich nach molekularen Daten - ergänzt werden (Fokin et al. 2006). Die geographische Verbreitung vieler Paramecium-Arten unterstützt nicht die Vorstellung, dass alle Ciliaten Kosmopoliten sind. Wegen einiger neuerer Funde ist zu erwarten, dass die Gattung Paramecium mehr Arten als bisher bekannt enthält. Ausserdem müssen auch die europäischen Varietäten erneut untersucht werden. Für die meisten Morphospezies von Paramecium sind genetische Arten nicht definiert (siehe die Übersichtsartikel von D. Nyberg, Y. Tsukii and W.G. Landis in Görtz, H.D. [ed] 1988). Klar ist die Situation für den P. aurelia-Artenkomplex. Sonneborn hat 16 Varietäten (früher als Syngens bezeichnet) im P.aurelia - P. multimicronucleatum-Artenkomplex beschrieben. Nachdem die Syngens als bona fide - Arten erkannt wurden, wurden 14 Arten mit binomialen Namen belegt (Sonneborn 1975): aus Syngen 1 wurde P. primaurelia, Syngen 2 - P. biaurelia, Syngen 3 - P. triaurelia, Syngen 4 - P. tetraurelia usw., bis Syngen 14 - P. quadecaurelia. 1983 wurde eine weitere Art, P. sonneborni, gefunden (Aufderheide et al. 1983). Die sogenannten Syngens von P. bursaria, P. multimicronucleatum and P. caudatum wurden nicht als Arten bezeichnet bzw. mit Binomen belegt, zumal in verschiedenen Fällen Hybrisierungen mit lebensfähigen F2-Nachkommen gezeigt wurden. Die Bestimmung der verschiedenen Paramecium-Arten des P. aurelia-Komplexes gelingt jetzt zweifelsfrei mit der RAPD-Fingerprint-Analyse (Stoeck & Schmidt 1998). Literatur Adl S.A. et al. (2005): The New Higher Level Classification of Eukaryotes with Emphasis on the Taxonomy of Protists. J. Eukaryot. Microbiol. 52: 399-451. Fokin S. I. et al. (2004): Morphological and molecular investigations of Paramecium schewiakoffi sp. nov. (Ciliophora, Oligohymenophorea) and current status of distribution and taxonomy of Paramecium spp. Europ. J. Protistol. 40: 225-243. Fokin S. I. et al. (2006): How many Paramecium species we can expect. Morphological and molecular analysis. Abstr. Int. Meeting "Paramecium genomics" Dourdan, France. Without pagination. Görtz H.D. (ed.) (1988): Paramecium, Springer Verlag, Berlin, Heidelberg. Jankowski A.W., 1969. Proposed classication of Paramecium genus Hill, 1752 (Ciliophora). Zool. J. (Moscow) 48: 30-39 (in Russian with English summary). Stoeck T. & Schmidt H.J. (1998): Fast and Accurate Identification of European Species of the Paramecium aurelia Complex by RAPD-Fingerprints. Microb. Ecol. 35: 311-317. Paramecium als Bioindikator Berger H. & Foissner W. Technisches Büro für Ökologie und Universität Salzburg Drei Paramecium-Arten und ein Art-Komplex sind wichtige Indikatoren bei der biologischen Gewässeranalyse. Die "farblosen" Arten zeigen starke Verschmutzungen an, wenn sie in größeren Mengen vorkommen. Das grüne Paramecium (P. bursaria) indiziert dagegen reines bis leicht verschmutztes Wasser. Paramecien fehlen in zeitweise austrocknenden Gewässern und in terrestrischen Lebensräumen, da sie keine Dauercysten bilden. Die folgenden kurzen ökologischen Charakterisierungen sind dem praktischen Bestimmungsbuch von Berger, Foissner & Kohmann (1997) entnommen. Ausführliche Beschreibungen der Morphologie, Ökologie und Verbreitung dieser Paramecium-Arten sowie vieler anderer in Fließgewässern weit verbreiteter Ciliaten-Arten finden Sie im sogenannten Ciliaten-Atlas (Foissner et al. 1991, 1992, 1994, 1995). Paramecium bursaria (Ehrenberg, 1831) Focke, 1836: Ganzjährig weit verbreitet im Aufwuchs, Detritus und Plankton krautreicher, eutropher stehender (Tümpel, Uferzone von Seen) und langsam fließender (Altarme, lenitische Bereiche eutropher Bäche und Flüsse) Gewässer; ausgeprägtes Maximum von April bis Juni, hohe Abundanzen werden aber selten erreicht. Typisch für moorige und anmoorige Gewässer. Sitzt meist regungslos mit abgespreizten Wimpern im Detritus oder zwischen Algenfäden. Verträgt geringe Mengen an Fäulnisgiften und erreicht in sauerstoffreichen Gewässern auch während intensiver Abbauprozesse mittlere Abundanzen. Selten im Belebtschlamm und in Tropfkörpern. Oligo- bis meso-euryhalin. Kosmopolitisch. Paramecium bursaria frißt Bakterien, Diatomeen und andere Algen, Hefen und Stärkekörner. Eine P. bursaria enthält bis zu 1000 symbiotische Algen der Gattung Chlorella. Zoochlorellenfreie Populationen wurden im Freiland bisher nicht beobachtet; bei erhöhter Temperatur (30°C), Nährsalzmangel und guter Fütterung lassen sich jedoch algenfreie Stämme züchten. Bei Nahrungsmangel ernährt sich P. bursaria von den Photosyntheseprodukten (überwiegend Maltose) ihrer Symbionten. Generationszeit unter Laborbedingungen bei 8,5°C etwa 87 h, bei 15°C etwa 35 h und bei 20°C etwa 20 h. Positiv phototaktisch, negativ geotaktisch. Reagiert empfindlich auf größere pH-Schwankungen, niedrigen Sauerstoffgehalt und höhere Schwefelwasserstoffkonzentrationen. Saprobiologische Einstufung: betamesosaprob bis alphamesosaprob; Saprobienindex = 2,5. Paramecium aurelia-Komplex: Ganzjährig weit verbreitet und manchmal zahlreich (184 Individuen pro cm2) im Detritus, gelegentlich auch im Pelagial (Freiwasser) stehender Gewässer (Tümpel, Weiher, Seen, Stauseen, Altwässer, Moore). In Fließgewässern seltener als Paramecium caudatum und bei geringer bis mittlerer Belastung meist nur sporadisch und mit niedriger Abundanz. Die Schwesterarten haben ziemlich unterschiedliche ökologische Ansprüche, und sogar die Populationen einer Schwesterart zeigen erhebliche Abweichungen, zum Beispiel in der Toleranz von Schwermetallen. Es gibt mehrere Nachweise aus Belebtschlammanlagen, Tropfkörpern und Klärteichen (bis 75000 Individuen pro ml). Auch im Brackwasser; oligo- bis meso-euryhalin. Verbreitung des Komplexes kosmopolitisch, einzelne Arten endemisch. Arten des P. aurelia-Komplexes fressen Bakterien und sind auch axenisch kultivierbar. Generationszeit unter Laborbedingungen bei 8,5°C etwa 111 h, bei 15°C etwa 30 h, bei 20°C etwa 17 h und bei 27°C 5-6 h. Saprobiologische Einstufung: alphamesosaprob bis betamesosaprob; Saprobienindex = 2,9. Paramecium caudatum Ehrenberg, 1833: Ganzjährig zahlreich (120 Individuen pro cm2 und mehr) in stehenden und fließenden Gewässern mit hohem Gehalt an leicht abbaubauren organischen Substanzen und daher hohen Bakteriendichten. Typisches, mikroaerobes Mitglied der polysaproben Ciliatengesellschaft Colpidietum colpodae. Zahlreich bis massenhaft in Sphaerotilus-, Cyanobakterien, Beggiatoa- und Leptomitus-Rasen, zwischen faulenden Algen und Makrophyten, in der verschlammten Uferzone stark verunreinigter Fließgewässer, auf der Oberfläche von Faulschlamm und im Pelagial stark verschmutzter stehender und fließender Gewässer. Verbreitet im Belebtschlamm (zahlreich besonder während der Einarbeitungsphase und bei hoher Belastung und/oder permanenter Sauerstoffarmut), in Emscherbrunnen, in Tropf- und Scheibentauchkörpern, in Stabilisierungsteichen, Rieselfeldern und in der Kahmhaut von stehendem, grauschwarzem, stark nach H2S riechendem Abwasser (bis 40000 Individuen pro ml). Sporadisch und mit geringer Abundanz auch in bakterienreichen Mikrohabitaten reinerer Fließ- und eutropher Stehgewässer, in Thermal- und Schwefelquellen und in Brunnen und Trinkwasserfiltern. Läßt man solche Proben einige Tage stehen ("Aufgüsse"), vermehrt es sich bei einsetzender Fäulnis meist sehr stark. Oligo- bis meso-euryhalin. Kosmopolitisch. Paramecium caudatum frißt überwiegend Bakterien, gelegentlich Algen und Hefe; auch axenisch kultivierbar. Generationszeit bei 25°C etwa 10 h, bei 0°C erfolgt nur alle 19-20 Tage eine Teilung. Paramecium caudatum ist negativ geotaktisch und negativ phototaktisch. Schwimmgeschwindigkeit bei 15°C etwa 0,5 mm/s, bei 30° etwa 1,25 mm/s. Ziemlich unempfindlich gegenüber großen Sauerstoff- und pH-Schwankungen. Saprobiologische Einstufung: polysaprob bis alphamesosaprob; Saprobienindex = 3,6 (Foissner et al. 1994) bis 3,4 (Berger et al. 1997). Paramecium putrinum Claparède & Lachmann, 1859: Besonders im Winterhalbjahr weit verbreitet und manchmal massenhaft im Detritus stark bis sehr stark verschmutzter Gewässer aller Art (Tümpel, Teiche, Altwässer, Bäche, Flüsse, Staugewässer). In Fließgewässern - besonders in stark strömenden Bereichen - oft in größerer Dichte als P. caudatum. Paramecium putrinum bevorzugt bakterienreiche, kühle Gewässer mit hoher Sauerstoffzehrung, fehlt aber bei höheren H2S-Konzentrationen. Spärliches Vorkommen auch in der Oligosaprobie, dort wahrscheinlich in bakterienreichen Mikrohabitaten. Typisches Mitglied der polysaproben Ciliatengemeinschaft Colpidietum colpodae und daher charakteristisch für Sphaerotilus-, Beggiatoa- und Leptomitus-Rasen. Zahlreiche Nachweise aus Emscherbrunnen, Belebtschlammanlagen (besonders bei hoher Belastung und/oder permanenter Sauerstoffunterversorgung), Scheibentauchkörpern und Tropfkörpern (vor allem in der oberen, polybis alphamesosaproben Zone, bei schlecht arbeitenden Anlagen auch weiter unten). Auch in Ästuaren; oligo- bis meso-euryhalin. Fehlt vermutlich in den Tropen, wo es durch andere Arten (z. B. Paramecium pseudotrichium) vertreten wird. Paramecium putrinum frißt Bakterien (Schwefelbakterien, Cyanobakterien, Rhodobakterien etc.), kleine Grünalgen, Kieselalgen, Hefe, heterotrophe Flagellaten und Stärkekörner. Im Freiland ingestiert ein Individuum etwa 48000 Bakterien pro Tag. Generationszeit im Freiland zwischen 15 und 336 h, im Mittel bei 103 h. Fakultativ anaerob. Saprobiologische Einstufung: polysaprob; Saprobienindex = 3,6. Literatur Berger H., Foissner W. & Kohamnn F. (1997): Bestimmung und Ökologie der Mikrosaprobien nach DIN 38 410. G. Fischer, Stuttgart, Jena, Lübeck, Ulm. 291 Seiten. Restbestände noch erhältlich bei www.protozoology.com. Berger H. & Foissner W. (2003): Illustrated guide and ecological notes to ciliate indicator species (Protozoa, Ciliophora) in running waters, lakes, and sewage plants. Handbuch Angewandte Limnologie, 17. Erg. Lfg. 10: 1–160. Foissner W., Blatterer H., Berger H. & Kohmann F. (1991): Taxonomische und ökologische Revision der Ciliaten des Saprobiensystems - Band I: Cyrtophorida, Oligotrichida, Hypotrichia, Colpodea. – Informationsberichte des Bayer. Landesamtes für Wasserwirtschaft, 1/91: 1–478. Foissner W., Berger H. & Kohmann F. (1992): Taxonomische und ökologische Revision der Ciliaten des Saprobiensystems - Band II: Peritrichia, Heterotrichida, Odontostomatida. – Informationsberichte des Bayer. Landesamtes für Wasserwirtschaft, 5/92: 1–502. Foissner W., Berger H. & Kohmann F. (1994): Taxonomische und ökologische Revision der Ciliaten des Saprobiensystems - Band III: Hymenostomata, Prostomatida, Nassulida. – Informationsberichte des Bayer. Landesamtes für Wasserwirtschaft, 1/94: 1–548 (enthält die Gattung Paramecium). Foissner W., Berger H., Blatterer H. & Kohmann F. (1995): Taxonomische und ökologische Revision der Ciliaten des Saprobiensystems - Band IV: Gymnostomatea, Loxodes, Suctoria. – Informationsberichte des Bayer. Landesamtes für Wasserwirtschaft, 1/95: 1–540. Paramecium - Fortpflanzung, Sexualität und Vererbung Hans-Dieter Görtz Universität Stuttgart, Biologisches Institut Paramecien vermehren sich durch Zweiteilung. Das ist eine hochgeordnete Querteilung, der eine Mitose des Mikronukleus vorausgeht (eine geschlossene Mitose, d.h. die Kernhülle bleibt erhalten, die Spindel wird an der Innenseite der Kernhülle gebildet) und ebenso eine amitotische MakronukleusTeilung. Im Verlauf der Kernteilungen beginnt eine komplexe Morphogenese, die in der Cytokinese, der eigentlichen Zellteilung, ihren Abschluß findet. In die Cilienreihen, die sogenannten Kineten, werden dabei zu beiden Seiten der Teilungsebene neue Basalkörper eingereiht. Ein neues, zusätzliches Mundfeld wird gebildet, was nur möglich ist, wenn das alte Mundfeld nicht durch irgendeine Störung verloren gegangen ist. Auch die kontraktilen Vakuolen und andere Organellen werden verdoppelt. Paramecium tetraurelia, die Zellkerne (DAPI-Färbung. Aufnahme: M. Simon) Paramecien haben ein begrenztes Klonalter. Manche P. aurelia-Arten haben nur eine Lebenserwartung von ca. 250 Teilungen, P. bursaria altert erst mit ca. 6000 Teilungen. In der unterschiedlichen Lebenserwartung offenbaren sich die unterschiedlichen Lebensstrategien der Arten. Einige sind sogenannte "inbreeder" und r-Strategen, andere sogenannte "outbreeder" und KStrategen. Die spezifische Form der sexuellen Fortpflanzung von Paramecium ist die Konjugation (Abbildung 1, Abbildung 2). Dabei macht der Mikronukleus eine Meiose durch. Eines der Meioseprodukte (haploid) teilt sich dann mitotisch und eines der Teilungsprodukte wird dabei in die Konjugationspartnerzelle hinüber geschoben. Die Partnerzelle ihrerseits liefert auch einen solchen Wanderkern (entspricht dem männlichen Vorkern). Der jeweils zweite aus diesen Mitosen hervorgehende Kern (Ruhekern, weiblicher Vorkern) bleibt in seiner Zelle. Die beiden Vorkerne (ein Ruhekern und der Wanderkern der Partnerzelle) verschmelzen zum Synkaryon. Jede Zelle produziert also einen männlichen und einen weiblichen Vorkern, ist damit quasi zwittrig. Dennoch kann nicht jedes Paramecium einer Art mit jedem anderen konjugieren. Es gibt vielmehr stets zwei oder mehr Paarungstypen, deren Zellen nur mit Zellen eines jeweils anderen Paarungstyps konjugieren können. Das Synkaryon (diploid) teilt sich zweimal mitotisch. Zwei der resultierenden vier Kerne werden neue Mikronuklei, zwei entwickeln sich zu Makronuklei. Die Zelle teilt sich dann und ihre Tochterzellen haben wieder die normale Ausstattung von einem Mikronukleus und einem Makronukleus. Bei einigen Arten gibt es zwei Mikronuklei oder sogar mehr pro Zelle. Nach einer Konjugation sind die Zellen wieder jung und Ausgang eines neue Klons. Paramecium aurelia, Exkonjugant (DAPI-Färbung). Die Mikronuklei durchlaufen eine Meiose, der alte Makronucleus fragmentiert Manche Arten, typischerweise die Inbreeder unter den Paramecien mit geringer Lebenserwartung, können die sexuelle Fortpflanzung notfalls auch ohne Partner durchführen. Man nennt das Autogamie. Dabei teilt sich wie bei der Konjugation eines der Meioseprodukte, mangels einer Partnerzelle bleiben aber Ruhe- und Wanderkern in einer Zelle und verschmelzen direkt zum Synkaryon. Die interessante genetische Konsequenz der Autogamie ist, dass damit alle Gene gleichzeitig homozygot werden. Da ja Ruhe- und Wanderkern aus demselben haploiden Meioseprodukt hervorgehen, sind nach der Synkaryonbildung jeweils beide Allele eines Gens identisch. Übrigens: Paramecium kann sich nicht enzystieren. Es gibt also keine Paramecien im Heuaufguss. Das Genom von Paramecium tetraurelia Wie alle Ciliaten hat Paramecium einen oder mehrere generative Mikronuklei, die das gesamte Genom im diploiden Satz enthalten, und einen somatischen Makronukleus, der nicht alle Sequenzen des Mikrounkleus besitzt, dessen Gene aber in hoher Kopienzahl, also hoch amplifiziert, vorliegen. Der Makronukleus wird im Zuge der sexuellen Fortpflanzung, der Konjugation, aus dem neuen Mikronukleus aufgebaut (siehe Sexualität). Im Zuge der Makronukleus-Entwicklung wird das Mikronukleus-Genom durchgreifend umstrukturiert, kurze sogenannte intervening eliminated sequences, IES-Elemente, aus den Genen heraus geschnitten ebenso wie das meiste Heterochromatin. Paramecium tetraurelia ist das genetisch am besten untersuchte Paramecium. Ein großes europäisches Konsortium (The European Group of Research, bzw. Groupement de Recherches Européen or GDRE, "Paramecium Genomics") hat unlängst das Genom von P. tetraurelia sequenziert (Aury et al. 2006) und seine Untersuchung begonnen. Schon jetzt zeigen sich interessante Ergebnisse. So hat Paramecium mehr Gene als der Mensch, aber viel weniger Proteine; es gibt anscheinend bei Paramecium kein differentielles splicing. Anscheinend hat Paramecium mehrere Genomverdopplungen erlebt, die letzte wohl vor nicht allzu langer Zeit. Dadurch doppelt vorliegende Gene werden vermutlich als "Spielwiese der Evolution" genutzt und so möglicherweise neue Genfunktionen gefunden. Man darf gespannt sein, was noch alles gefunden wird, zumal in der Vergangenheit ja viele genetische Phänomene bei Ciliaten entdeckt wurden - so z.B. die Ribozyme und die Telomerasen. Schon seit längerem weiß man, dass Paramecium nur das Stoppkodon TGA nutz. TAA und TAG werden als Kodon für Glutamin genutzt. Detaillierte und aktuelle Informationen über das Paramecium-Genom-Projekt sind zu finden unter: http://www.genoscope.cns.fr/externe/English/Projets/Projet_FN/organisme_FN.html Literatur Aury et al. (2006): Nature 444:171-178 Nanney D.L (1980): Experimental Ciliatology. J. Wiley & Sons, New York. Endo- und Exocytose: Membrandynamik in Paramecium Plattner H. Universität Konstanz Paramecium tetraurelia ist ein sehr komplex organisierter Einzeller (Ciliat), dessen (makronukleäres) Genom soeben von einem europäischen Forscherkonsortium unter französischer Federführung mit deutscher Beteiligung sequenziert wurde (Aury et al. 2006, Nature 444:171-178). Mehrfache Duplikationen des Gesamtgenoms könnten eine der Voraussetzungen beispielsweise für die äusserst differenzierten Interaktionen von Membranvesikeln darstellen, wovon sich bei diesem Zelltyp leicht einige Dutzend ausmachen lassen. Beispiele sind die Komponenten des sekretorischen Apparates (namentlich die Exocytose von Trichocysten) und des unvergleichlich komplexen Phagocytose-Zyklus - mit seinen Verbindungen zu Endocytose-Abläufen und zum lysosomalen System sowie mit einem distikten Ort der Exocytose am Ende des Verdauungszyklus (Cytoproct) und Recycling-Vesikeln. Um die Spezifität der einzelnen Membraninteraktionen bei diesen komplexen biogenetischen Prozessen zu gewährleisten, braucht es u.a. jeweils komplexe Kombinationen spezifischer "SNARE"-Proteine, monomerer GTP-Bindeproteine ("G-Proteine", GTPasen), variabler Komponenten einer heterooligomeren H+-ATPase ("Protonenpumpe"') etc. Das europäische Genomprojekt bietet nun die Möglichkeit, die einmalige Vielfalt solcher Interaktionen und ihrer Steuerung molekular aufzuschlüsseln. Einen sehr aktuellen Aspekt bietet auch die nahe Verwandtschaft zu Parasiten aus der Gruppe der Apicomplexa, wie Plasmodium und Toxoplasma (Erreger der Malaria bzw. der Toxoplasmose), welche mit den Ciliaten zu den Alvolata zusammengefasst werden. Es bleibt zu sehen, wieviel sich von der komplexen Calcium-Signalgebung (und der daran beteiligten Moleküle) von Paramecium auf die weniger leicht analysierbaren Parasiten übertragen lässt, bei denen Calcium-Signale die Penetration der Wirtszellen begleiten. Daneben finden sich bei Paramecium Beispiele zur Ausbildung neuer Funktionen duplizierter Gene ("Neofunktionalisation"), aber auch solche, bei denen Mutationen keinen Effekt auf die Translationsprodukte (Proteine) haben. Man kann an diesem Zelltyp buchstäblich der Evolution beim Spielen zuschauen… Endo- und Exozytosewege in Paramecium tetraurelia. Farbig unterlegt sind jeweils: gelb das System der kontraktilen Vakuole; grün - die Exozytose der Trichozysten und Endozytose an parasomalen Säckchen (parasomal sacs); rosa - der Phagozytoseweg. Für Details sei auf Übersichtsartikel verwiesen (s. Literaturliste). Literatur Aury J-M, Jaillon O, Duret L, Noel B, Jubin C, Porcel B M, Ségurens B, Daubin V, Anthouard V, Aiach N, Arnaiz O, Billaut A, Beison J, Blanc I, Bouhouche K, Camara F, Duharcourt S, Guigo R, Gogendeau D, Katinka M, Keller A-M, Kissmehl R, Klotz C, Koll F, Le Mouel A, Lepère G, Malinsky S, Nowacki M, Nowak J, Plattner H, Poulain J, Ruiz F, Serrano V, Zagulski M, Dessen P, Bétermier M, Weissenbach J, Scarpelli C, Schächter V, Sperling L, Meyer E, Cohen J, Wincker P (2006) Global trends of whole genome duplications revealed by the genome sequence of the ciliate Paramecium tetraurelia. Nature 444, 171-178. Kissmehl R, Schilde C, Wassmer T, Danzer C, Nuehse K, Lutter K, Plattner H. (2007) Molecular identification of 26 syntaxin genes and their assignment to the different trafficking pathways in Paramecium. Traffic 8 (in press) Plattner H (2002) My favorite cell - Paramecium. BioEssays 24: 649-658. Plattner H, Kissmehl R (2003) Molecular aspects of membrane trafficking in Paramecium. Int Rev Cytol 232, 185-216. Schilde C, Wassmer T, Mansfeld J, Plattner H, Kissmehl R (2006) A multigene family encoding RSNAREs in the ciliate Paramecium tetraurelia. Traffic 7, 440-455. Wassmer T, Kissmehl R, Cohen J, Plattner H (2006) Seventeen a-subunit isoforms of Paramecium V-ATPase provide high specialization in localization and function. Mol Biol Cell 17, 917-930. Wassmer T, Froissard M, Plattner H, Kissmehl R, Cohen J (2005) The vacuolar Proton-ATPase plays a major role in several membrane bounded organelles in Paramecium. J Cell Sci 118, 28132825. Die Oberflächenantigene: der variable Proteinmantel von Paramecium Simon M. Universität Kaiserslautern Obwohl ein Paramecium bei oberflächlicher Betrachtung sehr einfach gebaut wirkt, so gehört der Organismus dennoch zu den am höchst entwickelten Zellen überhaupt. Neben zahlreichen cytoplasmatischen Differenzierungen, wie z.B. das osmoregulatorische System oder auch der Kerndimorphismus, sind sicherlich die Cilien eines der charakteristischsten Merkmale. Jedoch ist Paramecium nicht "nackt": auf der kompletten Oberfläche, d.h. auf der extrazellulären Seite der Plasmamembran die alle Cilien überzieht, befindet sich eine Proteinschicht. Diese umgibt quasi die ganze Zelle wie ein Mantel und überaus interessant ist dabei, dass Paramecium diesen Mantel wechseln kann! Dieses Phänomen, genannt "Antigenic Variation", ist ein weit verbreiteter Mechanismus, nicht nur bei Protisten: der HI-Virus, der pathogene Pilz Pneumocystis, der Erreger der Malaria Plasmodium und der Erreger der Schlafkrankheit Trypanosoma sind sehr prominente Vertreter von Organismen die wechselnde Protein (Antigen-) Strukturen aufweisen. Sehr unterschiedlich sind dabei die Mechanismen wie dies realisiert wird, d.h. wie insbesondere Genexpression und Antigenwechsel reguliert werden. Dabei sind dies ganz essentielle Fragen, ermöglichen die Antigene, oder genauer gesagt der Wechsel der Antigene doch diesen Parasiten dem Immunsystem der Wirte zu entkommen. Werden von der Immunantwort des Säugers Antikörper gegen die Oberflächenproteine des Einzellers gebildet, führt der Wechsel des Oberflächenmantels dazu, dass diese Antikörper funktionslos werden. Somit ist Antigenic Variation ein Mechanismus der Einzellern die Möglichkeit verleiht chronische Infektionen hervorzurufen. Paramecium bietet ein ideales Testsystem um den gezielten Antigenwechsel zu erforschen und welche Möglichkeiten eine Zelle überhaupt hat, dies zu realisieren. Das Genom von Paramecium tetraurelia weist ca. 100 verschiedene Gene für Oberflächenproteine auf. Diese sind leicht zu identifizieren haben sie doch eine sehr konservative Struktur: Sie besitzen interne Wiederholungen, welche die immunologische Information tragen, d.h. dort findet die Erkennung der Proteine statt. Deswegen bilden sie auch eine spezielle tertiär Struktur die genau diese Bereiche dem umgebenden Medium exponiert. Neben dem N-terminalen ER (Endoplasmatisches Retikulum) Translokationssignal besitzen die Peptide eine C-terminale Signalsequenz die für Anheftung einer GPI-(Glykosylphosphatidylinositol) Ankerstruktur verantwortlich ist. Auf diese Weise werden die einzelnen Proteine in der äußeren Membran befestigt; es sind keine Transmebranproteine. Sehr eindrucksvoll kann man den Antigenwechsel sichtbar machen indem man Antikörper mit Fluoreszenzmarkierungen verwendet: In der Abbildung erkennt man deutlich, wie das alte Antigen (Antigen 51A, grün markiert) sich im Zwischenstadium nur noch auf den Cilien befindet, jedoch das neu synthetisierte Antigen schon auf dem Kortex erscheint. Schon nach wenigen Zellteilungen, also innerhalb von 24 Stunden, wird exklusiv das neue Antigen (hier 51D) präsentiert. Paramecium reagiert auf wechselnde Umwelteinflüsse mit gezielten Antigenwechseln. In über 100 Jahren Forschung wurden viele Auslöser beschrieben, die diesen komplizierten Genregulationsmechanismus initiieren können darunter z.B. starke Temperaturwechsel, aber auch, was zunächst für einen nicht Parasiten überraschend erscheint, die Anwesenheit von Oberflächenprotein spezifischen Antikörpern. Der frei lebende Ciliat regiert also in vergleichbarer Weise wie die parasitischen Protisten und macht sich selbst auf diese Weise zum geeigneten Modellorganismus den gezielten Antigenwechsel zu studieren. Neben vielen Faktoren betreffend der Regulation der Genexpression, die schon identifiziert wurden, bietet nun das Genom Projekt eine extrem gute Arbeitsgrundlage um weitere "Cofaktoren" zu identifizieren, die Antigenregulation mit kontrollieren. Literatur Capdeville Y. (2000): Paramecium GPI proteins: variability of expression and localization. Protist. 151:161-169. Craig A. & Scherf A. (2003) (ed.): Antigenic variation. Elsevier Books, Oxford. Simon M.C. & Schmidt H.J. (2007) Antigenic variation in ciliates. J. Euk. Mikrobiol. 54: 1-7. Simon M. C., Marker S. & Schmidt H. J. (2006b): Post-transcriptional control is a strong factor enabling mutual exclusive expression of surface antigens in Paramecium tetraurelia. Gene Expr. 13: 167-178.