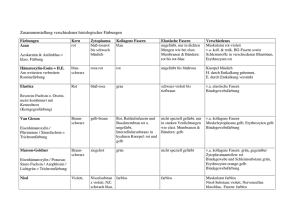
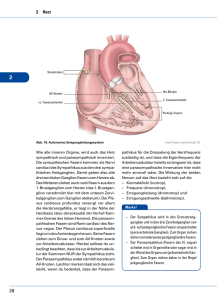
Interzellularsubstanz
Werbung

Interzellularsubstanz 1.) Bindegewebsfasern 2.) Grundsubstanz Bindegewebsfasern • kollagene Fasern • retikuläre Fasern • elastische Fasern kollagene Fasern • häufigste Faserart des BGW • unverzweigt • bilden Faserbündel - gewellter paralleler Verlauf - scherengitterartige Anordnung - geflechtartig • zugfest (bis 6 kp / mm2) • geringe Dehnungsfähigkeit (max. 5 %) - vor Zerreissen – fließen, - verkürzen sich wenn die Spannung nachlässt (dehnen!!) • quellen in saurem Milieu • lösen sich in schwachen Alkalien auf • beim Kochen mit Wasser entsteht Leim (Gelatine) • wenig lichtbrechend im Lichtmikroskop • anisotrop (positiv einachsig doppellichtbrechend) im Polarisationsmikroskop – verstärkt bei Dehnung kollagene Fasern Aufbau • KOLLAGEN: – häufigstes Protein im menschlichen Körper – ca 25% des gesamten Körperproteins – wird von Fibroblasten, Chondroblasten, Osteoblasten, Endothelzellen, glatten Muskelzellen, Fettzellen synthetisiert • besteht aus • Aminosäuren • Peptidketten • Prokollagen (bzw.Tropokollagen)(Durchmesser = 1,5 nm) • Aminosäuren • Glycin (jede 3.Aminosäure) • Prolin und Hydroxyprolin (typisch für Kollagen) • Lysin und Hydroxylysin (für Aggregation zum Prokokollagen) (Vitamin C für Hydroxylierung wichtig – Zahnausfall,Knochenbildungsstörungen) • Peptidketten - 3 Ketten bilden eine Tripel-Helix • Prokollagen - Durch Abspaltung der Registerpeptide entsteht extrazellulär 1 Tropokollagen • 5 Tropokollageneinheiten bilden • Primärfilamente (= 4-5 nm) diese bilden • Mikrofibrillen (= 20-100 nm) • Fibrillen (= 0,2-0,5 μm) • Faser (= 1-15 μm) Kollagenarten • Aufgrund unterschiedlicher Aminosäuresequenzen und unterschiedlicher Primärstrukturen entstehen gering modifizierte Peptidketten (α1,2,3 Ketten) • Die Kombination dieser Peptidketten ergibt verschiedene Kollagenarten (I bis XIX) mit unterschiedlicher Lokalisation und Funktion • Fibrilläre Kollagene – Typ I Sehnen, Bänder, Knochen, Dentin,Faserknorpel – Typ II Hyaliner und elastischer Knorpel – Typ III Retikuläre Fasern – Typ V vergesellschaftet mit Typ I, III – Typ XI vergesellschaftet mit Typ II Benninghoff 2002 • Fibrillen-assoziierte Kollagene – Typ IX Oberfläche von Typ II, Knorpel – Typ XII Oberfläche von Typ I, Sehnen • Nicht-fibrilläre Kollagene – Typ IV Basalmembran (Lamina densa) – Typ VII Verbindung: (Haut) Epidermis-Dermis – Typ VIII Descemetsche Membran - Cornea – Typ X Knorpel Ehlers-Danlos-Syndrom (klinischer Bezug) • Störung der Prokollagenbildung • verschiedene Formen (je nach Kollagentyp) • Hyperelastizität der Haut • erhöhte Zerreißbarkeit der Haut • Erhöhte Beweglichkeit der Gelenke Bindegewebsfasern • kollagene Fasern • retikuläre Fasern • elastische Fasern retikuläre Fasern • sind verzweigt und bilden • dreidimensionale Netzwerke um Einzelzellen Fettzellen, Leberzellen (dargestellt durch Versilberung) • Stützgerüste ganzer Organe (Lymphatische Organe, Leber....) 2 • sind aus Kollagen Typ III aufgebaut, • 3 Peptidketten (Tripelhelix) • Prokollagen • Tropokollagen (extrazellulär durch Abspaltung der Registerpeptide) • Mikrofibrillen = ca 50 nm) – Querstreifung - Periodizität wie bei Kollagenen Fasern • Fibrillen ( = 0,1 μm) • Fasern ( = 0,2 – 1 μm) Bindegewebsfasern • kollagene Fasern • retikuläre Fasern • elastische Fasern elastische Fasern • sind stark lichtbrechend, homogen – bestehen aus Elastin und Mikrofibrillen • bilden Fasernetze und Membranen (z.B:Blutgefäße) • chemischer Aufbau des amorphen Elastins: – Polypeptidkette mit Glycin, Prolin, wenig Hydroxyprolin aber kein Hydroxylysin – Valin, – Desmosin, Isodesmosin nur im Elastin – bilden Querbrücken • Mikrofibrillen werden in amorphes Elastin eingelagert • Mikrofibrillen ( =10-20 nm) bestehen aus dem Protein Fibrillin und den Glykoproteinen Amyloid P und Fibronectin • Mikrofibrillen ohne Elastin nennt man Oxytalanfasern (Zonulafasern – Augenlinse) • Polypeptidketten • (Pro)ELASTIN – = 5-7 nm – verknäuelt sich – nimmt globuläre Form an • bei der Dehnung wird das Molekül gestreckt • elastische Dehnbarkeit: 100-150% • isotrop im entspannten Zustand • anisotrop im gespannten Zustand • lösen sich weder in Säuren noch in Laugen gut auf – im Auswurf bei Tuberkulose und Lungenabzessen nachweisbar • werden synthetisiert von Fibroblasten, glatten Muskelzellen Marfan Syndrom (klinischer Bezug) • Gendefekt für das Protein, Fibrillin – Minderwertigkeit des elastischen – Aortenklappen – Skelettanomalien – Gefäßdefekte (Aotenaneurysmen) – Gewebes Hochwuchs..... – Überstreckbarkeit der Gelenke 3