Ipilimumab (Yervoy®) kann langanhaltende Tumorremissionen
Werbung

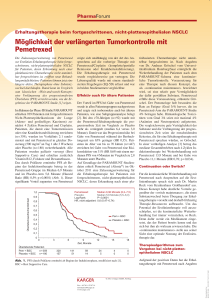
PharmaForum Immuntherapie beim vorbehandelten fortgeschrittenen malignen Melanom Ipilimumab (Yervoy®) kann langanhaltende Tumorremissionen induzieren Der monoklonale Antikörper Ipilimumab interagiert mit dem immunregulativen «Checkpoint»-Molekül CTLA-4 (zytotoxisches T-Lymphozytenantigen 4), das im Normalfall die T-Zell-vermittelte Immunantwort begrenzt und überschießenden Immunantworten vorbeugt [3]. Durch die Blockade des negativen Immunregulativs wird ein Teil der immunsuppressiven Mechanismen außer Kraft gesetzt, die auch dazu beitragen, dass Krebszellen der Zerstörung durch T-Zellen entgehen. Dass mit diesem Wirkprinzip auch erstmals die immuntherapeutisch benötigte Verlängerung der antitumoralen Immunaktivität möglich wurde [4], erklärt möglicherweise auch die Dauer und Nachhaltigkeit der Tumorkontrolle, wie sie schon in der Zulassungsstudie beobachtet wurde: 45,6 vs. 25,3% der Patienten im Vergleichsarm überlebten nach einem Jahr unter Ipilimumab, nach einem weiteren Jahr noch 23,5 vs. 13,7% (Abb. 1) [1]. Zudem wurden unter Ipilimumab Therapieverläufe beobachtet, die sich vom klassischen Tumoransprechverhalten unterscheiden [5]: Klinische Hinweise für eine antitumorale Immunantwort können bis zu 12 Wochen oder auch Monate später auftreten und dann längerfristig sowie nachhaltiger ausfallen, als etwa von Zytostatikatherapien bekannt. In einigen Fällen wurden im Vorfeld des Therapieeffekts sogar zunächst neu aufgetretene Läsionen beobachtet. Die Zulassung von Ipilimumab im März 2011 durch die US-amerikanische Zulassungsbehörde (FDA) und im Juli 2011 durch die europäische Zulassungsbehörde EMA ging auf die große, randomisierte Phase-III-Studie MDX010-20 zurück, die bei vorbehandelten Melanompatienten im nicht-resezierbaren Stadium III oder metastasierten Stadium IV unter der neuen Immuntherapie eine signifikante Verlängerung des medianen Gesamtüberlebens gegenüber der KontrollGesamt therapie gezeigt hat (10,1 vs. 6,4 Monate; p = 0,003). Mit dem Nachweis dieses Überlebensvorteils hat jetzt auch der Gemeinsame Bundesausschuss (G-BA) im Zuge des frühen Nutzungsbewertungsverfahrens den Beschluss zum Hinweis für einen beträchtlichen Zusatznutzen von Ipilimumab begründet (2. August 2012). Durch diesen Beschluss wurde die Kategorie 2 für das gesamte zugelassene Patientenkollektiv bestätigt. Gesamtüberleben, % 100 Ipilimumab im Therapiealltag In der Praxis bestätigen erste Interimsauswertungen von 12 Zentren aus dem deutschen «Compassionate Use»-Programm von Ipilimumab die Ergebnisse der Zulassungsstudie im YERVOY® 10,1 (8,0–13,8)** YERVOY® + gp100-Peptid-Impfstoff* 10,0 (8,5–11,5)** gp100-Peptid-Impfstoff* 6,4 (5,5–8,7)** 80 **Monate (95%-KI) 60 46% 40 24% 20 0 0 4 8 12 16 20 24 28 32 36 40 44 48 52 56 Zeit, Monate * Bei dem gp100-Peptid-Impfstoff handelt es sich um eine experimentelle Verumkontrolle. Abb. 1 Signifikant verlängertes Gesamtüberleben mit Ipilimumab: Die Studienarme trennen sich nach etwa 4 Monaten auf und bleiben konstant getrennt, modifiziert nach [1]. © 2012 S. Karger GmbH, Freiburg Fax + 49 761 4 52 07 14 [email protected] www.karger.com Hinblick auf Verträglichkeit und Wirksamkeit [6]. Wie sich das neue immuntherapeutische Wirkprinzip in den Therapiealgorithmus des vorbehandelten fortgeschrittenen Melanoms integrieren lässt, wird derzeit von den nationalen und internationalen Fachgesellschaften thematisiert: Die amerikanischen Experten haben in der NCCN (National Comprehensive Cancer Network)-Leitlinie zum Melanom bei der systemischen Therapie des fortgeschrittenen Melanoms eine erste Einordnung von Ipilimumab in den Therapiealgorithmus vorgenommen: Demnach profitieren insbesondere Patienten mit noch niedriger Tumorlast von der Immuntherapie, wenn dem Patienten noch ausreichend Zeit verbleibt, die tumorspezifische Immunreaktion zu entwickeln [7]. Die Veröffentlichung der neuen deutschen Leitlinie «Diagnostik, Therapie und Nachsorge des Melanoms» der Deutschen Dermatologischen Gesellschaft (DDG) und der Arbeitsgemeinschaft Dermatologische Onkologie (ADO) wird in Kürze erwartet: Sie entspricht der höchsten Qualitätsstufe (S3) und der Konsultationsfassung zufolge, die bereits Ende Juni zur Kommentierung online ging, wurde die neue Immuntherapie bereits in den Therapiealgorithmus aufgenommen [8]. Die Publikation der Leitlinie wird in Kürze erwartet. Dr. Yuri Sankawa, Stuttgart Literatur 1 2 3 4 5 6 7 8 Hodi FS et al.: N Engl J Med 2010;363:711–23. Dierks C: Onkologie 2012;35(Suppl 2):7. Finn L et al.: BMC Medicine 2012;10:23. Verschraegen C: Cancer Management Res 2012;4:1–8. Wolchok JD et al.: Clin Cancer Res 2009;15:7412–20. Eichhorn C et al.: J Clin Oncol 2012;30(Suppl):abstr e19031. Coit DG et al.: J Natl Compr Canc Netw 2012;10:366–400. Leitlinienprogramm Onkologie, S3 LL Melanom, Version 2.5.: http://hautkrebs.files.wordpress.com/2012/06/s3ll-melanom_konsultationsfassung_v2-6-_29-06-12.pdf. Impressum Immuntherapie beim vorbehandelten fortgeschrittenen malignen Melanom Ipilimumab (Yervoy®) kann langanhaltende Tumorremissionen induzieren PharmaForum in OnkOlOgie 35 l 10 l 12 © 2012 by S. Karger Verlag für Medizin und Naturwissenschaften GmbH Wilhelmstraße 20A 79098 Freiburg, Deutschland Mit freundlicher Unterstützung durch Bristol­Myers Squibb GmbH & Co. KGaA. Verlag, Herausgeber, Redaktion und Verlagsgeschäftsführung übernehmen keine Verantwortung für den Inhalt dieser Rubrik. Downloaded by: 88.99.70.242 - 11/3/2017 8:41:43 AM Besonderheiten der immun­ induzierten Tumorregression Für Melanompatienten im fortgeschrittenen Tumorstadium standen bis vor kurzem keine Therapieoptionen zur Verfügung, die das Mortalitätsrisiko nachweislich hätten senken können. Als First-in-Class-Therapeutikum nutzt Ipilimumab die seit langem bekannte hohe Immunogenität dieser Tumorentität aus und zeigt erstmals eine signifikante VerlänVerlän gerung des Gesamtüberlebens beim vorbehandelten fortgeschrittenen (nicht-resezierbaren oder metastasierten) Melanom [1]. Der Gemeinsame Bundesausschuss (G-BA) hat daher einen Hinweis für einen beträchtlichen Zusatznutzen für Ipilimumab beschlossen. Nationale und internationale Fachgesellschaften beschäftigen sich bereits seit einiger Zeit mit der Frage nach der optimalen Integration des neuen Wirkprinzips in die Therapiealgorithmen beim Melanom. PharmaForum Pemetrexed in der Erstlinientherapie des fortgeschrittenen Nicht-Plattenepithelkarzinoms der Lunge Signifikante Überlebensvorteile mit dem Konzept der «Continuation Maintenance» PARAMOUNT-Studie zur Erhaltungstherapie Patienten, die eine Erstlinientherapie mit Pemetrexed/Cisplatin erfolgreich abgeschlossen haben, können die Behandlung mit Pemetrexed im Sinne einer Erhaltungstherapie weiterführen. Dieses Konzept – das als «Continuation Maintenance» bzw. Erstlinien-Erhaltungstherapie bezeichnet wird – kann nachweislich die weitere Tumorprogression verzögern und das Leben verlängern, wie die zulassungsrelevante PARAMOUNT-Studie zeigt [2]. Die Phase-III-Studie schloss 939 NSCLCPatienten mit lokal fortgeschrittenen oder metastasierten Nicht-Plattenepithelkarzinomen ein, die zunächst eine Induktionstherapie mit 4 Zyklen Pemetrexed (500 mg/m2 an Tag 1 alle 3 Wochen) in Kombination mit Cisplatin erhielten. Patienten mit partieller/ kompletter Tumorremission oder Krankheitsstabilisierung und ausreichendem Performance Status (ECOG 0 oder 1) wurden im Verhältnis 2:1 randomisiert und mit Pemetrexed in gleicher Dosierung oder Placebo weiterbehandelt. In beiden Gruppen wurde mit Vitamin B12, Folsäure und Dexamethason supplementiert und Best Supportive Care angeboten. Pemetrexed (Alimta®) ist ein Multi-TargetEnzym-Inhibitor, der Schlüsselenzyme der DNA- und RNA-Nukleotidsynthese in der Tumorzelle blockiert. In der Erstlinientherapie bei fortgeschrittenen Nicht-Plattenepithelkarzinomen der Lunge (Adenokarzinom und großzelliges Karzinom) ist die Kombination von Pemetrexed und Cisplatin ein Standard [1]. Am deutlichsten fiel der Überlebensvorteil bei Patienten mit Adenokarzinom aus: Sie lebten bei Gabe von Pemetrexed/Cisplatin im Median 12,6 Monate versus 10,9 Monate unter einem Vergleichsregime mit Gemcitabin/Cisplatin. Mit Pemetrexed als Kombinationspartner konnte somit das mediane Überleben dieser HR (unadjusted): 0,78 (0,64–0,96) Überlebenswahrscheinlichkeit 1,0 p = 0,0191 (Log-rank) 0,9 Pemetrexed + Best Supportive Care (n = 359) Placebo + Best Supportive Care (n = 180) 0,8 0,7 Pem + BSC 16,9 Monate 0,6 0,5 0,4 0,3 0,2 0,1 0,0 16,9 14,0 0 3 6 9 12 15 18 21 24 27 30 33 36 Überlebenszeit ab Induktion, Monate ● Im Rahmen der Phase-III-Studie PARAMOUNT erhielten die Studienteilnehmer zunächst vier Zyklen einer Induktionstherapie mit Pemetrexed und Cisplatin und im Falle des Therapieansprechens eine Weiterbehandlung mit Pemetrexed oder Placebo (2:1 randomisiert). Abb. 1. Verlängertes Gesamtüberleben mit Pemetrexed als Erhaltungstherapie, modifiziert nach [3]. © 2012 S. Karger GmbH, Freiburg Fax + 49 761 4 52 07 14 [email protected] www.karger.com Verzögerter Tumorprogress … Der primäre Studienendpunkt war das progressionsfreie Überleben (PFS). Es betrug ab Beginn der Induktionstherapie in der Pemetrexed-Gruppe im Median 6,9 Monate und im Placebo-Arm 5,6 Monate (durch Prüfärzte ermittelt); der Unterschied war signifikant (Hazard Ratio 0,59; 95%-Konfidenzintervall 0,47–0,74; p < 0,0001). Die Monotherapie mit Pemetrexed zeigte ihre Wirksamkeit in allen prädefinierten Studiensubgruppen (differenziert u.a. nach Alter, Performance-Status und Histologie). … und verlängertes Gesamtüberleben Die zur ASCO-Jahrestagung 2012 vorgestellten finalen Ergebnisse der PARAMOUNTStudie [3] beinhalten auch eine Überlebenszeit-Analyse. Demnach erreichten die durchgehend mit Pemetrexed behandelten Patienten ein medianes Gesamtüberleben von 16,9 Monaten (ab Beginn der Induktion) im Vergleich zu 14,0 Monaten bei Gabe von Placebo (s. Abb. 1). Dies entspricht einer signifikanten Risikoreduktion von 22% (HR 0,78; p = 0,0191) zugunsten der Behandlung mit Pemetrexed. 37% der Patienten in der Pemetrexed-Gruppe konnten die Erhaltungstherapie für mehr als sechs Therapiezyklen durchführen, während dies nur 18% der mit Placebo behandelten Patienten möglich war. Der mit Pemetrexed zu erzielende Therapievorteil zeigte sich auch in den Überlebensraten nach einem Jahr (58% vs. 45%) und nach 2 Jahren (32% vs. 21%). Wie schon zuvor bei der Analyse des PFS gezeigt, war es unerheblich, ob die Patienten mit der Induktionstherapie eine Tumorrückbildung oder eine Tumorstabilisierung erreicht hatten. Ein Überlebensvorteil wurde in allen Patientengruppen nachgewiesen und war statistisch unabhängig von Tumorstadium (IIIb oder IV), Geschlecht, PerformanceStatus und anderen Parametern. Nach Angaben von Studienleiter Luis Paz-Ares (Universitätsklinik Sevilla/Spanien) sei PARAMOUNT die erste Studie, die das Konzept der «Continuation Maintenance» untersucht habe. Sie konnte einen Überlebensvorteil für dieses Konzept nachweisen und könne deshalb einen Paradigmenwechsel in der Erstlinientherapie von Patienten mit nicht-plattenepithelialen NSCLC einleiten. Downloaded by: 88.99.70.242 - 11/3/2017 8:41:43 AM Patienten erstmals auf über ein Jahr verlängert werden. Beim fortgeschrittenen nicht-plattenepithelialen NSCLC kann eine kontinuierliche Weiterbehandlung mit Pemetrexed die progressionsfreie Zeit und das Gesamtüberleben der Patienten signifikant verlängern. Dies belegen die Ergebnisse der PARAMOUNT-Studie, die das Konzept der «Continuation Maintenance» umgesetzt hat: Die Patienten wurden nach erfolgreicher Erstlinientherapie mit Pemetrexed/Cisplatin mit Pemetrexed weiterbehandelt und waren somit länger unter aktiver Tumorkontrolle. In einer Interimsanalyse konnte gezeigte werden, dass auch bei den Studienteilnehmern im Alter von über 70 Jahren die Erhaltungstherapie effektiv war und über durchschnittlich 5,5 Zyklen zu jeweils 21 Tagen durchgeführt werden konnte. PharmaForum Die Erhaltungstherapie mit Pemetrexed wurde im Rahmen der PARAMOUNT-Studie vergleichsweise gut vertragen. Die häufigsten unerwünschten Ereignisse (Grad 3/4) waren Anämie (6,4% vs. 0,6%), Neutropenie (5,8% vs. 0%) und Fatigue (4,7% vs. 1,1%). In einer Interimsanalyse zeigte sich, dass die Rate an hämatologischen Toxizitäten (Laborbefunde) bei den älteren Patienten (≥ 70 Jahre) höher war als bei den jüngeren Patienten (21% vs. 7%). Das vorteilhafte Applikationsschema der 10-MinutenInfusion ermöglicht eine ambulante Behandlung, was die Compliance fördert. Wirkung der Erstlinientherapie maximal nutzen Bei der «Continuation Maintenance» wird die Erstlinientherapie durch Nutzung von Pemetrexed als aktiver Therapiekomponente konsequent weitergeführt. Sie schöpft damit ihr Potential sehr gut aus, statt – wie bei der «Switch Maintenance» üblich – auf eine weitere Substanz zuzugreifen. Durch die kontinuierliche Weiterbehandlung mit einem in der Induktionsphase verwendeten Zytostatikum kann der Tumor länger unter aktiver Kontrolle gehalten werden. Die Fortführung der Therapie mit einer schon erfolgreich eingesetzten Erstlinien-Substanz ist im Hinblick auf die Tumorbiologie sinnvoll und entspricht auch dem Vorgehen bei anderen Tumorentitäten, wie Paz-Ares bei der ASCO-Tagung erläuterte. Das Konzept der «Continuation Maintenance» ermögliche die maximale Nutzung einer effektiven Substanz unter Schonung der weiteren Therapieressourcen. Von einer Erhaltungstherapie können auch Ältere profitieren Nicht-kleinzellige Lungenkarzinome machen etwa 70–80% der pulmonalen Tumore aus [4] und sind damit die häufigsten bösartigen Enzym-Inhibitor mit Dreifach-Blockade NSCLC lassen sich anhand der zytologischen und histologischen Befunde in Adenokarzinome, Plattenepithelkarzinome und großzellige Karzinome unterteilen. Der histologische Befund eines Adenokarzinoms oder eines großzelligen Karzinoms ist prädiktiv für das Ansprechen auf Pemetrexed/Cisplatin und ist somit die Voraussetzung für einen guten Erfolg der individualisierten Therapie. Pemetrexed blockiert 3 verschiedene Enzyme, eines davon ist die Thymidylat-Synthase (TS). Sie wird in den histologischen Subtypen des NSCLC unterschiedlich stark exprimiert. Die relativ niedrige TS-Konzentration in Adenokarzinomen könnte erklären, weshalb Pemetrexed bei diesen Tumoren besser wirkt [9]. Dr. Beate Grübler, Hannover Referenzen 1 2 3 Therapieerfolge auch in hohem Lebensalter möglich 4 Diese Subgruppenanalyse ergänzt die bereits vorhandene Datenlage zur Effektivität und vergleichsweise guten Verträglichkeit von Pemetrexed im höheren Lebensalter. In den Studien zur Erstlinientherapie auf Basis von Pemetrexed waren ältere Patienten in den histologischen Subgruppen gleichmäßig vertreten [6]. Das Lebensalter hatte keinen Einfluss auf den Therapieerfolg, tendenziell profitierten die alten Patienten sogar stärker von der Behandlung als die <65jährigen [7]. Aufschlussreich insbesondere im Hinblick auf die Therapie älterer Patienten sind auch die Ergebnisse einer Analyse zum klinischen Nutzen, die Scagliotti et al. [8] auf Basis vorliegender Phase-III-Studienergebnisse [1] vorgenommen haben. Das Gesamtüberleben ohne therapiebedingte Grad-3/4-Toxizitäten («klinischer Benefit») war in der Gesamt- 6 7 8 9. © 2012 S. Karger GmbH, Freiburg Fax + 49 761 4 52 07 14 [email protected] www.karger.com 5 Scagliotti G et al.: J Clin Oncol 2008;26:3543–3551. Paz-Ares L et al.: Lancet Oncol 2012;13(3):247–255. Paz-Ares L et al.: J Clin Oncol 2012;30(suppl):abstr LBA7507 (presented at the ASCO Annual Meeting 2012). www.atlasgeneticsoncology.org/Tumors/LungTumOver viewID5030.html Gridelli C et al.: The European Multidisciplinary Cancer Congress, Stockholm 2011, abstr 9072. Scagliotti G et al.: Oncologist 2009;14(3):253–263. Syrigos KN et al.: Ann Oncol 2009;21(3):556–561. Scagliotti G et al.: Eur J Cancer 2009;45:2298–2303. Ceppi P et al.: Cancer 2006;107:1589–1596. Impressum Pemetrexed in der Erstlinientherapie des fortgeschrittenen Nicht-Plattenepithelkarzinoms der Lunge Signifikante Überlebensvorteile mit dem Konzept der «Continuation Maintenance» PharmaForum in OnkOlOgie 35 l 10 l 12 © 2012 by S. Karger Verlag für Medizin und Naturwissenschaften GmbH Wilhelmstraße 20A 79098 Freiburg, Deutschland Mit freundlicher Unterstützung durch Lilly Deutschland GmbH. Verlag, Herausgeber, Redaktion und Verlagsgeschäftsführung übernehmen keine Verantwortung für den Inhalt dieser Rubrik. Downloaded by: 88.99.70.242 - 11/3/2017 8:41:43 AM Erhaltungstherapie ist praktikabel gruppe der Patienten (n = 1725) bei Gabe von Pemetrexed/Cisplatin signifikant länger als bei Gabe von Gemcitabin/Cisplatin (5,6 Monate vs. 2,8 Monate; HR 0,70, p < 0,001). Bei Patienten mit nicht-plattenepithelialer Tumorhistologie fiel der so definierte Überlebensvorteil noch deutlicher aus (HR 0,64). Ferner war die Überlebensrate ohne Grad-3/4-Toxizitäten in der Pemetrexed/Cisplatin-Gruppe nach 6 Monaten höher (48,1%) als in der Vergleichsgruppe (33,3%), ähnlich groß war der Unterschied nach insgesamt einem Jahr (28,6% vs. 17,9%). DEALM01103 Abb. 2. Zellteilung in einem Adenokarzinom der Lunge Lungentumore. Wegen des zunächst asymptomatischen Verlaufs sind viele NSCLC-Erkrankungen bereits zum Zeitpunkt der Diagnose in einem inoperablen, fortgeschrittenen Stadium. Das mittlere Lebensalter der Patienten mit Lungenkrebs liegt bei etwa 69 Jahren. Vor diesem Hintergrund gingen Gridelli et al. der Frage nach, ob das neue Konzept der Erstlinien-Erhaltungstherapie mit Pemetrexed auch für die große Gruppe der älteren NSCLCPatienten eine effektive Option sein kann. Aufschluss darüber gibt eine Subgruppenanalyse der PARAMOUNT-Studie [5], die voriges Jahr beim European Multidisciplinary Cancer Congress in Stockholm vorgestellt wurde. Die Autoren verglichen in einer Interimsanalyse die Kohorte der ≥ 70jährigen (n = 92; medianes Alter 73 Jahre) mit der Kohorte der <70jährigen (n = 447; medianes Alter 60 Jahre). In beiden Kohorten war die Erhaltungstherapie mit Pemetrexed effektiver als Placebo, dabei zeigte sich der Vorteil im PFS bei den älteren Patienten besonders deutlich: Bei den ≥70jährigen wurde die progressionsfreie Zeit mit Pemetrexed gegenüber Placebo mehr als verdoppelt (median 6,4 Monate versus 3,0 Monate). Damit war das Progressionsrisiko bei Gabe von Pemetrexed während der Beobachtungszeit um 65% geringer (HR 0,35). Die Patienten waren durchschnittlich über 5,5 Zyklen unter Pemetrexed-Therapie und damit deutlich länger als unter Placebo (3,7 Zyklen). Die Studie weise für Pemetrexed einen Nutzen gerade auch für ältere Patienten mit NSCLC nach, bei denen aufgrund von Komorbiditäten eine Krebstherapie bislang als schwierig gelte und teilweise gar nicht angeboten werde, so Studienleiter Dr. Cesare Gridelli (Avellino/Italien). PharmaForum Therapie des metastasierten kolorektalen Karzinoms Hohe Ansprech- und Überlebensraten mit Anti-EGFR-Antikörper In der randomisierten First-Line-Studie PRIME (Panitumumab Randomized Trial In Combination With Chemotherapy for Metastatic Colorectal Cancer to Determine Efficacy [1]) wurde bei insgesamt 1183 Patienten mit unbehandeltem metastasierten kolorektalen Karzinom (mCRC) die Wirksamkeit von Vectibix® (Panitumumab) in Kombination mit FOLFOX (einer Oxaliplatin-basierten Chemotherapie) als Erstlinientherapie untersucht. Der Mutationsstatus des KRAS-Onkogens im Tumorgewebe war ein Stratifizierungsfaktor. Als primärer Endpunkt war das progressionsfreie Überleben (PFS), als sekundäre Endpunkte das Gesamtüberleben und die objektive Ansprechrate definiert. Hier zeigte sich die Rolle des KRAS-Mutationsstatus als prädiktiver Faktor, so PD Dr. Sebastian Stintzing, München: Patienten mit KRAS-Wildtyp wiesen unter der zusätzlichen Panitumumab-Therapie ein hochsignifikant längeres PFS auf als unter der Chemotherapie alleine (10,0 vs. 8,6 Monate; Hazard Ratio (HR) 0,80; p = 0,009). Außerdem war ihre Gesamtüberlebensdauer mit 23,9 Monaten die längste, die bisher überhaupt bei metastasierten kolorektalen Karzinomen unter einer Antikörpertherapie beobachtet wurde [1, 2]: Sie lag mehr als 4 Monate über der mit alleiniger FOLFOX-Therapie (19,7 Monate; HR 0,88; p = 0,17; (Abb. 1)). Dass dieser Unterschied nicht signifikant ausfiel, mag vor allem auch daran liegen, dass im Kontrollarm 25% der Patienten und damit doppelt so viele wie im experimentellen Arm nach Studienende Anti-EGFRTherapien erhalten hatten; außerdem waren bei ihnen diese Second-Line-Therapien viel früher als in der Verumgruppe gegeben worden (median 15,6 vs. 21,5 Monate nach Randomisierung). Auch bei der Ansprechrate war Panitumumab in der KRAS-Wildtyp-Gruppe mit 57% versus 48% signifikant überlegen (p < 0,02). Panitumumab ist damit der bislang einzige Anti-EGFR-Antikörper mit 4,2 Monate Gesamtüberlebensvorteil 100 Überlebenswahrscheinlichkeit, % 90 FOLFOX + Vectibix® 80 FOLFOX 70 HR = 0,88 (95% KI: 0,73–1,06) p = 0,17 60 50 40 30 19,7 23,9 20 10 0 0 2 4 6 8 10 12 14 16 18 20 22 24 26 28 30 32 34 36 38 40 42 44 46 Monate Abb. 1. Gesamtüberleben in der PRIME-Studie, modifiziert nach [2]. © 2012 S. Karger GmbH, Freiburg Fax + 49 761 4 52 07 14 [email protected] www.karger.com positiven Phase-III-Daten beim mCRC in der Kombination mit einer Oxaliplatin-haltigen Chemotherapie. Höchste Ansprechrate in der Second-Line Auch in der Zweitlinientherapie in Kombination mit einer FOLFIRI-Chemotherapie war Panitumumab bei Patienten mit KRASWildtyp erfolgreich, so Stintzing [3]: Neben einem signifikanten Vorteil beim PFS mit median 6,7 versus 4,9 Monaten (HR 0,82; p = 0,023) und einer auch hier nicht signifikanten Überlegenheit beim Gesamtüberleben (14,5 vs. 12,5 Monate; HR 0,92; p = 0,366) zeigte die Kombination aus Panitumumab und FOLFIRI mit 36% die höchste Ansprechrate aller vergleichbaren Optionen in der Zweitlinientherapie (im Kontrollarm 10%; Odds Ratio 5,50; p < 0,0001). Auch hier wurde ein Gesamtüberlebensvorteil sehr wahrscheinlich dadurch verhindert, dass 31% der Patienten im Kontrollarm (vs. 10% derer im Panitumumab-Arm) nach Studienende noch Anti-EGFR-Antikörper erhalten hatten. Hohe Wirksamkeit hat Panitumumab schon lange als Drittlinienbehandlung in der Monotherapie zusätzlich zu «Best Supportive Care» bei «austherapierten» Patienten gezeigt [4, 5] – mit einem Vorteil von 12,3 versus 7,3 Wochen beim PFS (HR 0,45; p < 0,0001) und einer Progressionsrate von lediglich 50%: Jeder zweite Patient mit gegen Chemotherapie refraktärem mCRC profitiert also von der Panitumumab-Monotherapie in der Drittlinie, während von den Patienten, die nur «Best Supportive Care» erhalten hatten, zwei Drittel unter der Behandlung progredient waren. Panitumumab ist also eine hochwirksame und gut verträgliche Therapieoption in allen drei Therapielinien des mCRC. Der frühe Einsatz kann sich für Patienten mit Lebermetastasen positiv auswirken. So konnte eine Posthoc-Analyse der PRIME-Studie zeigen, dass signifikant mehr Patienten, deren Metastasierung auf die Leber beschränkt war, komplett reseziert werden konnten als im Kontrollarm (27,9 vs. 17,5%; p = 0,02). Die Konsequenz: 24 von 27 komplett resezierten Patienten leben noch, in der nicht komplett resezierten Gruppe verstarben hingegen 54 von 91 (59%). Downloaded by: 88.99.70.242 - 11/3/2017 8:41:43 AM In der Therapie des kolorektalen Karzinoms hat vor allem die Einführung monoklonaler Antikörper gegen den Rezeptor für epidermalen Wachstumsfaktor (EGFR) in den letzten Jahren erhebliche Fortschritte gebracht. Für alle Therapielinien zugelassen ist beim kolorektalen Karzinom mit KRAS-Wildtyp inzwischen der vollhumane Anti-EGFR-Antikörper Panitumumab (Vectibix®). Zur Intensivierung der FOLFOX-Chemotherapie in der Erstlinienbehandlung eingesetzt, hat er in einer Phase-III-Studie die bislang längsten Überlebenszeiten bei Tumoren mit KRASWildtyp erzielt. In der Second-Line wird Panitumumab mit FOLFIRI kombiniert und hat in diesem Setting die höchsten Ansprechraten aller vergleichbaren Optionen gezeigt. PharmaForum Interview mit PD Dr. Sebastian Stintzing, München Therapie mit Panitumumab gut verträglich Unsere Klinik hat Erfahrungen mit Panitumumab in allen Therapielinen gemacht. Panitumumab ist nach unseren Erfahrungen gut verträglich, die 2-wöchentliche Gabe ist angenehm, weil man es einfach parallel zur Chemotherapie geben kann und die Patienten dazwischen nicht zwingend gesehen werden müssen. Von den Patienten wird als einzige Nebenwirkung die Hauttoxizität als problematisch angesehen, die aber gut behandelbar ist. In Kombination mit Irinotecan ist die oft als kumulativ dargestellte gastrointestinale Toxizität, also v.a. eine Diarrhö, klinisch nicht wirklich ein Problem. Das kommt vor, aber ich würde sagen, es ist mit den Antikörpern nicht häufiger als ohne und meist klinisch nicht relevant. Panitumumab ist für First-, Second- und «Further»-Line-Therapien zugelassen. Ist es möglich, den gleichen Antikörper beim gleichen Patienten in mehreren Linien, jeweils nach Progress, zu geben? Zu diesem Thema gibt es eine interessante kleine italienische Studie [7], die die Reexposition in «Further»-Line nach einer wie auch immer gearteten EGFR-Antikörper-freien Therapie getestet hat: Patienten, die in der Erstlinie gut auf einen EGFR-Antikörper angesprochen und nach Progress eine Antikörper-freie Therapie Fast alle untersuchten Subgruppen profitieren Hinsichtlich des Überlebens profitierten in der PRIME-Studie nahezu alle untersuchten Subgruppen von der Zugabe von Panitumumab zur FOLFOX-Chemotherapie. Panitumumab zeigte insbesondere einen signifikanten Überlebensvorteil für Patienten mit Lebermetasten und multiplen Metastasen. Fazit Die Zugabe von Panitumumab zur Chemotherapie verbessert Stintzing zufolge Ansprechen, progressionsfreies und Gesamtüberleben von Patienten mit metastasiertem kolorektalem Karzinom und einem Wild-KRASGen [6]. Die Tatsache, dass Panitumumab ein vollhumaner Antikörper ist, macht die erhalten hatten, haben nach erneutem Progress bei Reexposition wieder gut auf den Antikörper angesprochen, sodass eine Reexposition prinzipiell denkbar ist. Dieses Prinzip muss allerdings noch in größeren Studien untersucht werden. In den Studien zur First- und Second-LineTherapie mit Panitumumab war der Unterschied beim Gesamtüberleben nicht signifikant. Was sind die möglichen Gründe dafür? Man kann wohl davon ausgehen, dass der in der progressionsfreien Zeit sichtbare Effekt durch Zweit- oder «Further»-Line-Therapien mit AntiEGFR-Strategien verringert worden ist: So lag ja auch bei der Second-Line-Studie die Ansprechrate mit Panitumumab mit 36% 4-mal so hoch wie mit Chemotherapie alleine, wo sie 9% betrug. Wenn man daher bei Patienten mit KRAS-Wildtyp in der First-Line FOLFOX alleine gibt, und es erhalten dann 25% der Patienten in der SecondLine noch eine Anti-EGFR-Therapie, die wirksam ist bezüglich des Ansprechens – wie das in der PRIME-Studie der Fall war – dann gewinnt man damit natürlich noch einmal Überlebenszeit. Ich denke, das ist einer der Hauptgründe. Es gab in der PRIME-Studie auch Unterschiede bezüglich des Performancestatus. Ist das klinisch relevant für den Alltag? Sollte man den Performancestatus bei der Anwendung berücksichtigen? Da gibt es mehrere Probleme: Zum einen gibt es bei der Bestimmung des ECOG-Status keine wirklich harte Definition. Ich denke, in der Stu- Applikation sehr sicher und zeitsparend, weil keine Vorsichtsmaßnahmen wegen möglicher Überempfindlichkeitsreaktionen zu beachten sind. die wurden unter dem Label «ECOG 2» die vom Allgemeinzustand schlechtesten Patienten geführt. Wenn man den Karnofsky-Status nimmt, ist das übrigens das Gleiche, das ist alles sehr subjektiv gefärbt. Jedenfalls denke ich, dass die Patienten mit ECOG 2 tendenziell den schlechtesten Allgemeinzustand hatten – das waren etwas weniger als 10%, jeweils 20 Patienten in jedem Arm. Deshalb glaube ich, dass man hier keine generelle Antwort für die Praxis geben kann. Der Zulassungstext lässt das offen, d.h. ich kann jedem Patienten eine intensive Therapie anbieten. Aber ich muss mir natürlich überlegen, ob das bei einem Patienten mit ECOG 2 noch sinnvoll ist – wenn, dann sicherlich nur mit dem Ziel einer hohen Remissionschance und einer potenziellen Resektabilität. Ansonsten würden wir bei diesen Patienten doch andere Therapien vorziehen. Intensive Therapie heißt in dem Fall: Eine Chemotherapie-Doublette plus den Antikörper. Wäre es eine Option, in diesem Fall bei einem schlechten Performancestatus eine Monotherapie mit dem Antikörper zu geben? Grundsätzlich ist das denkbar, da EGFR Antikörper eine eigene antitumorale Wirkung besitzen. aber hier muss man graduieren: In der First-Line wird man davor eher zurückschrecken. Hier sind dann mehr Kombinationen denkbar mit einer Monochemotherapie mit 5-FU plus einem Antikörper. Das wäre meines Erachtens eine weniger toxische Therapiemöglichkeit bei älteren Patienten in schlechtem Allgemeinzustand. 4 5 6 7 van Cutsem E et al.: J Clin Oncol 2007;25:1658–1664. Amado RG et al.: J Clin Oncol 2008;26:1626–1634. Siena S et al.: J Natl Cancer Inst 2009;101;1308–1324. Santini D et al.: Ann Oncol 2012,DOI 10.1093/annonc/ mdr623. Josef Gulden, Grafrath Impressum Quelle Therapie des metastasierten kolorektalen Karzinoms 20. Münchener Fachpresse-Workshop «Neues und Wissenswertes aus der Onkologie» am 26. Juli 2012 in München, unterstützt von Amgen GmbH und Mundipharma GmbH & Co. KG Hohe Ansprech- und Überlebensraten mit Anti-EGFR-Antikörper PharmaForum in OnkOlOgie 35 l 10 l 12 © 2012 by S. Karger Verlag für Medizin und Naturwissenschaften GmbH Referenzen Wilhelmstraße 20A 79098 Freiburg, Deutschland 1 2 Mit freundlicher Unterstützung durch Amgen GmbH 3 Douillard JY et al.: J Clin Oncol 2010;28:4697–4705. Douillard JY et al.: J Clin Oncol 2011;29(15S):223s, abstr 3510. Sobrero AF et al.: J Clin Oncol 2012;30(15S):211s, abstr 3535. © 2012 S. Karger GmbH, Freiburg Fax + 49 761 4 52 07 14 [email protected] www.karger.com Verlag, Herausgeber, Redaktion und Verlagsgeschäftsführung übernehmen keine Verantwortung für den Inhalt dieser Rubrik. Downloaded by: 88.99.70.242 - 11/3/2017 8:41:43 AM Welche klinischen Erfahrungen haben Sie selbst mit Panitumumab in der First-Line-Therapie gemacht?