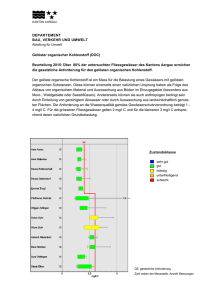
1_Eutrophierung Beurteilung der Gewaessergueter
Werbung

Ausarbeitung der Maturafragen ISGS Frage 1: Gewässereutrophierung 1.Definition: Eutrophierung E. bezeichnet die Gewässeranreicherung mit Pflanzennährstoffen (Überdüngung). Dieser Prozeß finde meist in langsam fließenden oder stehenden Gewässern statt und kann durch menschliche Eingriffe stark beschleunigt werden. Durch den Menschen zusätzlich eingeführte Nährstoffe sind v.a. Zu den wichtigsten Stickstoffverbindungen gehören Ammoniak, Nitrate, Nitrit, Nitrosamine und Stickstoffoxide.Stickstoffverbindungen (Nitrate und Ammonium-Stickstoff) und Im engeren Sinne Bezeichnung für Salze der einfachen Phosphorsäure (Orthophosphorsäure H3PO4). Phosphate. Sie stammen aus abgeschwemmten Düngemitteln und aus dem kommunalen Man unterscheidet kommunales Abwasser und Industrieabwasser. Kommunales Abwasser enthält neben schadstoffbelastetem Regenwasser (z.B. Auswaschung von Fahrbahnen/Parkplätzen) häusliche Abwässer mit Fäkalien, Speiseresten, Desinfektionsmitteln und Spül- und Reinigungsmitteln, die schwer abbaubare Bestandteile enthalten können. Abwasser (siehe Fäkalien Exkremente, Zur Säuberung von Textilien im wässrigen Medium bestimmte, komplex zusammengesetzte Wirkstoffgemische, die immer Tenside, meist auch Gerüststoffe, Bleichmittel etc. enthalten.Waschmittel) und gelangen gemeinsam mit natürlichen Nährstoffen (z.B. durch den Laubfall) in die Gewässer (Gewässerbelastung). In Seen setzt durch das große Nährstoffangebot ein Massenwachstum von Algen ein (Phyto-Im Wasser schwebende, mikroskopisch kleine Organismen, die sich nicht selbst fortbewegen können.Plankton). Die Artenreiche Abteilung des Pflanzenreichs. Niedere, autotroph lebende Pflanzen aus einzelnen Zellen oder Zellverbänden, die zumeist im Wasser, aber auch Boden leben.Algen trüben das Wasser ist eine Verbindung von zwei Wasserstoff- und einem Sauerstoffatom. Die Bezeichnung Wasser wird v.a. für den flüssigen Aggregatzustand verwendet, im festen, also gefrorenen Zustand wird es Eis genannt, im gasförmigen Zustand Wasserdampf Wasser bedeckt rund 2/3 der Erdoberfläche und befindet sich in einem ständigen Kreislauf.Wasser, so dass nach einiger Zeit nur noch in der oberflächennahen Schicht genügend Licht gehört zur elektromagnetischen Strahlung, es umfasst den für Menschen sichtbaren Spektralbereich zwischen UV-Strahlung und Infrarotstrahlung.Licht für die In einem komplexen Prozess, Photosynthese genannt, zerlegen diese Lebewesen mit Hilfe von Sonnenlicht und ihrer Blutfarbstoffe, vor allem den grünen Chlorophyllen, Wasser in seine Bestandteile Sauerstoff und Wasserstoff.Photosynthese vorhanden ist. Die Algen der tieferen Schichten sterben ab. Durch die anschließenden Zersetzungsprozesse werden große Mengen an Chemisches Element der VI. Hauptgruppe, Symbol O, Ordnungszahl 8, Siedepunkt 182,97 °C, Schmelzpunkt –218,79 °C, bei Normalbedingungen farb- und geruchloses Gas, tritt normalerweise als S.-Molekül auf, kann aber auch kurzzeitig atomar oder als Ozon auftreten. Es ist das häufigste Element auf der Erde (Erdrinde 46,5 Gew-%, Gewässer 89 Gew-%, Luft 23 Gew-%). Sauerstoff verbraucht (Als Sauerstoffzehrung bezeichnet man den Verbrauch von Bassem BOUHAFA Seite 1 Ausarbeitung der Maturafragen ISGS Sauerstoff beim Abbau von organischen Bestandteilen durch Mikroorganismen in Gewässern.Sauerstoffzehrung). In fortgeschrittenem Stadium führt dies zu Fäulnis und Bildung toxischer Stoffe wie z.B. A. ist ein farbloses Gas mit stechendem Geruch. Ammoniak, Schwefelwasserstoff ist eine Verbindung aus Schwefel und Wasserstoff, die nach faulen Eiern riechendes Ga wobei der Geruch des farblosen, sehr giftigen Gases noch in einer Verdünnung von 0,1 ppm wahrnehmbar ist.Schwefelwassersto und Methan ist ein farbloses, geruchloses, ungiftiges Gas, das zu Kohlendioxid und Wasser verbrennt. Methan gehört zu den klimarelevanten Treibhausgasen. Methan ist der Hauptbestandteil von Erdgas und Biogas und im Holzgas enthalten.Methan. Die Gesamtartenzahl sinkt sehr stark ab, es kann zu einem verstärktem siehe Sauerstoffzehrung, Eutrophierung, Fischerei, Meeresverschmutzung, Ölpest, EndosulfanFischsterben kommen, der See „kippt um“ (Hypertrophie). Um Eutrophierung zu verhindern oder bereits überdüngte Gewässer in einen niedrigeren Trophiezustand (System zur Bestimmun der Gewässergüte von Seen anhand der Intensität der pflanzlichen Produktion im Gewässer.Trophiesystem) zurückzuführen, mu die Nährstoffzufuhr verringert werden. Möglichkeiten Maßnahmen sind: Verringerung des Phosphateintrags z.B. durch biologische Phosphatelimination oder Phosphatfällung (Fällung) in der dritten Reinigungsstufe (weitergehende Die Abwasserreinigung wird meist in Kläranlagen durchgeführt. In der mechanischen ersten Stufe einer Kläranlage werden durch Rechen, Sandfang und Absetz- oder Vorklärbecken grobe Bestandteile, Sand und absetzbar Stoffe abgetrennt. Abwasserreinigung), Die sich seit Ende der 60er Jahre abzeichnende Brisanz des Phosphateintrags in unsere Oberflächengewässer (Eutrophierung) führte schon frühzeitig zur Entwicklung von P..Phosphatersatzstoffe in Waschmitteln, Die ist eine Möglichkeit der Sanierung eutrophierter Seen, die durch die Einleitung von Abwässern verunreinigt sind (Eutrophierung, Gewässersanierung).Ringkanalisation. Verringerung des Stickstoffeintrags z.B. durch biologische Stickstoffelimination in der dritten Reinigungsstufe (Die Abwasserreinigung wird meist in Kläranlagen durchgeführt. In der mechanischen ersten Stufe einer Kläranlage werden durch Rechen, Sandfang und Absetz- oder Vorklärbecken grobe Bestandteile, Sand und absetzbare Stoffe abgetrennt. Abwasserreinigung, 1.) In schlecht durchlüfteten Böden veratmen Mikroorganismen (Denitrifikanten) den in Nitrat (NO3) gebundenen Sauerstoff. Als Ergebnis der D. entweichen elementarer Stickstoff, Stickoxide (N2O) und Ammoniak aus dem Boden.Denitrifikation, siehe Mikrobielles Transformationsvermögen.Nitrifikation) und v.a. geringeren Düngemitteleinsatz in der Oberbegriff für gewerblichen Pflanzenanbau und Tierhaltung. Landwirtschaft (ökologischer Landbau). Während v.a. seit 1990 der Nährstoffeintrag aus dem Man unterscheidet kommunales Abwasser und Industrieabwasser. Kommunales Abwasser enthält neben schadstoffbelastetem Regenwasser (z.B. Auswaschung von Fahrbahnen/Parkplätzen) häusliche Abwässer mit Fäkalien, Speiseresten, Desinfektionsmitteln und Spül- und Reinigungsmitteln, die schwer abbaubare Bestandteile enthalten können. Abwasser durch aufwendigere Klärtechnik erheblich reduziert werden konnte, befindet sich der Nährstoffeintrag aus der Oberbegriff für gewerblichen Pflanzenanbau und Tierhaltung. Landwirtschaft (diffuse Einträge) weiterh auf hohem Niveau. Nach einer Verringerung der Nährstoffeinträge reagieren Seen nur sehr langsam auf die verbesserte Nährstoffsituation, da Nährstoffe im Boden ist ein Teil der belebten obersten Erdkruste. Boden gespeichert und später wieder freigesetzt werden können. Ursprünglich nährstoffarme Seen (Nährstoff- und humusarm (Gegensatz: eutroph)oligotroph) lassen sich aufgrund des atmosphärischen Nährstoffeintrags meist nicht mehr in den Ausgangszustand zurückversetzen. Bassem BOUHAFA Seite 2 Ausarbeitung der Maturafragen ISGS Eutrophierung ist die Nährstoffanreicherung in einem Gewässer und damit verbundenes übermäßiges Wachstum von Wasserpflanzen (z. B. Algen, Laichkraut). Mit dem Abwasser (u. a. Rückstände von Wasch- und Reinigungsmitteln, Fäkalien) und Abschwemmungen landwirtschaftlicher Flächen (Düngung) können große Mengen Nährstoffe (vor allem Phosphate und Nitrate) in die Gewässer gelangen und das Wachstum der Wasserpflanzen beschleunigen. Durch das vermehrte Absterben von Pflanzen wird bei dem anschließenden Zersetzen übermäßig Sauerstoff verbraucht. Fällt der Sauerstoffgehalt des Wassers unter ein bestimmtes Mindestmaß, hört der Abbau organischer Verunreinigungen durch aerobe Bakterien auf. Bei den danach von anaeroben Bakterien verursachten Zersetzungsprozessen können sich giftige Stoffe wie Schwefelwasserstoff, Ammoniak oder Methan bilden. Das Gewässer beginnt „umzukippen“ (Fischsterben und belästigende Gerüche). Kläranlagen mit weitergehender Reinigung (dritte Reinigungsstufen) können die Nährstoffbelastung der Gewässer erheblich verringern 2. Zusammenfassung der Eutrophierung: Wichtige Nährstoffe für das Wachstum von phototropen Organismen sind N und P. Unkontrollierter Algenwachstum(dh. Eine starke Biomasseproduktion). Lichtmangel(Algen absterben). Diese werden von heterotrophen Organismen abgebaut. Es kommt rasch zu einem O2 –Mangel. Sodass können nur noch anaerobe Prozesse ablaufen. Das Umkippen vom Wasser. Frage 2: Beurteilung der Gewässergüte Die Qualität der Gewässer lässt sich durch biologische, chemisch- physikalische und bakteriologische Indikatoren charakterisieren. 1. Arten der Beurteilungsmöglichkeiten 1.1 Formen der Beurteilungsmöglichkeiten Chemisch – physikalische Arten Biologische Arten Chemischer Sauerstoffbedarf (CSB) Biochemischer Sauerstoffbedarf (BSB) Totaler gesamter Kohlenstoff (TOC) Adsorbierbare organische gebundene Halogene (AOX) Bassem BOUHAFA Seite 3 Ausarbeitung der Maturafragen ISGS pH – Wert NH4+, NO3-, PO43-, SO42-, Cl-, NO2 Einwohnergleichwert (EGW) 1.2. Übersicht über die Verschiedene Verfahren Parameter CSB BSB TOC CSB / TOC AOX POX EOX Angabe in mg O2/L mg O2/L nach n Tagen mg C/L mg O2/mg C mg Cl/L mg Cl/L mg Cl/L Aussage Verunreinigungen mit chem. oxidierbaren org. Substanzen Verunreinigung mit biochem. Abbaubaren Substanzen Kohlenstoffgehalt der org. Verunreinigungen Wie viel O2 für die Oxidation von 1mg C nötig ist Verunreinigung mit org. Halogenverbindungen Verunreinigungen mit leichtflüchtigen org. Halogenverbindungen Verunreinigungen mit extrahierbaren org. Halogenverbindungen. 2. Chemischer Sauerstoffbedarf (CSB) Der CSB ist ein Summenparameter für die Verschmutzung von Wasser / Abwasser mit oxidierbaren organischen Stoffen. Die Methode gibt keine Auskunft über die Art der Verbindungen, außerdem gibt der Messwert keine Auskünfte über die Masse der Verschmutzung (560mg Oxalsäure und 48mg Ethanol haben den gleichen CSB – Wert von 100mg O2/L) 2.1 Chemische Grundlage K2Cr2O7 – Methode Organische Substanzen werden in stark schwefelsaurem Milieu mit Kaliumdichromat zu CO2 und H2 O oxidiert. Der Cr2O72- - Verbrauch kann entweder direkt oder indirekt bestimmt werden. Bei der Normmethode wird der Verbrauch an Dichromat indirekt durch die Titration des Überschusses mit Mohr`schem Salz [(NH4)2Fe(SO4)2)] bestimmt. Küvettenschnelltest Bei dem Schnelltest (Küvettentest) kann die photometrische Bestimmung sowohl indirekt, das überschüssige Dichromat wird bei einer Wellenlänge von 435nm durchgeführt, als auch direkt erfolgen. Bei der direkten Bestimmung wird das gebildete Cr3+ bei 620nm gemessen. Der Unterschied der beiden Methoden liegt im Messbereich. Mit der indirekten Methode kann eine Konzentration von 10150mg O2/L gemessen werden. Die der direkten hingegen hat einen Messbereich von 100-1000mg O2/L. Störungen des CSB können durch alle anorganischen Verbindungen hervorgerufen werden. z.B.: Chlorid, Nitrit, Sulfid, … Da Chlorid in Wasserprobe oft in höheren Konzentrationen vorliegt, stört es am häufigsten. Bassem BOUHAFA Seite 4 Ausarbeitung der Maturafragen ISGS Bis zu einer Konzentration von 1g Cl-/L kann HgCl2 als Komplexbildner zugesetzt werden. Bei höheren Konzentrationen muss die Probe verdünnt werden. 2.2 KMnO4 – Methode Dieses Verfahren ist nur für Trinkwasser und mittelbelastete Oberflächengewässer geeignet, da organische Stoffe nicht vollständig oxidiert werden. Die Probe wird mit einem Überschuss an KMnO4 versetzt, am Wasserbad für mindestens 10 Minuten auf 100°C erhitzt und mit einem Überschuss an Oxalsäure versetzt. Der nicht verbraucht Oxalsäure – Überschuss wird mit KMnO4 rücktitriert. Die Konzentrationsangabe erfolgt ebenfalls in mg O2/L 2.3 Biochemischer Sauerstoffbedarf(BSB) Der biochemischer Sauerstoffbedarf (BSB, engl. biochemical oxygen demand, BOD) ist eine Maßzahl für die Menge an im Wasser gelöstem Sauerstoff, der zum biologischen Abbau gelöster organische Verbindungen im Abwasser benötigt wird. Grundlage ist der biochemische Abbau von organischen Substanzen in Gewässern. Es wird dabei von den eingesetzten Bakterien O2 verbraucht. Der Vorteil des BSB zum CSB ist die Simulation der Realität. Man weiß dadurch, was in der Natur wirklich abgebaut wird. Probleme bei den Bestimmungen sind mögliche Parallelreaktionen, wie zum Beispiel die Nitrifikation. Es muss daher bei jeder Bestimmung angegeben werden, ob Hemmstoffe zugegeben wurden, oder ob die Nitrifikation im Ergebnis berücksichtigt wurde. 2.3.1 Durchführung Die Probe wird mit einem Überschuss an O2 in Kontakt gebracht, danach für n – Tage bei 20°C und in Dunkelheit aufgehoben. Bei sterilen Proben wird das Wasser geimpft (z.B.: mit Wasser aus einer Kläranlage, Erdextrakt); bei Proben aus Kläranlagen ist dies nicht nötig. Außerdem ist eine Zugabe von Nährsalzen nötig, wie zum Beispiel N, P, Ca, Mg, … 2.3.2 Verdünnungsmethode Bei der am häufigsten Verwendeten Methode, der Verdünnungsmethode wird die Probe mit O2 – gesättigtem Wasser in unterschiedlichen Verhältnissen verdünnt und Luftblasenfrei in Glasflaschen aufgefüllt. Die Messung muss auf jeden Fall an Tag 0 und an Tag n durchgeführt werden, um über die Differenz den O2 – Verbrauch errechnen zu können. Der O2 – Gehalt an Tag n darf nicht 0 sein. Sollte er in allen Verdünnungen 0, oder knapp bei 0 liegen, so muss die Messung wiederholt werden. Die Bestimmung erfolgt amperometrisch mit einer Messzelle nach Clark. Bassem BOUHAFA Seite 5 Ausarbeitung der Maturafragen ISGS Sauerstoff geht durch die Membran durch. Es stellt sich ein Gleichgewicht ein zwischen Probe und Elektrode. O2 + 2H2 O + 4e- 4OH- 2.3.3 Manometrische Methode Das zu untersuchende Wasser wird in eine Flasche eingebracht, wobei ein Großteil der Flasche mit Luft gefüllt bleibt. Die Flasche wird luftdicht verschlossen und der Druck in dem Gefäß mit einem Manometer bestimmt. Das entstehende CO2 wird chemisch gebunden. Der Sauerstoffverbrauch bewirkt eine Druckabnahme, woraus der Biologische Sauerstoffbedarf errechnet werden kann. Die Apparatur wird bei konstanter Temperatur gehalten. Vorteil des Verfahrens ist die Möglichkeit der laufenden Aufzeichnung der Entwicklung des Sauerstoffbedarfs. Nachteilig ist der erhebliche apparative Aufwand. 2.3.4 Coulometrische Methode Wie bei der manometrischen Methode wird die Probe mit einem O2 – Überschuss angesetzt und das entstehende CO2 absorbiert in NaOH. Der O2 wird elektrochemisch hergestellt. Der Stromverbrauch dient als Messgröße, der Stromverbrauch wird direkt aufgezeichnet. 3. Gesamter organischer Kohlenstoff (TOC) 3.1 Definition Der gesamte organische Kohlenstoff oder TOC (engl.: total organic carbon) ist ein Summenparameter in der Wasser- und Abwasseranalytik und spiegelt die Belastung des Wassers mit organischen Stoffen wieder. Dabei wird die Konzentration des gesamten organisch gebundenen Kohlenstoffs im Wasser bestimmt und meist in automatisierten Messverfahren ermittelt. 3.2 Begriffe a) TC Gesamter Kohlenstoff (Total Carbon): Er umfasst die Summe des organisch und anorganisch gebundenen Kohlenstoffs in gelösten und ungelösten Verbindungen b) TIC Gesamter anorganisch gebundener Kohlenstoff (Total Inorganic Carbon) Darunter versteht man die Summe des anorganisch gebundenen Kohlenstoffs in gelösten und ungelösten Verbindungen. c) TOC Gesamter organisch gebundener Kohlenstoff (Total Organic Carbon): Bassem BOUHAFA Seite 6 Ausarbeitung der Maturafragen ISGS Das ist die Summe des organisch gebundenen Kohlenstoffs in gelösten und ungelösten Verbindungen. d) DOC Gelöster organisch gebundener Kohlenstoff (Dissolved Organic Carbon): Damit wird die Summe des in gelösten organischen Verbindungen enthaltenen Kohlenstoffs angegeben. e) POC Flüchtige organischer Kohlenstoff (Purgeable Organic Carbon) Der Anteil des TOC, der unter den Bedingungen dieses Verfahrens austreibbar ist. f) NPOC Nicht flüchtige organischer Kohlenstoff (Non Purgeable Organic Carbon) Der Anteil des TOC, der unter den Bedingungen dieses Verfahrens nicht austreibbar ist. 3.3 Verfahrensgrundlage anhand der Verbrennungsmethode: Verbrennung der Probe in einem beheizten Reaktor: 2C+2O2 -----------------2CO2 Verbrennungsgase werden mit einem Trägergas transportiert, entfeuchtet, getrocknet und abschließend mittels eines nicht dispersiven Infrarotdetektor NDIR detektiert. 3.4 Rechenverfahren a) Differenzverfahren (TOC = TC – TIC) Zuerst wird TC ermittelt und bei einer zweiten Messung die TIC und abschließend durch eine Abstraktion des TIC vom TC wird der gesamten Anteil an TOC ermittelt. b) Direktverfahren (TOC als NPOC) Vor der Messung wird der Probe angesäuert, dabei erfolgt die Umwandlung vom TIC über kohlensäure in CO2. Das entstehende CO2 gas wird mit einem inertem Treibgas aus der Probe getrieben. Dabei gehen allerdings auch flüchtige Säuren, sowie alle leicht flüchtigen organischen Substanzen für die Messung verloren. Deshalb wird auch der so erhaltene TOC als „NPOC“ (Non Purgeable Organic Carbon, nicht ausblasbarer organischer Kohlenstoff) bezeichnet. c) Additionsverfahren Leicht flüchtige organische Verbindungen werden beim Direktverfahren nicht mit erfasst. Darf ihr Anteil am TOC nicht vernachlässigt werden, setzt man das „Additionsverfahren“ ein. Dazu wird der ausgeblasene Gasstrom vom CO2 befreit und die enthaltenen flüchtigen Verbindungen anschließend oxidiert und bestimmt. Der so erhaltene „POC“ (Purgeable Organic Carbon) wird dann mit dem NPOC zum TOC addiert. 4. Einwohnergleichwert (EGW) Der Einwohnergleichwert dient als Referenzwert der Schmutzfracht in der Wasserwirtschaft. Er kann auf den Biochemischen Sauerstoffbedarf (BSB5), den Chemischen Sauerstoffbedarf (CSB), den Stickstoff, den Phosphor, den TOC (Totalen Organischen Bassem BOUHAFA Seite 7 Ausarbeitung der Maturafragen ISGS Kohlenstoff), die Schwebstoffe oder auf den Wasserverbrauch bezogen werden. Er gibt jeweils das Äquivalent der Tagesmengen dieser Stoffe bzw. Verbräuche im Abwasser eines Einwohners an. Die Summe aus tatsächlichen Einwohnern EZ (Einwohnerzahl) und Einwohnergleichwerten EGW als Maß für die Schmutzfracht aus Industrie, Gewerbe, Landwirtschaft etc. ergibt den für die Bemessung von Abwasserreinigungsanlagen wichtigen Einwohnerwert EW. Es gilt: EW = EZ + EGW Mit Hilfe des Einwohnerwertes lässt sich die zu erwartende biologische Belastung von Kläranlagen abschätzen. 5. Saprobienindex: Als Saprobie wird die Belastung eines Gewässers mit toter organischer Substanz bezeichnet. Die organischen Substanzen werden im natürlichen Stoffkreislauf durch Organismen abgebaut und dabei Sauerstoff verbraucht (aerobe Organismen). Wird der verbrauchte Sauerstoff nur in ungenügenden Maß wieder ins Gewässer eingebracht, übernehmen anaerobe Organismen den Abbau (Fäulnis). Aus der Beobachtung, dass verschiedene Wasserorganismen unterschiedliche Beziehung zur Saprobität besitzen, haben KOLKWITZ & MARSSON vier Saprobienstufen eingeführt und die dazugehörigen Lebensgemeinschaft beziehungsweise Leitformen beschrieben. Liebmann (1951) hat diese vier Stufen als Güteklassen bezeichnet und ihnen Farben zugeordnet. Saprobie Gewässergüteklasse Farbe organische Belastung oligosaprob I blau beta - mesoaoprob alpha - mesosaprob II III grün gelb unbelastet bis sehr gering belastet mäßig belastet stark verschmutzt polysaprob IV rot übermäßig verschmutzt Bassem BOUHAFA Seite 8 Ausarbeitung der Maturafragen ISGS Bassem BOUHAFA Seite 9