Universität Konstanz Fachbereich Biologie Priv.
Werbung
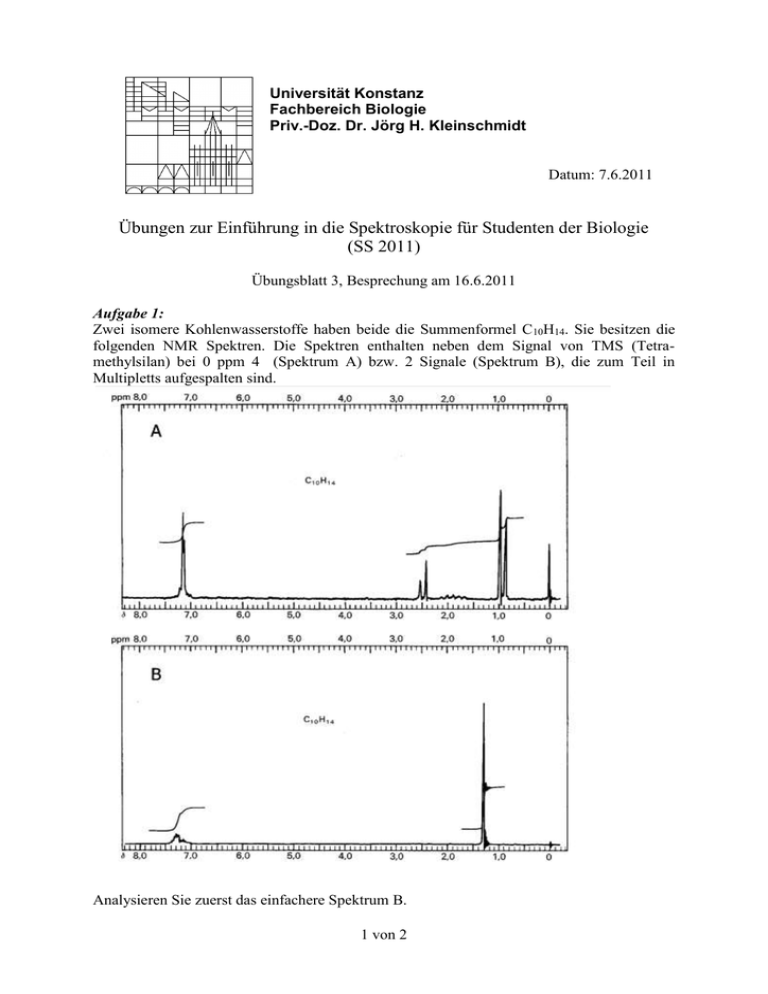
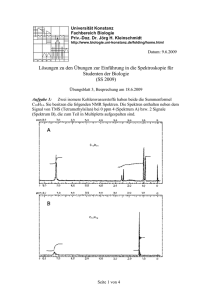
Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt Datum: 7.6.2011 Übungen zur Einführung in die Spektroskopie für Studenten der Biologie (SS 2011) Übungsblatt 3, Besprechung am 16.6.2011 Aufgabe 1: Zwei isomere Kohlenwasserstoffe haben beide die Summenformel C10H14. Sie besitzen die folgenden NMR Spektren. Die Spektren enthalten neben dem Signal von TMS (Tetramethylsilan) bei 0 ppm 4 (Spektrum A) bzw. 2 Signale (Spektrum B), die zum Teil in Multipletts aufgespalten sind. Analysieren Sie zuerst das einfachere Spektrum B. 1 von 2 a) Welche Protonenarten enthalten die Spektren (vergleichen Sie mit dem unten angegebenen Schema für die chemischen Verschiebungen verschiedener Protonenarten) ? b) Geben Sie an, welches ganzzahlige Verhältnis der Zahlen der Protonen in den identifizierten Gruppen mit der angegebenen Summenformel im Einklang steht (d.h. wieviele Protonen gehören zur jeweiligen Protonenenart) ? c) Zwei der Signale in Spektrum A sind Dubletts. Was lässt sich daraus für die Zahl der unmittelbar benachbarten Protonen dieser absorbierenden Wasserstoffkerne ableiten ? d) Um welche Verbindungen handelt es sich ? Aufgabe 2: gN = 5.585 . Das gyromagnetische Verhältnis des Protons ist g ( H ) = 47894152.9 As / kg . Es steht ein Magnetfeld B0 der Stärke 12 T Der Kern g-Faktor des Protons ist 1 (1 T = 1 Vsm–2 = 1 JA–1m–2) zur Verfügung. Bei welcher Frequenz zeigt ein isoliertes Proton eine NMR Absorption? Bei welcher Frequenz ein isoliertes Kohlenstoffatom 13C? Es ist gN(13C)=1.404 und g ( 13C) = 4.7815 ×10 7 Ckg-1 . 2 von 2