Document
Werbung
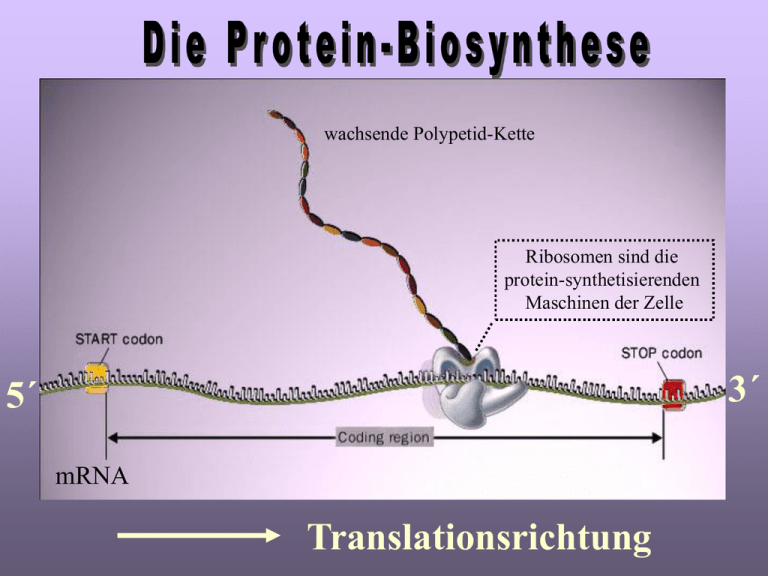
wachsende Polypetid-Kette Ribosomen sind die protein-synthetisierenden Maschinen der Zelle 3´ 5´ mRNA Translationsrichtung Fragen aus der schriftlichen Physikumsprüfung Welche Aussage übe r die Mechan ismen der Informationsüber tragung vom Gen zum Protein trifft zu? (A) Die Ablesung de DNA-Matrize b ei der Repli kation e rfolgt in 5 ’ 3’- Richtung . (A) Die Poly merisation der Ribonuc leotide bei der Transk ription erfolgt in 3 ’ 5’-Richtung. (B) Rever se Transk riptase polymerisiert 2’-Desoxy ribonuc leotide in 5 ’ 3’- Richtung . (C) Die Ablesung der reif en mR NA bei der Translation erfolgt in 3’ 5’- Richtung (D) Die Richtung der Proteinsynthese (von de r C-termi nalen zur N-terminalen Ami nos äure ode r umgek ehrt) wir d durch die zu tanslatie rend e mRNA bestimmt. 60S Untereinheit 40S Untereinheit 80S Ribosom Jede menschliche Zelle besitzt ca. 1 Million Ribosomen (bei E. coli ca. 15 000). In Zusammenarbeit mit mRNA, tRNA und weiteren Proteinfaktoren koordinieren die Ribosomen die Proteinsynthese Bakterien Eukaryonten 70S Ribosom 80S Ribosom 2.5 MDa 4.2 MDa 60S 50S 40S 30S 40S Ribosomen bauen sich aus rRNA und r-Proteinen auf 16S rRNA Bakterien 70S Ribosom 2.5 MDa 50S 23S rRNA (3200 Nt) 5S rRNA (120 Nt) 34 r-Proteine 5‘ 3‘ 30S 16S rRNA (1540 Nt) 21 r-Proteine 16S rRNA Die Kristallstruktur der 30S Untereinheit 5‘ 3‘ Die Ribosomen-Biogenese läuft im Nukleolus ab >> eukaryontische Ribosomen entstehen im Zellkern, genauer im Nukleolus, und müssen von dort über das Nukleoplasma ins Zytoplasma gelangen, wo sie die mRNA translatieren Zellkern Nukleolus rDNA 5S rRNA Prä-rRNA (45S) Ribosomale Proteine (L, S) 28S 18S Präribosomale Partikel 18S Zytoplasma 40S Untereinheit 5.8S 5S 28S 5.8S 60S Untereinheit 5S Die komplizierte Ribosomen-Entstehung im Nukleolus erfordert zeitliche und räumliche Koordination von vielen Teilprozessen. Dies wird durch die hohe strukturelle Organisation des Nukleolus gewährleistet. mRNA 60S Bereich für Peptidsynthese QuickTime™ and a Cinepak decompressor are needed to see this picture. 40S Ausgang für die Polypeptidkette die mRNA liegt wie ein Kabel auf einer Plattform in einer Einbuchtung der 40S bzw. 60S Untereinheit. Dort ist auch der Bereich der Peptid-Synthese. Die wachsende Polypeptid-Kette tritt durch einen Art Tunnel innerhalb der großen Untereinheit aus dem Ribosom heraus. Nach der Polypeptid-Synthese faltet sich die Aminosäure-Kette in ihre korrekte 3-D-Konformation Die Initiation der Protein-Synthese mRNA Initiationsfaktor IF-3 bindet an die 30S Untereinheit, was die Anlagerung der 50S Untereinheit zunächst vehindert Prokaryontische mRNA Anbindung der mRNA: Shine-Delgarno-Sequenz komplementär zum 3‘-Ende der 16S rRNA >> Positionierung des AUG im P-Bereich Shine-Delgarno-Sequenz 5‘ fMet Bindung der fMethionyl-tRNA im P (=Peptidyl)-Bereich 16S rRNA 3‘ durch Codon::Anticodon-Wechselwirkung. Die tRNAfMet kann nur im P-Bereich, nicht im A-Bereich binden,50S wasUnterdurch IF2 kontrolliert wird. 5‘-Kappe m7G einheit 3‘ fMet fMet Eukaryontische mRNA 40S Untereinheit 5‘ 3‘ Ribosomen-Scan 7 m Gdurch IF2 IF2 ist eine GTPase. Unter5‘-Kappe GTP-Hydrolyse kann schließlich die 50S Untereinheit andocken, wobei IF2 und IF3 das Ribosom verlassen >> Ende der Initiation 3‘ fMet Die Elongation bei der Protein-Synthese C C C Pro G G G verschiedene (EF-Tu, EF-Ts), die nachdem sichElongationsfaktoren der Initiationskomplex (funktionelles 70SGTPasen Ribosom) sind und GTP hydrolysieren, sind an der korrekten Anlagerung gebildet hat, kann sich die zweite tRNA, die mit der entsprechenden von tRNA an das Ribosom beteiligt Aminosäure beladen ist, an die A-Position anlagern. Die Auswahl der richtigen tRNA aufein Grund der richtigen dabei bildet sicherfolgt zunächst Komplex zwischenCodon::AnticodonWechselwirkung der 2. tRNAPro und EF-Tu::GTP. Erst dann kann die Bindung im A-Bereich erfolgen fMet Pro G G G Pro G G G C C C anschließend wird GTP hydrolysiert und EF-Tu::GDP wird aus dem 70S Ribosom freigesetzt. Unter Vermittlung von EF-Ts wird EF-Tu::GTP wieder regeneriert Die Verknüpfung der beiden Aminosäuren im Aminoacyl (A)Bereich > Bildung der Peptidbindung dadurch wird im A-Bereich eine Dipeptidyl-tRNA erzeugt, während im P-Bereich eine deacylierte tRNAfMet entsteht. fMet Pro ursprünglich wurde angenommen, daß ein Enzym (Peptidyl-Transferase) die Peptid-Bindung im 70S Ribosom katalysiert. 1992 jedoch entdeckte man, daß die 23S rRNA diese Katalyse-Wirkung hat (keine Enzym, sondern ein Ribozym!) G G G C C C nach die Anlagerung der 2. Aminoacyl-tRNA an der A-Stelle, wird die neue Peptid-Bindung zwischen den Bildung derdie NH bei den Aminosäuren geknüpft. Dabei greift 2 Peptid-Bindung Gruppe der Aminosäure 2 die COOH-Gruppe der AminoSäure 1 an der Initiator-tRNAfMet an. fMet Pro G GG C C C das geschieht dadurch, daß das gesamte Ribosom sich exakt um die Länge eines Triplett-Codons 2 in Richtung 3‘-Ende der mRNA bewegt (= Translokation) Die Translokation der Dipeptidyl-tRNA fMet fMet Pro Pro da die Dipeptidyl-tRNA2 noch immer am 2. Codon befestigt ist, wird sie durch die Bewegung des Ribosoms vom A-Bereich in den P-Bereich verschoben, wodurch die deacylierte tRNAfMet aus dem P-Bereich ins Zytoplasma verdrängt wird G G G G G G C C C C C C damit der Elongationszyklus nicht stopptEF-G und weitere Aminosäuren angeknüpft werden, muß die Dipeptidyl-tRNA2 von der A-PositionEF-G zur P-Position übertragen werden. + Translokation Gly fMet Pro GDP + Pi das 3. Codon (UGU) der mRNA liegt jetzt im A-Bereich, das 2. Codon im P-Bereich. Diese Verschiebung benötigt ein Enzym (EF-G), das als Translokase unter GTP-Verbrauch diesen Schritt katalysiert. G G G C C CU G U der Elongationszyklus schreitet solange fort, bis das Ribosom die letzte Aminosäure angefügt hat und damit das von der mRNA codierte Polypeptid fertiggestellt hat NH2 Die Termination der Polypeptid-Synthese Ser U G G A C C UAG = Stop-Codon Hydrolyse der Polypetidyl-tRNAVerknüpfung NH2 die Termination wird durch eines der 3 Stop-Codons (UAG - UAA - UGA) in der mRNA, für welche es keine komplementären Anticodons in der tRNA gibt, signalisiert sobald ein Stopcodon im A-Bereich erscheint, beteiligen sich 3 Terminationsfaktoren (RF = “releasing factors“) an der: 1. Hydrolyse der terminalen Peptidyl-tRNA-Bindung 2. Freisetzung des Polypeptids 3. Dissoziation des 70S Ribosoms Ser U G G Dissoziation der Komponenten 50S A C C 30S QuickTime™ and a Animation decompressor are needed to see this picture. QuickTime™ and a Cinepak decompressor are needed to see this picture. QuickTime™ and a Cinepak decompressor are needed to see this picture. QuickTime™ and a H.264 decompressor are needed to see this picture. Die Protein-Biosynthese ist sehr energie-aufwendig > Bildung der Aminoacyl-tRNA > Elongation > Translokation = 2 ATP = 1 GTP = 1 GTP ______________________________________________ 4 ATP = 4 x energiereiche Bindungen pro 1 Peptid-Bindung = 122 kJ/mol-1 1 Peptid-Bindung hat dagegen einen Energie-Gehalt von -21 kJ/mol -1 Ribosom mit kurzer Polypeptid-Kette Start-Codon mRNA fertig-gestellte Polypeptid-Kette Stop-Codon Fragen aus der schriftlichen Physikumsprüfung Ribosomen w erden zu Po lysomen v erbunden du rch (A) Zyto skelettelemente, z. B. Spektrin (B) ribosomale RNA (rRNA) (C) chromosomale Proteine (Histone ) (D) die mRNA (E) die wachsende Polypep tidkette Fragen aus der schriftlichen Physikumsprüfung Fragen aus der schriftlichen Physikumsprüfung Fragen aus der schriftlichen Physikumsprüfung Fragen aus der schriftlichen Physikumsprüfung Hemmung der Protein-Biosynthese durch viele Puromycin Die Wirkweise des Puromycins (aus Streptomyces alboniger) bei der Hemmung der Protein-Biosynthese Puromycin ähnelt in seiner Struktur dem 3‘-Ende einer Aminoacyl-tRNA und kann daher im A-Bereich binden PeptidylPuromycin PeptidylTransferase Puromycin nimmt anschließend an allen Elongations-Schritten Teil bis einschließlich der Bildung der Peptid-Bindung (Peptidyl-Puromycin) Puromycin kann dagegen nicht im P-Bereich binden und dissoziiert daher als Peptidyl-Puromycin vom Ribosom ab. • die Protein-Biosynthese ist ein zentraler Vorgang in der Zelle • und daher ein Hauptangriffs-Ziel natürlich vorkommender • Antibiotica und Toxine (Tetracyclin, Chloramphenicol etc.) • wegen der Unterschiede bei der Proteinsynthese • Bakterien/Eukaryonten hemmen die meisten Antibiotica/Toxine • bei den Eukaryonten nicht! Antibiotica and Protein-Synthese Bakterien sind für eine Reihe von mit unter letalen Infektionskrankheiten verantwortlich z. B. Tuberkulose,Pneumonia, Meningitis, Wundinfektionen, Syphilis, Gonorrhö. Vor 1940 keine effektive Behandlungsmöglichkeit mit der Entdeckung des Pencillins (hemmt bakterielle Zellwand-Synthese) änderte sich das schlagartig.Viele Antibiotica hemmen die Protein-Biosynthese. Chloramphenicol Tetracyclin hemmt Peptidyl-Transferase > Prokaryonten hemmt Initiation > Prokaryonten Cycloheximid hemmt Peptidyl-Transferase > Eukaryonten Streptomycin Diphtherie-Toxin hemmt die Protein-Biosynthese bei Eukaryonten durch Blockierung der Translation >> Diphtherie war lange Zeit eine häufige Todesursache bei Kindern. Verursacht durch ein Toxin des Corynebakteriums diphtheriae, das sich im oberen Respirationstrakt einnistet und vermehrt >> bereits wenige mg des Gifts sind für nicht-immunisierte Personen tödlich A-Domäne B-Domäne Die B-Domäne vermittelt die Aufnahme in die Zelle Die A-Domäne ist ein Enzym und katalysiert die Übertragung eines ADP-Ribosyl-Restes vom NAD+ auf den ElongationsFaktor EF2 Hemmung der Translation Zelltod Fragen aus der schriftlichen Physikumsprüfung Fragen aus der schriftlichen Physikumsprüfung Fragen aus der schriftlichen Physikumsprüfung Viele antibiotisch w irksame Substanzen blockieren d ie bakteriell e Proteinb iosynthes e. Bei we lcher der folgenden Substanzen hande lt es sich um einen Inh ibit or der prokaryon tis chen Trans la tion? (A) Amaniti n (B) Tetracycli n (C) Actinomycin (D) Penicilli n (E) Rif ampicin Adäquate Häm-Menge Regulation der Protein-Synthese inaktiv Inadäquate Häm-Menge inaktiv eIF2-Phosphorylierung aktiv inaktiv Austausch von GDP zu GTP ist blockiert Translation läuft kontinuierlich ab Translation ist blockiert QuickTime™ and a Cinepak decompressor are needed to see this picture. Der Lebenszyklus einer mRNA QuickTime™ and a Animation decompressor are needed to see this picture. Protein-Synthese Zytoplasma Ribosom Protein Import Gen Export Transkription Zellkern QuickTime™ and a decompressor are needed to see this picture.