Rationaler Antibiotika-Einsatz
Werbung

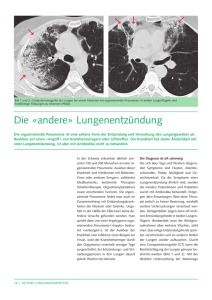
Rationaler Antibiotika-Einsatz Anna Tankovics Quellen • Epidemiologie, Diagnostik, antimikrobielle Therapie und Management von erwachsenen Patienten mit ambulant erworbenen tiefen Atemwegsinfektionen (akute Bronchitis, akute Exazerbation einer chronischen Bronchitis, Influenza und andere respiratorische Virusinfektionen) sowie ambulant erworbener Pneumonie Leitlinie der Paul-Ehrlich-Gesellschaft für Chemotherapie, der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin, der Deutschen Gesellschaft für Infektiologie und des Kompetenznetzwerks CAPNETZ • Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie. Ein Konsensuspapier der Paul-Ehrlich-Gesellschaft für Chemotherapie (PEG) und der Deutschen Gesellschaft für Pneumologie (DGP) unter Mitarbeit von Experten der Deutschen Gesellschaft für Anästhesiologie und Intensivmedizin (DGAI) Chemotherapie Journal 2003;12(2):33-44 • Rationaler Einsatz oraler Antibiotika bei Erwachsenen und Schulkindern (Lebensalter ab 6 Jahre) Empfehlungen einer Expertenkommision der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Chemotherapie Journal 2006;15:129-145 • http://www.p-e-g.org/econtext/leitlinien Therapie-Prinzipien • Berechtigte Indikation • Gezielter Wechsel der Antibiotika (inter- und intraindividuell) • Schonung von Reservesubstanzen • Förderung der Compliance Rationaler Antibiotika-Einsatz • bei akuter Infektion liegt Erregernachweis nicht vor Beginn der Behandlung kalkuliert • Kalkulierte Antibiose: Auswahl des Antibiotikum wird beeinflusst durch: • Lokalisation der Infektion • Erregerspektrum • Lokale Resistenzsituation der Erreger • Antibakterielle Aktivität • Pharmakokinetik • Unerwünschte Wirkung des Antibiotikum Antibiotika • Betalaktam-Antibiotika • • • • • • Penicilline Cephalosporine Carbapeneme Monobactame Beta-Laktamase-Inhibitoren (BLI) Übrige Antibiotika • • • • • • • • • • MLS – Gruppe (Makrolid – Linkosamid – Streptogramin) Aminoglykoside Tetracyclin-Gruppe Gyrasehemmer (Chinolone) Oxazolidinone Nitroimidazole Sulfonamid-Kombinationen Glykopeptid-Antibiotika Lipopeptid-Antibiotika Tuberkulostatika Betalactam-Antibiotika • Hemmung der bakteriellen Zellwandsynthese • Nicht wirksam gegen intrazelluläre Bakterien • Chlamydien • Coxiellen • Legionellen • Nicht wirksam gegen zellwandlose Bakterien • Mykoplasmen Betalactam-Antibiotika: Penicilline • Benzylpenicilline (parenteral) • Penicillin G • gut wirksam gegen Streptokokken und Staphylokokken • Phenoxypenicilline (oral) • Penicillin V, Azidocillin, Propicillin • Streptokokken inkl. Pneumokokken Betalactam-Antibiotika: Penicilline • Isoxazolylpenicilline • Dicloxacillin, Flucloxacillin, Oxacillin • Methicillin wegen Toxizität nicht mehr im Handel nur noch zur Resistenzprüfung bei Staphylokokken • Schmales Wirkspektrum: Staph. aureus • Einsatz: leichte Haut- und Wundinfektionen Betalactam-Antibiotika: Penicilline • Aminobenzylpenicilline • Amoxicillin, Ampicillin • Erweitertes Spektrum: Haemophilus (wenn keine Betalactamasebilder), E. coli, Proteus mirabilis • Unzureichend gegen Staphylokokken, Klebsiellen und Moraxella catarrhalis (Betalactamasebilder) Betalactam-Antibiotika: Penicilline • Acylaminopenicilline • Mezlocillin, Piperacillin • zusätzlich wirksam gegen Enterobacteriaceae, Pseudomonas (Piperacillin) Betalactamase-Inhibitoren (BLI) • Clavulansäure (nur in Kombination) • Sulbactam (Combactam®) • Tazobactam (nur in fester Kombination mit Piperacillin) Breitband-Penicilline + BLI • Ampicillin + Sulbactam (Unacid®) Amoxicillin + Clavulansäure (Augmentan®) Piperacillin + Tazobactam (Tazobac®) Sultamicillin = Ampicillin-Sulbactam-Ester (Unacid PD®) • Erweitertes Spektrum: Haemophilus, Klebsiellen, Moraxella catarrhalis, Anaerobier Betalactam-Antibiotika: Cephalosporine Parenterale Cephalosporine Gruppe 1 • Cefazolin (Basocef®) • Orale Cephalosporine Gruppe 1 • Cefaclor, Cefadroxil, Cefalexin • grampos. Erreger: Streptokokken, Staphylokokken • unzureichend wirksam gegen H. influenzae, Enterobacteriaceae • Indikation: Haut- und Weichteilinfektionen Betalactam-Antibiotika: Cephalosporine • Parenterale Cephalosporine Gruppe 2 • Cefotiam (Spizef®) • Cefuroxim (Zinacef®) • Orale Cephalosporine Gruppe 2 Cefuroxim-Axetil, Loracarbef (Lorafem®) • erweitertes Wirkspektrum wegen besserer β-Lactamase-Stabilität: Streptkokken, Staphylokokken, H. Influenzae, Moraxella catarrhalis, Klebsiellen, Proteus mirabilis, E. coli keine ausreichende Aktivität gegen Anaerobiern • Indikation: Infektionen oberer Respirationstrakt, Otitis media acuta, akute Sinusitis, Harnwegsinfektionen, Haut- und Weichgewebsinfektionen, Lyme-Borreliose Stadium I (Cefuroxim-Axetil) Betalactam-Antibiotika: Cephalosporine • Parenterale Cephalosporine Gruppe 3a • Cefotaxim (Claforan®), Ceftriaxon (Rocephin®) • Parenterale Cephalosporine Gruppe 3b • Cefepim (Maxipime®), Ceftazidim (Fortum®) • Orale Cephalosporine Gruppe 3 • Cefixim (Cephoral®), Cefpodoxim-Proxetil (Orelox®), Ceftibuten (Keimax®) • verbesserte Aktivität im gramneg. Bereich Wirkung im grampos. Bereich unterschiedlich • bei durch Staphylokokken vermuteten Infektionen ungeeignet • keine ausreichende Wirkung gegen Anaerobier • 3b wirksam gegen Pseudomonas (gehören zu den aktivsten) Betalactam-Antibiotika: Carbapeneme • • • • Ertapenem (Invanz®) Imipenem (Zienam®) Meropenem (Meronem®) gute Wirksamkeit gegen Streptokokken, Enterobacteriaceae, Anaerobier • Imipenem, Meropenem: wirksam gegen Pseudomonas Tetracycline • • • • Doxycyclin (Supracylin®) Proteinbiosyntheseinhibitor Bakteriostatisch Gut wirksam gegen Haemophilus, Moraxella, Mycoplasma pneumoniae, Chlamydia pneumoniae, Rickettsien, Coxiella burnetii, Borrelien • mäßig aktiv gegen Legionellen • Weniger gut: S. pneumoniae und S. aureus Makrolide • Erythromycin Clarithromycin (Klacid®) Roxythromycin (Rulid®) Azithromycin (Zithromax®) • Proteinbiosynthese-Inhibitoren • Bakteriostatisch • Sehr gute wirksam gegen C. pneumoniae (v.a. Chlarithromycin), M. pneumoniae (v.a. Azithromycin) • Gut wirksam gegen Moraxella spp., Legionellen • Weniger gut wirksam gegen Haemophilus spp. Ketolide • • • • Telithromycin (Ketek®) Proteinbiosynthesehemmer Weiterentwicklung der Makrolide, daher ähnliches Wirkspektrum Wirkung auch gegen Makrolid-resistente grampositive Bakterien Lincosamide • Clindamycin (Sobelin®) • gute Wirksamkeit gegen grampositive Kokken, Anaerobier • meist nicht wirksam gegen MRSA Chinolone (Gyrasehemmer) • Chinolone Gruppe I • • • • Norfloxacin (Barazan®) Gut wirksam gegen Enterobacteriaceae unwirksam gegen grampositive und atypische Erreger Harnwegsinfekte, Enteritis, chron. Prostatitis Chinolone (Gyrasehemmer) • Chinolone Gruppe II • Ciprofloxacin (Ciprobay®), Ofloxacin (Tarivid®), Enoxacin • gut wirksam gegen Enterobacteriaceae, H. influenzae, Legionellen • schwächer gegen Staphylokokken, Streptokokken, Enterokokken, Chlamydien, Mykoplasmen, Legionellen, Pseudomonas aeruginosa • Ciprofloxacin: sehr gegen Pseudomonas wirksam • Ofloxacin = Racemat, nur linksdrehendes Enantiomer, also 50% der Substanz antibakteriell wirksam • Indikation: Harnwegsinfekte, Gallenwegsinfektionen, gynäkologische Infektionen, abdominelle Infektionen. Nicht indiziert bei ambulant erworbenen Pneumonien (außer wenn Pseudomonas vermutet wird Ciprofloxacin) Chinolone (Gyrasehemmer) • Chinolone Gruppe III • Levofloxacin (Tavanic®) • im Unterschied zu Chinolonen der Gruppe II höhere Aktivität gegen Streptokokken inkl. Pneumokokken, Staphylokokken und Chlamydien, Mykoplasmen, Legionellen • linksdrehendes Enantiomer von Ofloxacin. Lange T½, daher 1x/d-Gabe möglich • In hoher Dosierung auch Pseudomonas-wirksam Chinolone (Gyrasehemmer) • Chinolone Gruppe IV • Moxifloxacin (Avalox®) • noch bessere Aktivität gegen grampos. Erreger wie Staphylokokken, Streptokokken inkl. Pneumokokken, und gegen Anaerobier • Geringere Aktivität gegen gramneg. Erreger als Ciprofloxacin und Levofloxacin Beachte Resistenz bei E. coli (gilt für alle Chinolone) Trimethoprim u. Sulfonamid-Kombinationen • Trimethoprim, Trimethoprim + Sulfamethoxazol Co-trimoxazol (Cotrim®) • Hauptindikation: Harnwegsinfekte Nitroimidazole • Metronidazol (Clont®, Vagimid®) • anaerobe Bakterien und Protozoen • In Kombination zur Eradikationstherapie Helicobacter pylori Glykopeptide • Teicoplanin, Vancomycin • Staphylokokken, einschließlich MRSA, grampos. Aerrobier • Unwirksam gegen gramnegative Erreger Oxazolidinone • • • • • Linezolid (Zyvoxid®) Proteinbiosynthese-Inhibitor MRSA-Infektionen Wöchentliche BB-Kontrollen MAO-Hemme Ambulant erworbene Pneumonie CAP = community-acquired pneumonia Ambulant erworbene Pneumonie • Häufigste registrierte Infektionserkrankung weltweit • Erregerspektrum: 40-50% Streptococcus pneumoniae 5-10% Haemophilus influenzae Mycoplasma penumoniae (v.a. jüngere Patienten) Enterobacteriaceae Respiratorische Viren (RS-, Adeno-, Influenzaviren) <5% Legionella spp Staphylococcus aureus Chlamydia pneumoniae 20-25% Erreger ungeklärt CAP DD Infektion der unteren Atemwege • Infektion der unteren Atemwege: • Akute Bronchitis • Influenza u.a. respiratorische Viren • Akute Exazerbation einer chronischen Bronchitis (AECOPD) CAP DD Infektion der unteren Atemwege Symptome: • • • • • • Allgemeines Krankheitsgefühl Fieber/Hypothermie Husten Eitriger Auswurf Dyspnoe „grippale“ Symptome (Myalgien, Arthralgien, Cephalgien) CAP DD Infektion der unteren Atemwege Körperliche Untersuchung V.a. CAP: • • • • • • • Dyspnoe mit erhöhter AF Tachykardie ggf. arterielle Hypotonie ggf. abgeschwächter Klopfschall (ausgedehnte Infiltrate/Erguss) fein-/mittelblasige ohrnahe RGs Bronchialatmen hohes Alter: oligosymptomatische Verläufe mit extrapulmonalen Symptomen (zunehmende Schwäche/Hinfälligkeit) CAP DD Infektion der unteren Atemwege Sichere Diagnose einer CAP: Nachweis eines Infiltrates im Röntgen-Thorax! im Krankenhaus: bei Symptomen eines akuten Infektes der unteren Atemwege immer Röntgen-Thorax in 2 Ebenen Infektion der unteren Atemwege • Akute Bronchitis: überwiegend virale Erreger Antibiotikabehandlung nicht indiziert • Influenza: antivirale Substanzen nur bei Risikofaktoren und sicherer Diagnose unter Berücksichtigung des Subtyps • AECOPD: Antibiotikatherapie? Infektion der unteren Atemwege Akute Exazerbation einer chronischen Bronchitis • • Symptome: Dyspnoe, Husten , Sputummenge , eitriges Sputum, Brustenge Mittelschwere AECOPD: Indikation zur Hospitalisierung – schwere Atemnot, schlechter AZ, rasche Progression der Symptomatik, Bewusstseinseintrübung, Zynaose/Ödeme, neue Arrythmien, schwere Komorbidität – Antimikrobielle Therapie bei Procalcitonin > 0,1 ng/ml • Schwere AECOPD: Indikation zur Intensivtherapie – schwere Atemnot mit fehlendem Ansprechen auf Notfalltherapie, komatöser Zustand, persistierende Hypoxämie (pO2 < 50 mmHg trotz O2-Gabe), schwere progediente Hyperkapnie (pCO2 > 70 mmHg), respiratorische Azidose (pH < 7,35), Kreislaufinsuffizienz • Leichte AECOPD: keine der oben genannten Kriterien trifft zu AECOPD: Antibiotikatherapie? • Leichte AECOPD: • Mittelschwere oder Schwere AECOPD: ohne bekannte Kolonisation durch P. aeruginosa, ohne individuellen Nachweis nur bei COPD Stadium III oder IV nach GOLD Procalcitonin > 0,1 ng/ml Mittel der Wahl: Aminopenicillin (Amoxicillin) Alternativ*: Makrolid (Azithromycin, Clarithromycin, Roxithromycin) oder Tetracyclin (Doxycyclin) von P. aeruginosa, ohne Bronchiektasen, ohne Beatmung Mittel der Wahl: Aminopenicillin + Betalactamaseinhibitor (Amoxicillin + Clavulansäure oder Sultamicillin) oder parenterale Cephalosporine 2./3. Generation Alternativ*: Peumokokken wirksames Fluorchinolon (Levofloxacin, Moxifloxacin) mit bekannter Kolonisation durch P. aeruginosa, mit individuellem Nachweis von P. aeruginosa, mit Bronchiektasen, beatmet: Acylureidopenicillin + Betalactamaseinhibitor (Piperacillin/Tacobactam) Pseudomonaswirksames Carbapenem (Imipenem, Meropenem) Pseudomonaswirksames Cephalosporin (Ceftazidim**, Cefepim) Pseudomonaswirksames Fluorochinolon (Ciprofloxacin**,Levofloxacin) * bei Therapieversagen oder Unverträglichkeit der anderen Substanzen ** in Kombination mit einer pneumokokkenwirksamen Substanz Therapiedauer: 7-10d; Moxifloxacin, Levofloxacin: 5d; Azithromycin 3d Ambulant erworbene Pneumonie Wann muss CAP im Krankenhaus behandelt werden? Vorliegen folgender Kriterien: CRB-65 (Praxis) oder CURB-Index (Klinik): • Alter > 65 Jahre • Harnstoff-N > 7 mmol/l • Atemfrequenz ≥ 30/min • RR syst. < 90 mm Hg/RR diast. ≤ 60 mm Hg • Bewusstseinseintrübung > 0 stationär Ambulant erworbene Pneumonie Therapie bei ambulanten CAP-Patienten: • Ohne Risikofaktoren: • – Mittel der Wahl: Aminopenicillin (Amoxicillin) > 70 kg: 3 x 1 g oral < 70 kg: 3 x 750 mg oral – Alternativ: 1 x 500 mg oral 3d 2 x 500 mg oral 7-10d 1 x 300 mg oral 7-10d 1 x 200 mg oral ini. 7-10d > 70 kg: 1 x 200; < 70 mg 1 x 100 Makrolid: Azithromycin Clarithromycin Roxithromycin oder Tetracyclin: Doxycylin Mit Risikofaktoren: – Mittel der Wahl: Amoxicillin + Clavulansäure Sultamicillin – • 7-10d 7-10d Alternativ: Risikofaktoren: Levofloxacin Moxifloxacin Cefpodoximproxetil Cefuroximaxetil > 70 kg: 3 x 1 g oral < 70 kg: 2 x 1 g oral 2 x 750 mg oral 7-10d 7-10d 7-10d 1 x 500 mg oral 1 x 400 mg oral 2 x 200 mg oral 2 x 500 mg oral 7-10d 7-10d 7-10d 7-10d - schwere Begleiterkrankungen - Antibiotika-Vortherapien oder Krankenhausaufenthalte - instabiler klinischen Zustand Ambulant erworbene Pneumonie Therapie bei hospitalisierten CAP-Patienten: • Einteilung in 2 Risikogruppen • Patienten ohne RF für P. aeruginosa • Patienten mit RF für P. aeruginosa » schwere strukturelle chronische Lungenerkrankungen wie schwere COPD mit Antibiotikavortherapie oder vorausgegangener Hospitalisierung jeweils in den letzten 3 Monaten » Bekannte Kolonisation durch P. aeruginosa » Bronchiektasen » Mukoviszidose Ambulant erworbene Pneumonie Diagnostik bei hospitalisierten CAP-Patienten: • Allgemein: Anamnese + Untersuchung, Rö-Thorax 2 Ebenen, Leukos, Diff-BB, CRP, E-lyte, Krea, HST, BZ, Transaminasen, GGT, BGA • Mikrobiologie • 2 mal 2 Blutkulturen von unterschiedlichen Entnahmestellen vor Einleitung der antimikrobiellen Therapie • Pleurapunktion (diagnostisch) bei Vorliegen eines Ergusses ( pH, Eiweiß, Gramfärbung, Kultur) • L.-pneumophila-Antigentest im Urin (Reiseanamnese, Immunsuppression, Exposition gegenüber Wasser von Aufbereitungsanlagen) • Sputum nur bei nicht antibiotisch vorbehandelten Patienten mit purulentem Sputum (Transport und Verarbeitung innerhalb von 2-4 h gewährleistet) Ambulant erworbene Pneumonie Therapie bei hospitalisierten CAP-Patienten ohne RF für P. aeruginosa: Antibiotika-Gabe so früh wie möglich! Verzögerung der Therapieeinleitung > 8 h Letalität Amoxicillin/Clavulansäure Ampicillin/Sulbactam Cefuroxim Ceftriaxon Cefotaxim 3 x 2,2 g i.v. 3 x 3,0 g i.v. 3 x 1,5 g i.v. 1 x 2,0 g i.v. 3 x 2,0 g i.v. 7-10d 7-10d 7-10d 7-10d 7-10d plus/minus Makrolid oral/parenteral 7-10d oder Chinolon: Levofloxacin Moxifloxacin 1 x 500 mg 1 x 400 mg 7-10d 7-10d oral/parenteral initial parenteral bevorzugt Trotz geringen Evidenzniveaus wird Kombinationstherapie empfohlen. Monotherapie mit Beta-Lactam Antibiotikum auch möglich Alternative: Monotherapie mit Levofloxacin/Moxifloxacin auch möglich Ambulant erworbene Pneumonie Therapie bei hospitalisierten CAP-Patienten mit RF für P. aeruginosa: Antibiotika-Gabe so früh wie möglich! Verzögerung der Therapieeinleitung > 8 h Letalität Piperacillin/Tazobactam Cefepim Imipenem Meropenem 3 x 4,5 g i.v. 3 x 2 g i.v. 3 x 1 g i.v. 3 x 1 g i.v. 7-14d 7-14d 7-14d 7-14d plus/minus oral oder i.v. (parenteral bevorzugt) Makrolid: Azithromycin Clarithromycin Roxithromycin 1 x 500 mg 2 x 500 mg 1 x 300 mg 7-10d 7-10d 7-10d Chinolon: Levofloxacin 1 x 500 mg 7-10d oder Ambulant erworbene Pneumonie • Orale versus parenterale Therapie • in den ersten Tagen parenteral • Ausnahme: Chinolone wg hoher oraler Bioverfügbarkeit • Ausnahme: Makrolide oral bei Kombination mit parenteralem Beta-Lactam • Orale Sequenztherapie rasche Umstellung auf oral (nach 2-3d) möglich bei: • HF < 100/min, • AF < 24/min, • RR syst. > 90/min, • Temp. < 37,8°C, • orale Aufnahme möglich, • Bewusstsein normal, • pO2 > 60 mmHg bzw. SO2 > 90% • Gesamttherapiedauer: • 7-10d • Bei nachgewiesener P. aeruginosa-Infektion: 8-15d • Adjuvante Therapie: • Sauerstoffgabe • Thromboseprophylaxe bei immobilisierten Patienten • Atemtherapie und Mobilisierung • Radiologische Abschlussuntersuchung • nach 4-6 Wochen bei Rauchern, Alter > 65, schwere Begeiterkrankungen Schwere ambulant erworbene Pneumonie (sCAP) • • • • • • AF > 30/min Oxigenierungsindex pO2/FiO2 < 250 (<200 bei COPD) Notwendigkeit eines Atmungs-Supports 50 %ige Zunahme des Infiltrates innerhalb 48 h nach Aufnahme Multilobuläre oder bilaterale Infiltrate Zeichen der schweren Sepsis/septischer Schock mit hämodynamischer Instabilität und Organversagen • • • • • • • RR syst. < 90 mmHg/ RR diast. < 60 mmHg Catecholamin-Gabe > 4 h Harnproduktion < 20 ml/h (ohne gleichzeitige Hypovolämie) Schwere Azidose (pH < 7,3) Schwere dissiminierte intravasale Gerinnung Akutes Nierenversagen mit Nierenersatztherapie Multiorganversagen Intensivmedizinische Überwachung und ggf. Intensivtherapie Schwere ambulant erworbene Pneumonie (sCAP) Einteilung in 2 Risikogruppen: • Patienten ohne RF für P. aeruginosa • Patienten mit RF für P. aeruginosa Mikrobiologische Diagnostik: • • • • 2 mal 2 BKs von unterschiedlichen Lokalisationen Sputum/Trachealsekret Pleurapunktion bei Erguss Legionella-pneumophila-Antigentest im Urin bei ALLEN Patienten mit sCAP • Bronchoskopie mit BAL (bronchoalveoläre Lavage): bei Immunsupprimierten, V.a. seltenen Erreger, Ausschluss Bronchusstenose Schwere ambulant erworbene Pneumonie (sCAP) Therapie der sCAP bei Patienten ohne RF für P. aeruginosa Antibiotika-Gabe so früh wie möglich! Verzögerung der Therapieeinleitung > 8 h Letalität Kombination plus Piperacillin/Tazobactam 3 x 4,5 g i.v. 8-10d Cetriaxon 1 x 2 g i.v. Cefotaxim 3 x 2 g i.v. Ertapenem (begrenzte Studienerfahrung) 1 x 1 g i.v. 8-10d 8-10d 8-10d Makrolid parenteral 8-10d Alternativ: Monotherapie mit Chinolon Levofloxacin Moxifloxacin 2 x 500 mg i.v. 1 x 400 mg i.v. 8-10d 8-10d Schwere ambulant erworbene Pneumonie (sCAP) Therapie der sCAP bei Patienten mit RF für P. aeruginosa Antibiotika-Gabe so früh wie möglich! Verzögerung der Therapieeinleitung > 8 h Letalität Kombination plus Piperacillin/Tazobactam 3 x 4,5 g i.v. 8-15d Cefepim Imipenem Meropenem 3 x 2 g i.v. 3 x 1 g i.v. 3 x 1 g i.v. 8-15d 8-15d 8-15d 2 x 500 mg i.v. 3 x 400 mg i.v. 8-10d 8-15d 8-15d Makrolid parenteral Chinolon: Levofloxacin Ciprofloxacin Dosisempfehlungen bei ambulant erworbener Pneumonie Aspirationspneumonie Mittel der Wahl: • • • Ampicillin + Sulbactam 3 x 3 g i.v. Amoxicillin + Clavulansäure 3 x 2,2 g i.v. Piperacillin + Tazobactam 3 x 4,5 g i.v. Alternativ: • • • • Cefotaxim + Clindamycin Cetriaxon + Clindamycin Moxifloxacin Carbapenem • Ertapenem • Imipenem • Meropenem 3 x 2 g i.v. + 3 x 600 mg i.v. 1 x 2 g i.v. + 3 x 600 mg i.v. 1 x 400 mg i.v. 1 x 1 g i.v. 3 x 1 g i.v. 3 x 1 g i.v. Dauer: 8-10d bzw. Antibiotika noch 5d nach Entfieberung weitergeben Nosokomiale Pneumonie • Symptome entwickeln sich nach Aufnahme im Krankenhaus • Gleichbehandelt werden Patienten, die innerhalb der ersten vier Wochen nach einer stationären Behandlung eine Pneumonie entwickeln • Patienten aus Alten- und Pflegeheimen, die chronisch bettlägerig sind oder antibiotisch vorbehandelt sind Nosokomiale Pneumonie • häufigste Todesursache unter den Krankenhausinfektionen • Diagnostik: • Nachweis eines neuen und persistierenden Infiltrates im Röntgen-Thorax • plus 2 der folgenden 3 Kriterien: » Leukozytose (>12000/μl) oder Leukopenie (<4000/ μl) » Fieber > 38,3°C oder Hypothermie < 36°C » Purulentes Bronchialsekret Nosokomiale Pneumonie Mikrobiologie: • • • • Probengewinnung vor Einleitung einer Antibiotikatherapie Bei bereits durchgeführter antimikrobieller Therapie möglichst keine Umstellung 72 h vor Probengewinnung Transport und Lagerungszeiten: < 4 h !!! Sputum: makroskopisch eitrig mikroskopisch: > 25 Granulozyten/Gesichtsfeld < 10 Plattenepithelien/Gesichtsfeld bei 100facher Vergrößerung mindestens 2 x aerob und anaerob von unterschiedlichen Entnahmestellen • Blutkultur: • • Serologie: spielt für Akutdiagnostik keine Rolle Antigen-Nachweis: S. pneumoniae: nützliche Zusatzinformation • • L. pneumophila: nosokomial selten nur bei begründetem Verdacht Ergusspunktat: pH, Eiweiß, LDH, Glucose, Zytologie, Gramfärbung, ggf. Mykobakterien, Kultur Tracheobronchialsekret, geschützte Bürste, BAL Nosokomiale Pneumonie - Therapie Auswahl der kalkulierten Therapie unter Berücksichtigung folgender Faktoren: • Spontanatmung ( seltener multiresistente Erreger) oder beatmet? typisches Erregerspektrum: S. aureus S. pneumoniae Enterobacteriaceae • innerhalb der ersten 4 Tage nach Aufnahme oder später? typisches Erregerspektrum: S. aureus S. pneumoniae H. influenzae Enterobacteriaceae • MRSA Pseudomonas spp. Acinetobacter spp. Enterobacter spp. Proteus vulgaris Serratia spp. Alter, strukturelle Lungenerkrankungen, antibiotische Vorbehandlung, Schweregrad der Pneumonie Nosokomiale Pneumonie - Therapie • • • Die einzelnen Risikofaktoren haben einen unterschiedlich stark ausgeprägten Einfluss auf den Schweregrad der Erkrankung und das zu erwartene Erregerspektrum Deshalb Bewertung mit 1 – 4 Punkten Bei Vorliegen mehrerer RF werden Punkte addiert • • • • • • Risikofaktor Alter > 65 Jahre Strukturelle Lungenerkrankung Antimikrobielle Vorbehandlung Erkrankung nach dem 5. Tag des Krankenhausaufenthaltes Schwere respiratorische Insuffizienz mit oder ohne Beatmung Extrapulmonales Organversagen (Schock, DIC, ANV, ALV) Punkte • •• •• ••• ••• •••• DIC=Disseminierte intravasale Gerinnung, ANV=Akutes Nierenversagen, ALV=Akutes Leberversagen Nosokomiale Pneumonie - Therapie Risikofaktor • Alter > 65 Jahre • Strukturelle Lungenerkrankung • Antimikrobielle Vorbehandlung • Erkrankung nach dem 5. Tag des Krankenhausaufenthaltes • Schwere respiratorische Insuffizienz mit oder ohne Beatmung • Extrapulmonales Organversagen (Schock, DIC, ANV, ALV) Punkte • •• •• ••• ••• •••• Therapieoption I bis 2 Punkte Therapieoption II 3 – 5 Punkte Therapieoption III > 5 Punkte Aminopenicillin/BLI Acylaminopenicillin/BLI Cephalosporin 3b Cephalosporin 2/3a Chinolon 3/4 Cephalosporin 3b Chinolon 2/3 Carbapenem Acylaminopenicillin/BLI Carbapenem Chinolon 3/4 oder Aminoglykosid Immer parenteral und in hoher Dosierung Dauer: Orientierung anhand klinischer Symptome Fortführung nach klinischer Besserung (Entfieberung, AZ, Gasaustausch gebessert) für 3-5d in Therapieoption I Umstellung auf oral nach klinischer Besserung möglich (Sequenztherapie) Gesamtdauer maximal 10-14d bei Legionellose: 3 Wochen Parenterale Antibiotika der nosokomialen Pneumonie Wertung der Evidenz für die Wirksamkeit von Antibiotika in der initialen Therapie der nosokomialen Therapie (Therapieoption I und II) Wirkstoff Handelsnahme Evidenzgrad Empfehlungen zur Therapie von bakteriellen Infektionen der Harnwege bei Erwachsenen Empfehlungen zur Therapie von bakteriellen Infektionen der Harnwege bei Erwachsenen Empfehlungen zur Therapie von bakteriellen Infektionen im HNO-Bereich Empfehlungen zur Therapie von bakteriellen Infektionen des Magen-Darm-Trakts und der Gallenwege Empfehlungen zur Therapie von gynäkologischen Infektionen Empfehlungen zur Therapie von bakteriellen Haut- und Weichgewebsinfektionen Endokarditisprophylaxe Bei Patienten mit der höchsten Wahrscheinlichkeit eines schweren oder letalen Verlaufs einer infektiösen Endokarditis – Patienten mit Klappenersatz (mechanische und biologische Prothesen) – Patienten mit rekonstruierten Klappen unter Verwendung von alloprothetischem Material in den ersten 6 Monaten nach Operation a – Patienten mit überstandener Endokarditis – Patienten mit angeborenen Herzfehlern – Zyanotische Herzfehler, die nicht oder palliativ mit systemisch-pulmonalem Shunt operiert sind – Operierte Herzfehler mit Implantation von Conduits (mit oder ohne Klappe) oder residuellen Defekten, d. h. turbulenter Blutströmung im Bereich des prothetischen Materials – Alle operativ oder interventionell unter Verwendung von prothetischem Material behandelten Herzfehler in den ersten 6 Monaten nach Operation a – Herztransplantierte Patienten, die eine kardiale Valvulopathie entwickeln a Nach 6 Monaten wird eine suffiziente Endothelialisierung der Prothesen angenommen. • • • 30 – 60 min vor einer Prozedur (bis zu 2 h danach noch sinnvoll) Nicht bei rein diagnostischer Bronchoskopie (bei Biopsie: ja!) Generelle Prophylaxe bei Gastroskopie, Koloskopie auch mit Biopsien nicht mehr empfohlen! nur bei Infektionen des GIT/Urogenitaltrakt: Ampicillin, Piperacillin oder Vancomycin Prophylaxe der infektiösen Endokarditis Der Kardiologe 2007;1:243–250 Ein Positionspapier der Deutschen Gesellschaft für Kardiologie – Herz- und Kreislaufforschung e.V. und der Paul Ehrlich Gesellschaft für Chemotherapie Empfohlene Prophylaxe vor zahnärztlichen Eingriffen Situation Antibiotikum Einzeldosis 30–60 min vor dem Eingriff Erwachsene Kinder Orale Einnahme Amoxicillin a 2 g p.o. 50 mg/kg p.o. Orale Einnahme nicht möglich Ampicillin a, b 2 g i.v. 50 mg/kg i.v. –orale Einnahme mg/kg p.o. Clindamycin c, d 600 mg p.o. –orale Einnahme nicht möglich Clindamycin b, d 600 mg i.v. Penicillin- oder Ampicillinallergie 20 20 mg/kg i.v. a Penicillin G oder V kann weiterhin als Alternative verwendet werden b Alternativ Cefazolin, Ceftriaxon 1 g i.v. für Erwachsene bzw. 50 mg/kg i.v. bei Kindern c Alternativ Cefalexin: 2 g p.o. für Erwachsene bzw. 50 mg/kg p.o. bei Kindern oder Clarithromycin 500 mg p.o. für Erwachsene bzw. 15 mg/kg p.o. bei Kindern