Honig.pps
Werbung

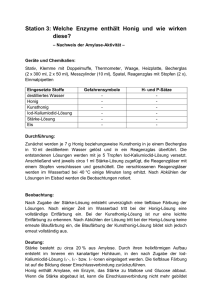
Honig © Werner Schalko Honig; Schalko 1 Phloemsaft pH = 7,3 – 8,6 Saccharose, Oligosaccharide, Zuckeralkohole Aminosäuren, Vitamine Kalium Honig; Schalko 2 Phloemsaft Nektarien Nektar Blätter und Rinden Phloemsauger = Blattläuse Honig; Schalko 3 Nektar pH = 2,7 – 6,4 80 % Wasser Saccharose Glucose, Fructose (enzymatische Hydrolyse) N-Verbindungen Mineralstoffe Farb- und Aromastoffe Honig; Schalko 4 Der Verdauungsapparat der Biene. Zunge (und Rüssel) nach unten geklappt. Kopfspeicheldrüse Ventiltrichter Brustspeicheldrüse Malpighische Gefäße Dünndarm Futtersaftdrüse Rektaldrüsen Schlund Oberkieferdrüse Enddarm Mitteldarm Zunge Honigmagen Honig; Schalko 5 Honigtau pH = 5,1 – 7,9 80 –95 % Wasser Saccharose, Glucose, Fructose, Erlose, Melezitose, Maltose Mineralstoffe Honig; Schalko 6 Honigtauerzeuger beim Anstechen einer Siebröhre – schematisch dargestellt Honigtauerzeuger (z.B. Lachnide) Siebröhren (Phloem) Holzröhren (Xylem) Gefäßbündel Borke (Rinde) Holz Honig; Schalko 7 Umwandlung von Siebröhrensaft in Honigtau – schematisch dargestellt Zucker Magen Enddarm Honigtau Mycetom Zucker Borke Siebröhre Holz (Vitaminproduktion, Stickstoffverwertung) Honig; Schalko 8 Honigreifung Wasserverdunstung Enzyme: Diastase Invertase (Saccharase) Glucoseoxidase Phosphatase Honig; Schalko 9 Diastase -Amylase – spaltet -1-4-Bindungen pH = 5,4 Tmax = 40 °C Honig; Schalko 10 Saccharase Spaltung der Saccharose Transglucosidierung pH = 5,9 Tmax = 40 – 42 °C Honig; Schalko 11 Invertierung der Saccharose -D-Glucopyranose CH2OH CH2OH O Hydrolyse CH2OH O O O OH OH Saccharose + CH2OH CH2OH OH O HO HO OH CH2OH OH b-D-Fructofuranose Honig; Schalko OH OH OH OH 12 Transglucosidierung der Glucose CH2OH CH2OH O 2 CH2OH O Transglucosidierung O OH OH OH OH OH O OH OH OH -D-Glucopyranose OH OH Maltose Honig; Schalko 13 Transglucosidierung der Saccharose CH2OH CH2OH O O HO OH O OH OH CH2OH OH Saccharose Transglucosidierung CH2OH CH2OH O CH2OH O O OH OH HO O OH OH O OH CH2OH OH Erlose Honig; Schalko 14 Glucoseoxidase Bildet Gluconsäure pH = 6,5 Tmax = 35 °C Sehr empfindlich Honig; Schalko 15 Oxidation der Glucose O2 H2O2 + CH2OH GlucoseFP oxidase FPH2 + CH2OH O O OH OH OH OH OH CH2OH O OH + H2O OH COOH OH OH OH Honig; Schalko OH 16 Honig Saccharide Proteine Aminosäuren Hormone Organische Säuren Aromastoffe Mineralstoffe Vitamine Farbstoffe Wasser Honig; Schalko 19 Saccharide Monosaccharide – Glucose, Fructose (Pflanze, Honigtau, Biene) Disaccharide – Saccharose (Pflanze, Honigtau), Maltose (Nektar, Honigtau, Biene) Trisaccharide – Melezitose (Honigtau), Erlose (Honigtau, Biene) Honig; Schalko 20 Monosaccharide Glucose : Fructose = Maß für Neigung zum Auskristallisieren Je mehr Fructose, desto geringer ist diese Tendenz Honig; Schalko 21 Strukturformeln von Melezitose und Erlose; beides sind Transglucosidierungsprodukte der Saccharose. CH2OH CH2OH O O HO OH O OH CH2OH OH OH OH O Melezitose OH O CH2OH CH2OH CH2OH O CH2OH O O OH HO OH O OH OH O OH CH2OH OH Honig; Schalko Erlose 22 Aromastoffe Maillard-Reaktion aus Fructose, Glucose und Prolin Enzymatische Aromabildung aus Aminosäuren Honig; Schalko 23 MAILLARD-Reaktion. Die komplexen Vorgänge, die unter dieser Reaktion zusammengefasst werden, sind für charakteristische Farb- und Aromanuancen des Honigs verantwortlich. CH2OH CH2OH OH H OH H OH H+ O + OH HN OH OH H COOH OH D-Glucose L-Prolin OH H OH N OH H COOH OH Addukt CH2OH OH H OH H H+ OH H+ H2O OH H H+ - OH H COOH Glykosylamin CH2OH CH2OH AMADORI OH H b-ElimiOH nierung OH H COOH OH N OH H+ OH N+ O N+ Schiff-Base-Kation H2O OH H O OH OH H COOH OH OH + CH2OH CH2OH H+ CH2OH H2O OH N OH H COOH OH H H N OH H COOH O 1,2-Enaminol CH2OH H OH H 1-Desoxy-1-L-prolino-D-fructose O OH H 3-Desoxyoson H OH O OH O OH Honig; Schalko OH C H2 24 N H COOH H C C O COOH + H2N CH O Aminosäure C - CO2 C CHO C C R -Diketon R - H 2O + C C OH N O N O C O CH R + H2 O CH R OH C O CH NH2 Honig; Schalko NH2 Aminoketon 25 COOH R2 R1 C C H H2N CH O CH2 + R2 - H 2O R1 O C C -Diketon O N O C O - CO2 CH CH2 Ph Phenylalanin R2 R1 C C OH N CH CH2 + H2 O R2 R1 C C Ph O OH + NH2 C H CH2 Ph Phenylacetaldehyd Honig; Schalko 26 Phenylalanin als Vorstufe verschiedener pflanzlicher Stoffe auf das Honigaroma. Enzyme: E1 = Phenylalnin-Ammonium-Lyase; E2 = Zimtsäure-4-Hydroxylase; E3 = p-Cumarsäure-3Hydroxylase; E4 = Phenylpyruvat-Decarboxylase; E5 = Phenylalanin-Amino-Transferase; E6 = Alkohol-Dehydrogenase; E7 = Aldehyd-Dehydrogenase. E6 COOH O CH2OH O E4 H Phenylbrenztraubensäure Phenylethanol Phenylacetaldehyd E5 H2N COOH COOH E7 Phenylessigsäure HO Phenylmilchsäure HO HO COOH Kaffeesäure E3 E1 COOH COOH E2 COOR Phenylessigsäureester HO p-Cumarsäure COOH Phenylpropionsäure trans-Zimtsäure Honig; Schalko 27 Physiologischer Abbau der Zimtsäure durch b-Oxidation CH2OH Red. C C COOH H H Zimtsäure Benzylalkohol CHO COOMe Benzaldehyd Ox. Veresterung COOH Benzoesäure Red. OH Phenol Honig; Schalko 28 Honiglagerung Optimale Kristallisationstemperatur: 10 – 18 °C (14 °C) Kristallisationsfehler Wassergehalt Luftfeuchtigkeit Veränderung der Honigfarbe (in Abh. von der Lagerungstemperatur) Honig; Schalko 29 Honigverflüssigung Luftbad Wasserbad Tauchwärmer Melitherm Mikrowelle Ultraschallbad Honig; Schalko 30 Honiguntersuchung Wassergehalt pH-Wert Elektrische Leitfähigkeit Verhalten im polarisierten Licht HMF Diastaseaktivität Invertaseaktivität Prolingehalt Honig; Schalko 31 Wassergehalt 15 – max. 21 % Trocknen des Honigs Karl-Fischer-Titration Refraktometer, bei 20 °C Aräometer Honig; Schalko 32 pH-Wert Blütenh.: 3,6 – 4,5 Honigtauh.: 4 – 5,4 pH-Meter 20 %-ige Honiglösung Honig; Schalko 33 Elektrische Leitfähigkeit Blütenh.: < 500 µS Honigtauh.: > 1000 µS LF-Messzelle Honiglösung mit genau 20 % TS Gesuchte Einwaage = 100.x/TS x = Gramm TS TS = refraktometrisch bestimmte TS Honig; Schalko 34 HMF-Gehalt < 40 ppm Lagerschäden, Enzymabbau Ca. 5 ppm/a Photometer: p-Toluidin Resorcin Honig; Schalko 36 HMF- Bildung O HO2HC CH2OH H OH HO H3 O+ H O O CH2OH OH H H 5-Hydroxymethylfurfural D-Fructose Honig; Schalko 37 HMF- Nachweis O H C O CH2OH O Honig; Schalko 38 Entstehung von Hydroxymethylfurfural (HMF) in Honig in Abhängigkeit von Temperatur und Zeit (nach WHITE 1978) Zeit [Tage] 1000 100 40 mg · kg-1 10 1 0,1 20 30 40 50 Honig; Schalko 60 70 80 °C 39 Diastaseaktivität > 3 nach Gothe Lagerschäden Photometer: Blaufärbung mit Iod-Kaliumiodidlösung Honig; Schalko 43 Prolin 250 – 550 ppm Ursprüngliche Enzymaktivität Unverfälschtheit Photometer: Ninhydrin Honig; Schalko 44 Prolin N H COOH (Pyrrolidin-2-carbonsäure) Honig; Schalko 45 Ninhydrinreaktion COO H3N CH O R H O C R + CO2 O O OH N OH O O O Ninhydrin Honig; Schalko 46 Honigverfälschung Kunsthonig Rohrzucker Stärkesirup Hochfructosesirup Zuckerfütterung Zusatz von Salzen Farbzusätze Melasse Honig; Schalko 47 Honig und Gesundheit Löst als Zucker Karies aus Antibakterielle Wirkung H2O2, Pinocembrin:Wundbehandlung, Erkältungskrankheiten, Darminfektion Honig; Schalko 48 Pinocembrin (5,7-Dihydroxyflavanon) HO O OH O Honig; Schalko 49 Honig und Gesundheit Acetylcholin führt zu einer Erweiterung der Venengefäße und einer Verbesserung des Herzkranzgefäßkreislaufes und senkt den Blutzuckerspiegel. Honig; Schalko 50 Gifte im Honig Brompropylat (Folbex VA neu) Dibrombenzophenon (Abbauprodukt von Folbex) Cymiazolhydrochlorid -(Apitol) Para-Dichlorbenzol (Wachsmottenbekämpfungsmittel, Imkerglobol) Honig; Schalko 53 Gifte im Honig Fluvalinat (Apistan, Klavtan) Flumethrin (Bayvarol) Amitraz Coumaphos (Perizin) Ameisensäure Milchsäure Oxalsäure Sulfathiazol Honig; Schalko 54 Höchstkonzentrationen für Rückstände im Honig Höchstkonzentration im Honig Wirkstoff Brompropylat Produkt Folbex VA Coumaphos Perizin 0.05 mg/kg Cymiazol Apitol 0.5 mg/kg Fluvalinat Apistan 0.05 mg/kg Flumethrin Bayvarol 0.005 mg/kg Thymol Apilife VAR 0.8 mg/kg Ameisensäure Milchsäure Oxalsäure alternative Methoden keine Höchstkonzentration festgelegt Honig; Schalko 0.1 mg/kg 55 Coumaphos (Perizin) O O S O C CH 3 H2 O P O C CH3 H2 Cl CH3 Honig; Schalko 58 Coumaphos (Perizin) Phosphorothiosäure-O-(3-chloro-4-methyl-2-oxo-2H-1benzopyran-7-yl)O,O-diethyl ester Lipophil Bienenwachs Wirkmechanismus der Organophosphate: – reversible bzw. irreversible Hemmung der Acetylcholinesterasen – Acetylcholinesterasen → Zerstörung des Neurotransmitters Acetylcholin → Regulierung der Neurotransmission an den Synapsen – Organischen Phosphorsäureester strukturell ähnlich Acetylcholin → binden an Acetylcholinesterase → Transphosphorylierung des Enzyms → Anstieg von Acetylcholin → depolarisierende Muskelrelaxation → spastische Paralyse → Tod Honig; Schalko 59 Amitraz CH3 H3C H3C N C N H CH3 C N H Honig; Schalko CH3 60 Amitraz 1,5-Di-(2,4-dimethylphenyl)3-methyl-1,3,5triazapenta-1,4-dion-bis N,N-(dimethyl-2,4phenyliminomethyl)-N-methylamin. Wirkung von Amitraz: – Antagonistischer Effekt auf Oktopaminrezeptoren im Gehirn der Parasiten → Übererregbarkeit, abnormen Verhalten, Paralyse und Tod. Lipophil Bienenwachs; Grenzwerte: Honig 0.2 mg/kg; Summe von Amitraz und seiner Metaboliten; gemessen als 2,4-Dimethyl-anilin" Honig; Schalko 61 Flumethrin Alpha-Cyano-(4-fluoro-3-phenoxy)-benzyl-3[2-chloro-2-(4-chlorophenyl)-ethenyl]-2,2dimethyl-cyclopropancarboxylat Zur Gruppe der Pyrethroide → schnell wirkendes Kontaktgift → rasch einsetzender Knock-down-Effekt ausgeprägte repellierende Eigenschaften Lipophil Bienenwachs Honig; Schalko 64 Sulfathiazol N1-(2-thiazolyl)benzolsulfonamid H2N S SO2NH N Sulfathiazol Honig; Schalko 65 Zur Bekämpfung der amerikanischen Faulbrut Hydrophil Rückstände im Honig Nachweis mit SC/MS Honig; Schalko 66