Das Auge als Kamera, der blinde Fleck und die - Das mp3
Werbung
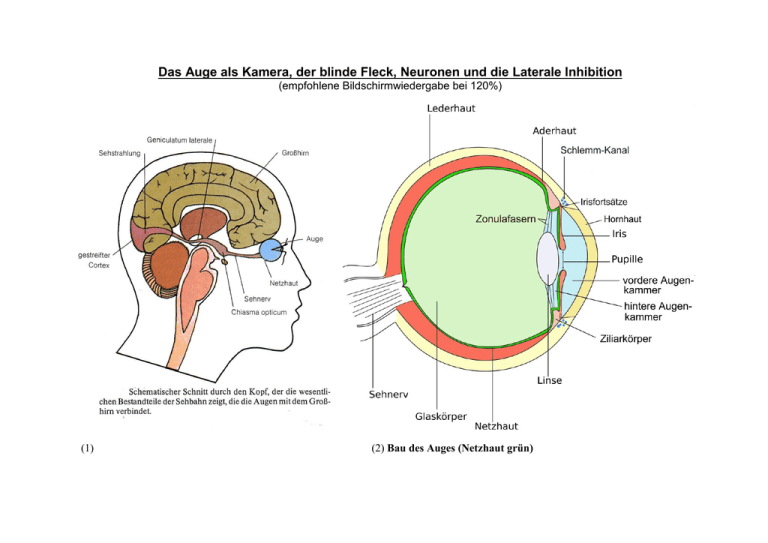
Das Auge als Kamera, der blinde Fleck, Neuronen und die Laterale Inhibition (empfohlene Bildschirmwiedergabe bei 120%) (1) (2) Bau des Auges (Netzhaut grün) 2 (3) Die optische Abbildung auf der Retina: 3 (4) 4 Experiment zum Nachweis des blinden Flecks: (5) Setzen Sie sich bitte so vor den Monitor, dass Sie senkrecht genau auf die Mitte des Bildschirms blicken, halten Sie das linke Auge mit der Hand zu, fixieren Sie das Kreuz auf der linken Seite und bewegen Sie das Gesicht auf den Monitor zu, bis der schwarze Punkt rechts – in einem Abstand von etwa 30 bis 45 cm – verschwindet. Anstelle des Punktes werden Sie jedoch kein ‚Loch’ im Sehfeld wahrnehmen; vielmehr füllt das visuelle System die Leerstelle, an der es definitiv nichts sieht, selbständig mit der Hintergrundsfarbe (weiß) aus. - Überprüfen Sie am folgenden Bild, was geschieht, wenn Sie ebenso verfahren, bis der schwarze Punkt rechts verschwunden ist. 5 (6) 6 Warum existiert dieser blinde Fleck? Die Antwort: Weil der Sehnerv (die Bündelung der Axone der optischen Sinnesrezeptoren der Netzhaut) an dieser Stelle durch den Augenhintergrund hindurch tritt. Aber warum muss er das? (7) (8) Naiverweise könnte man ja vermuten, dass die optischen Sinnesrezeptoren (Stäbchen und Zapfen) so in die Retina eingebettet seien wie das Abbildung (7) schematisch darstellt: so nämlich, dass diese Rezeptoren mit ihren lichtempfindlichen Teilen (partes opticae), welche den sog. Sehpurpur (Rhodopsin bzw. Porphyropsin oder Iodopsin) enthalten, in den Innenraum des Auges hineinragen und somit die Axone dieser Rezeptorzellen jenseits der Netzhaut (also rechts) zum Sehnerven zusammengebündelt werden könnten. Dem ist aber nicht so. Der gesamte neuronale Apparat der Retina ist zusammen mit dem übrigen Auge ein unmittelbarer Teil des Gehirns, der sich während der embryonalen Organogenese aus dem Ektoderm, dem äußeren der drei Keimblätter (Entoderm, Mesoderm und Ektoderm) ausstülpt. Infolge dieser Ausstülpung liegen die optischen Sinnesrezeptoren sozusagen verkehrt herum: wie Abb. 8 schematisch zeigt, liegen deshalb die lichtempfindlichen Teile der Rezeptoren jenseits des Augenhintergrunds (rechts), während die Axone derselben in das Auge hineinführen und ihre Bündelung, der Sehnerv, deshalb erst durch die Retina hindurch geführt werden muss, um zum Gehirn zu gelangen. An der Stelle dieses Durchtritts können sich deshalb keine optischen Rezeptoren befinden: eben dies ist der blinde Fleck. – Tatsächlich ist die Situation noch viel ‚verrückter’ als das obige Schema zeigt: die Retina enthält nämlich nicht nur die optischen Rezeptorzellen, sondern noch weitere drei Schichten nachgeschalteter Zellen, die alle diesseits des Augenhintergrunds (also innen !) auf der Rezeptorenschicht aufliegen: die Schichten der sog. Horizontalzellen, der Bipolaren und der Amakrinen. Zu allem Überfluss liegen auf diesen Zellverbänden auch noch weitere Geflechte aus Blutgefäßen, Epithelgewebe und Stützzellen auf! 7 (9a) Lage der Rezeptoren in der Retina (9b) Retinale Nervenzell-Schichten (das Licht kommt von unten !) 8 Aus diesen Gründen ist die optische Qualität des Auges – verglichen mit einer Kamera – eher äußerst dürftig. Da sich das Licht erst durch mehrere Zellschichten hindurcharbeiten muss, ehe es die lichtempfindlichen Teile der Rezeptoren erreicht, ist das aus den Stäbchen und Zapfen zusammengesetzte Rasterbild – aus rein physikalischen Gründen – offensichtlich sehr unscharf (auch wegen der starken Brechungsfehler). (10) Unscharfe Abbildung eines Lichtflecks in der Retina (11) Ein Goethebildnis und seine vermutliche retinale Abbildung 9 Die Frage ist nun, wieso wir dennoch die Dinge so scharf sehen können. Und die Antwort darauf ist, dass wir keineswegs die Dinge (in der sog. Außenwelt) scharf sehen, auch nicht deren Abbilder auf der Netzhaut (die ja überaus unscharf sind), sondern: was wir so scharf sehen, sind die ‚Dinge’, die bereits der retinale Zellapparat (und hernach das Gehirn) selbständig aus den unscharfen Netzhautbildern konstruiert oder ‚errechnet’. Um zu verstehen, wie das geschieht, muss man einige grundlegende Fakten über die Physiologie einer Nervenzelle kennen. Alle Nervenzellen (Neuronen), zu denen auch alle Rezeptoren gehören, haben die gleiche Funktion und im wesentlichen auch die gleiche Struktur: 12 13 14 10 Ein Neuron besteht aus einem Zellkörper mit Zellkern (Nucleus), der sich in feinen Verästelungen (Dendriten) verzweigt, sowie einem Nervenstrang (Axon), der mit einer Myelinschicht umkleidet ist und sich an seinem Ende ebenfalls verzweigt (Abb. 12). An den Endigungen dieser Verzweigungen befinden sich die Synpasen, die Schaltglieder, die sich an die Dendriten eines weiteren Neurons anlegen. (Abb. 13) Zwischen dem Inneren der Nervenzelle und der umgebenden Flüssigkeit besteht ein Spannungsunterschied, das sogenannte Ruhe- oder Membranpotential. Im Normalzustand liegt die Spannung im Zellinneren um 80 mV unter dem Zelläußeren, d.h. es besteht eine "Polarisation", welche durch Konzentrationsunterschiede verschiedener geladener Teilchen (Ionen) zwischen Zellinnerem und Zellumgebung (Extrazellularraum) hervorgerufen wird. (15) (16) Die Zellmembran ist unterschiedlich durchlässig für verschiedenartige Teilchen. Deshalb kommt es nicht zum Ausgleich der Konzentrationsunterschiede dieser Teilchen zwischen Intra- und Extrazellularraum. Bedeutsam für die Ausbildung des Ruhemembranpotentials ist einerseits ein intrazellulärer Überschuss negativ geladener, großer Anionen, überwiegend großmolekularer Eiweiße. Daneben besteht ein starker intrazellulärer Überschuss positiv geladener Kalium-Ionen. 11 Im Ruhezustand können Kalium-Ionen die Membran relativ gut passieren, so dass entsprechend dem Konzentrationsgefälle ein stetiger KaliumAusstrom existiert. Durch den Verlust positiv geladener Teilchen bildet sich eine Ladungsdifferenz aus, so dass das Zellinnere gegenüber dem Extrazellularraum negativ geladen ist. Diese Ladungsdifferenz wirkt allerdings einer weiteren Steigerung des Ausstroms der positiv geladenen Kalium-Ionen entgegen, so dass ab einer bestimmten elektrischen Spannung die Kraft, die die Kalium-Ionen nach außen drängt (Konzentrationsunterschied) einer gleichgroßen Kraft, die die Kalium-Ionen in die Zelle zurückdrängt (Ladungsunterschied), gegenübersteht. Man spricht von einem sogenannten Kalium-Gleichgewichtspotential, welches sich bei einem Potential von etwa -80 mV ausbildet, dem sogenannten Ruhemembranpotential. Gleichzeitig besteht eine erheblich geringe Permeabilität der Zellmembran für Natrium-Ionen. In diesem Fall sind die treibenden Kräfte extrazellulär erhöhte Natriumkonzentration sowie extrazellulär erhöhte Anzahl positiver Ladung - jedoch erheblich stärker, so dass trotz der geringeren Permeabilität ein merklicher kontinuierlicher Natriumeinstrom resultiert. Beständiger passiver Kaliumausstrom und Natriumeinstrom würden zwar das Membranpotential nicht verändern, es käme jedoch allmählich zu einem Ausgleich der Teilchenkonzentrationen zwischen Intra- und Extrazellularraum. Dem wirken energieabhängige sogenannte Ionenpumpen entgegen, welche aktiv jeweils ein Kalium-Ion in die Zelle hinein, und dafür ein Natrium-Ion heraus pumpen. (Die Energie für die ‚Pumpen’ liefert das Adenosintriphosphat bzw. das Enzym ATPase.) - Netto resultieren im Ruhezustand konstante Konzentrationsverhältnisse der extra- und intrazellulären Teilchen sowie ein konstantes Potential, eben das Ruhemembranpotential. Wird eine Nervenzelle erregt, so erhöht sich spontan die Durchlässigkeit (Permeabilität) der Membran für Na+-Ionen um das 500fache. Es strömen Na-Ionen nach innen, sodass das Innere der Nervenzelle jetzt gegenüber dem Äußeren eine positive Ladung von etwa +30 mV aufweist. Diesen Vorgang bezeichnet man als Depolarisation der Zelle. Bereits während (und als Folge) dieser Ladungsänderung schließt sich zunächst der Natriumkanal. Durch anschließendes Überwiegen der Kaliumpermeabilität dringen vermehrt positiv geladene Kalium-Ionen nach außen (die "umgekehrte" Ladungsdifferenz begünstigt dies zu diesem Zeitpunkt) und es kommt zum Wiederaufbau des Ruhemembranpotentials (RePolarisation), welches letztlich wieder mit Hilfe der sogenannten Ionenpumpen stabilisiert wird. Dieser gesamte, immer gleichförmig ablaufende Vorgang wird als Aktionspotential bezeichnet. (Abb. 17, 18, 19) Wird also ein Neuron durch einen Reiz, der über seiner Reizschwelle liegt, erregt, so ‚feuert’ es stets ein solches Aktionspotential ab, das immer gleich groß ist (-30 bis -45 mV außen gegen innen) und nun entlang des Axons fortgeleitet wird – allerdings nicht kontinuierlich (wie etwa Elektronen in einem Leiter), sondern ‚sprunghaft’ (saltatorisch) von Schnürring zu Schnürring (Ranvier’sche Schnürringe siehe Abb. 12, 13). Erhöht man die Reizintensität, so erhöht sich keineswegs auch das Aktionspotential. Vielmehr erhöht sich die Frequenz, also die Anzahl dieser Potentiale pro Sekunde. Ist das erregte Neuron ein Rezeptor, so teilt dieser dem ZNS (Gehirn) also lediglich zwei Nachrichten mit: 1. dass ein Reiz erfolgte, der über der Reizschwelle lag (unterhalb dieser Schwelle feuert das Neuron nämlich – nach dem sog. Alles-oder-Nichts-Gesetz – überhaupt nicht!) und 2. wie stark dieser Reiz war. Über die Art oder die Eigenschaften des Objekts, das diesen Reiz auslöste, teilt das Neuron dem Gehirn ebenso wenig mit wie über die Qualität des Reizes. (Prinzip der undifferenzierten Codierung). So kann ein optischer Rezeptor in der Retina durchaus nicht nur durch Licht (Photonen bzw. elektromagnetische Strahlung) erregt werden, sondern auch elektrisch, mechanisch oder chemisch: die Reaktion des Rezeptors ist stets die gleiche: er feuert – abhängig von der Reizstärke – Aktionspotentiale ab. 12 (17) (18) Aktionspotential (19) 13 (20) Aktionspotentiale zweier unterschiedlicher sensorischer Neuronen. Allerdings zeigen unterschiedliche Neuronen eventuell unterschiedliche Frequenzen bei gleicher Reizung. (Abb. 20, 23) Die saltatorische Fortleitung der Erregung entlang der Ranvier’schen Schnürringe führt für gewöhnlich zu den Synapsen an den Enden der Verzweigungen des Axons. Hier wird nun die Erregung auf chemischem Wege auf die Dendriten eines nachfolgenden Neurons übertragen. 21a 22 14 21b / 21c 23 15 Dies geschieht durch chemische Botenstoffe, die sog. Neurotransmitter: in Abhängigkeit von der Stärke (Frequenz) des eintreffenden neuroelektrischen Signals wird aus den Vesikeln (Speicherbläschen) der Synapse eine bestimmte Quantität solcher Botenstoffe in den synaptischen Spalt (synaptic cleft) ausgeschüttet, durch den sie auf die Transmitter-Rezeptoren des postsynaptischen Neurons diffundieren. (Die Neurotransmitter werden danach auf verschiedene Weise inaktiviert oder wieder abgebaut.) Die Wirkung dieser Neurotransmitter auf das postsynaptische Neuron kann allerdings ganz verschieden sein: ein Botenstoff kann letzteres entweder erregen oder dessen Reizschwelle herabsetzen, ein anderer aber kann die nachfolgende Nervenzelle auch hemmen oder deren Reizschwelle heraufsetzen. Der wichtigste erregende Transmitter im ZNS ist Glutamin, die wichtigsten hemmenden Transmitter sind Gamma-Aminobuttersäure (im ZNS) und Glycin (im peripheren Nervensystem). Andere bekannte Transmitter-Substanzen sind die Monoamine Nor-Adrenalin, Acetylcholin, Dopamin, Serotonin, Octopamin oder bestimmte Neuropeptide (Endorphine und Enkephaline; körpereigene morphiumähnliche Stoffe) usw. – Wir übergehen hier die Tatsache, dass manche Nervenfasern (z. B. fast alle Fasern des Parasympathicus, die präganglionären Fasern des Sympathicus und die meisten motorischen Neuronen) in ihren Synapsen nur (oder ganz überwiegend) Acetylcholin produzieren (sie werden deshalb cholinerge Fasern genannt), andere dagegen (wie die postganglionären Fasern des Sympathicus) nur Nor-Adrenalin (sog. adrenerge Neuronen). Wesentlich für die hier zu betrachtenden Sachverhalte ist lediglich, dass einige Transmitter die postsynaptische Faser hemmen, andere sie erregen können. Da das postsynaptische Neuron u. U. eine beträchtliche Zahl an Dendriten besitzt, an denen die Synapsen vieler verschiedener zuführender (präsynaptischer) Neuronen hängen, kann es von diesen zur gleichen Zeit eine Vielzahl sowohl hemmender als auch erregender Impulse empfangen. Und wie reagiert es auf diese vielfältigen Meldungen? Ganz einfach: es addiert die erregenden Impulse und subtrahiert davon die Summe der hemmenden Impulse. 24 16 Dass die Rechen- oder ‚Denk’-Tätigkeit des Neurons also hauptsächlich im Summieren positiver und negativer Impulsmeldungen aus den ihm vorgeschalteten Neuronen besteht, brauchte Douglas Hofstadter auf die einprägsame Formel I think – therefore I sum. (die natürlich an Descartes erinnern soll). Dieser Umstand ermöglicht es uns nun, zu der Frage zurück zu kehren, warum wir scharf sehen. Wir hatten bereits gezeigt, dass die Retina aus vier verschiedenen Zellschichten besteht (s. Abb. 9): Die Erregung der optischen Rezeptorzellen wird dabei zuerst – postsynaptisch ! – auf die sog. Horizontalzellen übertragen, die ihrerseits horizontal miteinander verschaltet sind. Stellen wir uns einen Rezeptor vor, der von einem starken Lichtreiz erregt wird und diese Erregung auf die nächste Horizontalzelle überträgt. Stellen wir uns ferner vor, dass diese Horizontalzelle ihre Nachbarzellen desto stärker hemmt, je stärker sie selbst erregt wurde. Auf die Nachbarrezeptoren fällt vielleicht etwas weniger Licht als auf den ersten, was zur Folge hat, dass die nachgeschaltete Horizontalzelle ihre Nachbarinnen etwas weniger hemmt. Die nachfolgenden Graphiken 26-29 zeigen, wie der Mini-Computer der Retina-Neuronenverbände durch diesen als Laterale Inhibition bezeichneten Verrechnungsmodus (der an so etwas wie das ‚Remastering’ alter Tonaufnahmen für digitale Medien erinnert) das ursprünglich unscharfe Retinabild zu einem selbsterzeugten neuen Bild rekonstruiert, welches gerade diskontinuierliche Helligkeits- oder Farbunterschiede besonders scharf hervorhebt. Im Ordner „Ergänzungen“ befinden sich zwei GIF-Animationen zur Lateralen Inhibition. Klicken Sie diese Dateien mit der rechten Maustaste an, gehen Sie auf „Öfnnen mit ...“ und wählen Sie zum Öffnen Ihren Internetbrowser aus. Übrigens ist es erstaunlich, dass wir wohlbekannte Gebilde sogar auf überaus unscharfen Bildern (ganz ohne ‚Remastering’) erkennen können – wie etwa im folgenden Bild Abraham Lincoln: 25 17 26 Wirkung der Lateralen Inhibition 27 18 28 29 19 Die Wirkung der Lateralen Inhibition kann direkt wahrgenommen werden an der sog. Hermann’schen Gittertäuschung (man achte auf die Kreuzungen!) sowie an den Mach’schen Bändern (benannt nach dem Physiker Ernst Mach). 30 31 20 32 Mach-Bänder: Die homogen gefärbten Bänder erscheinen jeweils rechts dunkler und links heller. 34 33 35 21 36 Mach-Bänder 22 37 ‚Light of Sweden’ 23 38 39 Assimilation: Alle grauen Felder sind gleich hell. Sie erscheinen aber auf schwarzem Hintergrund dunkler und heller auf weißem. Die Helligkeitsänderung ist dem Kontrast genau entgegengesetzt. 24 40 Die Fraser-Wilcox-Illusion: Die Scheiben scheinen in der Richtung schwarz → dunkelgrau → weiß → hellgrau → schwarz zu rotieren. Das Bild ist dennoch völlig statisch (keine Animation !) – Dieser Effekt tritt – infolge der Lateralen Inhibition – auch bei den Farbrezeptoren auf: 25 41 26 42