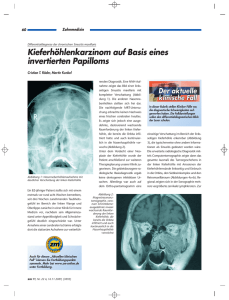
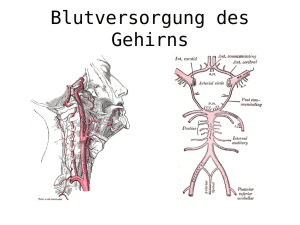
Das invertierte Papillom der Nase und Nasennebenhöhlen
Werbung

Aus der Universitätsklinik für Hals-Nasen-Ohrenheilkunde der Albert-Ludwigs-Universität Freiburg im Breisgau Das invertierte Papillom der Nase und Nasennebenhöhlen - Klinik, Diagnostik und Therapieergebnisse - INAUGURAL-DISSERTATION zur Erlangung des Medizinischen Doktorgrades der Medizinischen Fakultät der Albert-Ludwigs-Universität Freiburg im Breisgau vorgelegt 2006 von Stefanie Behringer geboren in Villingen Dekan Prof. Dr. med. Christoph Peters 1. Gutachter Priv.-Doz. Dr. Gerd Jürgen Ridder 2. Gutachter Prof. Dr. med. Georg Mols Jahr der Promotion: 2007 Gewidmet meiner Oma Elsbeth Kemperdick Inhaltsverzeichnis 1 Inhaltsverzeichnis 1. Einleitung___________________________________________________________ 3 1.1. Historisches ____________________________________________________________ 9 2. Patienten und Methoden ______________________________________________ 11 2.1. Untersuchungsdesign ___________________________________________________ 11 2.2. Patientenerhebung _____________________________________________________ 11 2.3. Datenauswertung_______________________________________________________ 13 2.4. Operationsmethoden ____________________________________________________ 13 2.5. Histopathologische Untersuchungen und Tumorklassifikation _________________ 14 2.6. Statistische Auswertung der gewonnenen Information ________________________ 16 3. Ergebnisse _________________________________________________________ 17 3.1. Alters- und Geschlechtsverteilung _________________________________________ 17 3.2. Klinische Symptomatik des invertierten Papilloms ___________________________ 18 3.3. Nebenbefunde _________________________________________________________ 19 3.4. Intervall zwischen erstem Auftreten der Symptomatik bis Diagnosestellung ______ 21 3.5. Lokalisationen des invertierten Papilloms __________________________________ 23 3.6. Ausdehnungsbestimmungen ______________________________________________ 24 3.7. Beziehung zwischen Lokalisation des Primärpapilloms und malignen Entartungen 26 3.8. Einteilung nach dem Staging-System von Krouse ____________________________ 27 3.9. Größe des invertierten Papilloms _________________________________________ 28 3.10. Beziehung zwischen der Tumorgröße und maligner Entartung ______________ 29 3.11. Histologische Auswertungen ___________________________________________ 31 3.11.1. Wachstumsformen _________________________________________________________ 31 3.11.2. Malignisierungstendenzen ___________________________________________________ 33 3.12. Potentielle Risikofaktoren für die Entstehung des invertierten Papilloms ______ 36 3.13. Präoperative Maßnahmen _____________________________________________ 38 3.13.1. Präoperativ verschriebene Medikation _________________________________________ 38 3.13.2. Präoperative Diagnostik ____________________________________________________ 38 3.14. Frühere OPs im Hals-Nasen-Ohren-Bereich ______________________________ 41 3.15. Operationsverfahren _________________________________________________ 43 3.15.1. 3.15.2. 3.15.3. 3.15.4. Techniken _______________________________________________________________ Anästhesie _______________________________________________________________ Operationszugang _________________________________________________________ Postoperativer Beobachtungszeitraum nach den einzelnen Operationszugängen _________ 43 43 44 45 3.16. Häufigkeit der einzelner Operationsmethoden ____________________________ 47 3.17. Nachresektionen _____________________________________________________ 54 3.18. Postoperative Beschwerdesymptomatik und Komplikationen ________________ 56 3.18.1. Intra- und postoperative Komplikationen _______________________________________ 56 3.18.2. Postoperative Beschwerdesymptomatik ________________________________________ 56 Inhaltsverzeichnis 2 3.19. Postoperativ verordnete Medikation_____________________________________ 62 3.20. Aufenthaltsdauer ____________________________________________________ 64 3.20.1. Durchschnittliche stationäre Aufenthaltsdauer nach einzelnen Operationstechniken ______ 65 3.21. Postoperativer Beobachtungszeitraum ___________________________________ 67 3.22. Rezidive ____________________________________________________________ 68 3.22.1. 3.22.2. 3.22.3. 3.22.4. 3.22.5. 3.22.6. 3.22.7. 3.22.8. 3.22.9. 3.22.10. 3.22.11. 3.22.12. 4. Frühere Papillome in der Krankengeschichte ____________________________________ Spätere Rezidive __________________________________________________________ Dauer bis zur Entstehung eines Tumorrezidivs ___________________________________ Lokalisation des Rezidivs ___________________________________________________ Vergleich der Ausbreitungsseite von Rezidiv und Primärtumor ______________________ Größe des Rezidivs ________________________________________________________ Vergleich der Größe des Primärtumors mit der Größe des Rezidivs___________________ Einteilung der Rezidivtumoren nach der Klassifikation von Krouse __________________ Anzahl der einzelnen Operationsmethoden zur Rezidivresektion _____________________ Tendenz zur Malignisierung der Rezidivtumoren ______________________________ Verlauf maligne transformierter IP __________________________________________ Analyse zur Rezidivwahrscheinlichkeit ______________________________________ 68 70 70 72 73 74 74 75 76 77 77 78 Diskussion _________________________________________________________ 79 4.1. Allgemeines zum invertierten Papillom ____________________________________ 79 4.2. Histologie und Staging Systeme ___________________________________________ 82 4.3. Lokalisation ___________________________________________________________ 85 4.4. Ätiologie ______________________________________________________________ 86 4.5. Inzidenz, Alters- und Geschlechtsverteilung ________________________________ 87 4.6. Klinische Symptomatik des invertierten Papilloms ___________________________ 89 4.7. Präoperative Maßnahmen _______________________________________________ 89 4.8. Operationsmethoden ____________________________________________________ 92 4.9. Anwendung der Radiochemotherapie ______________________________________ 98 4.10. Entwicklung von postoperativen Komplikationen _________________________ 99 4.11. Tendenz zur Rezidivierung des invertierten Papilloms _____________________ 100 4.12. Rezidive nach bestimmten Operationsmethoden __________________________ 104 4.13. Karzinomatöse Entartung des invertierten Papilloms _____________________ 106 4.14. Wahl der Operationstechnik bei karzinomatöser Entartung ________________ 109 5. Zusammenfassung __________________________________________________ 110 6. Literaturverzeichnis _________________________________________________ 112 7. Anhang ___________________________________________________________ 129 Einleitung 1. 3 Einleitung Invertierte Papillome, auch Schneider Papillome genannt, sind vorwiegend benigne Tumoren der Nase und Nasennebenhöhlen, welche trotz intensiver Forschung noch nicht vollständig erschlossen werden konnten und somit auch heute noch ein Thema lebhafter Kontroverse darstellen [20, 23, 55, 112, 116, 158]. Seinen Beinamen Schneider Papillom erhält der Tumor aufgrund dessen, dass sich die invertierten Papillome in einem Areal der Nasenschleimhaut befinden, das entwicklungsgeschichtlich der sogenannten „Schneider Membran“ entspricht. Dieses Schleimhautareal lässt sich embryologisch von den Riechplakoden ableiten und ist somit, im Gegensatz zur übrigen, entodermal abstammenden Respirationsschleimhaut, ektodermaler Herkunft [149]. Die „Schneider Membran“ entwickelt sich am Ende der vierten Woche der Embryonalentwicklung und erstreckt sich bis in die muköse Membranschicht des Nasopharynx, welche zwar entodermalen Ursprungs ist, sich jedoch histologisch als identisch zeigt [149]. Besonderen Stellenwert erhält dieser Tumor vor allem durch den Umstand, dass weder die Ätiologie ausreichend geklärt ist, noch einheitliche Literaturangaben zur Rezidivrate (1070%) und zu seinem Potential für maligne Entartung (1-53%) vorliegen [37, 62, 135]. Außerdem ist die Frage, ob es sich bei Malignisierungen um einen syn- oder metachronen Vorgang handelt, bis heute offen [31, 37]. Nur bei wenigen Merkmalen ist man sich allgemein einig, so unter anderem bei der Tatsache, dass das invertierte Papillom mit einem prozentualen Anteil von 0,5-4% eher zu den seltenen Tumoren des Nasen- und Nasennebenhöhlensystems gezählt wird [73]. Die jährliche Inzidenz wird mit ca. 0,6/100 000 angegeben [36]. Außerdem besteht weltweit darüber Übereinstimmung, dass Männer wesentlich häufiger betroffen sind als Frauen, und Weiße öfter an dieser Neubildung erkranken als Schwarzhäutige [158]. Das invertierte Papillom tritt vor allem in der 5. und 6. Lebensdekade auf [7], jedoch wurden diese Epithelgeschwülste bereits in allen Altersstufen von 6 bis 100 Jahren beobachtet [160], wobei invertierte Papillome in der Kindheit nur äußerst selten vorkommen [42]. Einleitung 4 In der Studie von Kelly et al. wird von einem sechsjährigen Jungen mit invertiertem Papillom (IP) berichtet [74]. 1985 wurde von Eavey die erste in der Literatur bekannte pädiatrische Studie über invertierte Papillome veröffentlicht, welche aus fünf Patienten im Alter von 6 bis 20 Jahren bestand, von denen in einem Fall auch eine maligne Entartung beschrieben wurde. Gemäß dieser Beobachtung setzte sich Eavey in besonderem Maße dafür ein, bei Kindern die gleiche radikale chirurgische Therapiestrategie wie bei erwachsenen Patienten anzuwenden [42]. Histopathologisch handelt es sich bei dieser Tumorentität um umschriebene Epithelgeschwülste, die breitbasig der Oberfläche aufsitzen. Je nach Wachstumsrichtung kann die Geschwulstmasse des invertierten Papilloms oberhalb (exophytisch) oder unterhalb der umgebenen Ausgangsoberfläche liegen (invertiert) [97, 124]. Sie gehen von den mit Plattenepithel bedeckten Schleimhäuten, von Plattenepithelien der Haut oder vom Urothel aus, können sich aber auch von metaplastischen Plattenepithelien herleiten [124]. Morphologisch imponiert das exophytisch wachsende Papillom als blumenkohlartig bis pilzförmig über das Mukosaniveau wachsende Geschwulst [3, 16]. Das invertierte Papillom wächst dagegen mit glatter Oberfläche unter das Mukosaniveau und breitet sich, seine umgebenden Strukturen verdrängend, endophytisch aus. Trotz der glatten Schleimhautoberfläche hat es dennoch eine unregelmäßige höckerige Form und ist, im Gegensatz zu den weichen, glasigen Nasenpolypen, von derber Konsistenz [7]. Makroskopisch erscheint das invertierte Papillom als gelblich bis lachsfarbene Raumforderung mit grauweißer Schnittfläche und blutet bei Berührung leicht [124]. Trotz dieser makroskopischen Unterschiede ist die Polyposis nasi die typische und häufigste Fehldiagnose [7]. Das invertierte Papillom hat meistens seinen Ursprung an der lateralen Nasenwand, kann aber auch dem Nasenseptum oder den Nasennebenhöhlen, wie vorzugsweise der Kieferhöhle und dem Sinus ethmoidalis entspringen. Gefährlich werden sie hierbei vor allem, wenn sie in die knöchernen Strukturen des Gesichtsschädels einwachsen, besonders des harten Gaumens sowie der Orbita [46, 76]. 1987 wurde von Stone et al. erstmals ein Schneider Papillom im Bereich des Mittelohrs und des Mastoids beschrieben, bei einem Patienten, der kurz zuvor erst an einem Einleitung 5 invertierten Papillom im Bereich der lateralen Nasenwand und des Sinus maxillaris litt. Seiner These nach diente hier die Tuba Eustachii als Führungskanal für die lokale Ausbreitung des Tumors [44, 152]. Im Jahre 1989 wurde von Altug et al. die Vermutung eines multizentrischen Ursprungs des Tumors geäußert [2]. 1993 wurde zum ersten Mal durch Roberts et al. ein invertiertes Papillom im Mittelohr, de novo wachsend, publiziert [127]. Ektopische Migrationen der „Schneider Membran“ während der Embryonalentwicklung könnten für diese außergewöhnlichen und selten vorkommenden Lokalisationen in Betracht gezogen werden [104]. Histologisch bestehen invertierte Papillome aus Invaginationen von plattenepithelial metaplastischen Epithelien, die sich in abgerundeten Zapfen in das darunterliegende Schleimhautstroma hineindrücken [124, 172]. Die Epithelnester werden allseits von einer zumeist gut abgrenzbaren Basalmembran umgeben. Zellulär sind keine wesentlichen Atypien erkennbar. In den Randbereichen invertierter Papillome ist nicht selten eine Übergangszone von respiratorischen Epithelien vorhanden, die sich metaplastisch in reifes Plattenepithel transformieren. Gelegentlich kann man Plattenepitheldysplasien und Zellatypien finden, weshalb das invertierte Papillom als potentiell maligne eingestuft wird [124], deshalb ist differentialdiagnostisch die Abgrenzung zum invasiven Plattenepithelkarzinom wichtig, welches teils unscharf begrenzte Epithelnester mit deutlichen Zell- und Kernpleomorphien sowie eine desmoplastische Stromareaktion zeigt. Vereinzelt kann man im IP mikroskopisch mehrere Stufen von Mitosen finden, welche als Hinweis für eine mögliche Rezidivhäufigkeit oder ein bösartiges Wachstumsmuster gewertet werden können. Darüber hinaus kann die Positivität von β-HCG auf die Neigung zu Rezidiven weisen [28, 89]. Klinisch ist das IP durch drei Hauptkriterien gekennzeichnet [176]: 1. Lokal destruierendes Wachstum 2. Häufige Rezidivierung 3. Tendenz zur malignen Entartung Einleitung 6 Die klinische Symptomatik der IP ist eher unspezifisch. Radiologische Hinweise auf das Vorliegen eines IP ergeben sich durch das, im Gegensatz zu der chronisch polypösen Sinusitis, fast immer einseitige Auftreten dieser Epithelgeschwulst. Bemerkbar macht es sich vor allem durch die über die Zeit zunehmende Obstruktion der oberen Atemwege [174]. Die Patienten beklagen deshalb vor allem eine Nasenatmungsbehinderung. Sobald die Raumforderung den Drainageweg innerhalb oder aus den Nasennebenhöhlen verlegt, kann es sekundär zu Cephalgien und rezidivierenden Sinusitiden kommen [51]. Selten kommt es aber auch zur Epistaxis und vereinzelt zum Verlust von Riech- und Geschmacksvermögen. Da der Tumor meist sehr langsam an Größe zunimmt, wird die Diagnose „Invertiertes Papillom“ häufig erst Monate bis Jahre später gestellt. Die Ätiologie für das Auftreten von invertierten Papillomen ist noch immer unklar. Mehrere Theorien sind bekannt. So vermutete Jahnke 1971 aufgrund elektronenmikroskopisch gefundener Kerneinschlusskörperchen eine virale Genese [67]. Respler et al. nutzte lange Zeit molekulare Hybridisierungstechniken wie dem „Southern Blot“ und konnte 1987 die Anwesenheit von einer Virus-DNA in invertierten Papillomen nachweisen, welche dem bis dahin bekannten humanen Papillomavirus (HPV) Nr. 11 auf das Äußerste ähnelte [123]. Weiterhin konnte auch Weber et al. in seinen in situ DNA-Hybridisierungen in 16 von 21 Fällen (76%) Papillomavirus-DNA Sequenzen feststellen [166]. Nach neuesten Kenntnissen werden vor allem Papillomaviren Typ 16 und 18 für die Entstehung von Papillomen verantwortlich gemacht [37], kürzlich wurde aber auch neben der Rolle des HPV für die Ätiologie des IP eine mögliche Beteiligung des Epstein-BarrVirus (EBV) angegeben [66]. Auch die Proliferation von Nasenpolypen bei der Entstehung von IP wurde diskutiert [104]. Lange Zeit wurde über die Möglichkeit einer allergischen Ursache nachgedacht, diese These wurde aber aufgrund des nahezu ausschließlich einseitigen Auftretens fast völlig ausgeschlossen [90]. In den Untersuchungen von Hyams und Coautoren, fand sich unter 149 IP-Patienten kein einziger Betroffener mit einer manifesten Allergie oder klinischen Symptomen, durch welche man auf eine atopische Diathese schließen konnte [65]. Einleitung 7 Bereits 1935 wurde ein Zusammenhang zwischen chronischen Sinusitiden und dem Entstehen von invertierten Papillomen diskutiert. Diesem Thema widmeten sich vor allem Kramer & Som. Da jedoch das IP in den meisten Fällen zu nasaler Obstruktion führt und diese wiederum eine Sinusitis fördert, gelang ihnen in diesem Bereich kein eindeutig überzeugender Beweis [77]. Eine entzündliche Ätiologie ist derzeit immer noch im Gespräch, doch auch hier gibt es keine eindeutigen Fakten, die diese Theorie beweisen würden [59]. Außerdem sind Sinusitiden viel zu allgemein vorkommend und invertierte Papillome viel zu selten, als dass sich in diesem Bereich eine eindeutige ätiologische Beziehung schlussfolgern ließe [104]. Auch ob eine genetische Vererbung, und wenn ja, welcher Art, eine Rolle bei der Entstehung von IP spielt, konnte derzeit noch nicht ausreichend geklärt werden. 1984 vertraten Majumdar & Beck die These, dass Stahlarbeiter durch extrinsische Faktoren einem höheren Risiko ausgesetzt sind, an einem IP zu erkranken, doch erwies sich auch dieses Argument als nicht haltbar [93]. Insgesamt kann man derzeit noch keine gesicherten Aussagen über die zugrunde liegende Ursache invertierter Papillome machen [90]. Unbestrittene Risikofaktoren sind auch hier, wie bei allen anderen Tumoren im HalsNasen-Ohren-Bereich, Nikotin- und Alkoholabusus [20, 118, 146]. Tatsache ist außerdem, dass die Mehrzahl der Patienten mit invertiertem Papillom bereits vorher an einer Sinusitis und/oder Polyposis nasi litten oder zum Zeitpunkt der Diagnose noch immer leiden [90]. Wegen des malignen Entartungspotentials des IP ist die weltweit akzeptierte Therapie der Wahl die radikale Entfernung des erkrankten Gewebes [58, 159]. In den 70er und 80er Jahren ging man vor allem dem Therapiekonzept der chronisch polypösen Rhinosinusitis nach, um eine größtmögliche Schleimhautprotektion zu gewährleisten, jedoch mussten diese Techniken bis zu 50% hohe Rezidivrate verbuchen [31], weshalb man in den 90ern meist ausgeweitete, radikalere Methoden wählte [68, 170]. Heutzutage wird die allgemeine Lehrmeinung vertreten, dass primär versucht werden sollte, das IP auf endonasalem Wege zu resezieren [102]. Handelt es sich jedoch um ausgedehntere Läsionen oder um Rezidivtumoren, oder kann aufgrund weiter lokaler Tumordestruktionen oder -lokalisation Einleitung 8 keine ausreichende Sicht z.B. zur Schädelbasis gewährleistet werden, so sollte man das endonasale Vorgehen um einen externen Zugang erweitern [27, 73]. Bei großen Tumoren der Kieferhöhle, welche auf endonasalem Wege schwer erreichbar ist, und somit ein vollständiges Entfernen des Tumors nicht in jedem Falle sicher gewährleistet werden kann, empfiehlt es sich, auf die radikalere Methode nach Caldwell-Luc zurückzugreifen, dies sollte allerdings bei jedem Patienten individuell entschieden werden. Vor allem die Weiterentwicklung der Endoskopie sowie der Gebrauch von CT und gelegentlich MRT, hat sich als unverzichtbare präoperative Diagnostik herausgestellt, die es dem Operateur ermöglicht, präoperativ genauere Aussagen über die Lokalisation und Ausbreitung dieses Tumors zu treffen, und erleichtert dadurch die radikale Entfernung des invertierten Papilloms [44, 104]. Die Fragestellungen der vorliegenden Arbeit konzentrieren sich nicht nur auf Klinik und Diagnostik von invertierten Papillomen, sondern beschäftigen sich auch mit den einzelnen Therapieoptionen Malignisierungsrate. sowie den Therapieergebnissen hinsichtlich Rezidiv- und Einleitung 1.1. 9 Historisches Erstmals wurde das invertierte Papillom 1854 durch Ward, einem Londoner Arzt, in Form von zwei Fallstudien beschrieben [165]. Er beobachtete dabei eine Neubildung, welche ihren Ausgang vom Oberflächenepithel der Nasenhaupt- und Nasennebenhöhle, auch bekannt unter dem Namen „Schneider Membran“ nahm und in das darunterliegende Stroma einwuchs [105]. Aufgrund dieses Befundes erhielt das invertierte Papillom des HNO-Bereichs später auch den Beinamen „Schneider Papillom“. Die Entdeckung Wards erregte seiner Zeit allgemeines Interesse, und so wurde bereits ein Jahr später, 1855 durch Billroth eine erste Publikation über diese Neubildung veröffentlicht. Damals gab er dem Papillom den Namen „villiformes Krebsgeschwür“ [15, 165]. Hopmann unterschied 1883 harte und weiche Papillome, welche er dadurch charakterisierte, dass die harten Papillome von Plattenepithel bedeckt waren und die weichen dagegen mit Zylinderepithel [60]. Das harte Papillom stellte sich als äußerst selten heraus. Bis 1897 konnten trotz sehr sorgfältiger Arbeit nur 19 Fälle aus der Literatur zusammengetragen werden, wobei es sich dabei um stets ältere Patienten, meistens Männer, handelte. Später erhielt das harte Papillom auch den Namen „Papilläres Fibrom“ [55]. Im Jahre 1932 veröffentlichten Kramer & Som eine Studie, welche 86 Patienten mit invertiertem Papillom umfasste [77]. 1938 wurden die nasalen Papillome durch Ringertz erstmals nach ihrem Epitheltyp unterteilt, er legte dabei drei Arten von Papillomen fest, die vom zylinder-, vom übergangs- und die vom plattenepithelialen Typ [126]. Von da an wurden mehrere Studien durchgeführt und publiziert, doch da bei dieser Tumorart nur ein sehr seltenes Auftreten beobachtet werden konnte, handelte es sich dabei meist um sehr kleine Studien mit nur wenigen Patienten. Erstmals 1971 veröffentlichte Hyams eine sehr umfangreiche Studie, welche 315 Patienten umfasste, und in der 10 Zylinderzell-, 149 invertierte und 156 fungiforme Papillome nach histologischen und klinischen Eigenschaften ausgewertet wurden [64]. Leider gab es noch keine einheitliche Nomenklatur, weshalb es auch aufgrund des relativ seltenen Auftretens zu einer Vielzahl von Bezeichnungen kam. Einleitung 10 Im Jahre 1985 listete Kristensen et al. in einer durch ihn veröffentlichen Studie 53 verschiedene Synonyme für das invertierte Papillom auf. Diese waren in ihrer Bedeutung zum Teil sehr vage und reichten von ziemlich verharmlosten Bezeichnungen wie „hypertrophische papilläre Sinusitis“ bis zu Begriffen wie „Zylinderzellkrebs“ [79]. Ebenfalls Hyams war es, der als Mitverfasser des im Jahre 1988 erschienenen „Atlas of Tumor Pathologie“, in seinem Kapitel „Tumors of the upper respiratory tract and ear“ vorschlug, die von Ringertz festgesetzten Begriffe „Zylinderzellpapillom, invertiertes und fungiformes Papillom“ aufzugeben, und statt dessen unter nur einer Bezeichnung „sinunasal tract papilloma“ zusammenzufassen [65, 126]. Im Jahre 1991 wurden dann von der World Health Organization drei verschiedene histologische Typen von nasalen Papillomen klassifiziert und als „Exophytische Papillome“, „Invertierte Papillome“ und als „Columnare Zellpapillome“ festgelegt. Man definierte sie allgemein nach ihrem Ausgangsort. So entspringen die exophytischen Papillome meist dem Nasenseptum, wohingegen die invertierten Papillome eher ihren Ausgang von der lateralen Nasenwand nehmen. Von columnaren Papillomen spricht man meist, wenn die Papillome innerhalb der Sinus maxillaris wachsen [143]. Histologisch charakterisierte die WHO 1991 das invertierte Papillom wie folgt: „Es besteht aus invaginierten Krypten, dicken Lagen oder Inseln von nicht keratinisiertem Plattenepithel, welches mit pseudostratifiziertem Säulen-(Zylinder-) epithel oder zilientragendem respiratorischem Epithel alternieren kann. Das mehrlagige Epithel enthält typischerweise Schleimzellen oder schleimgefüllte Mikrozysten. Aus den Einfaltungen der Mukosa können scheinbar diskontinuierliche Zellmassen tief unter Umständen als kontinuierliche Fortsetzung der Basalmembran des oberflächlichen Epithels dargestellt werden. Seltene Foci von oberflächlicher Keratinisierung sind zum Teil vorhanden. ...“ [143]. Patienten und Methoden 2. 2.1. 11 Patienten und Methoden Untersuchungsdesign Im Rahmen einer retrospektiven Untersuchung wurden anhand der Krankenunterlagen und histopathologischen Befunde die an der Universitätsklinik für Hals-, Nasen- und Ohrenheilkunde Freiburg behandelten Patienten mit invertierten Papillomen der Nase und Nasennebenhöhlen der Jahre 1986 bis 2005 ausgewertet. 2.2. Patientenerhebung Die Patientenerhebung stützte sich auf drei unterschiedliche Säulen: 1) Recherche nach den Suchbegriffen „invertiert“ und „Papillom“ im Operationsplanungsprogramm FileMaker Pro der Univ.-HNO-Klinik Freiburg 2) Recherche im Klinikrechenzentrum Freiburg nach stationär behandelten Patienten mit den Entlassungsdiagnose ICD-10 D38.5 Neubildung unsicheren oder unbekannten Verhaltens: Sonstige Atmungsorgane D14.0 Gutartige Neubildung: Mittelohr, Nasenhöhle und Nasennebenhöhlen J33.8 Sonstige Polypen der Nasennebenhöhlen ICD-9 212.0 Gutartige Neubildung der Atmungs- und intrathorakalen Organe, Nasenhöhlen und -nebenhöhlen sowie Mittelohr 235.9 Neubildung unsicheren Verhaltens der Verdauungs- und Atmungsorgane, Sonstige und nicht näher bezeichnete Atmungsorgane Patienten und Methoden 3) 12 Recherche im „PathMed“ des Pathologischen Instituts der Universitätsklinik Freiburg nach den Suchbegriffen „invertiert“ und „Papillom“ Akteneinsicht konnte dabei über das klinikumsinterne „Medizinische Dokumentationsund Informationssystem“ des Universitätsklinikums Freiburg „MeDoc“ gewonnen werden. In dem Zeitraum von 1995 bis 2005 wurden am Klinikum 58 an invertiertem Papillom erkrankte Patienten datiert, das beinhaltet, Nachresektionen sowie Rezidiventfernungen eingeschlossen, 92 Operationen an Papillomen in 10 Jahren an der HNO-Universitätsklinik Freiburg, Probeentnahmen oder frühere Operationen alio loco nicht mitgerechnet. Um die Krankheitsfälle zwischen den Jahren 1986 bis 1995 auswerten zu können, wendeten wir uns an das Zentralarchiv der Mikroverfilmung, wo weitere 29 Fälle von Papillomen auf so genannten „Fiches“ ausgemacht werden konnten, wovon 19 Papillome invertiert waren und sich somit für unsere Studie als geeignet herausstellten. Insgesamt wurden, in Zusammenarbeit mit dem Pathologischen Universitätsinstitut, 2043 Akten von Patienten mit Papillomen eingesehen, wovon 393 Fälle der Hals-Nasen-OhrenHeilkunde zugeordnet werden konnten. Unsere Studie bearbeitete davon 77 Fälle, da ausschließlich Papillom-Erkrankungen analysiert wurden, die erfahrene Pathologen histologisch eindeutig einem invertierten Wachstumsmuster zugeordnet hatten. Fungiforme Papillome oder Zylinderzellpapillome, also onkozytäre Formen wurden nicht in die Studie aufgenommen. Patienten und Methoden 2.3. 13 Datenauswertung Bei der Ausarbeitung der Krankenblätter wurden alle Daten erfasst, die Aufschluss gaben über das klinische Bild sowie Lokalisation und Ausbreitung von invertierten Papillomen, ebenso über deren Diagnostik und Therapieoptionen. Besonderes Augenmerk wurde auf die Analyse von Rezidiven invertierter Papillome als auch auf deren maligne Entartung gelegt. Die Ausdehnung der Tumoren wurde anhand der Operations- und Histologieberichte, der Endoskopie und Spiegeluntersuchungen sowie bildgebenden Verfahren wie CT und MRT bestimmt. Die hier verwendete Größeneinteilung richtet sich nach der Klassifikation von Krouse (siehe Tabelle 1) [80]. Der durchschnittliche postoperative Beobachtungszeitraum belief sich auf 22,56 Monate. 2.4. Operationsmethoden Alle Papillome wurden gemäß der weltweit akzeptierten Lehrmeinung möglichst radikal entfernt. Dies wurde je nach Ursprungsort meist mit Hilfe der lateralen Rhinotomie 36,36%, der Ethmoidektomie 53,25% oder der Technik nach Caldwell-Luc (16,88%) durchgeführt, aber auch das Midfacial Degloving oder Laserbehandlungen kamen gelegentlich zum Einsatz. Je nachdem, welcher Operationsmethode man sich bediente, war der Operationszugang zu 30,26% (n=23) von extern, zu 42,11% (n=32) endoskopisch und zu 27,63% (n=21) mit kombiniertem Operationszugang, wobei über die adäquate chirurgische Vorgehensweise bis heute Uneinigkeit besteht [40]. Patienten und Methoden 2.5. 14 Histopathologische Untersuchungen und Tumorklassifikation Bei der Tumorausdehnungsbestimmung richteten wir uns nach der Klassifikation nach Krouse (2000) [80]. Plattenepithelkarzinome auf dem Boden von IP wurden gemäß der Stadieneinteilung dem allgemein anerkannten TNM-Staging-System zugeordnet [124]. Die Gradeinteilung der Tumordifferenzierung wurde durch den Pathologen durchgeführt. Dabei beziehen sich die Angaben nach der allgemeinen Klassifikation Tumorgraduierung [124]. Tab. 1: Tumorklassifikation nach Krouse [80] T1 Tumorwachstum beschränkt sich auf ein einziges Gebiet in der Nasenhaupthöhle (wie zum Beispiel untere Muschel) T2 Zwei angrenzende intranasale Strukturen betroffen (zum Beispiel Septum und Nasengang) T3 Tumorausbreitung auf die Nasennebenhöhlen (zum Beispiel Sinus ethmoidalis oder sphenoidalis) T4 Extranasale Ausbreitung wie zum Beispiel Orbita, Nasopharynx, Dura, assoziiert mit Malignität zur Patienten und Methoden 15 Tab. 2: Postoperative histopathologische Tumorstadieneinteilung bei maligner Entartung (=Staging) gemäß UICC 1999 [124] pT-Primärtumor pTis pT0 pT1-4 pTx pN-Regionäre Lymphknoten pN0 pN1-3 pN4 pNx pM-Fernmetastasen pM0 pM1 pMx Präinvasives Karzinom (Carcinoma in situ) Keine histologische Evidenz für einen Primärtumor bei der Untersuchung des Resektats Evidenz der zunehmenden Ausdehnung des Primärtumors Die Ausdehnung der Tumorinvasion kann histopathologisch nicht bestimmt werden Keine Evidenz für den Befall regionärer Lymphknoten Evidenz für zunehmenden Befall regionärer Lymphknoten Evidenz für den Befall juxtaregionärer Lymphknoten Die Ausdehnung der Tumorinvasion kann nicht bestimmt werden Keine Evidenz für Fernmetastasen Evidenz für Fernmetastasen Das Vorliegen von Fernmetastasen kann nicht bestimmt werden Tab. 3: Tumordifferenzierungsgrade (=Grading) [124] Grading G1 G2 G3 G4 Gx Hochdifferenzierter Tumor (meist geringe Malignität) Mitteldifferenzierter Tumor (meist mäßiggradige Malignität) Wenig differenzierter Tumor (meist hohe Malignität) Undifferenzierter Tumor (anaplastischer Tumor) Der Differenzierungsgrad kann nicht bestimmt werden Patienten und Methoden 2.6. 16 Statistische Auswertung der gewonnenen Information Als Lage- und Lokalisationsmaße wurden der arithmetische Mittelwert und der Median verwendet. Um die kumulative rezidivfreie Überlebenszeit zu berechnen, verwendeten wir die Methode nach Kaplan & Meier [72]. Überlebensanalysen behandeln im allgemeinen Fall das Problem, mit welcher Wahrscheinlichkeit bestimmte Ereignisse im zeitlichen Verlauf auftreten. Dabei wird in dem zu untersuchenden Zeitraum die Häufigkeit des Auftretens der Ereignisse beobachtet, wobei auch diejenigen Fälle berücksichtigt werden, bei denen das Ereignis bis zum Ende des Beobachtungszeitraums nicht eingetreten ist [56]. Die Überlebenszeitanalyse nach Kaplan & Meier berücksichtigt Informationen, die in den sogenannten zensierten Daten vorhanden sind. Zensierte Daten sind Daten mit zunächst vorläufigem Charakter, weil bei den betreffenden Patienten das Ereignis (z.B. Tumorrezidiv oder Tod) noch nicht eingetreten ist oder sich der weiteren Beobachtung entzogen haben. Damit berücksichtigt die Kaplan-Meier-Methode die Informationen aller Patienten so lange, wie diese beobachtet worden sind. Die Berechnung erfolgt auf folgende Weise: immer dann, wenn für einen Fall das Ereignis (in unserem Beispiel: Rezidiv eines IP) eintritt, werden die Überlebenswahrscheinlichkeiten der noch Lebenden neu berechnet. Die statistischen Berechnungen führten wir mit dem Programm SPSS (Statistical Program for Social Sciences, Version 13.0 für Windows) durch. Ergebnisse 3. 3.1. 17 Ergebnisse Alters- und Geschlechtsverteilung Es wurden 77 Patienten mit der histologisch gesicherten Diagnose „Invertiertes Papillom“ ausgewertet. Dabei fiel ein deutlich höherer Anteil des männlichen Geschlechts mit 83,1% auf (n=64, dagegen nur n=13 Frauen, entspricht 16,9%). Das Durchschnittsalter der 77 Patienten betrug zum Operationszeitpunkt 61 Jahre, wobei der jüngste Betroffene 23 und der Älteste 89 Jahre alt war (Frauen 42-80 Jahre, Männer 23-89 Jahre). Die genauen Daten zur Alters- und Geschlechtsverteilung sind in Abbildung 1 dargestellt. Alters- und Geschlechtsverteilung 18 18 16 14 Anzahl (n) 14 12 12 11 10 8 6 4 4 3 2 0 0 3140 2 2030 2 4 4 3 0 Alter (Jahre) Abb. 1: Alters- und Geschlechtsverteilung 8190 7180 6170 5160 4150 0 Frauen Männer Ergebnisse 3.2. 18 Klinische Symptomatik des invertierten Papilloms Das mit Abstand häufigste klinische Leitsymptom war die einseitige Nasenatmungsbehinderung, die 96,1% (n=74) der Patienten beklagten. Als zweithäufigstes Symptom wurde in 33,8% (n=26) eine nasale Sekretion angegeben. Dem folgten ständige Cephalgien, unter denen 26,0% (n=20) der Patienten litten. Über rezidivierende Sinusitiden, welche später auch histologisch bestätigt wurden, berichteten 52 der Patienten (67,5%). In 11 Fällen wurde über rezidivierende Epistaxis geklagt (14,3%). Weitere, wenn auch nur vereinzelt auftretende Symptome waren Schmerzen beim Nachvornebeugen bei 2 Patienten und deutliche Abnahme bis Verlust des Geruchsinns bei 4 Patienten. In 3 Fällen wurde ein Druckschmerz über den Trigeminusaustrittspunkten berichtet, und einen Patient störte eine sehr trockene Nasenschleimhaut mit ständiger Krustenbildung. Symptomlos war lediglich ein Patient, bei dem das invertierte Papillom in Form eines Tumorrezidivs durch Zufall bei der Nachsorge eines vor Jahren entfernten invertierten Papilloms entdeckt wurde. Monosymptomatisch waren 14 Patienten (18,2%). 66,2% der Patienten litten unter 2 oder 3 der in Abbildung 2 zusammengestellten Symptome (n=51), und 15,6% wiesen sogar 4 bis 6 Symptome auf (n=12). Ergebnisse 19 Symptomatik 75 NAB 52 Rez. Sinusitiden 26 Rhinorrhoe 20 Cephalgie 11 Rez. Epistaxis 4 3 2 1 Verminderter Geruchssinn Druckschmerz Schmerzen beim Beugen Trockene Schleimhaut 0 20 40 60 80 Anzahl (n) Abb. 2: Symptomatik des IP 3.3. Nebenbefunde Für das Fach Hals-Nasen-Ohrenheilkunde spezifische Nebenbefunde waren in 43 Fällen eine Polyposis nasi. Des Weiteren stellte man bei 15 Patienten eine latente chronische Sinusitis fest, hiervon waren besonders die Cellulae ethmoidalis betroffen. Gelegentlich wurde ebenfalls histologisch eine chronische Rhinitis gesichert (n=13). 21 Patienten wiesen eine Septumdeviation auf, wobei diese elfmal nach links gerichtet war und zehnmal nach rechts gerichtet war. Eine Nasenmuschelhyperplasie wurde zehnmal diagnostiziert, davon in der Hälfte der Fälle beidseits. 5 Patienten berichteten über Hörstörungen, darunter Schallempfindungsstörungen und Tinnitus, und in einem Fall wurde ein Cholesteatom diagnostiziert. Des Weiteren mussten bei der stationären Aufnahme einiger Patienten ebenfalls einige internistische Nebenerkrankungen berücksichtigt werden, welche vor allem kardiologischer Natur, wie zum Beispiel Hypertonie (n=13), Herzinsuffizienz (n=3) oder Ergebnisse 20 Koronare Herzkrankheit (n=4), waren. Aber auch Erkrankungen wie zum Beispiel ein Diabetes mellitus (n=8), eine chronische Bronchitis, ein Pankreas- und Blasen-Karzinom, ein Pleuraergusses oder ein Magenulkus lagen vor. 6 Patienten litten an dermatologischen Erkrankungen wie in 2 Fällen einem Basaliom am Nasenflügel, welches bei der Papillomresektion exzidiert wurde, einer Fibrose am medialen Augenwinkel oder einem Hämangiom am Augenlid. Tab. 4: Histologisch gesicherte Nebenbefunde und deren Häufigkeiten Nebenbefunde Polyposis nasi Chron. Sinusitis, latent Chron. Rhinitis Septumdeviation Conchohyperplasie Hörstörungen Cholesteatom Kardiologische Erkrankungen Diabetes mellitus Chron. Bronchitis Pankreas-Karzinom Blasen-Karzinom Pleuraerguss Magenulkus Dermatologische Erkrankungen Anzahl (n) Häufigkeit (%) 43 55,8 15 19,5 13 16,9 21 27,3 10 13,0 5 6,5 1 1,3 10 8 1 1 1 1 1 6 13,0 10,4 1,3 1,3 1,3 1,3 1,3 7,8 Ergebnisse 3.4. 21 Intervall zwischen erstem Auftreten der Symptomatik bis Diagnosestellung Nur 62 der 77 Patienten konnten genauere Angaben über den Zeitrahmen ihrer Beschwerden machen. Von den restlichen 15 Personen hatte wie bereits erwähnt, ein Patient gar keine subjektiven Beschwerden, die weiteren 14 Betroffenen gaben vage Auskünfte wie „seit der Jugend“ oder „schon ewig“. Wegen der Gefahr der Ungenauigkeit wurden diese 15 Fälle in diesem Kapitel nicht in die Auswertungen mit aufgenommen. Detailliertere Angaben sind Tabelle 5 und Abbildung 3 zu entnehmen. Zeitintervall zwischen 1. Auftreten der Symptomatik und Diagnosestellung 20 16 15 Anzahl betroffener 10 Patienten (n) 5 10 7 5 2 1 36 0 96 1 60 48 36 24 1 12 0 3 1 18 12 13 2 1 8 1 6 4 3 1 5 2 2 0,75 1 0 7 Dauer (Monate) Abb. 3: Intervall zwischen erstem Auftreten der Symptomatik und Diagnosestellung Das kürzeste Intervall zwischen dem ersten Auftreten der Symptome und der definitiven Diagnosestellung lag bei 3 Wochen. In diesem Fall handelte es sich um hohen subjektiven Leidensdruck durch rasch progrediente Nasenatmungsbehinderung mit starken Cephalgien. Da der Betroffene kurze Zeit zuvor einer Choanalpolypentfernung unterzogen wurde und er sich ohnehin zur Nachkontrolle beim HNO-Arzt einfand, konnte das IP in seinem Initialstadium diagnostiziert werden. Ergebnisse 22 Tab. 5: Zeitrahmen der Dauer der Symptome Dauer der (Jahre) Bis zu ½ Jahr ½ bis 1 Jahr 1 bis 1,5 Jahre 1,5 bis 2 Jahre 2 bis 3 Jahre 3 bis 4 Jahre 4 bis 5 Jahre Mehr als 5 Jahre Symptome Anzahl der Betroffenen (n) 28 11 3 7 5 1 3 4 Häufigkeit (%) 45,2 17,7 4,8 11,3 8,1 1,6 4,8 6,5 Ergebnisse 3.5. 23 Lokalisationen des invertierten Papilloms Die synoptische Analyse der präoperativen Computertomographie, der starren Endoskopie, der Spiegel- und/oder Röntgendiagnostik sowie der intraoperativen Befunde und postoperativen histologischen Untersuchungen ergab eine bevorzugte Tumorlokalisation in der Nasenhaupthöhle (54,6%), in den Zellen des Siebbeins (50,7%) und im Sinus maxillaris (39,0%). Ebenfalls häufig infiltriert waren das Septum nasi (26,0%) und die mittlere und untere Muschel (15,6%, bzw. 18,2%). Zu 10,4% befand sich der Tumor im Bereich des Infundibulum nasi. Der Sinus sphenoidalis sowie der Sinus frontalis waren zu 9,1% betroffen. Das IP zeigte in insgesamt 42 Fällen Ausdehnungen bis an die vordere Schädelbasis. Detaillierte Angaben zum Manifestationort des IPs lassen sich aus Abbildung 4 entnehmen. Lokalisation des IP 42 NHH 39 Siebbein 29 Kieferhöhle 20 Septum 14 untere Muschel 12 mittlere Muschel 8 Infundibulum 7 Keilbeinhöhle 7 Stirnhöhle 5 Vestibulum 0 10 20 30 Anzahl (n) Abb. 4: Lokalisationen des IP 40 50 Ergebnisse 3.6. 24 Ausdehnungsbestimmungen Bei unseren Auswertungen bezüglich der Tumorausdehnung richteten wir uns nach den Angaben aus Operationsberichten und den Beschreibungen des Pathologen. In 88,3% nutzte man die Endoskopie (n=68) und in 40,3% die Spiegeluntersuchung (n=31). Bei 85,7% unseres Patientenkollektivs wurde ein CT angefertigt (n=66), welches guten Aufschluss über Lokalisation und Ausdehnung gab. Die eigentliche präoperative Diagnostik wird später abgehandelt. Bei 10 der 77 Patienten wurde zusätzlich eine Infiltration extranasaler Strukturen diagnostiziert und histologisch gesichert. Hierbei handelte es sich in 5 Fällen um Anteile des Orbitabodens (6,5%). Viermal zeigte sich, ursprünglich vom Sinus sphenoidalis ausgehend, ein Heranreichen des IP an die Dura (5,2%). Insgesamt reichte das Tumorwachstum in 42 Fällen an die vordere Schädelbasis heran. Tumorausdehnung 10 67 Abb. 5: Tumorausbreitung Infiltration in extranasale Strukturen Ausbreitung beschränkt sich auf endonasale Strukturen Ergebnisse 25 Bei unserem Patientenkollektiv trat der Tumor in 68,8% der Fälle multilokulär auf, wodurch sich die deutlich größere Anzahl an Manifestationsorten im Vergleich zur Patientenzahl erklären lässt. Der überwiegende Teil der invertierten Papillome trat unilateral auf, hierbei war vor allem die rechte Seite mit 53,3% befallen (n=41). Zu 35,1% konnte der Ausgangsort des IP auf der linken Seite ausgemacht werden (n=27). Lediglich in 9 Fällen unseres Patientenkollektivs wurde eine bilaterale Manifestation des Tumors festgestellt, was einen prozentualen Anteil von 11,7% ausmacht. Seite des Tumors Bilateral 12% Links 35% Abb. 6: Lokalisationen des IP Rechts 53% Ergebnisse 3.7. 26 Beziehung zwischen Lokalisation des Primärpapilloms und malignen Entartungen Insgesamt gab es in 8 Fällen unseres Patientenguts maligne Entartungen, da aber zum Teil pro Patient mehrere anatomische Strukturen betroffen waren, übersteigt hier die Zahl der Lokalisationen die Zahl der Betroffenen. In 4 Fällen entstand das Plattenepithelkarzinom auf dem Boden eines IP des Sinus ethmoidalis (50% der maligne entarteten Fälle). Dreimal gingen die entarteten Zellen vom Sinus maxillaris aus (37,5%), gefolgt von jeweils 2 Fällen von Malignisierung im Sinus frontalis, der Nasenhaupthöhle und dem Septum nasi (25,0%). Jeweils einmal waren Strukturen des Vestibulums, des Sinus sphenoidalis und des Processus uncinatus betroffen (12,5%). Detailliertere Angaben sind auch in Tabelle 6 ersichtlich. Tab. 6: Zusammenhang zwischen Lokalisation des IP und maligner Entartung Lokalisation des IPs Sinus maxillaris Septum nasi Sinus ethmoidalis Vestibulum Nasenhaupthöhle Sinus sphenoidalis Sinus frontalis Processus uncinatus Anzahl der Malignisierungen (n) 3 3 4 1 3 1 3 1 Häufigkeit (%) 37,5 37,5 50,0 12,5 37,5 12,5 37,5 12,5 Ergebnisse 3.8. 27 Einteilung nach dem Staging-System von Krouse Gemäß der Tumorklassifikation von Krouse [80] wurden die histologisch als invertiert gesicherten Papillome in 4 verschiedene Staging-Einheiten eingeteilt. So konnten 11 Epithelgeschwülste der Klasse T1 zugeordnet werden (14,3%), 24 Tumoren dem Stadium T2 (31,2%), die Mehrzahl der IPs (31 Fälle; 40,3%) gehörten der Klasse T3 an, und 11 Patienten erkrankten an einem IP des Stadiums T4 (14,3%). Genaueres wurde in Abbildung 7 dargestellt. Tumorstadium nach Krouse T4 14% T3 41% T1 14% T2 31% Abb. 7: Einteilung der Tumoren nach der Klassifikation von Krouse Ergebnisse 3.9. 28 Größe des invertierten Papilloms Die Größe der Tumoren wurde zum einen intraoperativ durch den behandelnden HNOArzt bestimmt, zum anderen durch den Pathologen. Mit einem Anteil von 37,1% überstieg die Mehrzahl der IPs nicht eine Größe über 1 cm. 28,9% der Epithelgeschwülste war zwischen 1 und 2 cm. Zwischen 2 und 3 cm waren 16,5% und zwischen 3 und 4 cm 10,3% der Tumorentnahmen. 3,1% hatten eine Größe zwischen 4 und 5 cm und 1,0% waren zwischen 5 und 6 cm groß. 6 bis 7 cm große Gewebestücke fand man zu 3,1%. Weitere Informationen sind in Tabelle 7 aufgeführt. Tab. 7: Tumorgröße und Häufigkeiten Tumorgröße (cm) 0-0,5 0,6-1 1,1-1,5 1,6-2 2,1-2,5 2,6-3 3,1-3,5 3,6-4 4,1-4,5 4,6-5 5,1-5,5 5,6-6 6,1-6,5 6,6-7 Anzahl (n) 11 25 12 16 7 9 3 7 1 2 0 1 1 2 Der kleinste Tumor unserer Auswertungen hatte eine Größe von 0,2 cm, die größten Tumorentnahmen waren bis zu 7 cm groß. Die durchschnittliche Größe der IPs belief sich auf 2,06 cm. Ergebnisse 29 3.10. Beziehung zwischen der Tumorgröße und maligner Entartung In 8 Fällen unseres Patientenguts entwickelte sich eine Malignisierung auf dem Boden des invertierten Papilloms, dabei konnte beobachtet werden, dass bei 4 der 16 invertierten Papillome, welche 1,6 bis 2 cm groß waren, eine Tendenz zur Malignisierung von 25,0% gesichert wurde, und zu 14,3% zeigten sich bösartige Entwicklungen in den 7 Tumoren der Größe 2,1 bis 2,5 cm (n=1). Bei den Tumorgrößen 3,1 bis 3,5 cm und 3,6 bis 4 cm (n=3; n=7) zeigten sich in jeweils einem Fall eine Malignisierung auf dem Boden des IP (33,3%; 14,3%). Bei der Hälfte (50%) der beiden 6,6 bis 7 cm großen Tumorgeschwülste wurden maligne Entwicklungen nachgewiesen (n=1). Somit konnte in unserem Patientenkollektiv kein eindeutiger Zusammenhang zwischen der Tumorgröße und eventuellen malignen Tendenzen sichergestellt werden. Detailliertere Angaben können Tabelle 8 entnommen werden. Tab. 8: Beziehung zwischen Tumorgröße und Malignisierung Größe (cm) 0-0,5 0,6-1 1,1-1,5 1,6-2 2,1-2,5 2,6-3 3,1-3,5 3,6-4 4,1-4,5 4,6-5 5,1-5,5 5,6-6 6,1-6,5 6,6-7 des IP Anzahl (n) Anzahl der Malignisierungen (n) Häufigkeit (%) 11 25 12 16 7 9 3 7 1 2 0 1 1 2 0 0 0 4 1 0 1 1 0 0 0 0 0 1 0 0 0 25,0 14,3 0 33,3 14,3 0 0 0 0 0 50 Ergebnisse 30 Anzahl der einzelnen Tumorgrößen 25 25 20 Anzahl (n) 15 16 11 12 10 5 9 7 3 1 2 0 1 1 2 0-0, 5 0,61, 0 1,11, 5 1,62, 0 2,12, 5 2,63, 0 3,13, 5 3,64, 0 4,14, 5 4,65, 0 5,15, 5 5,66, 0 6,16, 5 6,67, 0 0 7 Größe (cm) Abb. 8: Anzahl der einzelnen Tumorgrößen Ergebnisse 31 3.11. Histologische Auswertungen 3.11.1. Wachstumsformen In unsere Auswertungen gelangten ausschließlich Patienten mit histologisch gesicherten invertierten Papillomen (n=77; 100%). Zum Teil zeigten sich gelegentlich jedoch histologisch invertiert zuzuordnende Papillome mit Anteilen von exophytischem Wachstum. In unserem Patientenkollektiv war dies fünfmal der Fall (6,5%), bei keinem der untersuchten Fälle stand ein derartiges Wachstum jedoch im Vordergrund. Abb. 9: Histologisches Bild des invertierten Papilloms (H&E, x40) Ergebnisse Abb. 10: Histologisches Bild des invertierten Papilloms (H&E, x100) 32 Ergebnisse 33 3.11.2. Malignisierungstendenzen Histologisch wurden jeweils 7 Fälle von Plattenepithelmetaplasien und -dysplasien gesichert (9,1%). 8 Fälle von Malignisierung in einem IP wurden gefunden (11,7%), wobei es sich fünfmal um ein Primärpapillom handelte und sich dreimal ein metachrones Wachstum darstellte. Hierbei fand man in zwei Fällen ein Karzinom im ersten Papillomrezidiv, und einmal handelte es sich bereits um das 5. Rezidiv. Das Tumor-Grading verteilte sich in G3 (n=4), G2 (n=3) und G1 (n=1). Darunter konnte ein Fall unseres Patientenguts zur Auswertung kommen, bei dem erst ein minimal verhornendes Plattenepithelkarzinom diagnostiziert wurde und sich später als Zufallsbefund histologisch zusätzlich ein invertiertes Papillom auf dem Boden dieses Karzinoms sichern ließ. Von diesen 8 onkozytären Entwicklungen handelte es sich viermal um ein gering differenziertes Karzinom (50,0%), dreimal war das Karzinom mäßig (37,5%) und einmal stark differenziert (12,5%). Histologische Differenzierung der malignen Fälle 13% gering differenziert 49% 38% mäßig differenziert stark diferenziert Abb. 11: Histologische Differenzierung der Plattenepithelkarzinome (PEC) auf dem Boden invertierter Papillome Ergebnisse 34 Gemäß der derzeitigen TNM-Klassifikation maligner Tumoren der UICC (6. Auflage, 1999) [157] wurden 4 Plattenepithelkarzinome dem Stadium pT1 N0 M0 zugeordnet und ein PEC dem Stadium pT2 pN0 M0. In 3 Fällen fand man aufgrund weiter Tumorausdehnung Destruktionen von angrenzenden Knochenanteilen, weshalb man diese 3 Karzinome in das Stadium pT4a N0 M0 einteilte, darunter zweimal pN0. Abbildung 12 und 13 zeigen ein Karzinom auf dem Boden eines invertierten Papilloms sowie die Übergangszone einer Plattenepithelmetaplasie zur malignen Transformation. Tab. 9: Patienten mit maligner Transformation des invertierten Papilloms und deren Krankheitsverläufe Nr. Geschlecht Primär-OP Symptome Nachresektion Lokalisation UICC Stadium 1 m Laterale Rhinotomie Laterale Rhinotomie T4aN0M0 m NAB, Epistaxis NAB NHH 2 SB T1N0M0 21 3 w Laterale Rhinotomie Ethmoidektomie, Conchotomie, KHFensterung KH-Endoskopie, Ethmoidektomie, Neck Dissection Stat. Dauer (Tagen) 6 NAB, Epistaxis KH T4aN0M0 11 4* m T1N0M0 23 m NAB, Epistaxis NAB SB 5 Laterale Rhinotomie Laser NHH T1N0M0 18 6 w NAB, Laterale Rhinorrhoe KH T2N0M0 22 7 w 8 m Caldwell-Luc, Neck Dissection, Hemimaxillektomie, Orbitarevision Ethmoidektomie, Laterale Rhinotomie, Orbitarevision, Neck Dissection Endoskopische OP der SH, SB, KH Caldwell-Luc, Orbitarevision, Hemimaxillektomie Laterale Rhinotomie Laterale Rhinotomie Keine NAB, Rhinorrhoe, Cephalgie, Epistaxis Keine SB T4aN0M0 6 NAB Caldwell-Luc, Neck Dissection, Midfacial Degloving KH, SB, SH T1N0M0 5 * Patient zu Nachuntersuchungen nicht erschienen. Der Patient ist 2 Jahre postoperativ verstorben. Ergebnisse 35 Abb. 12: Histologisches Bild des Karzinoms auf dem Boden eines invertierten Papilloms (H&E, x4) Abb. 13: Histologisches Bild des Karzinoms auf dem Boden eines invertierten Papilloms (H&E, x20) Ergebnisse 36 3.12. Potentielle Risikofaktoren für die Entstehung des invertierten Papilloms Nikotinabusus wurde anamnestisch bei 46 Patienten (59,7%), davon 6 Frauen und 40 Männer festgestellt. Dabei rauchten die meisten Betroffenen schon mehr als 10 Jahre, vereinzelt sogar schon seit über 50 Jahren, 3 der Patienten hatten zwar das Rauchen aufgegeben, aber bis vor ca. 10 Jahren noch regelmäßig geraucht. 24 Fälle von regelmäßigem Alkoholkonsum (31,2%) wurden festgestellt, wobei es sich in den meisten Fällen um gelegentlichen Alkoholkonsum handelte. In 3 Fällen dagegen war ein bereits seit Jahren bestehender starker Alkoholabusus bekannt. 3 Patienten waren aus beruflichen Gründen ständigem Holzstaub ausgesetzt (3,9%), und ein Weiterer berichtete über häufige Reizgasexposition (1,3%). Ein Patient (1,3%) gab zu, sich bis vor 2 Jahren regelmäßig nasal Kokain zugeführt zu haben. 16 Patienten gaben an, Allergiker zu sein (20,8%), darunter 4 Frauen und 12 Männer. Die große Spannbreite an Allergenen erstreckte sich von Pollen über Milben und Haustieren. Tabelle 10 und Abbildung 14 bieten eine genaue Übersicht über Risiken und Allergien. Anzahl der Patienten mit Risikofaktoren 46 Nikotin 24 Alkohol 16 Allergie 3 Holzstaub Reizgas 1 Kokain 1 0 10 20 30 Anzahl (n) Abb. 14: Anzahl der Patienten mit Risikofaktoren 40 50 Ergebnisse 37 Tab. 10: Häufige Formen von Allergien Allergien Anzahl (n) Penicillin 4 Milben 4 Haustiere 2 Heuschnupfen 3 Nickel 2 Kobalt 1 Duftstoffe 1 Von den 46 Rauchern entwickelte sich in nur 4 Fällen ein Karzinom auf dem Boden des IP (8,7%), bei den 24 Patienten mit gelegentlichem C2-Konsum konnte viermal (16,7%) eine maligne Entwicklung der Epithelgeschwülste festgestellt werden. Von den 3 Personen, welche ständig Holzstaub ausgesetzt waren, litt ein Patient unter Malignisierung des Tumors (33,3%). Weder nach häufiger Reizgasexposition, nach jahrelangem Zuführen von Kokain, noch bei Allergikern konnte in unserem Patientengut eine Tendenz zur Malignisierung des Tumors identifiziert werden, was natürlich aber wegen der geringen Zahl Beteiligter nicht zwangsläufig als gesichert aussagefähig betrachtet werden muss. Ergebnisse 38 3.13. Präoperative Maßnahmen 3.13.1. Präoperativ verschriebene Medikation Bei einigen Patienten (n=6; 7,8%) wurde von den Ärzten unseres Hauses zunächst eine präoperative Medikation verschrieben, vor allem um den Patienten mit großem Leidensdruck die Beschwerden bis zur Operation zu lindern oder in Fällen, bei denen das IP zunächst differentialdiagnostisch mit einem Polyp verwechselt wurde. In Einzelfällen erhielten die Patienten die Medikamente zuvor von ihrem niedergelassenen HNO-Arzt. So verschrieb man in 6 Fällen (7,8%) Kortisonpräparate, welche entweder nasal inhalativ anzuwenden waren (Nasonex ® ; n=3, Flutide nasal ® ; n=1), oder in Tablettenform ® (Urbason ; n=2) verabreicht wurden. Fünfmal wurden Antibiotika verschrieben (6,5%), darunter in 2 Fällen Penicilline (Amoxypen ®), einmal ein Präparat der Wirkstoffgruppe der Tetracycline (Doxycyclin ®) und zweimal aufgrund einer bekannten Penicillinallergie ein Makrolid (Sobelin ®). Schmerzmittel bei Bedarf erhielten im präoperativen Stadium 6 Personen (7,8%), fünfmal kam der Wirkstoff Diclofenac (Voltaren ® ) und einmal Metamizol (Novalgin ® ) zur Anwendung. 3.13.2. Präoperative Diagnostik In unserem Hause ist es üblich, von jedem Patienten präoperativ ein Röntgenbild, bzw. eine Computertomographie anfertigen zu lassen, um die genaue Tumorausdehnung und eventuelle Infiltrationen in knöcherne Strukturen besser zu erfassen und diese bei der individuellen Operationsplanung berücksichtigen zu können. Ebenso werden alle Patienten mit Nasenatmungsbehinderung einer Rhinomanometrie unterzogen, um einen Überblick über die Atemstromverhältnisse zu bekommen. Bei bereits präoperativem Verdacht auf ein malignes Geschehen wird meist zusätzlich eine Magnetresonanztomographie der NNH angefertigt, wie dies bei zwei Patienten der Fall war. Detailliertere Angaben werden in Tabelle 11 gemacht. Ergebnisse 39 Tab. 11: Präoperative Diagnostiken und deren Häufigkeiten Diagnostik Gesamt Häufigkeit (%) Röntgen NNH bzw. In jedem Fall Computertomographie Rhinomanometrie Olfaktorische Tests Gustatorische Tests 9 11,7 MRT 2 2,6 Sonographie 4 5,2 Allergietest 4 5,2 Tonaudio 8 10,4 Kardiologisches Konsil Zahnärztliches Konsil Augenkonsil Neurokonsil 3 3,9 3 11 1 3,9 14,3 1,3 In unseren Auswertungen behielt die Computertomographie in allen Fällen Recht, was die Klassifikation nach Krouse anging. So konnte es zuverlässig vorhersagen, welches Ausbreitungsstadium des Tumors zu erwarten war. Wenn die CT-Auswertungen beispielsweise Stadium T3 vermuten ließen, konnte dies durch weitere Untersuchungen, wie zum Beispiel Endoskopie oder Spiegeldiagnostiken oder später intraoperativ bestätigt werden. Das Computertomogramm machte jedes Mal zuverlässige Aussagen über Weichteilverschattungen, Knochenarrosionen und extranasalen Infiltrationen, wie zum Beispiel dem Orbitaboden sowie möglichen Sinusitiden, welche später histologisch gesichert werden konnten. Von 21 Polyposis-Leiden konnten 19 (90,5%) bereits über das CT diagnostiziert werden. Auch Röntgenaufnahmen konnten recht aussagekräftige, wenn auch nicht so eindeutige Unterstützungen bei der Diagnosefindung bieten, jedoch wurde durch das Röntgenbild in zwei Fällen, wie sich später intraoperativ feststellte, eine Epithelgeschwulst in den Zellen des Siebbeinsystems übersehen. Ergebnisse 40 Abb. 15: Axiales und coronares Computertomogramm des Invertierten Papilloms in der rechten Kieferhöhle und dem vorderen rechten Siebbein. Ergebnisse 41 3.14. Frühere OPs im Hals-Nasen-Ohren-Bereich Unter unserem Patientenkollektiv befanden sich 42 Personen, welche bereits ein- oder mehrmals im Hals-Nasen-Ohrenbereich voroperiert wurden. Die häufigsten Voroperationen waren frühere Papillomentfernungen, denen sich 15 Patienten, davon 9 alio loco Operierte, zum Teil mehrfach unterziehen lassen mussten. Insgesamt sind aus den ausgewerteten Krankenblättern 22 frühere Papillomresektionen ersichtlich. Zwanzigmal wurde bei unseren 77 Patienten eine Polypektomie durchgeführt (26,0%), und bei 6 Personen wurde eine Tonsillektomie durchgeführt (7,8%), gefolgt von ebenfalls 6 früheren Sinus-maxillaris-Operationen (7,8%), 4 Operationen am Sinus ethmoidalis (5,2%) und einer Operation am Sinus frontalis (1,3%) wegen chronisch rezidivierenden Sinusitiden. Viermal (5,2%) wurde eine Septumplastik aufgrund von Nasenbeinfrakturen vollzogen, und 3 Operationen wurden wegen rezidivierenden schweren Fällen von Epistaxis durchgeführt (3,9%). Zweimal (2,6%) kam die Conchotomie und einmal die Laryngektomie sowie die Panendoskopie und die Resektion eines Stimmlippenknötchens zum Einsatz. Ergebnisse 42 Frühere OPs im HNO-Bereich 22 20 Papillomresektion Polypektomie OP wegen chron. Sinusitiden Tonsillektomie Septumplastik OP wegen Epistaxis Conchektomie Panendoskopie Stimmlippenknötchenentfernung Laryngektomie 11 6 4 3 2 2 1 1 0 5 10 15 20 25 Anzahl (n) Abb. 16: Frühere Operationen im HNO-Bereich Da sich manche Patienten mehrerer, zum Teil verschiedener Operationen unterziehen lassen mussten, übersteigt die Anzahl der früher durchgeführten Operationen die Zahl der Personen mit Voroperationen insgesamt. Ergebnisse 43 3.15. Operationsverfahren 3.15.1. Techniken Das operative Management des invertierten Papilloms besteht aus konservativer oder radikaler Resektion. Die konservative Handhabung umfasst Techniken wie zum Beispiel die endoskopische Exzision, die Kieferhöhlenoperation nach Caldwell-Luc mit oder ohne externe Ethmoidektomie oder lokale Exzisionen mit ausreichendem Sicherheitsabstand zu den Tumorgrenzen. Die radikaleren Operationsmethoden beinhalten Verfahren wie die in den letzten Dekaden bevorzugt verwendete laterale Rhinotomie, zum Teil kombiniert mit der medialen Maxillektomie oder auch Conchotomien. Bei histologischem Nachweis einer malignen Entartung oder hochgradiger Epitheldysplasien im IP führten wir eine onkochirurgische Revisionsoperation durch. Kleinere maligne Tumoren (n=2) konnten auch endonasal mikroskopisch/endoskopisch in sano reseziert werden. 3.15.2. Anästhesie Fast alle unsere Patienten wurden unter Intubationsnarkose (ITN) operiert (n=68; 88,3%). Nur in 9 Fällen wurde das invertierte Papillom unter Lokalanästhesie (LA) reseziert (11,7%), hierbei wurde jedes Mal ein endonasaler Zugangsweg gewählt, das IP befand sich dabei ausschließlich in der Nasenhaupthöhle, beziehungsweise war in 5 Fällen die Schleimhaut des Nasenseptums betroffen, dreimal das Vestibulum nasi und einmal wuchs das IP ausgehend von der Concha inferior nasi. Nach Anwendung der Lokalanästhesie konnten 3 der 8 Patienten (37,5%) noch am selben Tag nach Hause entlassen werden. Bei einer Person unseres Patientenkollektivs wurde lediglich eine ambulante Probeexzision einer unklaren Tumorentität in Lokalanästhesie durchgeführt und hierbei histologisch ein initiales invertiertes Papillom gesichert. Da man hier von einer R0-Resektion ausgehen Ergebnisse 44 konnte, und auch mehrere Wiedervorstellungen in der Ambulanz keinen Anhalt für ein Fortbestehen des Tumors gaben, wurde der Patient nicht operiert und als gesund gehandelt. 3.15.3. Operationszugang Die Erstoperation fand in 32 Fällen (42,1%) auf rein endoskopischem Wege statt. 23 Mal (30,3%) wurde über einen externen Zugang operiert (zum Beispiel laterale Rhinotomie, Operation nach Caldwell-Luc). Kombiniert wurden die Zugänge in 21 Operationen angewendet (27,6%), vor allem dann, wenn multiple Lokalisationen vom Tumorwachstum betroffen waren. Der Fall, bei dem eine ambulante Probeexzision bereits eine Tumorfreiheit brachte, wird hier nicht in die Auswertungen miteinbezogen. Bei genauerer Betrachtung der Tumorlokalisation entsprechend des gewählten Zugangswegs findet man in der Gruppe der primär endoskopisch Operierten v.a. einen Befall der Nasenhaupthöhle (22 von 32; 68,8%). Der transfaziale Weg wurde vor allem bei einer Beteiligung des Sinus maxillaris (3 von 5; 60,0%), aber auch gelegentlich des Sinus ethmoidalis oder Sinus sphenoidalis gewählt (je 1 von 5; 20,0%). Da der Tumor sich zum Teil multilokulär ausbreitete, sind auch hier Mehrfachnennungen möglich. Operationszugänge und deren Häufigkeit Kombinierter Zugang 28% Externer Zugang 30% Abb. 17: Operationszugänge und deren Häufigkeiten Endonasaler Zugang 42% Ergebnisse 45 Tab. 12: Vom invertierten Papillom befallene Regionen entsprechend dem gewählten Zugangsweg (Mehrfachnennungen möglich) Betroffener Bezirk Sinus ethmoidalis Nasenhaupthöhle Sinus maxillaris Sinus frontalis Septum Sinus sphenoidalis Endoskopisch (n=32) n=13; 40,6% n=22; 68,8% n=11; 34,4% n=2; 6,3% n=9; 28,1% n=4; 12,5% Extern (n=23) n=15; 65,2% n=7; 30,4% n=15; 65,2% n=3; 13,0% n=6; 26,1% n=5; 21,7% Kombiniert (n=21) n=12; 57,1% n=10; 47,6% n=7: 33,3% n=3; 14,3% n=4; 19,1% n=1; 4,8% 3.15.4. Postoperativer Beobachtungszeitraum nach den einzelnen Operationszugängen In unserem Patientenkollektiv wurden 32 Personen über eine endogene Operationsmethode IP-exzidiert. In dieser Gruppe war die längste postoperative Beobachtungszeit bis zu 13 Jahren, der kleinste Zeitrahmen belief sich auf einen Monat. In 4 Fällen begaben sich die Patienten direkt in die Obhut ihres niedergelassenen HNO-Arztes, bzw. erschienen nicht zum verabredeten ambulanten Termin (12,5%), diese werden somit in der folgenden Auswertung nicht berücksichtigt. 17 Personen (60,7%) wurden bis zu einem Jahr post-OP zur ambulanten Wiedervorstellung bestellt, bis sie als gesund dokumentiert werden konnten. Bei 3 Patienten dauerte die postoperative Beobachtungsphase bis zu 2 Jahren (10,7%), und 4 weitere Personen wurden bis zu 3 Jahren post-OP in der Ambulanz kontrolluntersucht (14,3%). In zwei Fällen wurde eine postoperative Beobachtungszeit von bis zu 4 Jahren dokumentiert (7,1%). Wegen schwerem Krankheitsverlauf mit onkozytärem Einschlag und im späteren Verlauf immer wieder auftretenden Beschwerden wie Nasenatmungsbehinderung, dauerte der postoperative Beobachtungszeitraum bei 2 Personen (7,1%) mehr als 4 Jahre, wobei hier einmal 86 Monate und im anderen Fall 156 Monate dokumentiert wurden. Vier Personen erschienen trotz mehrfacher telefonischer sowie brieflicher Aufforderung nicht zum vereinbarten Ambulanztermin, und eine Patientin befand sich zum Zeitpunkt der Datenerhebung noch in stationärer Obhut, weshalb der spätere postoperative Beobachtungszeitraum nicht mehr in unsere Auswertungen hineinlief. Ergebnisse 46 Im Patientenkollektiv der von extern Operierten erschien eine Person nicht zum vereinbarten Wiedervorstellungstermin in unserer Ambulanz, ansonsten dauerte bei dem Rest der Gruppe das kürzeste klinische Follow-up einen Monat, das längste 72 Monate. Vier Personen konnten nicht in die Auswertungen des späteren Beobachtungszeitrahmens mit aufgenommen werden, da sie noch stationär in unserer Klinik lagen. Bei 5 Personen wurde eine postoperative Beobachtungszeit von bis zu einem Jahr datiert (27,8%). 9 Patienten (50,0%) wurden bis zu 2 Jahren nach der Operation in unsere Ambulanz einbestellt, bis sie als geheilt datiert werden konnten. Im zeitlichen Rahmen von bis zu 4 Jahren bewegten sich 2 Fälle (11,1%), und in 2 weiteren Krankengeschichten belief sich der Post-OP-Zeitraum auf bis zu 6 Jahren (11,1%). In der Gruppe der Patienten, welche das IP über kombinierte operative Zugänge exzidiert bekamen, dauerte das klinische Follow-up in 47,6% bis zu einem Jahr (n=10) und in 28,6% bis zu 2 Jahren (n=6). Bei je 2 Patienten (9,5%) belief sich die postoperative Beobachtungsphase auf bis zu 3, beziehungsweise auf bis zu 4 Jahren. Eine Person wurde aufgrund eines schweren Verlaufs bis zu 7 Jahren später ambulant kontrolluntersucht (4,8%). In dieser Gruppe wurde der kürzeste postoperative Beobachtungszeitrahmen mit einen Monat, der längste mit 84 Monaten dokumentiert. Ergebnisse 47 3.16. Häufigkeit der einzelner Operationsmethoden In unserem Patientengut ist die laterale Rhinotomie mit eventueller Resektion der lateralen Nasenwand und Entfernung der Schleimhaut des Sinus maxillaris sowie der Ausräumung des Sinus ethmoidalis, die meist angewandte Operationsmethode. Insgesamt wurde die laterale Rhinotomie in 29 Fällen durchgeführt (37,7%), hierbei diente sie in 19 Fällen als Ersttherapie (19 von 29; 65,5%). Viermal entschieden sich die Operateure im Rahmen einer Nachresektion eines zuvor auf endoskopischem Wege nicht komplett entfernten Papilloms, für die laterale Rhinotomie (4 von 29; 13,8%). Von den 19 Erstoperationen der lateralen Rhinotomie fanden 10 OPs vor 1997 statt, was einen Anteil von 52,6% ausmacht, die restlichen 9 Operationen (47,4%) dieser Art kamen im Zeitraum von 1998 bis heute zur Anwendung, man sieht also eine deutlich abnehmende Tendenz. Bei 4 Patienten wurde die laterale Rhinotomie angewandt, um ein Rezidiv zu resezieren. Bei 6 Operationen dieser Art wurde zusätzlich eine Tränenwegsschienung durchgeführt aufgrund der Nähe des Operationsgebiets zum Ductus nasolacrimalis. Die laterale Rhinotomie ist gerade heute vor allem dann die Methode der ersten Wahl, wenn aufgrund der Tumorlokalisation und -ausbreitung eine besonders radikale Resektion notwendig ist, beziehungsweise ganze Knochenstrukturen, wie zum Beispiel das Os maxillaris oder Teile des Sinus ethmoidalis-Zellsystems entfernt werden müssen. Tab. 13: Anwendung der lateralen Rhinotomie Anwendung insgesamt Erstoperationen gesamt Erstoperationen vor 1997 Erstoperationen ab 1998 Frühere Papillomresektionen, in Universitätsklinik durchgeführt Als Nachresektion Als Rezidiv-OP Anzahl (n) 29 19 10 9 2 4 4 Ergebnisse 48 Abb. 18: Laterale Rhinotomie aus [18] Noch häufiger als die laterale Rhinotomie wurden bei unseren Patienten Operationen am Sinus ethmoidalis durchgeführt, welche insgesamt 30 Mal (39,0%) zur Anwendung kamen. Zehnmal (10 von 30; 33,3%) wurde sie im Rahmen einer lateralen Rhinotomie von extern vollzogen und bei 20 Operationen endonasal angewandt (20 von 30; 66,7%). Bei elf Patienten wurde eine Ethmoidektomie durchgeführt, was an den durchgeführten Siebbeinoperationen einen Anteil von 36,7% darstellt, unter dem Patientenkollektiv von 77 Personen entspricht dies einer Häufigkeit von 14,3%. Tab. 14: Anwendung von Operationen am Siebbeinzellsystem Anwendung Primäroperationen Von extern operiert Endoskopisch Frühere OPs, in Universitätsklinik durchgeführt Als Nachresektionen Als Rezidiv-OP Ethmoidektomie Anzahl (n) 30 10 20 3 3 5 11 gesamten Ergebnisse 49 17 Mal musste in unserem Patientengut eine Conchotomie im Rahmen der besagten Epithelgeschwulst primär durchgeführt werden (22,1%). Die Muscheln wurden bei 13 Patienten endonasal entfernt und bei 4 Personen von extern, hierbei in je 2 Fällen mittels lateraler Rhinotomie oder im Rahmen einer Caldwell-Luc Operation, wenn die intranasale Tumorausbreitung als sehr groß bewertet wurde und man auf diese Weise eine komplette Exzision sicherstellen wollte. Tab. 15: Anwendung der Conchotomie Anwendung Gesamt Endonasal Extern Anzahl (n) 17 13 4 In unserem Krankengut kam in 10 Fällen (13,1%) eine submuköse Septumresektion mit anschließender plastischer Rekonstruktion zur Anwendung, davon wurde die Operationsmethode in 4 Fällen alleine angewandt (4 von 10; 40,0%), in 6 weiteren Fällen in Kombination mit Radikaloperationen am Sinus ethmoidalis, sphenoidalis, maxillaris und der Nasenhaupthöhle (6 von 10; 60,0%). Bei einem Patienten befand sich das Papillom zwar im mittleren Nasengang, aufgrund dauerhafter Nasenatmungsbehinderung wurde bei dem operativen Zugriff zusätzlich noch eine Septumdeviation behoben. Tab. 16: Durchführung von Operationen am Septum nasi Anwendung Submuköse Septumresektionen, primär Als Primäroperation Als alleinige Operation angewandt In Kombination mit Radikaloperationen Als Nachresektion Behebung einer Septumdeviation Anzahl (n) 10 9 4 6 1 1 Aufgrund des IP-Wachstums mussten 19 Personen am Sinus sphenoidalis operiert werden (19 von 77; 24,7%), hierbei 14 Mal im Rahmen einer Primäroperation und bei 5 Patienten zur Resektion eines Tumorrezidivs. Ergebnisse 50 Fast ausschließlich führte man diese Operationen in Kombination mit endonasalen Ethmoidektomie, der Infundibulotomie oder der Nasenhaupthöhle durch (n=17; 89,5%). Bei 4 Patienten wählten unsere Operateure einen externen Zugangsweg, zum Beispiel in Verbindung mit der Caldwell-Luc-Operation. In einem Fall wurde diese Operation im Rahmen eines Midfacial Deglovings durchgeführt (1 von 19; 5,3%). Tab. 17: Anwendung von Operationen am Sinus sphenoidalis Anwendung Gesamt Als Primäroperation Als Rezidivoperation Endonasal durchgeführt Mit externem Zugang Midfacial Degloving Anzahl (n) Anteil (%) 19 24,5 14 73,7 5 26,3 14 73,7 4 21,1 1 5,3 Bei 5 unserer Patienten wurde die Kieferhöhlenfensterung durchgeführt (6,5%), wobei diese jedes Mal mikrochirurgisch und auf rein endoskopischem Weg durchgeführt wurde, dabei wurde viermal unterstützend mit einem Navigationssystem gearbeitet (4 von 5). Seit dem Jahre 2002 wurde in unserem Hause intraoperativ das Navigationssystem zu Hilfe genommen, wenn das IP an schlecht erreichbaren Stellen lokalisiert war. Insgesamt wurde es zwischen 2002 und 2004 14 Mal verwendet (18,2%), vor allem wenn sich das IP im Sinus sphenoidalis und ethmoidalis befand (je n=6; 42,9%). Ansonsten bediente man sich dieser Methode aber Kieferhöhlenoperation (n=4). auch im Rahmen einer Stirnhöhlen- (n=2) und Ergebnisse 51 Tab. 18: Anwendungen des Navigationsystems Anwendung Anzahl Bei Primäroperation 10 Im Rahmen einer Rezidivoperation 4 Aufgrund des Sitzes des IP wurde bei 14 Personen eine Stirnhöhlenoperation durchgeführt. Diese erfolgte in 10 Fällen auf endoskopischem Wege, davon zweimal mit Unterstützung des Navigationssystems und viermal über einen externen Zugang, wobei die Schnittführung in der Hälfte der Fälle oberhalb der Augenbraue lag, zur anderen Hälfte operierte man über eine bitemporale koronare Inzision (sogenannter „Unterbergerschnitt“). In 7 Fällen wurde aufgrund IP-Lokalisationen im Sinus ethmoidalis oder Sinus maxillaris die Infundibulotomie angewandt (9,1%), welche stets rein endonasal durchgeführt wurde. Sie wurde 6 Mal als Primäroperation durchgeführt und einmal im Sinne einer Rezidivexzision. Weitere 13 Male (16,9%) führte man in unserem Patientenkollektiv eine Caldwell-Luc Operation durch. In 8 Fällen wurde sie als Erstoperation angewandt, bei 2 Patienten in Form einer Nachresektion, wenn das IP zuvor nicht vollständig reseziert werden konnte. Bei 3 Personen wurde die Caldwell-Luc Operation angewandt, um ein Tumorrezidiv zu entfernen. Ergebnisse 52 Abb. 19: Technik nach Caldwell-Luc aus [169] Sechsmal wurde das IP laserchirurgisch reseziert (7,8%), vor allem dann, wenn die Lokalisation des IP sich auf das Vestibulum nasi oder auf obere Septumanteile beschränkte. Bei 4 Patienten wurde das IP in der Primäroperation laserchirurgisch entfernt, bei einer Person noch im Rahmen zweier Rezidivoperationen. Diese Methode wurde allerdings in unserem Patientenkollektiv nur in den Jahren 1994 bis 1997 durchgeführt, kommt heute allerdings nicht mehr zur Anwendung. Von der Technik des Midfacial Degloving machte man in 6 Fällen Gebrauch (7,8%). Hier befand sich das IP vor allem im Sinus maxillaris, ethmoidalis, aber auch im Sinus sphenoidalis. Hinzu kommen 2 Fälle, bei denen aufgrund eines Sitzes im Sinus frontalis, eine bitemporale koronare Inzision (der sogenannte „Unterbergerschnitt“) angewandt wurde. Ergebnisse 53 Abb. 20: Technik des Midfacial Deglovings aus [18] Viermal (5,2%) wurden infolge einer malignen Entwicklung sonographisch verdächtige Lymphknoten im Rahmen einer Neck Dissection exzidiert. Dreimal geschah dies direkt bei der Erstoperation und einmal bei einer Nachresektion. Bei histologischem Nachweis einer malignen Entartung oder hochgradiger Epitheldysplasien im IP führten wir eine onkochirurgische Revisionsoperation durch, welche meist in Form der lateralen Rhinotomie (n=4) oder der Technik nach Caldwell-Luc (n=3) durchgeführt wurde. Kleinere maligne Tumoren (n=2) konnten auch endonasal mikroskopisch/endoskopisch in sano reseziert werden. Ergebnisse 54 3.17. Nachresektionen Insgesamt mussten unsere Operateure bei 12 Patienten eine Nachresektion durchführen, ehe das invertierte Papillom histologisch eindeutig als in sano reseziert angesehen werden konnte. Da bei einigen Patienten mehrere Techniken innerhalb einer Operationssitzung zur Anwendung kamen, sind hier Mehrfachnennungen aufgeführt. Am häufigsten wurde zur Nachresektion die laterale Rhinotomie angewandt. Dies war bei 4 Personen der Fall. Je nach Lokalisation und Ausdehnung kamen in unserem Patientenkollektiv jeweils dreimal die Ethmoidektomie, der endoskopische Kieferhöhlen-Eingriff sowie die Laserexzision des Tumors zur Anwendung. Je zweimal kamen die Technik nach CaldwellLuc und die Tumorresektion mittels endoskopischer Nasenhaupthöhlenoperation zur Anwendung. In einem Fall führte man eine Septumteilresektion im Sinne einer Nachresektion durch. Unsere Operateure nahmen einmal bei Sitz des Tumors im Sinus sphenoidalis die Neuronavigation zur Hilfe. Detaillierte Angaben sind Tabelle 19 zu entnehmen. Tab. 19: Nachresektionen Art der Nachresektion Laterale Rhinotomie Ethmoidektomie Laserexzision Endoskopische Kieferhöhlen-Operation Caldwell-Luc Endoskopische Nasenhaupthöhlen-Operation Septumteilresektion Anwendung der Neuronavigation Anzahl (n) 4 3 3 3 2 2 1 1 Bei den meisten Patienten reichte eine Nachresektion aus, um den Tumor vollständig zu entfernen (n=9), bei 3 Personen musste man jedoch zweimal erneut operieren, ehe histologisch eine R0-Resektion gesichert werden konnte. Ergebnisse 55 In 6 Fällen wurde aufgrund geringer Tumorausdehnung nur eine einzige Operationstechnik durchgeführt. Bei 3 Patienten wurden 2 Methoden auf einmal durchgeführt, und bei 2 Personen wählte man 3 Techniken in Kombination. Als einzige Technik wurden vor allem die laterale Rhinotomie, die Laserresektion, die Operation nach Caldwell-Luc sowie die Keilbeinhöhlen-Operation angewandt. Kombiniert wurden hauptsächlich Eingriffe des Sinus ethmoidalis und Sinus maxillaris. In unserem Patientenkollektiv wurden Nachresektionen neunmal nach endoskopischen Eingriffen und in 2 Fällen nach Operationen mit externem Zugang benötigt. Sehr oft musste nach endoskopischen Sinus ethmoidalis- und Sinus maxillaris-Operationen nachreseziert werden (je n=4). Jeweils zweimal wurde wegen Residualtumor erneut operiert nach lateraler Rhinotomie, Conchotomie, Infundibulotomie und Operationen am Sinus sphenoidalis. In je einem Fall führte man eine Nachresektion nach Laserresektionen und Septumteilresektionen sowie nach endoskopischen Eingriffen des Sinus frontalis durch. Tab. 20: Anzahl der Nachresektionen nach bestimmten Operationstechniken Operationsmethode, nach der die Durchführung einer Nachresektion notwendig wurde Endoskopische Siebbeinoperation Endoskopische Kieferhöhlenoperation Conchotomie Laterale Rhinotomie Infundibulotomie Sphenoidektomie Septumteilresektion Laserresektion Stirnhöhlenoperation Endoskopische Eingriffe Operationen mit Zugang von extern Anzahl (n) 4 4 2 2 2 2 1 1 1 Häufigkeit, bezogen auf die Gesamtzahl der jeweiligen Technik (%) 9,8 28,6 11,8 6,9 28,6 10,5 10,0 10,0 7,1 9 3 28,1 13,0 Ergebnisse 56 3.18. Postoperative Beschwerdesymptomatik und Komplikationen 3.18.1. Intra- und postoperative Komplikationen Die intraoperative Hauptkomplikation war ein Defekt der Dura aufgrund von Tumorläsionen der vorderen Schädelbasis (n=4). Hierbei war das IP in 3 Fällen im Sinus sphenoidalis und einmal im hinteren Anteil des Sinus ethmoidalis lokalisiert. Der Defekt wurde intraoperativ über ein Titan-Mesh behoben. Zweimal wurde eine Stirnhöhlenmukozele nach Pansinektomie beobachtet (2,6%). Eine weitere intraoperative Komplikation (1,3%) erlitt ein 35-jähriger Mann mit großem IP des gesamten Sinus maxillaris. Hier entwickelte sich eine Kieferhöhlenfistel in den Mundvorhof mit Sekretübertritt, welche aber bei einer zweiten Operation erfolgreich gedeckt werden konnte. Der Betroffene erhielt im Anschluss an den stationären Aufenthalt eine Rehabilitation zugesprochen. 3.18.2. Postoperative Beschwerdesymptomatik Insgesamt entwickelten 31 unserer Patienten postoperative Beschwerden (40,3%), davon 3 Frauen (23,1% aller Frauen) und 28 Männer (43,8% aller Männer). 22 der 77 Betroffenen (28,6%) litten unter postoperativen Blutungen aus der Nase, jedoch konnten diese stets durch konservative Maßnahmen unter Kontrolle gebracht und nach kurzer Zeit gestillt werden. 12 Patienten (15,6%) hatten eine starke Borkenbildung, welche wiederum die Nasenatmung behinderte. In diesen Fällen wurden die Personen in kurzen Intervallen ambulant einbestellt und die Borken jeweils entfernt und die Nasenpflege intensiviert. Jeweils 2 Operierte (2,6%) klagten über starke Cephalgien, subjektiv übermäßige Schmerzen im Bereich der Naht, eitrigen Schnupfen und über eine sehr trockene Nasenschleimhaut. Nur ein Patient (1,3%) entwickelte eine Infraorbitalneuralgie und bei einer weiteren Person infizierte sich die Naht. Ergebnisse 57 Ein 86-jähriger multimorbider Patient erkrankte während des postoperativen Aufenthalts wegen ständigen Liegens an einer Thrombophlebitis. Eine Person erkrankte nach der Einnahme von Schmerzmittel an einer Voltareninduzierten Antrumgastritis. Postoperative Beschwerden 22 Blutung Borkenbildung Cephalgie Nahtschmerz Rhinorrhoe trockene Nase Mukozele Infraorbitalneuralgie Wundinfektion Thrombophlebitis Antrumgastritis 12 2 2 2 2 2 1 1 1 1 0 5 10 15 20 25 Anzahl (n) Abb. 21: Postoperative Beschwerden Fallbeispiel Exemplarisch wird ein Fall geschildert. Bei einer 36-jährigen Patientin haben wir aufgrund starker, vor allem auf der linken Seite empfundener Nasenatmungsbehinderung, welche seit ca. einem halben Jahr vorhanden war sowie rezidivierender Epistaxis und einem Druckschmerz über der linken Kieferhöhle in unserer Ambulanz probeexzidiert (7 mm großes Exzidat) und histologisch ein invertiertes Papillom des Sinus maxillaris und der Nasenhaupthöhle links gesichert. Die betroffenen Nasenschleimhäute zeigten Spuren einer chronischen Rhinitis mit offenbar reaktiver Plattenepithelmetaplasie. Außerdem stellten wir eine chronische Sinusitis maxillaris fest. Ergebnisse 58 Die Patientin wurde einige Tage später stationär aufgenommen und unter ITN endonasal und transmaxillär an Siebbein und Kieferhöhle operiert und erkranktes Gewebe unter Mitnahme eines ausreichenden Sicherheitsabstandes reseziert. Hierbei bestätigte die histologische Untersuchung der 1,5 bis 2,5 cm großen Gewebestücke erneut ein IP der Nasenhaupthöhle und des Sinus maxillaris, diesmal jedoch mit Übergang in ein mittelgradig differenziertes Plattenepithelkarzinom mit lokaler Knochendestruktion. 26 Tage später wurde die 36-Jährige nach Anfertigung einer Gaumenschutzplatte in der Mund- und Kieferchirurgie erneut zur Resektionskontrolle einer Operation unterzogen. Die Abbildungen 22-25 zeigen die präoperativen CT’s und MRT’s. Diesmal wendeten wir eine radikalere Operationstechnik in Form einer navigationsgestützten Hemimaxillektomie links (Abb. 25b) mit Neck dissection beidseits in ITN an, nachdem bei einer Halssonographie auf beiden Seiten je 2 kleine auffällige Lymphknoten der Größe 18 bis 21 mm entdeckt wurden. Der histopathologische Befund ergab ein gering differenziertes, gering verhornendes Plattenepithelkarzinom der linken Kieferhöhle. Der Tumor infiltrierte Teile des Processus pterygoideus medialis links sowie das Schleimhautdach und die Rückwand der linken Kieferhöhle (UICC-Tumorstadium pT4a pN0 cM0, G3). Da histopathologisch zum Orbitaboden der Verdacht auf eine R1-Resektion bestand führten wir noch eine Orbitabodenresektion und -rekonstruktion mit Hilfe eines Titan-Meshs links durch. Histopathologisch fanden sich dann keine weiteren Tumoranteile, so dass eine Resektion in sano (R0) erreicht wurde. Im Anschluss an die Operationen wurde bei der Patientin eine adjuvante Radiatio unter Einbeziehung des ehemaligen Orbitabodenbereichs links, des ehemaligen Gaumenbereichs sowie der Nasenhaupthöhle durchgeführt. Gleichzeitig erhielt sie eine entsprechende Schmerztherapie und für 8 Tage ein Antibiotikum (Amoxicillin, 3 × 1g; 1-1-1-0). Postoperativ entwickelte die Patientin eine Entzündung des Musculus pterygopalatinus, weshalb sie unter einer zunehmenden Kieferklemme mit maximaler Öffnung von nur 20 mm litt. Bei den ambulanten Kontrolluntersuchungen fiel sie zunehmend wegen schlechtem Ernährungs- und Allgemeinzustandes auf. Darüber hinaus stellten wir eine Rhinolalia aperta und einen Flüssigkeitsübertritt beim Essen über die Nase fest. Therapeutisch verordneten wir eine regelmäßige manuellen Munddehnung mittels eines Holzspatels („Tannenbaum“). Außerdem verordneten wir zusätzlich physiotherapeutische Anwendungen. Ergebnisse 59 Nach abgeschlossener adjuvanter Radiatio wurde der Patientin in der Mund- und Kieferchirurgie eine erneute Gaumenplatte angepaßt. Im weiteren Verlauf diagnostizierten wir leider eine metachrone kontralaterale temporale Kalottenmetastase. Derzeit wird bei der Patientin heimatnah eine systemische Chemotherapie durchgeführt. Abb. 22: Axiales Computertomogramm des Schädels: 36jährige Patientin mit einem Plattenepithelkarzinom des Sinus maxillaris links auf dem Boden eines IP mit Destruktion der medialen und lateralen Kieferhöhlenwand. Ergebnisse Abb. 23: Coronares MRT des Schädel der Patientin aus Abb. 22 Abb.24: Coronares MRT des Schädel der Patientin aus Abb. 22 60 Ergebnisse 61 Abb. 25a: Sagittales MRT des Schädel der Patientin aus Abb. 22 Abb. 25b: Navigiert kontrollierte Tumorresektion anhand des CT-3D-Datensatzes der Patientin aus Abb. 22 (Navigationssystem BrainLAB VectorVision 2 ®) Ergebnisse 62 3.19. Postoperativ verordnete Medikation Je nach postoperativem Zustand der Nase und der Nasennebenhöhlen wurden verschiedene Medikamente verordnet, um die Wundheilung des Operationsgebiets zu beschleunigen, bzw. zu unterstützen oder um eventuell auftretende postoperative Schmerzen zu minimieren. Besonders häufig wurde die Nase mit weicher Salbe versorgt, um einer Krusten- oder Borkenbildung vorzubeugen (n=27; 35,1%). In 20 Fällen wurde eine Medikationskombination mit dem Kortisonpräparat Urbason ® und dem Antibiotikum Doxycyclin® verordnet (26,0%). 20,8% der Patienten wurde postoperativ die Verwendung des Meerwassersprays Rhinomer® zugeraten (n=16) und 13 Patienten verwendeten sonstige abschwellende Nasensprays (16,9%). 4 Patienten wurden Amoxypen® (5,2%) und 7 Personen das Schmerzmittel Voltaren® verschrieben (9,1%). In je 2 Fällen erhielten die Patienten postoperativ die Präparate Nasonex® (ein cortisonhaltiges Nasenspray), Steurer-Nasensalbe® und zur Linderung eventueller Schmerzen Novalgin® (je 2,6%). Einmal wurde jeweils das Antibiotikum Sobelin®, Bactrin®, Bidocef® und eine Augensalbe verordnet (1,3%). Ergebnisse 63 Postoperativ verordnete Medikation 27 WNS 20 20 Urbason Handelsname Doxycyclin Rhinomer 16 13 abschwell.Sprays Diclofenac 7 4 Amoxypen Nasonex 2 2 2 Steurer Nasensalbe Novalgin 1 1 1 1 Bidocef Bactrin Sobelin Augensalbe 0 5 10 15 Anzahl (n) Abb. 26: Anzahl der postoperativ verordneten Medikamente 20 25 30 Ergebnisse 64 3.20. Aufenthaltsdauer Bei einem Patient konnte ein initiales invertiertes Papillom direkt bei der ambulanten Probeexzision des Tumorgewebes im Gesunden entfernt werden. In diesem Fall musste sich der Betroffene nur noch zur Histologiebesprechung in unserer Ambulanz einfinden und konnte nach 2 weiteren Kontrollterminen im Abstand von 4 und 6 Monaten als geheilt betrachtet werden. Zwei weitere Patienten verließen unsere Klinik nach nur einem Tag und nach ausreichender Aufklärung über mögliche Gefahren und später auftretenden Komplikationen auf eigene Verantwortung und begaben sich in die Hand ihres niedergelassenen Hals-Nasen-Ohren-Arztes. Der kürzeste stationäre Aufenthalt in unserer Klinik belief sich also auf einen Tag, der längste Aufenthalt hatte eine Dauer von 24 Tagen. Insgesamt konnte eine durchschnittliche stationäre Zeitspanne von 8,43 Tagen errechnet werden. Zum besseren Überblick dienen Tabelle 21 und Abbildung 27. Tab. 21: Stationäre Aufenthaltsdauer pro Person und deren Häufigkeiten Aufenthaltsdauer (Tage) 0-5 6-10 11-15 16-20 21-25 Frauen (n) 1 9 2 0 1 Männer (n) 17 29 8 7 2 Gesamt (n) Häufigkeit (%) 18 38 10 7 3 23,4 49,4 13,0 9,1 3,9 Ergebnisse 65 Aufenthaltsdauer und deren Häufigkeit 4 Dauer (d) 21,0 - 25,0 9 16,0 - 20,0 13 11,0 - 15,0 49 6,0 - 10,0 23 0,0 - 5,0 0 10 20 30 40 50 Häufigkeit (% ) Abb. 27: Aufenthaltsdauer und deren Häufigkeit Die durchschnittliche stationäre Aufenthaltsdauer der 9 Patienten, bei denen sich auf dem Boden des invertierten Papilloms ein Karzinom entwickelte, belief sich auf 14 Tage. 3.20.1. Durchschnittliche stationäre Aufenthaltsdauer nach einzelnen Operationstechniken Die längste durchschnittliche stationäre Aufenthaltsdauer mit 13,8 Tagen ermittelten wir nach der endonasalen Maxillektomie, gefolgt von durchschnittlich 11,4 Tagen nach der Infundibulotomie. Nach der Operation nach Caldwell-Luc bewegte sich die stationäre Zeitspanne bei 11,4 Tagen. Die Personen, welche mit der Technik des Midface Deglovings operiert wurden, verbrachten im Mittel 10,8 Tage stationär, und nach Ethmoidektomie war die mittlere stationäre Dauer 9,7 Tage. Nach der lateralen Rhinotomie wurden die Zeitspannen mit 9,3 Tagen datiert, ebenso wie nach Operationen am Sinus sphenoidalis, gefolgt von 8,6 Tage nach endoskopischem operativen Vorgehen am Sinus maxillaris. Ergebnisse 66 8,8 Tage befanden sich durchschnittlich die Personen, bei denen eine Tumorresektion mittels Laser durchgeführt wurde unter stationärer Beobachtung. Insgesamt belief sich die durchschnittliche stationäre Aufenthaltsdauer bei den Personen, welche durch kombinierten Zugang operiert wurden, auf 10,5 Tage. Bei den von extern Operierten ermittelten wir eine mittlere Zeitspanne von 9,1 Tagen. Am kürzesten befanden sich die endonasal Operierten in unserer Obhut. Sie mussten durchschnittlich 7,5 Tage in unserer Klinik verweilen. Genauere Angaben zeigt Abbildung 28. Durchschnittliche stationäre Aufenthaltsdauer nach den einzelnen Operationsmethoden 14 e to mi xillek a M le ie nasa endo lotom dibu n u f n I L uc we llCald -O P bein Sie b e tomi hino R e l ra Lat e P en-O höhl n i e Keilb mie h ot o Conc P en- O höhl St irn ng ste ru nfen e l h rhö Kiefe a ng r Zu g iert e n i b Ko m ang r Zug e n r e Ext gang er Zu l a s na Endo 11 11 10 9 9 9 8 7 11 9 8 0 5 10 15 Dauer in Tagen Abb. 28: Durchschnittliche Aufenthaltsdauer nach den einzelnen Operationstechniken und Zugangswege Ergebnisse 67 3.21. Postoperativer Beobachtungszeitraum Fünf Patienten (6,5%) wünschten weitere Kontrollen durch ihren niedergelassenen HalsNasen-Ohren-Arzt. Zwei Personen erschienen nach einem Wiedervorstellungstermin nicht zum vereinbarten ambulanten zweiten Termin. Wegen schlechtem Allgemeinzustand wurde 1991 und 1995 bei 3 Patienten mit gesichertem, aber nicht sicher in sano exzidiertem Plattenepithelkarzinom auf dem Boden eines IP auf eine erneute chirurgische Therapie verzichtet und eine Strahlentherapie (ca. 6000 rad Tumordosis) durchgeführt. Zusätzlich wurden in kurzen zeitlichen Abständen Nachsorgetermine in unserer Ambulanz durchgeführt und ein eventueller Größenrückgang des Karzinoms beurteilt. Spätere histologische Untersuchungen ergaben bei zwei Patienten völlige Tumorfreiheit. Ein Patient mit maligner Entartung des IP, welcher die Klinik auf eigene Verantwortung verlassen und die begonnene Strahlentherapie abgebrochen hatte, verstarb nach knapp 2 Jahren im Alter von 40 Jahren ohne klinische Anzeichen eines Tumorrezidivs. Eine Obstuktion wurde allerdings nicht durchgeführt. Die durchschnittliche Zeitspanne des Follow-ups der restlichen 7 Patienten mit Plattenepithelkarzinom betrug 25,7 Monate. Der kürzeste postoperative Beobachtungszeitraum der Patienten, die eine Tumornachsorge nachkamen, belief sich auf einen Monat, der längste auf 156 Monate (Frauen: Minimum 3, Maximum 86 Monate; Männer: Minimum 1, Maximum 156 Monate). Durchschnittlich dauerte der postoperative Beobachtungszeitraum 22,6 Monaten (Frauen durchschnittlich 19,2 Monate; Männer durchschnittlich 26,2 Monate). Siehe hierzu auch Tabelle 22. Tab. 22: Postoperative Beobachtungszeitspannen Minimum (Monate) Frauen 3 Männer 1 Maximum (Monate) 86 156 Durchschnitt (Monate) 19,2 26,2 Ergebnisse 68 3.22. Rezidive 3.22.1. Frühere Papillome in der Krankengeschichte 15 Patienten wurden uns mit einem Rezidiv eines zuvor alio loco vollständig entfernten invertierten Papilloms vorgestellt (19,5%). Bei den meisten Patienten (n=13) war ein früheres IP bekannt (16,9%), wir ermittelten in unseren Auswertungen aber auch eine Person, bei der bereits 3 Neubildungen eines in sano resezierten IP dokumentiert waren. Aus der Krankengeschichte eines weiteren Patienten gingen sogar 6 Fälle von früheren Tumoren dieser Art hervor. Insgesamt wurden in unserem Patientenkollektiv also 22 Operationen an früheren invertierten Papillomen durchgeführt. Tab. 23: Frühere IP Frühere IPs pro Patient (n) Anzahl (n) 1 13 3 1 6 1 Gesamt 15 Häufigkeit (%) 16,9 1,3 1,3 19,5 Die früheren Tumoren befanden sich vor allem in der Nasenhaupthöhle (n=8), aber auch der Sinus ethmoidalis stellte sich als häufig betroffene Lokalisation heraus (n=7). Dreimal lag der Ursprungsort im Sinus maxillaris, in zwei Fällen im Sinus sphenoidalis und einmal war das Wachstum auf den Sinus frontalis ausgedehnt. Die durchschnittliche Zeitspanne eines früher entfernten IP bis zur Vorstellung in unserer Klinik mit einem Rezidivtumor des IP dauerte 28 Monate. Dabei belief sich die kürzeste Dauer auf 4 Monate, in einem Fall entwickelte sich das Rezidiv eines IP erst nach 11 Jahren. Ergebnisse 69 Tab. 24: Lokalisationen der früheren IP und Dauer bis zur Entstehung des Rezidiv-IP Nr. 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Lokalisation des früheren IP Dauer bis zur Entstehung des Rezidivtumors Kieferhöhle, Keilbeinhöhle 12 NHH, Kieferhöhle 48 NHH 4 Siebbein, Kieferhöhle 6 Siebbein 12 NHH 12 NHH 36 NHH 12 Siebbein, Stirnhöhle 24 Siebbein 36 NHH, Siebbein 132 Siebbein 48 NHH 12 NHH 8 Siebbein, Keilbeinhöhle 12 Von den 15 Patienten, welche früher bereits an einem IP erkrankt waren, entwickelten 5 auch im späteren Verlauf, nach der Operation in unserem Hause ein Tumorrezidiv. Ergebnisse 70 3.22.2. Spätere Rezidive In unserem Patientengut entwickelten 17 Personen nach vollständiger Resektion des invertierten Papilloms in unserer Klinik ein Rezidiv des Tumors. Davon waren 5 Patienten bereits in der früheren Krankengeschichte an einem IP erkrankt. Von diesen 17 Personen wurde bei 15 Patienten (19,5%) ein einziger Fall einer späteren Neubildung des Tumors dokumentiert, doch gab es auch Fälle von mehreren späteren Rezidivtumoren (jeweils n=1, 1,3%). Tab. 25: Anzahl der Rezidive pro Person Anzahl der Rezidive (n) Anzahl der betroffenen Personen (n) Häufigkeit (%) 1 15 19,5 2 1 1.3 3 1 1,3 Auffallend ist die hohe Gesamtrezidivrate von 35%, wobei hier die 15 Patienten einbezogen sind, welche uns bereits mit einem Rezidiv eines invertierten Papilloms vorgestellt wurden. Bezogen auf unsere primär behandelten Patienten lag die Rezidivrate der nicht malignetransformierten invertierten Papillome bei 13%. 3.22.3. Dauer bis zur Entstehung eines Tumorrezidivs Die kürzeste Zeitdauer bis zur Entstehung eines Tumorrezidivs belief sich auf 3 Monate nach der ersten vollständigen Resektion, das längste rezidivfreie Intervall wurde mit 36 Monaten angegeben. Durchschnittlich dauerte das Zeitfenster bis zur Neubildung des invertierten Papilloms 12,6 Monate. Genauere Angaben sind Tabelle 26 zu entnehmen. Ergebnisse 71 Tab. 26: Rezidive eines invertierten Papilloms Lokalisation OP des Primär-IP des Primär-IP Kieferhöhle, Siebbein NHH Siebbein, NHH, Kieferhöhle NHH, Siebbein NHH, Siebbein Keilbeinhöhle KH-Fensterung, Endoskopie Laterale Rhinotomie Ethmoidektomie Dauer bis zur Entstehung eines Rezidivs (Mon) 6 Lokalisation des Rezidivtumors OP des Rezidivtumors Kieferhöhle, Siebbein NHH Kieferhöhle, NHH Caldwell-Luc, Ethmoidektomie Endoskopisch Caldwell-Luc, Ethmoidektomie 12 Kieferhöhle, Siebbein Kieferhöhle 7 Keilbeinhöhle 9 Kieferhöhle, Keilbeinhöhle Laterale Rhinotomie Ethmoidektomie, Caldwell-Luc Endoskopisch mit Navigationssystem Endoskopisch mit Navigationssystem 7 Siebbein, Keilbeinhöhle Laterale Rhionotomie 3 Laterale Rhinotomie Caldwell-Luc 4 12 Ethmoidektomie, Caldwell-Luc Ethmoidektomie, Endoskopie Endoskopie, Navigationssystem Ethmmoidektomie, KH-Fensterung, Endoskopie, Navigationssystem Ethmoidektomie, Endoskopie der Keiferhöhle Laterale Rhinotomie 36 5 9 36 NHH NHH Laser Endoskopisch Siebbein, Kieferhöhle NHH Ethmoidektomie, Caldwell-Luc Laser Ethmoidektomie, Endoskopie der Stirnhöhle Endoskopie, Ethmoidektomie Endoskopie NHH, Kieferhöhle Kieferhöhle 21 Stirnhöhle 6 NHH Septum Laterale Rhinotomie 7 NHH Kieferhöhle NHH KH-Fensterung Endoskopie 11 23 Kieferhöhle NHH KH-Fensterung, Ethmoidektomie Laterale Rhinotomie Laterale Rhinotomie Caldwell-Luc Laterale Rhinotomie Kieferhöhle, Siebbein, Keilbeinhöhle Siebbein, Kieferhöhle NHH, Kieferhöhle Kieferhöhle NHH Stirnhöhle Ergebnisse 72 3.22.4. Lokalisation des Rezidivs Bei 7 Personen beschränkte sich das Tumorwachstum auf nur eine Nasenstruktur, bei 6 Patienten waren 2 Strukturen betroffen. In einem Fall erstreckte sich die Epithelgeschwulst auf 3 Anteile der Nase und der Nasennebenhöhlen, und bei 3 Personen waren 4 Strukturen der Nase infiltriert. Tab. 27: Anzahl der vom IP-Wachstum betroffenen Nasenstrukturen Anzahl der vom IPWachstum betroffenen Nasenstrukturen (n) 1 2 3 4 Anzahl der Patienten (n) 7 6 1 3 Häufigkeit, bezogen auf die 17 Patienten mit Rezidiv (%) 41,2 35,3 5,9 17,7 Da auch das Rezidiv des invertierten Papilloms sich zum Teil auf mehrere Strukturen der Nase ausdehnte, sind hier Mehrfachnennungen möglich. Bevorzugte Lokalisationen für die Entstehung eines Rezidivs waren der Sinus maxillaris und die Nasenhaupthöhle in jeweils 8 Fällen (8 von 17, 47,1%), gefolgt vom Sinus ethmoidalis und dem Sinus sphenoidalis bei 3 Patienten (jeweils 3 von 17, 17,6%). In einem Fall (5,9%) erstreckte sich die Neubildung des IP auf den Sinus frontalis. Sehr häufig waren Strukturen wie zum Beispiel Sinus maxillaris und ethmoidalis (n=4), Septum und Nasenhaupthöhle (n=2) oder Muschel und Nasenhaupthöhle (n=2) gemeinsam vom Tumorwachstum betroffen. Das Rezidiv des invertierten Papilloms war in 11 Fällen auf der rechten Seite lokalisiert, und bei 5 Patienten befand es sich links. Nur ein Fall ist uns bekannt, bei dem sich die Rezidivausdehnung auf beide Seiten erstreckt. Ergebnisse 73 Tab. 28: Lokalisationen der IP-Neuentstehungen und deren Häufigkeit, bezogen auf die Gruppe der 17 Personen, welche an einem Rezidiv erkrankten Lokalisation des Rezidivs Anzahl (n) Sinus maxillaris Nasenhaupthöhle Sinus ethmoidalis Sinus sphenoidalis Sinus frontalis 8 8 3 3 1 Häufigkeit (%), bezogen auf die 17 Patienten mit Rezidiventwicklung 47,1 47,1 17,6 17,6 5,9 Rechte Seite Linke Seite Beidseits 11 5 1 64,7 29,4 5,9 3.22.5. Vergleich der Ausbreitungsseite von Rezidiv und Primärtumor Bei unseren 17 Patienten, welche postoperativ an einem Rezidiv erkrankten, hatte die Rezidivgeschwulst bei 13 Personen seinen Ursprung auf derselben Seite wie der Primärtumor (76,5%). Diese war bei 9 Personen rechts und bei 4 Patienten auf der linken Seite. In jeweils einem Fall breitete sich das Rezidiv auf der gegenüberliegenden Seite zum zuvor entfernten Primärtumor aus. Ein Fall wurde dokumentiert, bei dem das primäre IP links wuchs und sich das Rezidiv auf beide Seiten erstreckte. In den Fällen, in denen das IP zuvor beidseits lokalisiert war, begrenzte sich das Rezidivwachstum jedes Mal auf eine Seite. Tab. 29: Vergleich der Ausbreitungsseiten von Rezidiv und Primärtumor Rezidiv, rechte Seite Primärtumor rechts 9 Primärtumor links 1 Primärtumor beidseits 1 Seite gleich geblieben Seite abweichend 13 4 Rezidiv, linke Seite 0 4 1 Rezidiv, beidseits 0 1 0 Ergebnisse 74 3.22.6. Größe des Rezidivs Das kleinste uns bekannte Rezidiv hatte eine Größe von 0,3 cm, das größte Tumorwachstum wurde auf 3,5 cm gemessen. Die Durchschnittsgröße des Tumorrezidivs belief sich auf 1,3 cm. Tab. 30: Größe des Tumorrezidivs Rezidiv Minimum Maximum Durchschnitt Größe (cm) 0,3 3,5 1,3 3.22.7. Vergleich der Größe des Primärtumors mit der Größe des Rezidivs In unserem Patientengut entwickelten 17 Personen insgesamt 20 Rezidivtumoren eines zuvor im Gesunden entfernten invertierten Papilloms. In unseren Auswertungen richteten wir unser Augenmerk vor allem auch darauf, ob es wesentliche Unterschiede in der Größe der Primärtumoren und Rezidivgeschwulste gab und ob dies somit eventuelle Rückschlüsse auf die Entwicklungsgeschwindigkeit von postoperativen Tumorneubildungen zulässt. 10 der postoperativen Neubildungen waren kleiner als das zuvor entfernte IP, dabei lag der Größenunterschied in 4 Fällen unter 0,5 cm. Das Rezidiv war bei einem Patient bis zu 1 cm kleiner als die Primärgeschwulst und bei 2 weiteren Personen bis zu 1,5 cm. In je einem Fall lag die Größendifferenz im Bereich bis zu 2 cm, 2,5 cm und 3 cm. Die anderen 10 Rezidivfälle waren größenmäßig dem Primärtumor überlegen. Hier beobachteten wir 7 Rezidive, welche bis zu einem halben Zentimeter größer als der erste Tumor waren, 2 Fälle, bei dem das Rezidiv um bis zu 1 cm größer war, und einen Fall, bei dem die Größendifferenz sogar im Bereich bis zu 2,5 cm lag. Da die Dauer bis zur Entwicklung eines Tumorrezidivs in Bezug auf die Größe der Rezidivgeschwulst stark schwankt und sich in unserem Patientenkollektiv gleich viele Fälle von größeren und kleineren Tumorneuentwicklungen herausstellten, lässt sich an Ergebnisse 75 dieser Stelle kein Rückschluss darauf ziehen, ob ein Rezidiv zeitlich schneller an Größe zunimmt als der zuvor in sano resezierte Primärtumor. 3.22.8. Einteilung der Rezidivtumoren nach der Klassifikation von Krouse Die Ausdehnung der 20 Rezidivtumoren bestimmten wir entsprechend der Einteilung nach Krouse [70]. In jeweils 2 Fällen wurde ein Tumorwachstum des Stadiums 1 und 2 beobachtet, jedoch konnten wir die Mehrzahl der Rezidive dem Stadium 3 der Krouse-Klassifikation zuordnen (n=13). Eine Rezidivausbreitung des vierten Stadiums wurde in unserem Patientengut in 3 Fällen beobachtet. Einteilund der Rezidvtumoren nach dem Staging-System von Krouse 2 3 2 Stadium 1 Stadium 2 Stadium 3 Stadium 4 13 Abb. 29: Einteilung der Rezidivtumoren nach der Klassifikation von Krouse Ergebnisse 76 3.22.9. Anzahl der einzelnen Operationsmethoden zur Rezidivresektion Am Häufigsten wurde als Rezidivoperation die laterale Rhinotomie durchgeführt. Sie kamen bei den 17 Personen mit späterer Neubildung eines invertierten Papilloms sechsmal zur Anwendung (32,3%). Ebenfalls sehr oft führten die Operateure der Technik nach Caldwell-Luc in 5 Fällen durch (29,4%). Bei 4 Personen wurde die Resektion des IP-Rezidivs mittels einer Ethmoidektomie durchgeführt, was eine Häufigkeit von 23,5% ausmacht. Jeweils zweimal entschieden sich die Operateure je nach Tumorlokalisation für die Sphenektomie, die endoskopische IP-Resektion bei Sitz in der Nasenhaupthöhle (n=2) und Kieferhöhle (n=1), bis 1997 für die Laserexzision des Tumors, wenn dieser im Vestibulum nasi lokalisiert war (n=1), und seit dem Jahre 2002 wurde unter Zuhilfenahme der Neuronavigation operiert (n=2), hier vor allem bei Wachstum im Sinus sphenoidalis (je 11,8%). In einem Fall war der Rezidivtumor im Sinus frontalis lokalisiert, hier wurde endoskopisch vorgegangen. Genauere Angaben werden auch in Tabelle 31 gegeben: Tab. 31: Anzahl der einzelnen Operationstechniken bei Tumorrezidiv Operationsmethode Laterale Rhinotomie Caldwell-Luc Ethmoidektomie Sphenektomie Endoskopisch bei Sitz in der NHH Navigationsssystem Endoskopisch bei Sitz in der Kieferhöhle Endoskopisch bei Sitz in der Stirnhöhle Anzahl (n) 6 5 4 2 2 2 1 1 Häufigkeit (%), bezogen auf die 17 Patienten mit späterer Rezidiventwicklung 32,3 29,4 23,5 11,8 11,8 11,8 5,9 5,9 Ergebnisse 77 3.22.10. Tendenz zur Malignisierung der Rezidivtumoren In 3 Fällen konnte man histologisch auf dem Boden eines IP-Rezidivs ein malignes Wachstum sichern. Dies entspricht, bezogen auf die Gruppe der Personen, welche ein Rezidiv im postoperativen Verlauf entwickelten (n=17), einer Häufigkeit von 17,7%. Bei Sicht auf unser gesamtes Patientenkollektiv (n=77) betrug die Wahrscheinlichkeit, an einem Rezidiv mit onkozytärem Einschlag zu erkranken 3,9%. 3.22.11. Verlauf maligne transformierter IP Tab. 32: Patienten mit maligner Transformation des invertierten Papilloms und deren Krankheitsverläufe (vlg. Tab. 9) Nr. Geschlecht Primär-OP Primäre Lokalisation NHH Primäres UICC Stadium T4aN0M0 Rezidiv des PEC Zeitraum nein Therapie des PEC Follow-up 1 m Laterale Rhinotomie - SB T1N0M0 Ja / 24 Mon OP+adjuvante Radiatio Lebt rezidivfrei Lebt rezidivfrei 2 m 3 w 4 m Ethmoidektomie, Conchotomie, KHFensterung KH-Endoskopie, Ethmoidektomie, Neck Dissection Laterale Rhinotomie KH T4aN0M0 nein OP + adjuvante Radiatio Lebt rezidivfrei SB T1N0M0 nein OP + Interferontherapie Laser NHH T1N0M0 nein - Caldwell-Luc, Neck Dissection, Hemimaxillektomie, Orbitarevision Ethmoidektomie, Laterale Rhinotomie, Orbitarevision, Neck Dissection Endoskopische OP der SH, SB, KH KH T2N0M0 nein - Bricht Therapie selbstständig ab, Tod nach 2 Jahren Lebt rezidivfrei Lebt rezidivfrei 5 m 6 w 7 w SB T4aN0M0 nein OP+ adjuvante Radiatio Lebt rezidivfrei 8 m KH, SB, SH T1N0M0 nein - Lebt rezidivfrei Ergebnisse 78 3.22.12. Analyse zur Rezidivwahrscheinlichkeit Um die kumulative rezidivfreie Überlebenszeit unseres Patientenkollektivs zu ermitteln, verwendeten wir die Methode nach Kaplan & Meier [72]. Mit Hilfe dieses Tests konnten wir zeigen, dass die Wahrscheinlichkeit nach einer IP-Resektion rezidivfrei zu bleiben, in den ersten 12 Monaten postoperativ am schnellsten abnimmt. Sie fällt um nahezu 30% ab. Die Wahrscheinlichkeit, rezidivfrei zu bleiben, pendelt sich zu diesem Zeitpunkt also bei 73,8% ein, was sich beinahe durch das gesamte zweite Jahr der Nachbeobachtungszeit hindurch hält, um dann kurz vor Vollendung des zweiten postoperativen Jahres auf 70,3% zu sinken. Ab dem 36. postoperativen Monat reduziert sich die Wahrscheinlichkeit, bis dato kein erneutes Rezidiv aufzuweisen, auf knapp unter 60%, d.h. bei ca. 40% der postoperativ beobachteten Patienten lässt sich bis zum 3. Jahr des Follow-ups ein Rezidiv vermerken. Abb. 30: Kumulative rezidivfreie Überlebenswahrscheinlichkeit aller Patienten unserer Studie nach Kaplan & Meier Diskussion 4. 79 Diskussion Das invertierte Papillom wächst mit glatter Oberfläche endophytisch unter das Mukosaniveau und entspringt bevorzugt der lateralen Nasenwand [121, 124, 158]. Nach Beck und Mitarbeitern steht aus klinischer Sicht das IP zwischen den eindeutig benignen und eindeutig bösartigen Tumoren [7], weshalb man sich weltweit einig ist, dass das therapeutische Management dieser Läsion in einer in toto Resektion besteht [3, 5, 71, 70]. Rezidive treten vor allem dann auf, wenn der Tumor nur inkomplett entfernt wird [151, 176]. Der HNO-Arzt sollte deshalb Sorge tragen, dass postoperativ eine histologische Auswertung hinsichtlich der Resektionsränder erfolgt [71]. Unabhängig davon ist ein weiteres Charakteristikum dieser Tumorentität, dass auch nach vollständiger Resektion ein erneutes Auftreten möglich ist [7]. In der vorliegenden Arbeit haben wir uns nicht nur auf Klinik und Diagnostik von invertierten Papillomen konzentriert, sondern beschäftigten uns auch mit den einzelnen Therapieoptionen sowie den Therapieergebnissen hinsichtlich der Rezidiv- und Malignisierungsrate. 4.1. Allgemeines zum invertierten Papillom Seit der über 100 Jahre zurückliegenden Erstbeschreibung des invertierten Papilloms durch Ward, bestehen kontroverse Ansichten über die Ätiologie [165] sowie über das adäquate therapeutische Verhalten [20, 58, 114], weshalb diese primär benigne, sinunasale Tumorentität für den behandelnden HNO-Arzt noch immer eine Herausforderung darstellt [37, 75, 76]. Mit einem Anteil von 0,5-4% aller Tumoren der Nase und Nasennebenhöhlen zählt das IP eher zu den seltenen Tumoren [73]. Nur wenige Zentren überblicken mehr als 70 Fälle, so dass die Aussagekraft der meisten Studien schon deshalb begrenzt ist. Erhebliche Differenzen wichtiger nosologischer Daten treten allerdings auch im Vergleich jener Publikationen zu Tage, die sich auf größere Kollektive stützen bzw. prospektiv angelegt sind. Vor diesem Hintergrund ist es gerechtfertigt und notwendig, diese Thematik aufzugreifen [37]. Diskussion 80 Wir haben im Zeitraum von 1986 bis 2004 77 Patienten mit invertiertem Papillom der Nase und der Nasennebenhöhlen behandelt und retrospektiv ausgewertet. Tab. 33: Patientenzahl mit Invertiertem Papillom der verschiedenen Studien Autor Outzen et al., 1961 [112] Hyams et al., 1971 [64] Rudert, 1971 [131] Vrabec, 1975 [162] Suh et al., 1977 [153] Beck et al., 1984 [7] Kristensen et al., 1985 [79] Weissler, 1986 [168] Myers et al., 1989 [104] Vrabec et al., 1994 [163] Lawson et al., 1995 [83] Peter et al., 1997 [116] Nachtigal et al., 1999 [105] Weiner et al., 1999 [167] Klimek et al., 2000 [75] Smith et al., 2000 [146] Delank et al., 2000 [37] Luhn et al., 2002 [90] Oikawa et al., 2003 [107] Pasquini et al., 2004 [113] Tomenzoli et al., 2004 [159] Eigene Daten Patientenzahl 67 149 30 24 57 22 83 223 33 101 160 35 72 114 55 48 90 30 21 89 47 77 Die charakteristischen Merkmale dieses Tumors sind seine Tendenz, Rezidive zu entwickeln, seine lokale Destruktivität sowie seine Assoziation zur malignen Entartung [162]. Diskussion 81 Histopathologisch lassen sich nach Perzin und Mitarbeitern zwei Formen unterscheiden [115]: 1. die häufigste Form eines lokal invasiv wachsenden, nicht metastasierenden Tumors 2. das invertierte Papillom mit fokalem Karzinom oder Carcinoma in situ oder das von einem invertierten Papillom ausgehende invasiv wachsende Karzinom In unserem Patientenkollektiv handelte es sich in 69 Fällen um ein lokal wachsendes invertiertes Papillom, und in 8 Fällen handelte es sich um ein IP, auf dessen Boden ein Plattenepithelkarzinom hervorging. Diskussion 4.2. 82 Histologie und Staging Systeme Mikroskopische Untersuchungen haben gezeigt, dass die Hauptmasse der papillomatösen Neubildung aus vielfach geschichtetem, stellenweise verhornendem Plattenepithel besteht, in dessen tiefere Lagen zahlreiche Karyokinesen auf eine lebhafte Wachstumsgenese hinweisen [15, 38, 60]. Gelegentlich zeigen sich Entzündungszellen. Auch Epithelmetaplasien sind kein seltener Befund an der Oberfläche von Nasenschleimhautgeschwülsten [24, 55]. Sie werden auf entzündliche und mechanische Reize zurückgeführt [99]. In einzelnen Präparaten des invertierten Papilloms lassen sich auch Epitheldysplasien nachweisen [139, 143, 172]. Die invertierten Papillome sind Epithelgeschwülste, die der Oberfläche breitbasig aufsitzen und ein fingerförmig verästeltes, zapfenförmiges Stroma mit Epithelüberzug aufweisen [124]. Die treibende Kraft der invertierten Zapfenbildung sind die proliferierenden Basalzellen des Epithels. Diese Proliferation erfolgt unter einem metaplastisch entstandenen Plattenepithel (Desmosomennachweis), welches in seiner Schichtung oft übergangsepithelartig ist [149]. Unsere Fälle bieten histologisch ein weitgehend gleichartiges Bild im Sinne einer plattenepithelialen Differenzierung. Das mehrschichtige Epithel ist polar aufgebaut und die Basalmembran intakt. Nur in einem Präparat konnten Mitosen ohne sonstige Hinweise auf das Vorliegen einer malignen Entartung gefunden werden. Gelegentlich zeigten sich im histologischen Bild Epithelmetaplasien (n=7) und -dysplasien (n=7). Interepithelial gelegene Entzündungszellen sind von Fall zu Fall unterschiedlich zahlreich. In 8 Fällen zeigte sich bei den IPs eine maligne Entartung, wobei es sich in 5 Fällen um eine Primärmanifestation und in 3 Fällen um ein Karzinom im Rezidiv des invertierten Papilloms handelte. Da durch ähnliche Makroskopie und Symptomatik der Nasenpolyp die häufigste Differentialdiagnose des invertierten Papilloms darstellt [7], sollte der HNO-Arzt vor allem bei Polypenrezidiven stets dafür Sorge tragen, dass Nasenpolypen mit ausgeprägter Plattenepithelmetaplasie oder gar schon beginnender Epithelzapfenbildung histologisch besonders sorgfältig aufgearbeitet und auf ein invertiertes Papillom im Initialstadium untersucht werden [150]. Diskussion 83 Abb. 31: Operationspräparat eines in der rechten Nasenhaupthöhle lokalisierten vom Infundibulum ethmoidale ausgehenden IP (4,2 × 2,3 × 1,2 cm). Makroskopisch ist eine Unterscheidung zu einem chronisch-entzündlichen Nasenpolypen kaum möglich Im Gegensatz zu den Aussagen von Romashko und Mitarbeitern, welche die Meinung vertreten, Probeexzisionen sollten nur in bestimmten Fällen, wie zum Beispiel nur beim Vorliegen von unilateralen Polyposis nasi und unilateralen Sinusitiden oder nur in den Fällen, bei denen eine weiterführende Diagnostik benötigt wird, durchgeführt werden [129], sind wir in unserem Hause der Ansicht, dass eine Notwendigkeit der Probeentnahme zur histopathologischen Untersuchung generell bei allen operativen Eingriffen von Nasenund Nasennebenhöhlenpolypen und bei Verdacht auf eine chronische Sinusitis besteht, da die Diagnose des invertierten Papilloms oft einem Zufallsbefund entspricht. Mehrere Autoren haben versucht, das invertierte Papillom in Anlehnung an die Plattenepithelkarzinome zu klassifizieren [7]. Die meisten dieser Staging Systeme für IP beschreiben eine Vierer-Einteilung, welche sämtliche IP der Nasenhaupthöhle als T1Stadium bezeichnet, unabhängig von der Ausdehnung innerhalb der Nase [76, 138]. Skolnik et al. und Schneider gaben eine Klassifikation an, die im Wesentlichen den Knochenbefall berücksichtigt [136, 145]. Beide Staging Systeme geben aber weder einen Hinweis auf die Prognose noch die Therapie. Diskussion 84 Erst kürzlich entwickelte Krouse ein in der Handhabung einfaches Staging System für invertierte Papillome, welches dem HNO-Arzt ermöglicht, die Tumoren in klar definierte Kategorien einzuteilen, welche sowohl Ursprungslokalisation, als auch Tumorausdehnung berücksichtigen [80]. Diese Klassifikation lässt sich bei endoskopischen Untersuchungen genauso anwenden wie bei der Befundung von Computertomogrammen [76, 80]. Diskussion 4.3. 85 Lokalisation Das IP wächst vorzugsweise in der Nasenhaupthöhle, dem Siebbeinzellsystem und dem Sinus maxillaris. Ein bilaterales Wachstum sowie ein primärer Befall der Stirn- und Keilbeinhöhle sind Raritäten [9, 89]. Das IP entspringt der sogenannnten „Schneider Membran“, welche sich embryologisch von den Riechplakoden ableiten lässt [55]. Das IP kann seinen Wachstumsurprung deshalb von allen Strukturen nehmen, welche von dieser Membran ausgekleidet werden. Gelegentlich sind die HNO-Ärzte vor die Aufgabe gestellt, ein IP mit Ausbreitung in extranasale Gebilde zu therapieren wie zum Beispiel Nasopharynx, Orbita, Tränensack und Dura [162]. Gelegentlich wurde diese Tumorentität aber auch in Strukturen wie dem Mittelohr und dem Mastoid beschrieben [2, 69, 152]. Hier geht man davon aus, dass die Tuba Eustachii als eine Art Führungsschiene für die Ausbreitung des Tumors dient [46]. Auch ein IP ausgehend vom Temporalknochen wurde beobachtet [19]. Sogar ein pulmonales IP wurde beschrieben [47, 94]. Da das IP lokal erosiv vorwächst, kommt es nicht selten zu einer Infiltration von knöchernem Gewebe [104]. Die Angaben zur Häufigkeit in der Literatur schwanken hierbei zwischen 7,1% und 51,9% [103, 130]. In unserer Studie wurden Knocheninfiltrationen bei 10 Patienten beobachtet, was einen Anteil von 13,0% ausmacht. Obwohl die lokale Destruktion als pathognomonisch gilt [37], fanden wir eine die Nasennebenhöhlen überschreitende extranasale Tumorausbreitung lediglich in 9,1% der Fälle. Diese Beobachtung stützt die Hypothese, dass die Destruktion im Wesentlichen durch eine lokale Expansion zustande kommt, die auf die Schleimhaut begrenzt ist und vorgegebenen Ostien folgt [37]. Diskussion 4.4. 86 Ätiologie Obwohl die Entwicklung des invertierten Papilloms Subjekt verschiedenster Interpretationen ist, konnte die wahre Ätiologie dieser Tumorentität bis heute nicht eindeutig ausgemacht werden [28]. Einige Autoren betrachten die Geschwulst als eine Manifestationsform von chronischer Sinusitis [86, 176], andere dagegen sehen diese Tumorart bereits als „prämaligne“ an [19, 109, 170]. Da angenommen werden kann, dass die meisten IPs von der Nasenhaupthöhle und dem vorderen Siebbeinzellsystem ausgehen, könnte man annehmen, dass aerodynamische Faktoren hier eine Rolle spielen könnten [37], denn die Inspirationsluft strömt hauptsächlich durch den mittleren Nasengang, der deshalb in hohem Maße schadstoffexponiert ist. Derzeit kann tatsächlich nicht ausgeschlossen werden, dass eine langfristige Inhalation von Schadstoffen als Kofaktor in der Pathogenese invertierter Papillome in Betracht kommt [36, 93]. Zumindest tierexperimentell ließen sich Papillome durch Nitrosamine induzieren [57]. Auch unter unserem Patientengut befand sich eine Person, welche jahrelang beruflich unter Reizgasexposition stand. Außerdem werden von einigen Autoren Faktoren wie Rauchen, Allergien und Umweltfaktoren als krankheitsauslösend angesehen [20]. Auch die Hypothese einer viralen Genese wurde gestellt. Nach neuesten Kenntnissen wird das humane Papillomavirus (HPV) Typ 16 und 18 für die Entstehung des IP verantwortlich gemacht [4, 21, 22, 48, 49, 54, 75, 155], doch wurde kürzlich auch eine mögliche Beteiligung des Epstein-Barr-Virus in Betracht gezogen [66]. Diskussion 4.5. 87 Inzidenz, Alters- und Geschlechtsverteilung Die jährliche Inzidenz des invertierten Papilloms wird in der Literatur zwischen 0,6 bis 1,5 pro 100,000 Einwohner angegeben [23, 111] und macht fast 70% aller Nasenpapillome aus [71]. Männer sind ca. 4-5 Mal so häufig betroffen wie Frauen [64, 118, 171]. Auch in unserem Patientengut ist das männliche Geschlecht 4 Mal stärker vertreten, der Frauenanteil in unserer Studie mit 16,9% unterscheidet sich also nicht wesentlich von dem Durchschnitt der anderen Publikationen, hier beträgt dieser im Mittel 19,6%. Die Prävalenz des Tumors ist in der 5. bis 6. Lebensdekade datiert, es sind allerdings auch einzelne Beobachtungen in pädiatrischen Altersgruppen publiziert worden [42]. Das durchschnittliche Alter der Erstmanifestation der Tumorentität liegt in unserer untersuchten Patientengruppe nur gering über dem Altersdurchschnitt der in der Literatur vorgestellten Patienten, wo dieser bei 56 Jahren liegt, allerdings ist hierbei zu bedenken, dass zum Beispiel die umfangreiche Studie von Hyams mit 149 Fällen in einem Militärhospital durchgeführt wurde, und deshalb dort vor allem jüngere Patienten vorzufinden sind. Das mittlere Alter unseres Patientenkollektivs beträgt 62 Jahre. Diskussion 88 Tab. 34: Alters- und Geschlechtsverteilung des IP in verschiedenen Studien Autor Mittleres Alter bei Manifestation Smith et al. [146] 49 Vrabec [163] 60 Suh et al. [153] 61 Peter et al. [116] 56 Lawson et al. [83] 52 Hyams et al. [64] 35 Snyder et al. [147] 57 McLachlin et al. [96] 47 Outzen et al. [112] 58 Tomenzoli et al. [159] 53 Pasquini et al. [113] 57 Myers et al. [104] 66 Beck et al. [7] 62 Klimek et al. [75] 59 Oikawa et al. [107] 59 Nachtigal et al. [105] 62 Eigene Daten 62 Männer Frauen 87% 67% 83% 74% 80% 84% 77% 93% 73% 85% 70% 79% 75% 80% 81% 88% 13% 33% 17% 26% 20% 16% 23% 7% 27% 15% 30% 21% 25% 20% 19% 12% Verhältnis Männer:Frauen 7:1 2:1 5:1 3:1 4:1 5:1 3.1 13:1 3:1 6:1 2:1 4:1 3:1 4:1 4:1 7:1 83% 17% 5:1 Diskussion 4.6. 89 Klinische Symptomatik des invertierten Papilloms Das mit Abstand häufigste klinisch bemerkbare Symptom des invertierten Papilloms ist die Nasenatmungsbehinderung [61, 84, 111, 123, 129, 63, 161]. Andere Symptome wie Rhinorrhoe, Epistaxis, Cephalgien und Fremdkörpergefühl treten einzeln oder in Kombination deutlich seltener auf. Vereinzelt werden auch Beschwerden wie Geruchsund Geschmacksverlust, Tinnitus sowie Hör- und Sehstörungen angegeben [111, 140, 147, 160, 175], doch sind diese in Übereinstimmung mit den Literaturangaben eher als uncharakteristisch einzustufen [64, 116, 137, 149, 158]. Die von uns gewonnenen Daten unseres Patientenguts stimmen in Bezug auf das klinische Erscheinungsbild des invertierten Papilloms im Wesentlichen mit den Angaben der Literatur überein. Die Symptomatik des Tumors lässt sich zum einen durch die Verlegung der oberen Atemwege erklären, wie zum Beispiel die behinderte Nasenatmung und gestörtes Riechsowie Geschmacksempfinden, zum anderen ruft die Geschwulst eine direkte Irritation der Nasenschleimhaut hervor, was Symptome wie zum Beispiel Epistaxis, Rhinorrhoe und Fremdkörpergefühl zur Folge hat [117, 146]. 4.7. Präoperative Maßnahmen In der Literatur findet man häufig die Empfehlung, präoperativ systemische Antibiotika und Kortikoide zu verabreichen, da diese eine eventuell gleichzeitige Polyposis nasi deutlich reduzieren können und dem HNO-Arzt somit im Vorfeld einen besseren Überblick über die tatsächliche Ausdehnung und den Ursprungsort des invertierten Papilloms im Röntgenbild verschaffen [76]. Außerdem können diese Präparate intraoperativ die Blutungen signifikant verringern [161]. In unserem Patientengut wurden in 6 Fällen präoperativ Kortisonpräparate und fünfmal Antibiotika verschrieben, welche aber nur geringfügig die Tumorsymptomatik verbessern konnten. Darüber, ob die im Vorfeld verabreichten Medikamente auch intraoperativ Vorteile zeigten, liegen uns für unsere Studie keine Informationen vor. Diskussion 90 In der präoperativen Ausdehnungsbestimmung wird die Computertomographie als Mittel der Wahl angesehen. Dabei stellt sich das invertierte Papillom gewöhnlich als unilaterale Geschwulst mit lobulärer Oberfläche dar, welche sich meist vom Meatus medialis ausgehend in eine oder mehrere der Nebenhöhlen erstreckt [159]. Dabei ist das CT in der Frage nach knöchernen Destruktionen unverzichtbar [34, 44, 91, 167], jedoch sind die Möglichkeiten der Computertomographie auch limitiert, denn das CT erlaubt keine Aussagen darüber, ob neben dem Tumor auch eine eventuell begleitende Stauungssinusitis vorliegt, was zur genauen präoperativen Planung möglichst unterschieden werden sollte [171]. Bezogen auf die Aussagen von Ojiri et al. [108] können die Grenzen der Computertomographie durch die Anfertigung einer Magnetresonanztomographie überschritten werden, welches in der Lage ist, neoplastisches Gewebe von entzündlichen Veränderungen in 80% der Fälle zu unterscheiden [53, 108, 133, 177]. Doch auch die diagnostischen Möglichkeiten des MRT enden bei der Frage, ob sich auf dem Boden eines IP maligne Transformationen entwickeln [159, 177]. Minovi et al. ist der Ansicht, dass zur genauen präoperativen Diagnostik in jedem Falle ein Magnetresonanztomogramm angefertigt werden sollte [101], wir in unserem Hause vertreten jedoch die Meinung, dass dies nicht grundsätzlich notwendig ist. Wir bevorzugen vielmehr die Computertomographie und greifen nur bei präoperativem Verdacht auf ein malignes Geschehen auf die Magnetresonanztomographie zurück. Diskussion 91 Abb. 32: Coronares Computertomogramm eines 57jährigen Patienten mit einem IP des Sinus maxillaris und des vorderen Siebbeins rechts Diskussion 4.8. 92 Operationsmethoden Generell ist in der Literatur unstrittig, dass das operative Vorgehen die Methode der Wahl darstellt [51, 150]. Hierbei sollten gemäß Lawson et al. 3 grundlegende Regeln beachtet werden [84]: 1. Um den Tumor sicher vollständig entfernen zu können, ist eine ausreichende Exposition erforderlich. 2. Um Rezidive frühzeitig erkennen zu können, sollte der Situs postoperativ eine gute Übersicht des Operationsgebiets ermöglichen. 3. Kosmetische und funktionelle Beeinträchtigungen sollten so gering wie möglich gehalten werden. Mögliche operative Techniken beinhalten neben Methoden mit externem Zugangsweg, wie zum Beispiel der lateralen Rhinotomie, der OP nach Caldwell-Luc oder dem Midfacial Degloving auch den intranasalen, endoskopischen Zugang [25, 31, 41, 51, 68], wobei über die adäquate chirurgische Vorgehensweise in der Literatur bis heute Uneinigkeit besteht [58, 83, 99, 158]. In den 70er- und 80er Jahren vertrat man die Ansicht, das beste operative Vorgehen sei die radikale En bloc Resektion durch einen externen Zugang [80], wohingegen in den 90er Jahren vermehrt auch minimal invasive Techniken, wie die Mikroskopie und Endoskopie, zur Anwendung kamen [113]. Damals ging man vermehrt dazu über, operative Verfahren, die ursprünglich für die chronisch polypöse Rhinosinusitis unter dem Aspekt der Schleimhautprotektion und des größtmöglichen Funktionserhalts entwickelt worden waren, auch bei invertierten Papillomen anzuwenden [37], jedoch wiesen bald mehrere Autoren auf eine steigende Rezidivrate nach diesem Vorgehen hin [11, 26, 33, 37, 140]. Man kam zu dem Schluss, dass das endoskopische Konzept, welches für die polypöse Rhinosinusitis vorgesehen war, für den Anwendungsbereich des IP modifiziert werden und einen größeren Umfang beinhalten müsse [14, 83, 145]. Heute wird generell empfohlen, sich, wenn möglich, in der Operationsplanung auf die histopathologischen Ergebnisse einer zuvor entnommenen Probeexzision zu stützen. Liegt nämlich bereits eine präoperative Histologie vor, kann der Operateur das den Tumorursprungsort umgebende Schleimhautareal sicher mitexzidieren. Handelt es sich bei Diskussion 93 dem IP um eine kleinere, nicht destruierende Geschwulst, so sollte man eine endoskopische oder mikroskopische Kontrolle zu Hilfe nehmen. Ist dies aufgrund weiterer IP-Ausdehnung nicht mehr möglich, empfiehlt es sich, eher einen externen Zugangsweg, je nach Lokalisation z.B. eine laterale Rhinotomie oder Caldwell-Luc OP in Erwägung ziehen [149]. Dies gilt insbesondere dann, wenn z.B. das IP in der lateralen, weit superioren oder anterioren Stirnhöhle lokalisiert ist, welche für ein rein endoskopisch-operatives Vorgehen nicht sicher zu erreichen ist [41]. Die Arbeitsgruppe um Draf sieht die Einschränkung für eine endonasale mikroendoskopische Tumorresektion in einer weit lateralen Ausdehnung des IP in der Stirnhöhle, die eine fiktive vertikale Linie durch die Lamina papyracea überschreitet. In diesen Fällen sei eine subperiostale Resektion kaum möglich [101]. Die Kontraindikation des endonasalen Zugangs sieht Draf beim Ursprung des IP an der posterolateralen, antioren oder inferioren Kieferhöhlenwand, da an diesen Lokalisationen die Tumorwurzeln nicht sicher genug von endonasal her entfernt werden können. In beiden Fällen sollen nach Auffassung der Autoren primär osteoplastische Zugänge verwendet werden, d.h. die osteoplastische Stirnhöhlen- bzw. Kieferhöhlenoperation [101]. An der Univ.-HNO-Klinik Freiburg sind wir der Auffassung, bei externen Zugängen zur Kieferhöhle (Caldwell-Luc) nach Möglichkeit ein osteoklastisches Vorgehen zu wählen, da so die Gefahr einer potentiellen Knochennekrose der bei osteoplastischem Vorgehen wiedereinzusetzenden Kieferhöhlenvorderwand oder Osteomyelitis nicht gegeben ist sowie das Auftreten von Wundheilungsstörungen und Tumorrezidiven geringer zu sein scheint. Postoperative ästhetische narbige Einziehungen der Wangenweichteile oder ein Enophthalmus haben wir bisher nicht beobachtet. Bei einer osteoplastischen Kieferhöhlenoperation (nach Feldmann) wird die faziale Kieferhöhlenwand mit einer Mikrostichsäge ausgesägt und nach erfolgter Kieferhöhlensanierung wiedereingesetzt und mit Nähten über Bohrlöcher am Rand des Trepanationsbereichs fixiert. Erfolgt die Operation unter dem Aspekt von Nasenpolypen mit erst nachträglicher histologischer Diagnosestellung, so sollte bereits bei Verdacht auf mangelnde Radikalität eine endoskopische Kontrolle und gegebenenfalls eine Nachresektion durchgeführt werden [150]. Diskussion 94 Gemäß Raveh und Mitarbeitern ist man sich generell einig, dass das IP nach Möglichkeit im Ganzen entfernt werden sollte, da das Risiko eines Rezidivs ansonsten steigt [122], dabei konnte eine Reduktion der Invasivität heutzutage nicht nur durch die Einführung der endonasalen Operationstechniken erreicht werden [164], sondern erlauben heute ebenfalls osteoplastische Verfahren, verfeinerte Rekonstruktionstechniken und der kombinierte Einsatz von Mikroskop und Neuronavigationssystem, auch aufwendige schädelbasisnahe Operationen über externen Zugang funktionell und kosmetisch akzeptabel zu gestalten [10, 37, 40, 87, 134]. Gemäß Delank kann man nachweislich diesbezüglich auch mit der lateralen Rhinotomie gute Ergebnisse erzielen [37]. Sie ermöglicht es, den Tumor En bloc zu entfernen, vor allem dann, wenn die laterale Nasenwand und der Sinus maxillaris infiltriert sind [26, 104, 162]. Die laterale Rhinotomie bietet dabei eine exzellente dreidimensionale Übersicht und genügend operative Freiheitsgrade, was dem Operateur gegebenenfalls eine sichere Präparation an und in der Orbita sowie der Schädelbasis gewährleistet [37, 83, 112]. Aus diesen Gründen wird diese Methode auch heute noch von vielen Autoren weltweit favorisiert [104, 122, 140, 151]. Nachteile der lateralen Rhinotomie umfassen Epiphora, Dakrozystitis, Diplopie und infraorbitale Hypästhesie [110]. Die Methode des Midfacial Degloving kann als gute Alternative zur lateralen Rhinotomie betrachtet werden, vor allem dann, wenn das invertierte Papillom bilateral auftritt oder auf die laterale Nasenwand limitiert ist [132, 148, 162]. Es hat den Vorteil, dass postoperativ keine sichtbare Narbe entsteht, doch zeigt sich ein Nachteil, wenn der Sinus frontalis, die supraorbital gelegenen Zellen des Sinus ethmoidalis oder der Tränensack vom Tumor infiltriert sind [121, 162]. Auch die Technik nach Caldwell-Luc hat sich häufig in der operativen Sanierung des invertierten Papilloms vor allem dann bewährt, wenn man bei ausgedehnteren Tumoren einen Zugang zum lateralen Teil des Sinus maxillaris benötigt [63]. Unter anderem empfehlen Barzilai und Mitarbeiter diese Methode mit der endoskopischen medialen Hemimaxillektomie zu kombinieren [6, 35, 141, 154]. Die Lokalisation des IP im Sinus frontalis stellt für den Operateur aufgrund der anatomischen Gegebenheiten im Sinne der schweren Erreichbarkeit eine Herausforderung dar [135]. Hier bietet sich bei größeren Tumorläsionen neben der Endoskopie ein externer Diskussion 95 Zugang in Form einer bitemporalen koronaren Inzision (Bügelschnitt / UnterbergerSchnitt) als transfrontaler extraduraler Zugangsweg an [154], welcher auch bei 2 Patienten unserer Studie zur Anwendung kam. Dieses Vorgehen ermöglicht intraoperativ einen weit ausgedehnten, bilateralen Zugang zur Stirnhöhle und zum Siebbein [83]. Die mikroskopisch-endoskopische Tumorresektion kann vor allem dann durchgeführt werden, wenn die Tumorläsion noch nicht sehr ausgeweitet ist und sich auf die Nasenhaupthöhle, den Sinus ethmoidalis und sphenoidalis sowie auf die medialen Anteile des Sinus maxillaris begrenzt [16, 84, 102]. Sind jedoch computertomographisch sogenannte kritische Regionen wie der tiefe Recessus alveolaris, der Ductus nasolacrimalis betroffen oder gar Knochendestruktionen erkennbar, dann ist das endoskopische Vorgehen limitiert und sollte transoral oder transfazial ergänzt werden [171]. Tab. 35: Indikationen für konservative und radikale Operationstechniken [82] Operationsmethode Endoskopisch/ mikroskopisch Laterale Rhinotomie Midfacial Degloving Unterbergerschnitt Caldwell-Luc Lokalisation Nasenhaupthöhle Sinus maxillaris Sinus ethmoidalis Sinus sphenoidalis Ductus nasolacrimalis Laterale Nasenwand Supraorbitaler Teil des ethmoidalis Anteile der Orbita infiltriert Bilateraler Sitz Sinus frontalis Sinus maxillaris Sinus Zur genauen Abschätzung, inwieweit ein Tumor noch mikroskopisch/endoskopisch entfernt werden kann, oder ob vielmehr ein zusätzliches externes Vorgehen gewählt werden sollte, bedarf es jedoch auch einer großen Erfahrung des Operateurs [102, 171]. Schwierigkeiten in der Operationsplanung ergeben sich dann, wenn ein Patient bereits mehrfach im Operationsgebiet voroperiert wurde [163], denn dies führt zwangläufig zu Diskussion 96 anatomischen Veränderungen und erschwert die topographische Orientierung durch fehlende oder veränderte Landmarken. Beispielsweise kann das IP auf dem Boden von Narbengewebe entstehen oder schneller in Strukturen wie Periorbita oder Dura einwachsen [162], hier ist die Zuhilfenahme der Neuronavigation sinnvoll, welche in unserem Hause seit 2002 zur Anwendung kommt [134]. Auch bei unserem Patientenkollektiv waren unsere Operateure mehrfach vor die schwierige Aufgabe gestellt, eine wegen eines früheren IP alio loco voroperierte Nase therapeutisch zu versorgen (n=15). Bei 6 Patienten wurde dies mit Hilfe der Neuronavigation durchgeführt. Insgesamt wurden in unserem Patientenkollektiv 42 Personen in der Vorgeschichte aus diversen Gründen bereits im Hals-Nasen-Ohrenbereich voroperiert. In jedem Falle ist postoperativ eine sorgfältige Nachsorge notwendig [37, 75, 102, 162]. Diese ist am besten dann möglich, wenn die eigentliche Sanierung des Tumors und dessen Basis durch die Anlage glatter Übergänge und die Erweiterung der Ostien zum Nebenhöhlensystem ergänzt wird [37]. Die erstrebenswerte Forderung nach minimaler Invasivität kann deshalb in diesem Sinne nur begrenzt erfüllt werden [8, 104, 142, 162]. Nach Anwendung beispielsweise der lateralen Rhinotomie lässt sich eine endoskopische Kontrolle durch die erweiterte Nasenhöhle einfach durchführen [163], jedoch kann sich das endoskopische Follow-up bei den Patienten, bei denen konservativ vorgegangen war, als schwieriger und zeitaufwändiger gestalten, hier muss man unter Umständen vermehrt auf Bildgebung wie dem CT zurückgreifen [75, 162]. Die Tumornachsorge sollte in regelmäßigen Abständen stattfinden und insgesamt mindestens 5 Jahre umfassen [105, 176]. Dabei sollte gemäß Tomenzoli und Mitarbeitern der Patient im ersten postoperativen Jahr alle 4 Monate vorstellig werden und in den folgenden 4 Jahren alle 6 Monate zur ambulanten Kontrolle einbestellt werden [159], jedoch kann auch der niedergelassene HNO-Arzt in das Follow-up involviert werden oder die Nachsorge komplett übernehmen. Diskussion 97 Die Fälle, bei denen präoperativ histologisch maligne Kriterien, wie hochgradige Dysplasien oder infiltratives Wachstum, gesichert wurden, sind nach onkologischen Kautelen zu behandeln [7]. Nach Beck und Mitarbeitern muss die Therapieplanung bei Knocheninfiltrationen ohne zytologische Kriterien der Malignität vom Befall der Orbita abhängig gemacht werden, denn bei eindeutigem Einbruch des Tumors ist eine Exenteratio orbitae nicht zu vermeiden [7]. Intraoperativ lässt sich der Tumor jedoch meist leicht vom Periost der Periorbita trennen. Die gute Abgrenzbarkeit gilt auch für die Fälle mit tumorbedingter Freilegung der Dura der vorderen Schädelgrube [163]. Schwer zu beherrschen sind Infiltrationen des harten Gaumens. Hier führen oft nur verstümmelnde Operationen mit Resektion der Gaumenplatte zum Ziel [7]. Anschließend sollten in jedem Falle engmaschige klinische und radiologische Kontrollen vorgenommen werden [3]. Diskussion 4.9. 98 Anwendung der Radiochemotherapie Vielfach ist früher in der Literatur die Ansicht vertreten worden, dass die Radiotherapie bei der Behandlung von fortgeschrittenen, biologisch aggressiven invertierten Papillomen effektiv sein könnte [98]. Heute kann die Radio- bzw. Chemotherapie zur Behandlung des invertierten Papilloms alleine als obsolet betrachtet werden, denn ihr kommt heute lediglich als Adjuvans bei IP mit Plattenepithelkarzinomanteilen Bedeutung zu [51, 104, 153]. Einige Autoren sind allerdings der Meinung, die Radiochemotherapie sei nicht nur ziemlich ineffektiv, sondern birgt auch die Gefahr der malignen Entartung einer ansonsten benignen Läsion [52, 98, 162]. Nach den Aussagen von Ferlito und Mitarbeitern sollte die Radiochemotherapie nur dann als letzte Möglichkeit versucht werden, wenn ein maligne entartetes IP nicht mehr einer operativen Sanierung zugänglich sei [46]. In unserem Kollektiv wurde bei 3 Patienten mit maligne entarteten IP eine adjuvante Radiatio durchgeführt, zusätzlich erhielt ein Patient eine Interferontherapie. Nur bei einer Patientin wurde postoperativ eine systemische Chemotherapie angewandt, da diese eine metachrone Kalottenfiliae aufwies. Diskussion 99 4.10. Entwicklung von postoperativen Komplikationen In unserem Patientenkollektiv beklagten 31 Personen postoperative Beschwerden. Diese waren fast durchgehend eher leichterer Natur, wie gelegentlich schwache Nachblutungen, Borkenbildung und Schmerzen im Bereich des Operationsgebiets. Dabei stimmen unsere Daten mit denen in der Literatur genannten, weitgehend überein. Auch hier werden meist nur eher leichte Komplikationen beschrieben, wie leichte Epistaxis, Entzündung im Bereich der Naht und Cephalgien [37, 162]. Lesperance teilte die postoperativen Beschwerden in zwei Kategorien ein. Dabei unterschied er schwere und leichte Komplikationen [88]. Tab. 36: Einteilung postoperativerKomplikationen nach Lesperance [88] Schwere Komplikationen: Epiphora Mukozele Fisteln Diplopie Septumhämatom Leichtere Komplikationen: Wundinfektion Gesichtsschmerz Trockene Nase Epistaxis Nasale Obstruktion Borkenbildung Leichte Rhinorrhoe Vorübergehende Hypästhesie Von den 31 Personen, welche in unserer Studie postoperative Beschwerden entwickelten, zeigten sich nach diesem Schema nur in 3 Fällen schwere Komplikationen in Form von zweimal einer Mukozele und einmal einer Gaumenfistel. Diskussion 100 4.11. Tendenz zur Rezidivierung des invertierten Papilloms Ein häufig in der Literatur diskutiertes Thema ist die Neigung des Tumors zur Rezidivierung, dabei ist die Entwicklung einer erneuten Tumorbildung eines einmal entfernten IP ein multifaktorieller Prozess, welcher von vielfältigen Faktoren abhängt, wie zum Beispiel der Tumorlokalisation, der Ausdehnung, der Möglichkeit einer Probeexzision, der Histologie, der Multizentrizität, der Art der Operation, der Anzahl der notwendigen Nachresektionen und dem Follow-up. Aber auch Komponenten wie soziale Faktoren, Risikoverhalten wie zum Beispiel Nikotin- und C2-Abusus sowie der biologischen Variabilität des Tumors spielen eine nicht geringe Rolle [83]. Die Angaben in verschiedenen Publikationen bieten in Bezug auf die Rezidivierung eine weite Spannbreite zwischen 6% und 77% [112], wobei man die Entwicklung eines Rezidivs allgemein meist auf die unvollständige Entfernung des Tumors zurückführt [39, 95, 126, 155], deshalb sollten immer histologische Untersuchungen des, in einer Operation entfernten Tumorpräparates, in Bezug auf Vollständigkeit durchgeführt werden. Ein Hinweis darauf, dass einer der Hauptgründe für eine Rezidiventwicklung die unvollständige operative Entfernung des IP ist, könnte die Tatsache sein, dass die Rezidive meist die gleiche Lokalisation aufweisen wie der Primärtumor [79, 83, 162, 168]. In unserer Studie ist dies in 44,4% aller Rezidive der Fall. In unserer Studie entwickelten jedoch trotzdem 17,1% aller Fälle, welche als komplett reseziert dokumentiert wurden, ein Rezidiv. Viele Autoren haben sich der Frage nach der Rezidivquote gestellt, doch konnte man sich, aufgrund der zum Teil völlig unterschiedlichen Ergebnisse bislang auf kein eindeutiges Resultat festlegen. Kristensen et al. untersuchte die Aussagen mehrerer Autoren zur Rezidivquote [79] und konnte eine durchschnittliche Rezidivrate von 11% bei Patienten ausmachen, welche mit radikaler Operationsmethode therapiert wurden, und einen Durchschnitt von 64% bei Personen, welche nur mit limitierter Tumorexzision behandelt wurden [79]. Die Durchschnittsrezidivrate der in Tabelle 37 angegebenen Studien beträgt 36,4%. Die Tendenz zur Rezidivierung in unserem Patientengut beträgt im Mittel 35,1% und liegt somit leicht unter den durchschnittlichen Literaturangaben. Diskussion 101 Tab. 37: Angaben zur Rezidivhäufigkeit des invertierten Papilloms in der Literatur Autor Outzen et al. [112] (1961) Hyams [64] (1971) Rudert [131] (1971) Snyder et al. [147] (1972) Suh et al. [153] (1977) Segal et al. [140] (1986) Weissler et al. [168] (1986) Peterson et al. [117] (1991) Lawson et al. [84] (1995) Klimek et al. [75] (2000) Kretschmar [78] (2000) Smith et al. [146] (2000) Pasquini et al. [113] (2004) Minovi et al. [101] (2006) Minovi et al. [102] (2006) Eigene Daten Fallzahl (n) 67 149 30 39 57 30 223 35 112 55 64 48 89 64 87 Rezidivrate (%) 6 48 67 49 27 50 52 77 14,3 18,2 37,5 39 15 9,4 10,2 77 35 In den meisten Fällen tritt das Tumorrezidiv im ersten bis zweiten Jahr des postoperativen Follow-up in Erscheinung [126, 153], in seltenen Fällen wurden aber auch von Tumorrezidiven nach 10 bis 24 Jahren berichtet [104]. In unserer Studie belief sich die Dauer bis zur Entstehung eines Rezidivs im Mittel auf 12,6 Monate, wobei die größte Zeitspanne bis zur Rezidivbildung 3 Jahre betrug. Mit Hilfe des Kaplan-Meier-Tests konnten wir darstellen, dass die Wahrscheinlichkeit, postoperativ rezidivfrei zu bleiben, im ersten postoperativen Jahr am rasantesten fällt und im zweiten Jahr des Follow-up im Vergleich dazu nur wenig sinkt. Die Wahrscheinlichkeit, auch im 3. postoperativen Jahr noch kein Rezidiv aufzuweisen, ist am geringsten und liegt nur noch bei ca. 60% (siehe hierzu auch Abb. 30). Die Frage, ob ein Zusammenhang zwischen Geschlecht und Rezidiven besteht, wird in der Literatur kontrovers diskutiert. In unserer Studie scheint die Wahrscheinlichkeit, ein Rezidiv zu entwickeln, nicht vom Geschlecht abzuhängen, wobei die männlichen Patienten eine Rezidivhäufigkeit von 21,9% aufwiesen und das weibliche Geschlecht mit einer prozentualen Wahrscheinlichkeit von 23,1% an einem Rezidivtumor erkrankten. Diskussion 102 Auch Kristensen et al. beschrieb keine Unterschiede in der Rezidivrate zwischen Männern und Frauen [79], wohingegen Suh et al. bei Frauen eine höhere Neigung zur Rezidiventwicklung beschrieb, während Snyder et al. dem männlichen Geschlecht eine höhere Tendenz zur Rezidivierung zusprach [147, 153]. Tab. 38: Beziehung zwischen Geschlecht und Rezidivrate in der Literatur Autor Kristensen et al. [79] Suh et al. [153] Snyder et al. [147] Eigene Daten * keine genauen Zahlenangaben Rezidivrate bei Frauen (%) Rezidivrate bei Männern (%) Keine Unterschiede* 40 23 13 31 23,1 21,9 In der Literatur wird ebenfalls häufig über die Lokalisation des Tumors als mögliche Ursache für Rezidive diskutiert. So spricht zum Beispiel Outzen et al. in seiner 1991 veröffentlichten Arbeit davon, dass es bei Tumorsitz am Septum nasi deutlich seltener zur Rezidiventstehung kommt, als bei anderen Lokalisationen [112]. Im Gegensatz dazu beschreibt Ridolfi et al. in seiner Publikation von 1977, dass das IP am Nasenseptum dazu prädestiniert sei, zu rezidivieren [125]. Häufig wird jedoch auch davon gesprochen, dass die Rezidivrate wesentlich bei Beteiligung der Nasennebenhöhlen steigt [78, 84]. In unserer Studie zeigten die invertierten Papillome des Septum nasi eine Rezidivwahrscheinlichkeit von 5,0%, bei Befall der Nasenhaupthöhle eine Tendenz von 11,8% und bei Ausdehnung in den Nebenhöhlen eine Rezidivhäufigkeit von 29,3%. Diskussion 103 Tab. 39: Beziehung zwischen Lokalisation und Rezidivierung verschiedener Publikationen Autor Outzen et al. [112] Rudert [131] Lawson et al. [84] Eigene Daten Lokalisationsort Septum Laterale Nasenwand Septum Laterale Nasenwand Nasennebenhöhlen Septum nasi Nasenhaupthöhle Nebenhöhlen Rezidivrate (%) 8 12 80 60 Signifikant höher* 5,0 11,8 29,3 Eine mögliche Erklärung, die sich für die geringe Häufigkeit der Rezidivierung von IPs am Septum bei der Studie von Outzen und Koautoren [111] und unseren Daten bietet, ist die leichtere operative Erreichbarkeit septaler Läsionen. Das Stroma ist am Septum wesentlich dünner als an anderen Orten der Nase und den Nebenhöhlen [64], so dass die beim invertierten Papillom ins Stroma hinabreichenden Epithelzapfen nicht so tief einwachsen können [78]. Damit bleibt die Größe des Tumors an sich beschränkt, was eine weitere Invasion in andere Nasenanteile verlangsamen könnte [78]. Die operative Resektion gestaltet sich daher als einfacher. Des Weiteren lässt sich die Vermutung aufstellen, dass die anatomischen Gegebenheiten des Septums das Auftreten von klinischen Symptomen beschleunigen. Da nämlich der direkte Luftstrom dem mittleren Nasengang folgend am Nasenseptum vorbei strömt, gibt eine dortige Läsion Anlass zu früher auftretenden Beschwerden wie zum Beispiel der Nasenatmungsbehinderung. Somit kann sich das Intervall zwischen erstem Auftreten der Symptome und der Diagnosestellung eines IP merklich verkürzen, wodurch der Tumor in seinem Initialstadium operiert werden kann [78]. Unterstützen lässt sich diese Vermutung auch durch die Tatsache, dass in unserer Studie 66,7% aller septaler Läsionen in Lokalanästhesie operiert wurden, da sie relativ kleine Tumoren in frühem Stadium waren (0,3-0,5 cm). Diskussion 104 4.12. Rezidive nach bestimmten Operationsmethoden Fast alle Autoren sind sich einig, dass grundsätzlich die radikaleren Operationstechniken wie zum Beispiel die laterale Rhinotomie oder die OP nach Caldwell-Luc, den weniger radikaleren Verfahren wie der einfachen lokalen Abtragung, in Bezug auf die Rezidivhäufigkeit überlegen sind [64, 78, 83, 111, 140]. So berichtet Nachtigal et al. beispielsweise von einer Rezidivrate nach konservativen Verfahren von 46,0% [105]. Im Vergleich dazu fand er nach Radikaloperationen eine Rezidivhäufigkeit von nur 2,9%. Kristensen et al. setzten sich 1985 kritisch mit den Publikationen mehrerer Autoren auseinander und errechneten nach limitierten Exzisionen eine Durchschnittsrezidivrate von 64%, wohingegen Rezidive nach Radikalresektionen nur durchschnittlich in 11% der Fälle auftraten [79]. In der Studie von Lawson et al. zeigten sich nach radikalen operativen Verfahren Tumorrezidive zu 14,9%, nach konservativen Methoden zu 12,2%. Er räumt aber ein, dass die radikal therapierten Patienten eine fast doppelt so lange Nachbeobachtungszeit hatten [83]. Lund & Lloyd recherchierten eine Rezidivrate von 8% nach endoskopischer Vorgehensweise und demgegenüber eine Häufigkeit von 21% nach radikalen IPExzisionen [91]. Raveh et al. [122] konnte in seiner Studie keinen Unterschied zwischen den beiden OPMethoden finden und gab für die Rezidive jeweils eine Prozentzahl von 22% an. Auch die von uns untersuchten Patienten zeigten nach konservativen Operationsmethoden eine etwas höhere Rezidivrate als nach Radikalresektionen (25,0% vs. 17,4%). Man sollte sich allerdings auch vor Augen halten, dass die Tumorrezidivrate nicht nur von der Operationstechnik alleine abhängt. Es spielen natürlich auch Faktoren wie zum Beispiel die Größe und Ausdehnung des IP sowie die Lokalisation eine wesentliche Rolle und sollten ebenfalls in eine solche Analyse miteinbezogen werden. Einige Lokalisationen sind primär bereits durch anatomische Verhältnisse mit einem höheren Rezidivrisiko belastet, wie beispielsweise der Sinus sphenoidalis oder hintere Strukturen des Sinus ethmoidalis [83, 140, 158]. Diskussion 105 Außerdem sollte bedacht werden, dass auch die Ausbildung und Erfahrung des Operateurs einen nicht unwichtigen Anteil an der postoperativen Neuentwicklung dieser Tumorentität darstellt. Tab. 40: Prozentuale Häufigkeiten von Rezidiven nach radikalen OPs im Vergleich zu konservativem Vorgehen Autor Nachtigal et al. [105] Kristensen et al. [79] Lawson et al. [84] Lund et al. [91] Raveh et al. [122] Cummings et al. [33] Trible et al. [160] Calcaterra et al. [26] Segal et al. [140] Waitz et al. [164] Lawson et al. [83] Radikale OP (%) 3 11 15 21 22 25 33 15 29 19 14 Konservative OP (%) 46 64 12 8 22 68 71 78 71 17 20 17,4 25,0 Eigene Daten Tab. 41: Häufigkeit der Rezidivbildung nach endoskopischem Vorgehen Autor Fallzahl (n) Waitz et al. [164] Stankiewicz et al. [151] McCary et al. [92] Lesperance et al. [88] Kaddour et al. [69] Lawson et al. [84] Raveh et al. [122] Thorp et al. [156] Han et al. [53] Schlosser et al. [135] Winter et al. [171] Sukenik et al. [154] Lund et al. [91] Tribel et al. [160] Chee et al. [29] Sham et al. [142] 35 15 7 13 19 15 9 2 19 21 67 19 13 33 18 22 Eigene Daten 32 Rezidivrate (%) Nachbeobachtungszeit (Monate) 17 46 33 36 0 19 8 12 0 35,5 20 24 22 26 0 36 10 50 19 42 22 53 21 30 8 45 15 12 6 33 27 33 25 23,4 Diskussion 106 4.13. Karzinomatöse Entartung des invertierten Papilloms Die karzinomatöse Entartung ist, wie auch die Frage nach der Rezidivierung, ein in der Literatur häufig diskutierter Sachverhalt. Auch hier findet sich eine große Spanne von Prozentangaben, welche zwischen 0% und 53% schwanken [175]. Dies erklärt sich nicht zuletzt aus der Tatsache, dass sich die meisten Prozentangaben auf Fallzahlen stützen, die deutlich unter 50 liegen und deshalb ein leicht verzerrtes Bild liefern könnten [37]. Realistisch ist wahrscheinlich eine Malignisierungsrate um 12,5%, die sich aus einer Zusammenstellung von insgesamt 1765 publizierten Fällen ergibt (Tab. 42). Bei unserem untersuchten Patientengut beläuft sich die mittlere Häufigkeit maligner Entartungen auf 10,4%, zeigt also kaum Abweichungen zu den Ergebnissen aus der Literatur. 1994 publizierte Vrabec drei Alternativen, wie sich ein Karzinom aus einem invertierten Papillom entwickeln könnte [163]: 1. Das Karzinom entwickelt sich aus einem primär benignen IP im Rahmen eines Rezidivs (metachron). 2. Das IP ist von Anfang an maligne mit unterschiedlichem Differenzierungsgrad. 3. Es besteht eine Koexistenz zwischen IP und Karzinom (synchron). Im klinischen Alltag werden die letzten beiden Formen häufiger gesehen [83], es wird jedoch auch darauf hingewiesen, dass sich die Unterscheidung von direkter Genese des Karzinoms aus dem IP und einer Koexistenz sehr schwierig gestalten kann, erst recht, wenn bei Erstmanifestation des IP bereits ein Karzinom vorliegt [78, 79, 93, 147]. Wir konnten in unseren Auswertungen 5 Fälle dem synchronen Geschehen zuordnen (6,5%) und 3 Fälle der metachronen Kategorie (3,9%). In der Literaturrecherche fand sich ein synchrones Auftreten von IP und Karzinomen in 78 von 990 Fällen (7,9%). Eine metachrone Malignisierung wurde bei 174 berichteten Rezidiv-IPs lediglich in 12 Fällen beschrieben (6,9%) [37]. Die eigenen Resultate stehen also in guter Übereinstimmung mit den Literaturangaben. Diskussion 107 Tab. 42: Literaturangaben zur Häufigkeit der Malignisierung invertierter Papillome Autor Vrabec [162] Lampertico et al. [82] Phillips et al. [118] Bielamowicz et al. [13] Christensen et al. [30] Yamagucchi et al. [175] Hyams et al. [65] Kristensen et al. [79] Arndt et al. [4] Obermann [106] Suh et al. [153] Weissler et al. [168] Dolgin et al. [39] Segal et al. [140] Fechner et al. [45] Waitz et al. [164] Lawson et al. [83] Bielamowicz et al. [13] Tribel et al. [160] Peterson et al. [117] Smith et al. [146] Outzen et al. [112] Willis [170] Myers et al. [104] Barnes [5] Abildgaard-Jensen et al. [1] Skolnik et al. [145] Mickelson et al. [100] Lesperance et al. [88] Dammann et al. [34] Roh et al. [128] Thorp et al. [156] Durchschnittliche Fallzahl in der Literatur Eigene Daten Fallzahl gesamt (n) 101 19 112 61 39 15 149 83 29 15 57 223 41 30 14 51 112 61 30 28 48 67 51 33 61 21 33 15 51 32 30 53 Zahl der Malignisierungen (n) 8 3 8 10 7 8 19 7 3 3 4 11 5 3 1 2 6 10 6 4 3 1 2 7 8 2 5 1 14 6 1 5 Häufigkeit (%) 8 16 7 16 18 53 13 8 10 20 7 5 12 10 7 2 5 16 20 14 6 1 2 21 13 9,5 15 7 27 18,7 3 9 8 10,4 56 77 Bei der Suche nach Ursachen oder Hinweisen für die Entstehung einer karzinomatösen Entartung konnten keine sicheren Kriterien ermittelt werden. Diskussion 108 Hyams und Delank finden beispielsweise keinen Zusammenhang zwischen Rezidivrate und Entartungshäufigkeit [37, 65]. Andere Autoren beobachteten dagegen eine Häufigkeit von metachroner Malignität von bis zu 50% aller Rezidive [163]. In unserer Studie finden wir metachrone Entartung mit einer Häufigkeit von 37,5% in Bezug auf alle 8 Karzinomfälle. Tab. 43: Literaturangaben zur Häufigkeit der Malignisierung bei Rezidiven invertierter Papillome (metachrone Malignität) Autor Fallzahl (n) gesamt Peter et al. [116] Lawson et al. [83] Benninger et al. [8] Vrabec [162] Weissler et al. [168] Outzen et al. [112] Christensen et al. [30] Waitz et al. [164] Dolgin et al. [39] Myers et al. [104] Smith et al. [146] 20 108 34 88 215 66 33 50 24 26 18 Eigene Daten 77 Zahl der Rezidivmalignen rate Entartungen, (%) gesamt (n) 6 30 16 14 5 15 4 5 103 48 7 11 11 33 9 18 5 21 1 4 7 41 8 35,06 Zahl der Häufigkeit metachronen (%) Malignität (n) 1 17 2 13 0 0 2 50 3 3 0 0 1 9 1 11 1 20 0 0 1 14 3 37,5 Das Geschlecht scheint keine wesentliche Rolle in der Entwicklung von Karzinomen auf dem Boden eines IP zu spielen [8, 168]. Jedoch scheint das Alter der Person, bei der sich das Wachstum eines Karzinoms zeigt, von Bedeutung zu sein. In der Studie von Benninger und Coautoren hatten die Personen mit Malignisierung ein mittleres Alter von 61 Jahren, die Patienten mit benignem IP waren dagegen durchschnittlich nur 52 Jahre alt [8]. Bei Bielamowicz et al. belief sich die Altersgruppe der malignen IP-Erkrankten ebenfalls auf 61 Jahre, die der benignen IP-Patienten war erst im 52. Lebensjahr [13]. Christensen errechnete für seine Studie ein Durchschnittsalter von 66 Jahren gegenüber 49 Jahren bei benignem IP [30]. Diskussion 109 Bei unseren untersuchten Patienten stellte sich heraus, dass die Personen, welche eine maligne Entartung entwickelten, im Mittel 66,6 Jahre waren, die Personen mit rein benignem IP waren dagegen nur durchschnittlich 59,8 Jahre alt. 4.14. Wahl der Operationstechnik bei karzinomatöser Entartung Im Falle einer malignen Entartung sollte von vorneherein eine ausgedehntere tumorchirurgische Therapie geplant werden [76, 88]. Dabei schließt die Tatsache der Malignisierung das endonasale Vorgehen nicht automatisch aus, vor allem dann, wenn kleinere maligne Tumoren vorliegen [76, 164]. In unserer Studie wurden 2 von 8 Patienten mit malignem Geschehen, welches am Vestibulum, bzw. im Sinus maxillaris lokalisiert war, erfolgreich auf rein endoskopischem Operationswege therapiert. Handelt es sich bei der bösartigen Läsion jedoch um eine sehr große Geschwulst oder befindet diese sich an schwer erreichbaren Nasenstrukturen, ist es meist ratsam, den endonasalen Zugang um eine von extern durchgeführte Technik zu erweitern, um eine bessere Einsicht in das Operationsgebiet zu gewährleisten [12, 142]. Zusammenfassung 5. 110 Zusammenfassung Das invertierte Papillom (IP) der Nase und Nasennebenhöhlen zählt zu den häufigsten primär benignen Tumoren, welche aufgrund der immernoch ungeklärten Ätiologie, des lokal destruktiven Wachstums, einer hohen Rezidivrate und eines in der Literatur unterschiedlich eingeschätzten Entartungspotentials, auch heute noch eine Herausforderung für den behandelnden HNO-Arzt darstellt. In einer retrospektiven Studie untersuchten wir aus einem Gesamtkollektiv von 2043 behandelten Patienten mit Papillomen 77 Fälle mit invertiertem Papillom der Nase und/oder Nasennebenhöhlen, die in unserer Klinik im Zeitraum von 1986 bis 2005 behandelt wurden. Darunter befanden sich 13 Frauen und 64 Männer. Das mittlere Alter lag bei 60,9 Jahren (Median 61 Jahre). Die meisten Tumoren waren in der Nasenhaupthöhle (n=68), dem Sinus ethmoidalis (n=39) und dem Sinus maxillaris (n=29) lokalisiert. Die Tumorausdehnung bestimmten wir entsprechend der Einteilung nach Krouse [80]. Die Therapie der Wahl ist die radikale operative Entfernung der Tumorentität. Aus dieser Arbeit ergibt sich für die Klinik und Praxis folgendes Fazit: 1. Das invertierte Papillom ist gekennzeichnet durch ein lokal destruierendes Wachstum, weshalb stets eine sogfältige präoperative Diagnostik wie das Röntgen der Nase und Nasennebenhöhlen oder die Computertomographie durchgeführt werden sollte, um die genaue Tumorausdehnung zu bestimmen und eventuelle knöcherne Infiltrationen zu erkennen und dies in die exakte Operationsplanung miteinzubeziehen. 2. Das invertierte Papillom hat eine Tendenz zur malignen Entartung. Deshalb sollte immer sowohl bei Operationen an invertierten Papillomen, als auch bei dessen häufigster Differentialdiagnose der Polyposis nasi, eine sorgfältige histologische Untersuchung des gesamten Resektats veranlasst werden. Bei histopathologischem Nachweis einer malignen Entartung oder hochgradiger Zelldysplasien ist meist eine onkochirurgische Revisionsoperation indiziert. 3. Das invertierte Papillom weist eine hohe Rate an Rezidivierungen auf, weshalb stets eine regelmäßige HNO-ärztliche Nachsorge betrieben werden sollte. Schlussfolgernd sollte in Anbetracht der hohen Rezidivrate, des lokal destruktiven Wachstums und der hohen Rate maligner Entartungen stets das therapeutische Konzept einer radikalen und funktionserhaltenden Nasen- und Nasennebenhöhlenchirurgie bei dieser tückischen Tumorentität verfolgt werden. Zusammenfassung 111 Literaturverzeichnis 6. 112 Literaturverzeichnis 1. Abildgaard-Jensen J, Greisen O (1985) Inverted papilloma of the nose and paranasal sinuses. Clin Otolaryngol 10: 135-143 2. Altug T, Sunar O, Bilgin H (1989) Das invertierte Papillom, Annahme einer Multizentrizität. Rev Laryngol Otol Rhinol (Bord) 110: 299-301 3. Appel W, Schulte-Mattler, K, Uhlenbrock D (1983) Invertiertes Papillom der Nase und Nasennebenhöhlen. Fortsch Röntgenstr 138: 322-330 4. Arndt O, Nottelmann K, Brock J, Neumann OG (1994) Das invertierte Papillom und seine Assoziation mit dem humanen Papillomavirus (HPV). HNO 42: 670-676 5. Barnes EL (1985) Surgical Pathology of the Head and Neck (Vol. 1). Marcel Dekker, New York, p. 411 6. Barzilai G, Greenberg E, Uri N (2005) Indications for the Caldwell-Luc approach in the endoscopic era. Otolaryngol Head Neck Surg 132: 219-220 7. Beck A, Kaiserling E, Rudert H, Beigel A (1984) Papilloma inversum of the nose and paranasal sinuses, Clinical aspects and histology of 22 personal cases. Laryngol Rhino Otol (Stuttgart) 63: 347-352 8. Benninger MS, Roberts JK, Sebek BA, Levine HL, Tucker HM, Lavertu P (1990) Inverted papillomas and associated squamous cell carcinomas. Otolaryngol Head Neck Surg 103: 457-461 9. Berendes J (1961) Das klinisch maligne Papillom der Nasennebenhöhlen. HNO 9: 265269 10. Berghaus A, Bloching M (1990) Tumoren und tumorähnliche Läsionen der Nase und der Nasennebenhöhlen. HNO-Praxis heute, Bd 16, Berlin, Heidelberg, New York, Tokyo, Springer Literaturverzeichnis 11. 113 Berry R, Bonnet H, Light R (1992) Effect of ethanol on the arousal response to airway occlusion during sleep in normal subjects. Am Rev Respir Dis 145: 445-452 12. Bertand B, Eloy P, Jorissen M (2000) Surgery of inverted papillomas under endoscopic control. Acta Otolaryngol Belg 54: 139-150 13. Bielamowicz S, Calcaterra T, Watson D (1993) Inverting papilloma of the head and neck, the UCLA update. Otolaryngol Head Neck Surg 109: 71-76 14. Biller H (1994) Inverting papilloma. In: Gates GA (Hrsg.) Current therapy in Otolaryngology, Head and Neck Surgery. St Louis, Year Book Inc, Mosby 398 15. Billroth T (1855) Über den Bau des Schleimpolypen. Reimer G, Berlin S 7 ff 16. Block AJ, Wynne JW, Boysen PG, Lindsey S, Martin C, Cantor B (1981) Menopause, medroxyprogesterone and breathing during sleep. Am J Med 70: 506-510 17. Blokmanis A (1994) Endoscopic diagnosis, treatment, and follow-up of the nose and sinuses. J Otolaryngol 23: 366-369 18. Boenninghaus H, Lenarz T (1986) Hals-Nasen-Ohrenheilkunde für Studierende der Medizin. 10. Auflage, Springer-Verlag 19. Bold EL, Wanamaker JR, Hughes GB, Rhee CK, Sebek BA, Kinney SE (1995) Adenomatous lesions of the temporal bone: immunohistochemical analysis and theories of histogenesis. Am J Otol 16: 146-152 20. Bonora M, Shields GI, Knuth SL, Bartlett J Jr, St John WM (1984) Selective depression by ethanol of upper airway respiratory motor activity in cats. Am Rev Respir Dis 130: 156-161 21. Brandsma JL, Abramson AL, Sciubba J (1987) Papillomavirus infection of the nose. Cancer Cell 5: 301-308 22. Brandwein M, Steinberg B, Thung S (1989) Human papillomavirus 6/11 and 16/18 in Schneiderian papillomas, a DNA in situ hybridization with human papillomavirus RNA Literaturverzeichnis 114 probes. Cancer 63: 1708-1713 23. Buchwald C, Franzmann MB, Tos M (1995) Sinonasal papillomas: a report of 82 cases in Copenhagen Country, including a longitudinal epidemiological and clinical study. Laryngoscope 105: 72-79 24. Büngner v. (1889) Über eine ausgedehnte Hornwarzengeschwulst der oberen Nasenhöhle. Langenbecks Arch 39 25. Busquets JM, Hwang PH (2006) Endoscopic resection of sinonasal inverted papilloma: a meta-analysis. Otolaryngol Head Neck Surg 134: 476-482 26. Calcaterra TC, Thompson JW, Paglia DE (1980) Inverting papilloma of the nose and paranasal sinuses. Laryngoscope 90: 53-60 27. Caldwell G (1893) Diseases of the accessory sinuses of the nose and an improved method of treatment for suppuration of the maxillary antrum. N Y Med J 58: 526 28. Califano J, Koch W, Sidransky D, Westra WH (2000) Inverted sinonasal papilloma: a molecular genetic appraisal of its putative status as a Precursor to squamous cell carcinoma. Am J Pathol 156: 333-337, 2000 29. Chee LW, Sethi DS (1999) The endoscopic management of sinonasal inverted papillomas. Clin Otolaryngol 24: 61-66 30. Christensen WN, Smith RR (1986) Schneiderian papillomas: a clinicopathologic study of 67 cases. Hum Pathol 17: 393-400 31. Clark GT, Blumenfeld I, Yoffee N, Peled E, Lavie P (1996) A crossover study comparing the efficacy of continuous positive airway pressure with anterior mandibular positioning devices on patients with obstructive sleep apnea. Chest 109: 1477-1483 32. Cooter MS, Charlton SA, Lafreniere D, Spiro J (1998) Endoscopic management of an inverted nasal papilloma in a child. Otolaryngol Head Neck Surg 118: 876-879 Literaturverzeichnis 33. 115 Cummings C, Goodman M (1970) Inverting papilloma of the nose and paranasal sinuses. Arch Otolaryngol 92: 445-449 34. Dammann F, Pereira P, Laniado M, Plinkert P, Lowenheim H, Claussen CD (1999) Inverted papilloma of the nasal cavity and the paranasal sinuses: using CT for primary diagnosis and follow-up. Am J Roentgenol 172: 543-548 35. DeFreitas J, Lucente FE (1988) The Caldwell-Luc procedure, institutional review of 670 cases: 1975-1985. Laryngoscope 98: 1297-3000 36. Deitmer T, Wiener C (1996) Is there an occupational etiology of inverted papilloma of the nose and sinuses? Acta Otolaryngol Stockholm 116: 762-765 37. Delank KW, Alberty J, Schröter D, Eltze E (2000) Diagnostik und Behandlungskonzepte bei sinunasalen invertierten Papillomen. Laryngorhinootologie 226-232 38. Ders (1888) Über Warzengeschwülste (Papillome) der Respirationsschleimhäute. Volkmanns Sammlungen, No. 315 39. Dolgin SR, Zaveri VD, Casiano RR, Maniglia AJ (1992) Different option for treatment of inverting papilloma of the nose and paranasal sinuses: a report of 41 cases. Laryngoscope 102: 231-136 40. Draf W, Berghaus A (1993) Tumoren und Pseudotumoren der frontalen Schädelbasis, ausgehend von der Nase, den Nasennebenhöhlen und dem Nasenrachenraum. Eur Arch Otorhinolaryngol, Suppl 1: 105-186 41. Dubin MG, Sonnenburg RE, Melroy CT, Ebert CS, Coffey CS, Senior BA (2005) Staged endoscopic and combined open/endoscopic approach in the management of inverted papilloma of the frontal sinus. Am J Rhinol 19: 442-445 42. Eavey RD (1985) Inverted papilloma of the nose and paranasal sinuses in childhood and adolescence. Laryngoscope 95: 17-23 43. Eggers G, Eggers H, Sander N, Kößling F, Chilla R (2005) Histological features and malignant transformation of inverted papilloma. Eur Arch Otorhinolaryngol 262: 263- Literaturverzeichnis 116 268 44. Fakhri S, Citardi MJ, Wolfe S, Batra PS, Prayson RA, Lanza DC (2005) Challengs in the management of sphenoid inverted papilloma. Am J Rhinol 19: 207-213 45. Fechner RE, Alford DO (1968) Inverted papilloma and squamous carcinoma. An unusual case. Arch Otolaryngol 88: 73-78 46. Ferlito A, Devaney KO, Rinaldo A (2004) Association between Schneiderian Papilloma of the Temporal Bone and Carcinoma. A Critical Review of the Literature. Acta Otolaryngol 124: 121-123 47. Flieder DB, Koss MN, Nicholson A, Sesterhenn IA, Patras RE, Travis WD (1998) Solitary pulmonary papillomas in adults: a clinicopathologic and in situ hybridization study of 14 cases combined with 27 cases in the literature. Am J Surg Pathol 22: 13281342 48. Furuta Y, Shinohara T, Sano K, Nagashima K, Inoue K, Tanaka K, Inuyama Y (1991) Molecular pathologic study of human papillomavirus infection in inverted papilloma and squamous cell carcinoma of nasal cavities and paranasal sinuses. Laryngoscope 101: 79-85 49. Gaffey MJ, Frierson HF, Weiss LM, Barber CM, Baber GB, Stoler MH (1996) Human papillomavirus and Epstein-Barr virus in sinonasal Schneiderian papillomas, an in situ hybridization and polymerase chain reaction study. Am J Clin Pathol 106: 475-482 50. Garavello W, Gaini RM (2006) Incidence of inverted papilloma in recurrent nasal polyposis. Laryngoscope 116: 221-223 51. Grevers G (1998) Benigne Tumoren der Nase und der Nasennebenhöhlen. Praktische Rhinologie. Urban und Schwarzenberg Verlag. S. 204-206 und S. 266- 269 52. Guedea F, Mendenhall WM, Parsons JT, Million RR (1991) The role of radiation therapy in inverted papilloma of the nasal cavity and paranasal sinuses. Int J Radiat Oncol Biol Phys 20: 777-780 Literaturverzeichnis 53. 117 Han JK, Smith TL, Loehrl T, Toohill RJ, Smith MM (2001) An evolution in the management of sinonasal inverting papilloma. Laryngoscope 111: 1395-1400 54. Hausen H (1991) Viruses in human cancers. Science 254: 1167-1173 55. Hellmann (1897) Papilloma durum der Nasen- und Stirnhöhlenschleimhaut. Übergang in Carcinom. A., f., L. (Behandelt einen von KIESSELBACH in Virchows Arch. Bd. 132 in seinen Anfängen geschilderten Fall) 56. Henson DE, Ries LA (1995) The relative survival rate. Cancer 76: 1687-1688 57. Herrold KM (1964) Epithelial papillomas of the nasal cavity, experimental induction in syrian hamsters. Arch Pathol 78: 189-195 58. Hochban W, Brandenburg U, Peter JH (1994) Surgical treatment of obstructive sleep apnea by maxillomandibular advancement. Sleep 17: 624-629 59. Hommerich KW (1977) Gutartige Geschwülste der Nase und der Nasennebenhöhlen. In: Berendes, R, Link, R, Zöllner, F (Hrsg.) Hals-Nasen-Ohrenheilkunde in Praxis und Klinik, Bd. 2, Thieme Verlag, Stuttgart 60. Hopmann (1883) Die papillären Geschwülste der Nasenschleimhaut. Virchows Arch 93 (Fall 15. S. 234) 61. Hosemann W (1996) Die endonasale Chirurgie der Nasennebenhöhlen- Konzepte, Techniken, Ergebnisse, Komplikationen, Revisionseingriffe. Eur Arch Otorhinolaryngol, Suppl 1: 165-269 62. Hudgel DW, Hendricks C (1988) Palate and hypopharynx, sites of inspiratory narrowing of the upper airway during sleep. Am Rev Respir Dis 138: 1542-1547 63. Hulett KJ, Stankiewicz JA (2004) Primary sinus surgery. In: Cummings CW et al. (eds.): Otolaryngology Head and Neck Surgery. Eslevier Mosby, Philadelphia, 4. Auflage, S. 1229-1254 Literaturverzeichnis 64. 118 Hyams VJ (1971) Papillomas of the nasal cavity and paranasal sinuses: A clinicopathological study of 315 cases. Ann Otol Rhinol Laryngol 80: 192-206 65. Hyams VJ, Batsakis JG, Micheals L (1988) Papilloma of the upper respiratory tract. In: Atlas of Tumor Pathology, Second Series, Fascicle 25: Tumors of the upper respiratory tract and ear. Armed Forces Institut of Pathology, Washington, D.C., S. 34-44 66. Jäger L, Günther E, Gauger J, Nitz W, Kastenbauer E, Reiser M (1996) Funktionelle MRT des Pharynx bei obstruktiver Schlafapnoe mit schnellen 2D-FLASH-Sequenzen. Radiologe 36: 245-253 67. Jahnke V (1971) The fine structure of intranasal papillomas. Ann Otol Rhinol Laryngol 80: 78-82 68. Jessen M, Fryksmark U (1993) Is there a relationship between the degree of nasal obstruction and snoring? Clin Otolaryngol 18: 485-487 69. Kaddour HS, Woodhead CJ (1992) Transitional papilloma of the middle ear. J Laryngol Otol 106: 628-629 70. Kamel R, Khaled A, Kandil T (2005) Inverted papilloma: new classification and guidelines for endoscopic surgery. Am J Rhinol 19: 358-364 71. Kapadia SB, Barnes L, Pelzman K, Mirani N, Heffner DK, Bedetti C (1993) Carcinoma ex oncocytic Schneiderian (cylindrical cell) papilloma. Am J Otolaryngol 14: 332-338 72. Kaplan EL, Meier P (1958) Nonparametric estimation from incomplete observations. J Am Stat Assoc 53: 457-481 73. Katori H, Tsukuda M (2005) Staging of surgical approach of sinonasal inverted papilloma. Auris Nasus Larynx 32: 257-263 74. Kelly JH, Joseph M, Carroll E, Goodman ML, Pilch BZ, Levinson RM, Strome M (1980) Inverted Papilloma of the nasal septum. Arch Otolaryngol 106: 767-771 75. Klimek T, Atai E, Schubert M, Glanz H (2000) Inverted papilloma of the nasal cavity and paranasal sinuses: clinical data, surgical strategy and recurrence rate. Acta Literaturverzeichnis 119 Otolaryngol 120: 267-272 76. Kraft M, Simmen D, Kaufmann T, Holzmann D (2003) Long-term results of endonasal sinus surgery in sinonasal papillomas. Laryngoscope 113: 1541-1547 77. Kramer, Som (1935) True papilloma of the nasal cavity. Arch Otolaryngol 22: 24-43 78. Kretschmar G (2000) Invertierte Papillome der Nase und Nasennebenhöhlen. Klinische, histologische und immunhistochemische Untersuchungen. Inaugural-Dissertation, Ernst-Moritz-Arndt-Universität Greifswald 79. Kristensen S, Vorre P, Elbrond O, Sogaard H (1985) Nasal schneiderian papillomas: a study of 83 cases. Clin Otolaryngol Allied Sci 10: 125-134 80. Krouse JH (2000) Development of a staging system for inverted papilloma. Laryngoscope 110: 965-968 81. Krouse JH (2001) Endoscopic treatment of inverted papilloma, safety and efficacy. Am J Otolaryngol 22: 87-99 82. Lampertico P, Russell WO, MacComb WS (1963) Squamous papilloma of the upper respiratory epithelium. Arch Pathol Lab Med 7: 293-302 83. Lane AP, Bolger WE (2006) Endoscopic management of inverted papilloma. Curr Opin Otolaryngol Head Neck Surg 14: 14-18 84. Lawson W, Ho BT, Shaari CM, Biller HF (1995) Inverted papilloma, a report of 112 cases. Laryngoscope 105: 282-288 85. Lawson W, Kaufmann MR, Biller HF (2003) Treatment outcomes in the management of inverted papilloma: an analysis of 160 cases. Laryngoscope 113: 1548-1556 86. Lehmann R (1949) Papillary sinusitis. Ann Otol 58: 507 87. Lenarz T (1992) Midfacial Degloving, ein alternativer Zugangsweg zur Frontobasis, der Nasenhaupt- und der Nasennebenhöhlen. Laryngorhinootologie 71: 381-387 Literaturverzeichnis 88. 120 Lesperance MM, Esclamado RM (1995) Squamous cell carcinoma arising in inverted papilloma. Laryngoscope 105: 178-183 89. Loebell G (1964) Über das Papillom der Nase und Nasennebenhöhlen. Mschr Ohrenheilk 98: 54-57 90. Luhn JP, Hörmann K (2002) Das invertierte Papillom, Eine pathohistologische und klinische Analyse. HNO-Abteilung AK Barmbek. Rübenkamp 148, 2000 Hamburg 60 91. Lund VJ, Lloyd GA (1984) Radiological changes associated with inverted papilloma of the nose and paranasa sinuses. Br J Radiol 57: 455-461 92. Maitra A, Baskin BL, Lee EL (2001) Malignancies arising in oncocytic schneiderian papillomas: a report of 2 cases and review of the literature. Arch Pathol Lab Med 125: 1365-1367 93. Majumdar B, Beck S (1984) Inverted papilloma of the nose. Some aspects of etiology. J Laryngol Otol 98: 467-470 94. Margaritora S, Cesario A, Galetta D, Porziella V, Mule A, Granone P (2004) Pulmonary inverted schneiderian papilloma. Ann Thorac Surg 77: 1845-1846 95. McCary WS, Gross CW, Reibel JF, Cantrell RW (1994) Preliminary report: endoscopic versus external surgery in the management of inverting papilloma. Laryngoscope 104: 415-419 96. McLachlin CM, Kandel RA, Colgan TJ, Swanson DB, Witterick IJ, Ngan BY (1992) Presence of human papillomavirus in sinonasal papillomas, a study using Poymerase Chain Reaction and in situ Hybridization. Mod Pathol 5: 406-409 97. McNicholas WT, Coffey M, Boyle T (1993) Effects of nasal airflow on breathing during sleep in normal humans. Am Rev Respir Dis 147: 620-623 98. Mendenhall WM, Million RR, Cassisi NJ, Pierson KK (1985) Biologically aggressive papillomas of the nasal cavity, the role of radiation therapy. Laryngoscope 95: 344-347 Literaturverzeichnis 99. 121 Messerklinger W (1958) Die Schleimhaut der oberen Luftwege im Hinblick neuerer Forschungen. Arch Klin Exp Ohr- Nasen- und Kehlkopfheilkunde 173 100. Mickelson SA, Rosenthal LD, Rock JP, Senior BA, Friduss ME (1995) Obstructive sleep apnea syndrome and acromegaly. Otolaryngol Head Neck Surg 111: 362-366 101. Minovi A, Kollert M, Draf W, Bockmühl U (2006) Endonasale mikro-endoskopische Resektion invertierter Papillome der Nase und ihrer Nebenhöhlen. Laryngorhinootologie 85: 421-425 102. Minovi A, Kollert M, Draf W, Bockmühl U (2006) Inverted papilloma: feasibility of endonasal surgery and long-term results of 87 cases. Rhinology 44: 205-210 103. Momose KJ, Weber AL, Goodman ML (1980) Papilloma. Radiology 134: 73-79 104. Myers EN, Fernau JL, Johnson JT, Tabet JC, Barnes EL (1990) Management of inverted papilloma. Laryngoscope 100: 481-490 105. Nachtigal D, Yoskovitch A, Frenkiel A, Braverman I, Rochon L (1999) Unique characteristics of malignant schneiderian papilloma. Otolaryngol Head Neck Surg 121: 766-771 106. Oberman HA (1964) Papillomas of the nose and paranasal sinuses. Am J Clin Pathol 42: 245-258 107. Oikawa K, Furuta Y, Oridate N, Nagahashi T, Homma A, Ryu T, Fukuda S (2003) Preoperative staging of sinonasal inverted papilloma by magnetic resonance imaging. Laryngoscope 113: 1983-1987 108. Ojiri H, Ujita M, Tada S, Fukuda K (2000) Potentially distinctive features of sinonasal inverted papilloma on MR imaging. Am J Roentgenol 175: 465-468 109. Ormerod F (1952) Cylindrical-cell carcinoma of the nose. Acta Otolaryngol 100: 84-97, 1952 Literaturverzeichnis 110. 122 Osguthorpe JD, Weisman RA (1991) Medial maxillectomy for lateral nasal wall neoplasms. Arch Otolaryngol Head Neck Surg 117: 751-756, 111. Outzen KE, Grontved A, Jorgensen K, Clausen PP (1961) Inverted papilloma of the nose and paranasal sinuses, a study of 67 patients. Clin Otolaryngol Allied Sci 16: 309312 112. Outzen KE, Grontveld A, Jorgensen K, Clausen PP, Ladefoged C (1996) Inverted papilloma: incidence and late results of surgical treatment. Rhinology 34: 114-118 113. Pasquini E, Sciarretta V, Farneti G, Modugno GC, Ceroni AR (2004) Inverted papilloma: report of 89 cases. Am J Otolaryngol 25: 178-185 114. Patton TJ, Thawley SE, Waters RC, Vandermeer PJ, Ogura JH (1983) Expansion hyoidplasty: a potential surgical procedure designed for selected patients with obstructive sleep apnea syndrome, experimental canine results. Laryngoscope 93: 13871396 115. Perzin KH, Lefkowitch JH, Hui RM (1981) Bilateral nasal squamous carcinoma arising in papillomatosis: report of a case developing after chemotherapy for leukemia. Cancer 48: 2375-2382 116. Peter B, Grossenbacher R (1997) Invertierte Papillome der Nase und deren Nebenhöhlen. Laryngorhinootologie 76: 14-18 117. Peterson IM, Heim C (1991) Inverted squamous papilloma with neuro-ophtalmic features. J Clin Neuroophtalmol 11: 35-38 118. Phillips PP, Gustafson RO, Facer GW (1990) The clinical behavior of inverted papillomas of the nose and paranasal sinuses: report of 112 cases and review of the literature. Laryngoscope 100: 463-469 119. Plinkert PK, Zenner HP (1996) Transfazialer Zugang, kraniofaziale Resektion und Midfacial degloving bei der Chirurgie bösartiger Tumoren der vorderen Schädelbasis und der angrenzenden Nasennebenhöhlen. HNO 44: 192-200 Literaturverzeichnis 120. 123 Price JC (1986) The midfacial degloving approach to the central skull-base. Ear Nose Throat J 65: 46-53 121. Price JC, Holliday MJ, Johns ME, Kennedy DW, Richtsmeier WJ, Mattox DE (1988) The versatile midface degloving approach. Laryngoscope 98: 291-295 122. Raveh E, Feinmesser R, Shpitzer T, Yaniv E, Segal K (1996) Inverted papilloma of the nose and paranasal sinuses, a study of 56 cases and review of the literature. Isr J Med Sci 32: 1163-1167 123. Respler DS, Jahn A, Pater A, Pater MM (1987) Isolation and characterization of papillomavirus DNA from nasal inverting (schneiderian) papillomas. Ann Otol Rhinol Laryngol 96: 170-173 124. Riede UN, Schaefer HE (1999/2001) Allgemeine und spezielle Pathologie, 4. Auflage, aktualisierter Nachdruck. Georg Thieme Verlag Stuttgart-New York, S. 380 und 594 125. Ridolfi RL, Lieberman PH, Erlandson RA, Moore OS (1977) Schneiderian papillomas: a clinicopathologic study of 30 cases. Am J Surg Pathol 1: 43-53 126. Ringertz N (1938) Pathology of malignant tumors arising in the nasal and paranasal cavities and sinuses. Acta Otolaryngol (Stockholm) Suppl. XXVII 127. Roberts WH, Dinges DL, Hanly MG (1993) Inverted papilloma of the middle ear. Ann Otol Rhinol Laryngol 102: 890-892 128. Roh HJ, Procop GW, Batra PS, Citardi MJ, Lanza DC (2004) Inflammation and pathogenesis of inverted papilloma. Am J Rhinol 18: 65-74 129. Romashko AA, Stankiewicz JA (2005) Routine histopathology in uncomplicated sinus surgery: is it necessary? Otolaryngol Head Neck Surg 132: 407-12 130. Rothfeld P, Shapiro R, Lasser A, Kent D (1977) Epithelial (inverted) papilloma: a correlated radiological-histological study. Clin Radiol 28: 539-544 Literaturverzeichnis 131. 124 Rudert H (1971) Klinischer und histologischer Beitrag zum Papilloma inversum der Nase und Nasennebenhöhlen. Arch Klin Exp Ohren Nasen Kehlkopfheilkd 200: 15-33 132. Sachs ME, Conley J, Rabuzzi DD, Blaugrund S, Price J (1984) Degloving approach for total excision of inverted papilloma. Laryngoscope 94: 1595-1598 133. Savy L, Lloyd G, Lund VJ, Howard D (2000) Optimum imaging for inverted papilloma. J Laryngol Otol 114: 891-893 134. Schipper J, Ridder GJ, Aschendorff A, Klenzner T, Arapakis I, Maier W (2004) Verbessert die computergestützte Navigation in der endonasalen Nasennebenhöhlenchirurgie die Prozess- und die Ergebnisqualität? Laryngorhinootologie 83: 298-307 135. Schlosser RJ, Mason JC, Gross CW (2001) Aggressive endoscopic resection of inverted papilloma: An update. Otolaryngol Head Neck Surg 125: 49-53 136. Schneider D (1976) Ein Vorschlag zur Einteilung des invertiert wachsenden Papilloms der Nasennebenhöhlen. Laryngol Rhinol Otol (Stuttg) 55: 894-896 137. Schuss U (1999) Das Papilloma inversum von Nase und Nasennebenhöhlen. In: Ganz H, Iro H (Hrsg.) HNO-Praxis heute. Bd 19, Berlin, Heidelberg, New York, Tokyo, Springer 41 138. Schwab W, Schmeisser KJ, Steinhoff HJ, Mang WL (1985) Instructions for the documentation of neoplasms in the area of the head and neck following the TNM system. HNO 33: 337-348 139. Schwenn (1901) Ein Beitrag zur Lehre von den bösartigen Geschwülsten der Nebenhöhlen der Nase. A f L 11 (Fall 5) 140. Segal K, Atar E, Mor C, Har-El G, Sidi J (1986) Inverting papillomas of the nose and paranasal sinuses. Laryngoscope 4: 394-398 141. Sessions RB, Larson DL (1977) En bloc ethmoidectomy and medial maxillectomy. Arch Otolaryngol 103: 195-202 Literaturverzeichnis 142. 125 Sham CL, Woo JK, van Hasselt CA (1998) Endoscopic resection of inverted papilloma of the nose and paranasal sinuses. J Laryngol Otol 112: 758-764 143. Shanmugaratnam K (1991) Epithel tumors and precancerous lesion. In: K. Shanmugaratnam (Ed.), Histological typing of tumors of the upper respiratory tract [WHO-International Histological Classification of Tumors. Second Edition, Series No. 19] Springer Verlag, Berlin, Heidelberg S. 20-21 144. Simmen D, Jones N (2005) Chirurgie der Nasennebenhöhlen und der vorderen Schädelbasis. Thieme Verlag, Stuttgart, 1. Aufl. 145. Skolnik EM, Loewy A, Friedman JE (1966) Inverted papilloma of the nasal cavity. Arch Otolaryngol 84: 61-67 146. Smith O, Gullane PJ (2000) Inverting papilloma of the nose: analysis of 48 patients. J Otolaryngol 16: 154-156 147. Snyder RN, Perzin KH (1972) Papillomatosis of the nasal cavity and paranasal sinuses (inverted papilloma, squamous papilloma). Cancer 30: 668-690 148. Sofferman RA (1988) The septal translocation procedure: an alternative to lateral rhinotomy. Otolaryngol Head Neck Surg 98: 18-25 149. Stammberger H (1983) Aspekte zur Genese des invertierten Papilloms. Laryngol Rhinol Otol 62: 249 und 422 150. Stammberger H (1983) Neue Aspekte zur Genese des invertierten Papilloms, zweite Mitteilung, Vergleichende Untersuchungen. Laryngorhinootologie 62: 422-426 151. Stankiewicz JA, Girgis SJ (1993) Endoscopic surgical treatment of the nasal and paranasal sinus inverted papilloma. Otolaryngol Head Neck Surg 109: 988-995 152. Stone DM, Berktold RE, Ranganathan C, Wiet RJ (1987) Inverted papilloma of the middle ear and mastoid. Otolaryngol Head Neck Surg 97: 416-418 Literaturverzeichnis 153. 126 Suh KW, Facer GW, Devine KD, Weiland LH, Zujko RD (1977) Inverting papilloma of the nose and paranasal sinuses. Laryngoscope 87: 35-46 154. Sukenik MA, Casiano R (2000) Endoscopic maxillectomy for inverted papillomas of the paranasal sinuses, value of the intraoperative endoscopic examination. Laryngoscope 110: 39-42 155. Syrjanen S, Happonen RP, Virolainen E, Siivonen L, Syrjanen K (1987) Detection of human papillomavirus (HPV) structural antigens and DNA types in inverted papillomas and squamous cell carcinomas of the nasal cavities and paranasal sinuses. Acta Otolaryngol 104: 334-341 156. Thorp MA, Oyarzabal-Amigo MF, du Plessis JH, Sellars SL (2001) Inverted papilloma: a review of 53 cases. Laryngoscope 111: 1401-1405 157. TNM Klassifikation maligner Tumoren. (1999) UICC, Springer Verlag, Berlin Heidelberg, 6. Aufl. 158. Tolsdorff P, Müller R, Bechtelsheimer H (1972) Das invertierte Papillom der Nasen und Nasennebenhöhlen – Klinik und Pathologie. Z Laryngol Rhinol Otol 51: 573-590 159. Tomenzoli D, Castelnuovo P, Pagella F, Berlucchi M, Pianta L, Delu G, Maroldi R, Nicolai P (2004) Different endoscopic surgical strategies in the management of inverted papilloma of the sinonasal tract: experience with 47 patients. Laryngoscope 114: 193200 160. Tribel WM, Lekagul S (1971) Inverting papilloma of the nose and paranasal sinuses: Report of 30 cases. Laryngoscope 81: 663-668 161. Van Camp C, Clement PA (1994) Results of oral staroid treatment in nasa polyposis. Rhinology 32: 5-9 162. Vrabec DP (1975) The inverted Schneiderian papilloma: a clinical and pathological study. Laryngoscope 85: 186-220 Literaturverzeichnis 163. 127 Vrabec DP (1994) The inverted schneiderian papilloma: a 25-year study. Laryngoscope 104: 582-605, 1994 164. Waitz G, Wigand ME (1992) Results of endoscopic sinus surgery for the treatment of inverted papillomas. Laryngoscope 102: 917-922 165. Ward N (1854) Follicular tumour involving the nasal bones, nasal processes of superior maxillary bone and the septum of the nose, removal, death from pneumonia, autopsy. Lancet 2: 480-482 166. Weber RS, Shillitoe EJ, Robbins KT, Luna MA, Batsakis JG, Donovan DT, AdlerStorthz K (1988) Prevalence of human papillomavirus in inverted papillomas of the nose. Arch Otolaryngol Head and Neck Surg 114: 23-26 167. Weiner JS, Sherris D, Kasperbauer J, Lewis J, Li H, Persing D (1999) Relationship of human papillomavirus to Schneiderian papillomas. Laryngoscope 109: 21-26 168. Weissler MC, Montgomery WW, Turner PA, Montgomery SK, Joseph MP (1986) Inverted papilloma. Ann Rhinol Laryngol Otol 95: 215-221 169. Westhofen M, Weber C, Grzyska U (2001) Hals-Nasen-Ohrenheilkunde systematisch. 1. Auflage, Uni-Med Verlag AG, Bremen-London-Bosten 170. Willis R (1960) Pathology of tumours. London, Butterworth and company, pp 360-366 171. Winter M, Rauer RA, Göde U, Waitz G, Wigand ME (2000) Invertierte Papillome der Nase und ihrer Nebenhöhlen, Langzeitergebnisse nach endoskopischer endonasaler Resektion. HNO 48: 568-572 172. Wolff (1907) Zur Histologie der gutartigen Nasentumoren. M f O S. 431 173. Woodruff WW, Vrabec DP (1994) Inverted papilloma of the nasal vault and paranasal sinuses, spectrum of CT findings. Am J Roentgenol 162: 419-423 174. Wormald PJ, Ooi E, van Hasselt CA, Nair S (2003) Endoscopic removal of sinonasal inverted papilloma including endoscopic medial maxillectomy. Laryngoscope 113: 867- Literaturverzeichnis 128 873 175. Yamaguchi KT, Shapshay SM, Incze JS, Vaughan CW, Strong MS (1979) Inverted papilloma and squamous cell carcinoma. J Otolaryngol 8: 171-178 176. Yoskovitch A, Frenkiel S, Franco E, Coutlee F, Nachtigal D, Rochon L (2001) Analysis of human Papillomavirus in schneiderian papillomas as compared to chronic sinusitis and normal nasal mucosa. J Otolaryngol 30: 167-172 177. Yousem DM, Fellows DW, Kennedy DW, Bolger WE, Kashima H, Zinreich SJ (1992) Inverted papilloma: evaluation with MR imaging. Radiology 185: 501-505 Anhang 7. 129 Anhang Abkürzungsverzeichnis a Abb abschwell. Sprays bds C2 ca CA chron cm CT d Deglov Dissec DNA EBV et al. etc HCG H&E HNO HPV IP ITN i.v. KBH KH LA li. M m Max. Min. Mon MRT N n NAB NBZ NHH NNH OP PE PEC p.o. anno = Jahr Abbildung abschwellende Nasensprays beidseits C2H5OH = Äthylalkohol circa Karzinom chronisch Centimeter Computertomographie dies = Tag Midfacial Degloving Dissektion Desoxyribonukleinsäure Epstein Barr Virus et alteri et cetera Humanes Choriogonadotropin Hämatoxylin-Eosin Hals-Nasen-Ohrenheilkunde Humanes Papillomavirus invertiertes Papillom Intubationsnarkose intravenös Keilbeinhöhle Kieferhöhle Lokalanästhesie links Metastasen männlich Maximum Minimum Monate Magnetresonanztomographie Lymphknotenbefall numerus = Fallzahl Nasenatmungsbehinderung Nachbeobachtungszeit Nasenhaupthöhle Nasennebenhöhle Operation Probeexzision Plattenepithelkarzinom per os Anhang re. Rez SB SH SPSS Stat t T Univ.-HNO-Klinik usw w WHO 130 rechts rezidivierend/Rezidiv Siebbein Stirnhöhle Statistical Program for Social Sciences stationär tempore = Zeit Tumorstadium Universitätsklinik für Hals-Nasen-Ohrenheilkunde und so weiter weiblich World Health Organization Anhang 131 Curriculum vitae 1. Angaben zur Person: Name : Behringer Vorname : Stefanie Geburtstag : 27.01.1980 Geburtsort : Villingen Staatsangehörigkeit : Deutsch Familienstand : ledig Eltern : Ulrike Behringer Erich Behringer Geschwister : Daniela Behringer 2. Schulausbildung: 1986-1989 : Eichendorff-Grundschule, Donaueschingen 1989-1990 : Kreuzecker-Grundschule, Schwäbisch Hall 1990-2000 : Fürstenberg-Gymnasium, Donaueschingen 3. Studium: Seit 2000 : Studium der Medizin an der Albert-Ludwigs-Universität in Freiburg 2002 : Ärztliche Vorprüfung 2003 : Erster Abschnitt der Ärztlichen Prüfung 2006 : Zweiter Abschnitt der Ärztlichen Prüfung Anhang 132 4. Publikationen: Abstracts 1. Behringer S, Kayser G, Boedeker CC, Ridder GJ Das invertierte Papillom der Nase und Nasennebenhöhlen. Klinik, Diagnostik und Therapieergebnisse. HNO Informationen (Abstract) 2: 179, 2005 2. Behringer S, Kayser G, Boedeker CC, Ridder GJ Inverted papillomas of the nasal cavity and paranasal sinuses : cinical and diagnostic aspects and therapeutic results. Ger Med Sci (Abstract) (05hno668) 2005 3. Ridder GJ, Behringer S, Boedeker CC, Kayser G Recurrence, malignant transformation and therapeutic options in sinonasal inverted papillomas: Results of a retrospective study. Skull Base (Abstract) 15 Suppl 2: 47, 2005 Poster 1. Behringer S, Kayser G, Boedeker CC, Ridder GJ Das invertierte Papillom der Nase und Nasennebenhöhlen. Klinik, Diagnostik und Therapieergebnisse. 76. Jahresversammlung der Deutschen Gesellschaft für Hals-Nasen-Ohren-Heilkunde, Kopfund Hals-Chirurgie. Poster, Erfurt, 4. – 8. Mai 2005 2. Ridder GJ, Behringer S, Boedeker CC, Kayser G Recurrence, malignant transformation and therapeutic options in sinonasal inverted papillomas: Results of a retrospective study. 7th Congress of the European Skull Base Society und 13. Kongress der Deutschen Gesellschaft für Schädelbasischirurgie. Poster, Fulda, 18. – 21. Mai 2005 Anhang 3. 133 Behringer S, Boedeker CC, Kayser G, Ridder GJ Maligne transformierte invertierte Papillome der Nase und Nasennebenhöhlen: Klinische Befunde und Therapiestrategien. 89. Jahrestagung der Vereinigung Südwestdeutscher Hals-Nasen-Ohrenärzte. Poster, Ulm, 30.09. – 2. Oktober 2005 Vorträge 1. Behringer S, Kayser G, Boedeker CC, Ridder GJ Das invertierte Papillom der Nase und Nasennebenhöhlen. Klinik, Diagnostik und Therapieergebnisse. 76. Jahresversammlung der Deutschen Gesellschaft für Hals-Nasen-Ohren-Heilkunde, Kopfund Hals-Chirurgie. Vortrag, Erfurt, 08.05.2005 2. Ridder GJ, Behringer S, Boedeker CC, Kayser G Recurrence, malignant transformation and therapeutic options in sinonasal inverted papillomas: Results of a retrospective study. 7th European Skull Base Society Congress und 13. Kongress der Deutschen Gesellschaft für Schädelbasischirurgie.. Vortrag, Fulda, 20.05.2005 3. Ridder GJ, Behringer S, Boedeker CC, Schipper J Lokalisations- und stadienadaptierte Therapiestrategien beim invertierten Papillom der Nase und Nasennebenhöhlen: Endonasale oder extranasale Operationszugänge? 14. Jahrestagung der Deutschen Gesellschaft für Schädelbasischirurgie. Vortrag, Freiburg, 10.11.2006 Buchbeiträge 1. Ridder GJ, Behringer S, Kayser G, Boedeker CC Inverted Papillomas of the nasal cavity and the paranasal sinuses: Clinical aspects, diagnosis and therapeutic results. (im Druck) Anhang 134 Danksagung Mein besonderer Dank gilt Herrn Priv.-Doz. Dr. med. Gerd J. Ridder, nicht nur für die Bereitstellung des Themas und die außerordentlich kompetente Führung, sowohl während der Forschungsarbeit, als auch während der Verfassung meiner schriftlichen Arbeit, sondern auch für die stets sehr gute persönliche Betreuung und die zahlreichen Ratschläge über die Dissertation hinaus. Seine nachhaltige Unterstützung machte einen zügigen Beginn und ein baldiges Fertigstellen der Arbeit möglich. Des Weiteren schulde ich ihm Dank für die Verwirklichung einiger Publikationen und für die Ermöglichung der aktiven Teilnahme an der 76. Jahresversammlung der Deutschen Gesellschaft für Hals-Nasen-Ohren-Heilkunde, Kopfund Hals-Chirurgie e.V. und an der 89. Jahrestagung der Vereinigung Südwestdeutscher HalsNasen-Ohrenärzte e.V. Für sein mir entgegengebrachtes Vertrauen kann ich mich nicht genug bedanken. Danken möchte ich Herrn Prof. Dr. med. Dr. h.c. Roland Laszig, Direktor der Univ.-HNOKlinik Freiburg, für die Erlaubis zur Akteneinsicht und Datenauswertung. Einen nicht unerheblichen Anteil am Gelingen dieser Dissertation hat Herr Dr. med. Gian Kayser, Pathologisches Institut, dem ich herzlich danken möchte für die tatkräftige Unterstützung bei der Patientenrekrutierung, Diskussion histopathologischer Befunde sowie die freundliche Bereitstellung einiger Abbildungen. Darüber hinaus bedanke ich mich vielmals bei Herrn Dr. med. Carsten C. Boedeker für die Hilfe beim Sammeln klinischer Informationen und die Mithilfe und Korrektur englischsprachiger Publikationstexte. Ein stets angenehmes und freundliches Arbeitsklima durfte ich in der gesamten Abteilung für Hals-Nasen-Ohren-Heilkunde erfahren, hierfür danke ich auch den ärztlichen Kolleginnen und Kollegen, die mir jederzeit Einblick in aktuelle Krankenakten gewährt haben. Zuletzt danke ich meiner Mutter Ulrike Behringer, meiner Schwester Daniela Behringer und meiner Oma Elsbeth Kemperdick für den seelischen Rückhalt und die moralische Unterstützung, ohne die ich nie soweit gekommen wäre.