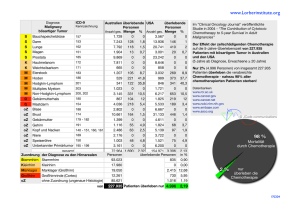
Konzept der zytoreduktiven Chirurgie (CRS)
Werbung

Konzept der zytoreduktiven Chirurgie (CRS) und hyperthermen intraperitonealen Chemotherapie (HIPEC) Gabriel Glockzin Klinik und Poliklinik für Chirurgie Universitätsklinikum Regensburg Mögliche Indikationen für CRS und HIPEC • Peritonealkarzinose bei Kolonkarzinom • Pseudomyxoma peritonei • Peritonealkarzinose bei Magenkarzinom • Malignes peritoneales Mesotheliom • Peritonealkarzinose bei Ovarialkarzinom • Peritoneale Sarkomatose • Adjuvante HIPEC (nach R0-Resektion bei KRK, MK) • Palliative HIPEC bei malignem Aszites • Seltene Entitäten (CUP, NET etc.) Das multimodale Konzept • Der chirurgische Eingriff bei peritonealer Metastasierung ist als integraler Bestandteil eines multimodalen Therapiekonzeptes zu verstehen, das sich aus kompletter makroskopischer Zytoreduktion (CC-0/1), hyperhermer intraperitonealer Chemotherapie (HIPEC) und systemischer Chemotherapie zusammensetzt. 1 2 3 CC-0/1 HIPEC sCTx Konzept der CRS und HIPEC - Zytoreduktive Chirurgie - • Entfernung aller sichtbaren intraperitonealen Tumormassen im Sinne einer kompletten makroskopischen Zytoreduktion (CC-0/1) Glockzin et al. Chirurg 2007 Chirurgische Technik • scharfe Dissektion – Pinzette und Schere – Zug und Gegenzug • • • • monopolare Koagulation bipolare Koagulation LigaSureTM / Ultracision® Argon-Beamer • stumpfe (digitale) Dissektion • laparoskopische Dissektion (partiell) Chirurgische Prozeduren Peritonektomie linker OB Peritonektomie rechter OB Omentektomie Splenektomie Resektion kl. Netz CHE Gastrektomie Hemikolektomie rechts anteriore parietale Peritonektomie Peritonektomie kl. Becken Rektumresektion Hysterektomie Sugarbaker et al. Ann Surg 1999 Komplette makroskopische Zytoreduktion (CC-0/1) Voraussetzung für die HIPEC Konzept der CRS und HIPEC - Hypertherme intraperitoneale Chemotherapie - • Lokale Applikation von Zytostatika in hoher Dosierung zur Zerstörung nach CC-0/1-Resektion verbliebener Tumorzellen 48 46 SET ° C elsiu s 44 Inflow 42 40 Douglas 38 36 34 1 31 61 91 121 Minuten 151 181 211 Theoretische Vorteile der HIPEC • hohe lokale Zytostatikakonzentration • verbesserte Gewebepenetration • erhöhte lokale Wirksamkeit • Hyperthermie-assoziierte Zytotoxizität • homogene Verteilung intraoperativ Los et al, Br J Cancer 1994; Steller et al, Cancer Chemother Pharmacol 1999 Zytostatika für intraperitoneale Chemotherapie hypertherm normotherm häufig verwendet • • • • • Mitomycin C Cisplatin Doxorubicin Oxaliplatin Irinotecan selten verwendet • • • • • • • Melphalan Cyclophosphamid Etoposid Docetaxel Carboplatin Gemcitabin Mitoxantron • 5-FU • Paclitaxel • Floxuridin Patientenselektion (Beispiel KRK) Primärtumorlokalisation Lymphknotenstatus Histologie/Grading Kolonkarzinom mit Peritonealkarzinose PCI < 20 (CT, PET-CT, Laparoskopie) keine extrabdominelle Metastasierung kein disseminierter Dünndarmbefall max. eine Dünndarmstenose (CT, PET-CT, Laparoskopie) keine Cholestase / kein Harnstau durch Tumorinfiltration Interdisziplinäres TUMORBOARD limitierter Befall des Ligamentum hepatogastricum (< 5 cm im CT) max. 3 periphere, resektable Leberfiliae guter Allgemeinzustand (ECOG < 2) keine limit. Begleiterkrankungen Patientenmotivation/Einverständnis postoperative Lebensqualität ggf. Ansprechen auf systemische Chemotherapie präoperative systemische Chemotherapie (optional) CRS + HIPEC CCR-O/1 nicht möglich Palliative Chirurgie (optional) Syst. Chemotherapie Palliative Chemotherapie Peritoneal Cancer Index (PCI) • Der PCI dient der Beschreibung und Quantifizierung des intraperitonealen Tumorbefalls. • Einteilung des Abdomens in 13 Regionen (9 abdominelle Regionen + 4 Dünndarmregionen) • Punktevergabe von 0-3 für jede Region (Lesion Size Score): - LS 0 = kein sichtbarer Tumor - LS 1 = Tumor ≤ 0,5 cm - LS 2 = Tumor 0,5-5 cm - LS 3 = Tumor > 5 cm oder konfluierend PCI 0-39 Morbidität und Mortalität Morbidität [%] Anast.Insuffizienz [%] Toxizität °3/4 [%] Infektion [%] Autor, Jahr Pat. Mortalität [%] Stephens, 1999 200 1.5 27 3 4 9.5 Glehen, 2003 216 3.2 24.5 6.5 4.6 7.3 Kusamura, 2006 205 0.9 12 8.9 4.8 11.3 Gusani, 2008 124 1.6 29.8 7.2 - 4 Glockzin/Piso, 2008 220 1.4 34 8.4 3.5 10.2 Angegeben sind höhergradide Komlikationen (°III/IV). Die Gesamtkomplikationsrate des multimodalen Behandlungsregimes ist sicher deutlich höher einzuschätzen. Zusammenfassung • CRS und HIPEC können in spezialisierten Zentren mit niedriger Mortalität und akzeptabler Morbidität durchgeführt werden. • Prognoseentscheidend ist eine konsequente präoperative Patientenselektion unter Berücksichtigung von Tumorlokalisation, Histologie und Verteilungsmuster. • Weitere prospektive klinische Studien unter Einbeziehung aktueller Therapieregime sind dringend notwendig.