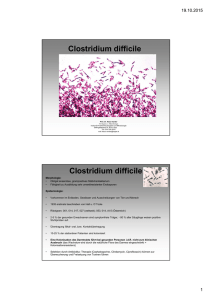
Falk Gastro-Kolleg Darm
Werbung
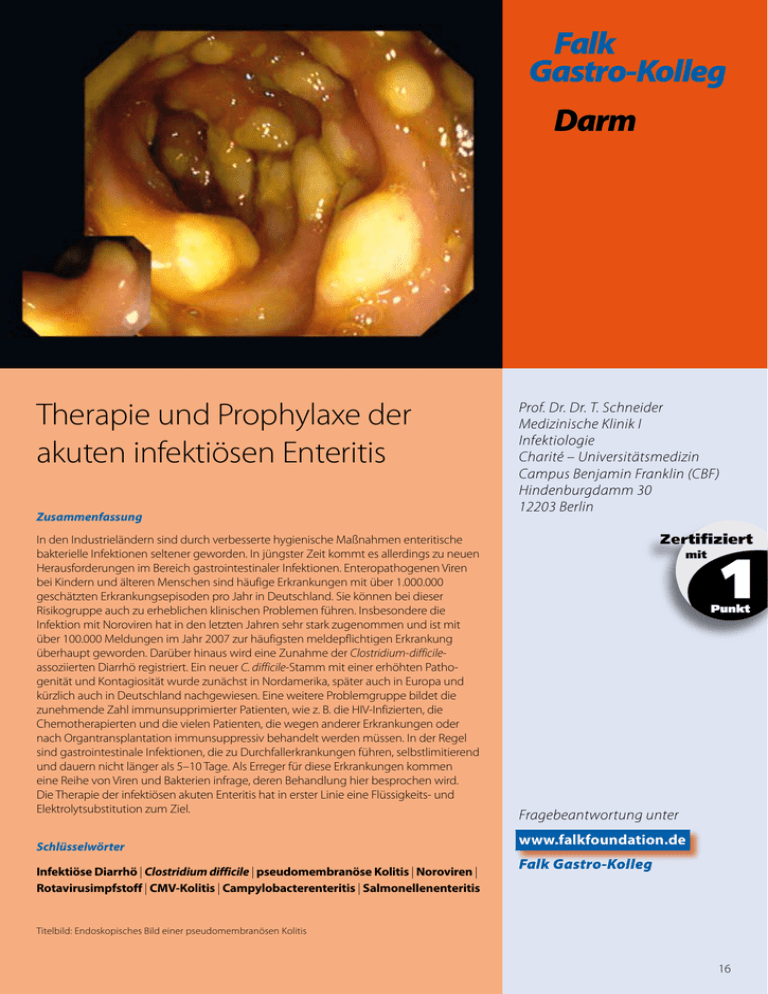
Falk Gastro-Kolleg Darm Therapie und Prophylaxe der akuten infektiösen Enteritis Zusammenfassung In den Industrieländern sind durch verbesserte hygienische Maßnahmen enteritische bakterielle Infektionen seltener geworden. In jüngster Zeit kommt es allerdings zu neuen Herausforderungen im Bereich gastrointestinaler Infektionen. Enteropathogenen Viren bei Kindern und älteren Menschen sind häufige Erkrankungen mit über 1.000.000 geschätzten Erkrankungsepisoden pro Jahr in Deutschland. Sie können bei dieser Risikogruppe auch zu erheblichen klinischen Problemen führen. Insbesondere die ­Infektion mit Noroviren hat in den letzten Jahren sehr stark zugenommen und ist mit über 100.000 Meldungen im Jahr 2007 zur häufigsten meldepflichtigen Erkrankung überhaupt geworden. Darüber hinaus wird eine Zunahme der Clostridium-difficileassoziierten Diarrhö registriert. Ein neuer C. difficile-Stamm mit einer erhöhten Patho­ genität und Kontagiosität wurde zunächst in Nordamerika, später auch in Europa und kürzlich auch in Deutschland nachgewiesen. Eine weitere Problemgruppe bildet die zunehmende Zahl immunsupprimierter Patienten, wie z. B. die HIV-Infizierten, die Chemotherapierten und die vielen Patienten, die wegen anderer Erkrankungen oder nach Organtransplantation immunsuppressiv behandelt werden müssen. In der Regel sind gastrointestinale Infektionen, die zu Durchfallerkrankungen führen, selbstlimitierend und dauern nicht länger als 5–10 Tage. Als Erreger für diese Erkrankungen kommen eine Reihe von Viren und Bakterien infrage, deren Behandlung hier besprochen wird. Die Therapie der infektiösen akuten Enteritis hat in erster Linie eine Flüssigkeits- und Elektrolytsubstitution zum Ziel. Schlüsselwörter Infektiöse Diarrhö | Clostridium difficile | pseudomembranöse Kolitis | Noroviren | Rotavirusimpfstoff | CMV-Kolitis | Campylobacterenteritis | Salmonellenenteritis Prof. Dr. Dr. T. Schneider Medizinische Klinik I Infektiologie Charité – Universitätsmedizin Campus Benjamin Franklin (CBF) Hindenburgdamm 30 12203 Berlin Fragebeantwortung unter www.falkfoundation.de Falk Gastro-Kolleg Titelbild: Endoskopisches Bild einer pseudomembranösen Kolitis 16 Therapie und Prophylaxe der akuten infektiösen Enteritis Einleitung In den Industrieländern konnten durch verbesserte hygienische Maßnahmen und besonders durch die Trennung zwischen Abwasser und Trinkwasser enteritische bakterielle Infektionen weitgehend zurückgedrängt werden. In jüngster Zeit kommt es allerdings zu neuen Herausforderungen im Bereich gastrointestinaler Infektionen. So sind Infektionen mit enteropathogenen Viren bei Kindern und älteren Menschen sehr häufig und können bei dieser Risikogruppe auch zu erheblichen klinischen Problemen führen. Insbesondere die Infektion mit Noroviren hat in den letzten Jahren sehr stark zugenommen und ist mit über 100.000 Meldungen im Jahr 2007 zur häufigsten meldepflichtigen Erkrankung überhaupt geworden. Bei dieser hochkontagiösen Infektion ist das Management zur Verhinderung einer weiteren Ausbreitung der Infektion im Krankenhaus oder in Pflegeeinrichtungen von größter Bedeutung. Darüber hinaus wird eine Zunahme der Clostridium-difficile-assoziierten Diarrhö registriert. Ältere Menschen sind durch diese Infektion besonders gefährdet. Hierbei spielt ein neuer C. difficile-Stamm mit einer erhöhten Pathogenität und Kontagiosität eine zentrale Rolle. Dieser Stamm wurde zunächst in Nordamerika, später in Europa und kürzlich auch in Deutschland nachgewiesen. Eine weitere Problemgruppe bildet die zunehmende Zahl immunsupprimierter Patienten, wie z. B. die HIV-Infizierten, die Chemotherapierten und die vielen Patienten, die wegen anderer Erkrankungen oder nach Organtransplantation immunsuppressiv behandelt werden müssen. Aufgrund der Fülle an verschiedenen Erregern, der Zunahme an neu beschriebenen Pathogenen und der Entwicklung von Resistenzen, ist die Behandlung der gastrointestinalen Infektionen äußerst komplex. Enteritische Infektionen manifestieren sich klinisch gewöhnlich durch Diarrhö, manchmal in Kombination mit Erbrechen und Fieber. In der Regel sind gastrointestinale Infektionen, die zu Durchfallerkrankungen führen, selbstlimitierend und dauern nicht länger als 5–10 Tage. Als Erreger für diese Erkrankungen kommen eine Reihe von Viren und Bakterien infrage, deren Behandlung hier besprochen wird. Die Therapie der infektiösen akuten Enteritis hat in erster Linie eine Flüssigkeitsund Elektrolytsubstitution zum Ziel. P Die infektiöse Diarrhö ist ein komplexes medizinisches Problem, welches besonders durch die Norovirusepidemien und das zunehmende Problem mit Clostridium-difficile-assoziierten Durchfallerkrankungen (CDAD) aktuell an Bedeutung gewonnen hat. Bakterielle Lebensmittelvergiftungen Enterotoxin-induzierte Erkrankungen Einige Bakterien produzieren Toxine, die in Lebensmitteln auch noch nach dem Absterben der Bakterien wirksam sein können. Die durch Staphylococcus aureus, Clostridium perfringens und Bacillus cereus produzierten Toxine führen nur zu kurz anhaltenden Episoden von Erbrechen, Diarrhö und abdominellen Krämpfen, die in der Regel nur wenige Stunden anhalten und keiner spezifischen Therapie bedürfen. Die wichtigste therapeutische Maßnahme bei allen Durchfallerkrankungen ist die ausreichende Flüssigkeits- und Elektrolytsubstitution. P Eine „Lebensmittelvergiftung“ durch Toxine von Staphylokokken hat eine sehr kurze Inkubationszeit und ist selbstlimitierend. Bakterielle Diarrhö Obwohl enteropathogene Bakterien in der Regel auf Antibiotika in vitro sensibel sind, profitieren die meisten dieser Patienten nicht von einer antibiotischen Therapie. In manchen Fällen kann diese sogar schädlich sein. Eine Zusammenfassung zur antibiotischen Therapie der bakteriellen Diarrhö ist in Tabelle 1 dargestellt. Nach Salmonellen- wie auch Campylobacterenteritis können gehäuft Reizdarmsyndrome auftreten. Der genaue pathogenetische Zusammenhang hierzu ist bisher nicht geklärt. P Die wichtigste Therapiemaßnahme bei jeder Diarrhö ist die Flüssigkeits­ substitution. Eine antibiotische Therapie ist nur bei schweren Verläufen oder bei Risikopatienten indiziert. Nach bakterieller Enteritis kann ein Reiz­darmsyndrom auftreten. 17 Behandlung bakterieller Enteritiden Erreger Antibiotische Therapie Medikament Salmonellen nein – Ausnahme: bei immungeschwächten Personen und septischen Verlaufsformen 2 x 500 mg Ciprofloxacin pro Tag oral über 7 Tage Shigellen und EIEC nur bei mittelschweren oder schweren Verlaufsformen oder Immun­ schwäche 4 x 500 mg Ampicillin pro Tag oral oder 2 x Trimethoprim/Sulfamethoxazol (160/800 mg) pro Tag oral oder 2 x 500 mg Ciprofloxacin pro Tag oral je über 5 Tage Campylobacter nur bei sehr schweren Verlaufsformen 4 x 500 mg Erythromycin pro Tag oral über 7 Tage Yersinien nein – Tab. 1 Ausnahme: Eisenüberladung z. B. 2 x 500 mg Ciprofloxacin und/oder Sepsis oral/Tag bis zu 8 Wochen EPEC, ETEC, EHEC nein – EPEC = enteropathogene Escherichia (E.) coli; ETEC = enterotoxische E. coli; EIEC = enteroinvasive E. coli; EHEC = enterohämorrhagische E. coli Salmonellen als Enteritiserreger (nicht-typhöse Salmonellen) Die enteritischen Salmonellen verursachen bei immunkompetenen Patienten meist mild verlaufende, selbstlimitierte Diarrhöen, die nur wenige Tage anhalten und keiner antibiotischen Therapie bedürfen. Die Diagnose wird durch den kuturellen Nachweis des Erregers im Stuhl gesichert. Hierfür wird meist ein Zeitraum von 3 Tagen benötigt. Bei Patienten mit Fieber kann der Erreger auch in Blutkulturen nachgewiesen werden. Die Schleimhautschädigung reicht von diskreten Entzündungszeichen über mäßige Entzündung mit Fibrinausschwitzung bis zu oberflächigen Ulzerationen. Eine anti­ biotische Therapie kann sogar den Krankheitsverlauf verlängern und zur Dauerausscheidung des Erregers führen. Daher sollten nur schwere, komplizierte Verläufe oder immunsupprimierte Patienten behandelt werden. Zurzeit wird hierfür Ciprofloxacin (2 x 500 mg/Tag) oral über 7 Tage empfohlen [1]. In den USA werden auch Patienten über 65 Jahre mit Antibiotika behandelt, da bei genereller Arteriosklerose das Risiko für eine Gefäßinfektion mit Ausbildung eines mykotischen Aneurysmas erhöht sein könnte. Bei Dauerausscheidern mit hohem Verbreitungsrisiko (z. B. Beschäftigte in Lebensmittelbetrieben) wird die Erregerelimination mit Ciprofloxacin (2 x 500 mg/Tag) über 4 Wochen in den meisten Fällen erreicht [2]. P Die Salmonellenenteritis ist in der Regel eine selbstlimitierende Erkrankung, die nur in besonderen klinischen Situationen einer antibiotischen Therapie bedarf. Shigellenenteritis Die Shigellenenteritis ist in Deutschland sehr selten und wird meist als Reiseerkrankung erworben. Die Shigellenenteritis kann sich klinisch unterschiedlich schwer von milden Verlaufsformen bis hin zu schweren blutigen Durchfallerkrankungen manifestieren. Die Diagnostik stützt sich auf die kulturelle Anzucht des Erregers aus dem Stuhl und dem Toxinnachweis. Die Behandlung von Shigellen ist weltweit durch die zunehmende Resistenz dieser Bakterien gegen diverse Antibiotika erschwert. Dies wird durch den unsachgemäßen übermäßigen Einsatz von Antibiotika und durch die Verwendung dieser Medikamente von Fleischlieferanten im Futter von Schweinen und Rindern gefördert [3]. In den meisten Fällen führt die Infektion zu einer kurzen selbstlimitierten Durchfallerkrankung, die keiner antibiotischen Therapie bedarf. Schwere Erkrankungsverläufe können eine antibiotische Therapie erforderlich machen. Auf- P Die Shigellenenteritis ist in Deutschland selten. 18 grund der erwähnten zunehmenden Resistenz ist eine nach einem Antibiogramm gezielte Behandlung wünschenswert. Ampicillin (4 x 500 mg/Tag), Trimethoprim-Sulfamethoxazol (2 x 160 mg/800 mg/Tag) oral und Ciprofloxacin (2 x 500 mg/Tag) oral, jeweils über 5 Tage, sind dabei wirksame Therapieoptionen [1, 4]. Campylobacterenteritis Campylobacterinfektionen zählen mittlerweile zu den häufigsten bakteriellen Enteritiden und sind in manchen Bundesländern schon häufiger als die Salmonelleninfektionen. Die Diagnostik beruht auf dem kulturellen Nachweis des Erregers aus dem Stuhl des Patienten. Die Anzucht gelingt in nur etwas über der Hälfte der Fälle. In den anderen Fällen kann man die Infektion im Nachhinein durch einen 3-fachen Antikörpertiter im Serum noch nachweisen. Dies hat aber keine klinische Relevanz. Die Infektion ist in der Mehrzahl der Fälle auf 1 Woche limitiert, in selteneren Fällen dauert die Erkrankung bis zu 2 Wochen. Rezidive werden bei Campylobacterinfektionen häufiger als bei Salmonelleninfektionen beobachtet. Im Gefolge der Campylobacterinfektion können immunologische Reaktionen wie Guillain-Barré-Syndrom, reaktive Arthritiden oder ein Erythema nodosum auftreten. Die meisten Campylobacterinfektionen verlaufen selbstlimitierend (Therapie: Flüssigkeits- und Elektrolytsubstitution). Eine Antibiotikabehandlung beeinflusst den Verlauf in diesen Fällen nicht und wird nur bei schweren Verlaufsformen und bei Patienten mit einer Immundefizienz empfohlen. Therapie der Wahl ist Erythromycin 4 x 500 mg pro Tag oral über 1 Woche. Wegen der Resistenzentwicklung von 41–88% gegenüber Quinolonen in Europa und Asien und auch einer zunehmenden Resistenz in den USA und Kanada sollten die bei anderen enteropathogenen Bakterien oft verwendeten Quinolone (z. B. Ciprofloxacin) nicht mehr eingesetzt werden [5]. Azithromycin in einer Dosierung von 500 mg pro Tag oral für 3 Tage konnte ebenfalls erfolgreich in Gebieten mit hoher Quinolon-Resistenz eingesetzt werden [6]. P Die Campylobacterenteritis gehört in Deutschland zu den häufigsten Ursachen einer bakteriellen Enteritis und ist nicht selten mit immunologischen Folgeerkrankungen assoziiert (Arthritis, Guillain-Barré-Syndrom, Erythema nodosum). Die Quinolon-Resistenz nimmt zu, Makrolide sind die Thera­peutika der Wahl. Yersinienenteritis Die Yersinienenteritis ist eine extrem seltene Erkrankung. Diese Durchfallerkrankung dauert meist nicht länger als 10 Tage und bedarf in der Regel keiner antibiotischen Therapie. Hochrisikopatienten mit Immundefizienz einschließlich Patienten mit Leberzirrhose und Patienten mit einer Eisenüberladung (z. B. Eisenspeichererkrankung) hingegen können eine Yersiniensepsis entwickeln und sollten antibiotisch behandelt werden. Kleine unkontrollierte Studien an Patienten mit Yersiniensepsis haben einen Effekt von Fluoroquinolonen allein oder in Kombination mit Cephalosporinen oder Aminoglycosiden der dritten Generation gezeigt [7]. P Hochrisikopatienten (Immun­ defizienz, Eisenüberladung) sollten antibiotisch behandelt werden. Clostridium-difficile-assoziierte Diarrhö (CDAD) C. difficile-assoziierte Erkrankungen (CDAD), von der Antibiotika-assoziierten Diarrhö bis zur pseudomembranösen Kolitis, stellen schwerwiegende nosokomiale Probleme dar [8]. Die Kosten u. a. durch intensivere Betreuung und verlängerte Krankenhaus­ aufenthalte werden in Europa bis auf 3 Milliarden Euro/Jahr geschätzt [9, 10]. In den letzten Jahren sind vor allem in Nordamerika Ausbrüche mit einem neuen hochvirulenten Stamm von C. difficile beschrieben worden, bei denen eine um den Faktor 5–20 erhöhte Inzidenz sowie eine um den Faktor 3–5 erhöhte Morbidität und Letalität auffiel. Seit 2003 konnte der neue Stamm auch in England, Belgien, den Niederlanden, Frankreich und Österreich isoliert werden. Mittlerweile wurde der Stamm auch in Deutschland nachgewiesen. Typischerweise manifestiert sich die CDAD als akute wässrige Diarrhö mit krampfartigen Unterbauchschmerzen, erhöhter Temperatur, einer Leukozytose im Blut und Leukozyten im Stuhl. Die abdominellen Beschwerden treten meist 5–10 Tage nach Beginn der Antibiotikatherapie auf, selten bereits am zweiten Tag oder erst mehrere Monate nach deren Abschluss. Das klinische Spektrum der CDAD reicht von einer leichten Diarrhö ohne entzündliche Schädigung der Mukosa über eine Kolitis unterschiedlicher Ausprägung mit fakultativer (in 10–20% der Fäl19 le) Bildung der charakteristischen Pseudomembranen (Abb. 1) mit den typischen histologischen Veränderungen bis hin zur fulminanten Kolitis. Die Durchfälle sind breiig bis wässrig, seltener auch blutig. Je nach Schweregrad kann es zur Dehydratation, Elektrolytentgleisung oder Hypoproteinämie kommen. Gefürchtete Komplikationen mit signifikanter Letalität sind das toxische Megakolon und die häufig zur Sepsis führende Darmperforation. Obwohl C. difficile als häufigste Ursache der erregerbedingten Antibiotika-assoziierten Kolitis identifiziert wurde, sollte betont werden, dass in der Mehrheit der Fälle die Antibiotika-assoziierte Diarrhö nicht infektiöser Genese, sondern durch Störungen der bakteriellen Flora bedingt ist. Bei Verdacht auf eine CDAD kann die Endoskopie mit dem Nachweis der typischen Pseudomembranen rasch zur Diagnosesicherung führen (Abb. 1). In den meisten Fällen ist jedoch eine weiterführende mikrobiologische Diagnostik notwendig. Diese beruht auf dem Nachweis der Toxine sowie des Erregers (bzw. seiner Antigene) aus einer frisch gewonnenen Stuhlprobe. Abb. 1 Endoskopisches Bild einer pseudomembranösen Kolitis Die erste und wichtigste Maßnahme nach Diagnosestellung einer CDAD ist das Absetzen von Antibiotika, soweit die klinische Situation des Patienten dies zulässt. Eine supportive Therapie zielt auf Normalisierung des Wasser- und Elektrolythaushalts. Asymptomatische Keimträger oder Erkrankte mit milder Symptomatik bedürfen keiner spezifischen Therapie. Indikationen zur antibiotischen Therapie sind Hinweise für das Vorliegen einer Kolitis (Fieber, Leukozytose, ggf. endoskopischer Befund), schwere Diarrhö, persistierende Diarrhö nach Absetzen des auslösenden Antibiotikums oder die Notwendigkeit einer fortgesetzten Antibiotikatherapie. In einer Metaanalyse fand sich kein Unterschied im klinischen Ansprechen auf Metronidazol, Bacitracin, Fusidinsäure oder Vancomycin (Evidenzlevel I–II) [11]. Bezüglich der Elimination der Clostridien aus dem Stuhl zeigte sich in einer kleinen Studie eine leichte Überlegenheit für Teicoplanin [12]. Um die Verbreitung Vancomycin-resistenter Enterokokken nicht zu begünstigen und auch aus Kostengründen (Tagestherapiekosten für Metronidazol ca. 2,50 für Vancomycin ca. 75 Euro) ist seit Mitte der 1990er-Jahre Metronidazol als Standardtherapie der CDAD etabliert [13]. Bei Ansprechen auf die Therapie kommt es in den meisten Fällen zur raschen Entfieberung und zum Sistieren der Diarrhö nach 4–5 Tagen. Verlaufsuntersuchungen auf Clostridien oder deren Toxin im Stuhl haben keinen Einfluss auf die Therapiedauer. Sollte eine orale Therapie nicht möglich sein, kann Metronidazol (nicht aber Vancomycin) auch intravenös appliziert werden. Für die Therapie schwerkranker (Sub-)Ileus-Patienten wird auf der Basis von Expertenmeinungen die Kombinationstherapie von Vancomycin (bis 4 x 500 mg) per Magensonde und intravenös appliziertem Metronidazol empfohlen [12] (Tab. 2). Aktuelle Beobachtungsstudien aus Nordamerika deuten auf eine Häufung schwerer Verläufe unter Metronidazol-Therapie hin [14, 15]. Da diese Daten retrospektiv erhoben wurden, der Einsatz von Metronidazol oder Vancomycin somit nicht randomisiert erfolgte und es zudem im Beobachtungszeitraum zu einer CDAD-Epidemie durch einen neuen, virulenteren Stamm gekommen war, ist die Aussagekraft dieser Studien nicht ausreichend, um derzeit zu einer Änderung der obigen Empfehlungen zu führen. 20 Ein erhebliches Problem in der Therapie der CDAD ist das signifikante Risiko zum klinischen Rezidiv. Es tritt in ca. 20% der mit Metronidazol oder Vancomycin behandelten Patienten meist innerhalb von 3–21 Tagen auf [12]. Risikofaktoren für ein Rezidiv sind erneute Antibiotikaexposition, Alter > 65 Jahre, schwere Grunderkrankung, Hypoalbuminämie, längerer Krankenhausaufenthalt, Aufenthalt auf Intensivstationen sowie noch nicht näher charakterisierte bakterielle Faktoren. Da die Therapie des ersten Rezidivs die gleiche Erfolgswahrscheinlichkeit besitzt wie die Therapie der Erst­ manifestation, erfolgt die erste Re-Therapie erneut mit Metronidazol. Beim zweiten Rezidiv wurde eine intermittierende ausschleichende Vancomycin-Therapie über 7 Wochen empfohlen [16]. In einer randomisierten Studie konnte das zusätzlich zu einer antibiotischen Therapie verabreichte Probiotikum Saccharomyces boulardii bei rezidivierender CDAD (nicht aber bei Erstmanifestation) das Risiko weiterer Rezidive senken [17] (Tab. 2). Tab. 2 Therapie der CDAD CDAD 1. Rezidiv Metronidazol oral (i. v.) (4 x 250 mg oder 3 x 500 mg) für 10 Tage Metronidazol oral (i. v.) (4 x 250 mg oder 3 x 500 mg) für 10 Tage > 1. Rezidiv Metronidazol oder Vancomycin oral 14–21 Tage + Saccharomyces bei Unverträglich- bei Unverträglich- boulardii keit, Gravidität keit, Gravidität oder Stillen: oder Stillen: Vancomycin oral Vancomycin oral (4 x 125 mg) (4 x 125 mg)* für 10 Tage* sehr schwere Fälle (Darmperforation, Peritonitis, toxisches Megakolon) Metronidazol evtl. i. v. + Vancomycin über Ernährungssonde totale Kolektomie erwägen * Vancomycin ist intravenös bei CDAD unwirksam Die geschilderten zunehmenden Probleme bei der Antibiotikatherapie machen die Entwicklung neuer Substanzen zur Behandlung der CDAD dringend notwendig. Ein monoklonaler Antikörper gegen das Toxin A von C. difficile wird gerade in einer PhaseII-Studie getestet [18]. Zurzeit läuft außerdem eine internationale, multizentrische Studie zur Wirksamkeit eines Toxinbinders (Tolevamer) im Vergleich zu Metronidazol und Vancomycin. In einer ersten klinischen Studie bei Patienten mit leichter bis mittelschwerer CDAD zeigte Tolevamer eine vergleichbare Wirksamkeit wie oral verabreichtes Vancomycin [19]. Tendenziell kam es unter Vancomycin zu einem schnelleren Ansprechen, hingegen wurde unter Tolevamer eine geringere Rezidivrate beobachtet (19). Die im Moment laufenden großen Studien müssen zeigen, ob sich dieses Ergebnis bestätigen lässt, und ob die Tendenz zur Hypokaliämie bei Tolevamer klinisch relevant wird. CDAD kann in seltenen Fällen zu Darmperforation, Peritonitis und toxischem Megakolon führen. Diese Verläufe sind mit einer erhöhten Letalität assoziiert, und ein chirurgisches Vorgehen muss in solchen Fällen erwogen werden. In einer kleinen retrospektiven Untersuchung war die totale Kolektomie anderen Resektionsverfahren überlegen. Es starben 11% (1/9) in der totalen Kolektomie- und alle in der Hemikolektomie-Gruppe (4/4) [20]. Die Übertragung erfolgt fäkal-oral, über die Umwelt und über die Hände des Personals, von einem kolonisierten oder infizierten Patienten ausgehend [21]. Die Prävention beruht auf drei Stufen: 1) rationale Antibiotikatherapie [22], 2) Kontaktisolierung der betroffenen Patienten sowie 3) Reinigung der Umgebung. P Die CDAD ist ein zunehmendes klinisches Problem, das vor allem bei älteren Patienten im Krankenhaus zur Mortalität beitragen kann. Wenn ein Absetzen des auslösenden Antibiotikums nicht ausreicht oder Antibiotika weiterhin gegeben werden müssen, sollte primär Metronidazol zur Therapie der CDAD gegeben werden. 21 Escherichia-coli-bedingte Diarrhö Escherichia coli (E. coli) gehört zur normalen Darmflora. Es gibt aber einige Vertreter dieser Gruppe, die durch die Bildung bestimmter Pathogenitätsfaktoren zu Erkrankungen führen können. Bei einigen E. coli wird die genetische Information für die Pathogenität durch bestimmte Viren (Bakteriophagen) übertragen. Enteropathogene E. coli (EPEC) EPEC wurden als erste E. coli-Gruppe erkannt, die Diarrhöen auslösen kann. Die Übertragung erfolgt von Person zu Person wahrscheinlich fäkal oral. Insbesondere bei Ausbrüchen von Durchfallerkrankungen bei Neugeborenen durch diesen Erreger kam es zu Verläufen mit hoher Mortalität. Die Anzahl der EPEC-Infektionen in den Industrienationen ist rückläufig. In den Entwicklungsländern ist die EPEC-Infektion bei Kindern unter 6 Monaten die häufigste bakterielle Ursache für Durchfallerkrankungen. Wie bei allen Durchfallerkrankungen stehen auch bei dieser Infektion die Flüssigkeits- und Elektrolytsubstitution sowie die ausreichende Kalorienzufuhr im Vordergrund. Da die Erkrankung meist selbstlimitierend verläuft, ist eine antibiotische Therapie in der ­Regel nicht notwendig. Trimethoprim-Sulfamethoxazol kann unter bestimmten Umständen die Erkrankungsdauer verkürzen [23]. Enterotoxische E. coli (ETEC) ETEC sind eine häufige Ursache für Diarrhöen bei Kindern in Entwicklungsländern. Darüber hinaus ist ETEC der bei der Reisediarrhö am häufigsten gefundene Erreger. Gelegentlich verursacht er auch lokale Epidemien von Durchfällen durch kontaminierte Speisen oder Getränke. Da die Erkrankung meist selbstlimitierend ist, sollte sich die Behandlung auf die Rehydratation und die Elektrolytsubstitution beschränken. Ein Nutzen von Antibiotika zur Verkürzung der Erkrankung ist nicht nachgewiesen. Da immer mehr resistente Stämme entstehen, sollte im Regelfall auf eine anti­biotische Therapie verzichtet werden. Enteroinvasive E. coli (EIEC) Zwischen EIEC und Shigellen gibt es eine große Antigenverwandtschaft. Die Symptomatik und Therapie ist bei beiden Infektionen gleich und wird deshalb dort abgehandelt. Enterohämorrhagische E. coli (EHEC) EHEC produzieren ein Zellgift, das Verotoxin oder Shigella-like Toxin (SLT). Mehr als 30 E. coli-Serotypen können SLT produzieren. In Europa und Nordamerika ist jedoch der Serotyp O157:H7 der häufigste. EHEC ist auch als Ursache des hämolytisch­urämischen Syndroms (HUS) erkannt worden. Die Frage, ob eine adäquate und rechtzeitige Antibiose die Entwicklung eines HUS beeinflussen kann, wird zurzeit kontrovers diskutiert. Einige Studien zeigten eine Verschlechterung der Erkrankung durch eine antibiotische Behandlung [24, 25]. Dies wurde auch durch eine neuere größere prospektive Studie bestätigt [26]. Die Zerstörung der Bakterien durch die Antibiose könnte hierbei zu einer vermehrten Toxinfreisetzung führen. Andere Studien deuten auf einen möglichen Vorteil einer antibiotischen Behandlung hin [27]. Auch die in-vitro-Daten sind widersprüchlich: Die einen berichten über eine vermehrte SLT-Produktion von E. coli O157:H7 unter Ciprofloxacin, die anderen über eine verminderte Toxinproduktion unter demselben Antibiotikum. Wichtig ist hervorzuheben, dass bei Patienten mit blutiger Diarrhö die Gabe von Motilitätshemmern kontraindiziert ist. In retrospektiven Untersuchungen konnte gezeigt werden, dass in Fällen mit Infektionen mit E. coli O157:H7, die länger als 24 Stunden mit Motilitätshemmern behandelt wurden, das Risiko, zentralnervöse Manifestationen im Rahmen eines HUS zu entwickeln, erhöht war. P Die E. coli-assoziierten Durchfall­ erkrankungen sollten nicht antibiotisch behandelt werden. EHEC können Auslöser des hämolytischurämischen Syndroms sein. 22 Aufgrund der unbefriedigenden zur Verfügung stehenden therapeutischen Möglichkeiten werden zurzeit Antiseren gegen das SLT auf ihre Wirksamkeit bei dieser Erkrankung geprüft. Zur Vermeidung von epidemischen Ausbrüchen ist eine strenge Kontrolle der Nahrungsmittel, insbesondere von Fleischprodukten notwendig. Virale Gastroenteritiden Enteropathogene Viren sind eine häufige Ursache von gastrointestinalen Infektionen bei Kindern (Rotaviren), aber auch bei Erwachsenen, besonders im höheren Lebens­ alter (Noroviren). Mittlerweile sind Noroviren die häufigste gemeldete Infektions­ erkrankung überhaupt und verursachen durch ihre hohe Kontagiosität erhebliche Probleme in Pflegeeinrichtungen und Krankenhäusern. Klinisch verlaufen die viralen Enteritiden in der Regel selbstlimitierend. Es gibt bisher keine spezifische Therapie. Die Behandlung beschränkt sich auf Flüssigkeits- und Elektrolytsubstitution. Je nach Schwere der Erkrankung muss diese oral und in einigen Fällen auch intravenös ­erfolgen. Rotaviren Die Infektion mit Rotaviren betrifft vorwiegend Kinder und erfolgt meist fäkal-oral. Die Rotaviren replizieren in den apikalen Enterozyten der Dünndarmzotten. Nach einer Inkubationszeit von 2–3 Tagen treten die klinischen Symptome auf. Meist tritt ­Erbrechen gefolgt von Fieber und Diarrhö auf. Die übliche Erkrankungsdauer kann 6 bis 8 Tage betragen. Vermutlich wird durch das virale Protein (NSP4), welches Eigenschaften eines Enterotoxins aufweist, die Wirkung noch verstärkt. Eine spezielle Therapie existiert nicht. Es ist in jedem Fall auf eine ausreichende Flüssigkeits- und Elektrolytzufuhr zu achten. Von der Einnahme von Antidiarrhoika (Loperamid) ist abzuraten, da diese die Ausscheidung des Erregers erschweren und somit den Krankheitsverlauf verlängern. Infizierte Kinder dürfen keine öffentlichen Gemeinschaftseinrichtungen, wie z. B. Kindertagesstätten, besuchen. Eine Infektion ist der Kindertagesstätte zu melden. Aufgrund der hohen Morbidität und auch Mortalität der Erkrankung bei Kleinkindern weltweit wurde intensiv an der Entwicklung eines Impfstoffs gearbeitet. Ein in den USA lizensierter Impfstoff zeigte eine Effektivität von 49–68% gegen alle Rotavirusbedingten Durchfallerkrankungen und eine Effektivität von 69–91% gegen schwere Verlaufsformen [28]. In einer weiteren Studie mit einem abgeschwächten oralen ­Lebendimpfstoff konnte bei Kindern ebenfalls die Häufigkeit einer Rota­virus-bedingten Durchfallerkrankung signifikant gesenkt werden [29]. 1998 wurde eine Schluckimpfung gegen Rotaviren (RotaShield®) in den USA in den normalen Impfplan auf­genommen. Die Impfung wurde aber schon bald wieder zurückgezogen, nachdem 76 Fälle einer Intussuszeption (Invagination, Darmeinstülpung) aufgetreten waren, und ein Zusammenhang mit der Impfung nicht ausgeschlossen werden konnte. Mittlerweile gibt es 2 zugelassene Impfstoffe (Rotarix® und Rotateq®), die eine noch bessere Wirksamkeit und eine hervorragende Verträglichkeit zeigen [30, 31, 32]. Insbesondere der zwischenzeitlich aufgekommene Verdacht, dass der Rotavirusimpfstoff vermehrt Dünndarminvaginationen induzieren könnte, wurde komplett ausgeräumt [30, 31, 32]. Das Impfschema besteht aus 2 oder 3 Teilimpfungen. Es handelt sich um Schluckimpfungen. Die Immunisierung muss mit dem vollendeten 6. Lebensmonat abgeschlossen sein. Ohne Impfung erkrankt bis zum 5. Lebensjahr nahezu jedes Kind an Rotaviren. P Rotaviren sind die häufigste Ursache für Durchfallerkrankungen bei Kindern. Die Infektion kann durch eine Impfung effektiv verhindert werden. Noroviren Norovirusinfektionen sind die häufigste Ursache akuter Gastroenteritiden [33, 34]. Die epidemiologische Bedeutung dieser meldepflichtigen Infektionserkrankung wurde in den letzten Jahren durch mehrere Ausbrüche auf Kreuzfahrtschiffen, in Krankenhäusern und in Altersheimen deutlich. Die Erkrankung äußert sich typischerweise durch 23 plötzlich auftretendes Erbrechen und akut einsetzende wässrige Diarrhö. Die Erkrankung dauert in der Regel nur 2–3 Tage. Die Infektion kann auch über Aerosole erfolgen, sodass insbesondere Erbrochenes als hochkontagiös gilt. Der Verdacht auf diese Erkrankung sollte klinisch gestellt werden, insbesondere, wenn mehrere Personen mit diesen Symptomen aus einer gemeinsamen Umgebung kommen. Genetische Veränderungen des Erregers haben wahrscheinlich zu der erhöhten Kontagiosität in den letzten Jahren beigetragen. Der Schutz einiger Personen vor der Erkrankung wird mit dem Fehlen des Rezeptors für Noroviren in Verbindung gebracht. Die letzten Epidemien haben gezeigt, dass nur strikte hygienische Maßnahmen die Ausbreitung des Erregers in Gemeinschaftseinrichtungen verhindern können. Der Verdacht auf die Noroviruserkrankung sollte schnell klinisch gestellt werden, dies gelingt meist durch die Anwendung der sogenannten Kaplan-Kriterien [4]: • Erbrechen (häufig explosiv) in > 50% der Fälle •wässrige akute Diarrhö (Dauer der Erkrankung 12–60 Stunden, Inkubationszeit 6–48 Stunden, Personal und Betreute betroffen) Sollten diese Kriterien erfüllt sein, muss man zunächst von einer Norovirusinfektion ausgehen und die entsprechenden hygienischen Maßnahmen einleiten. Auf keinen Fall sollte hiermit bis zum Eintreffen der labortechnischen Bestätigung der klinischen Diagnose gewartet werden. Es ist noch anzumerken, dass die Kaplan-Kriterien bei Chemotherapiepatienten zur Differenzierung zwischen Noroviruserkrankung und ­Nebenwirkungen der Chemotherapie versagen können. Die Laborbestätigung erfolgt durch den Nachweis des Erregergenoms im Stuhl mittels Polymerasekettenreaktion (PCR) oder durch den Nachweis von Norovirusantigenen im Stuhl mittels eines Capture-ELISAs. Es reicht voll aus, wenn aus jedem Infektionsherd höchstens 2–3 Patienten getestet werden. Die Infektion ist meldepflichtig. Die Therapie ist in erster Linie symptomatisch und konzentriert sich, wie bei anderen Durchfallerkrankungen, auf die ausreichende Flüssigkeits- und Elektrolytsubstitution. Bei Immungeschwächten, die eine chronische Diarrhö durch die Norovirusinfektion entwickeln, muss überlegt werden, ob die immunsuppressive Therapie zurückgefahren werden kann. Eine spezifische virustatische Therapie gibt es zurzeit nicht. Noroviren zeichnen sich durch eine hohe Umweltresistenz (Tenazität) und eine eingeschränkte Empfindlichkeit gegenüber üblichen Desinfektions- und Reinigungsmitteln aus. Diese Charakteristika sind – zusammen mit der geringen infektiösen Dosis von weniger als 100 Viruspartikeln und der Möglichkeit einer aerogenen Übertragung des Virus – Ursache für die erschwerte Kontrolle von Krankheitshäufungen. Norovirusinfektionen in Gemeinschaftseinrichtungen können auch in Zukunft nicht sicher verhindert werden. Daher ist die rasche klinische Diagnosestellung von größter Bedeutung. Die Einleitung eines adaptierten Hygieneregimes sollte dann unmittelbar erfolgen, ohne die Bestätigung durch virologische Untersuchungen abzuwarten. Betroffenes Personal ist bis 72 Stunden nach Sistierung der Symptomatik vom Dienst freizustellen [34, 35]. Die Patienten sowie Kontaktpatienten sollten sofort mittels ­Einzel- oder Kohortenisolierung vom übrigen Publikums- und Patientenverkehr ­abgeschirmt werden. Dies kann am sichersten auf einer dafür ausgelegten Infektionsstation mit entsprechender Vorzone umgesetzt werden. Besucher, Personal und Ärzte müssen vor Betreten des Zimmers Kittel, Handschuhe und einen Mundschutz (am besten OP-Maske) anlegen. Beim Verlassen des Zimmers verbleiben Kittel, Handschuhe und Mundschutz innerhalb der Vorzone in dafür vorgesehenen Entsorgungsbeuteln. Vor Verlassen einer betroffenen Pflegeeinheit wird eine hygienische Händedesinfektion mit einem alkoholischen Desinfektionsmittel durchgeführt (Wirkstoffbereich B der RKI-Liste). Die Zimmer und alle Kontaktflächen einschließlich Türklinken, Lichtschalter etc. müssen einer konsequenten Desinfektion mit aldehydhaltigen Reinigungsmitteln unterzogen werden. Die durch zeitweilige Schließung von Stationen und Freistellung von Mitarbeitern verursachten ökonomischen Belastungen sind dabei in Relation zu den vielfach höheren Kosten eines unkontrollierten Ausbruchs zu sehen [36]. P Noroviren sind hochkontagiös und können daher durch eine rasche Ausbreitung der Infektion auch auf das medizinische Personal für erhebliche ökonomische Belastungen führen. 24 Zytomegalievirus (CMV) Das Zytomegalievirus (CMV) kann bei immunsupprimierten Patienten eine Kolitis ­verursachen. Diese kann bei diesen Patienten sehr schwerwiegend verlaufen. Endoskopisch sieht man meist scharf begrenzte, wie ausgestanzt wirkende Ulzerationen (Abb. 2). Die Diagnose wird in der Regel bioptisch durch den Nachweis von Eulenaugenzellen oder den immunhistologischen Nachweis von CMV-Proteinen gesichert. Die CMV-Kolitis war früher bei AIDS-Patienten mit sehr niedriger CD4-Lymphozytenzahl relativ häufig. Heute ist sie in den Industrieländern seit Einführung der hochwirksamen antiretroviralen Kombinationstherapie (HAART) in dieser Risikogruppe seltener geworden. Dafür findet man sie jetzt gelegentlich bei anderweitig immunsupprimierten Patienten, wie z. B. bei Patienten mit einer chronisch entzündlichen Darmerkrankung, Patienten nach Organtransplantation oder Patienten unter Chemotherapie. Abb. 2 Typische ausgestanzte, scharf begrenzte Ulzerationen im Dickdarm bei CMV-Kolitis Die Behandlung der CMV-Infektion des Intestinaltrakts sollte mit Ganciclovir (5 mg/kg 2 x täglich) oder Foscarnet (60 mg/kg 3 x täglich oder 90 mg/kg 2 x täglich) in schweren Fällen über mindestens 2–3 Wochen intravenös erfolgen [34]. Die Haupt­nebenwirkung von Ganciclovir sind Thrombo- und Neutropenie; die von Foscarnet Nierenfunktionsstörungen. Die Frage nach einer Erhaltungstherapie bei immunrekonstituierten Patienten unter HAART ist nicht geklärt. Bei immunsupprimierten Patienten mit anderer Ursache als HIV ist eine Sekundärprophylaxe mit 3 x 1000 mg Ganciclovir 3 x täglich [37] oder mit Valganciclovir 1 x 900 mg pro Tag möglich und sollte solange fortgeführt werden, wie die Immunsuppression anhält. In Fällen, in denen eine dauerhafte ­Immunsuppression vorliegt oder durch eine Therapie eine anhaltende Immun­ suppression aufrechterhalten werden muss, sollte über die Dauer der Sekundär­ prophylaxe individuell entschieden werden. P Die CMV-Kolitis ist eine Erkrankung bei immunsupprimierten Patienten, die schwerwiegende Verläufe verursachen kann und daher rasch diagnostiziert und behandelt werden sollte. 25 Zu empfehlende Literatur Literatur 1 Bassily S, Hyams KC, el-Masry NA, Farid Z, Cross E, Bourgeois AL, Ayad E, Hibbs RG. Short-course norfloxacin and trimethoprim-sulfamethoxazole treatment of shigellosis and salmonellosis in Egypt. Am J Trop Med Hyg 1994; 51: 219–223. 2 Gotuzzo E, Guerra JG, Benavente L, Palomino JC, Carrillo C, Lopera J, Delgado F, Nalin DR, Sabbaj J. Use of norfloxacin to treat chronic typhoid carriers. J Infect Dis 1988; 157: 1221–1225. 3 Tauxe RV, Puhr ND, Wells JG, Hargrett-Bean N, Blake PA. Antimicrobial resistance of Shigella isolates in the USA: the importance of international travelers. J Infect Dis 1990; 162: 1107–1111. 4 Bennish ML, Salam MA, Haider R, Barza M. Therapy for shigellosis. II. Randomized, double-blind comparison of ciprofloxacin and ampicillin. J Infect Dis 1990; 162: 711–716. 5 Smith KE, Besser JM, Hedberg CW, Leano FT, Bender JB, Wicklund JH, Johnson BP, Moore KA, Osterholm MT. Quinolone-resistant Campylobacter jejuni infections in Minnesota, 1992–1998. Investigation Team. N Engl J Med 1999; 340: 1525–1532. 6 Kuschner RA, Trofa AF, Thomas RJ, Hoge CW, Pitarangsi C, Amato S, Olafson RP, Echeverria P, Sadoff JC, Taylor DN. Use of azithromycin for treatment of Campylobacter enteritis in travelers to Thailand, an area where ciprofloxacin resistance is prevalent. Clin Infect Dis 1995; 21: 536–541. 7 Crowe M, Ashford K, Ispahani P. Clinical features and antibiotic teatment of septic arthritis and osteomyelitis due to Yersinia enterocolitica. J Med Microbiol 1996; 45: 302–309. 8 Schneider T, Eckmanns T, Ignatius R, Weist K, Liesenfeld O. Clostridium-difficile-assoziierte Diarrhö: ein zunehmendes klinisches Problem durch neue hochvirulente Erreger. Clostridium difficile-associated diseases – an emerging problem. Dtsch Ärztebl 2007; 104: 22, A-1588/B-1403/C-1343. 9 Kuijper EJ, van den Berg RJ, Debast S, Visser CE, Veenendaal D, Troelstra A, van der Kooi T, van den Hof S, Notermans DW. Clostridium difficile ribotype 027, toxinotype III, the Netherlands. Emerg Infect Dis 2006; 12: 827–830. 10 Kyne L, Hamel MB, Polavaram R, Kelly CP. Health care costs and mortality associated with nosocomial diarrhea due to Clostridium difficile. Clin Infect Dis 2002; 34: 346–353. 11 Bricker E, Garg R, Nelson R, Loza A, Novak T, Hansen J. Antibiotic treatment for Clostridium difficile-associated diarrhea in adults. Cochrane Database Syst Rev 2005; 1: CD004610. 26 12 Bartlett JG. Narrative review: the new epidemic of Clostridium difficile-associated enteric disease. Ann Intern Med 2006; 145: 758–764. Literatur 13 Fekety R. Guidelines for the diagnosis and management of Clostridium difficile-associated diarrhea and colitis. American College of Gastroenterology, Practice Parameters Committee. Am J Gastroenterol 1997; 92: 739–750. 14 Fernandez A, Anand G, Friedenberg F. Factors associated with failure of metronidazole in Clostridium difficile-associated disease. J Clin Gastroenterol 2004; 38: 414–418. 15 Pépin J, Valiquette L, Alary ME, Villemure P, Pelletier A, Forget K, Pépin K, Chouinard D. Clostridium difficile-associated diarrhea in a region of Quebec from 1991 to 2003: a changing pattern of disease severity. CMAJ 2004; 171: 466–472. 16 Surawicz, CM. Treatment of recurrent Clostridium difficile-associated disease. Nat Clin Pract Gastroenterol Hepatol 2004; 1: 32–38. 17 McFarland LV, Surawicz CM, Greenberg RN, Fekety R, Elmer GW, Moyer KA, Melcher SA, Bowen KE, Cox JL, Noorani Z, et al. A randomized placebo-controlled trial of Saccharomyces boulardii in combination with standard antibiotics for Clostridium difficile disease. JAMA 1994; 271: 1913–1918. 18 Babcock GJ, Broering TJ, Hernandez HJ, Mandell RB, Donahue K, Boatright N, Stack AM, Lowy I, Graziano R, Molrine D, Ambrosino DM, Thomas WD Jr. Human monoclonal antibodies directed against toxins A and B prevent Clostridium difficile-induced mortality in hamsters. Infect Immun 2006; 74: 6339–6347. 19 Louie TJ, Peppe J, Watt CK, Johnson D, Mohammed R, Dow G, Weiss K, Simon S, John JF Jr, Garber G, Chasan-Taber S, Davidson DM; Tolevamer Study Investigator Group. Tolevamer, a novel nonantibiotic polymer, compared with vancomycin in the treatment of mild to moderately severe Clostridium difficile-associated diarrhea. Clin Infect Dis 2006; 43: 411–420. 20 Koss K, Clark MA, Sanders DS, Morton D, Keighley MR, Goh J. The outcome of surgery in fulminant Clostridium difficile colitis. Colorectal Dis 2006; 8: 149–154. 21 McFarland LV, Mulligan ME, Kwok RY, Stamm WE. Nosocomial acquisition of Clostridium difficile infection. N Engl J Med 1989; 320: 204–210. 22 Gerding DN, Johnson S, Peterson LR, Mulligan ME, Silva J Jr. Clostridium difficile-associated diarrhea and colitis. Infect Control Hosp Epidemiol 1995; 16: 459–477. 23 Thorén A, Wolde-Mariam T, Stintzing G, Wadström T, Habte D. Antibiotics in the treatment of gastroenterits caused by enteropathogenic Escherichia coli. J Infect Dis 1980; 141: 27–31. 27 24 Carter AO, Borczyk AA, Carlson JA, Harvey B, Hockin JC, Karmali MA, Krishnan C, Korn DA, Lior H. A severe outbreak of Escherichia coli O157:H7-associated hemorrhagic colitis in a nursing home. N Engl J Med 1987; 317: 1496–1500. Literatur 25 Pavia AT, Nichols CR, Green DP, Tauxe RV, Mottice S, Greene KD, Wells JG, Siegler RL, Brewer ED, Hannon D, Blake PA. Hemolytic-uremic syndrome during an outbreak of Escherichia coli O157:H7 infections in institutions for mentally retarded persons: clinical and epidemiologic observations. J Pediatr 1990; 116: 544–551. 26 Wong CS, Jelacic S, Habeeb RL, Watkins SL, Tarr PI. The risk of the hemolytic-uremic syndrome after antibiotic treatment of Escherichia coli O157:H7 infections. N Engl J Med 2000; 342: 1930–1936. 27 Ostroff SM, Kobayashi JM, Lewis JH. Infections with Escherichia coli O157:H7 in Washington State. The first year of statewide disease surveillance. JAMA 1989; 262: 355–359. 28 Joensuu J, Koskenniemi E, Pang XL, Vesikari T. Randomised placebo-controlled trial of rhesus-human reassortant rotavirus vaccine for prevention of severe rotavirus gastroenterits. Lancet 1997; 350: 1205–1209. 29 Bernstein DI, Sack DA, Rothstein E, Reisinger K, Smith VE, O’Sullivan D, Spriggs DR, Ward RL. Efficacy of live, attenuated, human rotavirus vaccine 89-12 in infants: a randomised placebo-controlled trial. Lancet 1999; 354: 287–290. 30 Ruiz-Palacios GM, Pérez-Schael I, Velázquez FR, Abate H, Breuer T, Clemens SC, Cheuvart B, Espinoza F, Gillard P, Innis BL, Cervantes Y, Linhares AC, López P, Macías-Parra M, Ortega-Barría E, Richardson V, Rivera-Medina DM, Rivera L, Salinas B, Pavía-Ruz N, Salmerón J, Rüttimann R, Tinoco JC, Rubio P, Nuñez E, Guerrero ML, Yarzábal JP, Damaso S, Tornieporth N, Sáez-Llorens X, Vergara RF, Vesikari T, Bouckenooghe A, Clemens R, De Vos B, O’Ryan M; Human Rotavirus Vaccine Study Group. Safety and efficacy of an attenuated vaccine against severe rotavirus gastroenteritis. N Engl J Med 2006; 354: 11–22. 31 Vesikari T, Matson DO, Dennehy P, Van Damme P, Santosham M, Rodriguez Z, Dallas MJ, Heyse JF, Goveia MG, Black SB, Shinefield HR, Christie CD, Ylitalo S, Itzler RF, Coia ML, Onorato MT, Adeyi BA, Marshall GS, Gothefors L, Campens D, Karvonen A, Watt JP, O’Brien KL, DiNubile MJ, Clark HF, Boslego JW, Offit PA, Heaton PM; Rotavirus Efficacy and Safety Trial (REST) Study Team. Safety and efficacy of a pentavalent human-bovine (WC3) reassortant rotavirus vaccine. N Engl J Med 2006; 354: 23–33. 32 Murphy TV, Gargiullo PM, Massoudi MS, Nelson DB, Jumaan AO, Okoro CA, Zanardi LR, Setia S, Fair E, LeBaron CW, Wharton M, Livengood JR; Rotavirus Intussusception Investigation Team. Intussusception among infants given an oral rotavirus vaccine. N Engl J Med 2001; 344: 564–572. 28 33 Schneider T, Mankertz J, Jansen A, Schreier E, Zeitz M. Norovirusinfektion – häufigste Ursache akuter Gastroenteritiden in den Winter­ monaten. Norovirus infection – the commonest cause of winter gastroenteritis. Dtsch Ärztebl 2005; 102; 38, A-2551/B-2153/C-2032 Literatur 34 Schneider T, Zeitz M. Behandlung gastrointestinaler Infektionen. Internist (Berl) 2000; 41: 1302–1317. 35 Jansen A, Beyer A, Brandt C, Höhne M, Schreier E, Schulzke J, Zeitz M, Schneider T. The norovirus-epidemic in Berlin – clinic, epidemiology and prevention. Z Gastroenterol 2004; 42: 311–316. 36 Johnston CP, Qiu H, Ticehurst JR, Dickson C, Rosenbaum P, Lawson P, Stokes AB, Lowenstein CJ, Kaminsky M, Cosgrove SE, Green KY, Perl TM. Outbreak management and implications of a nosocomial norovirus outbreak. Clin Infect Dis 2007; 45: 534–540. 37 Whitley RJ, Jacobson MA, Friedberg DN, Holland GN, Jabs DA, Dieterich DT, Hardy WD, Polis MA, Deutsch TA, Feinberg J, Spector SA, Walmsley S, Drew WL, Powderly WG, Griffiths PD, Benson CA, Kessler HA. Guidelines for the treatment of cytomegalovirus disease in patients with AIDS in the era of potent antiretroviral therapy: recommendations of an international panel. International AIDS Society-USA. Arch Intern Med 1998; 158: 957–969. 29 Fragen zur Therapie und Prophylaxe der akuten infektiösen Enteritis Falk Gastro-Kolleg Darm Frage 1: Welche Aussage ist richtig? Die Norovirusinfektion wist eine seltene Infektionskrankheit wist gut mit Antibiotika zu behandeln wkommt häufiger in den Wintermonaten vor whinterlässt eine lebenslange Immunität wist nur bedingt ansteckend Frage 2: Welche Aussage trifft für die Salmonellenenteritis zu? Bitte beachten Sie: Bei der Beantwortung der Fragen ist immer nur 1 Antwort möglich. wIn der Regel ist eine antibiotische Therapie notwendig wDie Diagnose wird durch die PCR bestätigt wEine Salmonelleninfektion kann lebensbedrohlich verlaufen wDie Entwicklung einer Dauerausscheidung von Salmonellen kann durch eine frühe antibiotische Therapie verhindert werden wNach einer Salmonelleninfektion tritt niemals ein Reizdarmsyndrom auf Die Beantwortung der Fragen und Erlangung des Fortbildungszertifikats ist nur online möglich. Bitte gehen Sie dazu auf unsere Homepage www.falkfoundation.de. Unter dem Menüpunkt Falk Gastro-Kolleg können Sie sich anmelden und die Fragen beantworten. Bitte diesen Fragebogen nicht per Post oder Fax schicken! Frage 3: Welche Aussage trifft für die Campylobacterenteritis zu? wDie Campylobacterenteritis ist eine seltene bakterielle Ursache einer akuten Diarrhö wIm Gefolge einer Campylobacterinfektion können sich eine reaktive Arthritis und/oder ein Erythema nodosum entwickeln wCiprofloxacin ist das Antibiotikum der Wahl zur Behandlung der Campylobacterenteritis wBei Fieber gelingt der Nachweis von Campylobacterspezies meist im Blut wEine Diarrhö verursacht durch Campylobacterspezies dauert in der Regel länger als 14 Tage Frage 4: Welche Aussage zur Yersinieninfektion ist richtig? wYersinien werden als Ursache einer Diarrhö in Deutschland häufig gefunden wYersinien können besonders bei Patienten mit einer Eisenüberladung einen schweren Verlauf nehmen wYersinien sind bei AIDS-Patienten ein wichtiger Erreger von Durchfallerkrankungen wEine Durchfallerkrankung, die durch Yersinien hervorgerufen wird, sollte in der Regel antibiotisch behandelt werden wDurchfälle, bedingt durch Yersinien, werden besonders häufig bei Reiserückkehrern gefunden Wichtig: Fragebeantwortung unter www.falkfoundation.de Falk Gastro-Kolleg 30 Frage 5: Welche Aussage trifft zur CDAD zu? wClostridien spielen bei der Diarrhö im Krankenhaus selten einer Rolle wWird Clostridium difficile im Stuhl eines Patienten mit Diarrhö ­gefunden, sollte er mit Clont oder Vancomycin behandelt werden wCDAD ist ein zunehmendes Problem in Industrieländern wWenn endoskopisch keine Pseudomembranen gesehen werden, ist eine CDAD ausgeschlossen wDer Verlauf der Erkrankung, besonders bei sehr alten Patienten, ist manchmal lebensbedrohlich Falk Gastro-Kolleg Darm Frage 6: Welche Aussage zur CDAD trifft nicht zu? wZur Therapiekontrolle sollte der Toxinnachweis im Stuhl herangezogen werden wMetronidazol (Clont) ist Mittel der ersten Wahl bei der Behandlung der CDAD wEines der wichtigsten Prinzipien der CDAD-Behandlung ist das Absetzen des auslösenden Antibiotikums wRezidive treten relativ häufig auf wIn der Regel wird bei einem Rezidiv wieder dasselbe Antibiotikum eingesetzt wie bei der ersten Therapie Frage 7: Welche Aussage zur CMV-Kolitis trifft zu? wDie CMV-Kolitis ist eine häufige Ursache einer Diarrhö bei Kindern wEine CMV-Kolitis muss in der Regel nicht spezifisch behandelt werden wDie CMV-Kolitis kann häufig erst durch Koloskopie mit der Abnahme von Biopsien gesichert werden wDie CMV-Kolitis kommt bei Patienten mit Colitis ulcerosa nicht vor wBei HIV-Patienten nimmt die Inzidenz der CMV-Kolitis in den letzten Jahren deutlich zu Frage 8: Welche Aussage zu Rotaviren trifft nicht zu? wRotaviren verursachen vor allem bei Kindern eine akute Diarrhö wRotaviren infizieren reife Enterozyten des Dünndarms wEin Peptid des Rotavirus wirkt wie ein Enterotoxin wEin Impfstoff gegen Rotaviren sollte erst nach dem ersten Lebensjahr eingesetzt werden, weil es sonst gehäuft zu Invaginationen des Dünndarms kommen kann wDie Flüssigkeitssubstitution ist bei der Behandlung einer Rotavirusinfektion das Wichtigste 31 Frage 9: Welche klinischen Symptome sind nicht typisch für eine Norovirusinfektion? wMuskelschmerzen wAbdominelle Krämpfe wDurchfall wSehstörungen wErbrechen Falk Gastro-Kolleg Darm Frage 10: Welche Maßnahme ist bei dem Verdacht auf einen Norovirus­ ausbruch im Krankenhaus nicht angezeigt? wInformation des Personals in der betroffenen Einrichtung einschließlich der Reinigungskräfte und der Krankentransporter wBei jedem Patienten ist eine Diagnosesicherung durch eine PCR notwendig wPatienten und Besucher sollten informiert werden, ggf. erfolgt eine zeitweilige Einschränkung des Besucherverkehrs wMeldung an das zuständige Gesundheitsamt wFreistellung von erkranktem Personal, ggf. Schließung von stark betroffenen Einheiten 32